增生型糖尿病視網膜病變(PDR)是糖尿病視網膜病變(DR)的晚期表現,常伴有玻璃體積血和視網膜脫離,嚴重影響患者的視力,甚至導致嚴重視力損傷。雖然玻璃體切割手術是治療PDR的有效方法,但手術操作具有一定的難度,不當處理可能會對患者手術后的視力恢復產生不利影響或引起并發癥。因此,明確PDR的手術適應證和規范操作流程至關重要。為此,中華醫學會眼科學分會眼底病學組、中國醫師協會眼科醫師分會眼底病專委會以及《玻璃體切割手術治療2型糖尿病視網膜病變專家共識》專家組,針對9個關鍵臨床問題,基于最新的循證醫學證據,并結合國際指南和我國的社會經濟發展現狀,就DR手術時機的選擇、圍手術期血糖管理、手術方式的選擇、手術操作方案的制定、藥物聯合或激光治療等方面提出了推薦意見,形成了我國《玻璃體切割手術治療2型糖尿病視網膜病變專家共識》。本共識適用于中國眼底病專科醫師和從事眼底病專業的醫師,旨在為PDR患者的玻璃體手術治療提供科學指導,輔助臨床決策制定,進一步提高我國DR的手術治療水平。
引用本文: 中華醫學會眼科學分會眼底病學組, 中國醫師協會眼科醫師分會眼底病專委會, 《玻璃體切割手術治療2型糖尿病視網膜病變專家共識》專家組. 玻璃體切割手術治療2型糖尿病視網膜病變專家共識. 中華眼底病雜志, 2024, 40(9): 663-686. doi: 10.3760/cma.j.cn511434-20240729-00286 復制
版權信息: ?四川大學華西醫院華西期刊社《中華眼底病雜志》版權所有,未經授權不得轉載、改編
糖尿病視網膜病變(DR)是由糖尿病引發的視網膜微血管損害,可導致一系列病變及全視網膜非血管組織的損傷,是一種可能嚴重影響視力乃至致盲的慢性疾病[1]。中華醫學會眼科學分會眼底病學組為規范DR的管理,分別在2014年和2022年發布了臨床診療指南,涵蓋了DR的定義、診斷、分期、治療等多方面的內容,并強調了預防、篩查、轉診、干預以及患者的整體管理。《我國糖尿病視網膜病變臨床診療指南(2022年)——基于循證醫學修訂》[2]特別關注了DR的激光和藥物治療,但對于較為嚴重的增生型DR(PDR)的手術治療原則和具體操作方法未作詳述。PDR標志著視網膜微血管病變已進入嚴重階段,對視力的影響極大,是糖尿病患者尋求眼科治療的主要原因之一,可能導致不可逆的視力損害。PDR可以分為以下三個階段:(1)增生早期:出現視網膜新生血管(NVE)或視盤新生血管(NVD)。當NVD覆蓋超過1/4~1/3的視盤面積(DA),或NVE覆蓋超過1/2 DA,或伴有視網膜前出血或玻璃體積血(VH)時,被稱為“高危PDR”。(2)纖維增生期:形成纖維膜,可能伴有視網膜前出血或VH。(3)增生晚期:出現牽拉性視網膜脫離(TRD),伴有纖維膜,可能合并或不合并VH,還包括虹膜和房角的新生血管[2-3]。在VH的情況下,深層的纖維血管膜和視網膜脫離往往難以直接觀察到,這增加了手術難度,不當處理可能會降低手術后視力恢復的效果,甚至引起并發癥。因此,需要明確手術時機、圍手術期血糖控制、手術計劃、手術技術選擇、纖維血管膜處理方法、聯合藥物或激光治療的應用,以及玻璃體填充物的選擇等關鍵點。鑒于此,中華醫學會眼科學分會眼底病學組、中國醫師協會眼科醫師分會眼底病專委會聯合組織了相關領域的專家,共同制定了《玻璃體切割手術治療2型糖尿病視網膜病變專家共識》,旨在為我國的眼底病專科醫生提供更具體的臨床指導。
1 共識編寫方法
1.1 制定共識的理論依據和方法學
本共識嚴格按照循證醫學指南原則制定,制定過程中參考了證據評價與推薦意見分級、制定和評價(GRADE)系統的理念和原則。共識專家組成員的遴選和組成、利益沖突管理、外部審查和組織批準均根據中華醫學會眼科學分會的政策和程序進行。
1.2 共識使用者和目標人群
本共識的適用范圍為DR玻璃體切割手術(PPV)治療的手術時機、圍手術期血糖管理、手術方式選擇、手術操作方案的制定等。其目標人群為中國眼底病專科醫師和從事眼底病專業的醫師。
1.3 共識專家組構成
共識專家組主要的臨床專家成員由中華醫學會眼科學分會眼底病學組、中國醫師協會眼科醫師分會眼底病專委會委員以及全國各省市具有多年玻璃體視網膜手術經驗、具有臨床影響力的醫生組成。
1.4 利益沖突說明
共識專家組成員(包括臨床專家和方法學專家)的利益沖突管理依據世界衛生組織以及國際指南聯盟對利益沖突管理的指導原則執行。共識專家組向中華醫學會眼科學分會報告了個人潛在的利益沖突(包含財務和專業相關的利益沖突)。所有成員均無實質性利益沖突。
1.5 臨床問題遴選和確定
方法學團隊與臨床專家對PPV治療DR相關的臨床問題進行了探討。經過對最初臨床問題的多輪修改和討論,最終確定了在本共識中要明確的9個臨床問題。
1.6 證據檢索及整合
共識的方法學團隊邀請中國臨床實踐指南聯盟與臨床專家合作,針對共識中的每一個臨床問題進行系統性證據檢索。檢索數據庫包括 PubMed、EMBASE和Cochrane Library,時間跨度為數據庫建立至2023年11月1日。檢索策略采用關鍵詞及關鍵詞結合自由詞的方式,在數據庫的題目和摘要中進行檢索。檢索詞包括 “proliferative diabetic retinopathy”、“diabetic macular oedema” 以及“vitrectomy”等(表1)。
除電子數據庫檢索外,共識專家組成員提供的關鍵研究以及已發表的系統評價中納入的研究也被作為補充資料。針對每一個臨床問題制定具體的納入和排除標準,并設計數據提取表格。在每個臨床問題上,優先納入系統評價;當系統評價無法回答關注的臨床問題時,則納入隨機對照試驗(RCT)。當RCT證據缺乏、間接性或證據體質量極低時,補充納入非隨機對照研究或其他觀察性研究證據。
兩名系統評價員獨立進行文獻篩查及數據提取;遇到分歧時,由第三名系統評價員協助解決。使用 RevMan 5.3 軟件,采用隨機效應模型進行薈萃分析。對于二分類結局,效應值采用比值比(OR)及其95%可信區間(CI);對于連續性結局,效應值采用均值差(MD)及其95%CI。在進行薈萃分析之前,充分考慮研究間的臨床異質性和方法學異質性。統計學異質性通過χ2檢驗和I2統計量評價。當χ2檢驗P<0.1且I2>50%時,認為存在統計學異質性。當研究間存在統計學異質性時,探索潛在的異質性來源,并根據異質性來源進行亞組分析。搜集到的證據主要圍繞2型糖尿病。
1.7 證據分級與推薦意見形成
采用《牛津循證醫學中心分級2011版》作為主要工具對本共識中的循證醫學證據進行等級評估(表2),同時也參考了GRADE系統。在評估證據等級時,考慮了偏倚風險、不一致性、間接性、不精確性和發表偏倚等因素,并據此對證據等級進行了相應的調整。
對于推薦意見的形成,共識專家組參考了GRADE系統中的要素,包括醫學干預的利弊平衡、證據質量、價值觀念與偏好、成本與資源耗費,以及可及性等因素,制定了推薦的方向和強度的標準。最終將推薦強度分為三個等級:強推薦、中等推薦和弱推薦(表3)。強推薦:共識臨床專家組對該推薦意見反映的最佳臨床實踐有高度的信心,建議目標用戶均采納該推薦意見。中等推薦:共識臨床專家組對該推薦意見反映的最佳臨床實踐有中等程度的信心,多數目標用戶應采納該推薦意見,但在執行過程中應注意考慮醫患共同決策。弱推薦:共識臨床專家組對該推薦意見有一定的信心,但應有條件地應用于目標群體,強調醫患共同決策的重要性。
共識專家組通過對研究證據進行公開討論后,以投票的形式達成了對推薦意見的共識。當專家組意見不一致時,則采用德爾菲問卷調查的方法[4]進行相應的修改和第二輪投票,直到達成共識。
1.8 共識的傳播和實施
共識發布后,將主要通過以下方式進行傳播和推廣:(1)專業期刊、網站和學術會議:將在相關專業期刊上發表,并通過官方網站和學術會議進行介紹。(2)共識推廣專場:有計劃地在我國部分地區組織共識推廣專場活動,確保臨床醫師及其他利益相關群體能夠充分了解并正確應用該共識。這些措施旨在確保共識的內容能夠廣泛傳播,并在實際臨床實踐中得到有效應用。
2 PDR的PPV治療原則和操作相關問題
問題1:2型糖尿病導致的PDR患者發生VH后,應在多長時間后考慮進行PPV?(鑒于1型糖尿病的發生率較低,相關文獻數量有限,納入的研究中2型糖尿病人群占比較大,因此對于此問題的證據總結主要針對2型糖尿病導致的PDR患者)
推薦意見:基于目前有限的證據,對于存在VH或合并血管纖維增生引起的視網膜牽拉及TRD的2型糖尿病PDR患者,建議積血早期進行PPV治療(中等推薦)。
兩項研究結果顯示,對于存在VH但尚未出現視網膜脫離的PDR患者,若在積血后的30 d內接受PPV治療,能夠顯著縮短患者低視力的持續時間,并且手術后1~2年的視力預后較好[5-6]。
一項回顧性隊列研究[5](證據等級Ⅲ)探討了PDR合并VH患者接受PPV的最佳時機。該研究納入了因PDR并發VH的患者,排除了并發視網膜脫離、既往有影響視力的其他視網膜病變或黃斑病變、各種類型青光眼以及隨訪時間少于24個月的患者。最終納入了符合標準的PDR合并VH患者67例70只眼,其中1型糖尿病患者4例5只眼(7.1%,5/70),2型糖尿病患者63例65只眼(92.9%,65/70)。患者按VH的時間分為三組:病程<1個月組22只眼,平均年齡45.23歲;病程1~3個月組23只眼,平均年齡45.78歲;病程>3個月組25只眼,平均年齡50.48歲。所有患者手術后均隨訪24~42個月。末次隨訪時,視力達到0.5及以上者的比例分別為:病程<1個月組41%、病程1~3個月組23%、病程>3個月組0%。病程<1個月組與其他兩組之間的差異均有統計學意義(P=0.03、P<0.001)。
另一項回顧性隊列研究[6](證據等級Ⅲ)比較了立即手術組(患者在積血30 d內接受了PPV治療)與延遲手術組(患者在積血30 d后接受了PPV治療)的視力改善情況。手術后12個月末次隨訪時,兩組患者的視力均較基線顯著改善(P=0.002、P<0.000 1),但兩組患者間視力無顯著差異(P=0.684)。考慮延遲手術組患者手術前視力狀況較差,即視力較差和(或)低水平視力維持時間較長,在隨訪終點時,立即手術組和延遲手術組的手術后視力曲線下面積無顯著性差異(P>0.05)。這表明,在積血30 d內接受PPV治療能夠顯著減少患者低視力的持續時間。
問題2:圍手術期的PDR患者目標血糖范圍是多少?如何有效控制其圍手術期血糖?( 由于目前尚無僅針對眼科手術的血糖管理指南/專家共識,故參考多個包含全身手術在內的圍手術期血糖管理指南/專家共識進行總結)
推薦意見一:建議PDR患者PPV前血糖盡可能控制在6.0~10.0 mmol/L之間,為預防低血糖,血糖允許值可放寬至13.9 mmol/L。如果有必要,可進行動態血糖監測。對于高齡患者或伴有多種合并癥的患者,為避免低血糖,建議血糖最高允許值為13.9 mmol/L,血糖監測頻率為0.5~2.0 h一次。對于擇期手術患者,如果隨機血糖水平≥10.0 mmol/L,則手術后建議每半小時監測一次血糖,直至血糖恢復至正常或降至 10.0 mmol/L 以下;如果血糖難以控制,應與其他相關科室進行會診,并與患者充分溝通可能的風險。對于不可擇期(增生晚期)的手術患者,建議更密切地監測血糖,以避免低血糖(低于 3.9 mmol/L)和酮中毒的發生(中等推薦)。
Cheisson等[7]研究(證據等級 V)指出,在進行眼科手術前,血糖范圍應控制在 6.6 ~10.0 mmol/L之間;血糖低于3.9 mmol/L時被認為是低血糖狀態,手術前應予以避免。2018 年《中國臨床實踐圍手術期血糖管理指南》[8](證據等級 V)建議,手術中血糖控制目標為 6.7~11.1 mmol/L,手術后血糖控制目標為<12.0 mmol/L;而對于 PDR 患者,手術后血糖不應超過 10.0 mmol/L。在建議的目標血糖范圍內,手術中應每1.0~2.0小時監測一次血糖,手術后應每4.0~ 6.0小時監測一次血糖。對于可擇期手術患者,如果隨機血糖≥12.0 mmol/L或糖化血紅蛋白≥9%,建議推遲手術時間。對于急診手術中出現酮癥酸中毒或高滲性昏迷的患者,如果患者的病情允許,建議在手術前首先糾正代謝紊亂、pH 值和滲透壓,直到恢復正常。中華醫學會麻醉學分會于 2016 年發布的《圍術期血糖管理專家共識》[9](證據等級 V)指出,圍手術期血糖應控制在 7.8~10.0 mmol/L之間;對于高齡、有嚴重合并癥、頻繁發作低血糖的患者,目標血糖范圍可適當放寬至不超過 13.9 mmol/L(表4)。對于正常飲食的患者,圍手術期應監測空腹血糖和三餐后的血糖;對于血糖高的患者,每 1.0~2.0小時監測一次血糖。
推薦意見二:建議對計劃接受PPV治療的 PDR 患者進行全面的手術前血糖水平評估及糖尿病相關并發癥檢查。對于那些伴有嚴重糖尿病并發癥(如糖尿病酮癥酸中毒、糖尿病腎病、糖尿病周圍神經病變、糖尿病心血管疾病等)的PDR患者,以及在圍手術期出現明顯且頻繁血糖波動的患者,建議咨詢內分泌科專家和其他相關并發癥的專業專家進行聯合管理(中等推薦)。
《中國臨床實踐圍手術期血糖管理指南》[8]指出,對于血糖波動較大或血糖水平不符合標準的圍手術期患者,建議咨詢內分泌科醫生并采取積極治療措施(證據等級 V)。對于腎功能正常的患者,手術前無需停用二甲雙胍治療(證據等級 V)。然而,對于腎功能異常且手術中需要全身麻醉的患者,應在手術前48 h停止使用二甲雙胍,并在手術后 48~72 h內繼續停用,直到腎功能恢復正常(證據等級 V)。若圍手術期隨機血糖兩次以上超過10 mmol/L,應請內分泌科會診,并通過降糖藥物或胰島素控制血糖(證據等級 V)。在低血糖的情況下,手術中輸液和胰島素的劑量應根據血糖水平來確定。中華醫學會麻醉學分會 2016 年發布的《圍術期血糖管理專家共識》[9]指出:當圍手術期血糖大于10.0 mmol/L時,應啟動胰島素治療(證據等級 V);對于正在接受靜脈輸注胰島素的患者,當血糖降至5.6 mmol/L以下時,應重新評估治療方案(證據等級 V);如果圍手術期血糖降至3.9 mmol/L或更低,應立即停用胰島素,并開始升血糖處理(證據等級 V)。
問題3:對于需要手術治療的PDR患者,是否推薦圍手術期聯合注射抗血管內皮生長因子(anti-VEGF)藥物?
推薦意見:PPV治療前 14 d內或手術完畢即刻注射anti-VEGF 藥物均可提高PDR患者的手術后視力,降低中央視網膜厚度,并有助于防止手術后近期的VH。因此,推薦PDR患者行PPV治療時,在圍手術期注射anti-VEGF藥物(中等推薦)。
共有22 項RCT( 1 396 只眼)比較了PPV前聯合注射anti-VEGF藥物與單純PPV治療 PDR 的臨床有效性[10-30](表5)。
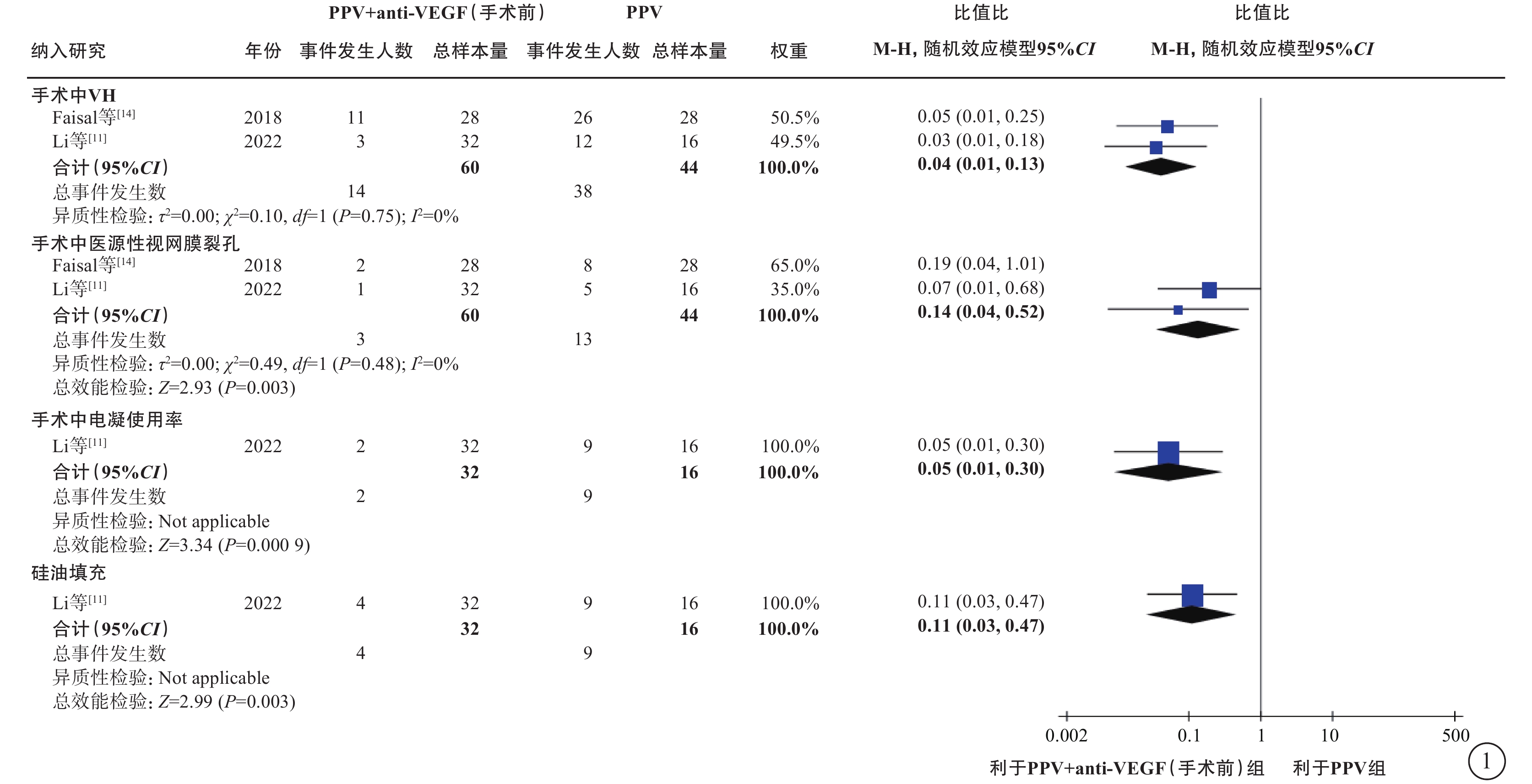
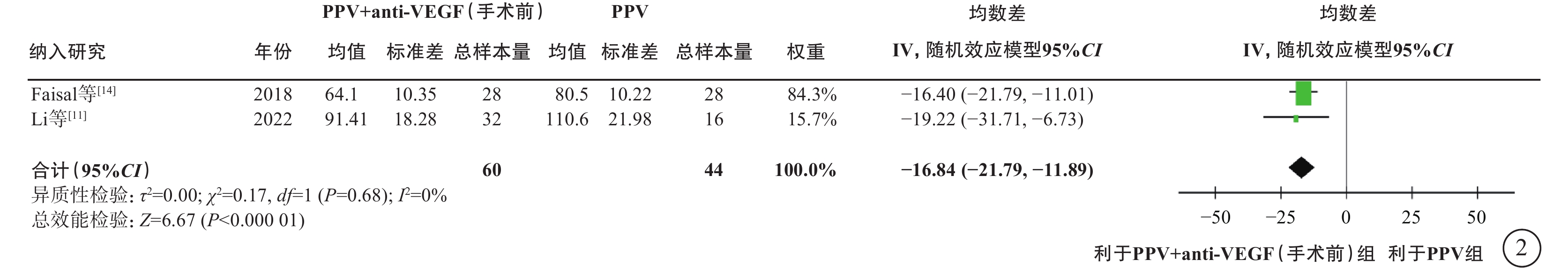
在PDR合并VH的人群中,薈萃分析(證據等級Ⅰ)結果顯示,與單純PPV相比,手術前聯合anti-VEGF藥物治療的患者具有以下優勢:手術中VH發生率較低(2 項研究[11, 14],OR=0.04,95%CI 0.01~0.13,P<0.000 01);醫源性視網膜裂孔發生率較低(2 項研究[11, 14],OR=0.14,95%CI 0.04~0.52,P=0.003);電凝使用率較低(1 項研究[11],OR=0.05,95%CI 0.01~0.30,P=0.000 9);硅油填充率較低(1項研究[11],OR=0.11,95%CI 0.03~0.47,P=0.003)(圖1);手術時間較短(2 項研究[11, 14],MD=-16.84 min,95%CI -21.79~-11.89,P<0.000 01)(圖2)。RCT證據(證據等級Ⅱ)顯示,與單純PPV相比,手術前聯合anti-VEGF藥物治療者,其手術后 1 周及1 、3 個月的VH發生率明顯更低(1 項研究[10],P= 0.021、 0.006、0.047);手術后 3 個月視力改善程度更好(1 項研究[11],P=0.04);兩者之間手術后視網膜脫離發生率無顯著差異(1 項研究[21],P=0.97)。
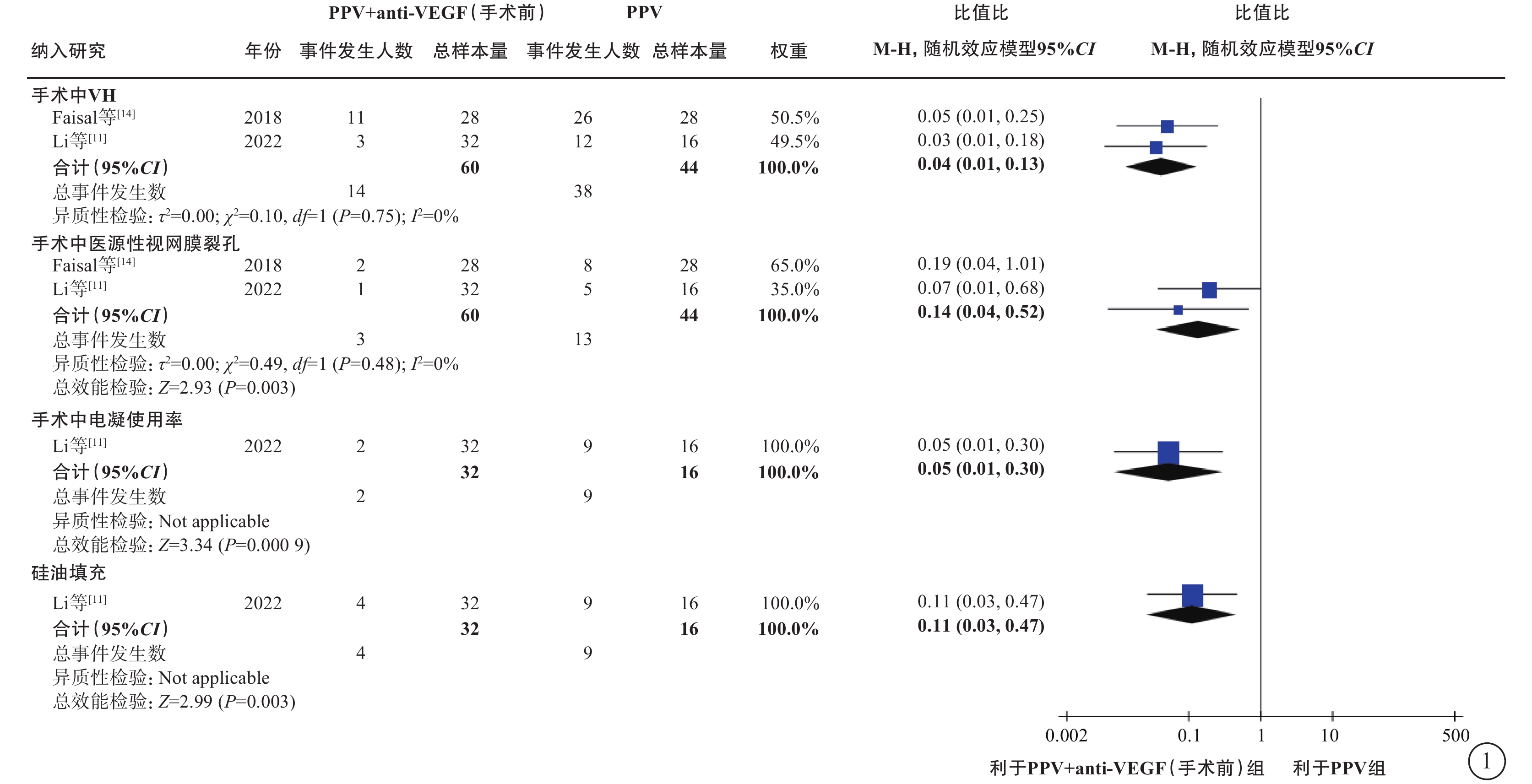 圖1
PDR合并VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術中情況比較 PDR:增生型糖尿病視網膜病變;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;Not applicable:不適用
圖1
PDR合并VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術中情況比較 PDR:增生型糖尿病視網膜病變;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;Not applicable:不適用
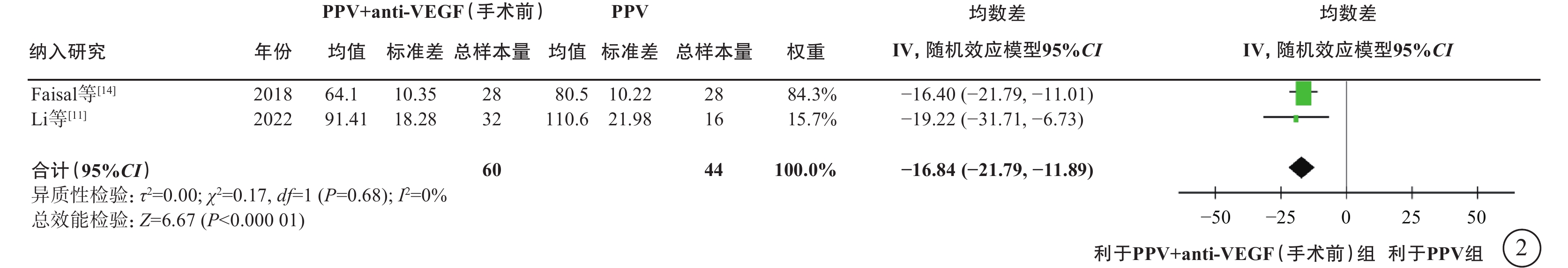 圖2
PDR合并VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術時間比較 PDR:增生型糖尿病視網膜病變;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間
圖2
PDR合并VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術時間比較 PDR:增生型糖尿病視網膜病變;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間
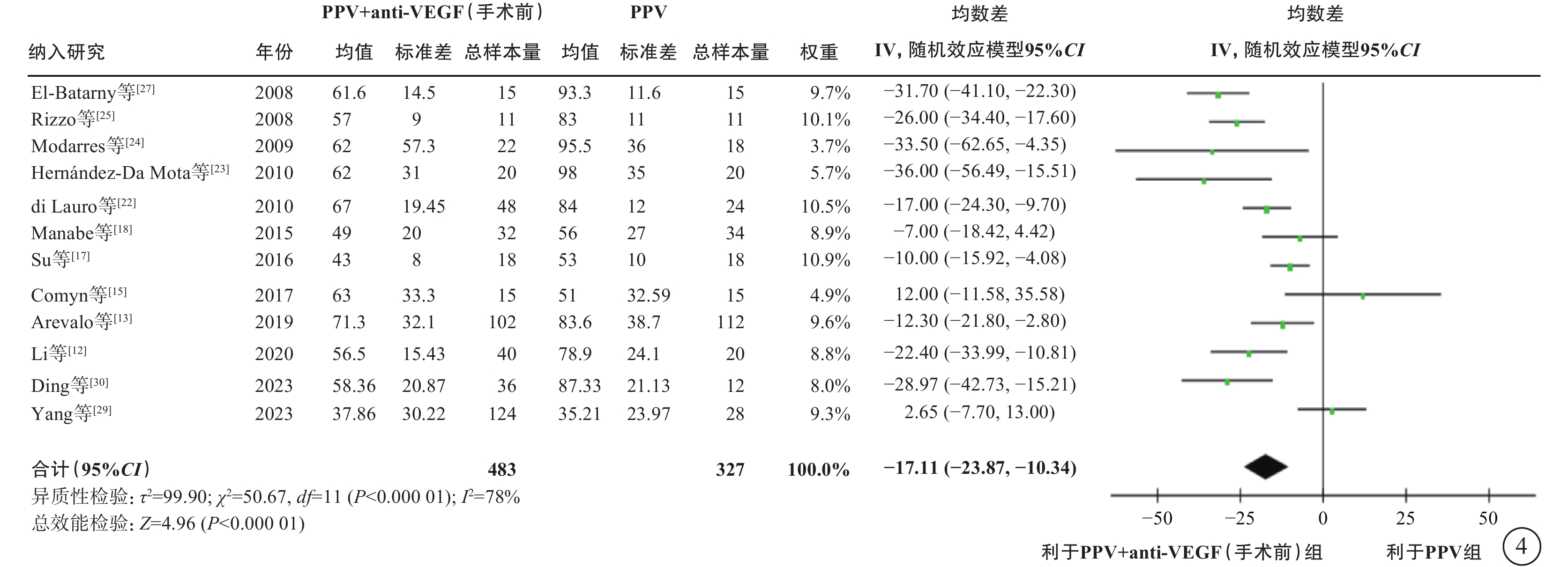
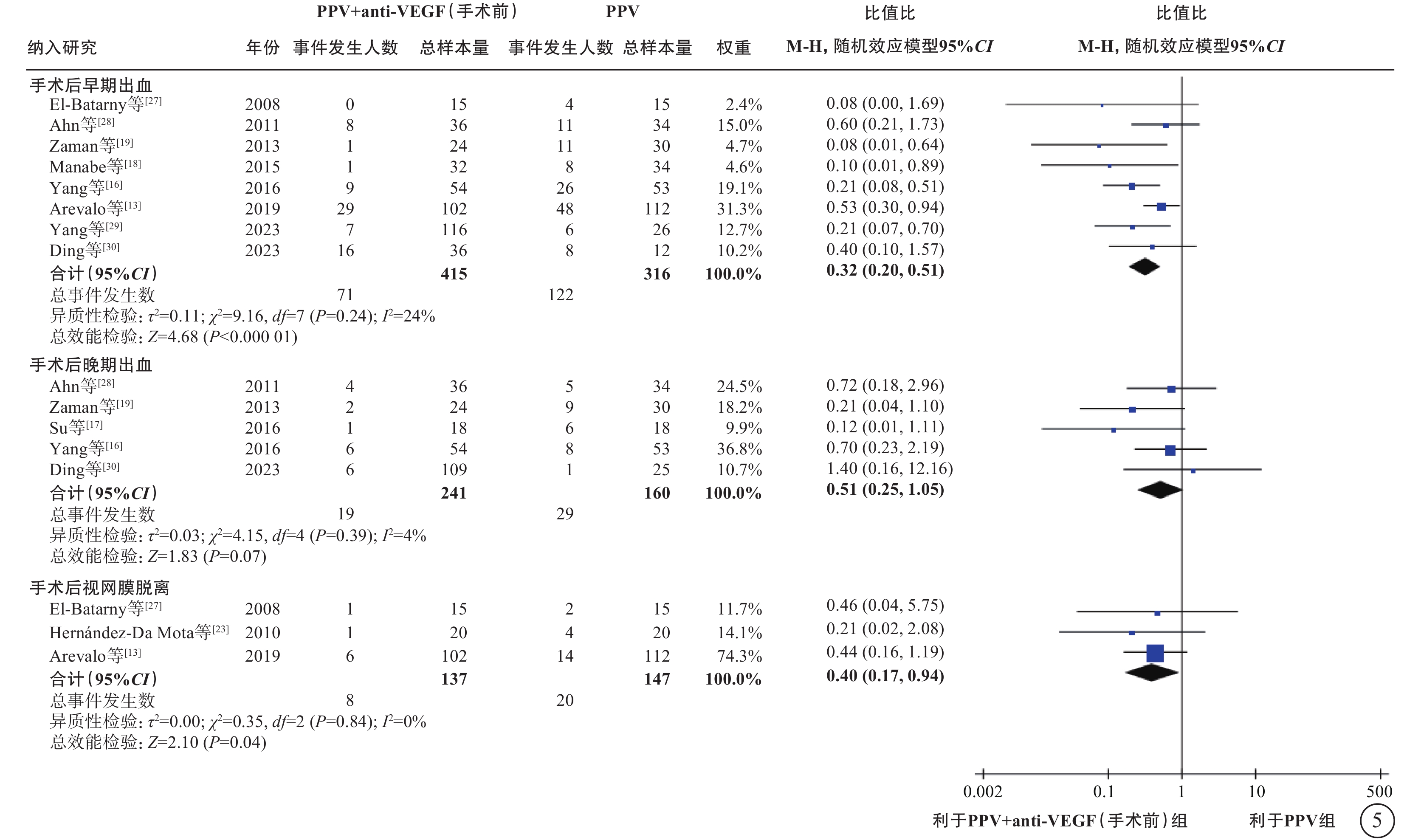
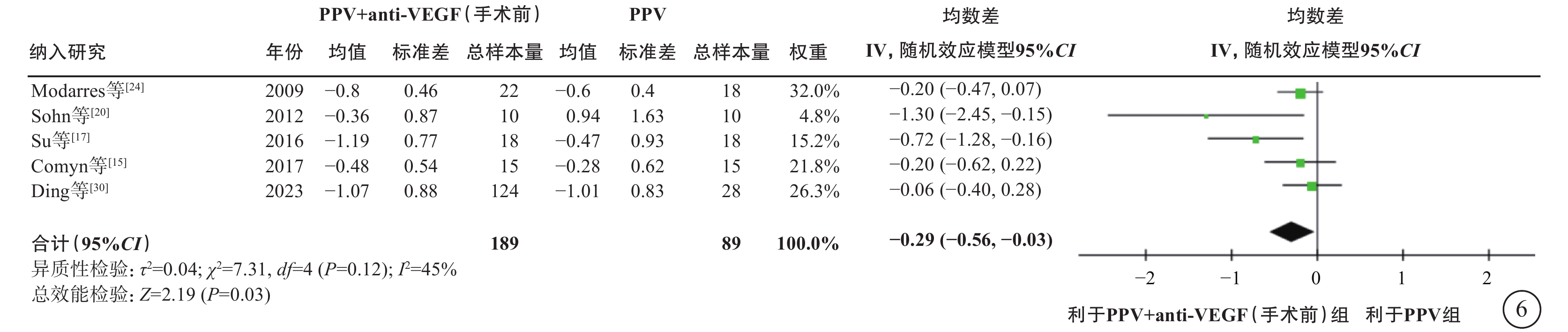
在PDR合并TRD伴或不伴VH的人群中,薈萃分析(證據等級Ⅰ)結果顯示,與單純PPV相比,手術前聯合anti-VEGF藥物治療者,手術中VH發生率較低(9 項研究[12-13, 16-17, 22-23, 26-27, 29],OR=0.18,95%CI 0.09~0.35,P<0.000 1);電凝使用率較低(3 項研究[13, 17, 22],OR=0.19,95%CI 0.05~0.79,P=0.02);硅油填充率較低(9項研究[13, 15, 17-18, 22, 24, 27, 29-30],OR=0.38,95%CI 0.17~0.87,P=0.02);氣體填充率(2項研究[29-30],OR=0.91,95%CI 0.42~1.94,P=0.80)和醫源性視網膜裂孔發生率(3 項研究[18, 26-27],OR=0.82,95%CI 0.31~2.13,P=0.68)在兩組間無統計學差異(圖3);手術時間較短(12項研究[12-13, 15, 17-18, 22-25, 27, 29-30],MD=-17.11 min,95%CI -23.87~-10.34,P<0.000 01)(圖4);手術后視網膜脫離發生率較低(3項研究[13, 23, 27],OR=0.40,95%CI 0.17~0.94,P=0.04)(圖5);手術后早期出血(4 周及 4 周內復發)發生率較低(8 項研究[13, 16, 18-19, 27-28, 29-30],OR=0.32,95%CI 0.20~0.51,P<0.000 01)(圖5);手術后晚期出血發生率(4 周以上復發)在兩組間無顯著差異(5項研究[16-17, 19, 28, 30],OR=0.51,95%CI 0.25~1.05,P=0.07)(圖5);手術后視力改善程度較好(5項研究[15, 17, 20, 24, 30],MD=-0.29,95%CI -0.56~-0.03,P=0.03)(圖6)。
 圖3
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術中情況比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;Not estimable:不可估
圖3
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術中情況比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;Not estimable:不可估
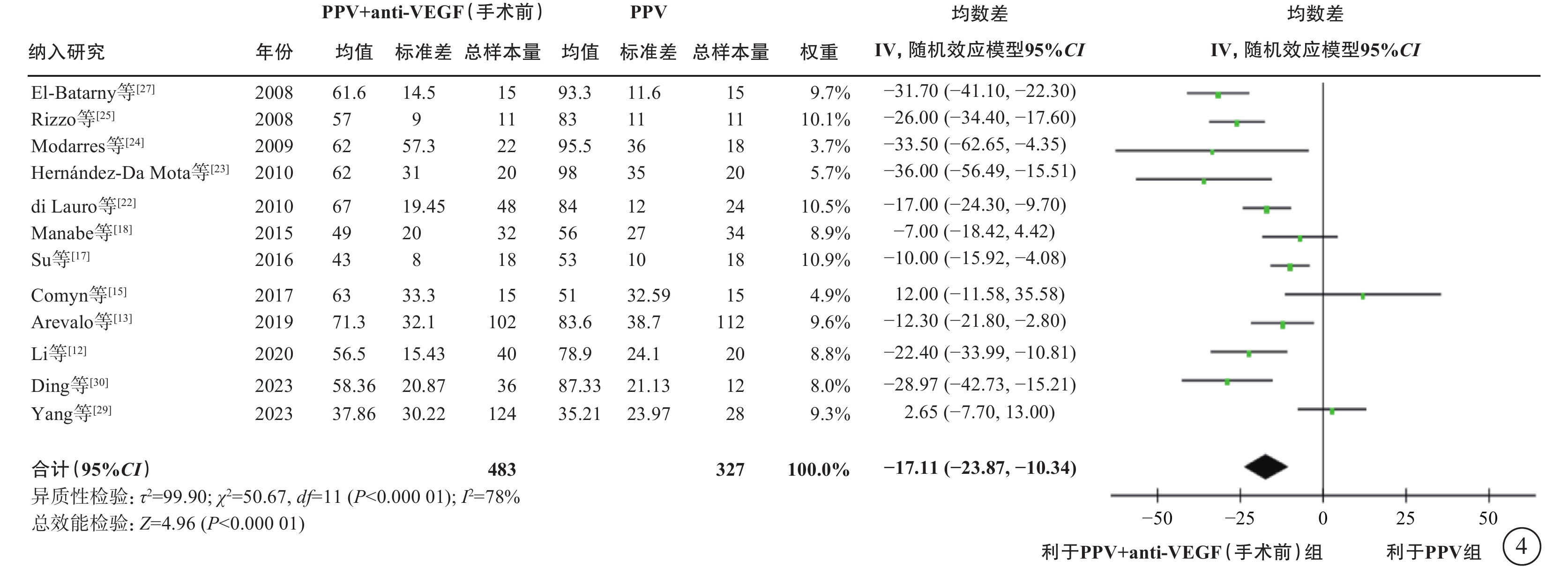 圖4
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術時間比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間
圖4
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術時間比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間
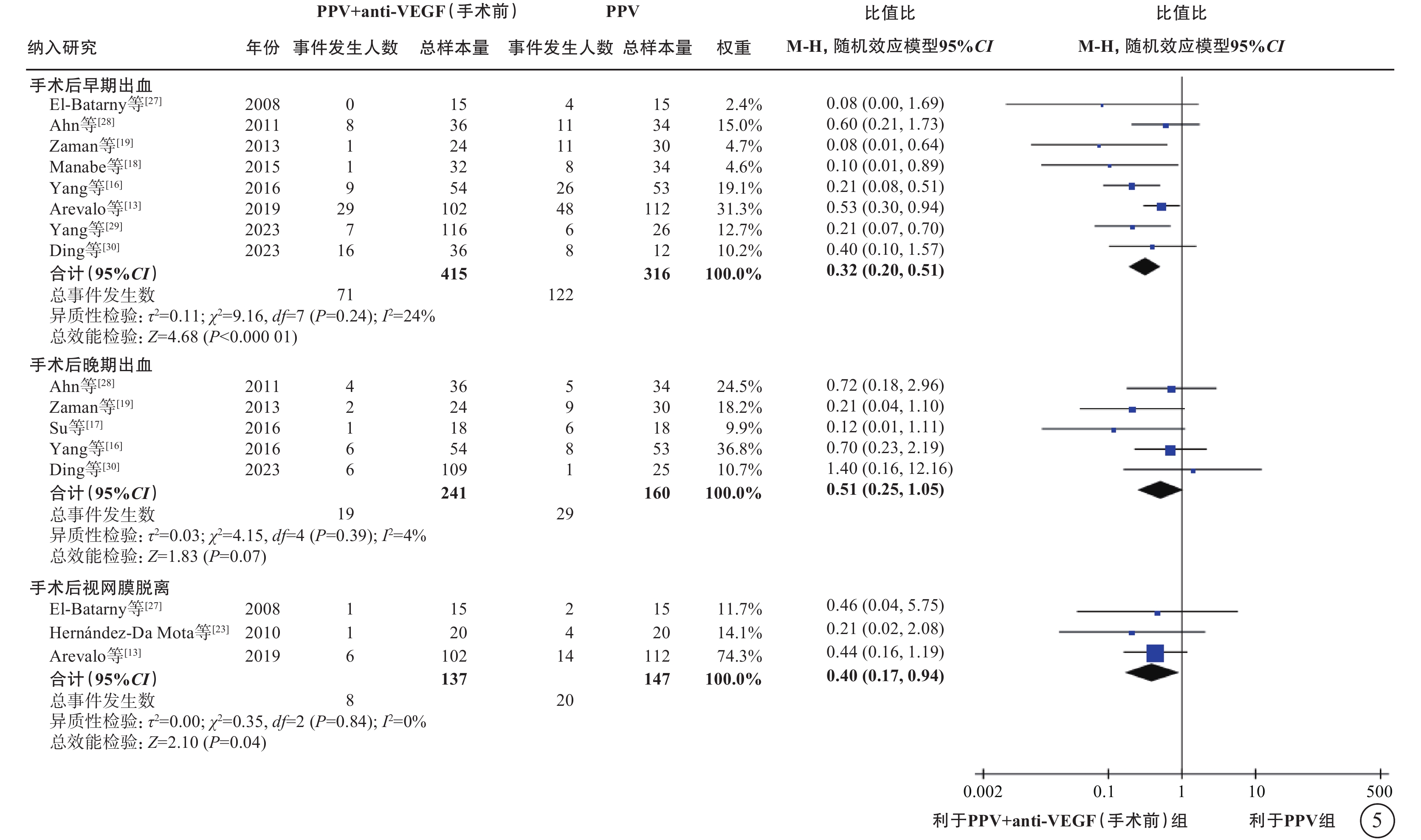 圖5
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術后結果比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;早期出血:手術后4周及4周內VH復發;晚期出血:手術后4周后VH復發
圖5
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術后結果比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;早期出血:手術后4周及4周內VH復發;晚期出血:手術后4周后VH復發
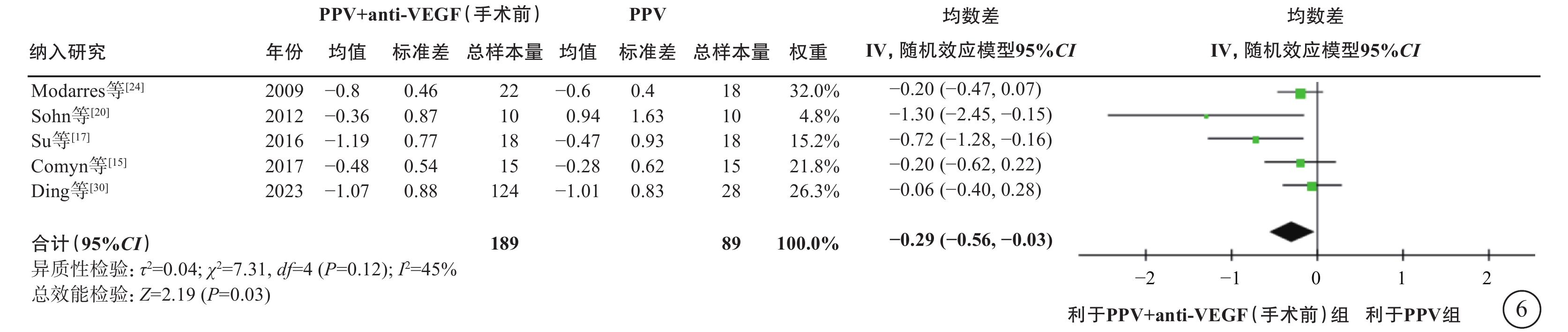 圖6
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療后視力變化值(logMAR單位)比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;logMAR:最小分辨角對數;CI:可信區間
圖6
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療后視力變化值(logMAR單位)比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;logMAR:最小分辨角對數;CI:可信區間
三項RCT和一項網狀薈萃分析比較了PPV完畢時聯合anti-VEGF藥物與單純PPV治療PDR的臨床有效性。一項網狀薈萃分析[31](證據等級Ⅰ)納入了26 項RCT 原始研究,包括1 802例需接受PPV治療的PDR伴TRD或不可吸收VH患者,比較了手術前1~5 d、手術前6~14 d、手術前>14 d及手術完畢時注射anti-VEGF 藥物的臨床結局。結果表明,手術前注射anti-VEGF藥物與手術完畢時注射anti-VEGF藥物在最佳矯正視力(BCVA)、手術后VH復發率和手術中出血發生率方面均無顯著差異。一項 RCT[32](證據等級Ⅱ)納入了 84例嚴重PDR患者(84 只眼),所有患者均表現為不吸收的VH和不伴TRD的纖維血管增生。該研究將患者隨機分為兩組,試驗組于手術前 3~5 d和手術完畢時均接受anti-VEGF藥物注射;對照組僅手術前3~5 d接受anti-VEGF藥物注射。手術后1個月,試驗組VH發生率較低(9.3% vs. 19.5%,P=0.046),BCVA[以最小分辨角對數(logMAR)視力記錄]較好(0.57±0.11 vs. 0.71±0.15,P=0.019);但手術后 3 、 6 個月,兩組間VH發生率和BCVA的差異均無統計學意義。手術后1、3個月,試驗組中央視網膜厚度更薄,但手術后 6 個月兩組之間無差異。總體而言,與僅在PPV前聯合注射anti-VEGF藥物相比,手術完畢時聯合注射anti-VEGF 藥物對嚴重PDR患者手術后早期(1 個月)的VH、視力提升及手術后 3 個月內視網膜水腫具有較好的改善作用。另外兩項RCT(證據等級Ⅱ)亦顯示,相較于不注射anti-VEGF藥物,手術完畢時即刻注射anti-VEGF 藥物可顯著降低手術后24周或1年內患者的中央視網膜厚度[33-34],顯著提高患者24周內的BCVA,并降低VH復發率[34]。
問題4:對于需要接受PPV治療的PDR患者,是否推薦其手術前行全視網膜激光光凝(PRP)治療?
推薦意見:與anti-VEGF藥物治療相比,PDR患者在PPV前接受PRP治療并不會顯著改善其視力。在決定是否進行PRP治療時,應依據熒光素眼底血管造影和(或)光相干斷層掃描血管成像(OCTA)對視網膜缺血狀況的評估結果。對于視網膜缺血癥狀不斷發展,且OCTA檢測顯示存在大面積無灌注區的患者,可以考慮在手術前增加PRP治療。然而,需要特別注意的是,對于合并TRD的患者,手術前行PRP治療可能會增加視網膜裂孔的風險,因此在進行此類治療時需謹慎權衡(中等推薦)。
自從anti-VEGF藥物上市以來,多個研究比較了PDR患者接受anti-VEGF藥物與PRP治療的獲益。一項RCT[35-36](Diabetic Retinopathy Clinical Research Network Protocol S研究,證據等級Ⅱ)納入了305例PDR患者394只眼,比較了單純anti-VEGF藥物與PRP治療后視力獲益的差異。結果顯示,治療后2年,anti-VEGF藥物治療組和PRP組視力字母評分較基線分別改善2.8、0.2(非劣效P<0.001);治療后5年,anti-VEGF藥物治療組和PRP組視力字母評分較基線分別改善3.1±14.3、3.0±10.5(P=0.68)[36-37],但anti-VEGF藥物治療組視野敏感性變化優于PRP組。另一項RCT[38-39](證據等級Ⅱ)表明,治療后12個月,anti-VEGF藥物治療組和PRP組視力字母評分較基線分別改善1.6和-3.9(P=0.049 5)。這說明,PDR患者PRP治療后視力差于anti-VEGF藥物。
一項隊列研究[37, 40](證據等級Ⅲ)納入106例PDR患者130只眼,比較了PPV聯合手術前PRP(60例67只眼)與單純PPV(46例63只眼)治療后6個月患者的視力變化情況(以logMAR為單位),并進行了長達1年的隨訪。結果顯示,手術前聯合PRP治療組在手術后6個月時視力從基線1.47±0.16提升為0.69±0.09 (P<0.000 1),而單純PPV治療組手術后6個月時視力從基線0.91±0.18提升至0.69±0.14(P=0.121)。結果表明,與單純PPV相比,PPV聯合手術前PRP治療可改善患者手術后視力,但差異無統計學意義。
問題5:PPV中處理PDR患者的纖維血管膜時,選擇膜分割還是膜清除技術?
推薦意見:在處理PDR患者的纖維血管膜時,應以確保手術安全性為首要原則,盡量將膜清除干凈。膜分割技術,即保留部分膜的方法,已被證明能夠改善患者的視力,并且造成裂孔的風險相對較小。這種方法同樣適用于那些新生血管膜上存在較多粗大血管的患者。對于手術經驗相對較少的醫生,可以從膜分割技術開始嘗試,并逐漸向膜清除技術過渡,以積累經驗和提高手術技巧(中等推薦)。
纖維血管膜是PDR患者VH的主要病理基礎,其有效清除在手術治療中占據核心地位。在PPV過程中,針對纖維血管膜的清除策略包括經典的Enbloc技術及其改良形式,即膜分割(membrane segmentation)與膜清除(delamination)技術[39-41]。Enbloc技術作為一種綜合性手段,強調在初始階段即進行精細的視網膜膜分割,隨后實施PPV以徹底清除膜組織[39]。而膜分割與膜清除作為改良Enbloc技術(modified Enbloc excision technique)的核心要素,為復雜膜性病變的處理提供了更為精細與靈活的操作方案[40]。膜清除技術通常在玻璃體切除的主體部分完成后實施,利用高轉速玻璃體切割頭、精密眼內剪刀或雙手協同的剝膜技術,實現對膜組織的直接、高效清除[41]。膜分割技術是在清除大部分玻璃體切除后將整片膜分割成數片孤立的小片機化膜,隨后逐一進行安全去除或根據具體情況選擇保留部分小片膜[42]。這一策略尤其適用于膜與視網膜緊密粘連、難以直接剝離的復雜情況,通過分割技術可以有效減輕牽拉力量,減少視網膜損傷的風險。在PPV中應用膜分割技術,不僅能夠有效緩解增生膜對視網膜的牽拉作用,保護視網膜結構的完整性,還能顯著降低手術過程中醫源性視網膜裂孔的發生率。此外,該技術還有助于減少因硅油或氣體填充等后續治療措施可能引發的并發癥,提高手術的整體安全性與療效[42-43]。
1994年Han等[40]、1997年Meier和Wiedemann[44]以及2002年Kakehashi[45]發表的三項病例系列研究(證據等級Ⅳ),均提供了強有力的證據表明,與傳統Enbloc技術相比,改良Enbloc技術在治療PDR患者時,能夠達到相似的視力改善效果,且伴隨著更高的視網膜復位率。尤為值得注意的是,這一技術革新顯著縮短了手術時長,同時并未增加手術并發癥的發生率,體現了其在提升治療效率與安全性方面的雙重優勢[40, 44-45]。
2004年黎曉新等[41]開展的一項回顧性隊列研究(證據等級Ⅲ)納入276例伴有纖維血管膜的PDR患者(296只眼),對比分析膜分割(106例110只眼)與膜清除(170例186只眼)這兩種手術方法的治療效果。結果顯示,與膜清除組相比,膜分割組在減少醫源性視網膜裂孔的發生率上展現出了顯著優勢(35.5% vs. 54.3%,P<0.01);此外,盡管膜分割組手術后視網膜再出血發生率(25.5%)略低于膜清除組(28.0%),但差異無統計學意義(P>0.05)。值得注意的是,兩組患者在手術后的視力改善上并未表現出顯著差異,這一結果表明,無論是膜分割還是膜清除,均能有效促進患者視力的恢復。這提示,在進行PDR手術時,初學者可以從膜分割技術入手,因其相對較低的醫源性視網膜裂孔風險,有助于在安全的前提下逐步掌握手術技巧,為患者帶來更佳的治療效果。
2021年鄭傳珍等[46]的病例系列研究(證據等級Ⅳ)探討了膜分割技術在治療伴有VH及TRD的嚴重PDR患者中的手術后效果。其聯合了手術前3 d玻璃體腔注射anti-VEGF藥物治療,并秉持“最小量化”PPV理念,采用27G玻璃體切割系統完成標準三通道PPV。手術中,研究團隊運用膜分割技術,以解除視網膜牽拉為主要目標,而非盲目追求增生膜的徹底清除。通過(18.8±9.7)(6~33)個月的隨訪觀察,該研究發現,患者BCVA(以logMAR視力記錄)較手術前顯著提升,從手術前的1.90(1.30,2.30)逐步提升至手術后1周的1.00(0.70,1.90)、手術后1個月的0.80(0.50,1.30),而手術后3、6個月均穩定在0.70(0.40,1.20)(各時間點P值均<0.01),彰顯了視力恢復的顯著性與持續性。此外,首次隨訪時視網膜復位率92.5%,至末次隨訪時提升至96.2%。該研究表明,PPV中應用膜分割技術不僅可解除增生膜對視網膜的牽拉,還能減少醫源性視網膜裂孔的發生。
問題6:PDR患者行PPV治療時如何選擇填充物?
推薦意見:建議對于患有PDR且在手術前已存在視網膜裂孔,或手術過程中產生醫源性視網膜裂孔或視網膜切開的患者,在進行PPV時使用長效氣體(如20%SF6、16%C2F6或14%C3F8[47-49])或硅油進行眼內填充。而對于沒有視網膜裂孔的PDR患者,在充分解除牽拉因素后,可以保留使用常規的眼內灌注液。對于合并有虹膜新生血管的少數患者,仍然可以選擇硅油填充。對于使用長效氣體或硅油填充的患者,手術后應嚴密監測眼壓(中等推薦)。
一項回顧性隊列研究[50](證據等級Ⅲ)納入了接受PPV治療的PDR合并VH患者73例73只眼,其中18只眼(24.7%)手術中未使用填充物,18只眼(24.7%)采用空氣填充,15只眼(20.5%)采用C3F8氣體填充,22只眼(30.1%)采用硅油填充,并以此分為四組。手術后1個月隨訪時,無填充組視力改善顯著優于C3F8氣體填充組;但手術后6個月隨訪時,無填充組、空氣填充組、C3F8氣體填充組三組患者間視力改善程度無明顯差異。四組手術后分別有11.1%、11.1%、6.7%和9.5%的患者出現復發性VH,但其VH復發率差異無統計學意義。手術后6個月隨訪時,無填充組、空氣填充組、C3F8氣體填充組和硅油填充組患者視力分別較基線改善0.98、0.94、0.97、0.19 logMAR單位。除硅油填充組患者視力改善幅度較小(僅為36%)外,其余三組患者視力改善幅度達67%~89%。該研究表明,PPV治療PDR合并VH時采用眼內填充物并不能減少手術后VH發生率,對未合并視網膜裂孔的PDR患者可以不使用眼內填充物。
一項回顧性病例系列研究[42](證據等級Ⅳ)納入PDR合并TRD患者42例50只眼,在PPV中采用膜分割技術去除增生膜。手術中12只眼發生醫源性視網膜裂孔,給予氣體或硅油填充;未發生醫源性視網膜裂孔的患眼給予灌注液填充。手術后隨訪9.7(3~29)個月,患者平均BCVA由手術前0.03±0.25提高到手術后0.17±0.78,68.0%的患眼視力提高,24.0%的患眼視力不變,8.0%的患眼視力下降。一次手術后視網膜復位率為84.0%,其中灌注液填充組(未發生醫源性視網膜裂孔)患眼復位率為89.5%;氣體或硅油填充組(發生醫源性視網膜裂孔)隨訪期間患眼復位率為66.7%,隨訪期結束時最終視網膜復位率為96.0%(2只眼放棄治療)。手術后34.0%(17/50)的患眼發生VH,其中3只眼VH自行吸收,余下14只眼給予anti-VEGF藥物和(或)玻璃體腔灌洗手術治療后積血吸收。發生并發癥的49只眼中,灌注液、氣體、硅油填充分別為28、11、10 只眼。該研究表明,對于未發生醫源性視網膜裂孔的患者可以不進行氣體或硅油填充。
一項回顧性隊列研究[51](證據等級Ⅲ)納入年齡50.44(20~82)歲的接受PPV治療的PDR患者451例536只眼,其中282只眼保留灌注液,138只眼填充氣體(包括空氣、SF6、C2F6和C3F8),116只眼填充硅油,隨訪時間15.2(2~53)個月,探索PPV后使用不同眼內填充物的治療效果。該研究發現,手術前或手術中是否合并視網膜裂孔是PDR患者手術中選擇眼內填充物的重要因素。對于手術中發現視網膜裂孔或手術中造成醫源性視網膜裂孔、視網膜切開的患者,一般采用硅油或膨脹性氣體填充;不存在視網膜裂孔的患者,在有效解除牽拉因素的基礎上,保留灌注液填充;對于少數合并虹膜新生血管等情況仍可選擇硅油填充。
一項RCT[52](證據等級Ⅱ)納入302例伴有TRD或纖維增生膜的PDR患者,手術中隨機接受硅油填充123只眼,14%~16% C3F8填充135只眼。其觀察發現,填充C3F8的患者手術后6個月時視力較好(logMAR視力中位數0.24,95%CI 0.02~0.46,P<0.05),兩組患者手術中視網膜裂孔的發生率相當,手術時間、手術中及手術后并發癥等觀察指標的差異均無統計學意義。該研究認為,對于伴有TRD或纖維增生膜的PDR患者,應當考慮選擇C3F8為一線填充物。當發生視網膜裂孔時,對于單眼患者或伴有新生血管性青光眼、眼球癆(phthisis bulbi)的高風險、無法解除玻璃體視網膜牽拉或視網膜無法解剖復位的情況下,硅油仍是填充物的一線選擇。
問題7:對于糖尿病黃斑水腫(DME),是否推薦PPV治療?
推薦意見:推薦存在牽拉因素的DME(T-DME)患者行PPV治療。對于非牽拉的難治性DME患者(激光光凝無效、anti-VEGF藥物治療無效以及抗炎治療效果不好),可選擇PPV治療(中等推薦)。
對于T-DME患者,PPV作為一線治療已被寫入多個指南和共識中[2, 53-54]。中華醫學會眼科學分會眼底病學組2023年發布的《我國糖尿病視網膜病變臨床診療指南(2022年)——基于循證醫學修訂》[2] 中明確指出,對于因玻璃體視網膜交界面異常引起的DME, 通過PPV解除玻璃體界面的牽拉,是有效緩解黃斑水腫的一種方法;對于非手術治療效果不佳的持續性DME患者,PPV聯合內界膜剝除能有效改善黃斑水腫(證據等級Ⅱ)。歐洲視網膜病專家組在《糖尿病黃斑水腫治療指南(2017年)》[53]中也指出,對存在玻璃體視網膜牽拉的患者,PPV的優勢顯而易見,尤其是存在前后縱向牽拉的DME患者。英國共識工作組2020年更新的《糖尿病視網膜病變和糖尿病黃斑水腫治療路徑管理》[54]指出,應用PPV治療T-DME可有效改善黃斑的解剖結構異常,可以預防視網膜脫離等嚴重并發癥的發生。
非牽拉的持續不吸收的黃斑水腫也可以考慮PPV,但需注意存在視力下降的風險[2]。Raizada等[55]在2015年的一項RCT(證據等級Ⅱ)中納入了44例(44只眼)激光光凝治療無效的非牽拉性DME(nT-DME)患者,其中22例(22只眼)接受了3次anti-VEGF藥物治療(anti-VEGF組),22例(22只眼)接受了PPV聯合內界膜剝除手術治療(PPV組),平均隨訪5.81個月。結果顯示,治療后120 d,PPV組有59.1%(13只眼)視力改善,18.2%(4只眼)視力無變化,22.7%(5只眼)視力下降,手術后視力相對手術前基線改善明顯(P=0.028);治療前后的平均視力差異為0.189 logMAR單位(95%CI 0.021~0.356)。anti-VEGF組有72.8%(16只眼)視力改善,13.6%(3只眼)視力無變化,13.6%(3只眼)視力下降;治療后視力相對基線改善明顯(P=0.018 1),治療前后的平均視力差異為0.203 logMAR單位(95%CI 0.036~0.369)。PPV組患者中央視網膜厚度由手術前410.1 μm顯著降至手術后248.8 μm(P<0.000 1),治療前后降幅平均值為161.4 μm(95%CI 3.28~219.45);anti-VEGF組由基線432.7 μm顯著降至治療后324.3 μm(P<0.000 1),治療前后降幅平均值為108.5 μm(95%CI 62.20~154.71)。但值得注意的是,PPV組與anti-VEGF組患者視力改善程度、中央視網膜厚度治療前后的降幅平均值比較,差異無統計學意義(P>0.05)。這說明,對于激光光凝治療無效的nT-DME患者,PPV治療后4個月中央視網膜厚度較手術前明顯下降,手術后視力較手術前明顯提升,但與單純anti-VEGF藥物3次治療相比,中央視網膜厚度和視力改善程度無顯著差異。
問題8:伴或不伴黃斑前膜(ERM)的DME患者行PPV治療時,是否聯合內界膜剝除?
推薦意見:伴有ERM的DME患者行PPV治療,剝除ERM時是否同時剝除內界膜沒有明確結論,不形成推薦意見。如不伴有ERM,只伴有內界膜增厚,則推薦PPV時剝除內界膜。
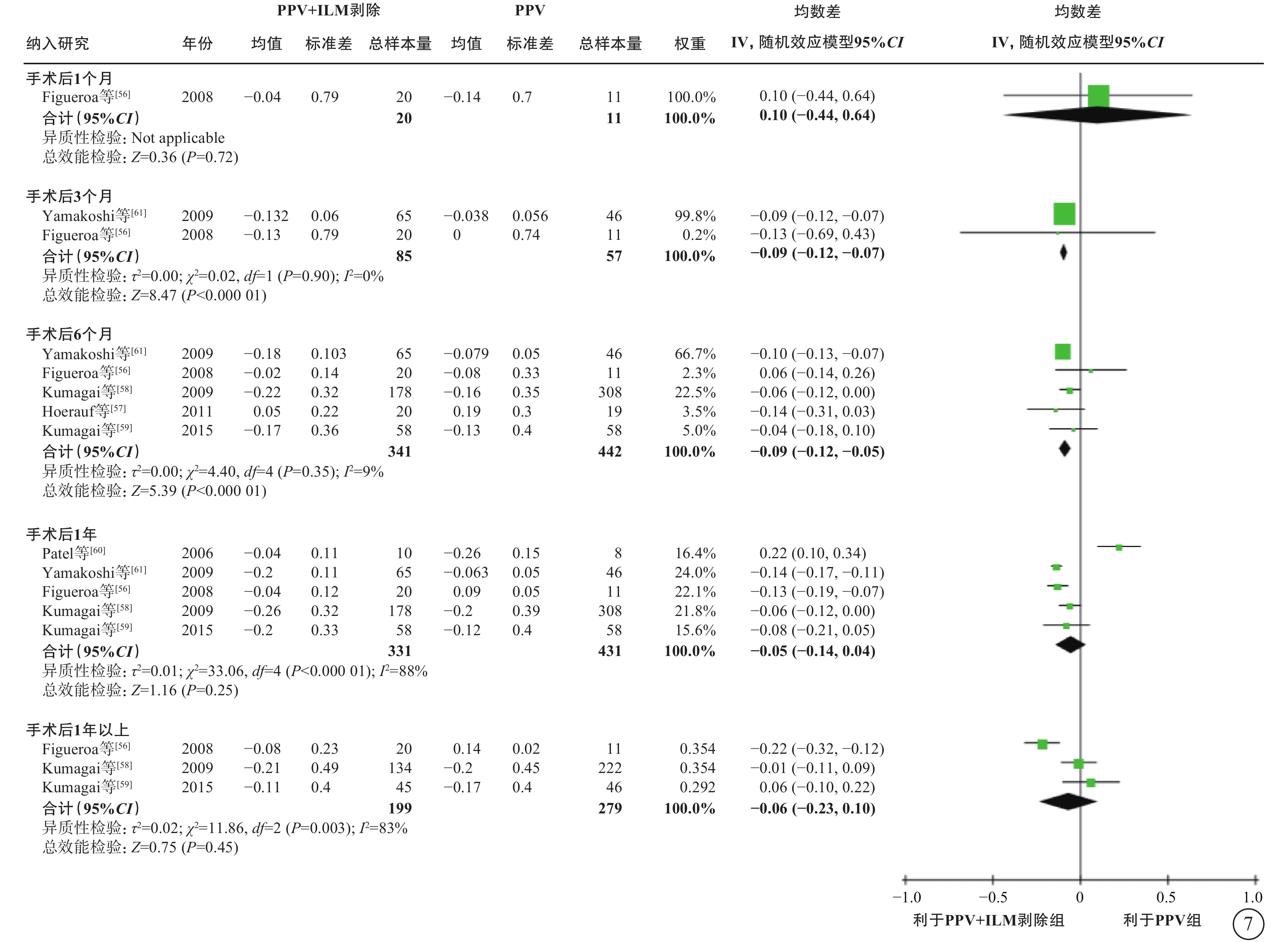
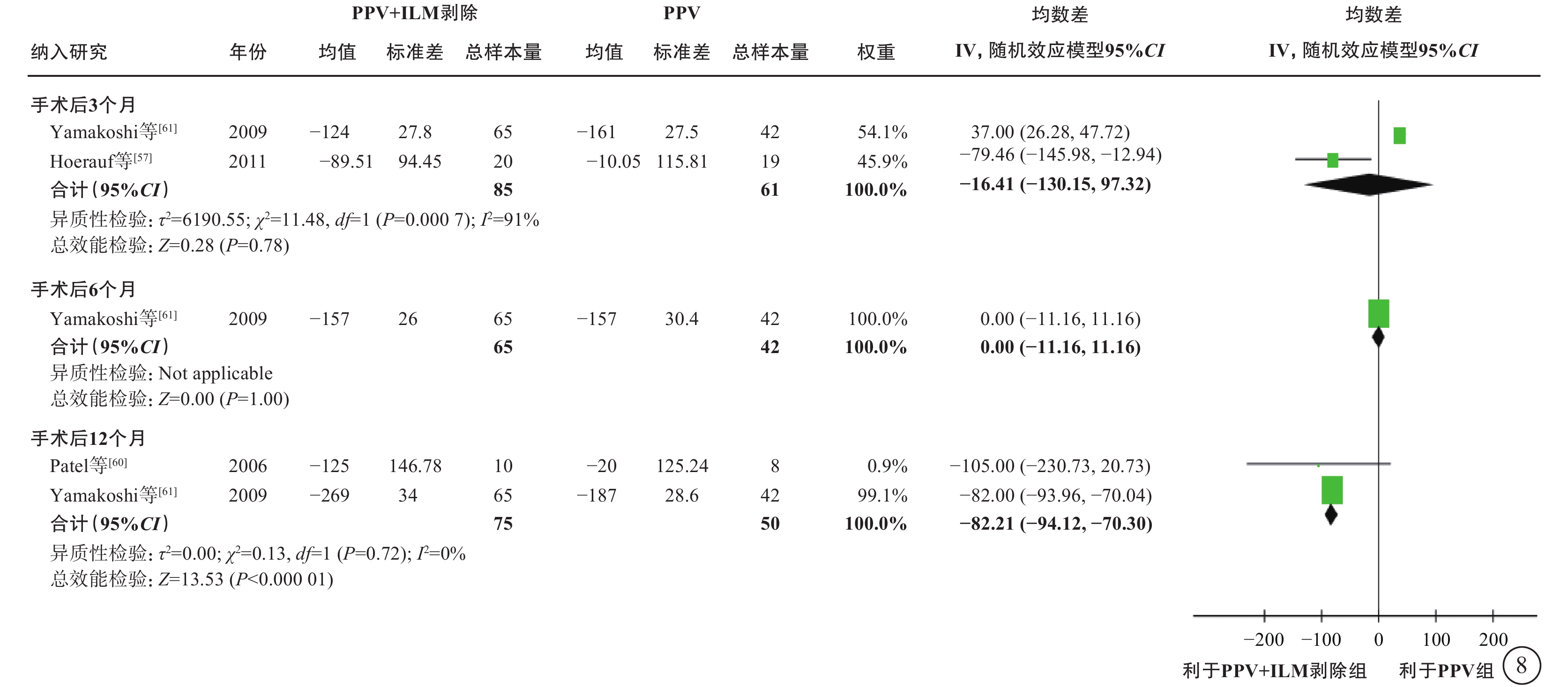
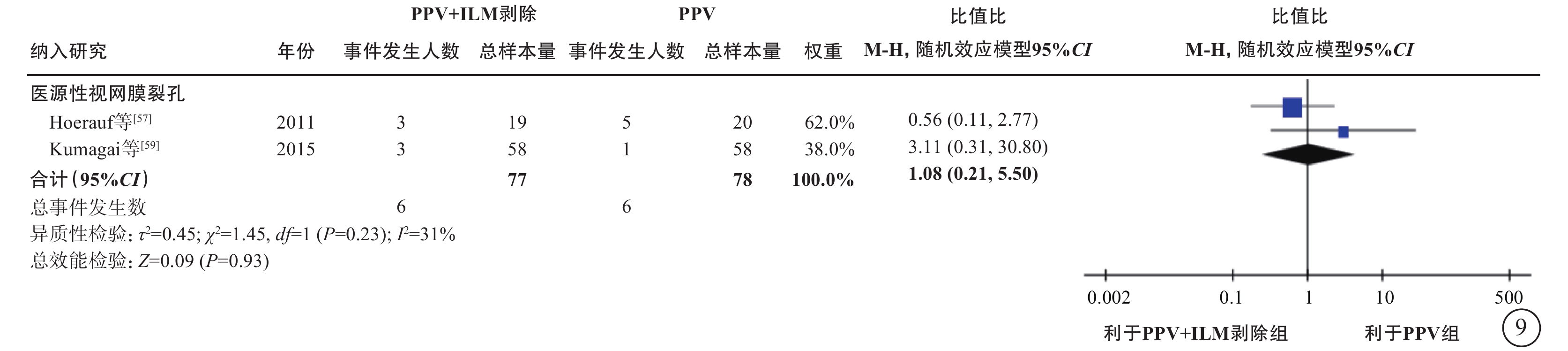
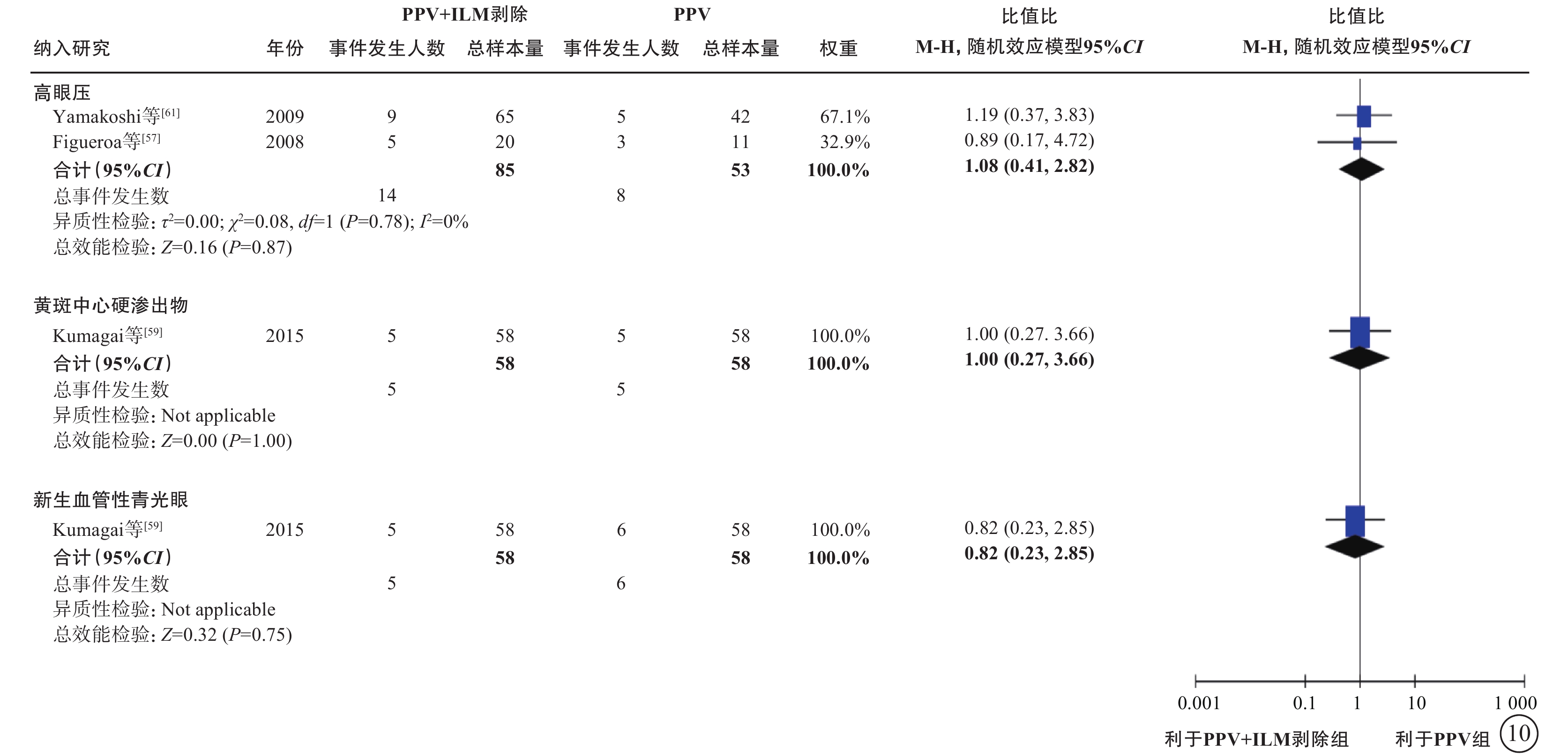
6項研究[56-61](包括2項RCT和4項觀察性研究,801只眼)探討了nT-DME患者行PPV治療時,是否需同時剝除內界膜(表6)。通過薈萃分析(證據等級Ⅲ)對比PPV聯合內界膜剝除和單純PPV的手術后相對手術前基線視力的變化值、中央視網膜厚度變化值及手術中和手術后并發癥發生情況。對于視力變化值,分析結果顯示:手術后1個月的視力較基線無顯著差異(1項研究[56],P=0.72);手術后3、6個月,PPV聯合內界膜剝除組的視力改善均優于單純PPV組(手術后3個月:2項研究[56, 61],-0.09 logMAR單位,95%CI -0.12~-0.07,P<0.000 01;手術后6個月:5項研究[56-59, 61],-0.09 logMAR單位,95%CI -0.12~-0.05,P<0.000 01);而手術后1年(5項研究[56, 58-61],P=0.25)及1年以上(最長隨訪時間點為5年)視力較基線的變化值,兩組間差異無統計學意義(3項研究[56, 58-59],P=0.45)(表6,圖7)。對于中央視網膜厚度變化值,共3項研究[57, 60-61](164只眼)報告了此指標。分析結果(證據等級Ⅲ)顯示:手術后3、6個月,兩組間差異無統計學意義(P=0.78、1.00);手術后12個月,PPV聯合內界膜剝除組的中央視網膜厚度較基線的下降值均顯著大于單純PPV組(中位數-82.21 μm,95%CI -94.12~-70.30,P<0.000 01),說明PPV聯合內界膜剝除能夠較好地減輕黃斑水腫(表6,圖8)。對于手術中并發癥情況,基于2項研究[57, 59](155只眼)的薈萃分析結果顯示,PPV聯合或不聯合內界膜剝除手術在手術中醫源性視網膜裂孔的發生率方面無顯著差異(P=0.95)(表6,圖9)。對于手術后并發癥情況,共3項研究[56, 59, 61](254只眼)報告了手術后高眼壓、黃斑中心硬性滲出及新生血管性青光眼的發生率情況。薈萃分析結果(證據等級Ⅲ)顯示:手術后高眼壓(P=0.87)、黃斑中心硬性滲出物(P=1.00)及新生血管性青光眼(P=0.75)的發生率在兩組間均無統計學差異(表6,圖10)。
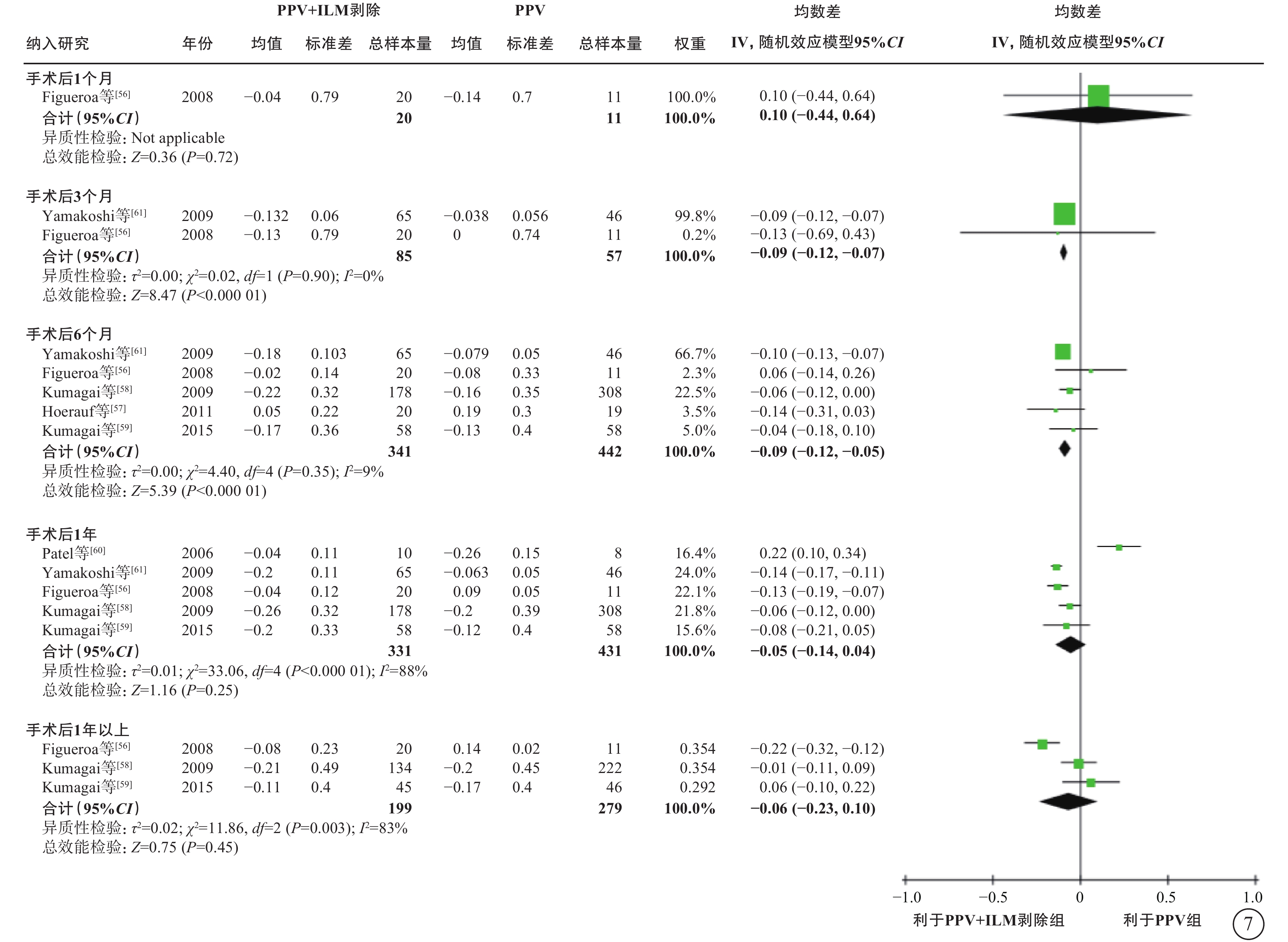 圖7
nT-DME患者PPV聯合或不聯合ILM剝除手術后視力變化值(logMAR單位)比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;logMAR:最小分辨角對數;CI:可信區間
圖7
nT-DME患者PPV聯合或不聯合ILM剝除手術后視力變化值(logMAR單位)比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;logMAR:最小分辨角對數;CI:可信區間
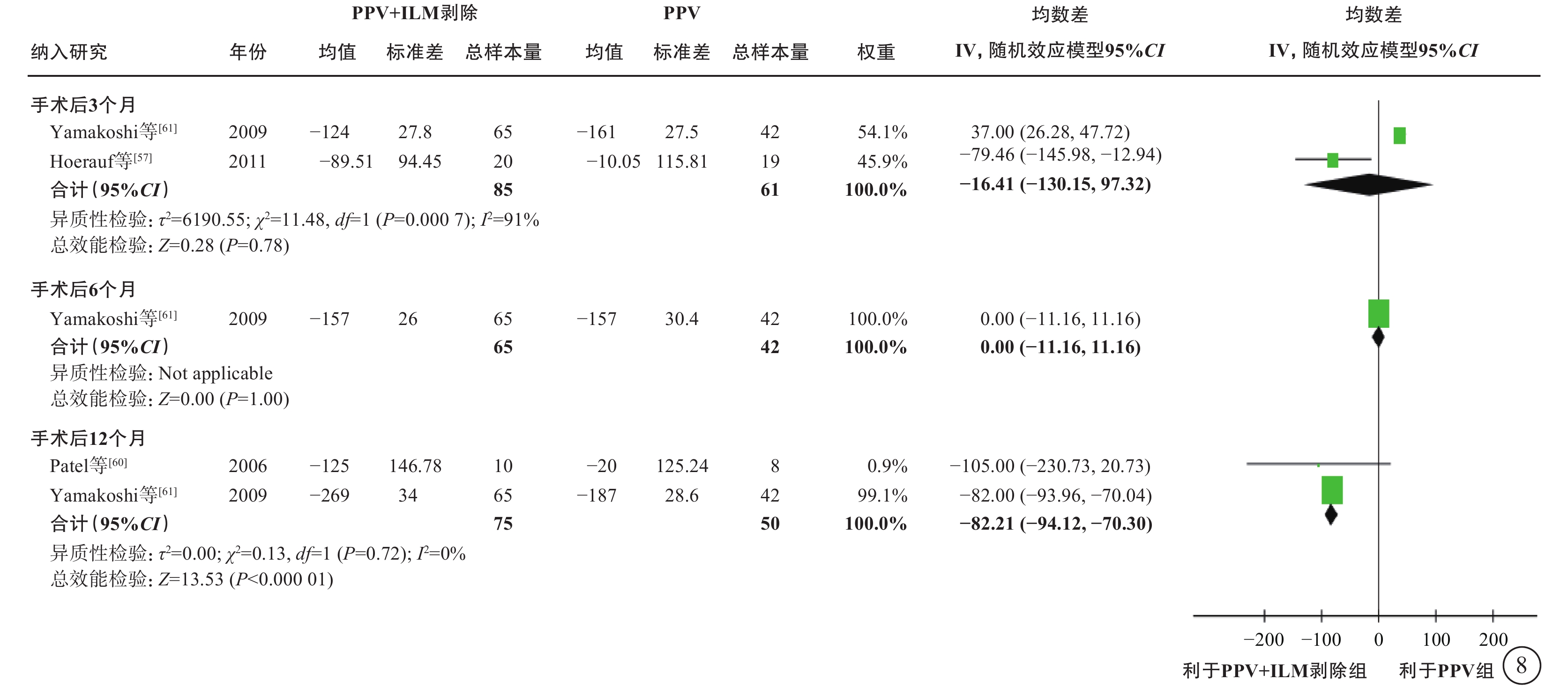 圖8
nT-DME患者PPV聯合或不聯合ILM剝除手術后中央視網膜厚度變化值(μm)比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間;Not applicable:不適用
圖8
nT-DME患者PPV聯合或不聯合ILM剝除手術后中央視網膜厚度變化值(μm)比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間;Not applicable:不適用
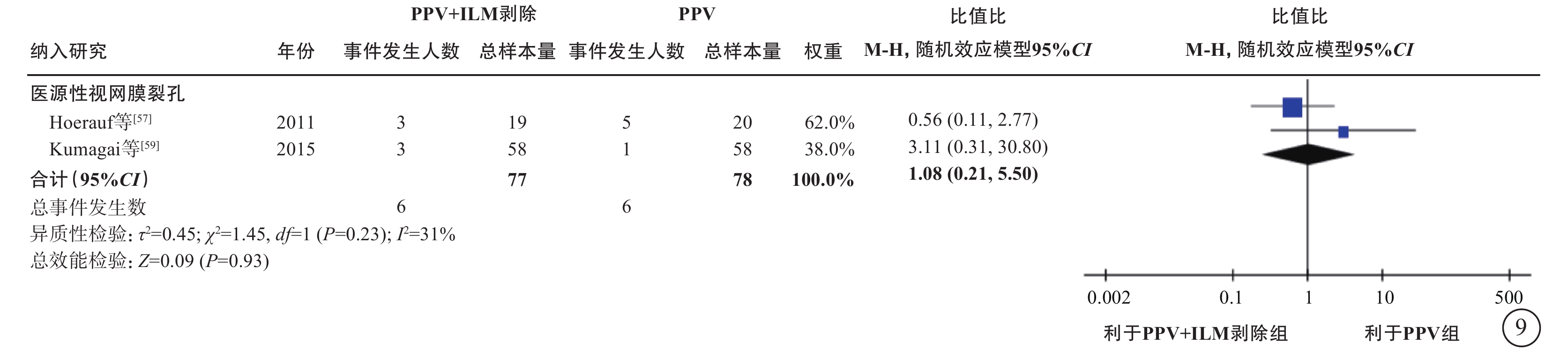 圖9
nT-DME患者PPV聯合或不聯合ILM剝除手術中并發癥發生率比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間
圖9
nT-DME患者PPV聯合或不聯合ILM剝除手術中并發癥發生率比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間
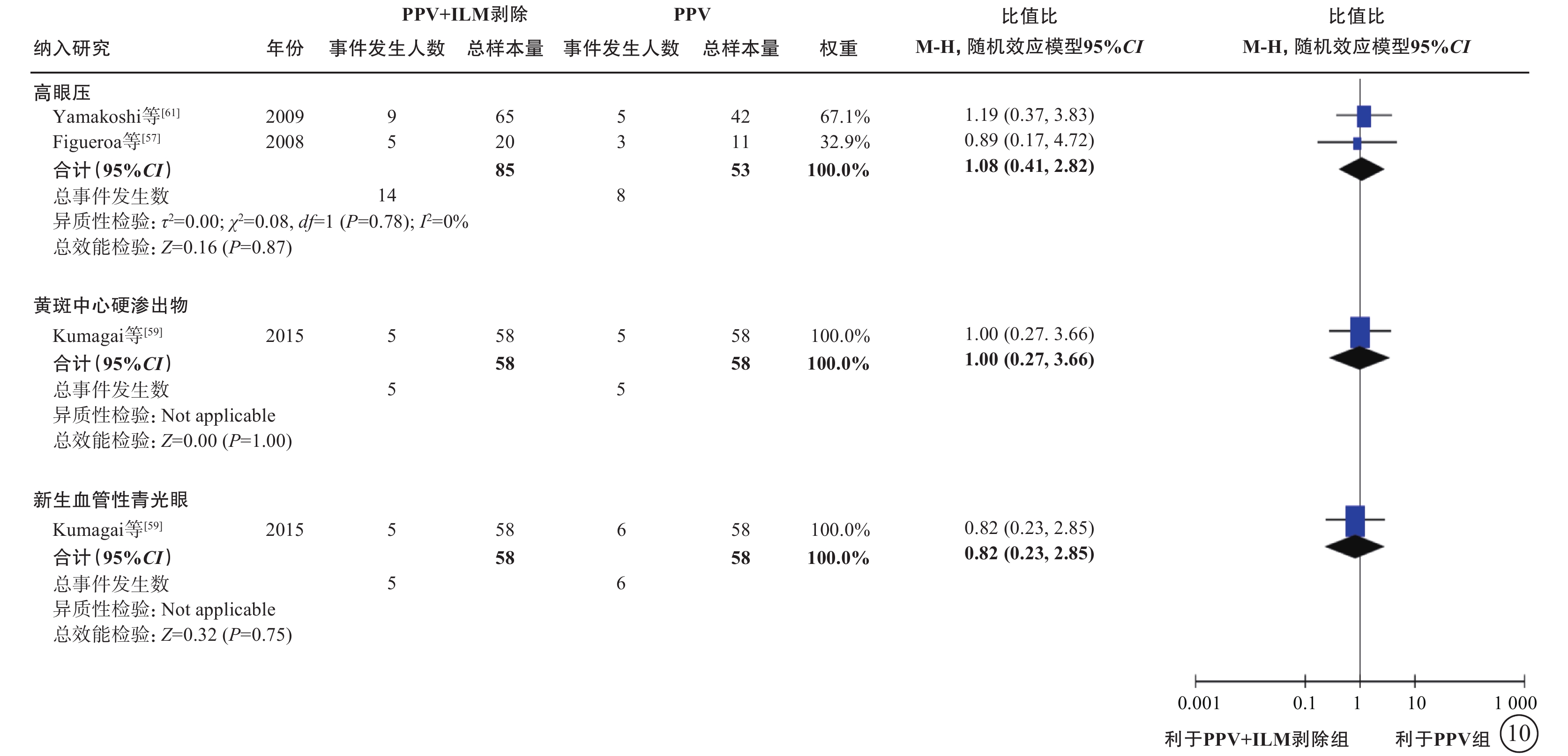 圖10
nT-DME患者PPV聯合或不聯合ILM剝除手術后并發癥發生率比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間;Not applicable:不適用
圖10
nT-DME患者PPV聯合或不聯合ILM剝除手術后并發癥發生率比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間;Not applicable:不適用
兩項研究[62-63]探討了對伴有ERM的DME患者行PPV治療時,在存在ERM的情況下是否推薦同時剝除內界膜。發表于2005年的一項RCT[62](證據等級Ⅱ)納入了視力在20/40(Snellen視力表)或以下的彌漫性DME患者29例30只眼,并將其隨機分為內界膜剝除組(15只眼)和內界膜保留組(15只眼),隨訪觀察(9.5±1.7)個月。內界膜剝除組中3只眼(20%)存在ERM,內界膜保留組中6只眼(40%)存在ERM,PPV中均將ERM予以剝除,同時盡量清除殘余玻璃體皮質和后玻璃體等視網膜中央凹前物質。手術后末次隨訪時,兩組患者BCVA均較手術前顯著提高,且兩組間BCVA較基線變化值以及較基線視力改善(內界膜剝除組、保留組分別為47%、60%)和視力維持(內界膜剝除組、保留組分別為53%、60%)的患者比例均無統計學差異(P=0.493 8)。兩組患者手術后1周及1、2、3、4、5、6個月平均視網膜厚度均較手術前明顯變薄,但所有時間點兩組的視網膜厚度差異無統計學意義。兩組患者均未發生嚴重的手術中并發癥。而另一項回顧性隊列研究[63](證據等級Ⅲ)納入累及黃斑中心凹的DME患者45例53只眼,對存在ERM的患眼予以ERM剝除(23只眼),視情況對部分患眼行內界膜剝除(35只眼)。單因素方差分析結果表明,內界膜剝除(P=0.007 0)和ERM剝除(P=0.042 5)與手術后12個月視力改善有關;而多因素方差分析結果則表明,內界膜剝除(P=0.075 2)、ERM剝除(P=0.868 4)及眼內糖皮質激素注射與手術后12個月視力改善無關,同樣印證了上述結果,即伴有ERM的DME患者行PPV治療時,剝除ERM合并內界膜剝除不能進一步改善手術后視力。
問題9:PDR合并白內障患者行PPV時,是否推薦聯合行白內障摘除及人工晶狀體(IOL)植入手術?
推薦意見:當白內障形成影響PPV時,要考慮聯合白內障手術。但鑒于目前的證據,不形成推薦意見。
5項觀察性研究[64-68](599只眼)報道了PDR合并白內障患者行PPV時聯合或不聯合白內障手術的臨床效果(表7)。其結果表明,PDR患者行PPV時聯合或不聯合白內障手術的手術后視力、VH和TRD發生率沒有顯著性差異,PDR患者PPV聯合白內障手術會增加手術后短期的炎癥反應(纖維蛋白形成、虹膜粘連、角膜水腫)。
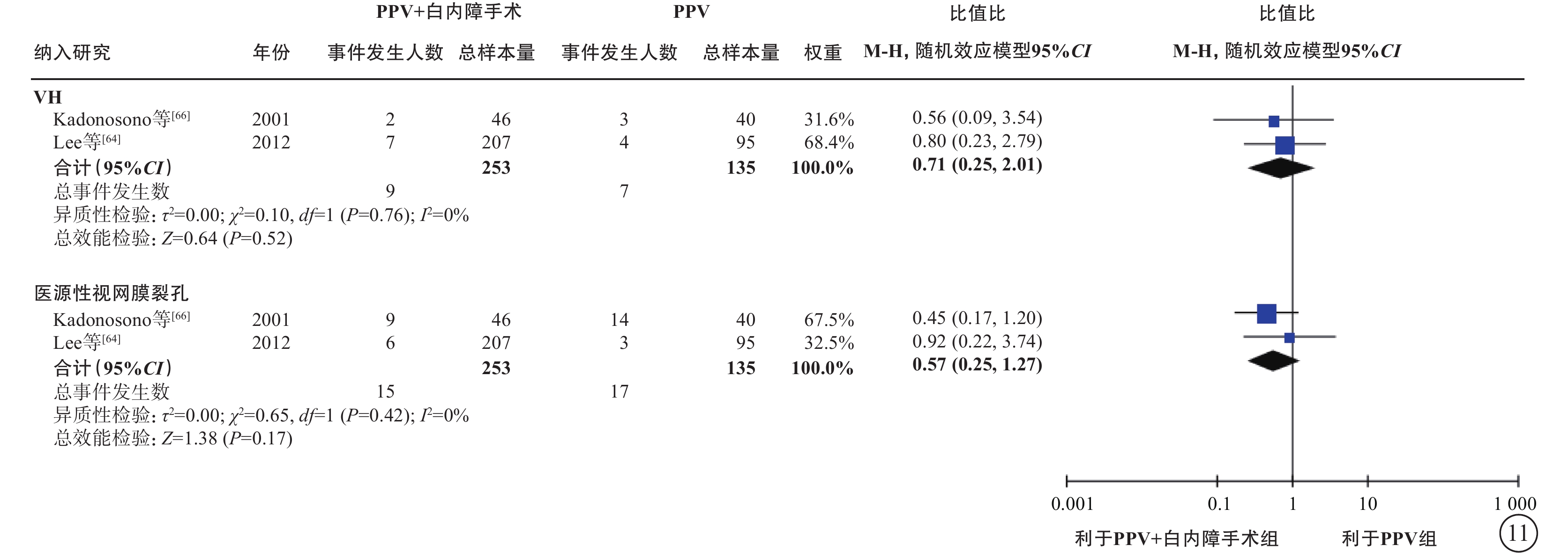
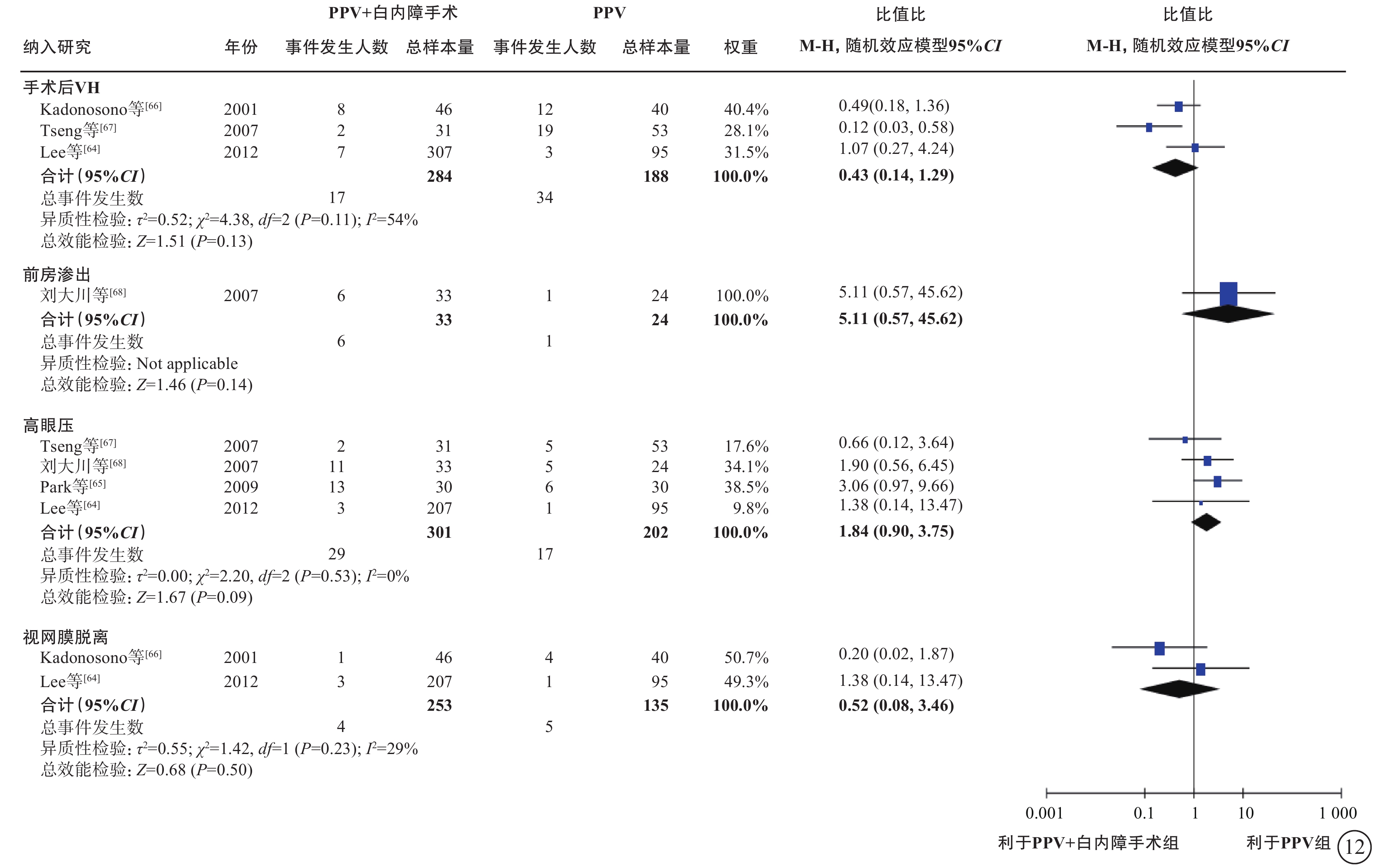
基于2項研究[64, 66](388只眼)的薈萃分析(證據等級Ⅲ)結果顯示:聯合組與單純PPV組之間手術中VH(OR=0.71,95%CI 0.25~2.01,P=0.52)、醫源性視網膜裂孔(OR=0.57,95%CI 0.25~1.27,P=0.17)的發生率無顯著差異(表6,圖11)。聯合組與單純PPV組之間手術后VH(3項研究[64, 66-67] ,OR=0.43,95%CI 0.14~1.29,P=0.13)、前房滲出(1項研究[68],OR=5.11,95%CI 0.57~45.62,P=0.14)、高眼壓(4項研究[64-65, 67-68],OR=1.84,95%CI 0.90~3.75,P=0.09)和視網膜脫離(2項研究[64, 66],OR=0.52,95%CI 0.08,3.46,P=0.50)的發生率均無顯著差異(表6,圖12)。3項研究(證據等級Ⅲ)報告了手術后其他前房并發癥的發生情況。結果顯示,聯合組手術后纖維蛋白形成[65-66](30% vs. 7%,P=0.042;17% vs. 2%,P=0.019)、手術后2周虹膜粘連[65](30% vs. 7%,P=0.042)、手術后角膜水腫[66](36.4% vs. 8.3%,P<0.05)的發生率顯著高于單純PPV組。而兩組間瞳孔后粘連[68](3.0% vs. 4.2%,P=1.000)、手術后前房出血[67](0.0% vs. 1.9%,P=0.631)、新生血管性青光眼[67](0.0% vs. 1.9%,P=0.631)、角膜混濁[66](2.2% vs. 4.3%,P>0.05)的發生率差異均無統計學意義。
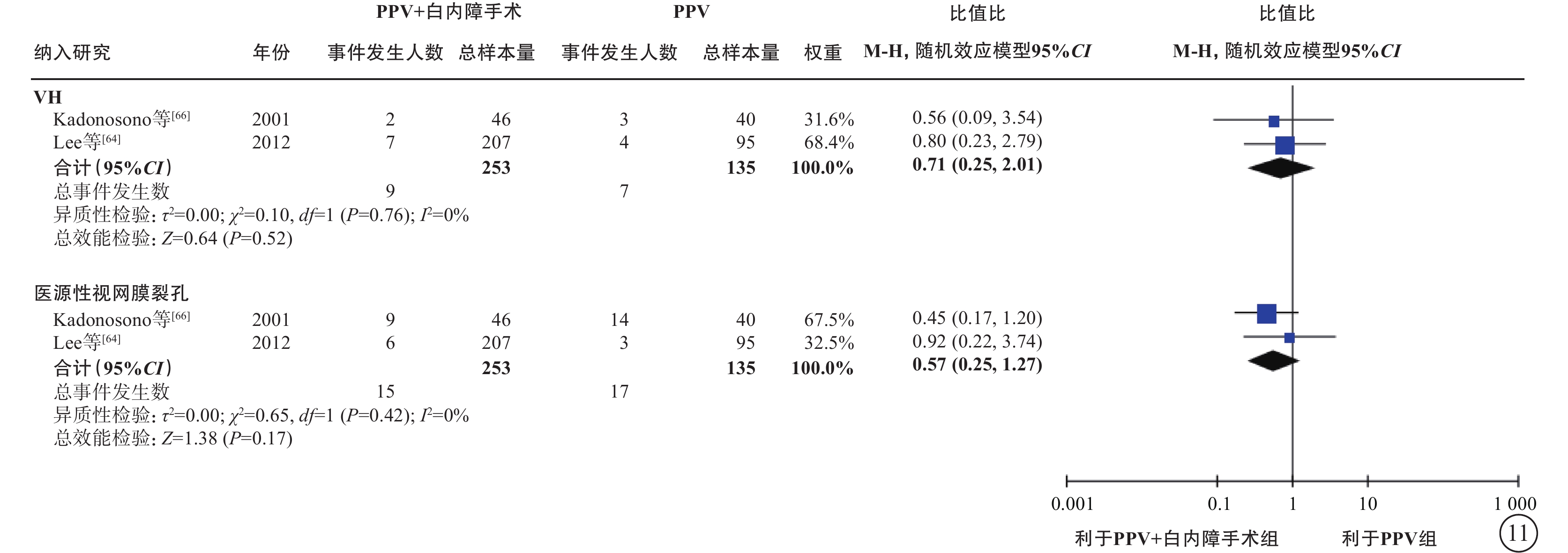 圖11
PDR合并白內障患者PPV聯合或不聯合白內障手術的手術中指標比較 PDR:增生型糖尿病視網膜病變;PPV:玻璃體切割手術;VH:玻璃體積血;CI:可信區間
圖11
PDR合并白內障患者PPV聯合或不聯合白內障手術的手術中指標比較 PDR:增生型糖尿病視網膜病變;PPV:玻璃體切割手術;VH:玻璃體積血;CI:可信區間
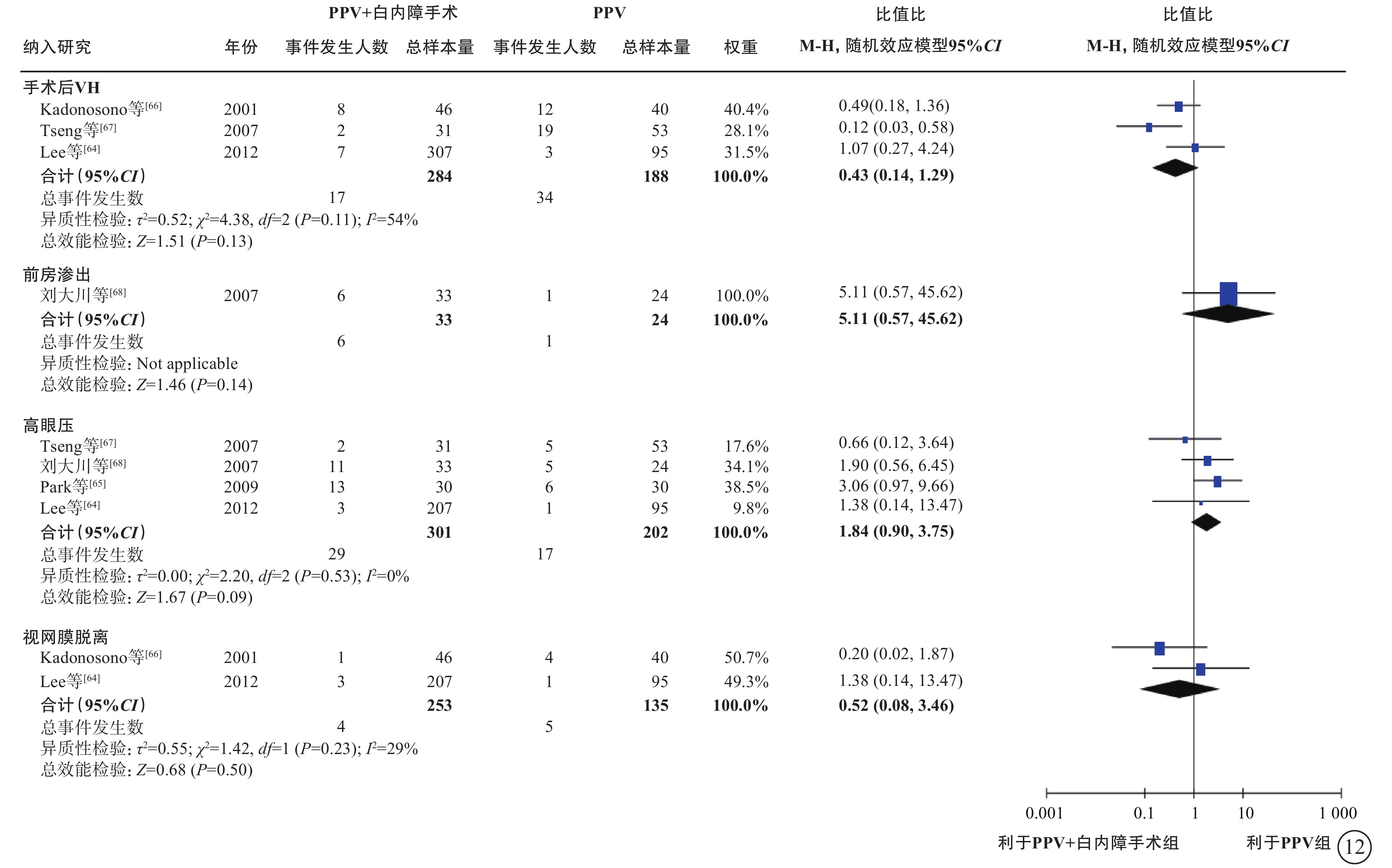 圖12
PDR合并白內障患者PPV聯合或不聯合白內障手術的手術后并發癥指標比較 PDR:增生型糖尿病視網膜病變;PPV:玻璃體切割手術;VH:玻璃體積血;CI:可信區間
圖12
PDR合并白內障患者PPV聯合或不聯合白內障手術的手術后并發癥指標比較 PDR:增生型糖尿病視網膜病變;PPV:玻璃體切割手術;VH:玻璃體積血;CI:可信區間
共5項研究[64-67, 69](448只眼)報告了PDR合并白內障患者行PPV時聯合或不聯合白內障手術的視力預后情況(證據等級Ⅲ)。Lee等[64]和Park等[65]研究發現,手術后1、2、3、6個月,兩組間視力差異均無統計學意義(P>0.05)。Kadonosono等[66]經過18.3(7~24)個月的隨訪觀察亦發現,兩組患者視力差異無統計學意義(P>0.05)。王萍等[69]通過一項回顧性隊列研究納入合并不同程度白內障的PDR患者72例82只眼,將其分為3組:A組25例28只眼,行PPV同期聯合白內障超聲乳化及IOL植入手術;B組20例24只眼,行玻璃體腔注射anti-VEGF藥物輔助PPV,同期聯合白內障超聲乳化及IOL植入手術;C組27例30 只眼,Ⅰ期行PPV,Ⅱ期行硅油取出聯合白內障超聲乳化及IOL植入手術。患者手術后隨訪(9.0±2.5)(6~12)個月,A組、B組、C組患者手術后logMAR BCVA 分別為1.007±0.455、1.000±0.482、1.033±0.531,三組患者視力較手術前均有明顯提高(P<0.05),但三組間差異無統計學意義(P=0.195)。Tseng等[67]納入84例84只眼觀察發現,聯合組[隨訪(15.6±7.0)個月]患者視力提高1行或更多的比例顯著高于單純PPV組[隨訪(16.1±0.5)個月](67.7% vs. 32.1%,P=0.003)。
3 展望
針對DR的手術治療,尤其是涉及玻璃體視網膜手術的操作,其復雜性和挑戰性主要取決于眼科醫生的專業知識、技術水平及臨床經驗。鑒于此領域的多樣性和復雜性,很難就具體的手術細節達成一致意見。本專家共識旨在為中國眼科專科醫生以及從事眼底病專業的醫生提供臨床指導,但不應被視為具有法律效力的醫療依據。
基于對現有證據的綜合評估,我們建議在中國人群中進行更系統性的研究,以驗證PPV是否能夠有效控制DR患者增生早期的病情進展。這些研究將為未來的 DR治療決策、指南制定以及實際臨床實踐提供堅實的基礎和可靠的科學依據。
形成指南意見的專家組成員
臨床主席
黎曉新 廈門大學附屬廈門眼科中心/北京大學人民醫院(執筆人)
許 迅 上海交通大學醫學院附屬第一人民醫院
方法學聯席主席
夏 君 寧波諾丁漢GRADE中心
核心專家(按照姓氏拼音排序)
常 青 復旦大學附屬眼耳鼻喉科醫院
丁小燕 中山大學中山眼科中心
李筱榮 天津醫科大學眼科醫院
梁建宏 北京大學人民醫院
劉 堃 上海交通大學醫學院附屬第一人民醫院
陸 方 四川大學華西醫院
羅 靜 中南大學湘雅二醫院
呂 林 中山大學中山眼科中心
馬 進 中山大學中山眼科中心
孫曉東 上海交通大學醫學院附屬第一人民醫院
唐仕波 中南大學愛爾眼科學院
陶 勇 首都醫科大學附屬北京朝陽醫院
王雨生 空軍軍醫大學西京醫院
魏文斌 北京同仁醫院
邢怡橋 武漢大學人民醫院
徐格致 復旦大學附屬眼耳鼻喉科醫院
于偉泓 北京協和醫院
張 風 北京同仁醫院
張美霞 四川大學華西醫院
張 明 四川大學華西醫院
張少沖 深圳市眼科醫院
趙明威 北京大學人民醫院
趙培泉 上海交通大學醫學院附屬新華醫院
周 鵬 上海百匯醫院
討論專家(按照姓氏拼音排序)
常 青 復旦大學附屬眼耳鼻喉科醫院
陳曉隆 中國醫科大學附屬盛京醫院
陳 宜 北京中日友好醫院
陳長征 武漢大學人民醫院
戴 虹 北京醫院
丁小燕 中山大學中山眼科中心
惠延年 空軍軍醫大學西京醫院
黎曉新 廈門大學附屬廈門眼科中心/北京大學人民醫院
李海平 北京大學第三醫院
李秋明 鄭州大學第一附屬醫院
李甦雁 徐州市第一人民醫院
李筱榮 天津醫科大學眼科醫院
梁建宏 北京大學人民醫院
劉慶淮 南京醫科大學第一附屬醫院
劉曉玲 溫州醫科大學附屬眼視光醫院
劉 勇 第三軍醫大學西南醫院
柳 林 上海交通大學醫學院附屬仁濟醫院
陸 方 四川大學華西醫院
羅 靜 中南大學湘雅二醫院
呂 林 中山大學中山眼科中心
馬 進 中山大學中山眼科中心
馬 翔 大連醫科大學附屬第一醫院
苗 恒 北京大學人民醫院
彭紹民 哈爾濱醫科大學附屬第二醫院
曲進鋒 北京大學人民醫院
沈 璽 上海交通大學醫學院附屬瑞金醫院
宋艷萍 中國人民解放軍中部戰區總醫院
宋宗明 河南省立眼科醫院
蘇冠方 吉林大學第二醫院
孫大衛 哈爾濱醫科大學第二附屬醫院
孫曉東 上海交通大學醫學院附屬第一人民醫院
孫旭芳 華中科技大學同濟醫學院附屬同濟醫院
唐羅生 中南大學湘雅二醫院
唐仕波 中南大學愛爾眼科學院
陶 勇 首都醫科大學附屬北京朝陽醫院
萬光明 鄭州大學第一附屬醫院
王常觀 北京大學第三醫院
王 方 同濟大學附屬第十人民醫院
王 鮮 貴州醫科大學附屬醫院
王艷玲 首都醫科大學附屬北京友誼醫院
王雨生 空軍軍醫大學西京醫院
王志軍 北京中日友好醫院
魏文斌 北京同仁醫院
邢怡橋 武漢大學人民醫院
徐格致 復旦大學附屬眼耳鼻喉科醫院
徐國興 福建醫科大學第一臨床醫學院
許 迅 上海交通大學醫學院附屬第一人民醫院
楊 波 吉林大學第二醫院
柳 林 上海交通大學醫學院附屬仁濟醫院
姚 勇 無錫市人民醫院
于偉泓 北京協和醫院
于旭輝 哈爾濱醫科大學附屬第一醫院
俞素勤 上海交通大學醫學院附屬第一人民醫院
喻曉兵 北京醫院
張 風 北京同仁醫院
張美霞 四川大學華西醫院
張 明 四川大學華西醫院
張少沖 深圳市眼科醫院
張文芳 蘭州大學第二醫院
趙明威 北京大學人民醫院
趙培泉 上海交通大學醫學院附屬新華醫院
趙鐵英 深圳市眼科醫院
周 鵬 上海百匯醫院
朱 丹 內蒙古醫學院附屬醫院
莊文娟 寧夏醫學院附屬醫院
糖尿病視網膜病變(DR)是由糖尿病引發的視網膜微血管損害,可導致一系列病變及全視網膜非血管組織的損傷,是一種可能嚴重影響視力乃至致盲的慢性疾病[1]。中華醫學會眼科學分會眼底病學組為規范DR的管理,分別在2014年和2022年發布了臨床診療指南,涵蓋了DR的定義、診斷、分期、治療等多方面的內容,并強調了預防、篩查、轉診、干預以及患者的整體管理。《我國糖尿病視網膜病變臨床診療指南(2022年)——基于循證醫學修訂》[2]特別關注了DR的激光和藥物治療,但對于較為嚴重的增生型DR(PDR)的手術治療原則和具體操作方法未作詳述。PDR標志著視網膜微血管病變已進入嚴重階段,對視力的影響極大,是糖尿病患者尋求眼科治療的主要原因之一,可能導致不可逆的視力損害。PDR可以分為以下三個階段:(1)增生早期:出現視網膜新生血管(NVE)或視盤新生血管(NVD)。當NVD覆蓋超過1/4~1/3的視盤面積(DA),或NVE覆蓋超過1/2 DA,或伴有視網膜前出血或玻璃體積血(VH)時,被稱為“高危PDR”。(2)纖維增生期:形成纖維膜,可能伴有視網膜前出血或VH。(3)增生晚期:出現牽拉性視網膜脫離(TRD),伴有纖維膜,可能合并或不合并VH,還包括虹膜和房角的新生血管[2-3]。在VH的情況下,深層的纖維血管膜和視網膜脫離往往難以直接觀察到,這增加了手術難度,不當處理可能會降低手術后視力恢復的效果,甚至引起并發癥。因此,需要明確手術時機、圍手術期血糖控制、手術計劃、手術技術選擇、纖維血管膜處理方法、聯合藥物或激光治療的應用,以及玻璃體填充物的選擇等關鍵點。鑒于此,中華醫學會眼科學分會眼底病學組、中國醫師協會眼科醫師分會眼底病專委會聯合組織了相關領域的專家,共同制定了《玻璃體切割手術治療2型糖尿病視網膜病變專家共識》,旨在為我國的眼底病專科醫生提供更具體的臨床指導。
1 共識編寫方法
1.1 制定共識的理論依據和方法學
本共識嚴格按照循證醫學指南原則制定,制定過程中參考了證據評價與推薦意見分級、制定和評價(GRADE)系統的理念和原則。共識專家組成員的遴選和組成、利益沖突管理、外部審查和組織批準均根據中華醫學會眼科學分會的政策和程序進行。
1.2 共識使用者和目標人群
本共識的適用范圍為DR玻璃體切割手術(PPV)治療的手術時機、圍手術期血糖管理、手術方式選擇、手術操作方案的制定等。其目標人群為中國眼底病專科醫師和從事眼底病專業的醫師。
1.3 共識專家組構成
共識專家組主要的臨床專家成員由中華醫學會眼科學分會眼底病學組、中國醫師協會眼科醫師分會眼底病專委會委員以及全國各省市具有多年玻璃體視網膜手術經驗、具有臨床影響力的醫生組成。
1.4 利益沖突說明
共識專家組成員(包括臨床專家和方法學專家)的利益沖突管理依據世界衛生組織以及國際指南聯盟對利益沖突管理的指導原則執行。共識專家組向中華醫學會眼科學分會報告了個人潛在的利益沖突(包含財務和專業相關的利益沖突)。所有成員均無實質性利益沖突。
1.5 臨床問題遴選和確定
方法學團隊與臨床專家對PPV治療DR相關的臨床問題進行了探討。經過對最初臨床問題的多輪修改和討論,最終確定了在本共識中要明確的9個臨床問題。
1.6 證據檢索及整合
共識的方法學團隊邀請中國臨床實踐指南聯盟與臨床專家合作,針對共識中的每一個臨床問題進行系統性證據檢索。檢索數據庫包括 PubMed、EMBASE和Cochrane Library,時間跨度為數據庫建立至2023年11月1日。檢索策略采用關鍵詞及關鍵詞結合自由詞的方式,在數據庫的題目和摘要中進行檢索。檢索詞包括 “proliferative diabetic retinopathy”、“diabetic macular oedema” 以及“vitrectomy”等(表1)。
除電子數據庫檢索外,共識專家組成員提供的關鍵研究以及已發表的系統評價中納入的研究也被作為補充資料。針對每一個臨床問題制定具體的納入和排除標準,并設計數據提取表格。在每個臨床問題上,優先納入系統評價;當系統評價無法回答關注的臨床問題時,則納入隨機對照試驗(RCT)。當RCT證據缺乏、間接性或證據體質量極低時,補充納入非隨機對照研究或其他觀察性研究證據。
兩名系統評價員獨立進行文獻篩查及數據提取;遇到分歧時,由第三名系統評價員協助解決。使用 RevMan 5.3 軟件,采用隨機效應模型進行薈萃分析。對于二分類結局,效應值采用比值比(OR)及其95%可信區間(CI);對于連續性結局,效應值采用均值差(MD)及其95%CI。在進行薈萃分析之前,充分考慮研究間的臨床異質性和方法學異質性。統計學異質性通過χ2檢驗和I2統計量評價。當χ2檢驗P<0.1且I2>50%時,認為存在統計學異質性。當研究間存在統計學異質性時,探索潛在的異質性來源,并根據異質性來源進行亞組分析。搜集到的證據主要圍繞2型糖尿病。
1.7 證據分級與推薦意見形成
采用《牛津循證醫學中心分級2011版》作為主要工具對本共識中的循證醫學證據進行等級評估(表2),同時也參考了GRADE系統。在評估證據等級時,考慮了偏倚風險、不一致性、間接性、不精確性和發表偏倚等因素,并據此對證據等級進行了相應的調整。
對于推薦意見的形成,共識專家組參考了GRADE系統中的要素,包括醫學干預的利弊平衡、證據質量、價值觀念與偏好、成本與資源耗費,以及可及性等因素,制定了推薦的方向和強度的標準。最終將推薦強度分為三個等級:強推薦、中等推薦和弱推薦(表3)。強推薦:共識臨床專家組對該推薦意見反映的最佳臨床實踐有高度的信心,建議目標用戶均采納該推薦意見。中等推薦:共識臨床專家組對該推薦意見反映的最佳臨床實踐有中等程度的信心,多數目標用戶應采納該推薦意見,但在執行過程中應注意考慮醫患共同決策。弱推薦:共識臨床專家組對該推薦意見有一定的信心,但應有條件地應用于目標群體,強調醫患共同決策的重要性。
共識專家組通過對研究證據進行公開討論后,以投票的形式達成了對推薦意見的共識。當專家組意見不一致時,則采用德爾菲問卷調查的方法[4]進行相應的修改和第二輪投票,直到達成共識。
1.8 共識的傳播和實施
共識發布后,將主要通過以下方式進行傳播和推廣:(1)專業期刊、網站和學術會議:將在相關專業期刊上發表,并通過官方網站和學術會議進行介紹。(2)共識推廣專場:有計劃地在我國部分地區組織共識推廣專場活動,確保臨床醫師及其他利益相關群體能夠充分了解并正確應用該共識。這些措施旨在確保共識的內容能夠廣泛傳播,并在實際臨床實踐中得到有效應用。
2 PDR的PPV治療原則和操作相關問題
問題1:2型糖尿病導致的PDR患者發生VH后,應在多長時間后考慮進行PPV?(鑒于1型糖尿病的發生率較低,相關文獻數量有限,納入的研究中2型糖尿病人群占比較大,因此對于此問題的證據總結主要針對2型糖尿病導致的PDR患者)
推薦意見:基于目前有限的證據,對于存在VH或合并血管纖維增生引起的視網膜牽拉及TRD的2型糖尿病PDR患者,建議積血早期進行PPV治療(中等推薦)。
兩項研究結果顯示,對于存在VH但尚未出現視網膜脫離的PDR患者,若在積血后的30 d內接受PPV治療,能夠顯著縮短患者低視力的持續時間,并且手術后1~2年的視力預后較好[5-6]。
一項回顧性隊列研究[5](證據等級Ⅲ)探討了PDR合并VH患者接受PPV的最佳時機。該研究納入了因PDR并發VH的患者,排除了并發視網膜脫離、既往有影響視力的其他視網膜病變或黃斑病變、各種類型青光眼以及隨訪時間少于24個月的患者。最終納入了符合標準的PDR合并VH患者67例70只眼,其中1型糖尿病患者4例5只眼(7.1%,5/70),2型糖尿病患者63例65只眼(92.9%,65/70)。患者按VH的時間分為三組:病程<1個月組22只眼,平均年齡45.23歲;病程1~3個月組23只眼,平均年齡45.78歲;病程>3個月組25只眼,平均年齡50.48歲。所有患者手術后均隨訪24~42個月。末次隨訪時,視力達到0.5及以上者的比例分別為:病程<1個月組41%、病程1~3個月組23%、病程>3個月組0%。病程<1個月組與其他兩組之間的差異均有統計學意義(P=0.03、P<0.001)。
另一項回顧性隊列研究[6](證據等級Ⅲ)比較了立即手術組(患者在積血30 d內接受了PPV治療)與延遲手術組(患者在積血30 d后接受了PPV治療)的視力改善情況。手術后12個月末次隨訪時,兩組患者的視力均較基線顯著改善(P=0.002、P<0.000 1),但兩組患者間視力無顯著差異(P=0.684)。考慮延遲手術組患者手術前視力狀況較差,即視力較差和(或)低水平視力維持時間較長,在隨訪終點時,立即手術組和延遲手術組的手術后視力曲線下面積無顯著性差異(P>0.05)。這表明,在積血30 d內接受PPV治療能夠顯著減少患者低視力的持續時間。
問題2:圍手術期的PDR患者目標血糖范圍是多少?如何有效控制其圍手術期血糖?( 由于目前尚無僅針對眼科手術的血糖管理指南/專家共識,故參考多個包含全身手術在內的圍手術期血糖管理指南/專家共識進行總結)
推薦意見一:建議PDR患者PPV前血糖盡可能控制在6.0~10.0 mmol/L之間,為預防低血糖,血糖允許值可放寬至13.9 mmol/L。如果有必要,可進行動態血糖監測。對于高齡患者或伴有多種合并癥的患者,為避免低血糖,建議血糖最高允許值為13.9 mmol/L,血糖監測頻率為0.5~2.0 h一次。對于擇期手術患者,如果隨機血糖水平≥10.0 mmol/L,則手術后建議每半小時監測一次血糖,直至血糖恢復至正常或降至 10.0 mmol/L 以下;如果血糖難以控制,應與其他相關科室進行會診,并與患者充分溝通可能的風險。對于不可擇期(增生晚期)的手術患者,建議更密切地監測血糖,以避免低血糖(低于 3.9 mmol/L)和酮中毒的發生(中等推薦)。
Cheisson等[7]研究(證據等級 V)指出,在進行眼科手術前,血糖范圍應控制在 6.6 ~10.0 mmol/L之間;血糖低于3.9 mmol/L時被認為是低血糖狀態,手術前應予以避免。2018 年《中國臨床實踐圍手術期血糖管理指南》[8](證據等級 V)建議,手術中血糖控制目標為 6.7~11.1 mmol/L,手術后血糖控制目標為<12.0 mmol/L;而對于 PDR 患者,手術后血糖不應超過 10.0 mmol/L。在建議的目標血糖范圍內,手術中應每1.0~2.0小時監測一次血糖,手術后應每4.0~ 6.0小時監測一次血糖。對于可擇期手術患者,如果隨機血糖≥12.0 mmol/L或糖化血紅蛋白≥9%,建議推遲手術時間。對于急診手術中出現酮癥酸中毒或高滲性昏迷的患者,如果患者的病情允許,建議在手術前首先糾正代謝紊亂、pH 值和滲透壓,直到恢復正常。中華醫學會麻醉學分會于 2016 年發布的《圍術期血糖管理專家共識》[9](證據等級 V)指出,圍手術期血糖應控制在 7.8~10.0 mmol/L之間;對于高齡、有嚴重合并癥、頻繁發作低血糖的患者,目標血糖范圍可適當放寬至不超過 13.9 mmol/L(表4)。對于正常飲食的患者,圍手術期應監測空腹血糖和三餐后的血糖;對于血糖高的患者,每 1.0~2.0小時監測一次血糖。
推薦意見二:建議對計劃接受PPV治療的 PDR 患者進行全面的手術前血糖水平評估及糖尿病相關并發癥檢查。對于那些伴有嚴重糖尿病并發癥(如糖尿病酮癥酸中毒、糖尿病腎病、糖尿病周圍神經病變、糖尿病心血管疾病等)的PDR患者,以及在圍手術期出現明顯且頻繁血糖波動的患者,建議咨詢內分泌科專家和其他相關并發癥的專業專家進行聯合管理(中等推薦)。
《中國臨床實踐圍手術期血糖管理指南》[8]指出,對于血糖波動較大或血糖水平不符合標準的圍手術期患者,建議咨詢內分泌科醫生并采取積極治療措施(證據等級 V)。對于腎功能正常的患者,手術前無需停用二甲雙胍治療(證據等級 V)。然而,對于腎功能異常且手術中需要全身麻醉的患者,應在手術前48 h停止使用二甲雙胍,并在手術后 48~72 h內繼續停用,直到腎功能恢復正常(證據等級 V)。若圍手術期隨機血糖兩次以上超過10 mmol/L,應請內分泌科會診,并通過降糖藥物或胰島素控制血糖(證據等級 V)。在低血糖的情況下,手術中輸液和胰島素的劑量應根據血糖水平來確定。中華醫學會麻醉學分會 2016 年發布的《圍術期血糖管理專家共識》[9]指出:當圍手術期血糖大于10.0 mmol/L時,應啟動胰島素治療(證據等級 V);對于正在接受靜脈輸注胰島素的患者,當血糖降至5.6 mmol/L以下時,應重新評估治療方案(證據等級 V);如果圍手術期血糖降至3.9 mmol/L或更低,應立即停用胰島素,并開始升血糖處理(證據等級 V)。
問題3:對于需要手術治療的PDR患者,是否推薦圍手術期聯合注射抗血管內皮生長因子(anti-VEGF)藥物?
推薦意見:PPV治療前 14 d內或手術完畢即刻注射anti-VEGF 藥物均可提高PDR患者的手術后視力,降低中央視網膜厚度,并有助于防止手術后近期的VH。因此,推薦PDR患者行PPV治療時,在圍手術期注射anti-VEGF藥物(中等推薦)。
共有22 項RCT( 1 396 只眼)比較了PPV前聯合注射anti-VEGF藥物與單純PPV治療 PDR 的臨床有效性[10-30](表5)。
在PDR合并VH的人群中,薈萃分析(證據等級Ⅰ)結果顯示,與單純PPV相比,手術前聯合anti-VEGF藥物治療的患者具有以下優勢:手術中VH發生率較低(2 項研究[11, 14],OR=0.04,95%CI 0.01~0.13,P<0.000 01);醫源性視網膜裂孔發生率較低(2 項研究[11, 14],OR=0.14,95%CI 0.04~0.52,P=0.003);電凝使用率較低(1 項研究[11],OR=0.05,95%CI 0.01~0.30,P=0.000 9);硅油填充率較低(1項研究[11],OR=0.11,95%CI 0.03~0.47,P=0.003)(圖1);手術時間較短(2 項研究[11, 14],MD=-16.84 min,95%CI -21.79~-11.89,P<0.000 01)(圖2)。RCT證據(證據等級Ⅱ)顯示,與單純PPV相比,手術前聯合anti-VEGF藥物治療者,其手術后 1 周及1 、3 個月的VH發生率明顯更低(1 項研究[10],P= 0.021、 0.006、0.047);手術后 3 個月視力改善程度更好(1 項研究[11],P=0.04);兩者之間手術后視網膜脫離發生率無顯著差異(1 項研究[21],P=0.97)。
 圖1
PDR合并VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術中情況比較 PDR:增生型糖尿病視網膜病變;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;Not applicable:不適用
圖1
PDR合并VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術中情況比較 PDR:增生型糖尿病視網膜病變;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;Not applicable:不適用
 圖2
PDR合并VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術時間比較 PDR:增生型糖尿病視網膜病變;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間
圖2
PDR合并VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術時間比較 PDR:增生型糖尿病視網膜病變;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間
在PDR合并TRD伴或不伴VH的人群中,薈萃分析(證據等級Ⅰ)結果顯示,與單純PPV相比,手術前聯合anti-VEGF藥物治療者,手術中VH發生率較低(9 項研究[12-13, 16-17, 22-23, 26-27, 29],OR=0.18,95%CI 0.09~0.35,P<0.000 1);電凝使用率較低(3 項研究[13, 17, 22],OR=0.19,95%CI 0.05~0.79,P=0.02);硅油填充率較低(9項研究[13, 15, 17-18, 22, 24, 27, 29-30],OR=0.38,95%CI 0.17~0.87,P=0.02);氣體填充率(2項研究[29-30],OR=0.91,95%CI 0.42~1.94,P=0.80)和醫源性視網膜裂孔發生率(3 項研究[18, 26-27],OR=0.82,95%CI 0.31~2.13,P=0.68)在兩組間無統計學差異(圖3);手術時間較短(12項研究[12-13, 15, 17-18, 22-25, 27, 29-30],MD=-17.11 min,95%CI -23.87~-10.34,P<0.000 01)(圖4);手術后視網膜脫離發生率較低(3項研究[13, 23, 27],OR=0.40,95%CI 0.17~0.94,P=0.04)(圖5);手術后早期出血(4 周及 4 周內復發)發生率較低(8 項研究[13, 16, 18-19, 27-28, 29-30],OR=0.32,95%CI 0.20~0.51,P<0.000 01)(圖5);手術后晚期出血發生率(4 周以上復發)在兩組間無顯著差異(5項研究[16-17, 19, 28, 30],OR=0.51,95%CI 0.25~1.05,P=0.07)(圖5);手術后視力改善程度較好(5項研究[15, 17, 20, 24, 30],MD=-0.29,95%CI -0.56~-0.03,P=0.03)(圖6)。
 圖3
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術中情況比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;Not estimable:不可估
圖3
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術中情況比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;Not estimable:不可估
 圖4
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術時間比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間
圖4
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術時間比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間
 圖5
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術后結果比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;早期出血:手術后4周及4周內VH復發;晚期出血:手術后4周后VH復發
圖5
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療手術后結果比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;CI:可信區間;早期出血:手術后4周及4周內VH復發;晚期出血:手術后4周后VH復發
 圖6
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療后視力變化值(logMAR單位)比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;logMAR:最小分辨角對數;CI:可信區間
圖6
PDR合并TRD伴或不伴VH患者PPV聯合或不聯合手術前anti-VEGF藥物治療后視力變化值(logMAR單位)比較 PDR:增生型糖尿病視網膜病變;TRD:牽拉性視網膜脫離;VH:玻璃體積血;PPV:玻璃體切割手術;anti-VEGF:抗血管內皮生長因子;logMAR:最小分辨角對數;CI:可信區間
三項RCT和一項網狀薈萃分析比較了PPV完畢時聯合anti-VEGF藥物與單純PPV治療PDR的臨床有效性。一項網狀薈萃分析[31](證據等級Ⅰ)納入了26 項RCT 原始研究,包括1 802例需接受PPV治療的PDR伴TRD或不可吸收VH患者,比較了手術前1~5 d、手術前6~14 d、手術前>14 d及手術完畢時注射anti-VEGF 藥物的臨床結局。結果表明,手術前注射anti-VEGF藥物與手術完畢時注射anti-VEGF藥物在最佳矯正視力(BCVA)、手術后VH復發率和手術中出血發生率方面均無顯著差異。一項 RCT[32](證據等級Ⅱ)納入了 84例嚴重PDR患者(84 只眼),所有患者均表現為不吸收的VH和不伴TRD的纖維血管增生。該研究將患者隨機分為兩組,試驗組于手術前 3~5 d和手術完畢時均接受anti-VEGF藥物注射;對照組僅手術前3~5 d接受anti-VEGF藥物注射。手術后1個月,試驗組VH發生率較低(9.3% vs. 19.5%,P=0.046),BCVA[以最小分辨角對數(logMAR)視力記錄]較好(0.57±0.11 vs. 0.71±0.15,P=0.019);但手術后 3 、 6 個月,兩組間VH發生率和BCVA的差異均無統計學意義。手術后1、3個月,試驗組中央視網膜厚度更薄,但手術后 6 個月兩組之間無差異。總體而言,與僅在PPV前聯合注射anti-VEGF藥物相比,手術完畢時聯合注射anti-VEGF 藥物對嚴重PDR患者手術后早期(1 個月)的VH、視力提升及手術后 3 個月內視網膜水腫具有較好的改善作用。另外兩項RCT(證據等級Ⅱ)亦顯示,相較于不注射anti-VEGF藥物,手術完畢時即刻注射anti-VEGF 藥物可顯著降低手術后24周或1年內患者的中央視網膜厚度[33-34],顯著提高患者24周內的BCVA,并降低VH復發率[34]。
問題4:對于需要接受PPV治療的PDR患者,是否推薦其手術前行全視網膜激光光凝(PRP)治療?
推薦意見:與anti-VEGF藥物治療相比,PDR患者在PPV前接受PRP治療并不會顯著改善其視力。在決定是否進行PRP治療時,應依據熒光素眼底血管造影和(或)光相干斷層掃描血管成像(OCTA)對視網膜缺血狀況的評估結果。對于視網膜缺血癥狀不斷發展,且OCTA檢測顯示存在大面積無灌注區的患者,可以考慮在手術前增加PRP治療。然而,需要特別注意的是,對于合并TRD的患者,手術前行PRP治療可能會增加視網膜裂孔的風險,因此在進行此類治療時需謹慎權衡(中等推薦)。
自從anti-VEGF藥物上市以來,多個研究比較了PDR患者接受anti-VEGF藥物與PRP治療的獲益。一項RCT[35-36](Diabetic Retinopathy Clinical Research Network Protocol S研究,證據等級Ⅱ)納入了305例PDR患者394只眼,比較了單純anti-VEGF藥物與PRP治療后視力獲益的差異。結果顯示,治療后2年,anti-VEGF藥物治療組和PRP組視力字母評分較基線分別改善2.8、0.2(非劣效P<0.001);治療后5年,anti-VEGF藥物治療組和PRP組視力字母評分較基線分別改善3.1±14.3、3.0±10.5(P=0.68)[36-37],但anti-VEGF藥物治療組視野敏感性變化優于PRP組。另一項RCT[38-39](證據等級Ⅱ)表明,治療后12個月,anti-VEGF藥物治療組和PRP組視力字母評分較基線分別改善1.6和-3.9(P=0.049 5)。這說明,PDR患者PRP治療后視力差于anti-VEGF藥物。
一項隊列研究[37, 40](證據等級Ⅲ)納入106例PDR患者130只眼,比較了PPV聯合手術前PRP(60例67只眼)與單純PPV(46例63只眼)治療后6個月患者的視力變化情況(以logMAR為單位),并進行了長達1年的隨訪。結果顯示,手術前聯合PRP治療組在手術后6個月時視力從基線1.47±0.16提升為0.69±0.09 (P<0.000 1),而單純PPV治療組手術后6個月時視力從基線0.91±0.18提升至0.69±0.14(P=0.121)。結果表明,與單純PPV相比,PPV聯合手術前PRP治療可改善患者手術后視力,但差異無統計學意義。
問題5:PPV中處理PDR患者的纖維血管膜時,選擇膜分割還是膜清除技術?
推薦意見:在處理PDR患者的纖維血管膜時,應以確保手術安全性為首要原則,盡量將膜清除干凈。膜分割技術,即保留部分膜的方法,已被證明能夠改善患者的視力,并且造成裂孔的風險相對較小。這種方法同樣適用于那些新生血管膜上存在較多粗大血管的患者。對于手術經驗相對較少的醫生,可以從膜分割技術開始嘗試,并逐漸向膜清除技術過渡,以積累經驗和提高手術技巧(中等推薦)。
纖維血管膜是PDR患者VH的主要病理基礎,其有效清除在手術治療中占據核心地位。在PPV過程中,針對纖維血管膜的清除策略包括經典的Enbloc技術及其改良形式,即膜分割(membrane segmentation)與膜清除(delamination)技術[39-41]。Enbloc技術作為一種綜合性手段,強調在初始階段即進行精細的視網膜膜分割,隨后實施PPV以徹底清除膜組織[39]。而膜分割與膜清除作為改良Enbloc技術(modified Enbloc excision technique)的核心要素,為復雜膜性病變的處理提供了更為精細與靈活的操作方案[40]。膜清除技術通常在玻璃體切除的主體部分完成后實施,利用高轉速玻璃體切割頭、精密眼內剪刀或雙手協同的剝膜技術,實現對膜組織的直接、高效清除[41]。膜分割技術是在清除大部分玻璃體切除后將整片膜分割成數片孤立的小片機化膜,隨后逐一進行安全去除或根據具體情況選擇保留部分小片膜[42]。這一策略尤其適用于膜與視網膜緊密粘連、難以直接剝離的復雜情況,通過分割技術可以有效減輕牽拉力量,減少視網膜損傷的風險。在PPV中應用膜分割技術,不僅能夠有效緩解增生膜對視網膜的牽拉作用,保護視網膜結構的完整性,還能顯著降低手術過程中醫源性視網膜裂孔的發生率。此外,該技術還有助于減少因硅油或氣體填充等后續治療措施可能引發的并發癥,提高手術的整體安全性與療效[42-43]。
1994年Han等[40]、1997年Meier和Wiedemann[44]以及2002年Kakehashi[45]發表的三項病例系列研究(證據等級Ⅳ),均提供了強有力的證據表明,與傳統Enbloc技術相比,改良Enbloc技術在治療PDR患者時,能夠達到相似的視力改善效果,且伴隨著更高的視網膜復位率。尤為值得注意的是,這一技術革新顯著縮短了手術時長,同時并未增加手術并發癥的發生率,體現了其在提升治療效率與安全性方面的雙重優勢[40, 44-45]。
2004年黎曉新等[41]開展的一項回顧性隊列研究(證據等級Ⅲ)納入276例伴有纖維血管膜的PDR患者(296只眼),對比分析膜分割(106例110只眼)與膜清除(170例186只眼)這兩種手術方法的治療效果。結果顯示,與膜清除組相比,膜分割組在減少醫源性視網膜裂孔的發生率上展現出了顯著優勢(35.5% vs. 54.3%,P<0.01);此外,盡管膜分割組手術后視網膜再出血發生率(25.5%)略低于膜清除組(28.0%),但差異無統計學意義(P>0.05)。值得注意的是,兩組患者在手術后的視力改善上并未表現出顯著差異,這一結果表明,無論是膜分割還是膜清除,均能有效促進患者視力的恢復。這提示,在進行PDR手術時,初學者可以從膜分割技術入手,因其相對較低的醫源性視網膜裂孔風險,有助于在安全的前提下逐步掌握手術技巧,為患者帶來更佳的治療效果。
2021年鄭傳珍等[46]的病例系列研究(證據等級Ⅳ)探討了膜分割技術在治療伴有VH及TRD的嚴重PDR患者中的手術后效果。其聯合了手術前3 d玻璃體腔注射anti-VEGF藥物治療,并秉持“最小量化”PPV理念,采用27G玻璃體切割系統完成標準三通道PPV。手術中,研究團隊運用膜分割技術,以解除視網膜牽拉為主要目標,而非盲目追求增生膜的徹底清除。通過(18.8±9.7)(6~33)個月的隨訪觀察,該研究發現,患者BCVA(以logMAR視力記錄)較手術前顯著提升,從手術前的1.90(1.30,2.30)逐步提升至手術后1周的1.00(0.70,1.90)、手術后1個月的0.80(0.50,1.30),而手術后3、6個月均穩定在0.70(0.40,1.20)(各時間點P值均<0.01),彰顯了視力恢復的顯著性與持續性。此外,首次隨訪時視網膜復位率92.5%,至末次隨訪時提升至96.2%。該研究表明,PPV中應用膜分割技術不僅可解除增生膜對視網膜的牽拉,還能減少醫源性視網膜裂孔的發生。
問題6:PDR患者行PPV治療時如何選擇填充物?
推薦意見:建議對于患有PDR且在手術前已存在視網膜裂孔,或手術過程中產生醫源性視網膜裂孔或視網膜切開的患者,在進行PPV時使用長效氣體(如20%SF6、16%C2F6或14%C3F8[47-49])或硅油進行眼內填充。而對于沒有視網膜裂孔的PDR患者,在充分解除牽拉因素后,可以保留使用常規的眼內灌注液。對于合并有虹膜新生血管的少數患者,仍然可以選擇硅油填充。對于使用長效氣體或硅油填充的患者,手術后應嚴密監測眼壓(中等推薦)。
一項回顧性隊列研究[50](證據等級Ⅲ)納入了接受PPV治療的PDR合并VH患者73例73只眼,其中18只眼(24.7%)手術中未使用填充物,18只眼(24.7%)采用空氣填充,15只眼(20.5%)采用C3F8氣體填充,22只眼(30.1%)采用硅油填充,并以此分為四組。手術后1個月隨訪時,無填充組視力改善顯著優于C3F8氣體填充組;但手術后6個月隨訪時,無填充組、空氣填充組、C3F8氣體填充組三組患者間視力改善程度無明顯差異。四組手術后分別有11.1%、11.1%、6.7%和9.5%的患者出現復發性VH,但其VH復發率差異無統計學意義。手術后6個月隨訪時,無填充組、空氣填充組、C3F8氣體填充組和硅油填充組患者視力分別較基線改善0.98、0.94、0.97、0.19 logMAR單位。除硅油填充組患者視力改善幅度較小(僅為36%)外,其余三組患者視力改善幅度達67%~89%。該研究表明,PPV治療PDR合并VH時采用眼內填充物并不能減少手術后VH發生率,對未合并視網膜裂孔的PDR患者可以不使用眼內填充物。
一項回顧性病例系列研究[42](證據等級Ⅳ)納入PDR合并TRD患者42例50只眼,在PPV中采用膜分割技術去除增生膜。手術中12只眼發生醫源性視網膜裂孔,給予氣體或硅油填充;未發生醫源性視網膜裂孔的患眼給予灌注液填充。手術后隨訪9.7(3~29)個月,患者平均BCVA由手術前0.03±0.25提高到手術后0.17±0.78,68.0%的患眼視力提高,24.0%的患眼視力不變,8.0%的患眼視力下降。一次手術后視網膜復位率為84.0%,其中灌注液填充組(未發生醫源性視網膜裂孔)患眼復位率為89.5%;氣體或硅油填充組(發生醫源性視網膜裂孔)隨訪期間患眼復位率為66.7%,隨訪期結束時最終視網膜復位率為96.0%(2只眼放棄治療)。手術后34.0%(17/50)的患眼發生VH,其中3只眼VH自行吸收,余下14只眼給予anti-VEGF藥物和(或)玻璃體腔灌洗手術治療后積血吸收。發生并發癥的49只眼中,灌注液、氣體、硅油填充分別為28、11、10 只眼。該研究表明,對于未發生醫源性視網膜裂孔的患者可以不進行氣體或硅油填充。
一項回顧性隊列研究[51](證據等級Ⅲ)納入年齡50.44(20~82)歲的接受PPV治療的PDR患者451例536只眼,其中282只眼保留灌注液,138只眼填充氣體(包括空氣、SF6、C2F6和C3F8),116只眼填充硅油,隨訪時間15.2(2~53)個月,探索PPV后使用不同眼內填充物的治療效果。該研究發現,手術前或手術中是否合并視網膜裂孔是PDR患者手術中選擇眼內填充物的重要因素。對于手術中發現視網膜裂孔或手術中造成醫源性視網膜裂孔、視網膜切開的患者,一般采用硅油或膨脹性氣體填充;不存在視網膜裂孔的患者,在有效解除牽拉因素的基礎上,保留灌注液填充;對于少數合并虹膜新生血管等情況仍可選擇硅油填充。
一項RCT[52](證據等級Ⅱ)納入302例伴有TRD或纖維增生膜的PDR患者,手術中隨機接受硅油填充123只眼,14%~16% C3F8填充135只眼。其觀察發現,填充C3F8的患者手術后6個月時視力較好(logMAR視力中位數0.24,95%CI 0.02~0.46,P<0.05),兩組患者手術中視網膜裂孔的發生率相當,手術時間、手術中及手術后并發癥等觀察指標的差異均無統計學意義。該研究認為,對于伴有TRD或纖維增生膜的PDR患者,應當考慮選擇C3F8為一線填充物。當發生視網膜裂孔時,對于單眼患者或伴有新生血管性青光眼、眼球癆(phthisis bulbi)的高風險、無法解除玻璃體視網膜牽拉或視網膜無法解剖復位的情況下,硅油仍是填充物的一線選擇。
問題7:對于糖尿病黃斑水腫(DME),是否推薦PPV治療?
推薦意見:推薦存在牽拉因素的DME(T-DME)患者行PPV治療。對于非牽拉的難治性DME患者(激光光凝無效、anti-VEGF藥物治療無效以及抗炎治療效果不好),可選擇PPV治療(中等推薦)。
對于T-DME患者,PPV作為一線治療已被寫入多個指南和共識中[2, 53-54]。中華醫學會眼科學分會眼底病學組2023年發布的《我國糖尿病視網膜病變臨床診療指南(2022年)——基于循證醫學修訂》[2] 中明確指出,對于因玻璃體視網膜交界面異常引起的DME, 通過PPV解除玻璃體界面的牽拉,是有效緩解黃斑水腫的一種方法;對于非手術治療效果不佳的持續性DME患者,PPV聯合內界膜剝除能有效改善黃斑水腫(證據等級Ⅱ)。歐洲視網膜病專家組在《糖尿病黃斑水腫治療指南(2017年)》[53]中也指出,對存在玻璃體視網膜牽拉的患者,PPV的優勢顯而易見,尤其是存在前后縱向牽拉的DME患者。英國共識工作組2020年更新的《糖尿病視網膜病變和糖尿病黃斑水腫治療路徑管理》[54]指出,應用PPV治療T-DME可有效改善黃斑的解剖結構異常,可以預防視網膜脫離等嚴重并發癥的發生。
非牽拉的持續不吸收的黃斑水腫也可以考慮PPV,但需注意存在視力下降的風險[2]。Raizada等[55]在2015年的一項RCT(證據等級Ⅱ)中納入了44例(44只眼)激光光凝治療無效的非牽拉性DME(nT-DME)患者,其中22例(22只眼)接受了3次anti-VEGF藥物治療(anti-VEGF組),22例(22只眼)接受了PPV聯合內界膜剝除手術治療(PPV組),平均隨訪5.81個月。結果顯示,治療后120 d,PPV組有59.1%(13只眼)視力改善,18.2%(4只眼)視力無變化,22.7%(5只眼)視力下降,手術后視力相對手術前基線改善明顯(P=0.028);治療前后的平均視力差異為0.189 logMAR單位(95%CI 0.021~0.356)。anti-VEGF組有72.8%(16只眼)視力改善,13.6%(3只眼)視力無變化,13.6%(3只眼)視力下降;治療后視力相對基線改善明顯(P=0.018 1),治療前后的平均視力差異為0.203 logMAR單位(95%CI 0.036~0.369)。PPV組患者中央視網膜厚度由手術前410.1 μm顯著降至手術后248.8 μm(P<0.000 1),治療前后降幅平均值為161.4 μm(95%CI 3.28~219.45);anti-VEGF組由基線432.7 μm顯著降至治療后324.3 μm(P<0.000 1),治療前后降幅平均值為108.5 μm(95%CI 62.20~154.71)。但值得注意的是,PPV組與anti-VEGF組患者視力改善程度、中央視網膜厚度治療前后的降幅平均值比較,差異無統計學意義(P>0.05)。這說明,對于激光光凝治療無效的nT-DME患者,PPV治療后4個月中央視網膜厚度較手術前明顯下降,手術后視力較手術前明顯提升,但與單純anti-VEGF藥物3次治療相比,中央視網膜厚度和視力改善程度無顯著差異。
問題8:伴或不伴黃斑前膜(ERM)的DME患者行PPV治療時,是否聯合內界膜剝除?
推薦意見:伴有ERM的DME患者行PPV治療,剝除ERM時是否同時剝除內界膜沒有明確結論,不形成推薦意見。如不伴有ERM,只伴有內界膜增厚,則推薦PPV時剝除內界膜。
6項研究[56-61](包括2項RCT和4項觀察性研究,801只眼)探討了nT-DME患者行PPV治療時,是否需同時剝除內界膜(表6)。通過薈萃分析(證據等級Ⅲ)對比PPV聯合內界膜剝除和單純PPV的手術后相對手術前基線視力的變化值、中央視網膜厚度變化值及手術中和手術后并發癥發生情況。對于視力變化值,分析結果顯示:手術后1個月的視力較基線無顯著差異(1項研究[56],P=0.72);手術后3、6個月,PPV聯合內界膜剝除組的視力改善均優于單純PPV組(手術后3個月:2項研究[56, 61],-0.09 logMAR單位,95%CI -0.12~-0.07,P<0.000 01;手術后6個月:5項研究[56-59, 61],-0.09 logMAR單位,95%CI -0.12~-0.05,P<0.000 01);而手術后1年(5項研究[56, 58-61],P=0.25)及1年以上(最長隨訪時間點為5年)視力較基線的變化值,兩組間差異無統計學意義(3項研究[56, 58-59],P=0.45)(表6,圖7)。對于中央視網膜厚度變化值,共3項研究[57, 60-61](164只眼)報告了此指標。分析結果(證據等級Ⅲ)顯示:手術后3、6個月,兩組間差異無統計學意義(P=0.78、1.00);手術后12個月,PPV聯合內界膜剝除組的中央視網膜厚度較基線的下降值均顯著大于單純PPV組(中位數-82.21 μm,95%CI -94.12~-70.30,P<0.000 01),說明PPV聯合內界膜剝除能夠較好地減輕黃斑水腫(表6,圖8)。對于手術中并發癥情況,基于2項研究[57, 59](155只眼)的薈萃分析結果顯示,PPV聯合或不聯合內界膜剝除手術在手術中醫源性視網膜裂孔的發生率方面無顯著差異(P=0.95)(表6,圖9)。對于手術后并發癥情況,共3項研究[56, 59, 61](254只眼)報告了手術后高眼壓、黃斑中心硬性滲出及新生血管性青光眼的發生率情況。薈萃分析結果(證據等級Ⅲ)顯示:手術后高眼壓(P=0.87)、黃斑中心硬性滲出物(P=1.00)及新生血管性青光眼(P=0.75)的發生率在兩組間均無統計學差異(表6,圖10)。
 圖7
nT-DME患者PPV聯合或不聯合ILM剝除手術后視力變化值(logMAR單位)比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;logMAR:最小分辨角對數;CI:可信區間
圖7
nT-DME患者PPV聯合或不聯合ILM剝除手術后視力變化值(logMAR單位)比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;logMAR:最小分辨角對數;CI:可信區間
 圖8
nT-DME患者PPV聯合或不聯合ILM剝除手術后中央視網膜厚度變化值(μm)比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間;Not applicable:不適用
圖8
nT-DME患者PPV聯合或不聯合ILM剝除手術后中央視網膜厚度變化值(μm)比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間;Not applicable:不適用
 圖9
nT-DME患者PPV聯合或不聯合ILM剝除手術中并發癥發生率比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間
圖9
nT-DME患者PPV聯合或不聯合ILM剝除手術中并發癥發生率比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間
 圖10
nT-DME患者PPV聯合或不聯合ILM剝除手術后并發癥發生率比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間;Not applicable:不適用
圖10
nT-DME患者PPV聯合或不聯合ILM剝除手術后并發癥發生率比較 nT-DME:非牽拉性糖尿病黃斑水腫;PPV:玻璃體切割手術;ILM:內界膜;CI:可信區間;Not applicable:不適用
兩項研究[62-63]探討了對伴有ERM的DME患者行PPV治療時,在存在ERM的情況下是否推薦同時剝除內界膜。發表于2005年的一項RCT[62](證據等級Ⅱ)納入了視力在20/40(Snellen視力表)或以下的彌漫性DME患者29例30只眼,并將其隨機分為內界膜剝除組(15只眼)和內界膜保留組(15只眼),隨訪觀察(9.5±1.7)個月。內界膜剝除組中3只眼(20%)存在ERM,內界膜保留組中6只眼(40%)存在ERM,PPV中均將ERM予以剝除,同時盡量清除殘余玻璃體皮質和后玻璃體等視網膜中央凹前物質。手術后末次隨訪時,兩組患者BCVA均較手術前顯著提高,且兩組間BCVA較基線變化值以及較基線視力改善(內界膜剝除組、保留組分別為47%、60%)和視力維持(內界膜剝除組、保留組分別為53%、60%)的患者比例均無統計學差異(P=0.493 8)。兩組患者手術后1周及1、2、3、4、5、6個月平均視網膜厚度均較手術前明顯變薄,但所有時間點兩組的視網膜厚度差異無統計學意義。兩組患者均未發生嚴重的手術中并發癥。而另一項回顧性隊列研究[63](證據等級Ⅲ)納入累及黃斑中心凹的DME患者45例53只眼,對存在ERM的患眼予以ERM剝除(23只眼),視情況對部分患眼行內界膜剝除(35只眼)。單因素方差分析結果表明,內界膜剝除(P=0.007 0)和ERM剝除(P=0.042 5)與手術后12個月視力改善有關;而多因素方差分析結果則表明,內界膜剝除(P=0.075 2)、ERM剝除(P=0.868 4)及眼內糖皮質激素注射與手術后12個月視力改善無關,同樣印證了上述結果,即伴有ERM的DME患者行PPV治療時,剝除ERM合并內界膜剝除不能進一步改善手術后視力。
問題9:PDR合并白內障患者行PPV時,是否推薦聯合行白內障摘除及人工晶狀體(IOL)植入手術?
推薦意見:當白內障形成影響PPV時,要考慮聯合白內障手術。但鑒于目前的證據,不形成推薦意見。
5項觀察性研究[64-68](599只眼)報道了PDR合并白內障患者行PPV時聯合或不聯合白內障手術的臨床效果(表7)。其結果表明,PDR患者行PPV時聯合或不聯合白內障手術的手術后視力、VH和TRD發生率沒有顯著性差異,PDR患者PPV聯合白內障手術會增加手術后短期的炎癥反應(纖維蛋白形成、虹膜粘連、角膜水腫)。
基于2項研究[64, 66](388只眼)的薈萃分析(證據等級Ⅲ)結果顯示:聯合組與單純PPV組之間手術中VH(OR=0.71,95%CI 0.25~2.01,P=0.52)、醫源性視網膜裂孔(OR=0.57,95%CI 0.25~1.27,P=0.17)的發生率無顯著差異(表6,圖11)。聯合組與單純PPV組之間手術后VH(3項研究[64, 66-67] ,OR=0.43,95%CI 0.14~1.29,P=0.13)、前房滲出(1項研究[68],OR=5.11,95%CI 0.57~45.62,P=0.14)、高眼壓(4項研究[64-65, 67-68],OR=1.84,95%CI 0.90~3.75,P=0.09)和視網膜脫離(2項研究[64, 66],OR=0.52,95%CI 0.08,3.46,P=0.50)的發生率均無顯著差異(表6,圖12)。3項研究(證據等級Ⅲ)報告了手術后其他前房并發癥的發生情況。結果顯示,聯合組手術后纖維蛋白形成[65-66](30% vs. 7%,P=0.042;17% vs. 2%,P=0.019)、手術后2周虹膜粘連[65](30% vs. 7%,P=0.042)、手術后角膜水腫[66](36.4% vs. 8.3%,P<0.05)的發生率顯著高于單純PPV組。而兩組間瞳孔后粘連[68](3.0% vs. 4.2%,P=1.000)、手術后前房出血[67](0.0% vs. 1.9%,P=0.631)、新生血管性青光眼[67](0.0% vs. 1.9%,P=0.631)、角膜混濁[66](2.2% vs. 4.3%,P>0.05)的發生率差異均無統計學意義。
 圖11
PDR合并白內障患者PPV聯合或不聯合白內障手術的手術中指標比較 PDR:增生型糖尿病視網膜病變;PPV:玻璃體切割手術;VH:玻璃體積血;CI:可信區間
圖11
PDR合并白內障患者PPV聯合或不聯合白內障手術的手術中指標比較 PDR:增生型糖尿病視網膜病變;PPV:玻璃體切割手術;VH:玻璃體積血;CI:可信區間
 圖12
PDR合并白內障患者PPV聯合或不聯合白內障手術的手術后并發癥指標比較 PDR:增生型糖尿病視網膜病變;PPV:玻璃體切割手術;VH:玻璃體積血;CI:可信區間
圖12
PDR合并白內障患者PPV聯合或不聯合白內障手術的手術后并發癥指標比較 PDR:增生型糖尿病視網膜病變;PPV:玻璃體切割手術;VH:玻璃體積血;CI:可信區間
共5項研究[64-67, 69](448只眼)報告了PDR合并白內障患者行PPV時聯合或不聯合白內障手術的視力預后情況(證據等級Ⅲ)。Lee等[64]和Park等[65]研究發現,手術后1、2、3、6個月,兩組間視力差異均無統計學意義(P>0.05)。Kadonosono等[66]經過18.3(7~24)個月的隨訪觀察亦發現,兩組患者視力差異無統計學意義(P>0.05)。王萍等[69]通過一項回顧性隊列研究納入合并不同程度白內障的PDR患者72例82只眼,將其分為3組:A組25例28只眼,行PPV同期聯合白內障超聲乳化及IOL植入手術;B組20例24只眼,行玻璃體腔注射anti-VEGF藥物輔助PPV,同期聯合白內障超聲乳化及IOL植入手術;C組27例30 只眼,Ⅰ期行PPV,Ⅱ期行硅油取出聯合白內障超聲乳化及IOL植入手術。患者手術后隨訪(9.0±2.5)(6~12)個月,A組、B組、C組患者手術后logMAR BCVA 分別為1.007±0.455、1.000±0.482、1.033±0.531,三組患者視力較手術前均有明顯提高(P<0.05),但三組間差異無統計學意義(P=0.195)。Tseng等[67]納入84例84只眼觀察發現,聯合組[隨訪(15.6±7.0)個月]患者視力提高1行或更多的比例顯著高于單純PPV組[隨訪(16.1±0.5)個月](67.7% vs. 32.1%,P=0.003)。
3 展望
針對DR的手術治療,尤其是涉及玻璃體視網膜手術的操作,其復雜性和挑戰性主要取決于眼科醫生的專業知識、技術水平及臨床經驗。鑒于此領域的多樣性和復雜性,很難就具體的手術細節達成一致意見。本專家共識旨在為中國眼科專科醫生以及從事眼底病專業的醫生提供臨床指導,但不應被視為具有法律效力的醫療依據。
基于對現有證據的綜合評估,我們建議在中國人群中進行更系統性的研究,以驗證PPV是否能夠有效控制DR患者增生早期的病情進展。這些研究將為未來的 DR治療決策、指南制定以及實際臨床實踐提供堅實的基礎和可靠的科學依據。
形成指南意見的專家組成員
臨床主席
黎曉新 廈門大學附屬廈門眼科中心/北京大學人民醫院(執筆人)
許 迅 上海交通大學醫學院附屬第一人民醫院
方法學聯席主席
夏 君 寧波諾丁漢GRADE中心
核心專家(按照姓氏拼音排序)
常 青 復旦大學附屬眼耳鼻喉科醫院
丁小燕 中山大學中山眼科中心
李筱榮 天津醫科大學眼科醫院
梁建宏 北京大學人民醫院
劉 堃 上海交通大學醫學院附屬第一人民醫院
陸 方 四川大學華西醫院
羅 靜 中南大學湘雅二醫院
呂 林 中山大學中山眼科中心
馬 進 中山大學中山眼科中心
孫曉東 上海交通大學醫學院附屬第一人民醫院
唐仕波 中南大學愛爾眼科學院
陶 勇 首都醫科大學附屬北京朝陽醫院
王雨生 空軍軍醫大學西京醫院
魏文斌 北京同仁醫院
邢怡橋 武漢大學人民醫院
徐格致 復旦大學附屬眼耳鼻喉科醫院
于偉泓 北京協和醫院
張 風 北京同仁醫院
張美霞 四川大學華西醫院
張 明 四川大學華西醫院
張少沖 深圳市眼科醫院
趙明威 北京大學人民醫院
趙培泉 上海交通大學醫學院附屬新華醫院
周 鵬 上海百匯醫院
討論專家(按照姓氏拼音排序)
常 青 復旦大學附屬眼耳鼻喉科醫院
陳曉隆 中國醫科大學附屬盛京醫院
陳 宜 北京中日友好醫院
陳長征 武漢大學人民醫院
戴 虹 北京醫院
丁小燕 中山大學中山眼科中心
惠延年 空軍軍醫大學西京醫院
黎曉新 廈門大學附屬廈門眼科中心/北京大學人民醫院
李海平 北京大學第三醫院
李秋明 鄭州大學第一附屬醫院
李甦雁 徐州市第一人民醫院
李筱榮 天津醫科大學眼科醫院
梁建宏 北京大學人民醫院
劉慶淮 南京醫科大學第一附屬醫院
劉曉玲 溫州醫科大學附屬眼視光醫院
劉 勇 第三軍醫大學西南醫院
柳 林 上海交通大學醫學院附屬仁濟醫院
陸 方 四川大學華西醫院
羅 靜 中南大學湘雅二醫院
呂 林 中山大學中山眼科中心
馬 進 中山大學中山眼科中心
馬 翔 大連醫科大學附屬第一醫院
苗 恒 北京大學人民醫院
彭紹民 哈爾濱醫科大學附屬第二醫院
曲進鋒 北京大學人民醫院
沈 璽 上海交通大學醫學院附屬瑞金醫院
宋艷萍 中國人民解放軍中部戰區總醫院
宋宗明 河南省立眼科醫院
蘇冠方 吉林大學第二醫院
孫大衛 哈爾濱醫科大學第二附屬醫院
孫曉東 上海交通大學醫學院附屬第一人民醫院
孫旭芳 華中科技大學同濟醫學院附屬同濟醫院
唐羅生 中南大學湘雅二醫院
唐仕波 中南大學愛爾眼科學院
陶 勇 首都醫科大學附屬北京朝陽醫院
萬光明 鄭州大學第一附屬醫院
王常觀 北京大學第三醫院
王 方 同濟大學附屬第十人民醫院
王 鮮 貴州醫科大學附屬醫院
王艷玲 首都醫科大學附屬北京友誼醫院
王雨生 空軍軍醫大學西京醫院
王志軍 北京中日友好醫院
魏文斌 北京同仁醫院
邢怡橋 武漢大學人民醫院
徐格致 復旦大學附屬眼耳鼻喉科醫院
徐國興 福建醫科大學第一臨床醫學院
許 迅 上海交通大學醫學院附屬第一人民醫院
楊 波 吉林大學第二醫院
柳 林 上海交通大學醫學院附屬仁濟醫院
姚 勇 無錫市人民醫院
于偉泓 北京協和醫院
于旭輝 哈爾濱醫科大學附屬第一醫院
俞素勤 上海交通大學醫學院附屬第一人民醫院
喻曉兵 北京醫院
張 風 北京同仁醫院
張美霞 四川大學華西醫院
張 明 四川大學華西醫院
張少沖 深圳市眼科醫院
張文芳 蘭州大學第二醫院
趙明威 北京大學人民醫院
趙培泉 上海交通大學醫學院附屬新華醫院
趙鐵英 深圳市眼科醫院
周 鵬 上海百匯醫院
朱 丹 內蒙古醫學院附屬醫院
莊文娟 寧夏醫學院附屬醫院