高效液相色譜法(HPLC)是目前主流的檢測血紅蛋白技術,糖化血紅蛋白(HbA1c)是診斷糖尿病的金指標,但 HPLC 檢測時 HbA1c 易受到地中海貧血因子血紅蛋白 F(HbF)/血紅蛋白 A2(HbA2)和血紅蛋白變異體的干擾而影響檢測結果的準確性。本研究基于高效液相色譜法提出一種新型抗干擾血紅蛋白分析系統,本系統通過改進高壓三梯度洗脫法,優化高壓層析柱中微球粒徑和篩板孔徑,并優化雙柱塞往復式串聯高壓泵的結構,既能檢測 HbA1c 又可檢測地中海貧血因子 HbF/HbA2 和血紅蛋白變異體,抗干擾性好,性能穩定,有望實現產業化。本系統與日本東曹 G8、美國伯樂Ⅶ和 D10 糖化血紅蛋白分析系統等世界一線品牌產品進行 HbA1c 和地中海貧血因子 HbF/HbA2 檢測性能對比,結果表明,本系統與世界一流系統的線性相關性好,檢測性能優異,是國內首次實現快速、精準篩查糖化血紅蛋白和地中海貧血因子 HbF/HbA2 的高效液相色譜法血紅蛋白分析系統。
引用本文: 徐巖, 姚甜甜, 胡文雍, 張波, 郭興明. 一種新型抗干擾高效液相色譜法血紅蛋白分析系統. 生物醫學工程學雜志, 2021, 38(5): 940-950. doi: 10.7507/1001-5515.202101069 復制
版權信息: ?四川大學華西醫院華西期刊社《生物醫學工程學雜志》版權所有,未經授權不得轉載、改編
引言
糖尿病已成為一個嚴重影響人類生命健康的全球性公共衛生問題,我國的糖尿病流行形勢尤為嚴峻[1-2]。與此同時,全世界約有 3.4 億人攜帶有血紅蛋白變異體致病基因,血紅蛋白變異體已經成為全球前三位常見的出生缺陷[3-6]。血紅蛋白(hemoglobin,Hb)包括血紅蛋白 A(HbA)、血紅蛋白 F(HbF)和血紅蛋白 A2(HbA2),HbA 分為未被糖基化(hemoglobin A0,HbA0)和糖基化(hemoglobin A1,HbA1)兩種,其中 HbA1 包括糖化血紅蛋白 A1a(HbA1a)、糖化血紅蛋白 A1b(HbA1b)和糖化血紅蛋白 A1c(HbA1c)。
在糖尿病管理中,糖尿病的診斷和監控對于患者的生命健康尤為重要。2010 年美國糖尿病協會(American Diabetes Association,ADA)和歐洲糖尿病協會(European Association for the Study of Diabetes,EASD)相繼發表糖尿病診斷和治療指南,均正式提出 HbA1c 是糖尿病早期診斷的金指標,同時可作為病情檢測指標[7]。美國糖尿病協會建議:HbA1c 含量 ≥ 6.5%,診斷為糖尿病;HbA1c 含量 ≥ 5.7%,診斷為糖尿病前期[8-9]。對于糖尿病的檢測和監控,高效液相色譜法(high performance liquid chromatography,HPLC)是 HbA1c 檢測的金標準,糖尿病控制及并發癥研究(Diabetes Control and Complications Trial,DCCT)將 HPLC 作為糖尿病研究中使用的唯一方法,美國國家糖化血紅蛋白標準化計劃(National Glycohemoglobin Standardization Program,NGSP)將 HPLC 作為標準化中的參考方法[10-12]。HPLC 的檢測原理為在一定離子強度緩沖液中,不同血紅蛋白會不同程度地與色譜柱表面的離子原基結合,因此,需要將 HbA1c 與其他血紅蛋白(HbA1b、HbA1a 和 HbA0)分離后進行檢測[13-20]。
在地中海貧血和血紅蛋白變異體的篩查中,由于 α-地中海貧血患者的 HbA2 含量下降,β-地中海貧血患者的 HbA2 和 HbF 含量上升[21-23],而 HbA2、HbF 和 HbA 所帶電荷相近,采用液相色譜法進行 HbA1c 檢測時易受到血紅蛋白變異體的干擾而影響檢測結果的準確性[12, 24-26]。
探索能夠有效分離糖化血紅蛋白、地中海貧血因子 HbF/HbA2 和血紅蛋白變異體的檢測方法是目前血紅蛋白分析研究的熱點。有研究發現,通過優化高效液相色譜法的洗脫方式,可以提高分離效率,減少干擾[27-28]。研究證明,通過改進填料微球的粒徑,或對微球表面進行化學修飾,也可以提高樣本的分離效率[29-31]。
因此,本文提出一種新型抗干擾高效液相色譜法血紅蛋白分析系統,通過改進高壓三梯度洗脫法,優化高壓層析柱中微球和篩板結構,優化雙柱塞往復式串聯高壓泵的結構,可實現樣本中不同血紅蛋白的洗脫和檢測,與世界一線品牌產品進行 HbA1c、地中海貧血因子 HbF/HbA2 和血紅蛋白變異體檢測性能對比,完成關于血紅蛋白檢測性能的驗證。
1 新型抗干擾高效液相色譜法血紅蛋白分析系統
本新型抗干擾高效液相色譜法血紅蛋白分析系統(以下簡稱“本系統”)的核心組成包括改進的高壓三梯度洗脫法、優化的高壓層析柱、改良的雙柱塞往復式串聯高壓泵和紫外-可見光學檢測裝置,以及液路、硬件和軟件等部分。
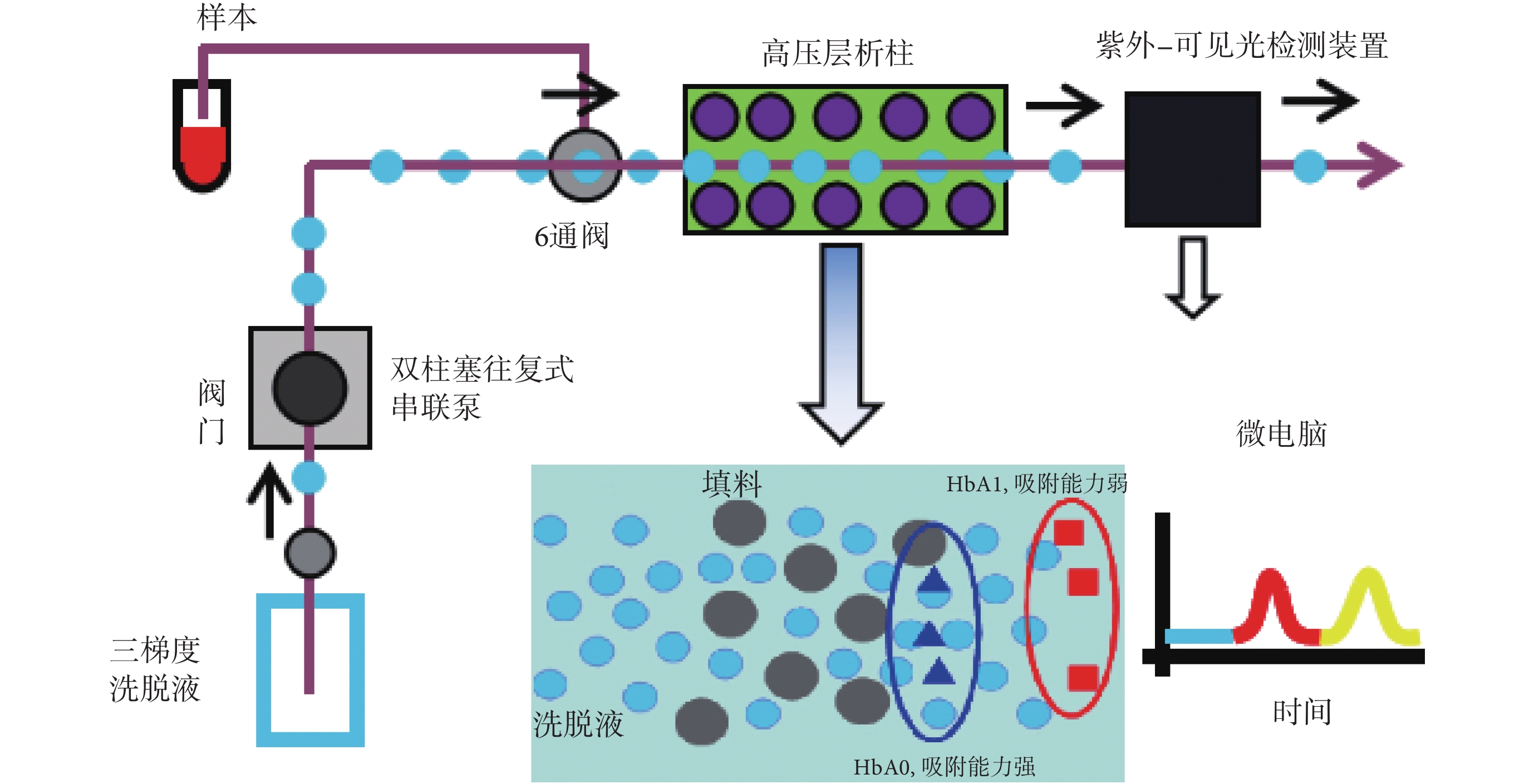
本系統旨在實現不同血紅蛋白分子的檢測,檢測流程如圖 1 所示,三梯度洗脫液溶劑通過雙柱塞往復式串聯高壓泵的抽吸作用進入液路管道,通過系統控制六通閥,使溶劑流進高壓層析柱,與此同時待測樣本通過自動進樣器進入高壓層析柱中,此時高壓層析柱中的填料微球和樣本中不同血紅蛋白分子及洗脫液由于電荷作用發生不同程度的吸附,使各血紅蛋白分子發生分離,在不同時刻進入紫外-可見光學檢測裝置檢測,根據光吸收率的不同,檢測出不同血紅蛋白分子的含量,得到血紅蛋白分析色譜圖。
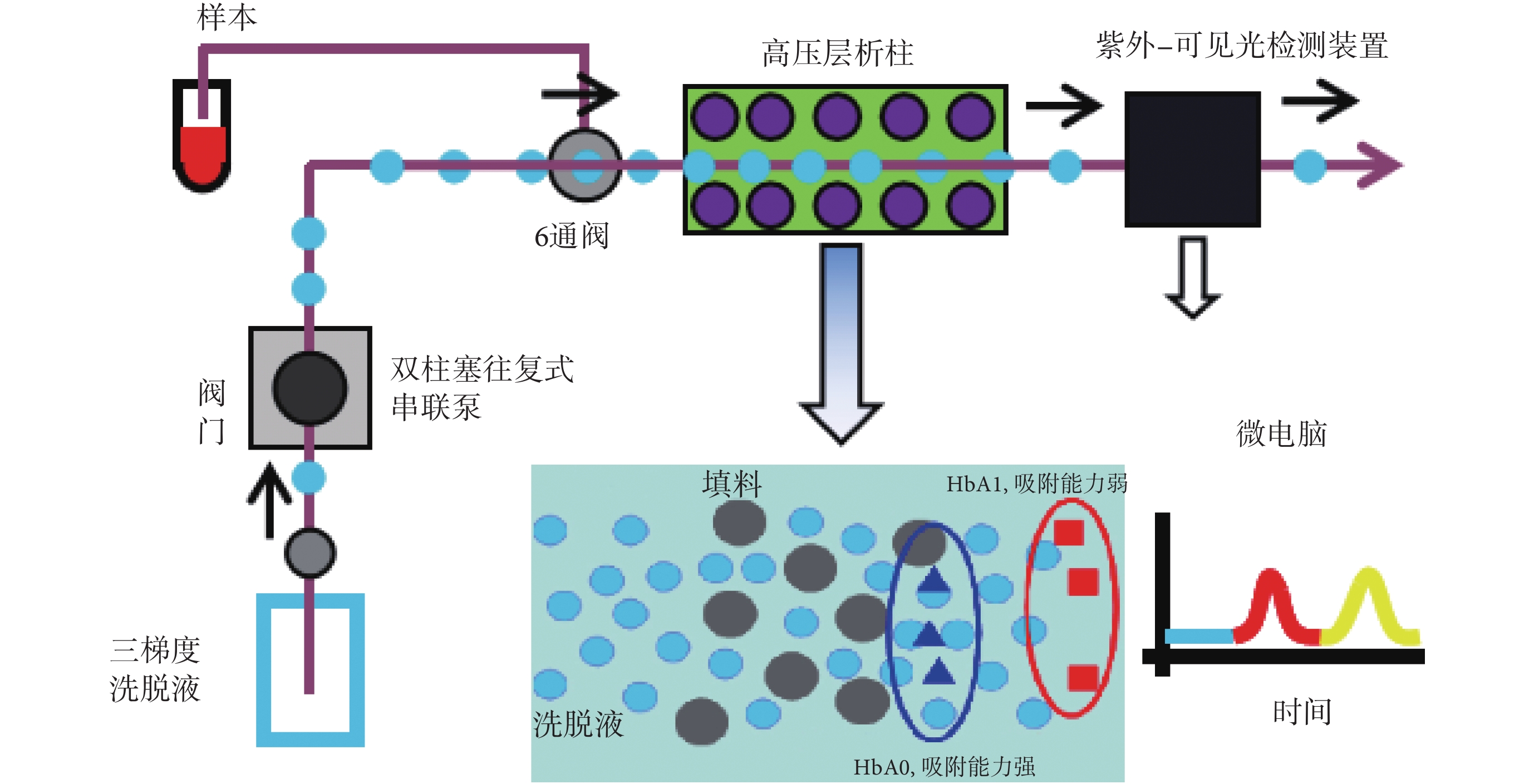 圖1
新型抗干擾高效液相色譜法血紅蛋白分析系統檢測示意圖
Figure1.
Schematic diagram of the new anti-interference hemoglobin analysis system by HPLC
圖1
新型抗干擾高效液相色譜法血紅蛋白分析系統檢測示意圖
Figure1.
Schematic diagram of the new anti-interference hemoglobin analysis system by HPLC
峰值計算:采用了基于正態分布的高斯擬合算法,獲取原始色譜信號中色譜峰的起點坐標、終點坐標和峰值點坐標;根據起點坐標和終點坐標,從原始色譜信號中分離出相應色譜峰的色譜信號;根據與色譜峰對應的擬合函數對相應的色譜信號進行擬合,得到與色譜峰對應的擬合信號;擬合函數是基于峰值點坐標構建的函數;基于擬合信號計算色譜峰的峰面積。
1.1 改進的高壓三梯度洗脫法
改進的高壓三梯度洗脫法是本系統中的核心技術,本研究采用帶不同正離子濃度的 A、B、C 三種洗脫液,通過改進高壓三梯度洗脫法,控制流動相流經高壓層析柱的時間和順序,實現 HbA1c、HbF 和 HbA2 的有效分離。
洗脫液 A、B、C 均帶不同濃度的正離子,且正離子濃度依次增加。洗脫液 A 為(40±10)mmol/L 的丁二酸鹽水溶液,用于洗脫糖化血紅蛋白 HbA1a 和 HbA1b;洗脫液 B 為(100±10)mmol/L 的丁二酸鹽水溶液,用于洗脫糖化血紅蛋白 HbA1c;洗脫液 C 為(500±10)mmol/L 的丁二酸鹽水溶液,用于洗脫非糖化血紅蛋白 HbA0 及變異體。
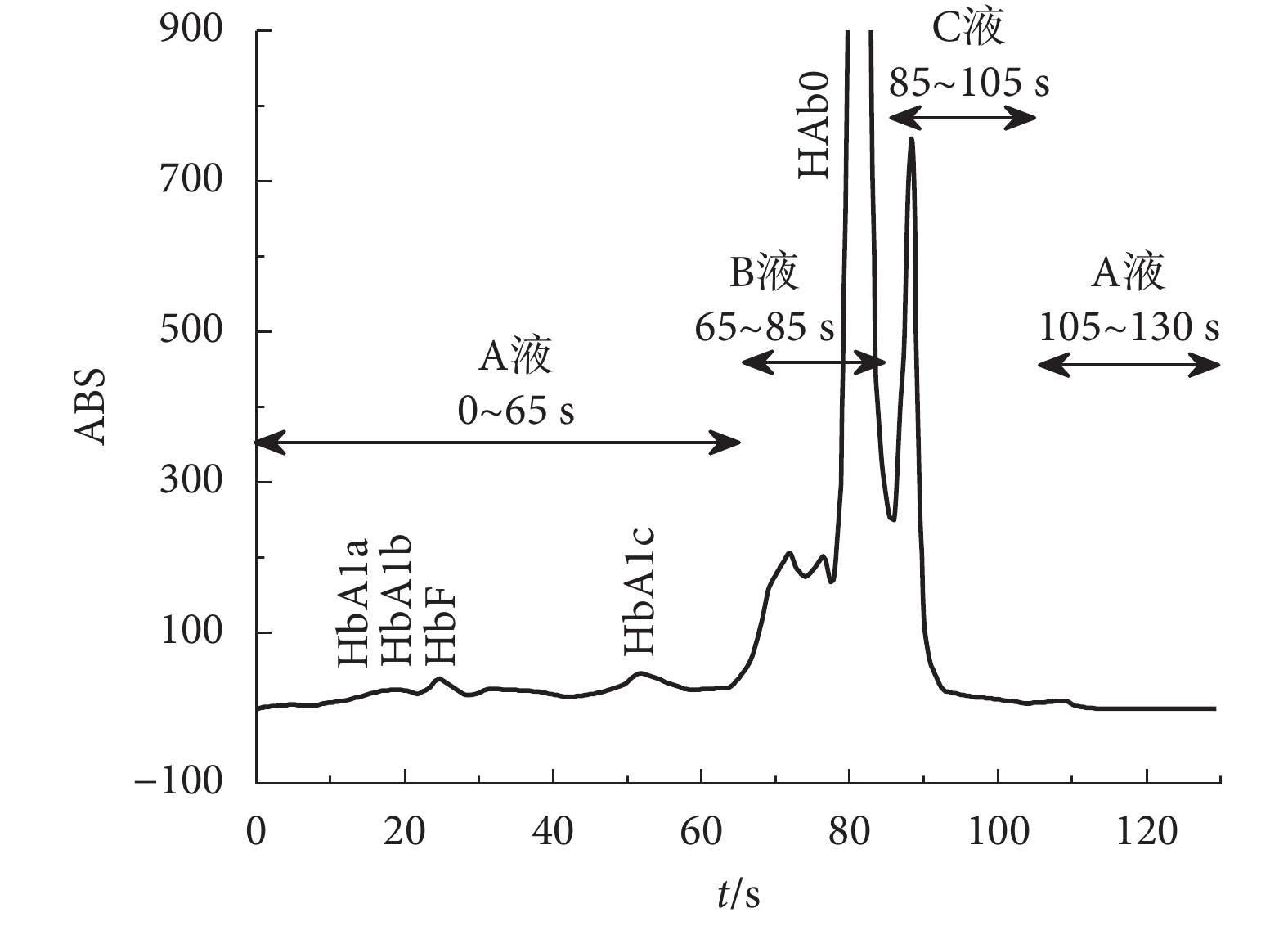
本系統將洗脫液 A、B、C 流經層析柱的兩種不同時間和順序分成糖化血紅蛋白檢測模式和地中海貧血檢測模式。糖化血紅蛋白檢測模式:可進行糖化血紅蛋白檢測,控制洗脫液 A、B、C 流經層析柱的時間為 130 s,其中 0~65 s 用 A 液進行洗脫,65~85 s 用 B 液進行洗脫,85~105 s 用 C 液進行洗脫,105~130 s 用 A 液進行洗脫,如圖 2 所示,實現 HbA1a、HbA1b、HbF、不穩定的 HbA1c(labile HbA1c,LA1c)、HbA1c、HbA0 的分離。
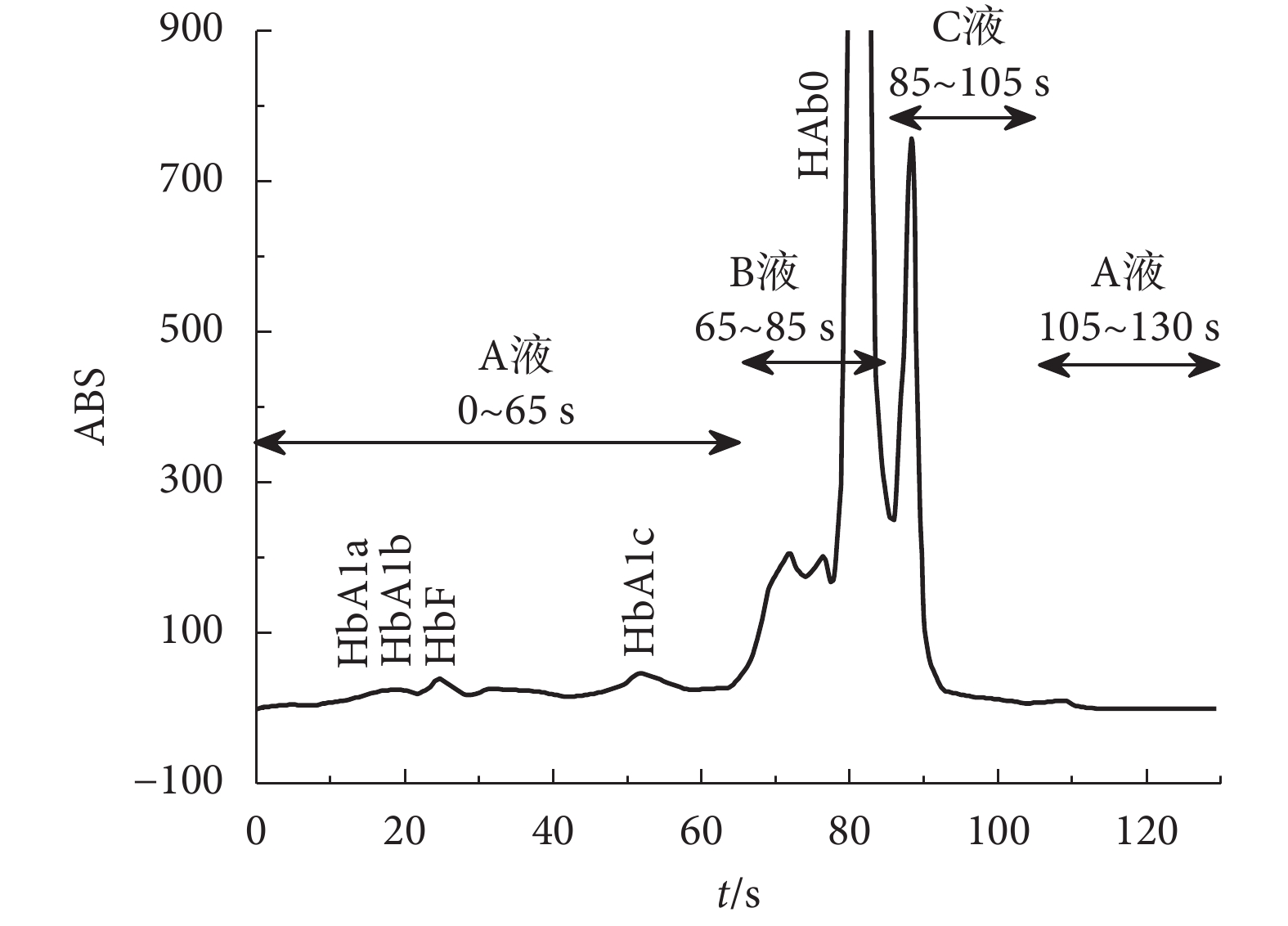 圖2
糖化血紅蛋白檢測模式下三種洗脫液的輸送時間
Figure2.
Delivery time of three eluents in glycosylated hemoglobin detection mode
圖2
糖化血紅蛋白檢測模式下三種洗脫液的輸送時間
Figure2.
Delivery time of three eluents in glycosylated hemoglobin detection mode
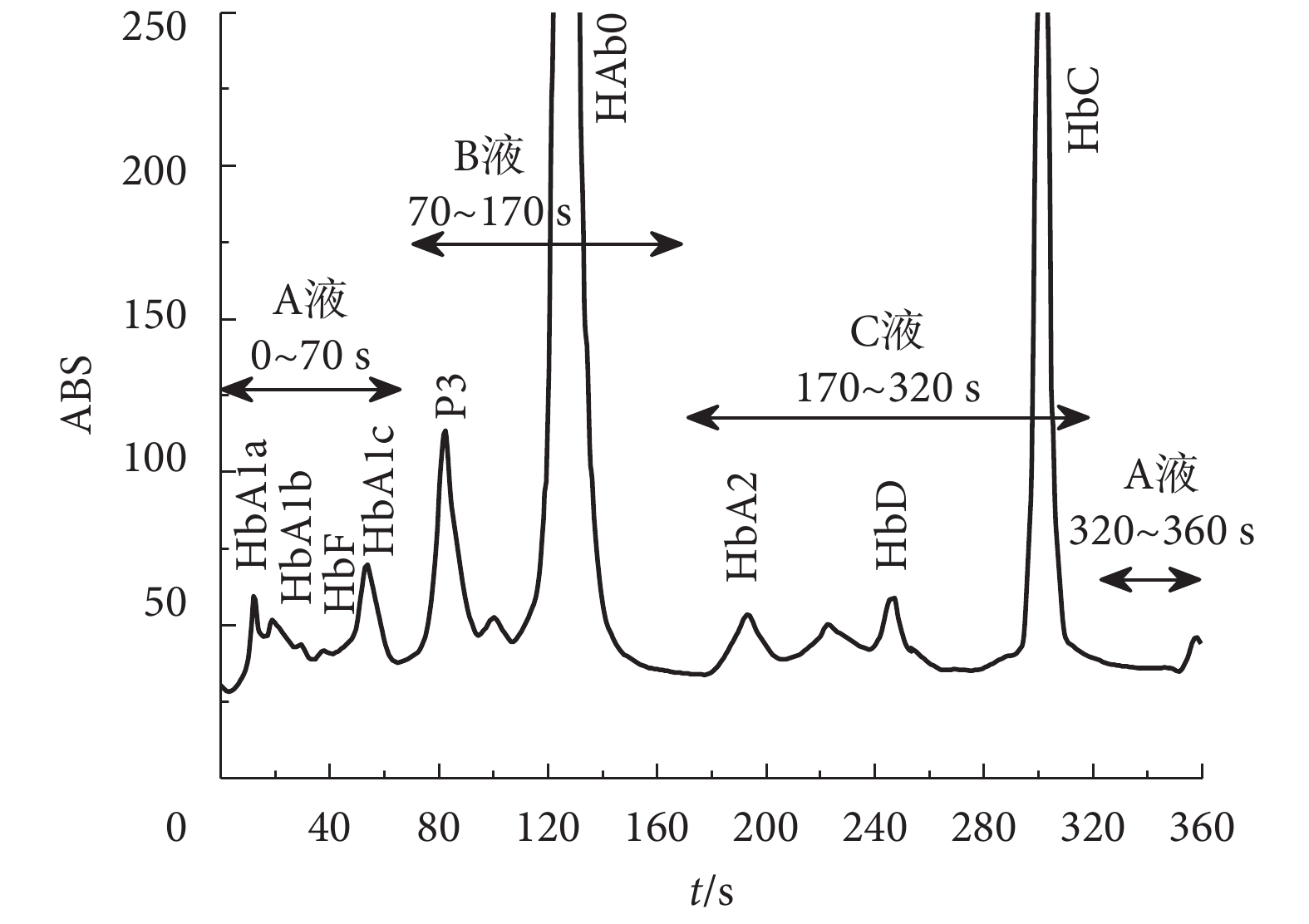
地中海貧血檢測模式:實現糖化血紅蛋白、血紅蛋白變異體和地中海貧血因子 HbF/HbA2 的分離、檢查,控制洗脫液 A、B、C 流經層析柱的時間為 360 s,其中 0~70 s 用 A 液進行洗脫,70~170 s 用 B 液進行洗脫,170~320 s 用 C 液進行洗脫,320~360 s 用 A 液進行洗脫,如圖 3 所示。將 HbA2 分離出來,還可分離 HbA1a、HbA1b、HbF、LA1c、HbA1c、HbA0,同時也會分離出變異血紅蛋白 EDSC(HbE/HbD/HbS/HbC)。
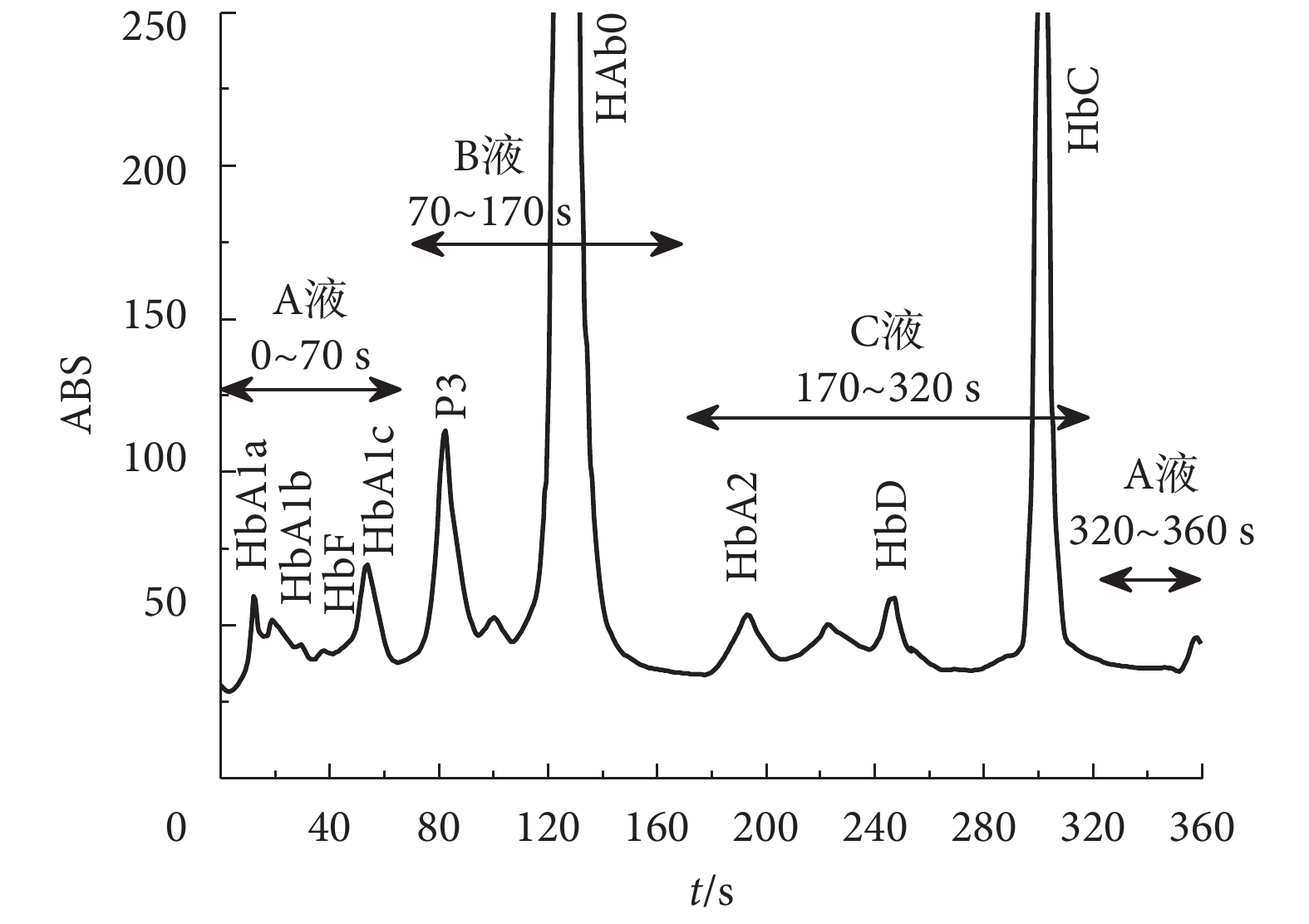 圖3
地中海貧血檢測模式下三種洗脫液的輸送時間
Figure3.
Delivery time of three eluents in thalassemia detection mode
圖3
地中海貧血檢測模式下三種洗脫液的輸送時間
Figure3.
Delivery time of three eluents in thalassemia detection mode
1.2 優化的高壓層析柱
高壓層析柱是整個高效液相色譜系統的心臟,層析柱離子交換填料微球是層析柱的核心材料,直接關系到檢測結果的精度。本系統優化了高壓層析柱中微球粒徑,通過改進單體結構,引入環氧基團,采用種子溶脹法成功制備出粒徑在 5~6 μm 且尺寸均一的聚苯乙烯填料微球,微球表面帶有大量帶負電的功能基團,如圖 4 所示。帶負電填料微球和 HbA1a、HbA1b、HbA1c、HbA0、HbF、HbA2 發生吸附作用,其中 HbA0 吸附作用最強,HbA1c、HbA1b 和 HbA1a 依次減弱。待測樣本通過自動進樣器進入層析柱中,與此同時三梯度洗脫液溶劑通過雙柱塞往復式串聯高壓泵的抽吸作用進入液路管道,通過系統控制六通閥,使溶劑流進高壓層析柱,其中流動相 A 首先進入層析柱中,其次是流動相 B、流動相 C,最后流動相 A 進入層析柱中進行洗滌。同時本系統通過增加篩板,優化篩板孔徑,可有效過濾掉樣本中殘留的絮狀物,延長使用壽命。本系統高壓層析柱的規格為 4.6 mm×30 mm,實現耐壓至少 20 MPa。
 圖4
層析柱微球的 SEM 圖
Figure4.
SEM images of column microspheres
圖4
層析柱微球的 SEM 圖
Figure4.
SEM images of column microspheres
本研究提供一種液相色譜用弱陽離子交換填料,首先采用帶有環氧基團的乙烯基單體和二乙烯基苯交聯劑合成表面具有環氧基的聚甲基丙烯酸縮水甘油醚-二乙烯基苯基質無孔微球,對環氧基進行水解處理,再接枝一層含多環氧基的縮水甘油醚,使微球表面帶有多活性環氧基官能團,最后在親水化涂層表面帶有多活性環氧基官能團基礎上,采用可逆加成-斷裂鏈轉移聚合技術在基質表面引入含羧基、磺酸基或氨基等官能團,并通過調節聚合過程中單體和鏈轉移試劑的比例來控制官能團的長度結構和密度,最終得到官能團結構和密度均可控的高性能離子交換色譜介質,具有更優良的離子交換性能。實現填料的粒徑為 5~6 μm,無孔,對微球進行離子交換容量(IEC)檢測,通過對洗滌過填料微球的 NaOH 溶液和氯化鈉溶液混合液進行滴定,得到干燥微球的離子交換容量為 25 mmol/L。
1.3 改良的雙柱塞往復式串聯泵
高壓泵是實現壓力的關鍵,本系統對雙柱塞往復式串聯泵的結構進行優化,采用兩個泵,并將其處于同一水平位置,通過優化控制系統的算法,控制兩個泵中柱塞的運動,實現壓力的穩定和流速的恒定,提高檢測結果的準確性;通過改進柱塞桿和單向閥的使用材料,提高該高壓泵的承受壓力和使用壽命,可承受 40 MPa 的壓力,往復壽命高達 400 萬次。
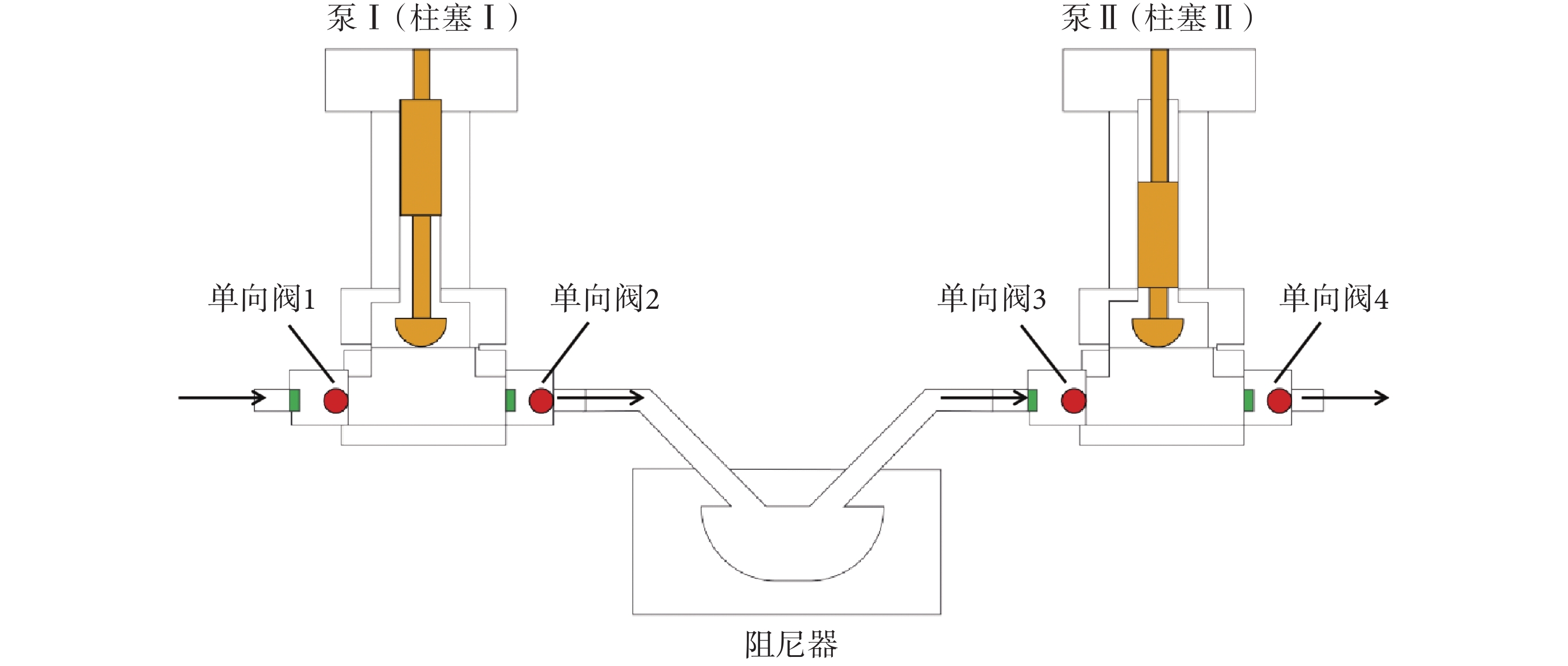
改良的雙柱塞往復式串聯泵工作原理:先在伺服系統中對柱塞Ⅰ和柱塞Ⅱ的運動最低點、最高點和恒定點進行設置,控制柱塞Ⅰ和柱塞Ⅱ移動到恒定點,如圖 5 所示。當系統控制伺服電機正向偏轉時,使泵Ⅰ中裝有最大體積的流動相;然后控制伺服電機發生反向偏轉,使泵Ⅰ和泵Ⅱ中有相同體積的流動相,完成設置。
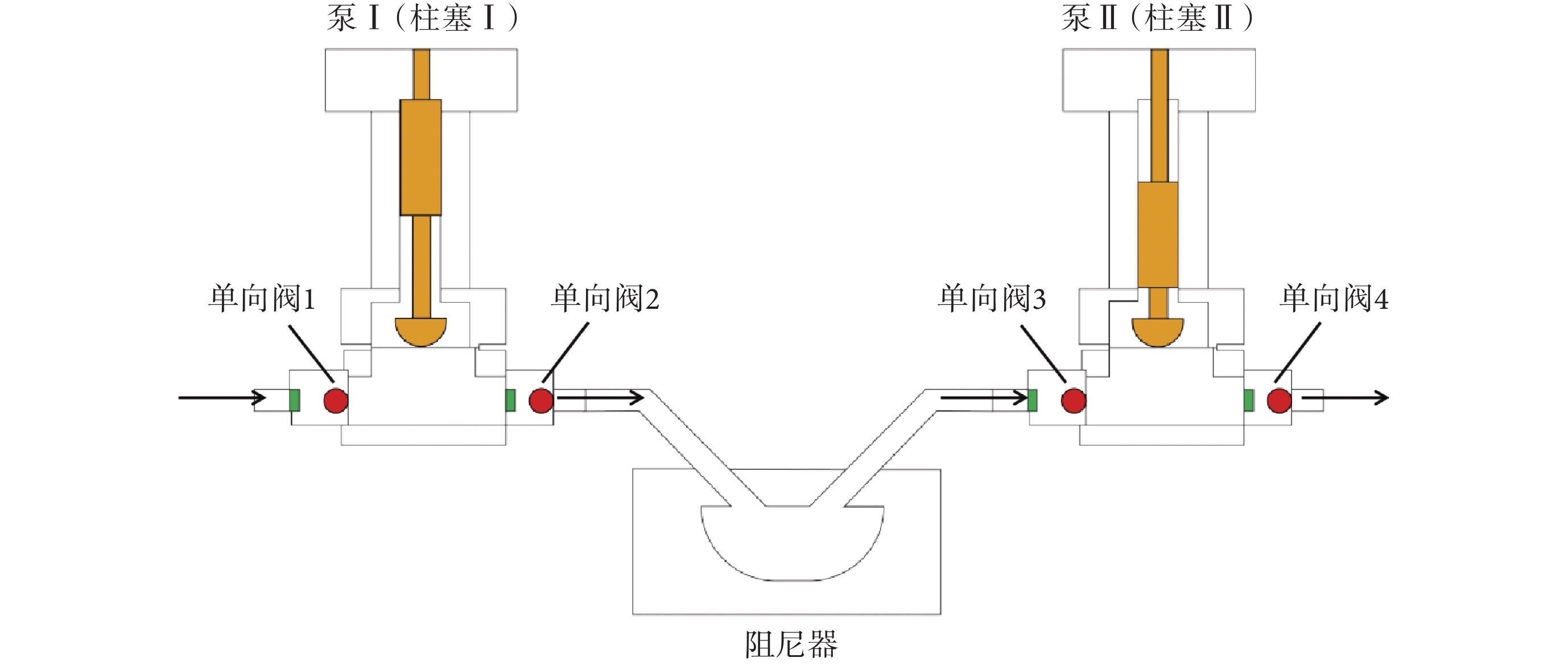 圖5
雙柱塞往復式串聯泵示意圖
Figure5.
Diagram of double plunger reciprocating high pressure pump
圖5
雙柱塞往復式串聯泵示意圖
Figure5.
Diagram of double plunger reciprocating high pressure pump
在系統正式進行測試時。首先正向偏轉伺服電機,打開泵Ⅰ中的單向閥 1,控制向上移動泵Ⅰ中的柱塞Ⅰ從設置點移動到最高點;然后反向偏轉伺服電機,打開泵Ⅰ中的單向閥 2 和泵Ⅱ的單向閥 3,控制泵Ⅰ從最高點到達設置點,控制泵Ⅱ中的柱塞Ⅱ從設置點向上移動到最高點。打開單向閥 4,控制泵Ⅱ中的柱塞Ⅱ從最高點向上移動到設置點,把流動相送入了色譜系統,重復這些過程,每次運行周期中都只輸出泵中流動相的一半,實現了連續恒定的流量控制。
2 實驗部分
2.1 研究對象
正常樣本:選取 2019 年 9 月至 11 月成都第三人民醫院體檢健康者血液樣本,納入標準為測定無異常血紅蛋白、無嚴重肝腎疾病、無血液系統疾病、無糖尿病史。
糖尿病樣本:選取 2019 年 9 月至 11 月成都第三人民醫院確認存在糖尿病的患者血液樣本,納入標準為測定無異常血紅蛋白、無嚴重肝腎疾病、無血液系統疾病。
α-地中海貧血樣本:選取 2019 年 9 月至 11 月成都第三人民醫院確認存在 α-地中海貧血的患者血液樣本,納入標準為測定存在異常血紅蛋白、無嚴重肝腎疾病、無血液系統疾病、無糖尿病史。
β-地中海貧血樣本:選取 2019 年 9 月至 11 月成都第三人民醫院確認存在 β-地中海貧血的患者血液樣本,納入標準為測定存在異常血紅蛋白、無嚴重肝腎疾病、無血液系統疾病、無糖尿病史。
血紅蛋白變異體樣本:選取 2020 年 10 月購買的國際臨床化學和實驗室醫學聯盟(International Federation of Clinical Chemistry and laboratory medicine,IFCC)的血紅蛋白變異體(HbE/HbD/HbS/HbC)樣本。
樣品前處理過程:樣本采集使用乙二胺四乙酸二鉀(ethylene diamine tetraacetic acid-K2,EDTA-K2)抗凝的真空采血管,每個樣品分裝 300 μL,–80℃ 冷凍保存;樣本檢測前,將樣本從–80℃ 冰箱取出置于 2~8℃ 冰箱過夜復融。
2.2 儀器與試劑
本系統及相應的配套試劑、校準品、質控品;美國伯樂Ⅶ系統和 D10 系統及其相應的配套試劑、校準品、質控品;日本東曹 G8 系統及配套試劑、校準品、質控品。
2.3 方法學評估
2.3.1 批內和日間精密度
依據美國臨床實驗室標準化協會(Clinical and Laboratory Standards Institute,CLSI)EP5-A2 文件[32]的精密度評估方法,選取 HbA1c 低、中、高值各 15 份樣本,在 1 天內對這些樣本進行測試,計算批內精密度。選取 HbA1c 低、中、高值各 1 份樣本,每份樣本分成 6 份,–80℃ 低溫儲存,每天取低、中、高值各 1 份進行測定,共測定 6 天,計算日間精密度。
2.3.2 線性測試
依據 CLSI EP6-A 文件[33]的線性評估方法,使用 HbA1c 低值樣本(4.3%)和高值樣本(15.6%)各 1 份,按 10/0、8/2、6/4、4/6、2/8、0/10 進行稀釋混合得到 6 個不同濃度(4.3%、6.56%、8.82%、11.08%、13.34%、15.6%),各濃度在本系統上測定 3 次,取平均值,以樣本實際測定結果的平均值為自變量,以稀釋比例為因變量作線性回歸,計算 R2 值,并進行線性分析。
2.3.3 準確度
分別用正常參考物質、異常參考物質(IFCC 糖化血紅蛋白參考方法或標準品的標準物質)進行平行測定 3 次,計算標準品測定結果均值(x),根據公式(1)計算測量結果的相對偏差(B)。
用參考物質作為樣本進行檢測,分析儀測定結果的相對偏差應在±8% 區間內。
 |
式中:B 為相對偏差,x 為 3 次測定結果的均值,T 為標準品的標示濃度。
2.3.4 與對比儀器的糖化血紅蛋白線性相關性測試
依據 CLSI EP9-A3 文件[34]的可比性評估方法,以日本東曹 G8 系統和美國伯樂Ⅶ系統為對比儀器。選取 30 例正常樣本和糖尿病樣本,樣本 HbA1c 濃度覆蓋高、中、低濃度,在測定范圍內盡量平均分布,分別采用本系統和日本東曹 G8 系統、美國伯樂Ⅶ系統檢測樣本的 HbA1c 測定 3 次,取平均值,以本系統測定的平均值為自變量,以日本東曹 G8 系統和美國伯樂Ⅶ系統測定的平均值分別為因變量作兩次線性回歸,計算 R2 值,并進行線性分析。
2.3.5 與對比儀器的地中海貧血因子 HbF/HbA2 線性相關性測試
以美國伯樂 D10 系統為對比儀器。選取 30 例 EDTA-K2 抗凝的新鮮靜脈血樣本,樣本已確認存在 α-和 β-地中海貧血,分成 2 份,采用本系統和美國伯樂 D10 系統分別檢測樣本的 HbF 和 HbA2 值,每個樣本測定 3 次,取平均值。以本系統測定 HbF 或 HbA2 的平均值為自變量,以美國伯樂 D10 測定 HbF 或 HbA2 的平均值為因變量作次線性回歸,計算 R2 值。
2.3.6 血紅蛋白變異體色譜測試
選取已確認存在 HbE、HbD、HbS 和 HbC 變異體的 EDTA-K2 抗凝的新鮮靜脈血樣本各 5 份,采用本系統進行樣本檢測,得到色譜圖,進行色譜分析。
2.3.7 抗變異體干擾試驗
對 IFCC 的血紅蛋白變異體(HbE、HbD、HbS 和 HbC)樣本進行平行測定 3 次,計算標準品測定結果均值,與樣本提供的靶值進行比較,并計算測量結果的相對偏差。
2.3.8 甘油三酯、膽紅素及葡萄糖干擾試驗
根據 CLSI 通過的 EP7-A2 文件《臨床化學干擾試驗批準指南》的要求,進行抗干擾實驗。血液中存在血紅蛋白和其他物質,包括膽紅素、葡萄糖、甘油三酯等,會對糖化血紅蛋白和地中海貧血的檢測存在干擾。選取正常樣本和糖尿病樣本的 2 份新鮮混合全血樣本,各分成 3 份,分別加入 0.6 g/L 膽紅素、10 g/L 葡萄糖、60 g/L 甘油三酯三種干擾物質,采用本系統進行 HbA1c 濃度檢測,每個樣本測定 3 次,取平均值。
2.3.9 統計學方法
采用 Excel 軟件對批內精密度、日間精密度、線性分析、相關性測試及干擾試驗結果進行統計。
3 實驗結果與分析
3.1 整體測試
本研究對該新型抗干擾高效液相色譜法血紅蛋白分析系統的性能,包括批內和日間精密度、線性進行測試,本系統表現出優異的穩定性、線性相關性和準確度。
3.1.1 批內和日間精密度及線性相關性
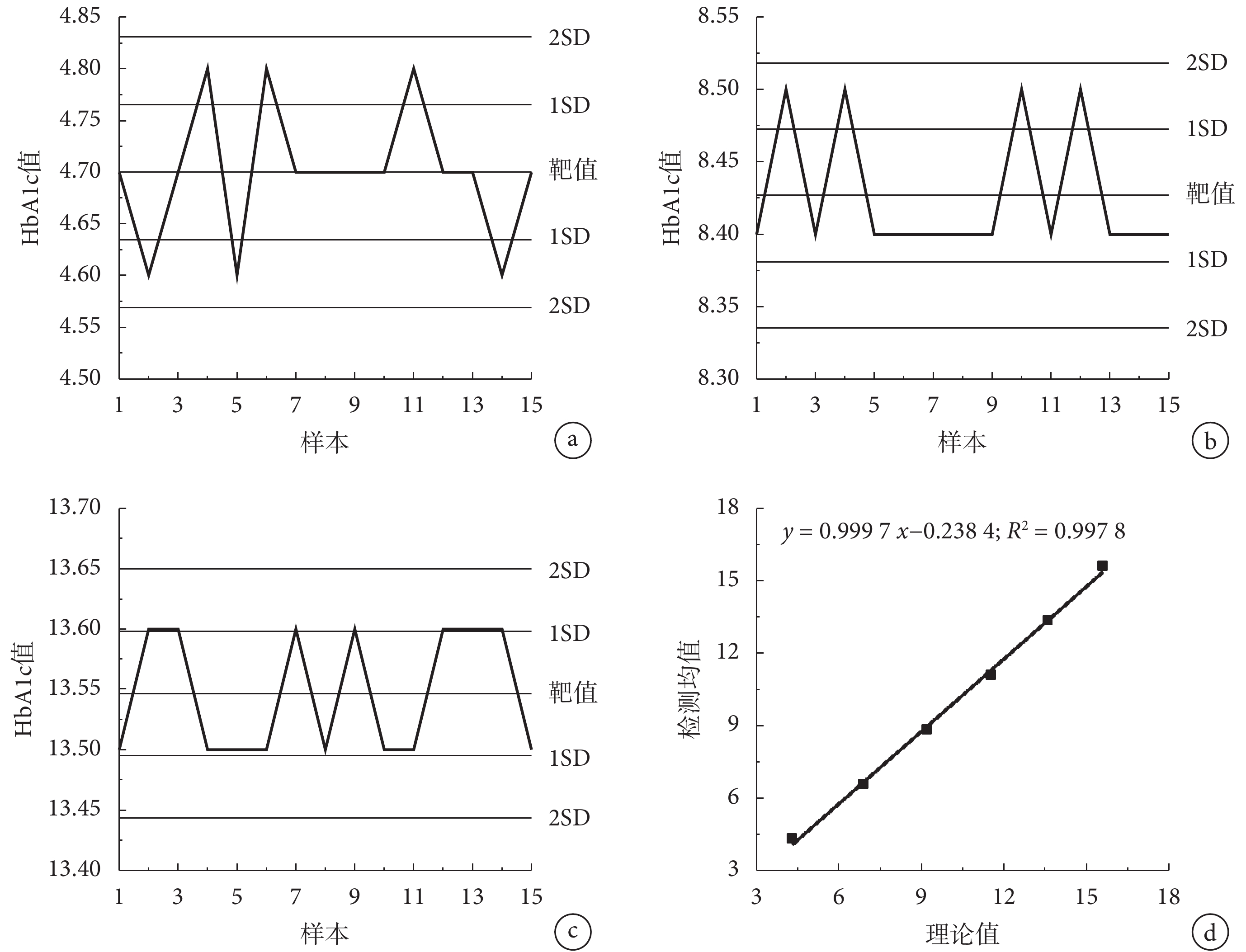
本文進行批內精密度和日間精密度測試,結果如表 1 所示,批內檢測時,所有樣本的 CV 值均<1.5%;日間檢測時,所有樣本的 CV 值均<2%,滿足我國衛生行業標準(WS/T 461—2015)的要求(室內 CV ≤ 3%,并盡量控制在 2% 內)。如圖 6a-c 所示,所有樣本的測試值均在 2SD 值內進行上下波動,批內差小,重復性能優良。采用本系統進行線性測試,線性范圍為 4.3%~15.6%,線性回歸方程為 y = 0.999 7 x ? 0.238 4,R2 = 0.997 8,如圖 6d 所示,線性相關性良好。
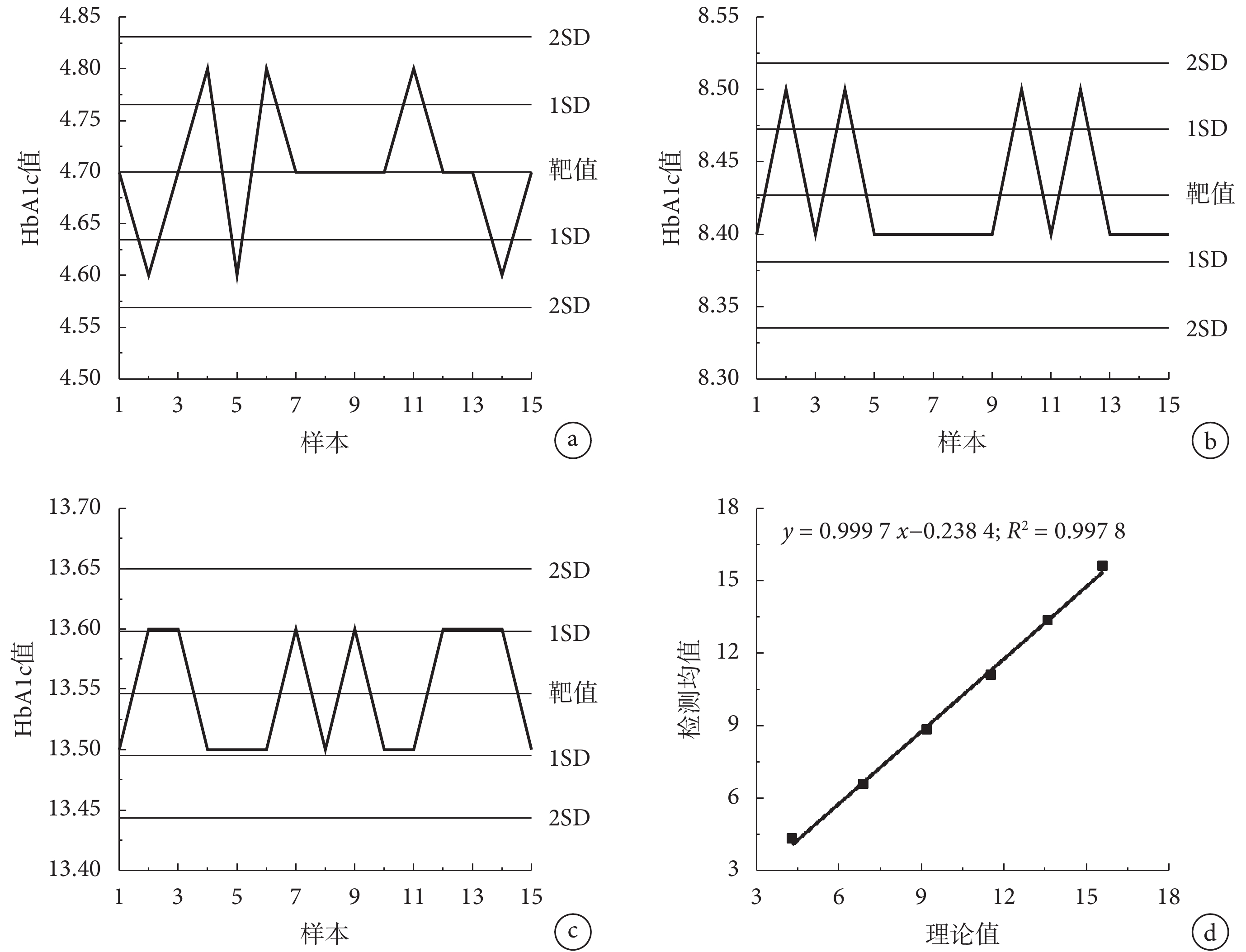 圖6
新型抗干擾高效液相色譜法血紅蛋白分析系統的性能測試圖
圖6
新型抗干擾高效液相色譜法血紅蛋白分析系統的性能測試圖
a-c.分別為 HbA1c 低、中、高值的重復性圖;d.為線性圖
Figure6. Performance graphs of the new anti-interference hemoglobin analysis system by HPLCa. the repeatability graph of low value of HbA1c; b. the repeatability graph of medium value of HbA1c; c. the repeatability graph of high value of HbA1c; d. the linear correlation graph of test values and theoretical values of HbA1c
3.1.2 準確度
儀器準確度檢測的參考指標:用參考物質作為樣本進行檢測,分析儀測定結果的相對偏差應在±8% 區間內(行標要求 8%,內部要求 6%)。
本文設計的新型抗干擾高效液相色譜法血紅蛋白分析系統分別對可溯源至 IFCC 的糖化血紅蛋白標準品的標準物質(Level 1、Level 3、Level 5、Level 7)進行檢測,平行測定 3 次,計算標準品測定結果均值(x)和相對偏差(B),如表 2 所示。結果表明儀器測試 IFCC 糖化血紅蛋白標準品的標準物質 Level 1、Level 3、Level 5、Level 7 的相對偏差分別為 1.80%、0.45%、0.83% 和–0.39%,遠遠低于行標和內部要求(行標要求 8%,內部要求 6%),實現了檢測結果的準確性,滿足檢測需求。
3.2 糖化血紅蛋白檢測分析模式
國產儀器以上海惠中生產的糖化血紅蛋白分析儀為主,其核心部件色譜柱中色譜填料微球為國外進口,且該進口的色譜柱填料微球的粒徑為 10 μm,儀器檢測速度為 160 s/樣本,重復性 CV ≤ 2%,只能進行 HbA1c 檢測。本文在進行糖化血紅蛋白分析時,將本系統設置為糖化血紅蛋白檢測分析模式,整個分離過程只需 130 s,可分離出 HbA1a、HbA1b、HbF、LA1c、HbA1c、HbA0 多個峰。本系統縮短了糖化血紅蛋白檢測時間,并與國際一流的糖化血紅蛋白分析儀相比,具有良好的線性相關性,性能優良。
3.2.1 線性相關性分析
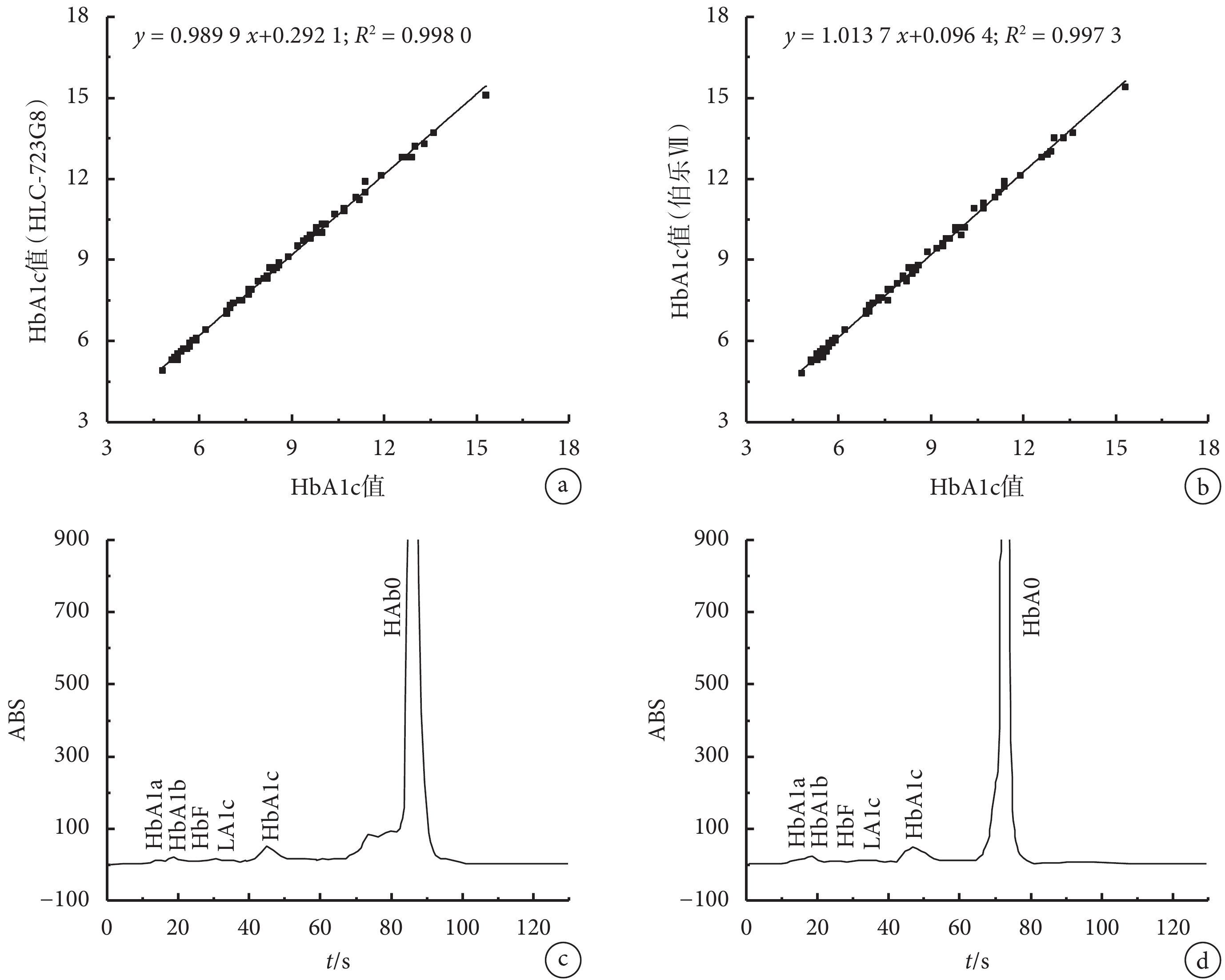
ADA 建議:HbA1c 含量 ≥ 6.5%,診斷為糖尿病;HbA1c 含量 ≥ 5.7%,診斷為糖尿病前期。糖化模式下不同血紅蛋白組分保留時間及范圍如表 3 所示。將本系統日本東曹 G8 和美國伯樂Ⅶ的糖化血紅蛋白分析系統進行 HbA1c 檢測值線性相關性研究,檢測結果如圖 7a-b 所示。本系統與日本東曹 G8 系統的 HbA1c 測量值的線性回歸方程為 y = 0.989 9 x + 0.292 1,R2 = 0.998 0;本系統與美國伯樂Ⅶ系統的 HbA1c 測量值的線性回歸方程為 y = 1.013 7 x + 0.096 4,R2 = 0.997 3。可見,本系統與日本東曹 G8 系統、美國伯樂Ⅶ系統 HbA1c 檢測的線性相關性均良好。
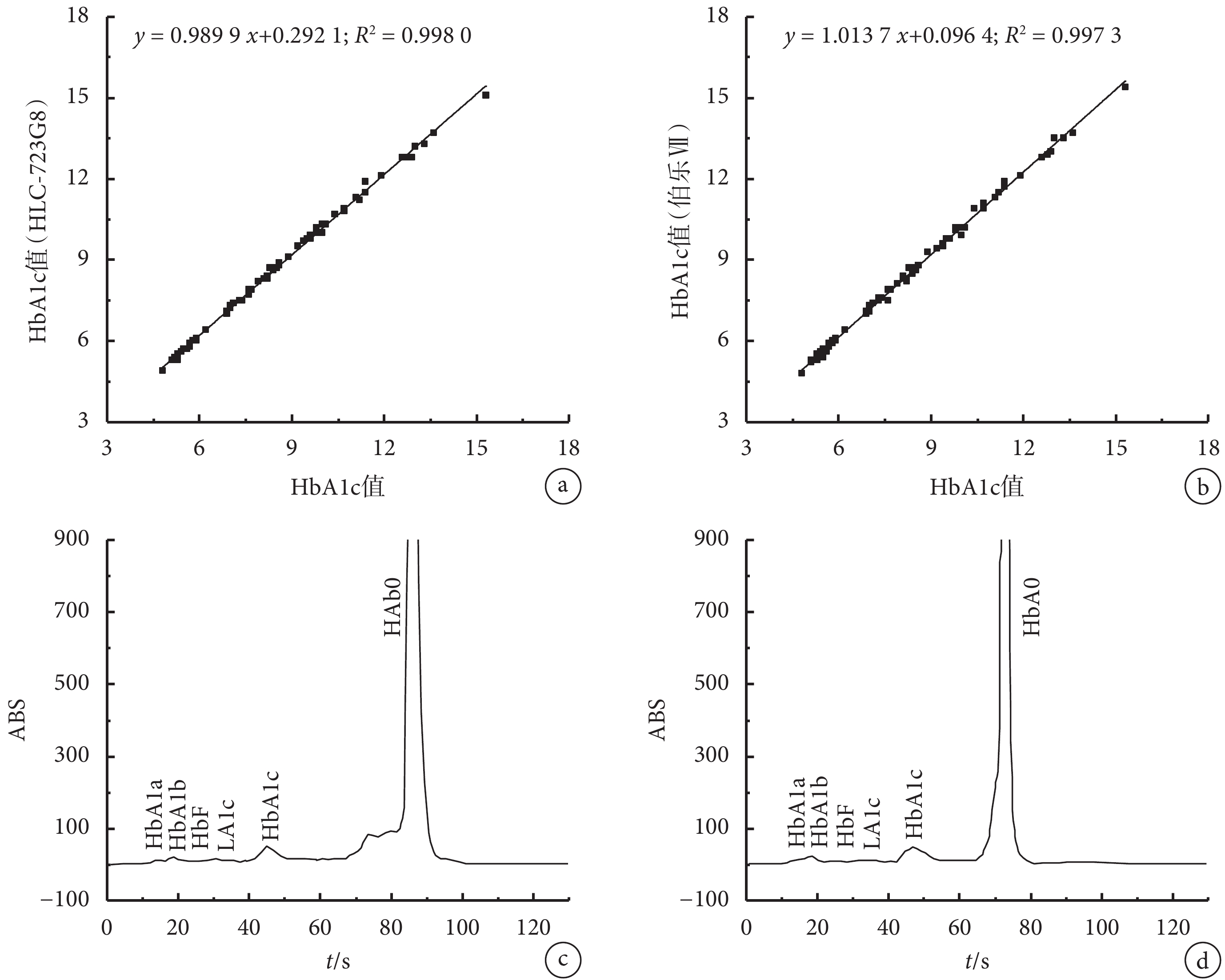 圖7
糖化血紅蛋白模式檢測結果
圖7
糖化血紅蛋白模式檢測結果
a.本系統和東曹 G8 系統的 HbA1c 檢測值比較圖;b.本系統與伯樂Ⅶ系統的 HbA1c 檢測值比較圖;c.正常標本的檢測圖譜,HbA1c 值為 4.9%;d.糖尿病樣本的檢測圖譜,HbA1c 值為 6.5%
Figure7. Detection results under glycated hemoglobin analysis modea. linear graph of HbA1c test values of the system compared with Tosoh G8 system; b. linear graph of HbA1c test values of the system compared with Bio-Rad Ⅶ system; c. the chromatogram of normal sample, and the value of HbA1c is 4.9%; d. the chromatogram of diabetes sample, and the value of HbA1c is 6.5%
3.2.2 色譜圖分析
本系統對正常樣本和糖尿病樣本的檢測譜圖如 7c-d 所示,兩種樣本的峰形光滑對稱無分叉,基線平整且無漂移,無明顯毛刺,各個峰識別正確。整個分離過程只需 130 s,可分離出 HbA1a、HbA1b、HbF、LA1c、HbA1c、HbA0 多個峰,大大縮短糖化血紅蛋白檢測時間。
3.3 地中海貧血檢測分析模式
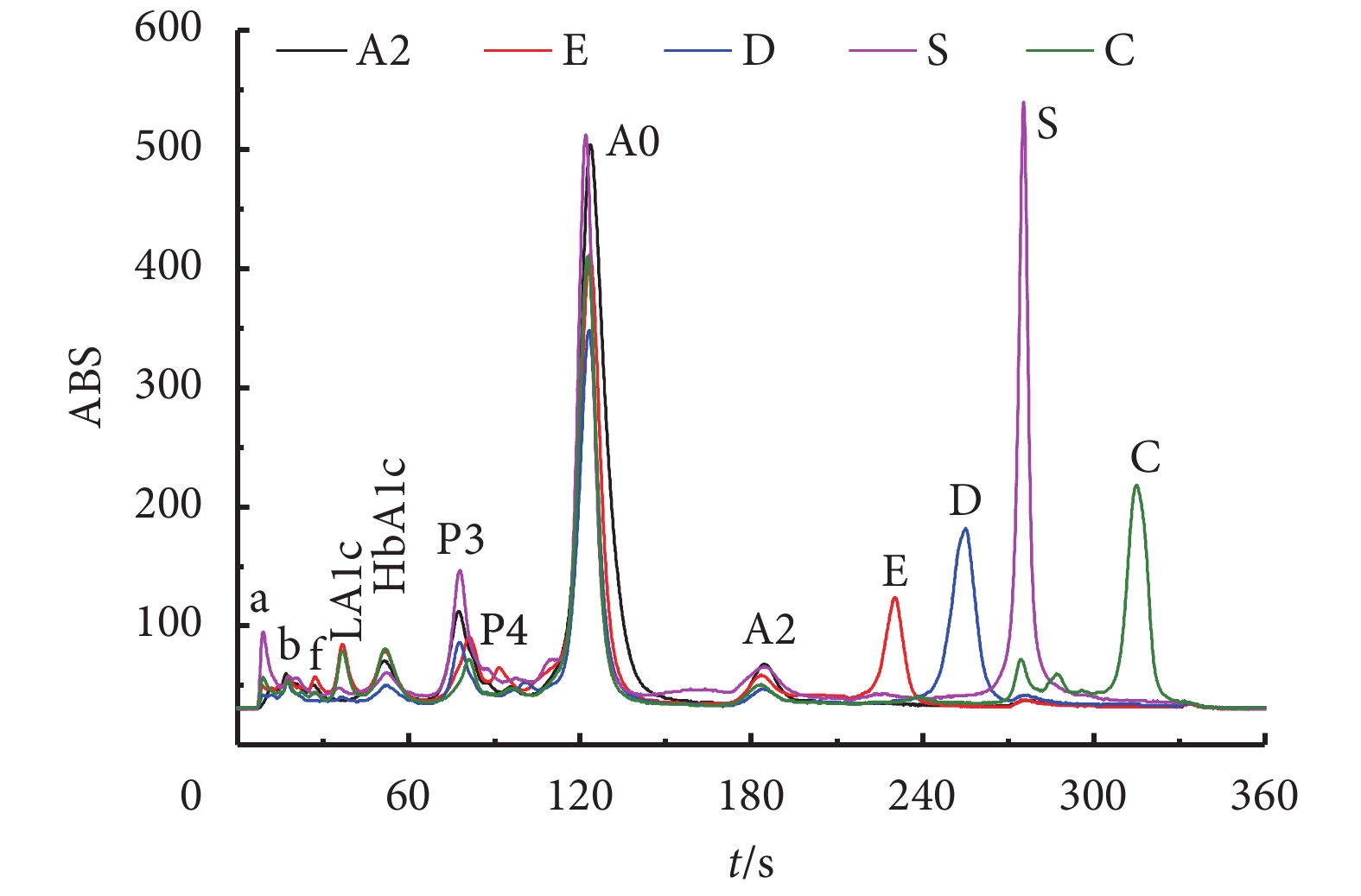
地中海貧血包括 α-地中海貧血和 β-地中海貧血。α-地中海貧血通常表現為 HbA2 含量降低。β-地中海貧血通常表現為 HbA2 和 HbF 含量升高。HbA2 的正常范圍為 2.5%~3.5%,HbF 的正常范圍為<1%。本系統利用不同種類的血紅蛋白對應不同保留時間這一基本原理,將儀器設置為地中海貧血檢測分析模式,在 360 s 內對血紅蛋白中的 HbA1a、HbA1b、HbF、LA1c、HbA1c、P3、P4、HbA0、HbA2 以及常見的 HbE/D/S/C 變異體進行分離,形成一系列的色譜峰,然后通過計算和比較每個峰的保留時間及峰面積,自動對應血紅蛋白的名稱及百分比含量。地中海貧血檢測分析模式下不同血紅蛋白組分保留時間如表 4 所示,色譜圖如圖 8 所示。在該模式下可以實現 HbA2 的分離,同時實現 HbA1c 和 HbF 的分離,并能出現血紅蛋白變異體 EDSC 的峰,實現糖化血紅蛋白、地中海貧血因子 HbF/HbA2 和血紅蛋白變異體的檢測。
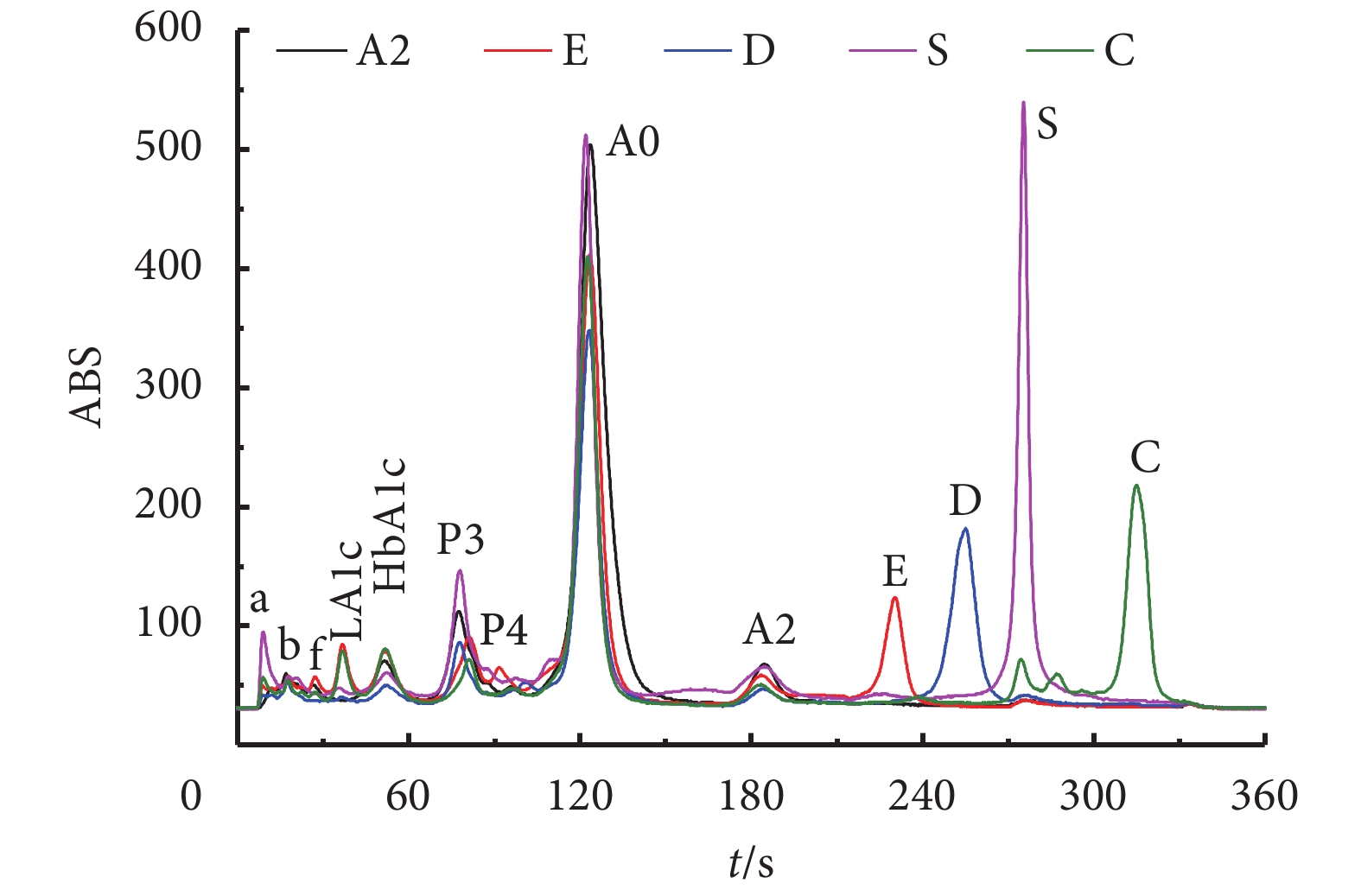 圖8
地中海貧血檢測分析模式下色譜圖
Figure8.
Chromatogram of the thalassemia analysis system by HPLC
圖8
地中海貧血檢測分析模式下色譜圖
Figure8.
Chromatogram of the thalassemia analysis system by HPLC
3.3.1 線性相關性分析
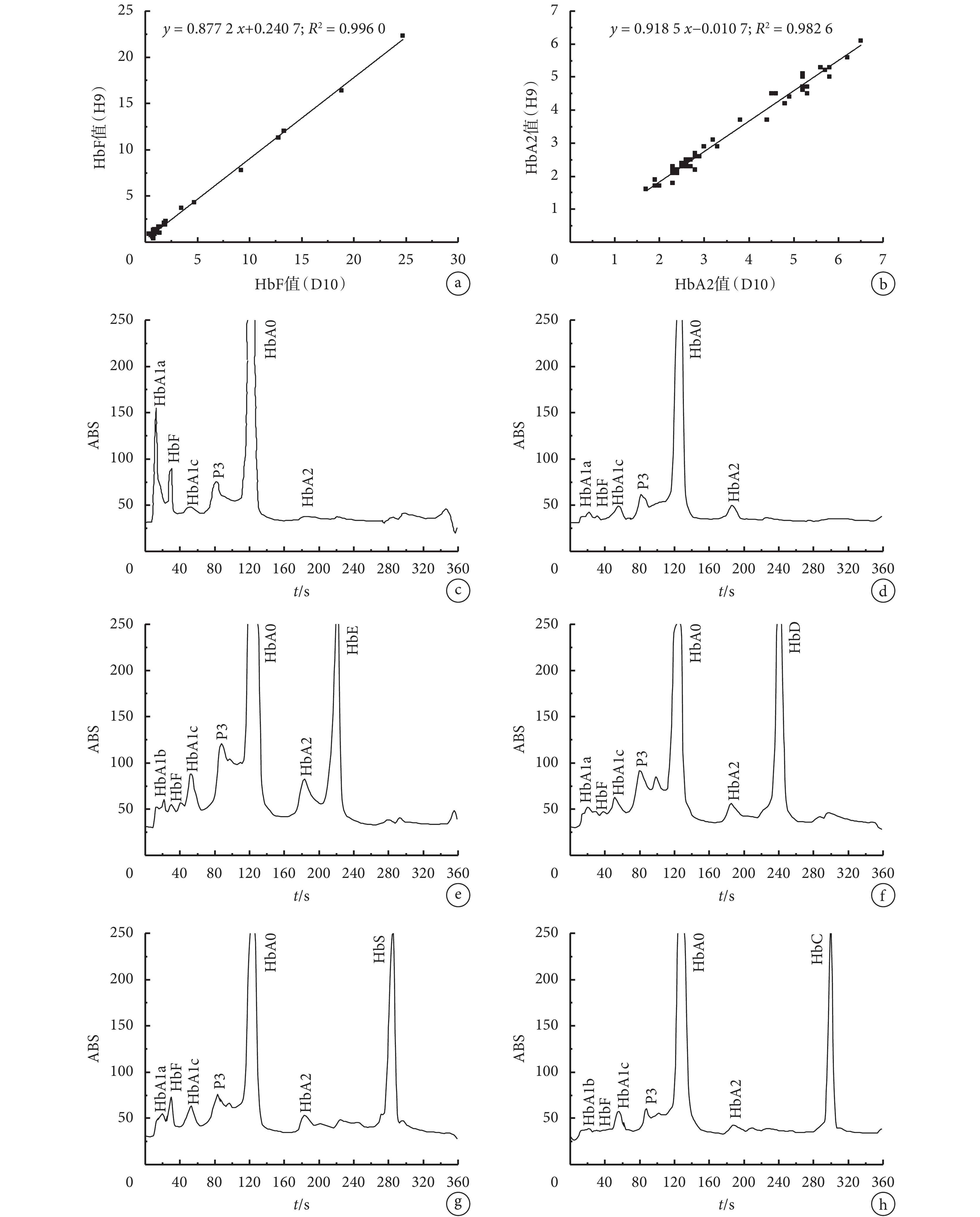
對于地中海貧血的診斷,主要是對 HbA2 和 HbF 測試值準確性的評判,本文將該系統與美國伯樂 D10 血紅蛋白分析系統進行 HbA2 和 HbF 測試值線性相關研究,如圖 9a-b 所示,本系統與美國伯樂 D10 系統的 HbF 測量值的相關性系數 R2 為 0.996 0,HbA2 測量值的相關性系數 R2 為 0.982 6,相關性均良好。因此,本系統在進行地中海貧血檢查時,具有高度準確性,性能達到國際先進水平。
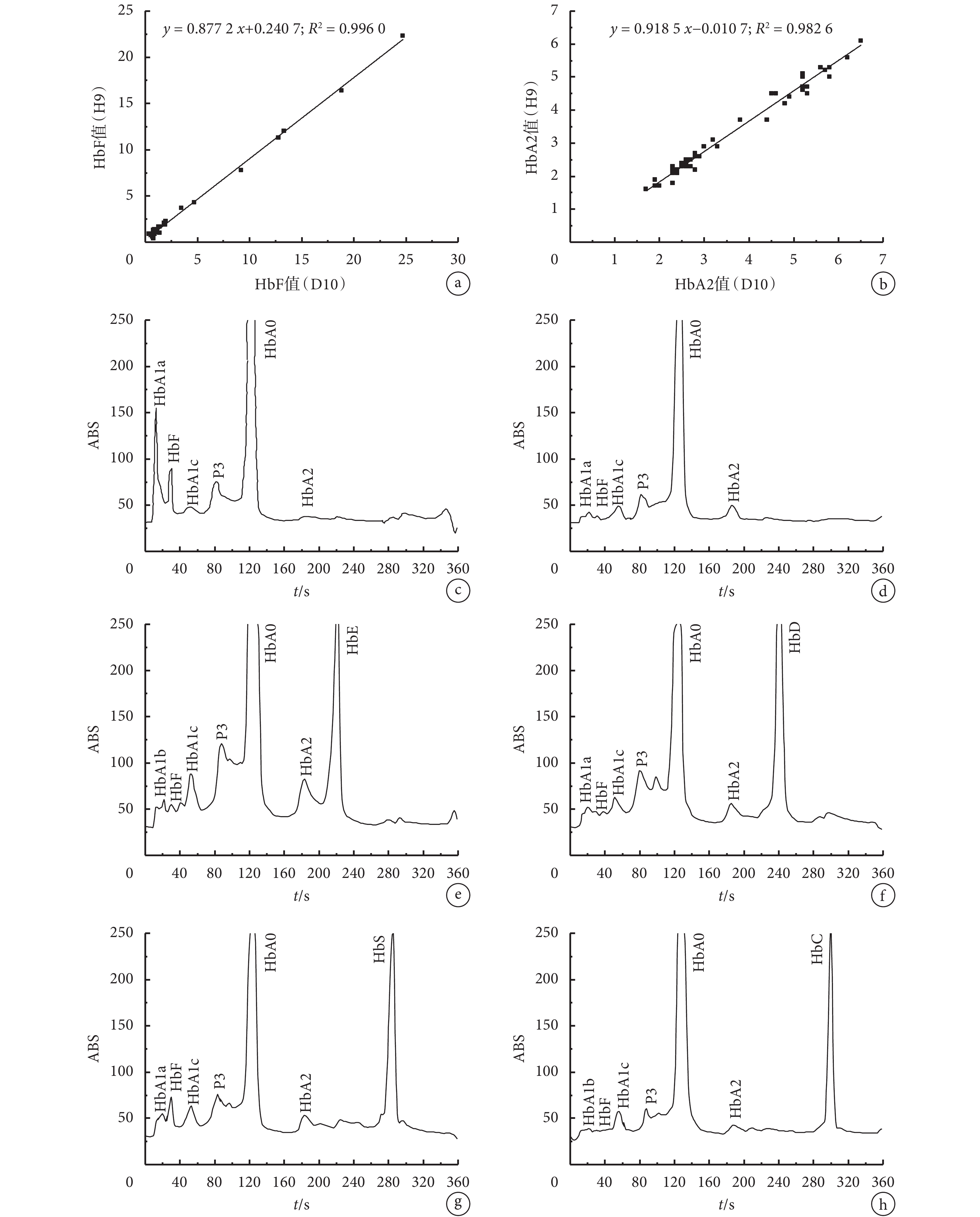 圖9
地中海貧血模式檢測結果
圖9
地中海貧血模式檢測結果
a.本系統和伯樂 D10 系統的 HbF 檢測值比較;b.本系統與伯樂 D10 系統的 HbA2 檢測值比較;c. α-地中海貧血 HbH/HbBart’s 的檢測圖譜;d. β-地中海貧血的檢測圖譜;e. HbE 變異體;f. HbD 變異體;g. HbS 變異體;h. HbC 變異體
Figure9. Detection result under thalassemia analysis modea. linear graph of HbF test values of the system compared with Bio-Rad D10 system; b. linear graph of HbA2 test values of the system compared with Bio-Rad D10 system; c. the chromatogram of α-thalassemia HbH/HbBart’s; d. the chromatogram of β-thalassemia; e. the chromatogram of HbE variant; f. the chromatogram of HbD variant; g. the chromatogram of HbS variant; h. the chromatogram of HbC variant
3.3.2 色譜圖分析
對 α-地中海貧血和 β-地中海貧血的血液樣本進行色譜表征,如圖 9c-d 所示。α-地中海貧血的色譜圖中 HbF 值明顯增高,如圖 9c 所示,達到 6.7%;HbA2 值明顯降低,達到 1.7%。β-地中海貧血的色譜圖中 HbA2 值明顯增高,如圖 9d 所示,達到 4.8%;HbF 達到 0.8%。與此同時,HbA1c 在圖譜中具有明顯的峰。因此,在此模式下,本系統可同時檢測出地中海貧血因子 HbF/HbA2 和糖化血紅蛋白(HbA1c)。
常見的 HbE、HbD、HbS 和 HbC 變異體檢測結果如圖 9e-h 所示,本系統可準確檢測出 HbE、HbD、HbS 和 HbC 變異體,在譜圖上出現非常明顯的強峰,同時 HbA1c 在圖譜中具有明顯的峰。因此,本系統可同時檢測出糖化血紅蛋白(HbA1c)、地中海貧血因子 HbF/HbA2 和血紅蛋白變異體 HbE/HbD/HbS/HbC。
3.4 抗干擾測試
為了驗證本系統能夠有效抵抗血液中其他物質的干擾對 HbA1c、HbF 和 HbA2 實現準確檢測,我們進行了抗變異體干擾和抗血液物質干擾測試。本系統表現了優異的抗干擾性。
3.4.1 抗變異體干擾試驗
對 IFCC 的血紅蛋白變異體(HbE/HbD/HbS/HbC)樣本進行檢測,將本系統檢測出的 HbA1c 值和靶值相比較,如表 5 所示,在存在變異體情況下,HbA1c 測試值和靶值的相對偏差均小于 ± 8%,表明該系統在血紅蛋白變異體存在的情況下,HbA1c 測試值具有準確性,同時表明該系統在進行 HbA1c 檢測時可以抵抗血紅蛋白變異體的干擾。
3.4.2 甘油三酯、膽紅素及葡萄糖干擾試驗
由于人體血液中除了血紅蛋白以外,還存在其他物質,包括膽紅素、葡萄糖、甘油三酯等,對糖化血紅蛋白和地中海貧血因子 HbF/HbA2 的檢測存在干擾。本研究分別將膽紅素、葡萄糖、甘油三酯作為干擾物質加入到正常血液和糖尿病血液樣本中,利用本系統檢測 HbA1c,如表 6 所示,HbA1c 的測試偏差均 < 2%,實現優異的抗干擾性能。
4 結論
本研究基于高效液相色譜分析原理,提出新型抗干擾高效液相色譜法血紅蛋白分析系統,包括:改進高壓三梯度洗脫法;優化高壓層析柱中微球粒徑和表面官能團,并增加篩板、優化篩板孔徑;優化雙柱塞往復式串聯高壓泵的結構和控制系統的算法,可快速實現 HbA1c、血紅蛋白變異體和地中海貧血因子 HbF/HbA2 的分離、檢測,實現抗干擾,性能穩定。本系統具有糖化血紅蛋白和地中海貧血兩種檢測模式。在糖化血紅蛋白檢測模式下,將本系統與日本東曹 G8 和美國伯樂Ⅶ糖化血紅蛋白分析系統等世界一線品牌產品進行 HbA1c 測試值的線性相關性研究,相關性很好。在地中海貧血檢測模式下,將本系統與美國伯樂 D10 血紅蛋白分析系統進行 HbF 和 HbA2 測試值的線性相關性研究,具有很好的相關性,在此模式下,本系統可檢測出 HbA1c 和血紅蛋白變異體 HbE/HbD/HbS/HbC。對本系統進行干擾性實驗發現,在血紅蛋白變異體存在的情況下,本系統檢測的 HbA1c 的偏差均 < 8%;在膽紅素、葡萄糖、甘油三酯干擾物存在的情況下,HbA1c 的測試偏差均 < 2%,抗干擾性良好。后續將加大測試樣本量,驗證系統的穩定性,實現真正的產業化。
利益沖突聲明:本文全體作者均聲明不存在利益沖突。
引言
糖尿病已成為一個嚴重影響人類生命健康的全球性公共衛生問題,我國的糖尿病流行形勢尤為嚴峻[1-2]。與此同時,全世界約有 3.4 億人攜帶有血紅蛋白變異體致病基因,血紅蛋白變異體已經成為全球前三位常見的出生缺陷[3-6]。血紅蛋白(hemoglobin,Hb)包括血紅蛋白 A(HbA)、血紅蛋白 F(HbF)和血紅蛋白 A2(HbA2),HbA 分為未被糖基化(hemoglobin A0,HbA0)和糖基化(hemoglobin A1,HbA1)兩種,其中 HbA1 包括糖化血紅蛋白 A1a(HbA1a)、糖化血紅蛋白 A1b(HbA1b)和糖化血紅蛋白 A1c(HbA1c)。
在糖尿病管理中,糖尿病的診斷和監控對于患者的生命健康尤為重要。2010 年美國糖尿病協會(American Diabetes Association,ADA)和歐洲糖尿病協會(European Association for the Study of Diabetes,EASD)相繼發表糖尿病診斷和治療指南,均正式提出 HbA1c 是糖尿病早期診斷的金指標,同時可作為病情檢測指標[7]。美國糖尿病協會建議:HbA1c 含量 ≥ 6.5%,診斷為糖尿病;HbA1c 含量 ≥ 5.7%,診斷為糖尿病前期[8-9]。對于糖尿病的檢測和監控,高效液相色譜法(high performance liquid chromatography,HPLC)是 HbA1c 檢測的金標準,糖尿病控制及并發癥研究(Diabetes Control and Complications Trial,DCCT)將 HPLC 作為糖尿病研究中使用的唯一方法,美國國家糖化血紅蛋白標準化計劃(National Glycohemoglobin Standardization Program,NGSP)將 HPLC 作為標準化中的參考方法[10-12]。HPLC 的檢測原理為在一定離子強度緩沖液中,不同血紅蛋白會不同程度地與色譜柱表面的離子原基結合,因此,需要將 HbA1c 與其他血紅蛋白(HbA1b、HbA1a 和 HbA0)分離后進行檢測[13-20]。
在地中海貧血和血紅蛋白變異體的篩查中,由于 α-地中海貧血患者的 HbA2 含量下降,β-地中海貧血患者的 HbA2 和 HbF 含量上升[21-23],而 HbA2、HbF 和 HbA 所帶電荷相近,采用液相色譜法進行 HbA1c 檢測時易受到血紅蛋白變異體的干擾而影響檢測結果的準確性[12, 24-26]。
探索能夠有效分離糖化血紅蛋白、地中海貧血因子 HbF/HbA2 和血紅蛋白變異體的檢測方法是目前血紅蛋白分析研究的熱點。有研究發現,通過優化高效液相色譜法的洗脫方式,可以提高分離效率,減少干擾[27-28]。研究證明,通過改進填料微球的粒徑,或對微球表面進行化學修飾,也可以提高樣本的分離效率[29-31]。
因此,本文提出一種新型抗干擾高效液相色譜法血紅蛋白分析系統,通過改進高壓三梯度洗脫法,優化高壓層析柱中微球和篩板結構,優化雙柱塞往復式串聯高壓泵的結構,可實現樣本中不同血紅蛋白的洗脫和檢測,與世界一線品牌產品進行 HbA1c、地中海貧血因子 HbF/HbA2 和血紅蛋白變異體檢測性能對比,完成關于血紅蛋白檢測性能的驗證。
1 新型抗干擾高效液相色譜法血紅蛋白分析系統
本新型抗干擾高效液相色譜法血紅蛋白分析系統(以下簡稱“本系統”)的核心組成包括改進的高壓三梯度洗脫法、優化的高壓層析柱、改良的雙柱塞往復式串聯高壓泵和紫外-可見光學檢測裝置,以及液路、硬件和軟件等部分。
本系統旨在實現不同血紅蛋白分子的檢測,檢測流程如圖 1 所示,三梯度洗脫液溶劑通過雙柱塞往復式串聯高壓泵的抽吸作用進入液路管道,通過系統控制六通閥,使溶劑流進高壓層析柱,與此同時待測樣本通過自動進樣器進入高壓層析柱中,此時高壓層析柱中的填料微球和樣本中不同血紅蛋白分子及洗脫液由于電荷作用發生不同程度的吸附,使各血紅蛋白分子發生分離,在不同時刻進入紫外-可見光學檢測裝置檢測,根據光吸收率的不同,檢測出不同血紅蛋白分子的含量,得到血紅蛋白分析色譜圖。
 圖1
新型抗干擾高效液相色譜法血紅蛋白分析系統檢測示意圖
Figure1.
Schematic diagram of the new anti-interference hemoglobin analysis system by HPLC
圖1
新型抗干擾高效液相色譜法血紅蛋白分析系統檢測示意圖
Figure1.
Schematic diagram of the new anti-interference hemoglobin analysis system by HPLC
峰值計算:采用了基于正態分布的高斯擬合算法,獲取原始色譜信號中色譜峰的起點坐標、終點坐標和峰值點坐標;根據起點坐標和終點坐標,從原始色譜信號中分離出相應色譜峰的色譜信號;根據與色譜峰對應的擬合函數對相應的色譜信號進行擬合,得到與色譜峰對應的擬合信號;擬合函數是基于峰值點坐標構建的函數;基于擬合信號計算色譜峰的峰面積。
1.1 改進的高壓三梯度洗脫法
改進的高壓三梯度洗脫法是本系統中的核心技術,本研究采用帶不同正離子濃度的 A、B、C 三種洗脫液,通過改進高壓三梯度洗脫法,控制流動相流經高壓層析柱的時間和順序,實現 HbA1c、HbF 和 HbA2 的有效分離。
洗脫液 A、B、C 均帶不同濃度的正離子,且正離子濃度依次增加。洗脫液 A 為(40±10)mmol/L 的丁二酸鹽水溶液,用于洗脫糖化血紅蛋白 HbA1a 和 HbA1b;洗脫液 B 為(100±10)mmol/L 的丁二酸鹽水溶液,用于洗脫糖化血紅蛋白 HbA1c;洗脫液 C 為(500±10)mmol/L 的丁二酸鹽水溶液,用于洗脫非糖化血紅蛋白 HbA0 及變異體。
本系統將洗脫液 A、B、C 流經層析柱的兩種不同時間和順序分成糖化血紅蛋白檢測模式和地中海貧血檢測模式。糖化血紅蛋白檢測模式:可進行糖化血紅蛋白檢測,控制洗脫液 A、B、C 流經層析柱的時間為 130 s,其中 0~65 s 用 A 液進行洗脫,65~85 s 用 B 液進行洗脫,85~105 s 用 C 液進行洗脫,105~130 s 用 A 液進行洗脫,如圖 2 所示,實現 HbA1a、HbA1b、HbF、不穩定的 HbA1c(labile HbA1c,LA1c)、HbA1c、HbA0 的分離。
 圖2
糖化血紅蛋白檢測模式下三種洗脫液的輸送時間
Figure2.
Delivery time of three eluents in glycosylated hemoglobin detection mode
圖2
糖化血紅蛋白檢測模式下三種洗脫液的輸送時間
Figure2.
Delivery time of three eluents in glycosylated hemoglobin detection mode
地中海貧血檢測模式:實現糖化血紅蛋白、血紅蛋白變異體和地中海貧血因子 HbF/HbA2 的分離、檢查,控制洗脫液 A、B、C 流經層析柱的時間為 360 s,其中 0~70 s 用 A 液進行洗脫,70~170 s 用 B 液進行洗脫,170~320 s 用 C 液進行洗脫,320~360 s 用 A 液進行洗脫,如圖 3 所示。將 HbA2 分離出來,還可分離 HbA1a、HbA1b、HbF、LA1c、HbA1c、HbA0,同時也會分離出變異血紅蛋白 EDSC(HbE/HbD/HbS/HbC)。
 圖3
地中海貧血檢測模式下三種洗脫液的輸送時間
Figure3.
Delivery time of three eluents in thalassemia detection mode
圖3
地中海貧血檢測模式下三種洗脫液的輸送時間
Figure3.
Delivery time of three eluents in thalassemia detection mode
1.2 優化的高壓層析柱
高壓層析柱是整個高效液相色譜系統的心臟,層析柱離子交換填料微球是層析柱的核心材料,直接關系到檢測結果的精度。本系統優化了高壓層析柱中微球粒徑,通過改進單體結構,引入環氧基團,采用種子溶脹法成功制備出粒徑在 5~6 μm 且尺寸均一的聚苯乙烯填料微球,微球表面帶有大量帶負電的功能基團,如圖 4 所示。帶負電填料微球和 HbA1a、HbA1b、HbA1c、HbA0、HbF、HbA2 發生吸附作用,其中 HbA0 吸附作用最強,HbA1c、HbA1b 和 HbA1a 依次減弱。待測樣本通過自動進樣器進入層析柱中,與此同時三梯度洗脫液溶劑通過雙柱塞往復式串聯高壓泵的抽吸作用進入液路管道,通過系統控制六通閥,使溶劑流進高壓層析柱,其中流動相 A 首先進入層析柱中,其次是流動相 B、流動相 C,最后流動相 A 進入層析柱中進行洗滌。同時本系統通過增加篩板,優化篩板孔徑,可有效過濾掉樣本中殘留的絮狀物,延長使用壽命。本系統高壓層析柱的規格為 4.6 mm×30 mm,實現耐壓至少 20 MPa。
 圖4
層析柱微球的 SEM 圖
Figure4.
SEM images of column microspheres
圖4
層析柱微球的 SEM 圖
Figure4.
SEM images of column microspheres
本研究提供一種液相色譜用弱陽離子交換填料,首先采用帶有環氧基團的乙烯基單體和二乙烯基苯交聯劑合成表面具有環氧基的聚甲基丙烯酸縮水甘油醚-二乙烯基苯基質無孔微球,對環氧基進行水解處理,再接枝一層含多環氧基的縮水甘油醚,使微球表面帶有多活性環氧基官能團,最后在親水化涂層表面帶有多活性環氧基官能團基礎上,采用可逆加成-斷裂鏈轉移聚合技術在基質表面引入含羧基、磺酸基或氨基等官能團,并通過調節聚合過程中單體和鏈轉移試劑的比例來控制官能團的長度結構和密度,最終得到官能團結構和密度均可控的高性能離子交換色譜介質,具有更優良的離子交換性能。實現填料的粒徑為 5~6 μm,無孔,對微球進行離子交換容量(IEC)檢測,通過對洗滌過填料微球的 NaOH 溶液和氯化鈉溶液混合液進行滴定,得到干燥微球的離子交換容量為 25 mmol/L。
1.3 改良的雙柱塞往復式串聯泵
高壓泵是實現壓力的關鍵,本系統對雙柱塞往復式串聯泵的結構進行優化,采用兩個泵,并將其處于同一水平位置,通過優化控制系統的算法,控制兩個泵中柱塞的運動,實現壓力的穩定和流速的恒定,提高檢測結果的準確性;通過改進柱塞桿和單向閥的使用材料,提高該高壓泵的承受壓力和使用壽命,可承受 40 MPa 的壓力,往復壽命高達 400 萬次。
改良的雙柱塞往復式串聯泵工作原理:先在伺服系統中對柱塞Ⅰ和柱塞Ⅱ的運動最低點、最高點和恒定點進行設置,控制柱塞Ⅰ和柱塞Ⅱ移動到恒定點,如圖 5 所示。當系統控制伺服電機正向偏轉時,使泵Ⅰ中裝有最大體積的流動相;然后控制伺服電機發生反向偏轉,使泵Ⅰ和泵Ⅱ中有相同體積的流動相,完成設置。
 圖5
雙柱塞往復式串聯泵示意圖
Figure5.
Diagram of double plunger reciprocating high pressure pump
圖5
雙柱塞往復式串聯泵示意圖
Figure5.
Diagram of double plunger reciprocating high pressure pump
在系統正式進行測試時。首先正向偏轉伺服電機,打開泵Ⅰ中的單向閥 1,控制向上移動泵Ⅰ中的柱塞Ⅰ從設置點移動到最高點;然后反向偏轉伺服電機,打開泵Ⅰ中的單向閥 2 和泵Ⅱ的單向閥 3,控制泵Ⅰ從最高點到達設置點,控制泵Ⅱ中的柱塞Ⅱ從設置點向上移動到最高點。打開單向閥 4,控制泵Ⅱ中的柱塞Ⅱ從最高點向上移動到設置點,把流動相送入了色譜系統,重復這些過程,每次運行周期中都只輸出泵中流動相的一半,實現了連續恒定的流量控制。
2 實驗部分
2.1 研究對象
正常樣本:選取 2019 年 9 月至 11 月成都第三人民醫院體檢健康者血液樣本,納入標準為測定無異常血紅蛋白、無嚴重肝腎疾病、無血液系統疾病、無糖尿病史。
糖尿病樣本:選取 2019 年 9 月至 11 月成都第三人民醫院確認存在糖尿病的患者血液樣本,納入標準為測定無異常血紅蛋白、無嚴重肝腎疾病、無血液系統疾病。
α-地中海貧血樣本:選取 2019 年 9 月至 11 月成都第三人民醫院確認存在 α-地中海貧血的患者血液樣本,納入標準為測定存在異常血紅蛋白、無嚴重肝腎疾病、無血液系統疾病、無糖尿病史。
β-地中海貧血樣本:選取 2019 年 9 月至 11 月成都第三人民醫院確認存在 β-地中海貧血的患者血液樣本,納入標準為測定存在異常血紅蛋白、無嚴重肝腎疾病、無血液系統疾病、無糖尿病史。
血紅蛋白變異體樣本:選取 2020 年 10 月購買的國際臨床化學和實驗室醫學聯盟(International Federation of Clinical Chemistry and laboratory medicine,IFCC)的血紅蛋白變異體(HbE/HbD/HbS/HbC)樣本。
樣品前處理過程:樣本采集使用乙二胺四乙酸二鉀(ethylene diamine tetraacetic acid-K2,EDTA-K2)抗凝的真空采血管,每個樣品分裝 300 μL,–80℃ 冷凍保存;樣本檢測前,將樣本從–80℃ 冰箱取出置于 2~8℃ 冰箱過夜復融。
2.2 儀器與試劑
本系統及相應的配套試劑、校準品、質控品;美國伯樂Ⅶ系統和 D10 系統及其相應的配套試劑、校準品、質控品;日本東曹 G8 系統及配套試劑、校準品、質控品。
2.3 方法學評估
2.3.1 批內和日間精密度
依據美國臨床實驗室標準化協會(Clinical and Laboratory Standards Institute,CLSI)EP5-A2 文件[32]的精密度評估方法,選取 HbA1c 低、中、高值各 15 份樣本,在 1 天內對這些樣本進行測試,計算批內精密度。選取 HbA1c 低、中、高值各 1 份樣本,每份樣本分成 6 份,–80℃ 低溫儲存,每天取低、中、高值各 1 份進行測定,共測定 6 天,計算日間精密度。
2.3.2 線性測試
依據 CLSI EP6-A 文件[33]的線性評估方法,使用 HbA1c 低值樣本(4.3%)和高值樣本(15.6%)各 1 份,按 10/0、8/2、6/4、4/6、2/8、0/10 進行稀釋混合得到 6 個不同濃度(4.3%、6.56%、8.82%、11.08%、13.34%、15.6%),各濃度在本系統上測定 3 次,取平均值,以樣本實際測定結果的平均值為自變量,以稀釋比例為因變量作線性回歸,計算 R2 值,并進行線性分析。
2.3.3 準確度
分別用正常參考物質、異常參考物質(IFCC 糖化血紅蛋白參考方法或標準品的標準物質)進行平行測定 3 次,計算標準品測定結果均值(x),根據公式(1)計算測量結果的相對偏差(B)。
用參考物質作為樣本進行檢測,分析儀測定結果的相對偏差應在±8% 區間內。
 |
式中:B 為相對偏差,x 為 3 次測定結果的均值,T 為標準品的標示濃度。
2.3.4 與對比儀器的糖化血紅蛋白線性相關性測試
依據 CLSI EP9-A3 文件[34]的可比性評估方法,以日本東曹 G8 系統和美國伯樂Ⅶ系統為對比儀器。選取 30 例正常樣本和糖尿病樣本,樣本 HbA1c 濃度覆蓋高、中、低濃度,在測定范圍內盡量平均分布,分別采用本系統和日本東曹 G8 系統、美國伯樂Ⅶ系統檢測樣本的 HbA1c 測定 3 次,取平均值,以本系統測定的平均值為自變量,以日本東曹 G8 系統和美國伯樂Ⅶ系統測定的平均值分別為因變量作兩次線性回歸,計算 R2 值,并進行線性分析。
2.3.5 與對比儀器的地中海貧血因子 HbF/HbA2 線性相關性測試
以美國伯樂 D10 系統為對比儀器。選取 30 例 EDTA-K2 抗凝的新鮮靜脈血樣本,樣本已確認存在 α-和 β-地中海貧血,分成 2 份,采用本系統和美國伯樂 D10 系統分別檢測樣本的 HbF 和 HbA2 值,每個樣本測定 3 次,取平均值。以本系統測定 HbF 或 HbA2 的平均值為自變量,以美國伯樂 D10 測定 HbF 或 HbA2 的平均值為因變量作次線性回歸,計算 R2 值。
2.3.6 血紅蛋白變異體色譜測試
選取已確認存在 HbE、HbD、HbS 和 HbC 變異體的 EDTA-K2 抗凝的新鮮靜脈血樣本各 5 份,采用本系統進行樣本檢測,得到色譜圖,進行色譜分析。
2.3.7 抗變異體干擾試驗
對 IFCC 的血紅蛋白變異體(HbE、HbD、HbS 和 HbC)樣本進行平行測定 3 次,計算標準品測定結果均值,與樣本提供的靶值進行比較,并計算測量結果的相對偏差。
2.3.8 甘油三酯、膽紅素及葡萄糖干擾試驗
根據 CLSI 通過的 EP7-A2 文件《臨床化學干擾試驗批準指南》的要求,進行抗干擾實驗。血液中存在血紅蛋白和其他物質,包括膽紅素、葡萄糖、甘油三酯等,會對糖化血紅蛋白和地中海貧血的檢測存在干擾。選取正常樣本和糖尿病樣本的 2 份新鮮混合全血樣本,各分成 3 份,分別加入 0.6 g/L 膽紅素、10 g/L 葡萄糖、60 g/L 甘油三酯三種干擾物質,采用本系統進行 HbA1c 濃度檢測,每個樣本測定 3 次,取平均值。
2.3.9 統計學方法
采用 Excel 軟件對批內精密度、日間精密度、線性分析、相關性測試及干擾試驗結果進行統計。
3 實驗結果與分析
3.1 整體測試
本研究對該新型抗干擾高效液相色譜法血紅蛋白分析系統的性能,包括批內和日間精密度、線性進行測試,本系統表現出優異的穩定性、線性相關性和準確度。
3.1.1 批內和日間精密度及線性相關性
本文進行批內精密度和日間精密度測試,結果如表 1 所示,批內檢測時,所有樣本的 CV 值均<1.5%;日間檢測時,所有樣本的 CV 值均<2%,滿足我國衛生行業標準(WS/T 461—2015)的要求(室內 CV ≤ 3%,并盡量控制在 2% 內)。如圖 6a-c 所示,所有樣本的測試值均在 2SD 值內進行上下波動,批內差小,重復性能優良。采用本系統進行線性測試,線性范圍為 4.3%~15.6%,線性回歸方程為 y = 0.999 7 x ? 0.238 4,R2 = 0.997 8,如圖 6d 所示,線性相關性良好。
 圖6
新型抗干擾高效液相色譜法血紅蛋白分析系統的性能測試圖
圖6
新型抗干擾高效液相色譜法血紅蛋白分析系統的性能測試圖
a-c.分別為 HbA1c 低、中、高值的重復性圖;d.為線性圖
Figure6. Performance graphs of the new anti-interference hemoglobin analysis system by HPLCa. the repeatability graph of low value of HbA1c; b. the repeatability graph of medium value of HbA1c; c. the repeatability graph of high value of HbA1c; d. the linear correlation graph of test values and theoretical values of HbA1c
3.1.2 準確度
儀器準確度檢測的參考指標:用參考物質作為樣本進行檢測,分析儀測定結果的相對偏差應在±8% 區間內(行標要求 8%,內部要求 6%)。
本文設計的新型抗干擾高效液相色譜法血紅蛋白分析系統分別對可溯源至 IFCC 的糖化血紅蛋白標準品的標準物質(Level 1、Level 3、Level 5、Level 7)進行檢測,平行測定 3 次,計算標準品測定結果均值(x)和相對偏差(B),如表 2 所示。結果表明儀器測試 IFCC 糖化血紅蛋白標準品的標準物質 Level 1、Level 3、Level 5、Level 7 的相對偏差分別為 1.80%、0.45%、0.83% 和–0.39%,遠遠低于行標和內部要求(行標要求 8%,內部要求 6%),實現了檢測結果的準確性,滿足檢測需求。
3.2 糖化血紅蛋白檢測分析模式
國產儀器以上海惠中生產的糖化血紅蛋白分析儀為主,其核心部件色譜柱中色譜填料微球為國外進口,且該進口的色譜柱填料微球的粒徑為 10 μm,儀器檢測速度為 160 s/樣本,重復性 CV ≤ 2%,只能進行 HbA1c 檢測。本文在進行糖化血紅蛋白分析時,將本系統設置為糖化血紅蛋白檢測分析模式,整個分離過程只需 130 s,可分離出 HbA1a、HbA1b、HbF、LA1c、HbA1c、HbA0 多個峰。本系統縮短了糖化血紅蛋白檢測時間,并與國際一流的糖化血紅蛋白分析儀相比,具有良好的線性相關性,性能優良。
3.2.1 線性相關性分析
ADA 建議:HbA1c 含量 ≥ 6.5%,診斷為糖尿病;HbA1c 含量 ≥ 5.7%,診斷為糖尿病前期。糖化模式下不同血紅蛋白組分保留時間及范圍如表 3 所示。將本系統日本東曹 G8 和美國伯樂Ⅶ的糖化血紅蛋白分析系統進行 HbA1c 檢測值線性相關性研究,檢測結果如圖 7a-b 所示。本系統與日本東曹 G8 系統的 HbA1c 測量值的線性回歸方程為 y = 0.989 9 x + 0.292 1,R2 = 0.998 0;本系統與美國伯樂Ⅶ系統的 HbA1c 測量值的線性回歸方程為 y = 1.013 7 x + 0.096 4,R2 = 0.997 3。可見,本系統與日本東曹 G8 系統、美國伯樂Ⅶ系統 HbA1c 檢測的線性相關性均良好。
 圖7
糖化血紅蛋白模式檢測結果
圖7
糖化血紅蛋白模式檢測結果
a.本系統和東曹 G8 系統的 HbA1c 檢測值比較圖;b.本系統與伯樂Ⅶ系統的 HbA1c 檢測值比較圖;c.正常標本的檢測圖譜,HbA1c 值為 4.9%;d.糖尿病樣本的檢測圖譜,HbA1c 值為 6.5%
Figure7. Detection results under glycated hemoglobin analysis modea. linear graph of HbA1c test values of the system compared with Tosoh G8 system; b. linear graph of HbA1c test values of the system compared with Bio-Rad Ⅶ system; c. the chromatogram of normal sample, and the value of HbA1c is 4.9%; d. the chromatogram of diabetes sample, and the value of HbA1c is 6.5%
3.2.2 色譜圖分析
本系統對正常樣本和糖尿病樣本的檢測譜圖如 7c-d 所示,兩種樣本的峰形光滑對稱無分叉,基線平整且無漂移,無明顯毛刺,各個峰識別正確。整個分離過程只需 130 s,可分離出 HbA1a、HbA1b、HbF、LA1c、HbA1c、HbA0 多個峰,大大縮短糖化血紅蛋白檢測時間。
3.3 地中海貧血檢測分析模式
地中海貧血包括 α-地中海貧血和 β-地中海貧血。α-地中海貧血通常表現為 HbA2 含量降低。β-地中海貧血通常表現為 HbA2 和 HbF 含量升高。HbA2 的正常范圍為 2.5%~3.5%,HbF 的正常范圍為<1%。本系統利用不同種類的血紅蛋白對應不同保留時間這一基本原理,將儀器設置為地中海貧血檢測分析模式,在 360 s 內對血紅蛋白中的 HbA1a、HbA1b、HbF、LA1c、HbA1c、P3、P4、HbA0、HbA2 以及常見的 HbE/D/S/C 變異體進行分離,形成一系列的色譜峰,然后通過計算和比較每個峰的保留時間及峰面積,自動對應血紅蛋白的名稱及百分比含量。地中海貧血檢測分析模式下不同血紅蛋白組分保留時間如表 4 所示,色譜圖如圖 8 所示。在該模式下可以實現 HbA2 的分離,同時實現 HbA1c 和 HbF 的分離,并能出現血紅蛋白變異體 EDSC 的峰,實現糖化血紅蛋白、地中海貧血因子 HbF/HbA2 和血紅蛋白變異體的檢測。
 圖8
地中海貧血檢測分析模式下色譜圖
Figure8.
Chromatogram of the thalassemia analysis system by HPLC
圖8
地中海貧血檢測分析模式下色譜圖
Figure8.
Chromatogram of the thalassemia analysis system by HPLC
3.3.1 線性相關性分析
對于地中海貧血的診斷,主要是對 HbA2 和 HbF 測試值準確性的評判,本文將該系統與美國伯樂 D10 血紅蛋白分析系統進行 HbA2 和 HbF 測試值線性相關研究,如圖 9a-b 所示,本系統與美國伯樂 D10 系統的 HbF 測量值的相關性系數 R2 為 0.996 0,HbA2 測量值的相關性系數 R2 為 0.982 6,相關性均良好。因此,本系統在進行地中海貧血檢查時,具有高度準確性,性能達到國際先進水平。
 圖9
地中海貧血模式檢測結果
圖9
地中海貧血模式檢測結果
a.本系統和伯樂 D10 系統的 HbF 檢測值比較;b.本系統與伯樂 D10 系統的 HbA2 檢測值比較;c. α-地中海貧血 HbH/HbBart’s 的檢測圖譜;d. β-地中海貧血的檢測圖譜;e. HbE 變異體;f. HbD 變異體;g. HbS 變異體;h. HbC 變異體
Figure9. Detection result under thalassemia analysis modea. linear graph of HbF test values of the system compared with Bio-Rad D10 system; b. linear graph of HbA2 test values of the system compared with Bio-Rad D10 system; c. the chromatogram of α-thalassemia HbH/HbBart’s; d. the chromatogram of β-thalassemia; e. the chromatogram of HbE variant; f. the chromatogram of HbD variant; g. the chromatogram of HbS variant; h. the chromatogram of HbC variant
3.3.2 色譜圖分析
對 α-地中海貧血和 β-地中海貧血的血液樣本進行色譜表征,如圖 9c-d 所示。α-地中海貧血的色譜圖中 HbF 值明顯增高,如圖 9c 所示,達到 6.7%;HbA2 值明顯降低,達到 1.7%。β-地中海貧血的色譜圖中 HbA2 值明顯增高,如圖 9d 所示,達到 4.8%;HbF 達到 0.8%。與此同時,HbA1c 在圖譜中具有明顯的峰。因此,在此模式下,本系統可同時檢測出地中海貧血因子 HbF/HbA2 和糖化血紅蛋白(HbA1c)。
常見的 HbE、HbD、HbS 和 HbC 變異體檢測結果如圖 9e-h 所示,本系統可準確檢測出 HbE、HbD、HbS 和 HbC 變異體,在譜圖上出現非常明顯的強峰,同時 HbA1c 在圖譜中具有明顯的峰。因此,本系統可同時檢測出糖化血紅蛋白(HbA1c)、地中海貧血因子 HbF/HbA2 和血紅蛋白變異體 HbE/HbD/HbS/HbC。
3.4 抗干擾測試
為了驗證本系統能夠有效抵抗血液中其他物質的干擾對 HbA1c、HbF 和 HbA2 實現準確檢測,我們進行了抗變異體干擾和抗血液物質干擾測試。本系統表現了優異的抗干擾性。
3.4.1 抗變異體干擾試驗
對 IFCC 的血紅蛋白變異體(HbE/HbD/HbS/HbC)樣本進行檢測,將本系統檢測出的 HbA1c 值和靶值相比較,如表 5 所示,在存在變異體情況下,HbA1c 測試值和靶值的相對偏差均小于 ± 8%,表明該系統在血紅蛋白變異體存在的情況下,HbA1c 測試值具有準確性,同時表明該系統在進行 HbA1c 檢測時可以抵抗血紅蛋白變異體的干擾。
3.4.2 甘油三酯、膽紅素及葡萄糖干擾試驗
由于人體血液中除了血紅蛋白以外,還存在其他物質,包括膽紅素、葡萄糖、甘油三酯等,對糖化血紅蛋白和地中海貧血因子 HbF/HbA2 的檢測存在干擾。本研究分別將膽紅素、葡萄糖、甘油三酯作為干擾物質加入到正常血液和糖尿病血液樣本中,利用本系統檢測 HbA1c,如表 6 所示,HbA1c 的測試偏差均 < 2%,實現優異的抗干擾性能。
4 結論
本研究基于高效液相色譜分析原理,提出新型抗干擾高效液相色譜法血紅蛋白分析系統,包括:改進高壓三梯度洗脫法;優化高壓層析柱中微球粒徑和表面官能團,并增加篩板、優化篩板孔徑;優化雙柱塞往復式串聯高壓泵的結構和控制系統的算法,可快速實現 HbA1c、血紅蛋白變異體和地中海貧血因子 HbF/HbA2 的分離、檢測,實現抗干擾,性能穩定。本系統具有糖化血紅蛋白和地中海貧血兩種檢測模式。在糖化血紅蛋白檢測模式下,將本系統與日本東曹 G8 和美國伯樂Ⅶ糖化血紅蛋白分析系統等世界一線品牌產品進行 HbA1c 測試值的線性相關性研究,相關性很好。在地中海貧血檢測模式下,將本系統與美國伯樂 D10 血紅蛋白分析系統進行 HbF 和 HbA2 測試值的線性相關性研究,具有很好的相關性,在此模式下,本系統可檢測出 HbA1c 和血紅蛋白變異體 HbE/HbD/HbS/HbC。對本系統進行干擾性實驗發現,在血紅蛋白變異體存在的情況下,本系統檢測的 HbA1c 的偏差均 < 8%;在膽紅素、葡萄糖、甘油三酯干擾物存在的情況下,HbA1c 的測試偏差均 < 2%,抗干擾性良好。后續將加大測試樣本量,驗證系統的穩定性,實現真正的產業化。
利益沖突聲明:本文全體作者均聲明不存在利益沖突。