無針注射技術是一種利用高速微射流將藥液遞送進皮下指定部位的新型給藥手段。盡管目前無針注射技術已在多個領域得到應用,但針對其藥液擴散機制和注射性能的研究仍存在一定的不足。本研究旨在確定無針注射過程中的關鍵參數,并描述其對注射效果的影響。本文通過小鼠實驗的方法,比較了不同注射條件下無針注射器的注射完成率和注射性能。結果表明,相比于其它注射參數,噴嘴直徑對射流性能的影響更為明顯。此外,注射完成率隨噴嘴直徑增大而增加,當噴嘴直徑為0.14 mm和0.25 mm時,注射完成率分別為89.7%和95.8%。進而,通過對小鼠血糖變化率的分析發現,采用無針注射的方式進行胰島素給藥可以獲得超過120 min的藥效持續時間,優于傳統針頭注射方式。綜上,本文所得結論可為氣動無針注射器的優化設計和拓展應用提供重要參考依據。
版權信息: ?四川大學華西醫院華西期刊社《生物醫學工程學雜志》版權所有,未經授權不得轉載、改編
0 引言
通過針頭進行藥物的皮下輸送是醫藥學領域常用的注射手段[1]。由于注射過程中極易導致疼痛感和交叉感染,以及針頭可能引起的恐懼問題,該注射方式的應用存在一定的限制[2-3]。無針注射技術于20世紀30年代問世[4-5],該技術利用高速微射流穿透皮膚組織,并將藥液輸送至皮下特定位置。在不使用針頭的情況下,該技術有效地解決了常規針頭注射給藥引起的各類弊端,并逐漸在疫苗接種和胰島素注射等場合得到應用[6-7]。
常見的無針注射系統通常由彈簧、壓縮氣體、電磁力和激光作為驅動[8-11]。其中,彈簧式無針注射器的體積小且便于攜帶,在市面上較為常見,但由于其注射動力不可調節且不具備連續注射功能,故應用范圍相對較窄。壓電式無針注射器通過電磁力和激光驅動,其優勢在于具備可控的驅動壓力和更精確的注射劑量調節,然而應用成本較高。氣動式無針注射器的結構合理、運行可靠、連續注射效率高、且驅動壓力可在大范圍內調節,展現出了良好的應用前景。在氣動式無針注射的過程中,受到壓縮氣體的作用,注射活塞移動并對注射腔內的流體加壓,使流體以高速微射流的形式自噴嘴噴出并完成注射。研究表明,當射流的滯止壓力高于15 MPa時[12-13],流體能夠穿透皮膚并在皮下組織中完成擴散。
近年來,胰島素的無針注射技術受到廣泛關注。國內外研究顯示,無針注射胰島素在提高患者的治療依從性和舒適度方面具有明顯優勢[14]。然而,目前針對胰島素無針注射器開展的系統性研究工作較少,相關的治療機制也尚未被完全揭示,限制了無針注射技術在胰島素注射方面的應用。目前,關于無針注射系統的研究主要集中于射流的流體動力學行為[15-16]以及穿透特性[17-18]。然而,對無針注射性能進行綜合評價還必須考慮注射完成后流體在皮下組織內的擴散模式、藥液的注射完成率等關鍵因素。以往研究中常采用聚丙烯酰胺凝膠代替人體組織以研究流體的擴散特性[19-20]。研究發現,射流在凝膠中的擴散行為呈現階段特性,且噴嘴的幾何參數對射流在凝膠中的擴散行為有著重要影響[21]。進一步的研究表明,射流在凝膠中的擴散特性并非由單一參數決定,而是受到噴嘴直徑、流體屬性和射流速度的共同影響。部分學者嘗試使用射流功率表征該特性[22],這有助于更全面地理解射流的擴散行為。盡管通過配比可使凝膠呈現出與人體組織相近的楊氏模量,但是基于凝膠介質獲得的結論仍然存在局限性。這是因為真實的皮膚組織具有更為復雜的孔隙結構和分層特性[23],因此使用在物理性質上與人體皮膚接近的實驗介質十分必要。此外,注射完成率是評估無針注射性能的重要指標,其一般定義為有效注射至皮下的藥劑量與設定注射劑量的比值[24-25]。受限于目前的技術手段,自噴嘴產生的射流在進入預定注射區域的過程中會發生損耗,如注射過程中偶爾出現藥液飛濺與回流、或是注射前期射流在穿透皮膚組織時因能量消耗而產生劑量損失等[26],這些現象均會導致實際注射完成率小于100%。因此,如何調節注射參數以獲得最佳注射完成率,并在此基礎上優化注射效果是無針注射技術研究中的重要內容。目前,對無針注射的注射完成率的研究鮮見報道。
基于以上分析,本文選取噴嘴直徑作為研究切入點,評估其在無針注射過程中發揮的作用,分析其對流體在組織內的擴散行為的影響,并研究其與無針注射過程中的注射完成率的關系。本文選擇小鼠為實驗對象,對比不同注射條件下胰島素對小鼠血糖的影響,并根據獲得的數據對無針注射的性能進行綜合評價,所得結論將有助于深入闡釋無針注射的作用機制,并為氣動無針注射器的優化設計和拓展應用提供重要參考依據。
1 實驗材料與方法
1.1 射流滯止壓力
本研究采用如圖1所示的實驗裝置采集射流的滯止壓力。該實驗裝置由高頻動態壓力傳感器(PCB113B27,PCB Piezotronics Inc.,美國)、數據采集系統(SCM05,LMS Co.,比利時)和數據處理計算機組成。實驗中采用的無針注射器是氣動式無針注射器(POK-H-I,江蘇鉑可醫療科技有限公司,中國)。在實驗過程中,通過夾具固定無針注射器,并確保射流方向垂直于傳感器表面。噴嘴出口和傳感器之間的間隙設置為1.0 mm,確保射流在到達傳感器表面時的速度與噴嘴出口處速度近似相等。當射流沖擊傳感器時,數據采集系統以20.4 kHz的速率采集壓力信號,通過軟件對獲得的壓力數據進行處理。
 圖1
射流壓力采集實驗裝置示意圖
Figure1.
Schematic view of experimental equipment for jet pressure measurement
圖1
射流壓力采集實驗裝置示意圖
Figure1.
Schematic view of experimental equipment for jet pressure measurement
1.2 小鼠實驗
本研究中選擇美國癌癥研究所(Institute of Cancer Research,ICR)培育的小鼠進行動物實驗。ICR小鼠由江蘇大學動物實驗中心提供,無特定病原體(specific pathogen free,SPF)級,7~8周齡,體重20~25 g,雌雄各半。所有小鼠實驗經江蘇大學倫理委員會批準,可用于科學研究(許可證號:SCXK2018-0012)。共選用32只小鼠,其中8只用于注射完成率和藥液擴散的研究,24只用于胰島素實驗和無針注射性能評估。實驗前使用10%水合氯醛溶液按照300 μL/100 g的劑量對小鼠進行全身麻醉,同時對待注射區域進行剃毛處理。
在注射完成率和藥液擴散實驗中,8只小鼠被隨機分為2組,每組4只,每只小鼠執行2次無針注射,選擇的注射部位為小鼠側后方大腿處,左右各注射一次。注射完畢后統計注射完成率,同時觀察皮丘狀態并記錄相關尺寸數據。
進行胰島素實驗前,測量所有小鼠的初始血糖值,并根據所得結果對小鼠進行排序;隨后按照血糖值梯度將24只小鼠分成6組,每組4只;最后從每組中隨機選擇1只小鼠,組成4個實驗組,每組共6只小鼠;這樣的分組方式可以盡可能地減小小鼠間個體差異引起的實驗誤差。此外,考慮到胰島素在實際應用中的每日總量一般為0.4~0.8 U/kg,因此具體分組方式如下:① 對照組:采用常規針頭腹腔注射的方式,注射生理鹽水(5 U/kg);② 胰島素針頭注射組:采用常規針頭腹腔注射的方式,注射0.1 U精蛋白重組人胰島素(1 U/mL);③ 胰島素0.14 mm無針注射組:采用噴嘴直徑(D)為0.14 mm的無針注射器,通過腹腔注射0.1 U精蛋白重組人胰島素(1 U/mL);④ 胰島素0.25 mm無針注射組:采用噴嘴直徑為0.25 mm的無針注射器,通過腹腔注射0.1 U精蛋白重組人胰島素(1 U/mL)。
2 結果與討論
2.1 壓力曲線
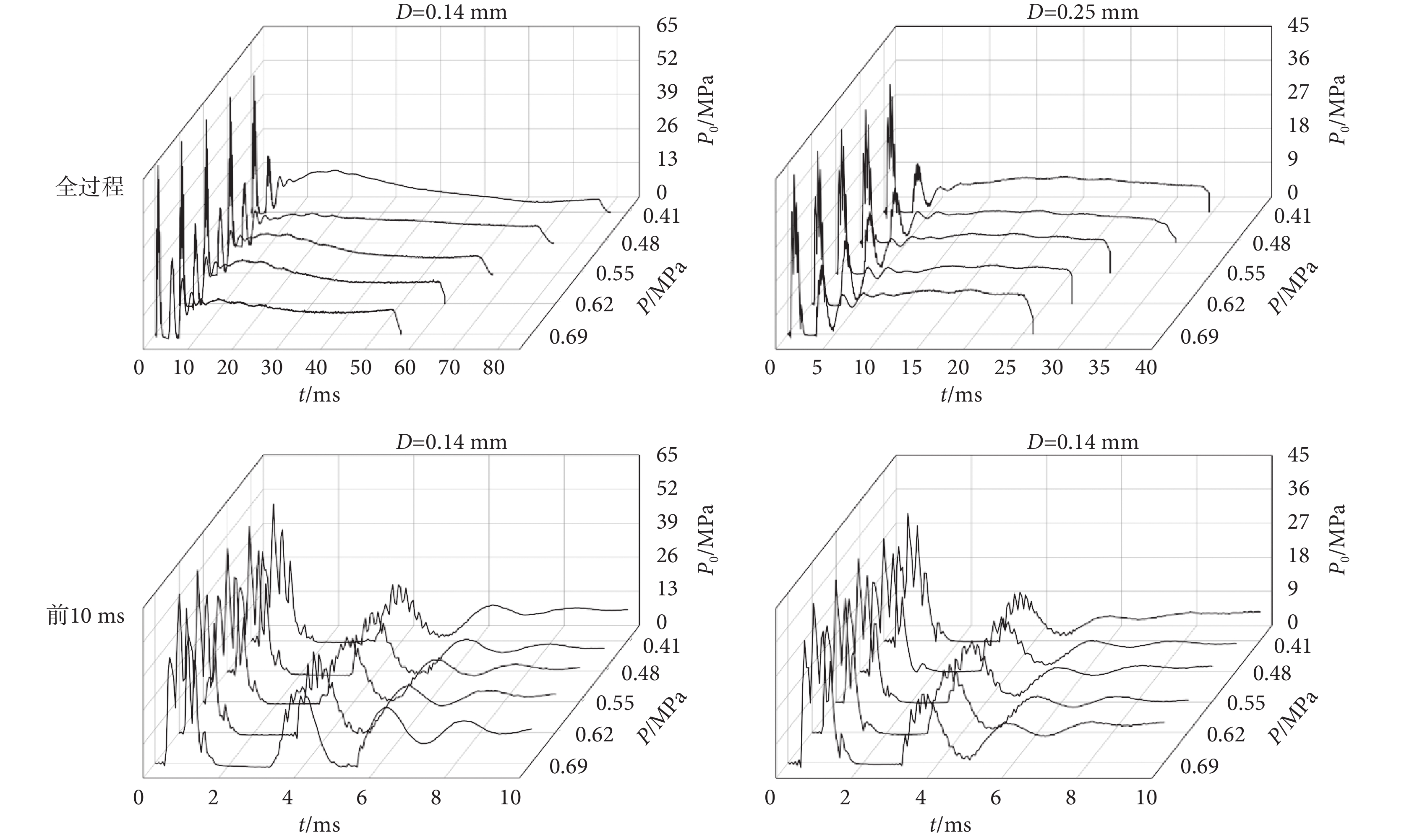
微射流的瞬態特性對于無針注射結果有著重要影響,通過沖擊實驗可以得到射流的滯止壓力(P0)隨噴射時間(t)變化的動態曲線。根據臨床應用的常用范圍,選取5種不同的驅動壓力(P),取值為0.41、0.48、0.55、0.62、0.69 MPa,對噴嘴直徑分別為0.14 mm和0.25 mm的無針注射系統進行研究,設定注射量(V)為0.1 mL。不同噴嘴直徑和驅動壓力條件下,無針注射器射流滯止壓力曲線的變化特征如圖2所示。
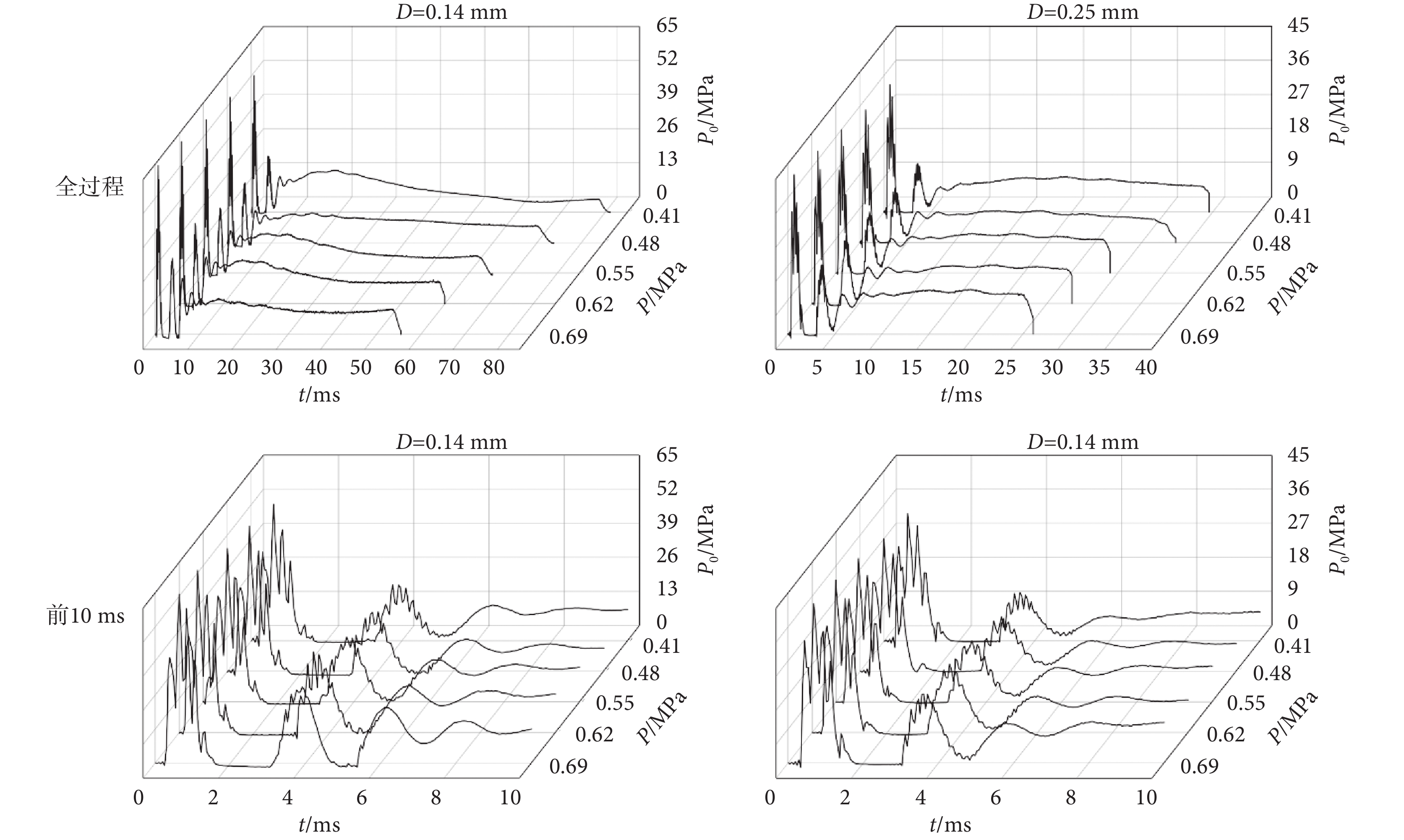 圖2
不同注射參數對應的射流滯止壓力隨時間的變化
Figure2.
Time-dependent stagnation pressure of jet at different injection parameters
圖2
不同注射參數對應的射流滯止壓力隨時間的變化
Figure2.
Time-dependent stagnation pressure of jet at different injection parameters
從圖2中可以看出,射流的最大峰值滯止壓力出現在t=0.8 ms處,隨后壓力急劇下降。在整個注射過程的前10 ms內,射流的滯止壓力劇烈震蕩。而在此之后,射流的滯止壓力逐漸趨于平穩并一直持續至整個注射過程結束。從能量轉換的角度來看,當活塞以較高的初速度撞擊流體時,會受到來自流體的阻力,導致活塞速度下降,注射腔內液體壓力升高。此時,在注射腔內外壓差的驅動下,液體自噴嘴中排出,并產生第一個壓力峰值。隨著注射腔內壓力釋放,作用在活塞上的液體阻力逐漸減小,活塞被壓縮空氣再次加速,并推動剩余流體排出注射腔,在t=3.6 ms時形成了第二個峰值壓力。然而,由于活塞動能減少,液體射流的峰值壓力和速度均下降。因此,隨著上述過程的重復,滯止壓力曲線不斷波動,并最終趨于穩定。總體來看,噴嘴直徑和驅動壓力的增加往往伴隨著射流滯止壓力和持續時間的變化。如圖2所示,選取驅動壓力為0.55 MPa的工況進行分析,當噴嘴直徑從0.14 mm增加至0.25 mm時,射流的峰值滯止壓力從58.6 MPa降低至37.9 MPa,持續時間從 65.3 ms縮短至29.2 ms,變化率分別為35.3和55.3%。而當噴嘴直徑為0.14 mm時,隨著驅動壓力從0.41 MPa增加至0.69 MPa,射流的峰值滯止壓力從52.1 MPa增加至64.4 MPa,持續時間從80.9 ms縮短至55.5 ms,變化率分別為23.6%和31.4%。因此,噴嘴直徑的改變對無針注射器射流特性的影響更為明顯。
2.2 注射完成率
藥液的注射完成率為另一個評價無針注射效果的重要指標。注射完成率表征實際進入至目標區域且能發揮作用的有效注射量與設定注射量的比值,如式(1)所示:
 |
式中, 代表注射完成率,
代表注射完成率, 代表有效注射量,
代表有效注射量, 代表設定注射量。
代表設定注射量。
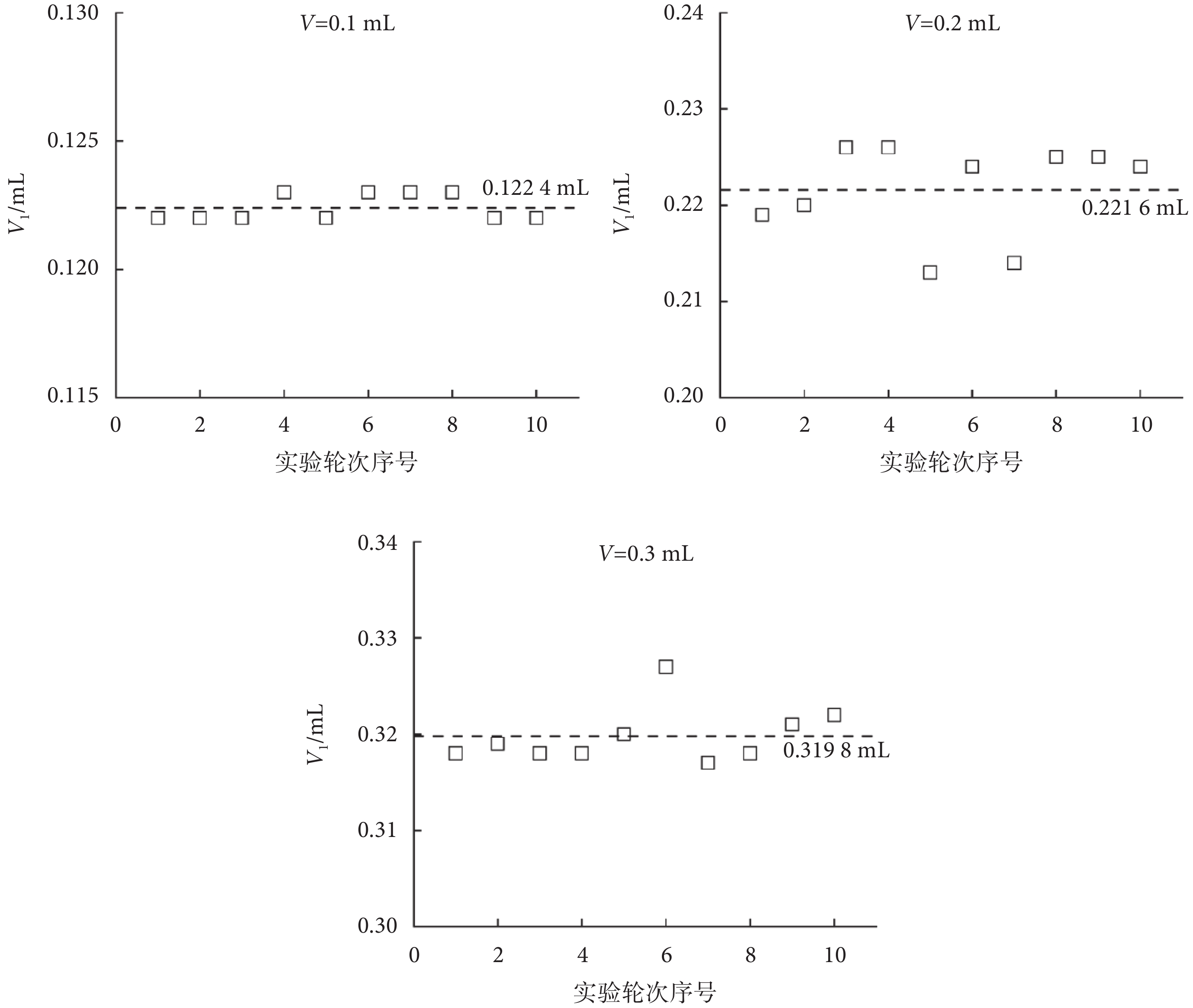
受注射過程中可能發生的藥液殘留或飛濺等因素的影響,實際注射完成率一般無法達到100%,因此在滿足射流滯止壓力可以穿透皮膚的前提下,提高給藥劑量的準確性和穩定性,是提高無針注射效率和改善注射效果的重要途徑。在給定噴嘴直徑和注射量的條件下,本文測量了無針注射器通過噴嘴排出的實際注射量(V1)。采用直徑為0.25 mm的噴嘴,驅動壓力固定為0.55 MPa,設定注射量分別為0.1、0.2、0.3 mL,使用醫用離心管對無針注射器單次注射的藥液進行收集并稱重,每組實驗重復10次,所得結果如圖3所示。可以看出,當設定注射量在0.1~0.3 mL范圍時,無針注射器平均單次排出的藥液體積分別為0.122 4、0.221 6、0.319 8 mL,即在所有工況下無針注射器的實際注射量均大于設定注射量。值得注意的是,盡管設定注射量的變化范圍較大,但不同實驗組的絕對誤差均趨近于0.02 mL,因此注射量的設定值和實際值之間的偏差取決于無針注射器的結構及驅動機制。考慮到藥液自無針注射器中排出到進入皮膚組織這一過程中還會存在藥液損耗[27],故最終的注射完成率還需進一步分析。
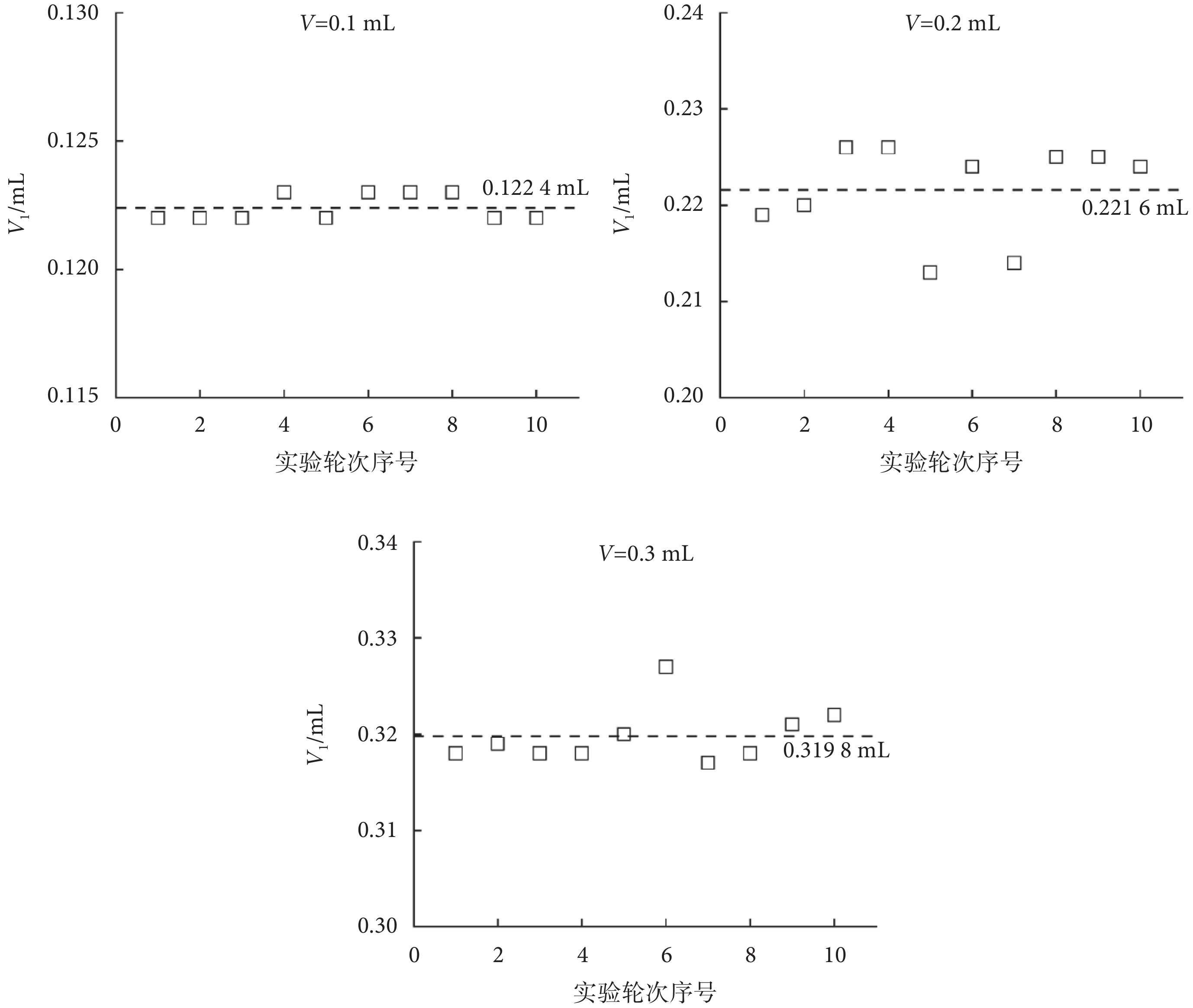 圖3
D = 0.25 mm,P = 0.55 MPa工況下無針注射器的實際注射量
Figure3.
Actual injection volume of the needle-free injector at D = 0.25 mm,P = 0.55 MPa
圖3
D = 0.25 mm,P = 0.55 MPa工況下無針注射器的實際注射量
Figure3.
Actual injection volume of the needle-free injector at D = 0.25 mm,P = 0.55 MPa
為了更準確地獲取無針注射器的注射完成率,以小鼠為對象進行實驗。根據先前文獻[22]的研究結果可知,無針注射器的射流功率隨噴嘴直徑增大而增大,且過大的噴嘴尺寸可能導致不必要的組織損傷和預期之外的注射深度。因此,綜合考慮小鼠的體積與皮膚厚度,實驗中選擇的噴嘴直徑分別為0.14 mm和0.25 mm,設定注射量為0.1 mL。每次注射后使用濾紙吸取殘留在小鼠皮膚表面和噴嘴外側的藥液,并使用精密電子天平(精度為:± 0.1 mg)進行稱重,將所得質量減去濾紙的質量后得到無效注射量的質量,最終可得注射完成率,如式(2)所示:
 |
式中,ρ代表藥液的密度,V代表無針注射器的設定注射量,m代表無效注射量的質量。
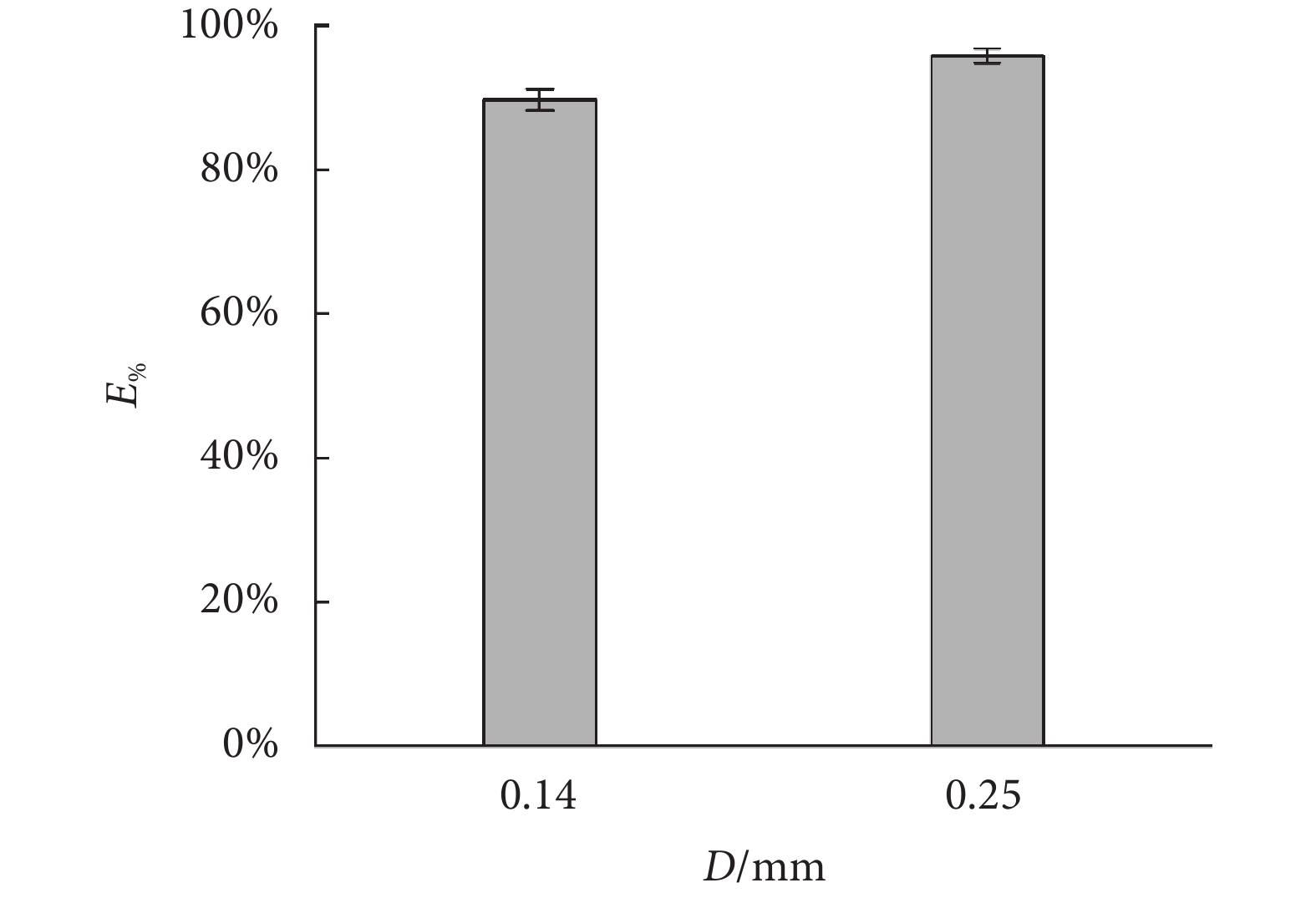
通過式(2)計算無針注射器的實際注射完成率,所得結果如圖4所示。從圖4中可以看出,噴嘴出口尺寸對無針注射器的注射完成率存在一定影響,當噴嘴直徑分別為0.14 mm和0.25 mm時,對應的注射完成率分別為89.7%和95.8%。從已獲得的實驗結果來看,當驅動壓力不變時,噴嘴直徑的增加會導致注射完成率的增大,這與射流的功率有關[28]。較大的噴嘴直徑可以產生更高的射流功率,使射流更容易穿透人體皮膚并在組織內形成一條輸送通道,這有助于抑制射流在該過程中因皮膚阻力和變形所引起的飛濺現象。同時,增大噴嘴直徑可以增加無針注射的深度[22, 29],而注射深度增加則意味著皮膚組織內可以容納的藥液量增多,這在一定程度上也避免了藥液積聚后自注射孔回流溢出。此外,結合前文中測得的無針注射器單次注射時的實際注射量,當前注射完成率所對應的有效注射量大于0.1 mL,滿足規定劑量條件下的給藥要求。
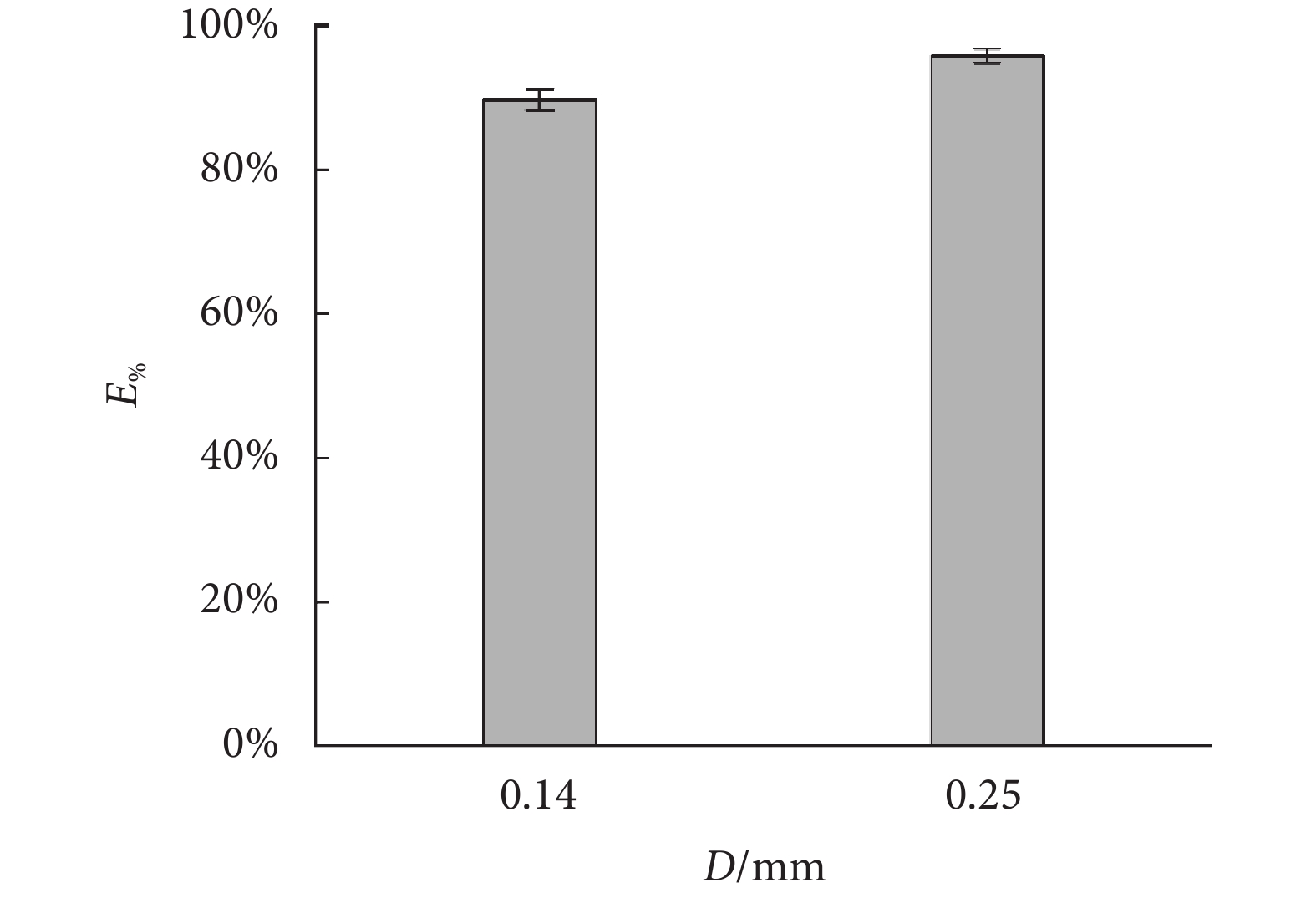 圖4
通過小鼠實驗獲得的注射完成率
Figure4.
Injection completion rate obtained from mouse experiments
圖4
通過小鼠實驗獲得的注射完成率
Figure4.
Injection completion rate obtained from mouse experiments
2.3 皮丘的特征尺寸
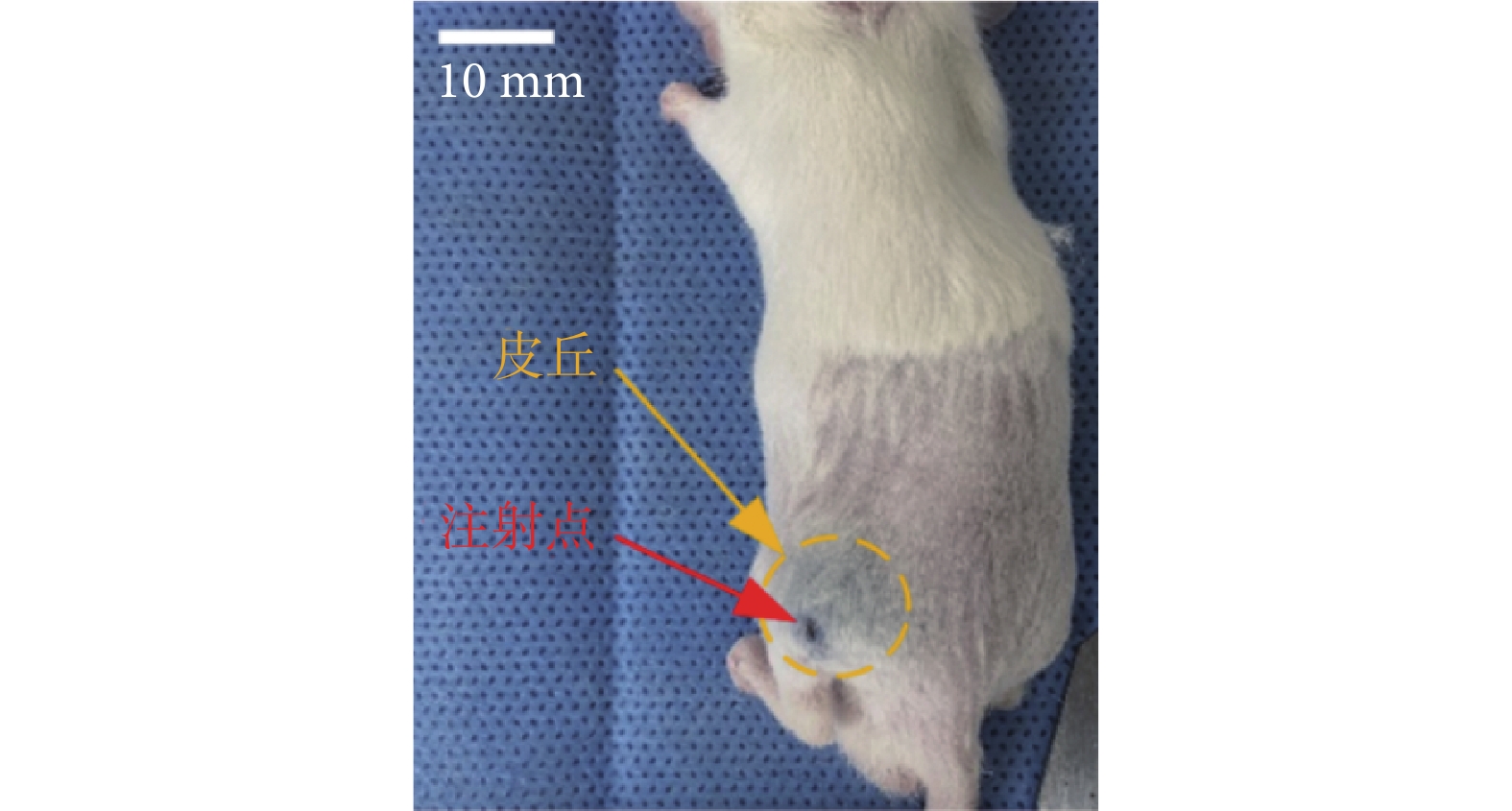
小鼠實驗中,執行無針注射后的效果如圖5所示,其中無針注射的目標區域為小鼠側后方的大腿組織處。圖5中紅色箭頭指示注射點,而黃色虛線標注的區域即為射流在小鼠皮下形成的皮丘。
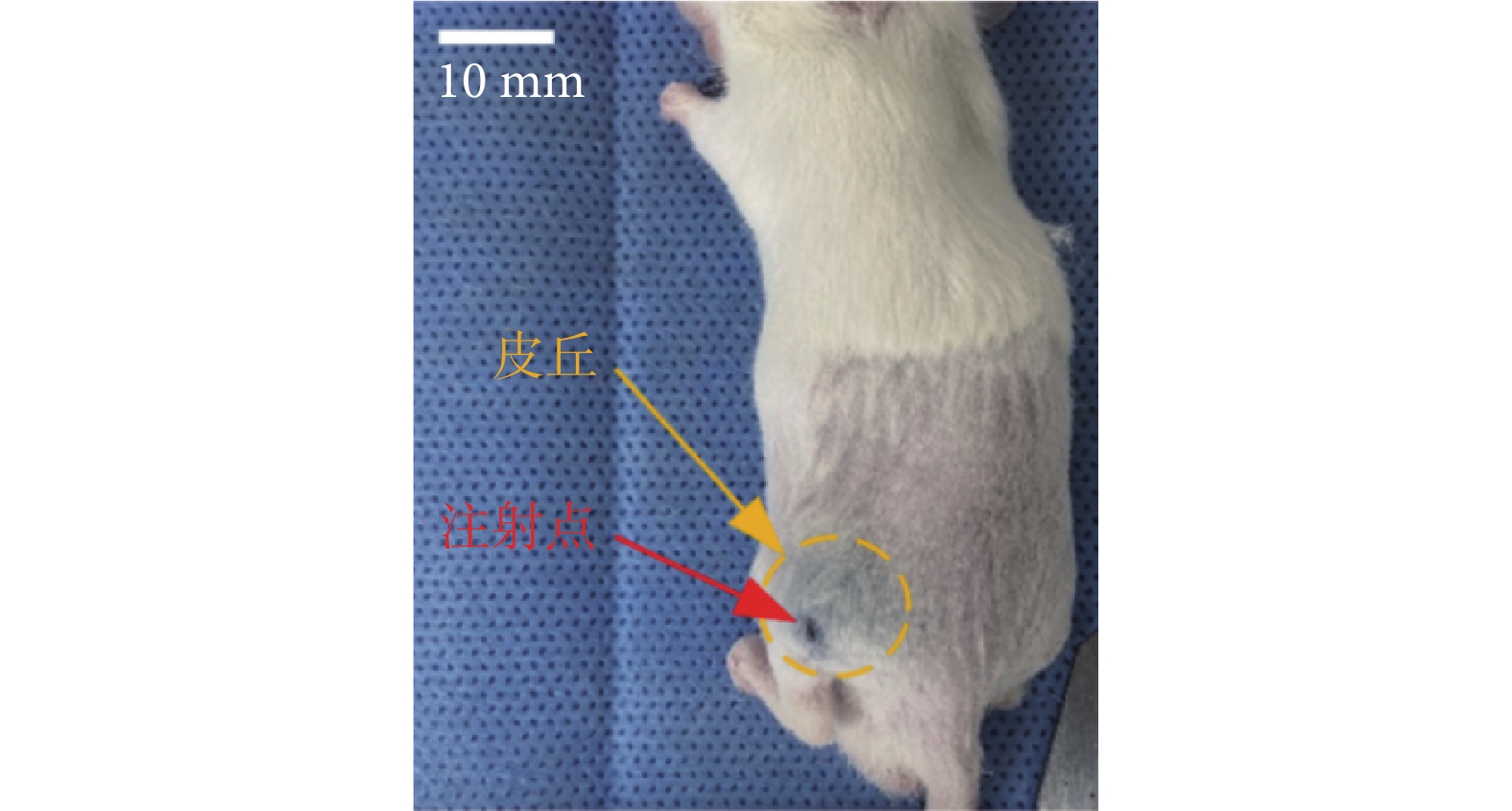 圖5
注射區域與皮丘形狀
Figure5.
Injection area and skin mound
圖5
注射區域與皮丘形狀
Figure5.
Injection area and skin mound
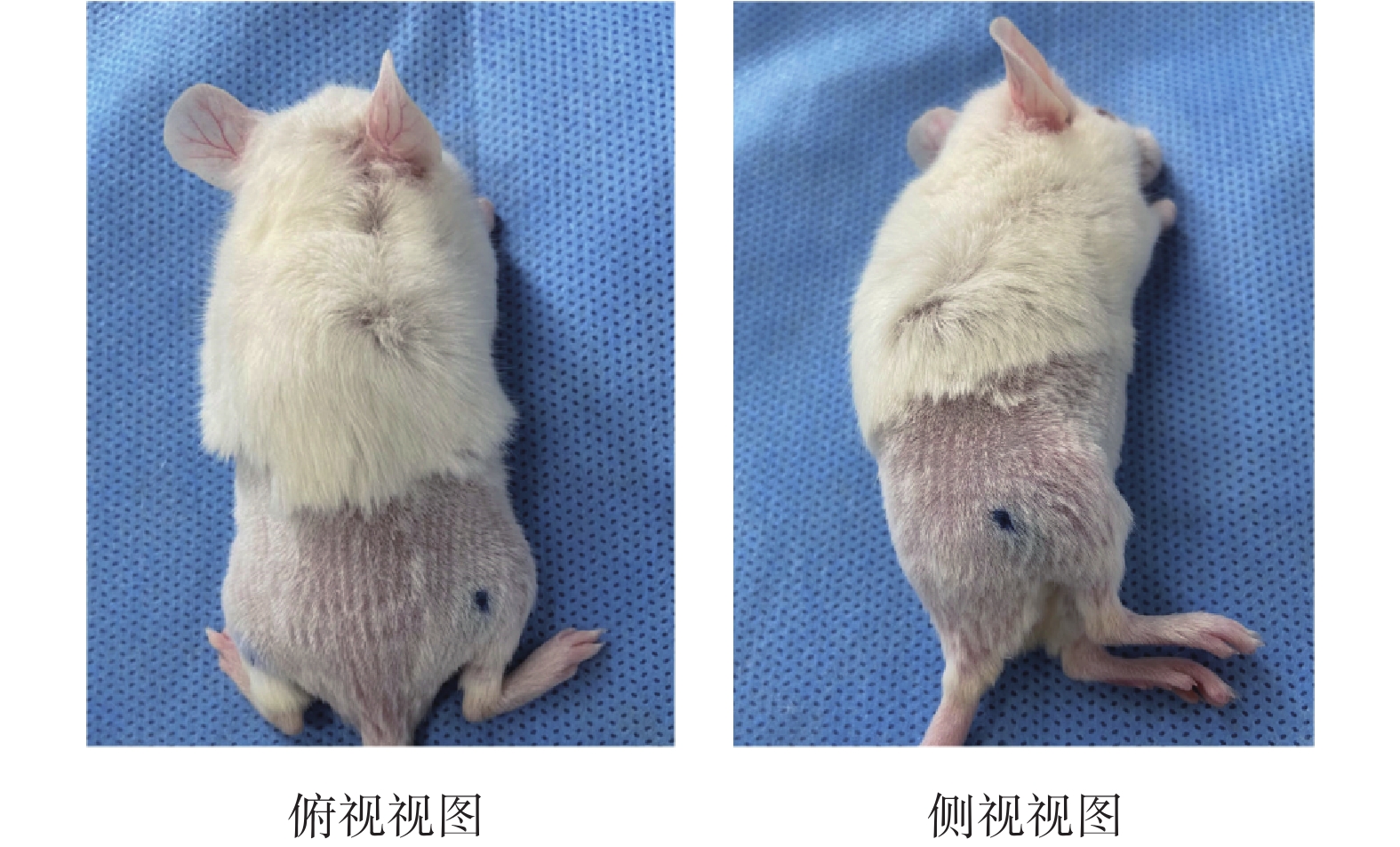
選取D = 0.14 mm條件下的注射結果為例進行進一步分析。如圖6所示,沿注射方向觀察,皮丘的形狀大多為近似橢圓形。
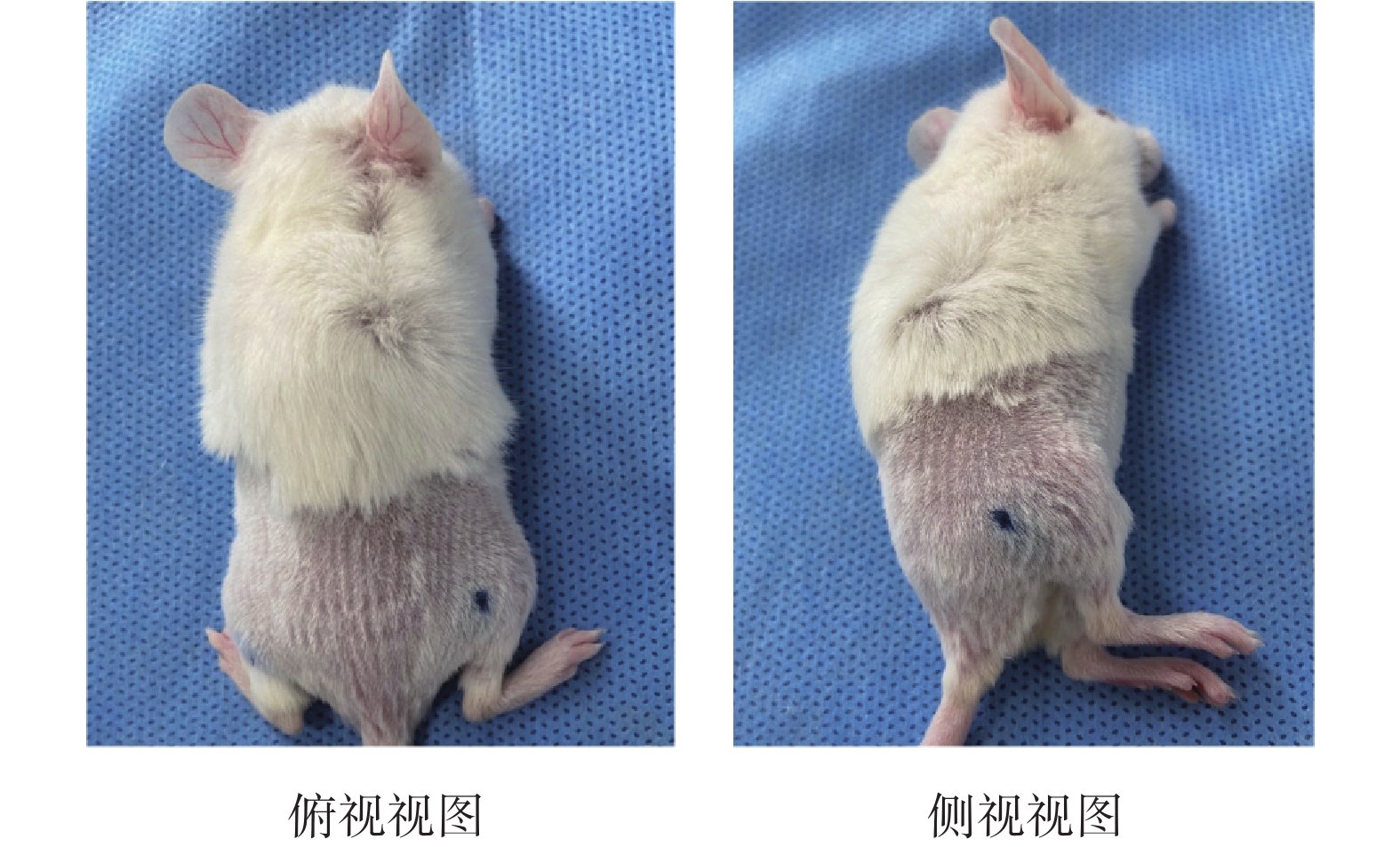 圖6
不同視角下的注射結果圖
Figure6.
Injection result under different views
圖6
不同視角下的注射結果圖
Figure6.
Injection result under different views
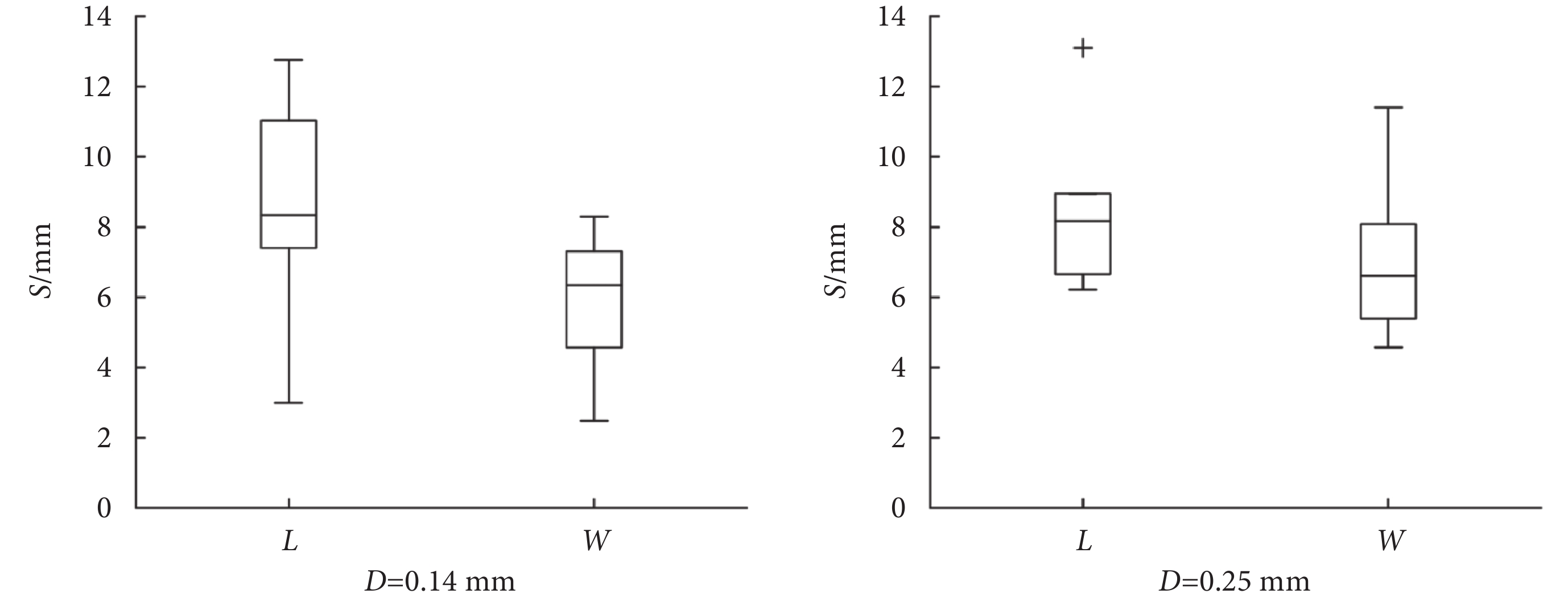
為了深入分析無針注射器的注射效果,對小鼠注射后的皮丘特征尺寸進行量化分析與比較,所得結果如圖7所示,定義皮丘在橫向上擴散的最大距離(S)為皮丘的長度(L);定義垂直于長度方向上的最大擴散距離(S)為皮丘的寬度(W);測量并記錄每次注射后皮丘的長度和寬度值以進行后續分析,其中黑色十字表示異常值。從圖7中可以看出,在不同噴嘴直徑條件下,注射后形成的皮丘尺寸存在明顯差異。當噴嘴直徑為0.14 mm時,皮丘長度值的中位數為8.3 mm,分布范圍為3.0~13.0 mm。皮丘寬度值的中位數為6.3 mm,分布范圍為2.5~8.3 mm。這些數據表明,小鼠皮下組織和肌肉的柔韌程度會對注射結果產生重要的影響。在實驗中觀察到,每次注射時,受小鼠皮膚和肌肉組織變形及相對位移的影響,射流在進入皮膚后主要沿橫向隨機擴散,這也導致皮丘的尺寸在較大范圍內變化。盡管這種擴散行為在一定程度上受到組織纖維分布的影響,但整體來看并未呈現出明顯的規律性。相比之下,將噴嘴直徑增大至0.25 mm時,皮丘在長度方向上的分布范圍明顯減小,所有數據點基本分布在6.0~9.0 mm范圍內,同時皮丘的寬度主要集中在5.0~8.0 mm范圍。當噴嘴直徑增大后,積聚在小鼠皮下的藥液減少,而大多數藥液被輸送至更深的肌肉組織內,導致這一變化的主要原因是射流功率的增加[17, 28]。總體來看,較小的噴嘴直徑更適用于皮下注射,因為從形成的皮丘尺寸來看,此時藥液將更多地聚集在皮下組織中而非肌肉內,而較大的噴嘴直徑則在肌肉注射時具有優勢。
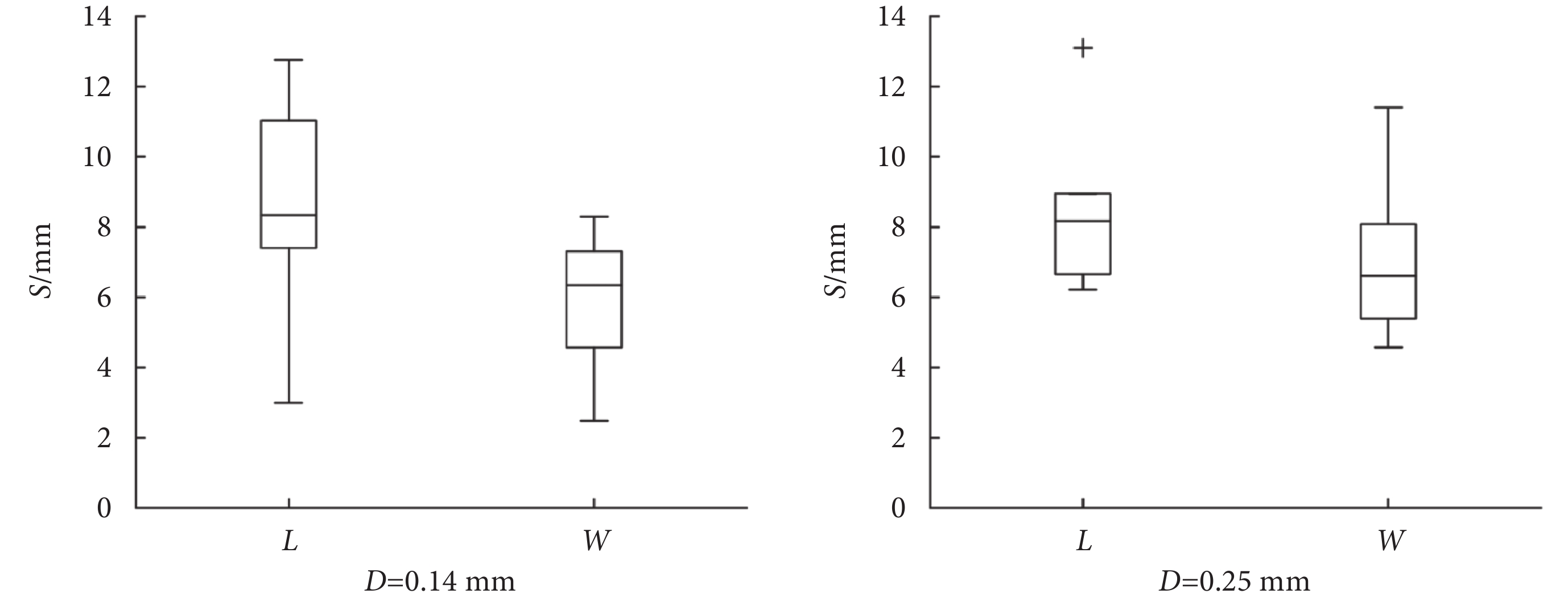 圖7
噴嘴直徑對小鼠皮丘特征尺寸的影響
Figure7.
Effect of nozzle diameter on characteristic dimensions of mouse skin mound
圖7
噴嘴直徑對小鼠皮丘特征尺寸的影響
Figure7.
Effect of nozzle diameter on characteristic dimensions of mouse skin mound
2.4 血糖數值
盡管無針注射技術已在胰島素給藥領域得到應用,但其擴散機制與治療效果尚不明確[30]。為了進一步比較不同注射條件下的藥理作用,本文對小鼠進行了胰島素注射,并分別記錄對照組、胰島素針頭注射組、胰島素0.14 mm無針注射組、胰島素0.25 mm無針注射組小鼠血糖值的變化和藥效持續時間(t),結果如圖8所示。
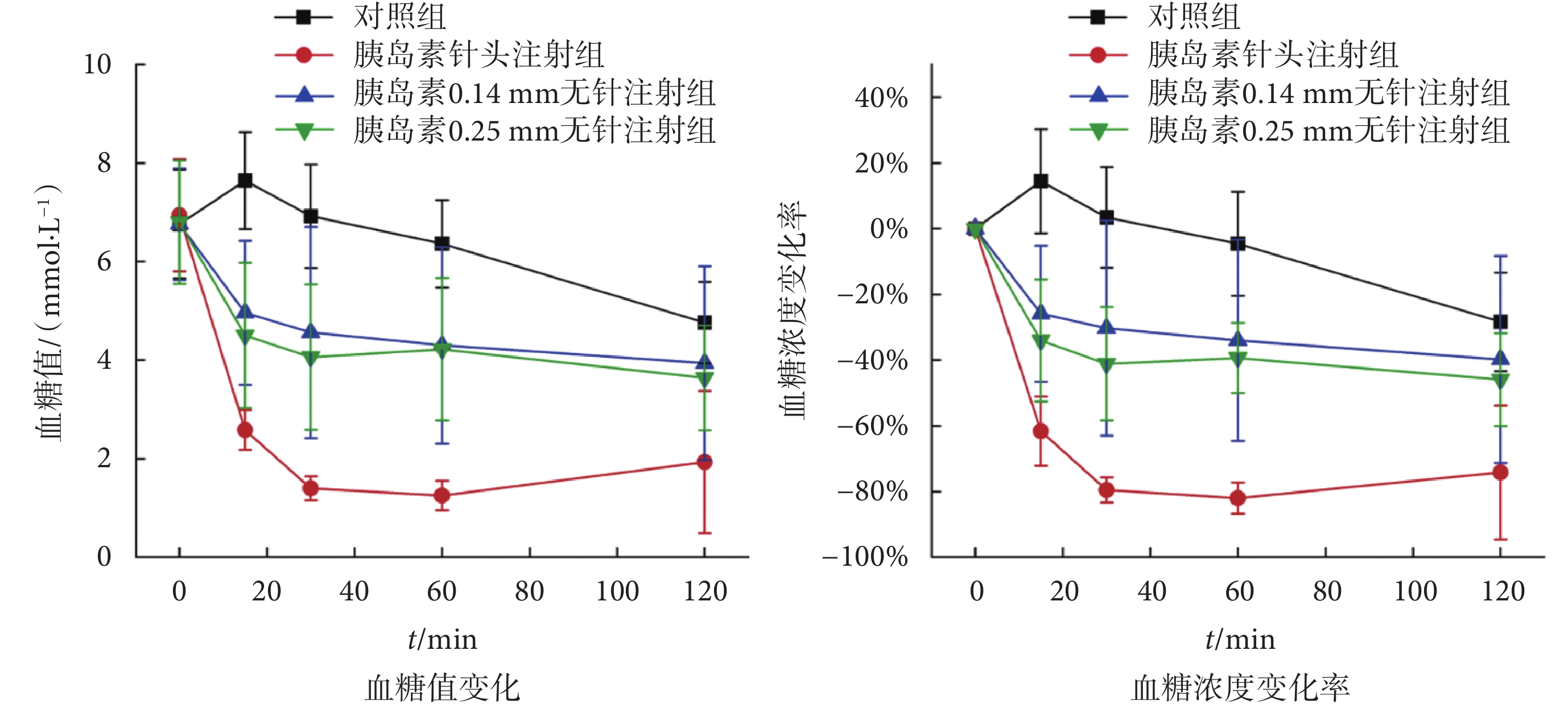 圖8
小鼠血糖參數隨注射時間的變化
Figure8.
Variations of mouse blood glucose parameters with injection duration
圖8
小鼠血糖參數隨注射時間的變化
Figure8.
Variations of mouse blood glucose parameters with injection duration
從圖8中可以看出,注射胰島素后15 min內,小鼠的血糖值明顯降低,而注射生理鹽水的小鼠血糖值則無明顯變化,這說明采用無針注射的方式進行小鼠血糖值的調控是有效的。隨著藥效作用的持續,小鼠的血糖值逐漸下降,直至t = 60 min。然而,對比注射后60~120 min內小鼠血糖值的變化趨勢可以發現,采用無針注射方式的小鼠血糖值仍在持續緩慢降低,而采用常規針頭注射的小鼠血糖值則逐漸升高,這說明采用無針注射的方式進行胰島素注射能獲得更長的藥效持續時間。
為了更為直觀的評估血糖值的變化程度,對血糖濃度變化率進行計算,如式(3)所示:
 |
式中, 代表血糖濃度變化率,
代表血糖濃度變化率, 代表當前血糖值,
代表當前血糖值, 代表初始血糖值。
代表初始血糖值。
從圖8中可以看出,在時間相同時,采用不同注射方式的小鼠血糖值的變化率存在明顯差異,其中采用常規針頭注射的小鼠血糖值的最大變化率為82%,出現在t = 60 min;而在采用無針注射時,小鼠血糖值的最大變化率為46%,出現在t = 120 min。整體來看,采用無針注射方式進行胰島素給藥可以獲得更平穩的血糖變化曲線,這有助于降低患者在治療過程中的低血糖風險。相比之下,常規針頭注射的方式則更適合在人體血糖值已經處于較高狀態、且需要盡快降低到正常范圍的情況。
3 結論
本文以氣動式無針注射器為研究對象,重點分析了噴嘴直徑對無針注射器注射完成率和注射性能的影響,主要結論如下:
(1) 無針注射器的射流特征同時受系統驅動壓力與噴嘴直徑的影響,選取不同的參數組合會導致射流的滯止壓力和持續時間產生差異,其中噴嘴直徑對射流性能的影響更明顯。
(2) 得益于更高的注射功率,無針注射器的注射完成率隨著噴嘴直徑的增加而提高;在本文采用的運行工況條件下,無針注射系統可以滿足規定劑量下的給藥要求。
(3) 皮下組織和肌肉的柔韌程度會對無針注射系統的注射完成率和注射性能產生明顯影響。根據預定注射區域合理選擇噴嘴直徑可以獲得更好的注射效果。進行胰島素注射時,選擇0.14 mm的噴嘴直徑更為合適。
(4) 相較于傳統針頭注射,采用無針注射的方式進行胰島素給藥可以獲得更平穩的血糖變化曲線和更長的藥效持續時間。由于避免了針頭的使用,無針注射技術在提升患者治療體驗上具有明顯優勢。
總體來看,盡管目前已經證實可以通過調節無針注射器的注射參數以獲得不同的注射效果,但對于適應不同要求的無針注射參數的最優化組合仍需進一步探討。同時,由于無針注射的結果還會受到皮膚屬性的影響,因此在接續的研究中可以使用不同的動物模型以進一步分析皮膚屬性對無針注射性能的影響。
重要聲明
利益沖突聲明:本文全體作者均聲明不存在利益沖突。
作者貢獻聲明:朱洋主要負責實驗方案設計和無針注射器的性能測試,以及論文撰寫及修訂;康燦主要負責實驗指導及論文審閱修訂;蔡偉主要負責設備加工和數據預處理;黃超主要負責醫學背景知識指導和小鼠實驗數據分析。
倫理聲明:本研究通過了江蘇大學倫理委員會的審批(許可證號:SCXK2018-0012)。
0 引言
通過針頭進行藥物的皮下輸送是醫藥學領域常用的注射手段[1]。由于注射過程中極易導致疼痛感和交叉感染,以及針頭可能引起的恐懼問題,該注射方式的應用存在一定的限制[2-3]。無針注射技術于20世紀30年代問世[4-5],該技術利用高速微射流穿透皮膚組織,并將藥液輸送至皮下特定位置。在不使用針頭的情況下,該技術有效地解決了常規針頭注射給藥引起的各類弊端,并逐漸在疫苗接種和胰島素注射等場合得到應用[6-7]。
常見的無針注射系統通常由彈簧、壓縮氣體、電磁力和激光作為驅動[8-11]。其中,彈簧式無針注射器的體積小且便于攜帶,在市面上較為常見,但由于其注射動力不可調節且不具備連續注射功能,故應用范圍相對較窄。壓電式無針注射器通過電磁力和激光驅動,其優勢在于具備可控的驅動壓力和更精確的注射劑量調節,然而應用成本較高。氣動式無針注射器的結構合理、運行可靠、連續注射效率高、且驅動壓力可在大范圍內調節,展現出了良好的應用前景。在氣動式無針注射的過程中,受到壓縮氣體的作用,注射活塞移動并對注射腔內的流體加壓,使流體以高速微射流的形式自噴嘴噴出并完成注射。研究表明,當射流的滯止壓力高于15 MPa時[12-13],流體能夠穿透皮膚并在皮下組織中完成擴散。
近年來,胰島素的無針注射技術受到廣泛關注。國內外研究顯示,無針注射胰島素在提高患者的治療依從性和舒適度方面具有明顯優勢[14]。然而,目前針對胰島素無針注射器開展的系統性研究工作較少,相關的治療機制也尚未被完全揭示,限制了無針注射技術在胰島素注射方面的應用。目前,關于無針注射系統的研究主要集中于射流的流體動力學行為[15-16]以及穿透特性[17-18]。然而,對無針注射性能進行綜合評價還必須考慮注射完成后流體在皮下組織內的擴散模式、藥液的注射完成率等關鍵因素。以往研究中常采用聚丙烯酰胺凝膠代替人體組織以研究流體的擴散特性[19-20]。研究發現,射流在凝膠中的擴散行為呈現階段特性,且噴嘴的幾何參數對射流在凝膠中的擴散行為有著重要影響[21]。進一步的研究表明,射流在凝膠中的擴散特性并非由單一參數決定,而是受到噴嘴直徑、流體屬性和射流速度的共同影響。部分學者嘗試使用射流功率表征該特性[22],這有助于更全面地理解射流的擴散行為。盡管通過配比可使凝膠呈現出與人體組織相近的楊氏模量,但是基于凝膠介質獲得的結論仍然存在局限性。這是因為真實的皮膚組織具有更為復雜的孔隙結構和分層特性[23],因此使用在物理性質上與人體皮膚接近的實驗介質十分必要。此外,注射完成率是評估無針注射性能的重要指標,其一般定義為有效注射至皮下的藥劑量與設定注射劑量的比值[24-25]。受限于目前的技術手段,自噴嘴產生的射流在進入預定注射區域的過程中會發生損耗,如注射過程中偶爾出現藥液飛濺與回流、或是注射前期射流在穿透皮膚組織時因能量消耗而產生劑量損失等[26],這些現象均會導致實際注射完成率小于100%。因此,如何調節注射參數以獲得最佳注射完成率,并在此基礎上優化注射效果是無針注射技術研究中的重要內容。目前,對無針注射的注射完成率的研究鮮見報道。
基于以上分析,本文選取噴嘴直徑作為研究切入點,評估其在無針注射過程中發揮的作用,分析其對流體在組織內的擴散行為的影響,并研究其與無針注射過程中的注射完成率的關系。本文選擇小鼠為實驗對象,對比不同注射條件下胰島素對小鼠血糖的影響,并根據獲得的數據對無針注射的性能進行綜合評價,所得結論將有助于深入闡釋無針注射的作用機制,并為氣動無針注射器的優化設計和拓展應用提供重要參考依據。
1 實驗材料與方法
1.1 射流滯止壓力
本研究采用如圖1所示的實驗裝置采集射流的滯止壓力。該實驗裝置由高頻動態壓力傳感器(PCB113B27,PCB Piezotronics Inc.,美國)、數據采集系統(SCM05,LMS Co.,比利時)和數據處理計算機組成。實驗中采用的無針注射器是氣動式無針注射器(POK-H-I,江蘇鉑可醫療科技有限公司,中國)。在實驗過程中,通過夾具固定無針注射器,并確保射流方向垂直于傳感器表面。噴嘴出口和傳感器之間的間隙設置為1.0 mm,確保射流在到達傳感器表面時的速度與噴嘴出口處速度近似相等。當射流沖擊傳感器時,數據采集系統以20.4 kHz的速率采集壓力信號,通過軟件對獲得的壓力數據進行處理。
 圖1
射流壓力采集實驗裝置示意圖
Figure1.
Schematic view of experimental equipment for jet pressure measurement
圖1
射流壓力采集實驗裝置示意圖
Figure1.
Schematic view of experimental equipment for jet pressure measurement
1.2 小鼠實驗
本研究中選擇美國癌癥研究所(Institute of Cancer Research,ICR)培育的小鼠進行動物實驗。ICR小鼠由江蘇大學動物實驗中心提供,無特定病原體(specific pathogen free,SPF)級,7~8周齡,體重20~25 g,雌雄各半。所有小鼠實驗經江蘇大學倫理委員會批準,可用于科學研究(許可證號:SCXK2018-0012)。共選用32只小鼠,其中8只用于注射完成率和藥液擴散的研究,24只用于胰島素實驗和無針注射性能評估。實驗前使用10%水合氯醛溶液按照300 μL/100 g的劑量對小鼠進行全身麻醉,同時對待注射區域進行剃毛處理。
在注射完成率和藥液擴散實驗中,8只小鼠被隨機分為2組,每組4只,每只小鼠執行2次無針注射,選擇的注射部位為小鼠側后方大腿處,左右各注射一次。注射完畢后統計注射完成率,同時觀察皮丘狀態并記錄相關尺寸數據。
進行胰島素實驗前,測量所有小鼠的初始血糖值,并根據所得結果對小鼠進行排序;隨后按照血糖值梯度將24只小鼠分成6組,每組4只;最后從每組中隨機選擇1只小鼠,組成4個實驗組,每組共6只小鼠;這樣的分組方式可以盡可能地減小小鼠間個體差異引起的實驗誤差。此外,考慮到胰島素在實際應用中的每日總量一般為0.4~0.8 U/kg,因此具體分組方式如下:① 對照組:采用常規針頭腹腔注射的方式,注射生理鹽水(5 U/kg);② 胰島素針頭注射組:采用常規針頭腹腔注射的方式,注射0.1 U精蛋白重組人胰島素(1 U/mL);③ 胰島素0.14 mm無針注射組:采用噴嘴直徑(D)為0.14 mm的無針注射器,通過腹腔注射0.1 U精蛋白重組人胰島素(1 U/mL);④ 胰島素0.25 mm無針注射組:采用噴嘴直徑為0.25 mm的無針注射器,通過腹腔注射0.1 U精蛋白重組人胰島素(1 U/mL)。
2 結果與討論
2.1 壓力曲線
微射流的瞬態特性對于無針注射結果有著重要影響,通過沖擊實驗可以得到射流的滯止壓力(P0)隨噴射時間(t)變化的動態曲線。根據臨床應用的常用范圍,選取5種不同的驅動壓力(P),取值為0.41、0.48、0.55、0.62、0.69 MPa,對噴嘴直徑分別為0.14 mm和0.25 mm的無針注射系統進行研究,設定注射量(V)為0.1 mL。不同噴嘴直徑和驅動壓力條件下,無針注射器射流滯止壓力曲線的變化特征如圖2所示。
 圖2
不同注射參數對應的射流滯止壓力隨時間的變化
Figure2.
Time-dependent stagnation pressure of jet at different injection parameters
圖2
不同注射參數對應的射流滯止壓力隨時間的變化
Figure2.
Time-dependent stagnation pressure of jet at different injection parameters
從圖2中可以看出,射流的最大峰值滯止壓力出現在t=0.8 ms處,隨后壓力急劇下降。在整個注射過程的前10 ms內,射流的滯止壓力劇烈震蕩。而在此之后,射流的滯止壓力逐漸趨于平穩并一直持續至整個注射過程結束。從能量轉換的角度來看,當活塞以較高的初速度撞擊流體時,會受到來自流體的阻力,導致活塞速度下降,注射腔內液體壓力升高。此時,在注射腔內外壓差的驅動下,液體自噴嘴中排出,并產生第一個壓力峰值。隨著注射腔內壓力釋放,作用在活塞上的液體阻力逐漸減小,活塞被壓縮空氣再次加速,并推動剩余流體排出注射腔,在t=3.6 ms時形成了第二個峰值壓力。然而,由于活塞動能減少,液體射流的峰值壓力和速度均下降。因此,隨著上述過程的重復,滯止壓力曲線不斷波動,并最終趨于穩定。總體來看,噴嘴直徑和驅動壓力的增加往往伴隨著射流滯止壓力和持續時間的變化。如圖2所示,選取驅動壓力為0.55 MPa的工況進行分析,當噴嘴直徑從0.14 mm增加至0.25 mm時,射流的峰值滯止壓力從58.6 MPa降低至37.9 MPa,持續時間從 65.3 ms縮短至29.2 ms,變化率分別為35.3和55.3%。而當噴嘴直徑為0.14 mm時,隨著驅動壓力從0.41 MPa增加至0.69 MPa,射流的峰值滯止壓力從52.1 MPa增加至64.4 MPa,持續時間從80.9 ms縮短至55.5 ms,變化率分別為23.6%和31.4%。因此,噴嘴直徑的改變對無針注射器射流特性的影響更為明顯。
2.2 注射完成率
藥液的注射完成率為另一個評價無針注射效果的重要指標。注射完成率表征實際進入至目標區域且能發揮作用的有效注射量與設定注射量的比值,如式(1)所示:
 |
式中, 代表注射完成率,
代表注射完成率, 代表有效注射量,
代表有效注射量, 代表設定注射量。
代表設定注射量。
受注射過程中可能發生的藥液殘留或飛濺等因素的影響,實際注射完成率一般無法達到100%,因此在滿足射流滯止壓力可以穿透皮膚的前提下,提高給藥劑量的準確性和穩定性,是提高無針注射效率和改善注射效果的重要途徑。在給定噴嘴直徑和注射量的條件下,本文測量了無針注射器通過噴嘴排出的實際注射量(V1)。采用直徑為0.25 mm的噴嘴,驅動壓力固定為0.55 MPa,設定注射量分別為0.1、0.2、0.3 mL,使用醫用離心管對無針注射器單次注射的藥液進行收集并稱重,每組實驗重復10次,所得結果如圖3所示。可以看出,當設定注射量在0.1~0.3 mL范圍時,無針注射器平均單次排出的藥液體積分別為0.122 4、0.221 6、0.319 8 mL,即在所有工況下無針注射器的實際注射量均大于設定注射量。值得注意的是,盡管設定注射量的變化范圍較大,但不同實驗組的絕對誤差均趨近于0.02 mL,因此注射量的設定值和實際值之間的偏差取決于無針注射器的結構及驅動機制。考慮到藥液自無針注射器中排出到進入皮膚組織這一過程中還會存在藥液損耗[27],故最終的注射完成率還需進一步分析。
 圖3
D = 0.25 mm,P = 0.55 MPa工況下無針注射器的實際注射量
Figure3.
Actual injection volume of the needle-free injector at D = 0.25 mm,P = 0.55 MPa
圖3
D = 0.25 mm,P = 0.55 MPa工況下無針注射器的實際注射量
Figure3.
Actual injection volume of the needle-free injector at D = 0.25 mm,P = 0.55 MPa
為了更準確地獲取無針注射器的注射完成率,以小鼠為對象進行實驗。根據先前文獻[22]的研究結果可知,無針注射器的射流功率隨噴嘴直徑增大而增大,且過大的噴嘴尺寸可能導致不必要的組織損傷和預期之外的注射深度。因此,綜合考慮小鼠的體積與皮膚厚度,實驗中選擇的噴嘴直徑分別為0.14 mm和0.25 mm,設定注射量為0.1 mL。每次注射后使用濾紙吸取殘留在小鼠皮膚表面和噴嘴外側的藥液,并使用精密電子天平(精度為:± 0.1 mg)進行稱重,將所得質量減去濾紙的質量后得到無效注射量的質量,最終可得注射完成率,如式(2)所示:
 |
式中,ρ代表藥液的密度,V代表無針注射器的設定注射量,m代表無效注射量的質量。
通過式(2)計算無針注射器的實際注射完成率,所得結果如圖4所示。從圖4中可以看出,噴嘴出口尺寸對無針注射器的注射完成率存在一定影響,當噴嘴直徑分別為0.14 mm和0.25 mm時,對應的注射完成率分別為89.7%和95.8%。從已獲得的實驗結果來看,當驅動壓力不變時,噴嘴直徑的增加會導致注射完成率的增大,這與射流的功率有關[28]。較大的噴嘴直徑可以產生更高的射流功率,使射流更容易穿透人體皮膚并在組織內形成一條輸送通道,這有助于抑制射流在該過程中因皮膚阻力和變形所引起的飛濺現象。同時,增大噴嘴直徑可以增加無針注射的深度[22, 29],而注射深度增加則意味著皮膚組織內可以容納的藥液量增多,這在一定程度上也避免了藥液積聚后自注射孔回流溢出。此外,結合前文中測得的無針注射器單次注射時的實際注射量,當前注射完成率所對應的有效注射量大于0.1 mL,滿足規定劑量條件下的給藥要求。
 圖4
通過小鼠實驗獲得的注射完成率
Figure4.
Injection completion rate obtained from mouse experiments
圖4
通過小鼠實驗獲得的注射完成率
Figure4.
Injection completion rate obtained from mouse experiments
2.3 皮丘的特征尺寸
小鼠實驗中,執行無針注射后的效果如圖5所示,其中無針注射的目標區域為小鼠側后方的大腿組織處。圖5中紅色箭頭指示注射點,而黃色虛線標注的區域即為射流在小鼠皮下形成的皮丘。
 圖5
注射區域與皮丘形狀
Figure5.
Injection area and skin mound
圖5
注射區域與皮丘形狀
Figure5.
Injection area and skin mound
選取D = 0.14 mm條件下的注射結果為例進行進一步分析。如圖6所示,沿注射方向觀察,皮丘的形狀大多為近似橢圓形。
 圖6
不同視角下的注射結果圖
Figure6.
Injection result under different views
圖6
不同視角下的注射結果圖
Figure6.
Injection result under different views
為了深入分析無針注射器的注射效果,對小鼠注射后的皮丘特征尺寸進行量化分析與比較,所得結果如圖7所示,定義皮丘在橫向上擴散的最大距離(S)為皮丘的長度(L);定義垂直于長度方向上的最大擴散距離(S)為皮丘的寬度(W);測量并記錄每次注射后皮丘的長度和寬度值以進行后續分析,其中黑色十字表示異常值。從圖7中可以看出,在不同噴嘴直徑條件下,注射后形成的皮丘尺寸存在明顯差異。當噴嘴直徑為0.14 mm時,皮丘長度值的中位數為8.3 mm,分布范圍為3.0~13.0 mm。皮丘寬度值的中位數為6.3 mm,分布范圍為2.5~8.3 mm。這些數據表明,小鼠皮下組織和肌肉的柔韌程度會對注射結果產生重要的影響。在實驗中觀察到,每次注射時,受小鼠皮膚和肌肉組織變形及相對位移的影響,射流在進入皮膚后主要沿橫向隨機擴散,這也導致皮丘的尺寸在較大范圍內變化。盡管這種擴散行為在一定程度上受到組織纖維分布的影響,但整體來看并未呈現出明顯的規律性。相比之下,將噴嘴直徑增大至0.25 mm時,皮丘在長度方向上的分布范圍明顯減小,所有數據點基本分布在6.0~9.0 mm范圍內,同時皮丘的寬度主要集中在5.0~8.0 mm范圍。當噴嘴直徑增大后,積聚在小鼠皮下的藥液減少,而大多數藥液被輸送至更深的肌肉組織內,導致這一變化的主要原因是射流功率的增加[17, 28]。總體來看,較小的噴嘴直徑更適用于皮下注射,因為從形成的皮丘尺寸來看,此時藥液將更多地聚集在皮下組織中而非肌肉內,而較大的噴嘴直徑則在肌肉注射時具有優勢。
 圖7
噴嘴直徑對小鼠皮丘特征尺寸的影響
Figure7.
Effect of nozzle diameter on characteristic dimensions of mouse skin mound
圖7
噴嘴直徑對小鼠皮丘特征尺寸的影響
Figure7.
Effect of nozzle diameter on characteristic dimensions of mouse skin mound
2.4 血糖數值
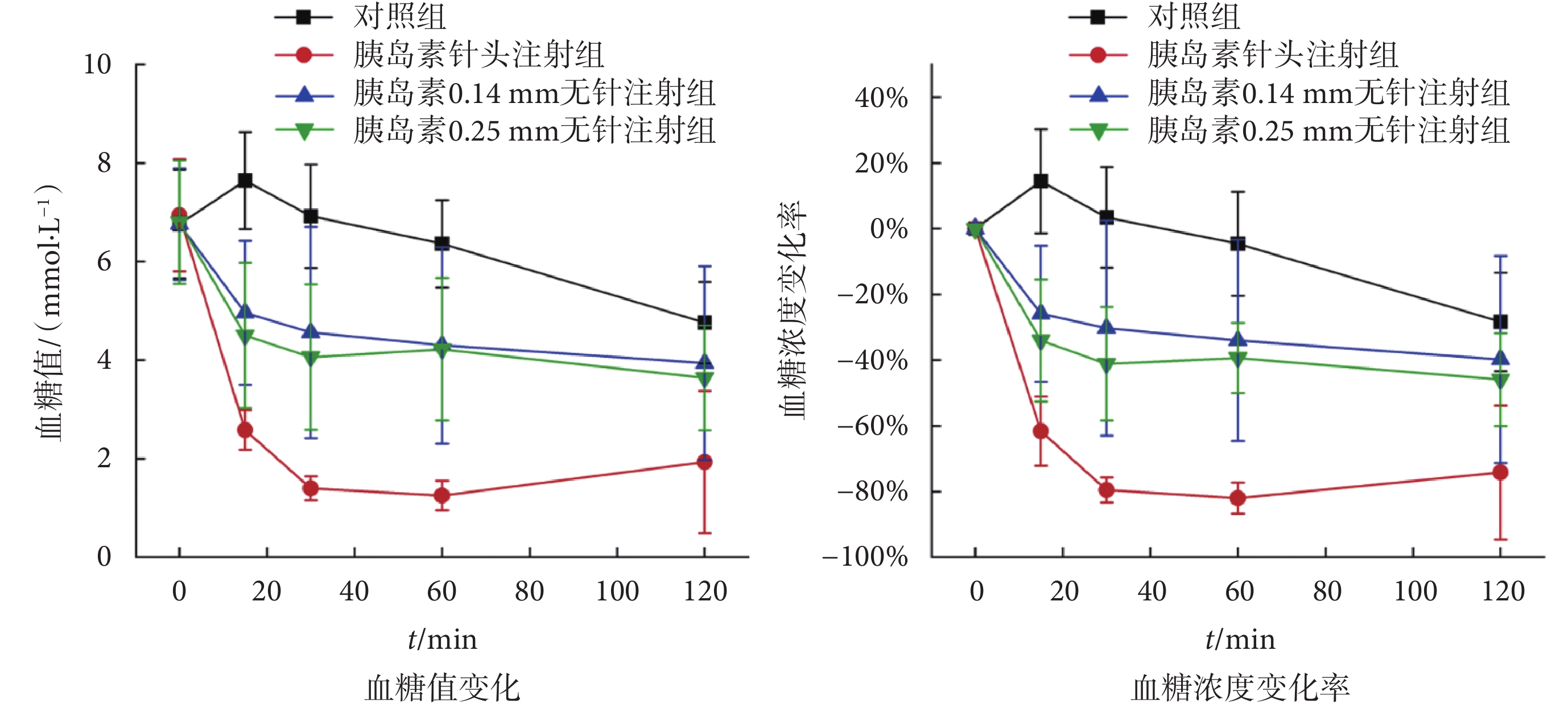
盡管無針注射技術已在胰島素給藥領域得到應用,但其擴散機制與治療效果尚不明確[30]。為了進一步比較不同注射條件下的藥理作用,本文對小鼠進行了胰島素注射,并分別記錄對照組、胰島素針頭注射組、胰島素0.14 mm無針注射組、胰島素0.25 mm無針注射組小鼠血糖值的變化和藥效持續時間(t),結果如圖8所示。
 圖8
小鼠血糖參數隨注射時間的變化
Figure8.
Variations of mouse blood glucose parameters with injection duration
圖8
小鼠血糖參數隨注射時間的變化
Figure8.
Variations of mouse blood glucose parameters with injection duration
從圖8中可以看出,注射胰島素后15 min內,小鼠的血糖值明顯降低,而注射生理鹽水的小鼠血糖值則無明顯變化,這說明采用無針注射的方式進行小鼠血糖值的調控是有效的。隨著藥效作用的持續,小鼠的血糖值逐漸下降,直至t = 60 min。然而,對比注射后60~120 min內小鼠血糖值的變化趨勢可以發現,采用無針注射方式的小鼠血糖值仍在持續緩慢降低,而采用常規針頭注射的小鼠血糖值則逐漸升高,這說明采用無針注射的方式進行胰島素注射能獲得更長的藥效持續時間。
為了更為直觀的評估血糖值的變化程度,對血糖濃度變化率進行計算,如式(3)所示:
 |
式中, 代表血糖濃度變化率,
代表血糖濃度變化率, 代表當前血糖值,
代表當前血糖值, 代表初始血糖值。
代表初始血糖值。
從圖8中可以看出,在時間相同時,采用不同注射方式的小鼠血糖值的變化率存在明顯差異,其中采用常規針頭注射的小鼠血糖值的最大變化率為82%,出現在t = 60 min;而在采用無針注射時,小鼠血糖值的最大變化率為46%,出現在t = 120 min。整體來看,采用無針注射方式進行胰島素給藥可以獲得更平穩的血糖變化曲線,這有助于降低患者在治療過程中的低血糖風險。相比之下,常規針頭注射的方式則更適合在人體血糖值已經處于較高狀態、且需要盡快降低到正常范圍的情況。
3 結論
本文以氣動式無針注射器為研究對象,重點分析了噴嘴直徑對無針注射器注射完成率和注射性能的影響,主要結論如下:
(1) 無針注射器的射流特征同時受系統驅動壓力與噴嘴直徑的影響,選取不同的參數組合會導致射流的滯止壓力和持續時間產生差異,其中噴嘴直徑對射流性能的影響更明顯。
(2) 得益于更高的注射功率,無針注射器的注射完成率隨著噴嘴直徑的增加而提高;在本文采用的運行工況條件下,無針注射系統可以滿足規定劑量下的給藥要求。
(3) 皮下組織和肌肉的柔韌程度會對無針注射系統的注射完成率和注射性能產生明顯影響。根據預定注射區域合理選擇噴嘴直徑可以獲得更好的注射效果。進行胰島素注射時,選擇0.14 mm的噴嘴直徑更為合適。
(4) 相較于傳統針頭注射,采用無針注射的方式進行胰島素給藥可以獲得更平穩的血糖變化曲線和更長的藥效持續時間。由于避免了針頭的使用,無針注射技術在提升患者治療體驗上具有明顯優勢。
總體來看,盡管目前已經證實可以通過調節無針注射器的注射參數以獲得不同的注射效果,但對于適應不同要求的無針注射參數的最優化組合仍需進一步探討。同時,由于無針注射的結果還會受到皮膚屬性的影響,因此在接續的研究中可以使用不同的動物模型以進一步分析皮膚屬性對無針注射性能的影響。
重要聲明
利益沖突聲明:本文全體作者均聲明不存在利益沖突。
作者貢獻聲明:朱洋主要負責實驗方案設計和無針注射器的性能測試,以及論文撰寫及修訂;康燦主要負責實驗指導及論文審閱修訂;蔡偉主要負責設備加工和數據預處理;黃超主要負責醫學背景知識指導和小鼠實驗數據分析。
倫理聲明:本研究通過了江蘇大學倫理委員會的審批(許可證號:SCXK2018-0012)。