冠狀動脈疾病(coronary artery disease, CAD)是一種主要由動脈粥樣硬化引起的心血管疾病,其涉及脂質代謝、炎癥反應、內皮功能障礙等多種病理生理機制。胎球蛋白 B 是一種由肝臟分泌的糖蛋白,能夠參與細胞炎癥、血管鈣化及脂質代謝等多個過程,與 CAD 的發病密切相關。該文就胎球蛋白 B 和 CAD 的關系及發生發展機制進行了綜述,以期為 CAD 的預防和診治提供新的選擇和方法。
引用本文: 李樊丹, 徐靜, 陳蕓, 呂湛. 胎球蛋白 B 與冠狀動脈疾病的研究進展. 華西醫學, 2024, 39(8): 1314-1318. doi: 10.7507/1002-0179.202405135 復制
版權信息: ?四川大學華西醫院華西期刊社《華西醫學》版權所有,未經授權不得轉載、改編
冠狀動脈疾病(coronary artery disease, CAD)是世界上影響人體健康最常見的心血管疾病[1]。CAD 是一種由多種因素導致的疾病,主要由冠狀動脈粥樣硬化引起。而冠狀動脈粥樣硬化是一個包含多種生理病理過程的疾病狀態,主要涉及脂質代謝、血栓形成、炎癥、內皮功能障礙、氧化應激等過程。并且在大量的普通人群之中,也有著導致 CAD 的多種危險因素,例如高血糖、高血壓、高血脂、慢性腎臟疾病、年老、吸煙、過胖、性別、高鹽高脂飲食及遺傳病史等[2]。因此通過識別與 CAD 發展相關的細胞因子,對于實現 CAD 的早期診斷和預防具有重要意義。肝臟分泌的多種細胞因子與 CAD 的發生及發展密切相關,這些細胞因子水平異常可能導致 CAD 的發生或進展。國外研究表明胎球蛋白 B 作為一種由肝臟分泌的糖蛋白,不僅在細胞炎癥反應中起到關鍵作用,還與血管鈣化過程、脂質代謝失衡以及斑塊穩定性等方面密切相關[3],這些過程都是 CAD 發病機制的重要組成部分。雖然胎球蛋白 B 在 CAD 中的具體作用尚未十分明確,但隨著研究的不斷深入,其或許可以為 CAD 的預防和診斷提供新選擇。因此,本文現就胎球蛋白 B 與 CAD 的研究進展作一綜述。
1 胎球蛋白 B
胎球蛋白是胎牛血清中含量最多的球蛋白,其構成了一組廣泛的肝源性血漿和基質蛋白,其中包括胎球蛋白 A(又稱 α2-Heremans-Schmid 糖蛋白)以及胎球蛋白 B,而胎球蛋白 B 作為胎球蛋白 A 的旁系同源物在 1999 年被 Olivier 等[4]發現。目前國外大量實驗已經表明胎球蛋白 A 可參與胰島素信號通路的調節,還具有作為異位鈣化抑制劑、蛋白酶抑制劑、炎癥介質、抗炎伴侶、致動脈粥樣硬化因子和成脂肪因子的作用[5]。隨著研究的進一步擴展,實驗表明胎球蛋白 A 與 CAD 的進程有著密不可分的關系[6]。而作為胎球蛋白 A 的旁系同源物,胎球蛋白 B 是否影響 CAD 的進展尚不完全清楚。
胎球蛋白 B 是一種復雜的多域蛋白質,由 382 個氨基酸組成,分子量達 60 kDa。這種蛋白質的結構特征在于含有 2 個串聯的胱抑素結構域,并通過二硫鍵結合。胎球蛋白 B 的編碼基因為 FETUB,該基因與胎球蛋白 A 的基因序列相似性達到 22%[7]。胎球蛋白 A 和胎球蛋白 B 具有相似的進化起源,在脊椎動物基因組中具有相近的染色體位置。具體來說,他們的編碼基因主要并排位于人類基因組的單個染色體區域(3q27)[5]。這就暗示胎球蛋白 B 可能與胎球蛋白 A 具有部分重疊但不完全相同的功能。胎球蛋白 B 可參與炎癥、鈣化與脂代謝等多個方面的調控,并且與內皮功能障礙和斑塊破裂密切相關。這些功能表明胎球蛋白 B 在 CAD 的發展中扮演著重要角色。
2 胎球蛋白 B 與 CAD 的關系
2.1 胎球蛋白 B 與動脈粥樣硬化
研究提示,血脂水平異常可以推進動脈粥樣硬化進程,而動脈粥樣硬化是多種心血管疾病發生的主要原因[8]。在這一背景下,有學者提出胎球蛋白 B 可能通過影響血脂水平,間接促進動脈粥樣硬化或其他心血管疾病的發展;進而為驗證這一假設,研究人員在一項針對家族性高膽固醇血癥(一種常見的遺傳性疾病,與早期 CAD 的增長有關)的動物實驗中,對動物樣品進行整體血漿蛋白質譜分析,結果顯示家族性高膽固醇血癥血清中胎球蛋白 B 水平顯著增加[8]。此外,國內學者在一項
2.2 胎球蛋白 B 與冠心病
冠心病是一種慢性免疫炎癥性纖維增生性疾病,大致可分為急性冠脈綜合征(acute coronary syndrome, ACS)和慢性冠脈綜合征(chronic coronary syndrome, CCS)[11]。其中 ACS 是冠心病的最重要階段,主要原因是動脈粥樣硬化斑塊破壞導致冠狀動脈部分或完全血栓性閉塞[12]。有研究發現胎球蛋白 B 可能與 ACS 密切相關[13-14]。有學者采用酶聯免疫吸附法檢測 87 例冠心病患者和 87 例健康對照組血清胎球蛋白 B 水平,結果顯示冠心病患者的血清胎球蛋白 B 水平明顯高于健康對照組[(90.7±32.1) vs. (110.0±32.7) μg/mL,P<0.001],且 ACS 組血清胎球蛋白 B 水平極高[(115.0±35.2) μg/mL)][13]。該實驗首次提出高水平的胎球蛋白 B 與冠心病存在獨立相關性。此外該實驗還發現在斑塊不穩定的急性心肌梗死(acute myocardial infarction, AMI)患者中,血清胎球蛋白 B 的表達發生了改變,這表明它可能與 AMI 的發展有關[13]。盡管胎球蛋白 B 參與冠心病的機制不完全明確,但實驗發現胎球蛋白 B 濃度與低密度脂蛋白膽固醇(low-density lipoprotein cholesterol, LDL-C)水平呈正相關,而 LDL-C 水平被認為是動脈粥樣硬化斑塊形成和發展的關鍵因素[14]。當 LDL-C 在內皮下滯留,它容易被活性氧氧化,進而導致內皮功能障礙,并誘發炎癥反應進而推進動脈粥樣硬化形成過程。因此,實驗推測胎球蛋白 B 可能通過其對炎癥的影響,部分參與冠心病的發展和進展[13]。此外,有學者通過一項回顧性研究發現,血清胎球蛋白 B 水平越高,冠心病患者的心血管事件發生風險越高(r=0.990,P<0.05);進一步將 ACS 組分為 AMI 組和不穩定型心絞痛組,結果顯示前者胎球蛋白 B 水平較后者明顯升高[15]。這些實驗結果顯示,胎球蛋白 B 可預測患者發生冠心病的風險。
心肌缺血一直被認為是 CCS 的重要因素[16]。胎球蛋白 B 可能通過影響心肌缺血與 CCS 相聯系。有學者通過一項動物研究構建心肌缺血模型,發現高水平的胎球蛋白 B 會提高小鼠心肌缺血易感性;此外,胎球蛋白 B 直接與胰島素受體 β 亞單位作用,抑制其酪氨酸位點和下游信號通路的磷酸化,從而增加心肌缺血易感性,該項實驗首次證實胎球蛋白 B 上調會導致心臟胰島素抵抗,并促使心肌缺血/再灌注損傷[17]。這些發現進一步證實了胎球蛋白 B 與 CCS 存在一定的相關性。
3 胎球蛋白 B 在 CAD 中的可能作用機制
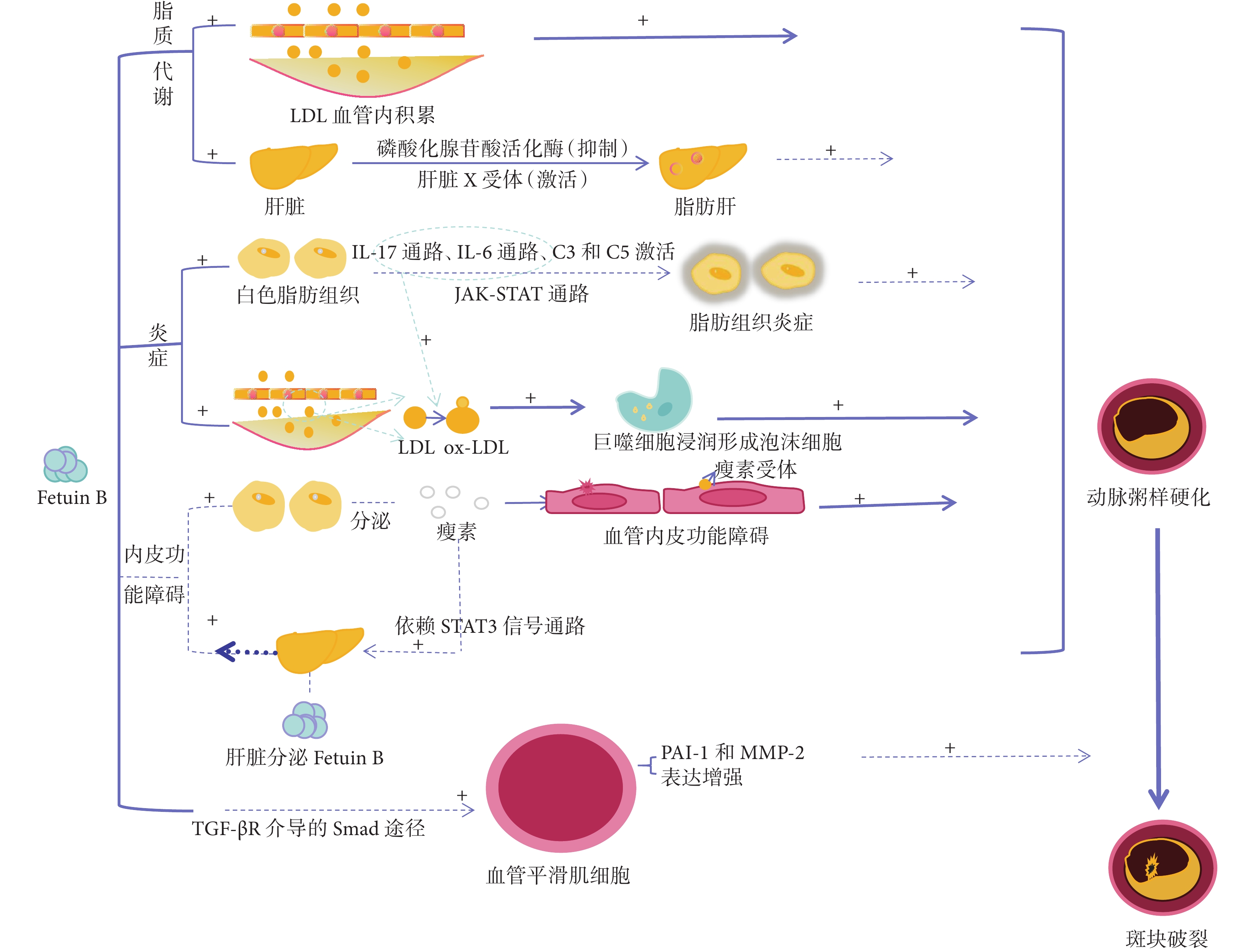
胎球蛋白 B 促進動脈粥樣硬化的可能機制涉及脂質代謝、炎癥、血管鈣化、內皮功能障礙、斑塊破裂等(圖1)。
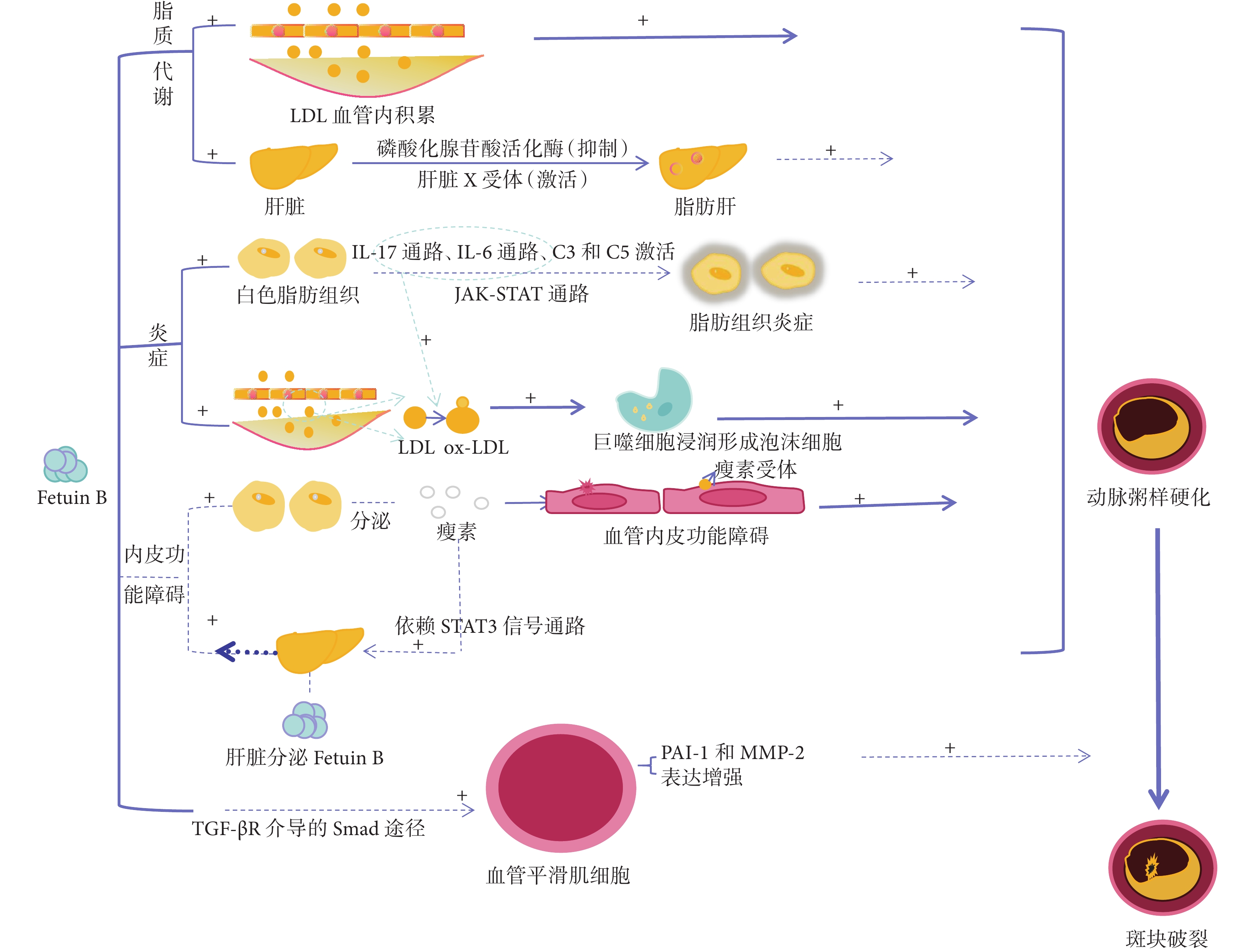 圖1
胎球蛋白 B 促進動脈粥樣硬化的可能機制
圖1
胎球蛋白 B 促進動脈粥樣硬化的可能機制
Fetuin B:胎球蛋白 B;LDL:低密度脂蛋白;IL-17:白細胞介素-17;IL-6:白細胞介素-6;C3、C5:補體 C3、補體 C5;JAK:酪氨酸蛋白激酶;STAT:信號轉導與轉錄激活因子;ox-LDL:氧化型低密度脂蛋白;TGF-βR:轉化生長因子-β 受體;Smad:響應 TGF-βR 的一種關鍵信號分子;PAI-1:纖溶酶原激活物抑制物 1;MMP-2:基質金屬蛋白酶-2
3.1 脂質代謝
隨著對 CAD 研究的深入,有學者提出血脂異常是 CAD 的促發因素[18]。早期血脂異常可促使血管內皮細胞功能受損和通透性增加,使循環中的脂蛋白進入受損內膜區,加速氧化型低密度脂蛋白形成[19],加重或誘發動脈粥樣硬化。研究人員通過油紅 O 染色實驗表明,使用重組胎球蛋白 B 處理人肝細胞系 HepG2 細胞后,血脂含量顯著增加,而去除胎球蛋白 B 則 HepG2 細胞中的肝臟脂質積聚現象明顯減弱[20]。這表明胎球蛋白 B 可能會加重肝臟脂質積聚。研究還發現,胎球蛋白 B 可能通過減少抑制脂肪酸氧化的磷酸化腺苷酸活化蛋白激酶和激活上調脂肪生成肝臟 X 受體和甾醇調節元件結合轉錄因子 1 來參與脂質代謝[20]。此外,一項全基因組鑒定研究顯示,在非酒精性脂肪肝病患者中 FETUB 基因通過法尼醇 X 受體/類視黃醇 X 受體通路高表達[21]。然而,胎球蛋白 B 參與脂質代謝的確切機制仍需進一步研究證實。
3.2 炎癥
CAD 的發病機制和進展主要由炎癥驅動[22]。研究者觀察到胎球蛋白 B 主要被白色脂肪組織吸收,與胰島素抵抗有關[23]。此外,胎球蛋白 B 可以直接誘導脂肪細胞炎癥,并且通過對全 RNA 測序發現它與多個炎癥通路相關,包括白細胞介素-17 信號通路、白細胞介素-6 家族信號通路、補體 C3 和補體 C5 的激活、酪氨酸蛋白激酶信號轉導及轉錄激活因子信號通路等[23]。有研究提示胎球蛋白 B 過表達可通過激活小膠質細胞和核轉錄因子 κB 信號通路進而促進某些疾病的炎癥[24],但尚不能確定胎球蛋白 B 可通過這種途徑促進 CAD 炎癥。因此,目前仍無法清楚闡明胎球蛋白 B 參與 CAD 炎癥反應的確切分子機制。
3.3 血管鈣化
血管鈣化與 CAD 的病理過程密切相關,涉及復雜的病理生理機制,包括鈣和磷異常、鈣化和礦化抑制因子的丟失、血管平滑肌細胞向鈣化血管細胞的成骨轉化等[25]。近期研究表明,胎球蛋白 A 通過介導蛋白質-礦物質膠體的形成,促使網狀內皮系統快速清除蛋白質-礦物質膠體,防止礦物質異常沉淀,從而防止病理性礦化(鈣化)[26]。另外,胎球蛋白 A 具有富含鈣的礦物質和轉化生長因子-β(transforming growth factor β, TGF-β)超家族高親和力的結合位點,可抵消骨礦化所需的 TGF-β 超家族以及清除骨外區域的沉淀鈣,防止鈣鹽沉淀、血管鈣化,進而防止 CAD[5]。由于胎球蛋白 B 是胎球蛋白 A 的旁系同源物[8],有學者進行了沉淀抑制試驗,結果顯示胎球蛋白 B 可延緩血管鈣化進程,只是效果不如胎球蛋白 A[27]。這提示胎球蛋白 B 和血管鈣化有聯系,但是二者聯系的具體機制仍需要更加深入的研究。
3.4 內皮功能障礙
內皮細胞功能障礙是動脈粥樣硬化的早期病變之一[28],其中瘦素水平升高也是內皮功能障礙的危險因素。有研究發現肥胖患者血清胎球蛋白 B 水平與瘦素呈正相關,暗示胎球蛋白 B 可能與內皮功能障礙有關;并且瘦素信號通路主要通過信號傳導及轉錄激活因子 3 依賴的方式直接激活原代肝細胞和 AML12 細胞中胎球蛋白 B 的轉錄和表達[29]。這一結果進一步支持了胎球蛋白 B 與內皮功能障礙可能相關,但具體機制尚未確切。
3.5 斑塊破裂
斑塊破裂可促使 CAD 進一步發展。就目前的研究已知,Smad2 和 Smad3 是細胞中響應 TGF-β 受體(TGF-β receptor, TGF-βR)的關鍵信號分子,其中胎球蛋白 B 與 TGF-βR 的相關蛋白在血管平滑肌細胞(vascular smooth muscle cell, VSMC)中相互結合。同時胎球蛋白 B 通過劑量依賴的方式提高 VSMC 中 Smad2 和 Smad3 的磷酸化信號水平,并可刺激胞質磷酸-Smad2 和胞質磷酸-Smad3 轉移至細胞核部分。纖溶酶原激活物抑制物 1(plasminogen activator inhibitor 1, PAI-1)和基質金屬蛋白酶-2(marix metalloproteinase-2, MMP-2)是 VSMC 中斑塊脆弱性的調節因子,胎球蛋白 B 可通過對 VSMC 中組蛋白脫乙酰酶 1 介導的啟動子區域表觀遺傳變化(其中包括組蛋白去乙酰基酶 1 和 RNA 聚合酶Ⅱ)進而誘導 PAI-1 和 MMP-2 上調。一方面,胎球蛋白 B 可通過 TGF-βR 介導的 Smad 途徑提高 VSMC 中斑塊易損性調節因子(PAI-1 和 MMP-2)的表達水平,進而降低血管斑塊穩定性,從而促使血管斑塊破裂的發生[7, 30]。血管斑塊破裂容易誘發 CAD 事件,同時也是心肌梗死常見誘發機制之一。另一方面,胎球蛋白 B 同樣具有抑制鈣化形成的作用。雖然胎球蛋白 B 抑制組織鈣化的能力不及同源蛋白(胎球蛋白 A),但其仍可抑制堿性磷酸鈣沉淀,與組織鈣化密切關聯,進一步增加斑塊破裂可能性,增加心血管事件發生概率[31]。而目前,胎球蛋白 B 與斑塊破裂的具體機制仍需進一步探索。
4 結語
綜上所述,胎球蛋白 B 在 CAD 的發生發展中扮演著重要角色。它是一種由肝臟分泌且具有多種功能的糖蛋白,可通過參與調控細胞炎癥、血管鈣化、脂質代謝、斑塊破裂等多個方面,進而與 CAD 聯系。雖然胎球蛋白 B 影響 CAD 發展的具體機制尚不完全清楚,甚至其在不同階段的 CAD 中的作用以及與其他心血管風險因素的相互作用也需要進一步研究,但不可否認,胎球蛋白 B 具有成為 CAD 發病風險生物標志物的潛力,未來隨著研究的不斷深入,胎球蛋白 B 可能對 CAD 的診斷、潛在治療靶點及預后評估提供新的思路。
利益沖突:所有作者聲明不存在利益沖突。
冠狀動脈疾病(coronary artery disease, CAD)是世界上影響人體健康最常見的心血管疾病[1]。CAD 是一種由多種因素導致的疾病,主要由冠狀動脈粥樣硬化引起。而冠狀動脈粥樣硬化是一個包含多種生理病理過程的疾病狀態,主要涉及脂質代謝、血栓形成、炎癥、內皮功能障礙、氧化應激等過程。并且在大量的普通人群之中,也有著導致 CAD 的多種危險因素,例如高血糖、高血壓、高血脂、慢性腎臟疾病、年老、吸煙、過胖、性別、高鹽高脂飲食及遺傳病史等[2]。因此通過識別與 CAD 發展相關的細胞因子,對于實現 CAD 的早期診斷和預防具有重要意義。肝臟分泌的多種細胞因子與 CAD 的發生及發展密切相關,這些細胞因子水平異常可能導致 CAD 的發生或進展。國外研究表明胎球蛋白 B 作為一種由肝臟分泌的糖蛋白,不僅在細胞炎癥反應中起到關鍵作用,還與血管鈣化過程、脂質代謝失衡以及斑塊穩定性等方面密切相關[3],這些過程都是 CAD 發病機制的重要組成部分。雖然胎球蛋白 B 在 CAD 中的具體作用尚未十分明確,但隨著研究的不斷深入,其或許可以為 CAD 的預防和診斷提供新選擇。因此,本文現就胎球蛋白 B 與 CAD 的研究進展作一綜述。
1 胎球蛋白 B
胎球蛋白是胎牛血清中含量最多的球蛋白,其構成了一組廣泛的肝源性血漿和基質蛋白,其中包括胎球蛋白 A(又稱 α2-Heremans-Schmid 糖蛋白)以及胎球蛋白 B,而胎球蛋白 B 作為胎球蛋白 A 的旁系同源物在 1999 年被 Olivier 等[4]發現。目前國外大量實驗已經表明胎球蛋白 A 可參與胰島素信號通路的調節,還具有作為異位鈣化抑制劑、蛋白酶抑制劑、炎癥介質、抗炎伴侶、致動脈粥樣硬化因子和成脂肪因子的作用[5]。隨著研究的進一步擴展,實驗表明胎球蛋白 A 與 CAD 的進程有著密不可分的關系[6]。而作為胎球蛋白 A 的旁系同源物,胎球蛋白 B 是否影響 CAD 的進展尚不完全清楚。
胎球蛋白 B 是一種復雜的多域蛋白質,由 382 個氨基酸組成,分子量達 60 kDa。這種蛋白質的結構特征在于含有 2 個串聯的胱抑素結構域,并通過二硫鍵結合。胎球蛋白 B 的編碼基因為 FETUB,該基因與胎球蛋白 A 的基因序列相似性達到 22%[7]。胎球蛋白 A 和胎球蛋白 B 具有相似的進化起源,在脊椎動物基因組中具有相近的染色體位置。具體來說,他們的編碼基因主要并排位于人類基因組的單個染色體區域(3q27)[5]。這就暗示胎球蛋白 B 可能與胎球蛋白 A 具有部分重疊但不完全相同的功能。胎球蛋白 B 可參與炎癥、鈣化與脂代謝等多個方面的調控,并且與內皮功能障礙和斑塊破裂密切相關。這些功能表明胎球蛋白 B 在 CAD 的發展中扮演著重要角色。
2 胎球蛋白 B 與 CAD 的關系
2.1 胎球蛋白 B 與動脈粥樣硬化
研究提示,血脂水平異常可以推進動脈粥樣硬化進程,而動脈粥樣硬化是多種心血管疾病發生的主要原因[8]。在這一背景下,有學者提出胎球蛋白 B 可能通過影響血脂水平,間接促進動脈粥樣硬化或其他心血管疾病的發展;進而為驗證這一假設,研究人員在一項針對家族性高膽固醇血癥(一種常見的遺傳性疾病,與早期 CAD 的增長有關)的動物實驗中,對動物樣品進行整體血漿蛋白質譜分析,結果顯示家族性高膽固醇血癥血清中胎球蛋白 B 水平顯著增加[8]。此外,國內學者在一項
2.2 胎球蛋白 B 與冠心病
冠心病是一種慢性免疫炎癥性纖維增生性疾病,大致可分為急性冠脈綜合征(acute coronary syndrome, ACS)和慢性冠脈綜合征(chronic coronary syndrome, CCS)[11]。其中 ACS 是冠心病的最重要階段,主要原因是動脈粥樣硬化斑塊破壞導致冠狀動脈部分或完全血栓性閉塞[12]。有研究發現胎球蛋白 B 可能與 ACS 密切相關[13-14]。有學者采用酶聯免疫吸附法檢測 87 例冠心病患者和 87 例健康對照組血清胎球蛋白 B 水平,結果顯示冠心病患者的血清胎球蛋白 B 水平明顯高于健康對照組[(90.7±32.1) vs. (110.0±32.7) μg/mL,P<0.001],且 ACS 組血清胎球蛋白 B 水平極高[(115.0±35.2) μg/mL)][13]。該實驗首次提出高水平的胎球蛋白 B 與冠心病存在獨立相關性。此外該實驗還發現在斑塊不穩定的急性心肌梗死(acute myocardial infarction, AMI)患者中,血清胎球蛋白 B 的表達發生了改變,這表明它可能與 AMI 的發展有關[13]。盡管胎球蛋白 B 參與冠心病的機制不完全明確,但實驗發現胎球蛋白 B 濃度與低密度脂蛋白膽固醇(low-density lipoprotein cholesterol, LDL-C)水平呈正相關,而 LDL-C 水平被認為是動脈粥樣硬化斑塊形成和發展的關鍵因素[14]。當 LDL-C 在內皮下滯留,它容易被活性氧氧化,進而導致內皮功能障礙,并誘發炎癥反應進而推進動脈粥樣硬化形成過程。因此,實驗推測胎球蛋白 B 可能通過其對炎癥的影響,部分參與冠心病的發展和進展[13]。此外,有學者通過一項回顧性研究發現,血清胎球蛋白 B 水平越高,冠心病患者的心血管事件發生風險越高(r=0.990,P<0.05);進一步將 ACS 組分為 AMI 組和不穩定型心絞痛組,結果顯示前者胎球蛋白 B 水平較后者明顯升高[15]。這些實驗結果顯示,胎球蛋白 B 可預測患者發生冠心病的風險。
心肌缺血一直被認為是 CCS 的重要因素[16]。胎球蛋白 B 可能通過影響心肌缺血與 CCS 相聯系。有學者通過一項動物研究構建心肌缺血模型,發現高水平的胎球蛋白 B 會提高小鼠心肌缺血易感性;此外,胎球蛋白 B 直接與胰島素受體 β 亞單位作用,抑制其酪氨酸位點和下游信號通路的磷酸化,從而增加心肌缺血易感性,該項實驗首次證實胎球蛋白 B 上調會導致心臟胰島素抵抗,并促使心肌缺血/再灌注損傷[17]。這些發現進一步證實了胎球蛋白 B 與 CCS 存在一定的相關性。
3 胎球蛋白 B 在 CAD 中的可能作用機制
胎球蛋白 B 促進動脈粥樣硬化的可能機制涉及脂質代謝、炎癥、血管鈣化、內皮功能障礙、斑塊破裂等(圖1)。
 圖1
胎球蛋白 B 促進動脈粥樣硬化的可能機制
圖1
胎球蛋白 B 促進動脈粥樣硬化的可能機制
Fetuin B:胎球蛋白 B;LDL:低密度脂蛋白;IL-17:白細胞介素-17;IL-6:白細胞介素-6;C3、C5:補體 C3、補體 C5;JAK:酪氨酸蛋白激酶;STAT:信號轉導與轉錄激活因子;ox-LDL:氧化型低密度脂蛋白;TGF-βR:轉化生長因子-β 受體;Smad:響應 TGF-βR 的一種關鍵信號分子;PAI-1:纖溶酶原激活物抑制物 1;MMP-2:基質金屬蛋白酶-2
3.1 脂質代謝
隨著對 CAD 研究的深入,有學者提出血脂異常是 CAD 的促發因素[18]。早期血脂異常可促使血管內皮細胞功能受損和通透性增加,使循環中的脂蛋白進入受損內膜區,加速氧化型低密度脂蛋白形成[19],加重或誘發動脈粥樣硬化。研究人員通過油紅 O 染色實驗表明,使用重組胎球蛋白 B 處理人肝細胞系 HepG2 細胞后,血脂含量顯著增加,而去除胎球蛋白 B 則 HepG2 細胞中的肝臟脂質積聚現象明顯減弱[20]。這表明胎球蛋白 B 可能會加重肝臟脂質積聚。研究還發現,胎球蛋白 B 可能通過減少抑制脂肪酸氧化的磷酸化腺苷酸活化蛋白激酶和激活上調脂肪生成肝臟 X 受體和甾醇調節元件結合轉錄因子 1 來參與脂質代謝[20]。此外,一項全基因組鑒定研究顯示,在非酒精性脂肪肝病患者中 FETUB 基因通過法尼醇 X 受體/類視黃醇 X 受體通路高表達[21]。然而,胎球蛋白 B 參與脂質代謝的確切機制仍需進一步研究證實。
3.2 炎癥
CAD 的發病機制和進展主要由炎癥驅動[22]。研究者觀察到胎球蛋白 B 主要被白色脂肪組織吸收,與胰島素抵抗有關[23]。此外,胎球蛋白 B 可以直接誘導脂肪細胞炎癥,并且通過對全 RNA 測序發現它與多個炎癥通路相關,包括白細胞介素-17 信號通路、白細胞介素-6 家族信號通路、補體 C3 和補體 C5 的激活、酪氨酸蛋白激酶信號轉導及轉錄激活因子信號通路等[23]。有研究提示胎球蛋白 B 過表達可通過激活小膠質細胞和核轉錄因子 κB 信號通路進而促進某些疾病的炎癥[24],但尚不能確定胎球蛋白 B 可通過這種途徑促進 CAD 炎癥。因此,目前仍無法清楚闡明胎球蛋白 B 參與 CAD 炎癥反應的確切分子機制。
3.3 血管鈣化
血管鈣化與 CAD 的病理過程密切相關,涉及復雜的病理生理機制,包括鈣和磷異常、鈣化和礦化抑制因子的丟失、血管平滑肌細胞向鈣化血管細胞的成骨轉化等[25]。近期研究表明,胎球蛋白 A 通過介導蛋白質-礦物質膠體的形成,促使網狀內皮系統快速清除蛋白質-礦物質膠體,防止礦物質異常沉淀,從而防止病理性礦化(鈣化)[26]。另外,胎球蛋白 A 具有富含鈣的礦物質和轉化生長因子-β(transforming growth factor β, TGF-β)超家族高親和力的結合位點,可抵消骨礦化所需的 TGF-β 超家族以及清除骨外區域的沉淀鈣,防止鈣鹽沉淀、血管鈣化,進而防止 CAD[5]。由于胎球蛋白 B 是胎球蛋白 A 的旁系同源物[8],有學者進行了沉淀抑制試驗,結果顯示胎球蛋白 B 可延緩血管鈣化進程,只是效果不如胎球蛋白 A[27]。這提示胎球蛋白 B 和血管鈣化有聯系,但是二者聯系的具體機制仍需要更加深入的研究。
3.4 內皮功能障礙
內皮細胞功能障礙是動脈粥樣硬化的早期病變之一[28],其中瘦素水平升高也是內皮功能障礙的危險因素。有研究發現肥胖患者血清胎球蛋白 B 水平與瘦素呈正相關,暗示胎球蛋白 B 可能與內皮功能障礙有關;并且瘦素信號通路主要通過信號傳導及轉錄激活因子 3 依賴的方式直接激活原代肝細胞和 AML12 細胞中胎球蛋白 B 的轉錄和表達[29]。這一結果進一步支持了胎球蛋白 B 與內皮功能障礙可能相關,但具體機制尚未確切。
3.5 斑塊破裂
斑塊破裂可促使 CAD 進一步發展。就目前的研究已知,Smad2 和 Smad3 是細胞中響應 TGF-β 受體(TGF-β receptor, TGF-βR)的關鍵信號分子,其中胎球蛋白 B 與 TGF-βR 的相關蛋白在血管平滑肌細胞(vascular smooth muscle cell, VSMC)中相互結合。同時胎球蛋白 B 通過劑量依賴的方式提高 VSMC 中 Smad2 和 Smad3 的磷酸化信號水平,并可刺激胞質磷酸-Smad2 和胞質磷酸-Smad3 轉移至細胞核部分。纖溶酶原激活物抑制物 1(plasminogen activator inhibitor 1, PAI-1)和基質金屬蛋白酶-2(marix metalloproteinase-2, MMP-2)是 VSMC 中斑塊脆弱性的調節因子,胎球蛋白 B 可通過對 VSMC 中組蛋白脫乙酰酶 1 介導的啟動子區域表觀遺傳變化(其中包括組蛋白去乙酰基酶 1 和 RNA 聚合酶Ⅱ)進而誘導 PAI-1 和 MMP-2 上調。一方面,胎球蛋白 B 可通過 TGF-βR 介導的 Smad 途徑提高 VSMC 中斑塊易損性調節因子(PAI-1 和 MMP-2)的表達水平,進而降低血管斑塊穩定性,從而促使血管斑塊破裂的發生[7, 30]。血管斑塊破裂容易誘發 CAD 事件,同時也是心肌梗死常見誘發機制之一。另一方面,胎球蛋白 B 同樣具有抑制鈣化形成的作用。雖然胎球蛋白 B 抑制組織鈣化的能力不及同源蛋白(胎球蛋白 A),但其仍可抑制堿性磷酸鈣沉淀,與組織鈣化密切關聯,進一步增加斑塊破裂可能性,增加心血管事件發生概率[31]。而目前,胎球蛋白 B 與斑塊破裂的具體機制仍需進一步探索。
4 結語
綜上所述,胎球蛋白 B 在 CAD 的發生發展中扮演著重要角色。它是一種由肝臟分泌且具有多種功能的糖蛋白,可通過參與調控細胞炎癥、血管鈣化、脂質代謝、斑塊破裂等多個方面,進而與 CAD 聯系。雖然胎球蛋白 B 影響 CAD 發展的具體機制尚不完全清楚,甚至其在不同階段的 CAD 中的作用以及與其他心血管風險因素的相互作用也需要進一步研究,但不可否認,胎球蛋白 B 具有成為 CAD 發病風險生物標志物的潛力,未來隨著研究的不斷深入,胎球蛋白 B 可能對 CAD 的診斷、潛在治療靶點及預后評估提供新的思路。
利益沖突:所有作者聲明不存在利益沖突。