引用本文: 俞銀賢, 易誠青, 馬金忠, 王秋根. 人工髖關節表面置換術治療股骨頭壞死療效觀察. 中國修復重建外科雜志, 2016, 30(2): 133-137. doi: 10.7507/1002-1892.20160027 復制
版權信息: ?四川大學華西醫院華西期刊社《中國修復重建外科雜志》版權所有,未經授權不得轉載、改編
人工全髖關節置換術(total hip arthroplasty,THA)是治療股骨頭壞死FicatⅢ期或Ⅳ期患者的金標準。但對于活動量大的中青年患者,因預期壽命較長,活動量大導致假體磨損碎屑產生的骨溶解可能更嚴重,假體松動發生率更高,因此這部分患者THA后翻修率增加,且嚴重骨溶解亦會增加翻修難度;另外,這部分患者若術中不能使用直徑達32 mm以上的大股骨頭假體,因術后運動量相對活躍,會增加脫位風險。因此針對這部分患者,如何在初次髖關節置換手術時降低上述風險具有重要意義。
人工髖關節表面置換術(hip resurfacing arthoplasty,HRA)可一定程度上降低上述風險,在中青年患者中具有優勢。骨關節炎患者初次HRA術后10年以上隨訪結果顯示臨床療效良好[1],但關于HRA治療股骨頭壞死的報道較少,目前對其療效尚不明確。現回顧性分析2008年1月-2009年4月于我院初次行HRA治療的FicatⅢ、Ⅳ期股骨頭壞死且年齡<60歲的中青年患者臨床資料,總結HRA治療中青年股骨頭壞死患者的臨床療效及術后并發癥發生情況。報告如下。
1 臨床資料
1.1 患者選擇標準
納入標準:①股骨頭壞死FicatⅢ期或Ⅳ期患者;②年齡<60歲;③體質量指數(body mass index,BMI)<35 kg/m2;④單側患病。排除標準:①雙側股骨頭壞死或對側有其他髖關節疾病,如類風濕性關節炎等;②患有其他任何可能影響全身骨骼肌肉系統的疾病。2008年1月-2009年4月我院共收治65例股骨頭壞死患者,其中34例符合選擇標準納入研究。
1.2 一般資料
本組男19例,女15例;年齡33~59歲,平均54歲。左髖16例,右髖18例。BMI 22~31 kg/m2,平均26.8 kg/m2。病因:酒精性9例,激素性8例,創傷性7例,不明原因10例。病程2~11年,平均5年。患者主要臨床表現為患髖疼痛,患髖活動受限,行走疼痛。術前行X線片、CT及MRI檢查,股骨頭壞死Ficat分期為Ⅲ期26例、Ⅳ期8例。
1.3 手術方法
手術均由同一組醫生完成。患者于全麻下取側臥位,采用后外側入路。先切開闊筋膜張肌和臀大肌,牽開臀中肌后切斷梨狀肌和外旋肌群,T形切開關節囊,將股骨頭脫位。測量股骨頭、頸直徑,選擇相應型號假體。沿股骨頸放置導引器,夾緊股骨頸,在導引器導引下按頸干角(140±5)°自股骨頭中軸打入導針,安裝測試器,調整導針確定在股骨頭中軸,以免造成股骨頭切割。沿導針用磨銼清除軟骨面和死骨。顯露髖臼,切除髖臼內軟組織,髖臼銼由小到大按照正常方向磨削髖臼,直至與選定的髖臼假體型號相匹配。最后在股骨頭上鉆數個直徑3 mm、深4 mm的孔道,徹底沖洗碎屑、凝血塊以及髓內脂肪,骨水泥固定假體后復位關節。本組所用假體為DuromTM髖關節表面置換系統假體(Zimmer公司,美國),股骨頭假體直徑40~48 mm,平均46?mm;髖臼直徑46~54 mm,平均50 mm。術后放置負壓引流管1根。
1.4 圍手術期處理
術后12 h后常規予以低分子肝素預防下肢深靜脈血栓形成,持續2周;術前2 h及術后2 d予以一代或二代頭孢類抗炎藥物預防感染。抬高患側肢體,術后36 h內拔除引流管。術后第2天即開始進行功能訓練,包括肌肉力量、關節活動度等。根據術中骨質情況與患者術后恢復情況決定下地時間,在助行器輔助下部分負重行走。
1.5 療效評價指標
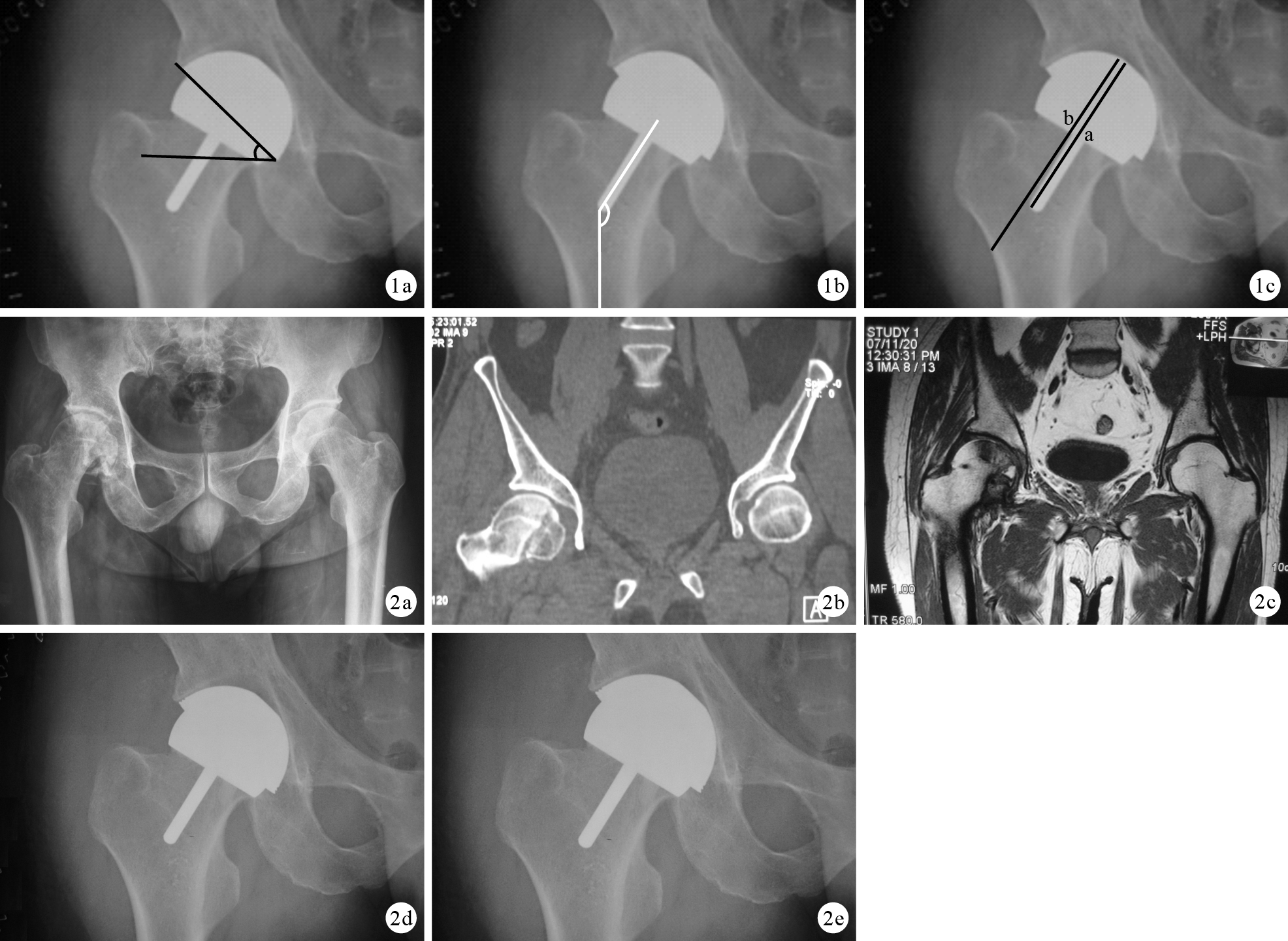
手術前后采用Harris髖關節評分系統(Harris hip score,HHS)和改良加州大學洛杉磯分校(UCLA)活動評分評估患者臨床效果。術后3 d及末次隨訪時攝X線片評估假體位置及是否發生松動,測量臼杯外展角,同時以頸干角(即股骨側假體柄和股骨干的夾角)評估假體內外翻情況;以股骨假體-股骨外側皮質長度比判斷術后有無股骨頭假體塌陷。見圖 1。
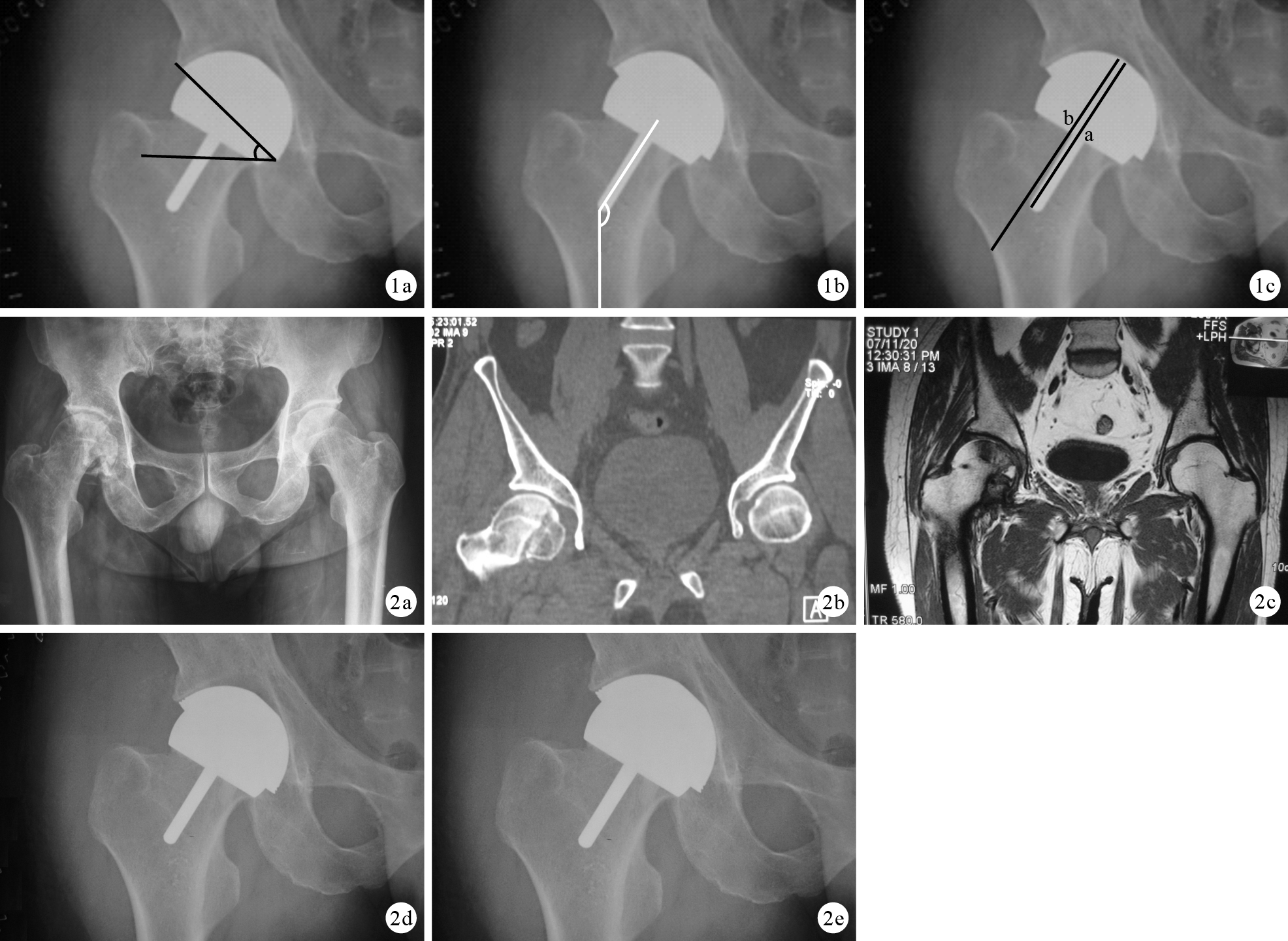 圖1
骨盆正位X線片上測量各指標 ?臼杯外展角 ?頸干角 ?股骨假體長度(a)與股骨外側皮質長度(b)比值 ? ?圖 2 患者,男,53歲,右側股骨頸骨折內固定術后發生股骨頭壞死(FicatⅢ期) ?術前X線片示右側股骨頭軟骨下骨不連續 ?術前CT示壞死區呈低密度影 ?術前MRI冠狀位T1WI加權像示股骨頭壞死區低信號 ?術后即刻X線片 ?術后6年X線片
Figure1.
Measurement of index on the anteroposterior X-ray film of pelvis ?Abduction angle ?Stem-shaft angle ?The ratio of the prosthesis length (a) to the length of lateral femoral cortex (b) ? ?Fig. 2 A 53-year-old male patient with right ONFH at Ficat stage III after internal fixation of femoral neck fracture ?X-ray film before operation,showing the discontinuity of the subchondral bone ?CT scan before operation,showing low density area in the right femoral head ?Coronal T1WI MRI image of both hips before operation,showing low signal intensity in the right femoral head ?X-ray film at immediate after operation ?X-ray film at 6 years after operation
圖1
骨盆正位X線片上測量各指標 ?臼杯外展角 ?頸干角 ?股骨假體長度(a)與股骨外側皮質長度(b)比值 ? ?圖 2 患者,男,53歲,右側股骨頸骨折內固定術后發生股骨頭壞死(FicatⅢ期) ?術前X線片示右側股骨頭軟骨下骨不連續 ?術前CT示壞死區呈低密度影 ?術前MRI冠狀位T1WI加權像示股骨頭壞死區低信號 ?術后即刻X線片 ?術后6年X線片
Figure1.
Measurement of index on the anteroposterior X-ray film of pelvis ?Abduction angle ?Stem-shaft angle ?The ratio of the prosthesis length (a) to the length of lateral femoral cortex (b) ? ?Fig. 2 A 53-year-old male patient with right ONFH at Ficat stage III after internal fixation of femoral neck fracture ?X-ray film before operation,showing the discontinuity of the subchondral bone ?CT scan before operation,showing low density area in the right femoral head ?Coronal T1WI MRI image of both hips before operation,showing low signal intensity in the right femoral head ?X-ray film at immediate after operation ?X-ray film at 6 years after operation
1.6 統計學方法
采用SPSS19.0統計軟件進行分析。數據以均數±標準差表示,各時間點間比較采用配對t檢驗;檢驗水準α=0.05。
2 結果
術后患者切口均Ⅰ期愈合,無切口感染、下肢深靜脈血栓形成等術后早期并發癥發生。術后32例患者獲隨訪,隨訪時間70~84個月,平均78個月。術后患髖疼痛明顯緩解,髖關節活動范圍達95~135°。隨訪期間均無假體松動、感染、股骨頸骨折、脫位及炎性假瘤等并發癥發生。末次隨訪時患者HHS評分和改良UCLA活動評分分別為(95.22±1.47)、(7.70±1.13)分,均顯著優于術前的(50.10±2.27)、(3.90±0.90)分,比較差異有統計學意義(t=1.510,P=0.008;t=0.830,P=0.003)。末次隨訪時患者臼杯外展角、頸干角及股骨假體-股骨外側皮質長度比分別為(51.4±2.3)°、(140.4±4.2)°、0.6±0.2,與術后3 d的(49.1±4.4)°、(138.7±5.6)°、0.6±0.1比較差異均無統計學意義(P>0.05)。見圖 2。
3 討論
HRA治療髖骨關節炎雖然取得了良好療效,但術后可能存在股骨頸骨折、血清金屬離子濃度升高等問題[2-5],HRA治療股骨頭壞死也存在爭議。中青年患者壽命長,對術后關節活動量要求高。因此,探討該技術在中青年股骨頭壞死患者中的運用具有重要意義。
3.1 HRA的臨床療效
HRA是金屬對金屬界面,耐磨損性高,關節活動度大,因此HRA具有較長假體生存率和良好臨床療效。Azam等[1]的一組244髖HRA術后平均隨訪12.05年的假體生存率為93.7%;Sandiford等[6]的前瞻性研究中,107例109髖HRA術后8年僅有7髖(6.4%)需要翻修,失敗病例主要是女性患者(6 例);Pailhe等[7]報道的平均年齡69.2歲的老年患者,HRA術后10年假體生存率仍有96.4%;Daniel等[8]的1 000髖大樣本研究顯示,HRA術后12年和15年的假體生存率分別為97.4%和95.8%。國內毛遠青等[9]發現HRA治療髖關節發育不良中期療效良好,術后髖關節功能評分較高、活動范圍較大。
對于活動量大的中青年患者,即使是年齡<30歲的患者,HRA術后同樣可取得良好臨床療效[10]。Matharu等[11]報道一組年齡14.9~49.9歲、平均41.5歲的患者,HRA術后14年假體生存率達94.1%。本組平均年齡54歲的患者末次隨訪時臨床療效良好,假體生存率100%,未見明顯假體松動、股骨頸骨折等并發癥。因為HRA保留了較多骨量,股骨頭假體直徑更大,術后活動范圍更廣,而且金屬對金屬界面耐磨損高,在中青年患者中具有很大優勢。
3.2 HRA在股骨頭壞死患者中的運用
雖然HRA具有較多優點,但其治療股骨頭壞死的療效尚不確切。本組平均年齡54歲的中青年股骨頭壞死患者,HRA術后平均隨訪78個月的HHS評分和改良UCLA活動評分均較術前明顯提高,這與國外一些研究相似。Yoo等[12]對185例術前MRI確診壞死范圍為11%~60%(平均42.7%)的股骨頭壞死患者行HRA治療后平均隨訪88個月,HHS評分和UCLA活動評分均明顯提高,無假體松動和翻修;Revell等[13]對73例股骨頭壞死范圍超過35%的患者行HRA并平均隨訪6.1年顯示假體生存率為93.2%;Chun等[14]對股骨頭壞死范圍超過50%的HRA患者術后平均隨訪88個月,HHS評分從術前平均77分提高至術后平均98分。
但Daniel等[15]對59例66髖平均年齡43.9歲的中青年股骨頭壞死患者行HRA,術后7.1年隨訪結果顯示失敗率高達7.6%,作者認為股骨頭壞死是HRA的一個相對禁忌證。Bose等[16]對96例股骨頭壞死患者行HRA,經術后平均5.4年隨訪發現有2例發生股骨頸骨折。部分學者研究了HRA術后股骨頸骨量的重塑變化,試圖解釋HRA術后股骨頸骨折的原因。Kohan等[17]研究了39例患者HRA術后6年的股骨頸直徑變化情況,以非手術側作為對照,其中82.7%患者發生股骨頸近端直徑變細,26.9%發生遠端變細;反之,則有17.3%和73.1%的患者分別發生股骨頸近端和遠端增寬。作者認為性別、BMI、假體尺寸和年齡并不影響術后骨重塑,骨重塑廣泛發生于股骨頸而不是局限于假體與股骨頸交界處。另外一項研究顯示,HRA術后3個月內會發生股骨頸變細,但之后會逐漸穩定,股骨頸過細在術后2年很少發生,也與股骨頸骨折無關[18]。因此HRA術后股骨頸骨折多發生在早期。因為股骨頭壞死因素的持續存在,股骨頭壞死患者HRA術后股骨頸骨折發生率可能更高[8]。本組患者術后平均隨訪78個月,未發生股骨頸骨折,這可能與正確選擇病例有關,即盡量避免選擇肥胖患者,同時應盡量選擇男性或絕經前女性,因絕經期女性容易發生骨質疏松,增加了術后骨折風險。
除術后發生股骨頸骨折外,近年來HRA術后血清金屬離子濃度升高也備受關注。雖然血清金屬離子濃度并不必然預測HRA失敗[19],但HRA術后金屬離子不良反應仍是翻修的主要原因之一[20]。Langton等[21]的研究顯示,血清鈷離子濃度是關節手術失敗的重要風險因素,血清鈷離子濃度升高超過2.5 μg/L則預示術后功能較差[22]。將HRA術后血清金屬離子濃度的常規監測和臨床結果結合起來,更有助于評估術后療效[4]。Sepp?nen等[23]認為假體的設計特點是決定術后血清金屬離子濃度的最重要因素,股骨頭直徑大小與此關系不大[24]。Savarino等[3]在一項隊列研究后指出,HRA術后血清金屬粒子濃度在個體之間差異較大,因此對中青年患者選擇HRA治療時需慎重。本組研究受條件所限,未進行血清金屬離子濃度的檢測,未能深入分析血清金屬離子濃度與臨床療效的直接關系,這是本研究的不足之處。但鑒于金屬離子可能存在的毒性,術前選擇患者時應排除腎功能不全患者。
為了提高手術成功率和減少術后并發癥,我們的體會是:①高度重視術前評估和選擇合適患者[25],尤其是學習曲線階段。肥胖是影響手術顯露和導致術后股骨頸骨折的重要因素,因此應選擇BMI值不高的患者,本組患者平均BMI為26.8 kg/m2。②需注意微創操作,因不截斷股骨頸,髖臼顯露可能比較困難,應注意保護股骨近端血供。③術中需注意觀察股骨頭囊性變范圍,若發現股骨頭囊腫范圍超過1?cm則建議改行THA,以降低術后股骨頸骨折風險。④術中可適當增加髖臼杯外展角,本組術后3?d臼杯外展角為(49.1±4.4)°。毛遠青等[9]認為將臼杯放置于外展角稍大的位置,能夠使假體有更多的骨性接觸和覆蓋,而且可使用相對更大的臼杯和股骨頭假體,減少術后失敗的危險因素,減少切割股骨頸從而降低骨折風險。
綜上述,HRA學習曲線陡峭、對技術要求較高,在該階段應盡量選擇男性或絕經前女性及BMI合適的患者,術前及術中需仔細評估股骨頭壞死范圍,術中注意保護組織并適當增加臼杯外展角。若能嚴格掌握HRA的手術適應證,HRA治療中青年股骨頭壞死能取得良好的中期結果。但本研究病例有限、隨訪時間不夠長,可能對結果有所影響,關于術后血清金屬離子濃度升高帶來的系列問題尚需要進一步跟蹤隨訪。
人工全髖關節置換術(total hip arthroplasty,THA)是治療股骨頭壞死FicatⅢ期或Ⅳ期患者的金標準。但對于活動量大的中青年患者,因預期壽命較長,活動量大導致假體磨損碎屑產生的骨溶解可能更嚴重,假體松動發生率更高,因此這部分患者THA后翻修率增加,且嚴重骨溶解亦會增加翻修難度;另外,這部分患者若術中不能使用直徑達32 mm以上的大股骨頭假體,因術后運動量相對活躍,會增加脫位風險。因此針對這部分患者,如何在初次髖關節置換手術時降低上述風險具有重要意義。
人工髖關節表面置換術(hip resurfacing arthoplasty,HRA)可一定程度上降低上述風險,在中青年患者中具有優勢。骨關節炎患者初次HRA術后10年以上隨訪結果顯示臨床療效良好[1],但關于HRA治療股骨頭壞死的報道較少,目前對其療效尚不明確。現回顧性分析2008年1月-2009年4月于我院初次行HRA治療的FicatⅢ、Ⅳ期股骨頭壞死且年齡<60歲的中青年患者臨床資料,總結HRA治療中青年股骨頭壞死患者的臨床療效及術后并發癥發生情況。報告如下。
1 臨床資料
1.1 患者選擇標準
納入標準:①股骨頭壞死FicatⅢ期或Ⅳ期患者;②年齡<60歲;③體質量指數(body mass index,BMI)<35 kg/m2;④單側患病。排除標準:①雙側股骨頭壞死或對側有其他髖關節疾病,如類風濕性關節炎等;②患有其他任何可能影響全身骨骼肌肉系統的疾病。2008年1月-2009年4月我院共收治65例股骨頭壞死患者,其中34例符合選擇標準納入研究。
1.2 一般資料
本組男19例,女15例;年齡33~59歲,平均54歲。左髖16例,右髖18例。BMI 22~31 kg/m2,平均26.8 kg/m2。病因:酒精性9例,激素性8例,創傷性7例,不明原因10例。病程2~11年,平均5年。患者主要臨床表現為患髖疼痛,患髖活動受限,行走疼痛。術前行X線片、CT及MRI檢查,股骨頭壞死Ficat分期為Ⅲ期26例、Ⅳ期8例。
1.3 手術方法
手術均由同一組醫生完成。患者于全麻下取側臥位,采用后外側入路。先切開闊筋膜張肌和臀大肌,牽開臀中肌后切斷梨狀肌和外旋肌群,T形切開關節囊,將股骨頭脫位。測量股骨頭、頸直徑,選擇相應型號假體。沿股骨頸放置導引器,夾緊股骨頸,在導引器導引下按頸干角(140±5)°自股骨頭中軸打入導針,安裝測試器,調整導針確定在股骨頭中軸,以免造成股骨頭切割。沿導針用磨銼清除軟骨面和死骨。顯露髖臼,切除髖臼內軟組織,髖臼銼由小到大按照正常方向磨削髖臼,直至與選定的髖臼假體型號相匹配。最后在股骨頭上鉆數個直徑3 mm、深4 mm的孔道,徹底沖洗碎屑、凝血塊以及髓內脂肪,骨水泥固定假體后復位關節。本組所用假體為DuromTM髖關節表面置換系統假體(Zimmer公司,美國),股骨頭假體直徑40~48 mm,平均46?mm;髖臼直徑46~54 mm,平均50 mm。術后放置負壓引流管1根。
1.4 圍手術期處理
術后12 h后常規予以低分子肝素預防下肢深靜脈血栓形成,持續2周;術前2 h及術后2 d予以一代或二代頭孢類抗炎藥物預防感染。抬高患側肢體,術后36 h內拔除引流管。術后第2天即開始進行功能訓練,包括肌肉力量、關節活動度等。根據術中骨質情況與患者術后恢復情況決定下地時間,在助行器輔助下部分負重行走。
1.5 療效評價指標
手術前后采用Harris髖關節評分系統(Harris hip score,HHS)和改良加州大學洛杉磯分校(UCLA)活動評分評估患者臨床效果。術后3 d及末次隨訪時攝X線片評估假體位置及是否發生松動,測量臼杯外展角,同時以頸干角(即股骨側假體柄和股骨干的夾角)評估假體內外翻情況;以股骨假體-股骨外側皮質長度比判斷術后有無股骨頭假體塌陷。見圖 1。
 圖1
骨盆正位X線片上測量各指標 ?臼杯外展角 ?頸干角 ?股骨假體長度(a)與股骨外側皮質長度(b)比值 ? ?圖 2 患者,男,53歲,右側股骨頸骨折內固定術后發生股骨頭壞死(FicatⅢ期) ?術前X線片示右側股骨頭軟骨下骨不連續 ?術前CT示壞死區呈低密度影 ?術前MRI冠狀位T1WI加權像示股骨頭壞死區低信號 ?術后即刻X線片 ?術后6年X線片
Figure1.
Measurement of index on the anteroposterior X-ray film of pelvis ?Abduction angle ?Stem-shaft angle ?The ratio of the prosthesis length (a) to the length of lateral femoral cortex (b) ? ?Fig. 2 A 53-year-old male patient with right ONFH at Ficat stage III after internal fixation of femoral neck fracture ?X-ray film before operation,showing the discontinuity of the subchondral bone ?CT scan before operation,showing low density area in the right femoral head ?Coronal T1WI MRI image of both hips before operation,showing low signal intensity in the right femoral head ?X-ray film at immediate after operation ?X-ray film at 6 years after operation
圖1
骨盆正位X線片上測量各指標 ?臼杯外展角 ?頸干角 ?股骨假體長度(a)與股骨外側皮質長度(b)比值 ? ?圖 2 患者,男,53歲,右側股骨頸骨折內固定術后發生股骨頭壞死(FicatⅢ期) ?術前X線片示右側股骨頭軟骨下骨不連續 ?術前CT示壞死區呈低密度影 ?術前MRI冠狀位T1WI加權像示股骨頭壞死區低信號 ?術后即刻X線片 ?術后6年X線片
Figure1.
Measurement of index on the anteroposterior X-ray film of pelvis ?Abduction angle ?Stem-shaft angle ?The ratio of the prosthesis length (a) to the length of lateral femoral cortex (b) ? ?Fig. 2 A 53-year-old male patient with right ONFH at Ficat stage III after internal fixation of femoral neck fracture ?X-ray film before operation,showing the discontinuity of the subchondral bone ?CT scan before operation,showing low density area in the right femoral head ?Coronal T1WI MRI image of both hips before operation,showing low signal intensity in the right femoral head ?X-ray film at immediate after operation ?X-ray film at 6 years after operation
1.6 統計學方法
采用SPSS19.0統計軟件進行分析。數據以均數±標準差表示,各時間點間比較采用配對t檢驗;檢驗水準α=0.05。
2 結果
術后患者切口均Ⅰ期愈合,無切口感染、下肢深靜脈血栓形成等術后早期并發癥發生。術后32例患者獲隨訪,隨訪時間70~84個月,平均78個月。術后患髖疼痛明顯緩解,髖關節活動范圍達95~135°。隨訪期間均無假體松動、感染、股骨頸骨折、脫位及炎性假瘤等并發癥發生。末次隨訪時患者HHS評分和改良UCLA活動評分分別為(95.22±1.47)、(7.70±1.13)分,均顯著優于術前的(50.10±2.27)、(3.90±0.90)分,比較差異有統計學意義(t=1.510,P=0.008;t=0.830,P=0.003)。末次隨訪時患者臼杯外展角、頸干角及股骨假體-股骨外側皮質長度比分別為(51.4±2.3)°、(140.4±4.2)°、0.6±0.2,與術后3 d的(49.1±4.4)°、(138.7±5.6)°、0.6±0.1比較差異均無統計學意義(P>0.05)。見圖 2。
3 討論
HRA治療髖骨關節炎雖然取得了良好療效,但術后可能存在股骨頸骨折、血清金屬離子濃度升高等問題[2-5],HRA治療股骨頭壞死也存在爭議。中青年患者壽命長,對術后關節活動量要求高。因此,探討該技術在中青年股骨頭壞死患者中的運用具有重要意義。
3.1 HRA的臨床療效
HRA是金屬對金屬界面,耐磨損性高,關節活動度大,因此HRA具有較長假體生存率和良好臨床療效。Azam等[1]的一組244髖HRA術后平均隨訪12.05年的假體生存率為93.7%;Sandiford等[6]的前瞻性研究中,107例109髖HRA術后8年僅有7髖(6.4%)需要翻修,失敗病例主要是女性患者(6 例);Pailhe等[7]報道的平均年齡69.2歲的老年患者,HRA術后10年假體生存率仍有96.4%;Daniel等[8]的1 000髖大樣本研究顯示,HRA術后12年和15年的假體生存率分別為97.4%和95.8%。國內毛遠青等[9]發現HRA治療髖關節發育不良中期療效良好,術后髖關節功能評分較高、活動范圍較大。
對于活動量大的中青年患者,即使是年齡<30歲的患者,HRA術后同樣可取得良好臨床療效[10]。Matharu等[11]報道一組年齡14.9~49.9歲、平均41.5歲的患者,HRA術后14年假體生存率達94.1%。本組平均年齡54歲的患者末次隨訪時臨床療效良好,假體生存率100%,未見明顯假體松動、股骨頸骨折等并發癥。因為HRA保留了較多骨量,股骨頭假體直徑更大,術后活動范圍更廣,而且金屬對金屬界面耐磨損高,在中青年患者中具有很大優勢。
3.2 HRA在股骨頭壞死患者中的運用
雖然HRA具有較多優點,但其治療股骨頭壞死的療效尚不確切。本組平均年齡54歲的中青年股骨頭壞死患者,HRA術后平均隨訪78個月的HHS評分和改良UCLA活動評分均較術前明顯提高,這與國外一些研究相似。Yoo等[12]對185例術前MRI確診壞死范圍為11%~60%(平均42.7%)的股骨頭壞死患者行HRA治療后平均隨訪88個月,HHS評分和UCLA活動評分均明顯提高,無假體松動和翻修;Revell等[13]對73例股骨頭壞死范圍超過35%的患者行HRA并平均隨訪6.1年顯示假體生存率為93.2%;Chun等[14]對股骨頭壞死范圍超過50%的HRA患者術后平均隨訪88個月,HHS評分從術前平均77分提高至術后平均98分。
但Daniel等[15]對59例66髖平均年齡43.9歲的中青年股骨頭壞死患者行HRA,術后7.1年隨訪結果顯示失敗率高達7.6%,作者認為股骨頭壞死是HRA的一個相對禁忌證。Bose等[16]對96例股骨頭壞死患者行HRA,經術后平均5.4年隨訪發現有2例發生股骨頸骨折。部分學者研究了HRA術后股骨頸骨量的重塑變化,試圖解釋HRA術后股骨頸骨折的原因。Kohan等[17]研究了39例患者HRA術后6年的股骨頸直徑變化情況,以非手術側作為對照,其中82.7%患者發生股骨頸近端直徑變細,26.9%發生遠端變細;反之,則有17.3%和73.1%的患者分別發生股骨頸近端和遠端增寬。作者認為性別、BMI、假體尺寸和年齡并不影響術后骨重塑,骨重塑廣泛發生于股骨頸而不是局限于假體與股骨頸交界處。另外一項研究顯示,HRA術后3個月內會發生股骨頸變細,但之后會逐漸穩定,股骨頸過細在術后2年很少發生,也與股骨頸骨折無關[18]。因此HRA術后股骨頸骨折多發生在早期。因為股骨頭壞死因素的持續存在,股骨頭壞死患者HRA術后股骨頸骨折發生率可能更高[8]。本組患者術后平均隨訪78個月,未發生股骨頸骨折,這可能與正確選擇病例有關,即盡量避免選擇肥胖患者,同時應盡量選擇男性或絕經前女性,因絕經期女性容易發生骨質疏松,增加了術后骨折風險。
除術后發生股骨頸骨折外,近年來HRA術后血清金屬離子濃度升高也備受關注。雖然血清金屬離子濃度并不必然預測HRA失敗[19],但HRA術后金屬離子不良反應仍是翻修的主要原因之一[20]。Langton等[21]的研究顯示,血清鈷離子濃度是關節手術失敗的重要風險因素,血清鈷離子濃度升高超過2.5 μg/L則預示術后功能較差[22]。將HRA術后血清金屬離子濃度的常規監測和臨床結果結合起來,更有助于評估術后療效[4]。Sepp?nen等[23]認為假體的設計特點是決定術后血清金屬離子濃度的最重要因素,股骨頭直徑大小與此關系不大[24]。Savarino等[3]在一項隊列研究后指出,HRA術后血清金屬粒子濃度在個體之間差異較大,因此對中青年患者選擇HRA治療時需慎重。本組研究受條件所限,未進行血清金屬離子濃度的檢測,未能深入分析血清金屬離子濃度與臨床療效的直接關系,這是本研究的不足之處。但鑒于金屬離子可能存在的毒性,術前選擇患者時應排除腎功能不全患者。
為了提高手術成功率和減少術后并發癥,我們的體會是:①高度重視術前評估和選擇合適患者[25],尤其是學習曲線階段。肥胖是影響手術顯露和導致術后股骨頸骨折的重要因素,因此應選擇BMI值不高的患者,本組患者平均BMI為26.8 kg/m2。②需注意微創操作,因不截斷股骨頸,髖臼顯露可能比較困難,應注意保護股骨近端血供。③術中需注意觀察股骨頭囊性變范圍,若發現股骨頭囊腫范圍超過1?cm則建議改行THA,以降低術后股骨頸骨折風險。④術中可適當增加髖臼杯外展角,本組術后3?d臼杯外展角為(49.1±4.4)°。毛遠青等[9]認為將臼杯放置于外展角稍大的位置,能夠使假體有更多的骨性接觸和覆蓋,而且可使用相對更大的臼杯和股骨頭假體,減少術后失敗的危險因素,減少切割股骨頸從而降低骨折風險。
綜上述,HRA學習曲線陡峭、對技術要求較高,在該階段應盡量選擇男性或絕經前女性及BMI合適的患者,術前及術中需仔細評估股骨頭壞死范圍,術中注意保護組織并適當增加臼杯外展角。若能嚴格掌握HRA的手術適應證,HRA治療中青年股骨頭壞死能取得良好的中期結果。但本研究病例有限、隨訪時間不夠長,可能對結果有所影響,關于術后血清金屬離子濃度升高帶來的系列問題尚需要進一步跟蹤隨訪。