引用本文: 劉鋅, 陳浩, 薛鵬, 席洪鐘, 何帥, 孫光權, 杜斌. 基于CT影像組學和臨床資料可視量化評估非血管化植骨的保髖療效. 中國修復重建外科雜志, 2023, 37(7): 846-855. doi: 10.7507/1002-1892.202303072 復制
版權信息: ?四川大學華西醫院華西期刊社《中國修復重建外科雜志》版權所有,未經授權不得轉載、改編
股骨頭壞死(osteonecrosis of the femoral head,ONFH)是一種起病隱匿、進展迅速的功能毀滅性疾病[1],一旦進展到股骨頭塌陷、髖關節炎等ONFH晚期,人工全髖關節置換術(total hip arthroplasty,THA)將成為患者唯一治療手段[2-3]。然而,過早接受THA將面臨手術相關并發癥和假體耐久性不足等問題[4]。因此,對于中青年患者,在ONFH早期選擇合適保髖手術以保留股骨頭并延遲初次置換時間,具有重要臨床意義[2-3,5]。但是相對于THA,保髖手術療效不確切,不同術式間的保髖成功率存在差異[6-8],相當一部分患者保髖術后早期即發生失敗,無疑增加了時間和經濟成本。因此,如何在術前預測保髖手術療效、評估患者是否適合保髖手術,進而選擇合理保髖策略,以降低術后股骨頭塌陷風險、提高保髖成功率,逐漸成為保髖研究領域的新焦點。
目前,保髖策略需要綜合考慮患者的臨床癥狀、體征及影像學資料,其中髖關節CT能較為準確顯示壞死區大小、硬化帶范圍等信息[9-10],是臨床制定治療方案的重要參考依據[11]。但是,不同醫生對壞死分期、部位及范圍的診斷存在主觀差異,并且大量深層次影像信息難以通過肉眼直接主觀提取、量化和充分利用。隨著醫學人工智能技術的飛速發展,“影像組學”的概念逐漸興起,作為一種新興的醫學影像方法[12],它通過使用算法或統計分析工具從診斷圖像中捕獲目標區域的明顯表型差異,所提取出的影像學特征可以提供肉眼分析之外的大量信息,能敏感地確定不同部位間形態和功能的微妙異質性,因此在診斷和預后預測領域得到廣泛應用[13-15]。然而,既往將影像組學應用于骨科尤其是保髖領域的相關研究較少。
本研究以非血管化植骨(non-vascularized bone grafting,NVBG)這一經典保髖術式為例,嘗試應用影像組學方法提取患者的CT影像學特征,與臨床資料相結合,構建一種可視量化且有效的保髖策略評估方法,以期為治療方案的制定提供參考。
1 資料與方法
1.1 研究對象
納入標準:① 經術中病理證實為ONFH;② 采用NVBG進行保髖治療;③ 無其他保髖手術治療史;④ 隨訪時間3年以上且隨訪資料完整。排除標準:① 未遵術后3個月內免負重醫囑、提前下地負重者;② CT圖像質量較差,無法進行影像組學分析者。
根據納排標準,篩選2009年6月—2019年6月于南京中醫藥大學附屬醫院接受NVBG進行保髖治療的153例(182髖)ONFH患者納入研究,按7∶3比例隨機分為訓練集(130髖)和測試集(52髖)。兩組患者性別、年齡、身體質量指數(body mass index,BMI)、病程、患側側別、病因、是否繼續接觸致病因素、國際骨循環協會(ARCO)分期、日本骨壞死研究會(JIC)分型以及術前Harris評分、ALP、D-二聚體(D-dimer,D-D)、中性粒細胞(nutrophils,NEUT)百分比、α-L-巖藻糖苷酶(α-L-fucosidase,AFU)等基線資料比較差異均無統計學意義(P>0.05)。見表1。
1.2 實驗方法
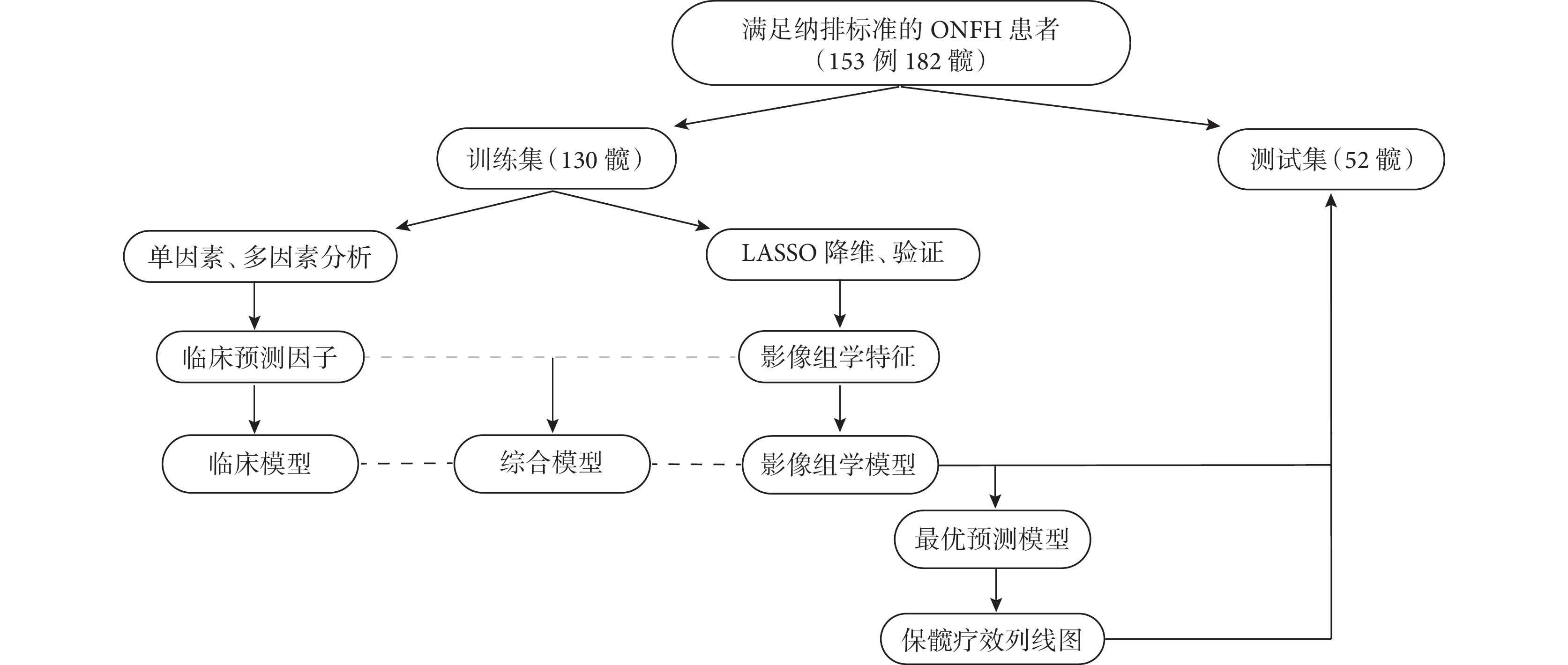
將術后行THA或髖關節出現明顯疼痛和活動受限、術后Harris評分<90分及影像學出現股骨頭進行性塌陷設為生存終點;根據術后3年隨訪時是否出現上述結果定義保髖成敗。以2022年6月作為隨訪終點,計算術側股骨頭生存率和生存時間,采用Kaplan-Meier生存曲線進行分析。本研究流程圖見圖1。
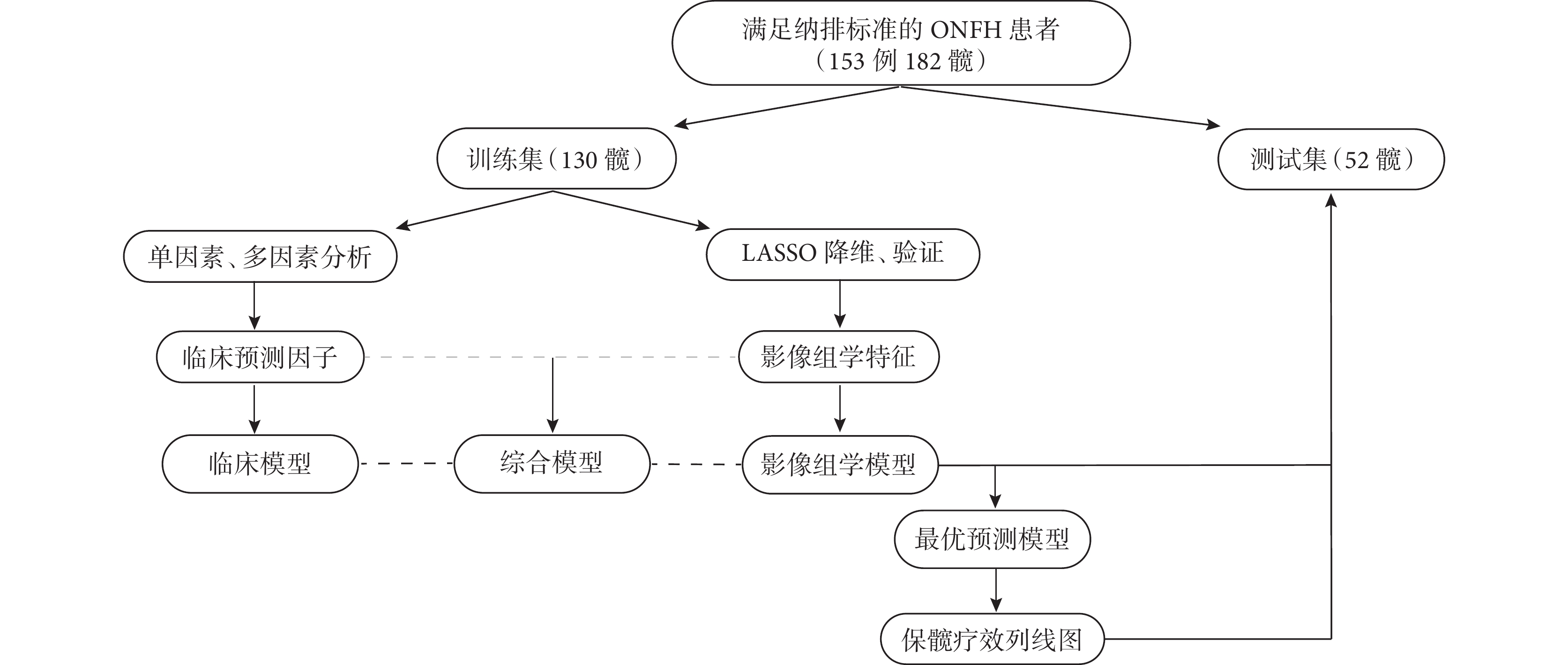 圖1
研究流程圖
Figure1.
Flowchart of the study
圖1
研究流程圖
Figure1.
Flowchart of the study
1.2.1 病灶分割及影像學特征提取
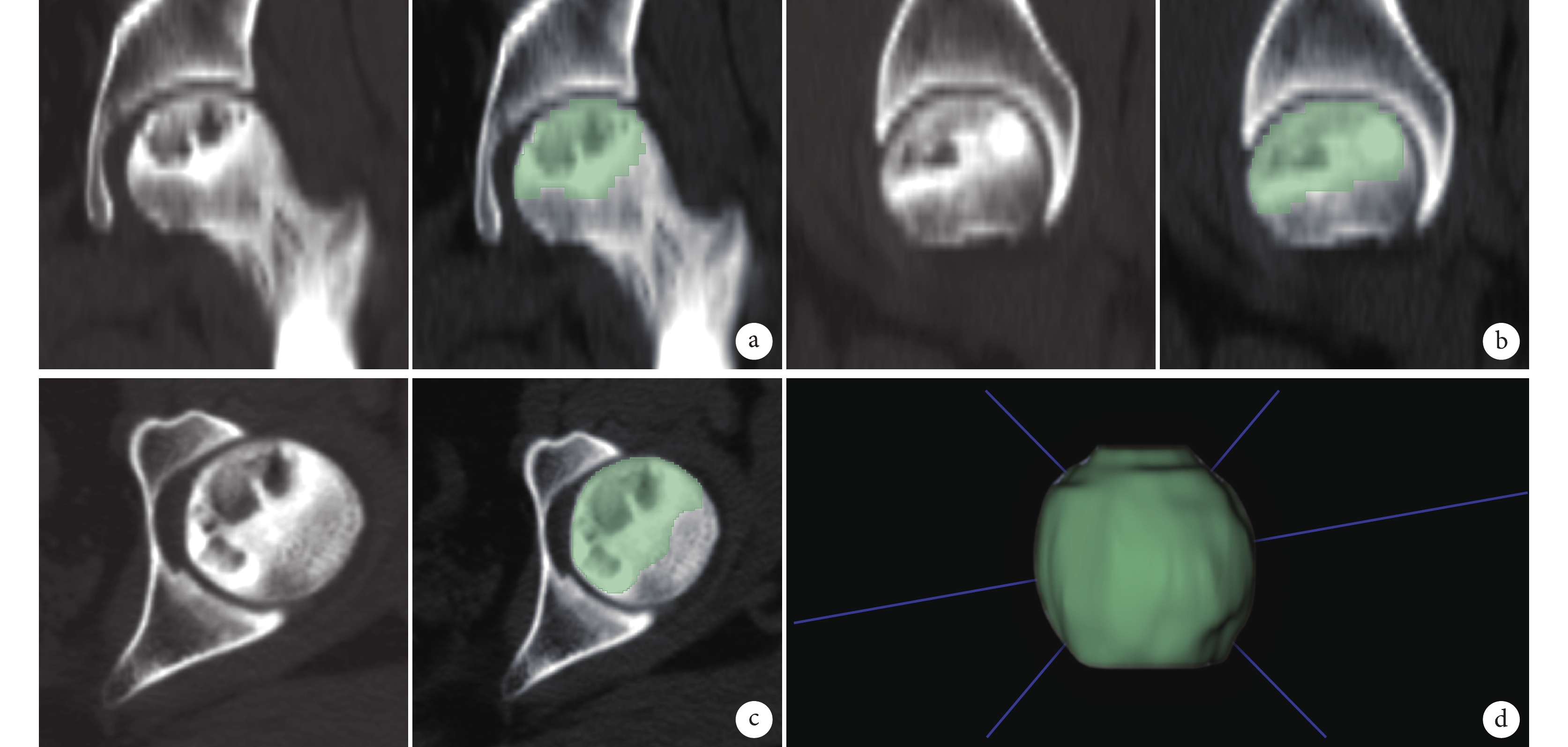
所有患者術前均接受雙髖關節CT平掃(荷蘭飛利浦公司128排Brilliance CT或美國通用公司64排LightSpeed VCT),從PCAS系統中獲取圖像。掃描參數:管電壓120~140 kV,管電流220~680 mA,曝光時間250~800 ms,層厚1.0~3.0 mm,層間距1.0~3.0 mm,重建矩陣512×512。將CT圖像以DICOM格式導入免費開放獲取的軟件3D Slicer(https://www.slicer.org,V5.0.2)中,按照1 mm×1 mm×1 mm體素大小、1~64灰度值進行標準化處理。將股骨頭星芒征缺失、負重區骨小梁缺失斷裂及硬化帶包繞囊變區等密度異常的壞死區域定義為感興趣區(region of interesting,ROI)。首先由1名具有10年以上工作經驗的影像科醫師,于骨窗(窗寬1 500 HU,窗位400 U)手動分割勾勒冠狀位、矢狀位和軸位的ROI;再由1名高年資ONFH專科醫師加以修正,最終生成三維ROI(圖2)。使用“Pyradiomics”插件對每個ROI進行影像組學特征提取,該插件能自動從每個ROI中提取851個特征值,包括18個直方圖強度特征、14個形狀特征、75個紋理特征(24個灰度共生矩陣、14個灰度依賴矩陣、16個灰度行程矩陣、16個灰度區域大小矩陣、5個鄰域灰度差矩陣)和744個小波特征,所有提取的影像學特征值均進行Z-score標準化。
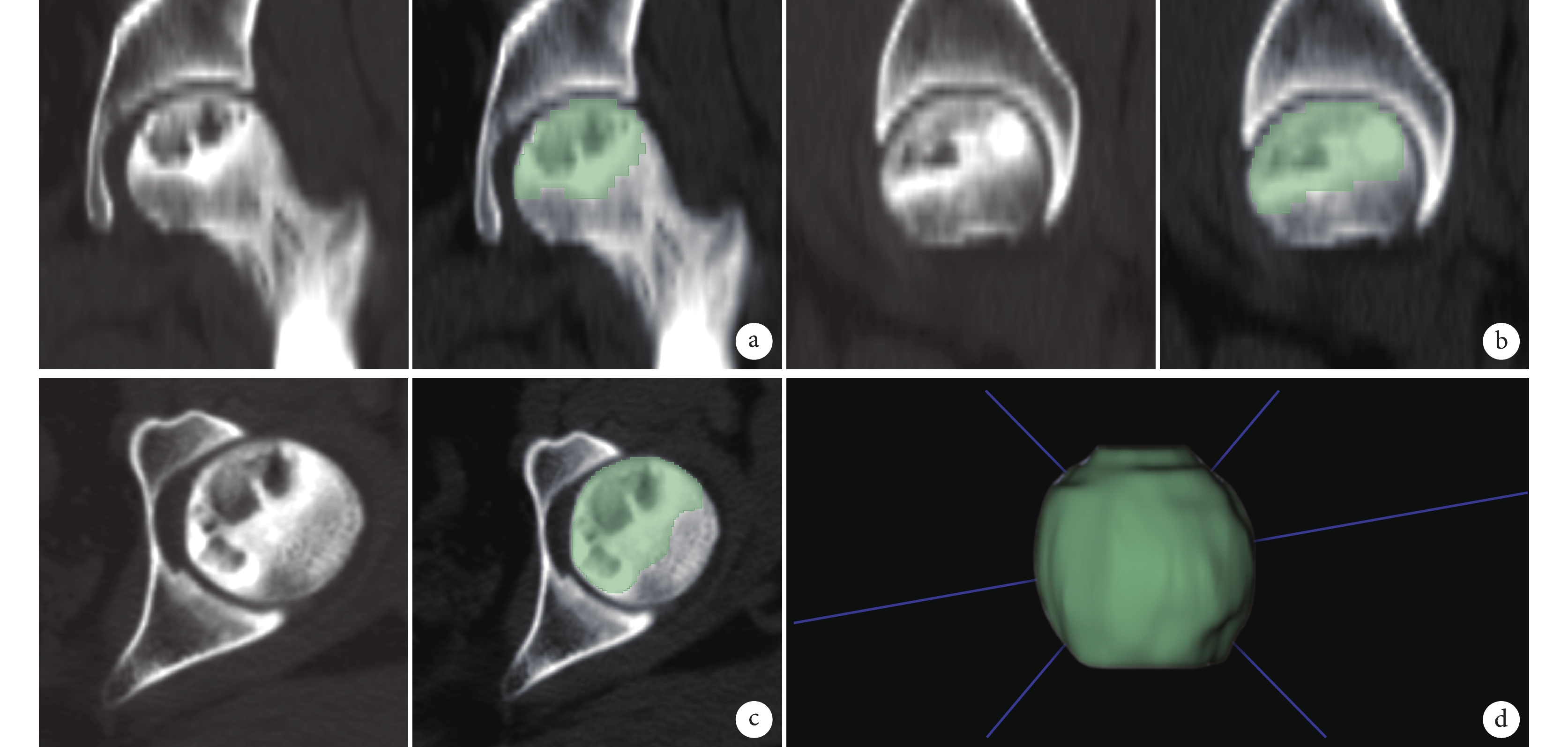 圖2
于CT圖像骨窗手動勾畫壞死區ROI示意圖
圖2
于CT圖像骨窗手動勾畫壞死區ROI示意圖
a~c. 冠狀位、矢狀位、軸位骨窗CT圖;d. 生成的壞死區三維ROI
Figure2. Schematic diagram of ROI segmented and outlined by manual mode in the bone window of CT imagesa-c. CT images in the bone window in coronal, sagittal, and axial positions; d. Three-dimensional ROI of necrotic area generated from them
1.2.2 特征篩選
對患者的臨床資料和影像組學特征進行降維和篩選。在訓練集中,使用“glmnet”軟件包進行最小絕對收縮和選擇算子(least absolute shrinkage and selection operator,LASSO)回歸降維,通過十折交叉驗證確定最優log(λ)以篩選影像組學特征,根據篩選出的特征所對應的LASSO權重系數構建影像組學標簽,并計算所有患髖的影像組學評分(Rad-scores);收集并記錄文獻報道中與保髖療效相關的風險因素,使用單因素、多因素Cox回歸分析從中篩選臨床預測因子,使用“survminer”軟件包進行Cox回歸分析,評價影像組學評分和臨床預測因子的價值。
1.2.3 保髖決策模型的構建與評價
根據所提取的特征,以保髖成敗作為結局變量,在訓練集中分別構建3種保髖決策模型。根據患者的Rad-scores構建保髖療效的影像組學模型,使用臨床預測因子構建臨床模型,使用臨床預測因子和Rad-scores聯合構建綜合模型。在訓練集及測試集中對3種模型的預測效能進行評價、驗證,使用“pROC”軟件包繪制3種模型的受試者工作特征(receiver operating characteristic curve,ROC)曲線,計算曲線下面積(area under curve,AUC),采用DeLong檢驗比較AUC,根據C-index、敏感度、特異度和校準曲線評估各模型的性能。為了給臨床醫生提供一種保髖決策的定量工具,以預測術后股骨頭的生存概率,使用“rms”和“hdnom”軟件包構建列線圖對最佳模型進行可視化,并使用“rmda”和“ggDCA”軟件包繪制決策曲線分析該列線圖的臨床效用。
1.3 統計學方法
采用SPSS26.0、R軟件(版本號 4.1.2)和RStudio軟件(版本號1.2.5042)進行分析。計量資料行正態性檢驗,符合正態分布的數據以均數±標準差表示,訓練集和測試集間比較采用獨立樣本t檢驗;不符合正態分布的數據以M(Q1,Q3)表示,組間比較采用Mann-Whitney U檢驗;計數資料組間比較采用χ2檢驗。檢驗水準取雙側α=0.05。
2 結果
2.1 隨訪結果
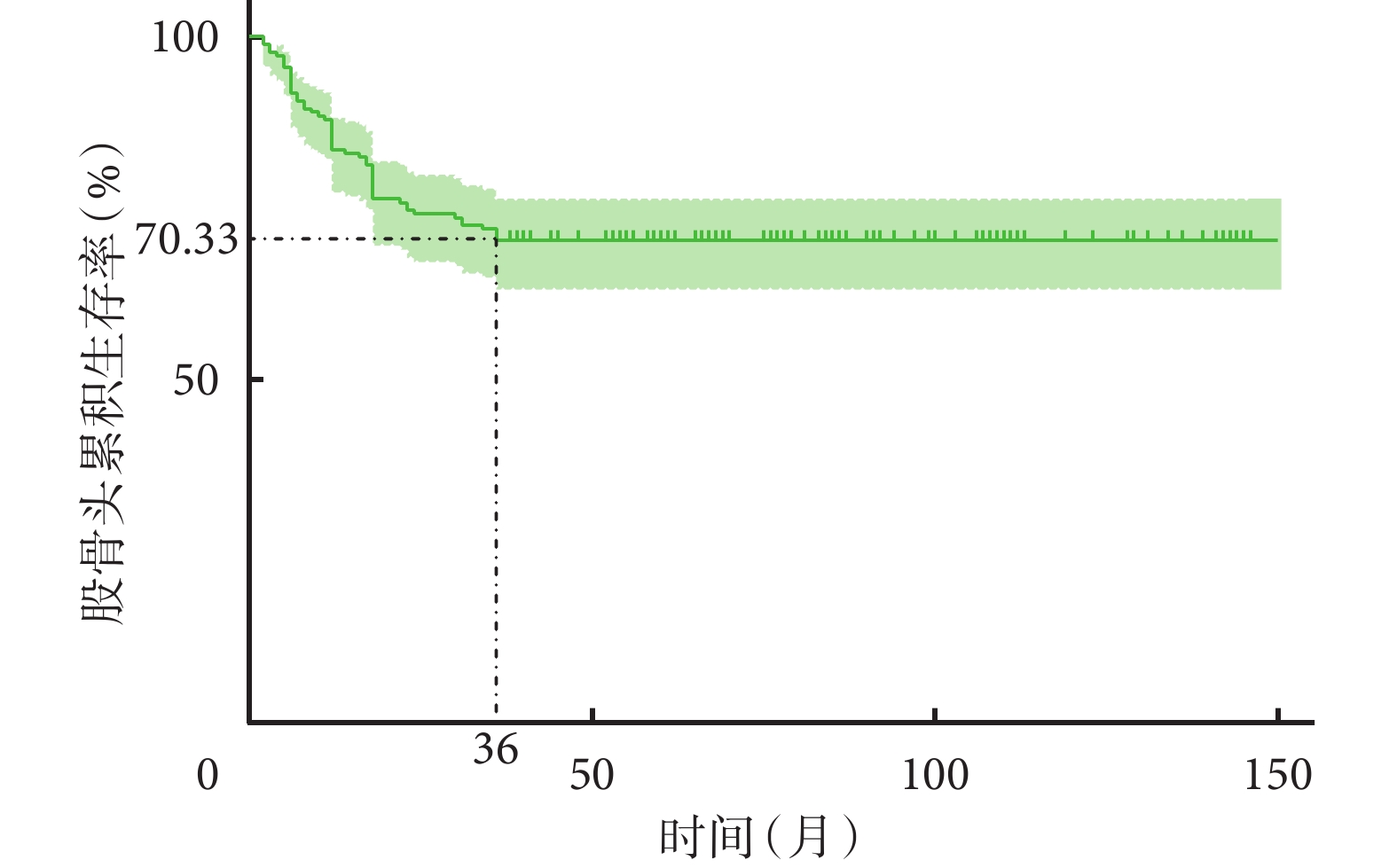
術后3年隨訪時,128髖功能良好,未進行關節置換,保髖成功率為70.33%; Kaplan-Meier生存曲線示,36個月后股骨頭生存率基本穩定。末次隨訪時120髖保髖成功,保髖成功率65.93%,生存時間(65.56±43.27)個月。見圖3。
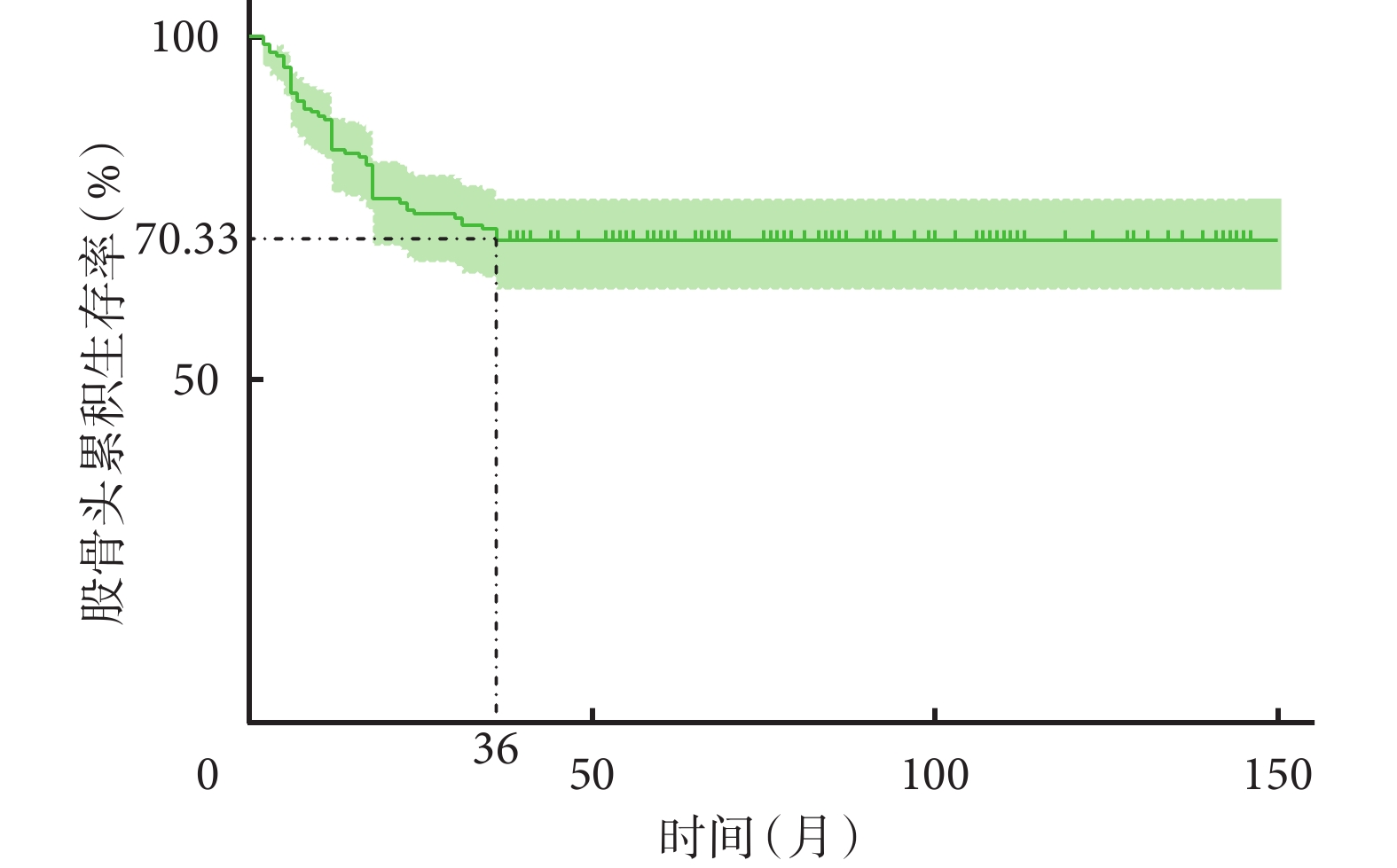 圖3
股骨頭生存率的Kaplan-Meier曲線分析
Figure3.
Kaplan-Meier curve analysis of the survival rate of femoral head
圖3
股骨頭生存率的Kaplan-Meier曲線分析
Figure3.
Kaplan-Meier curve analysis of the survival rate of femoral head
2.2 特征篩選
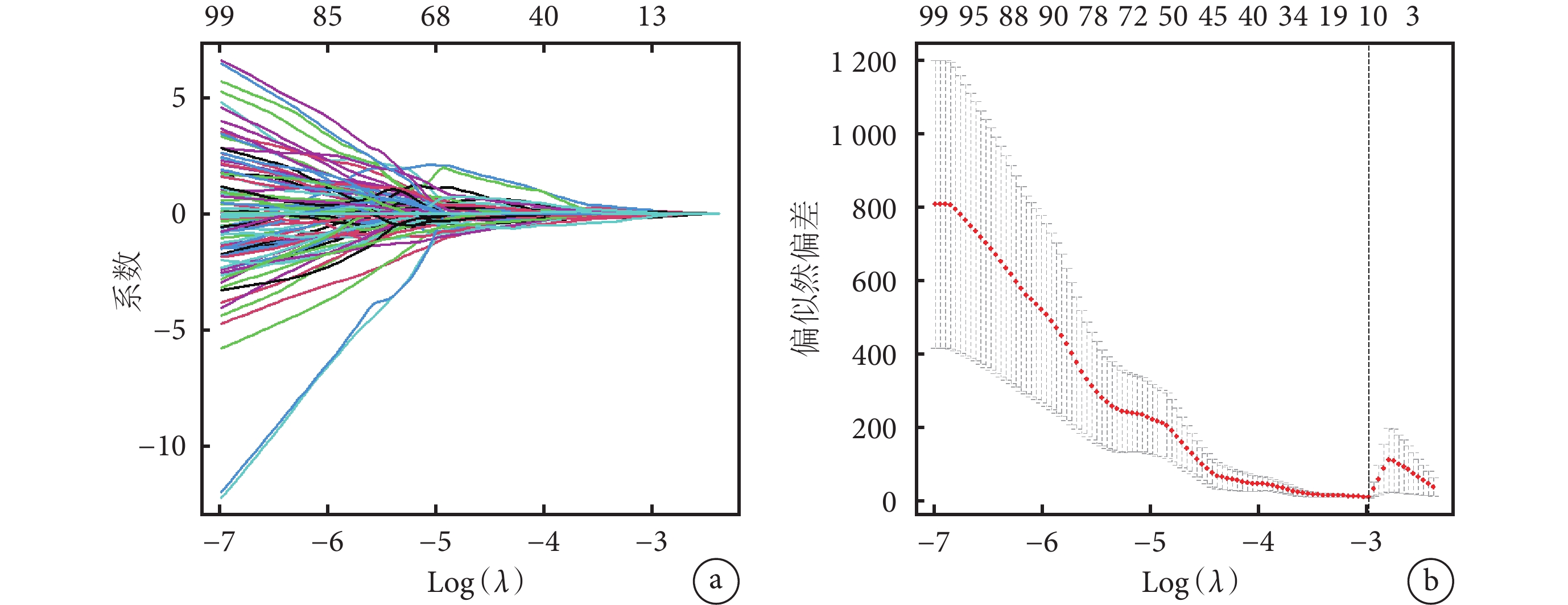
訓練集中對患者臨床特征進行單因素及多因素Cox回歸分析結果示,術后繼續接觸致病因素、JIC分型是影響保髖療效的獨立預測因子(P<0.05)。見表2、3。以LASSO進行回歸降維,經交叉驗證確定最優log(λ)為–3.00,最終將851個特征降維為13個非零系數的特征(圖4),包括3個原始圖像特征以及10個經小波變換采用高、低通濾波器處理后重新計算獲得的高階特征,并根據這些特征所對應的權重系數構建Rad-scores。在訓練集中,Cox回歸分析顯示Rad-scores、JIC分型、術后是否繼續接觸致病因素與保髖療效顯著相關,Rad-scores較低、術后不再接觸致病因素、JIC分型中B型及C1型患者的保髖成功率較高(P<0.05)。見圖5。
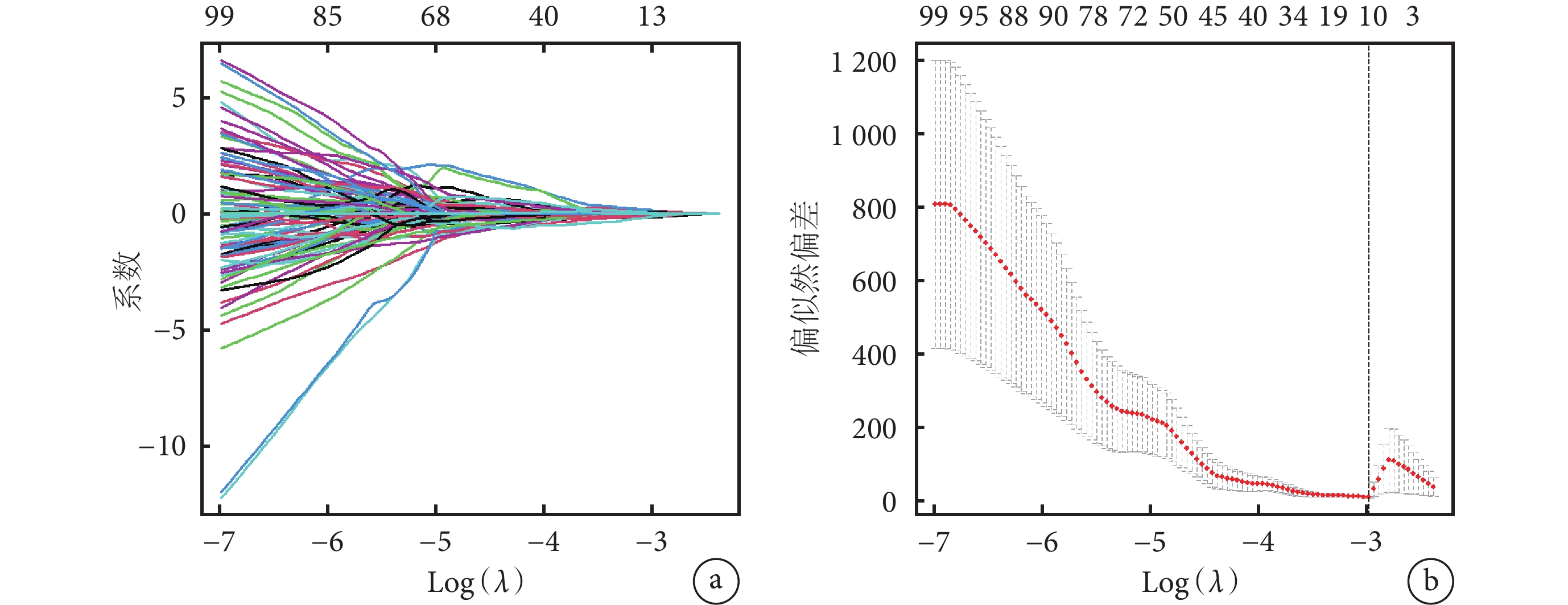 圖4
以LASSO算法篩選的判斷保髖成敗的影像組學特征
圖4
以LASSO算法篩選的判斷保髖成敗的影像組學特征
a. 回歸系數圖;b. 交叉驗證圖
Figure4. Radiomics features selected by LASSO to determine the hip preservation efficacya. Regression coefficient plot; b. Cross-validation plot
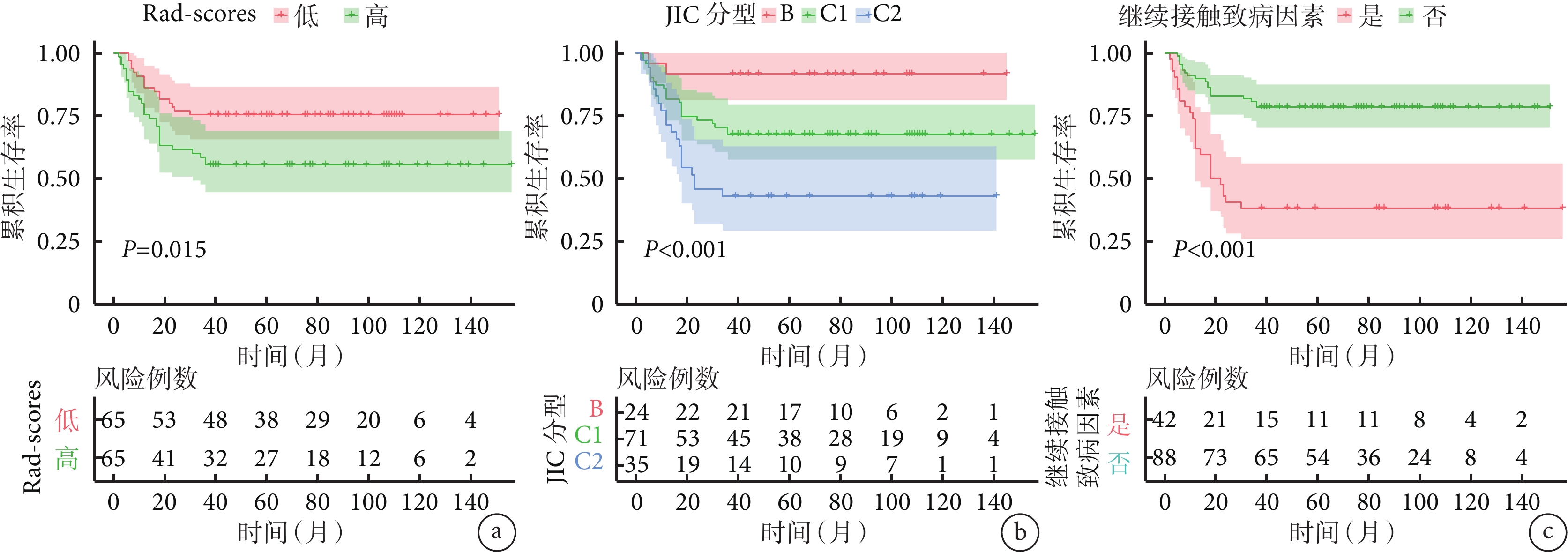
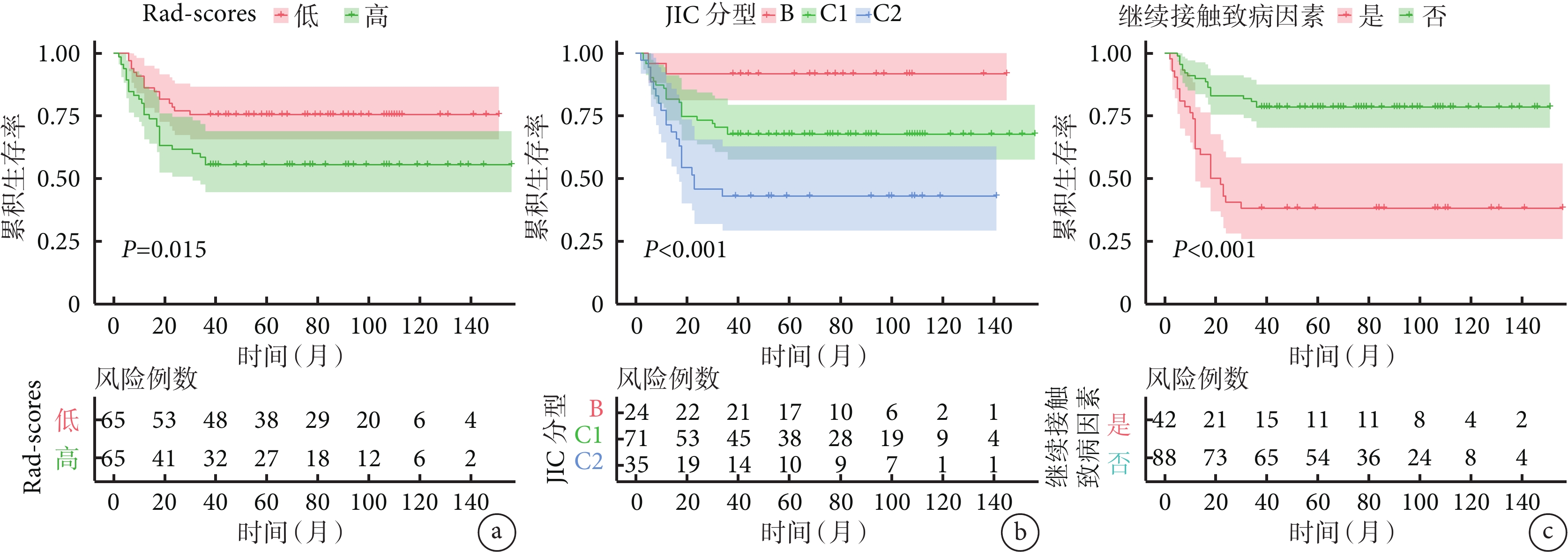 圖5
訓練集患者影像組學評分和臨床預測因子的Cox回歸分析
圖5
訓練集患者影像組學評分和臨床預測因子的Cox回歸分析
a. Rad-scores;b. JIC分型;c. 繼續接觸致病因素
Figure5. Cox regression survival analysis of imaging omics scores and clinical predictors for patients in the training seta. Rad-scores; b. JIC staging; c. Exposure to risk factors
2.3 模型的構建與驗證
訓練集和測試集中3種模型預測術后1~3年保髖療效的性能及ROC曲線和校準曲線結果顯示,綜合模型的AUC均大于臨床模型和影像組學模型,差異有統計學意義(P<0.05);結合校準曲線,綜合模型的預測值和實際觀察值之間均顯示出良好一致性。結合C-Index、敏感度和特異度評估,綜合模型的預測性能最優。見表4,圖6、7。
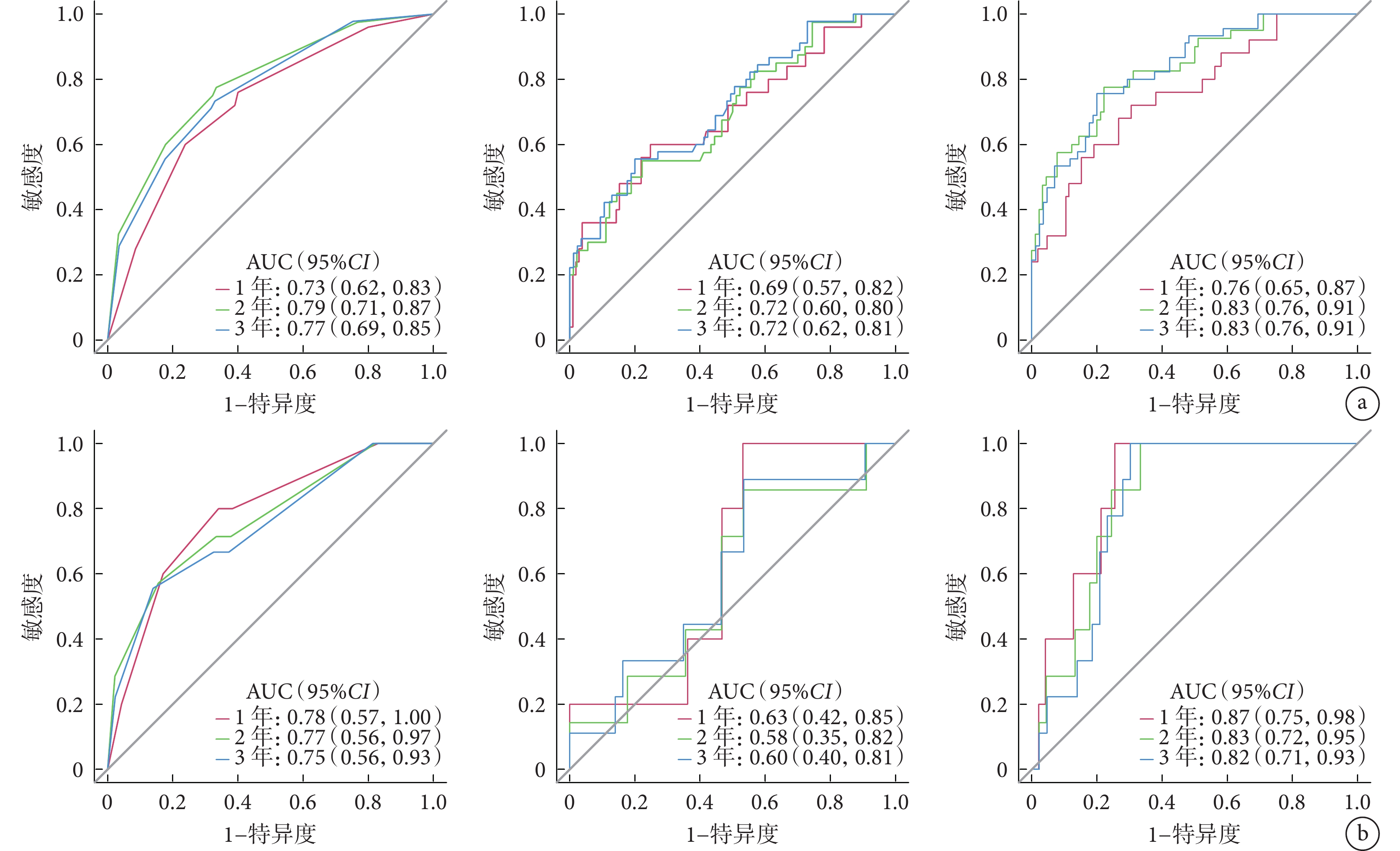 圖6
訓練集和測試集中3種模型的ROC曲線
圖6
訓練集和測試集中3種模型的ROC曲線
從左至右依次為臨床模型、影像組學模型、綜合模型 a. 訓練集;b. 測試集
Figure6. ROC curves of 3 models in the training set and testing setFrom left to right for clinical model, radiomics model, and C-R model, respectively a. Training set; b. Testing set
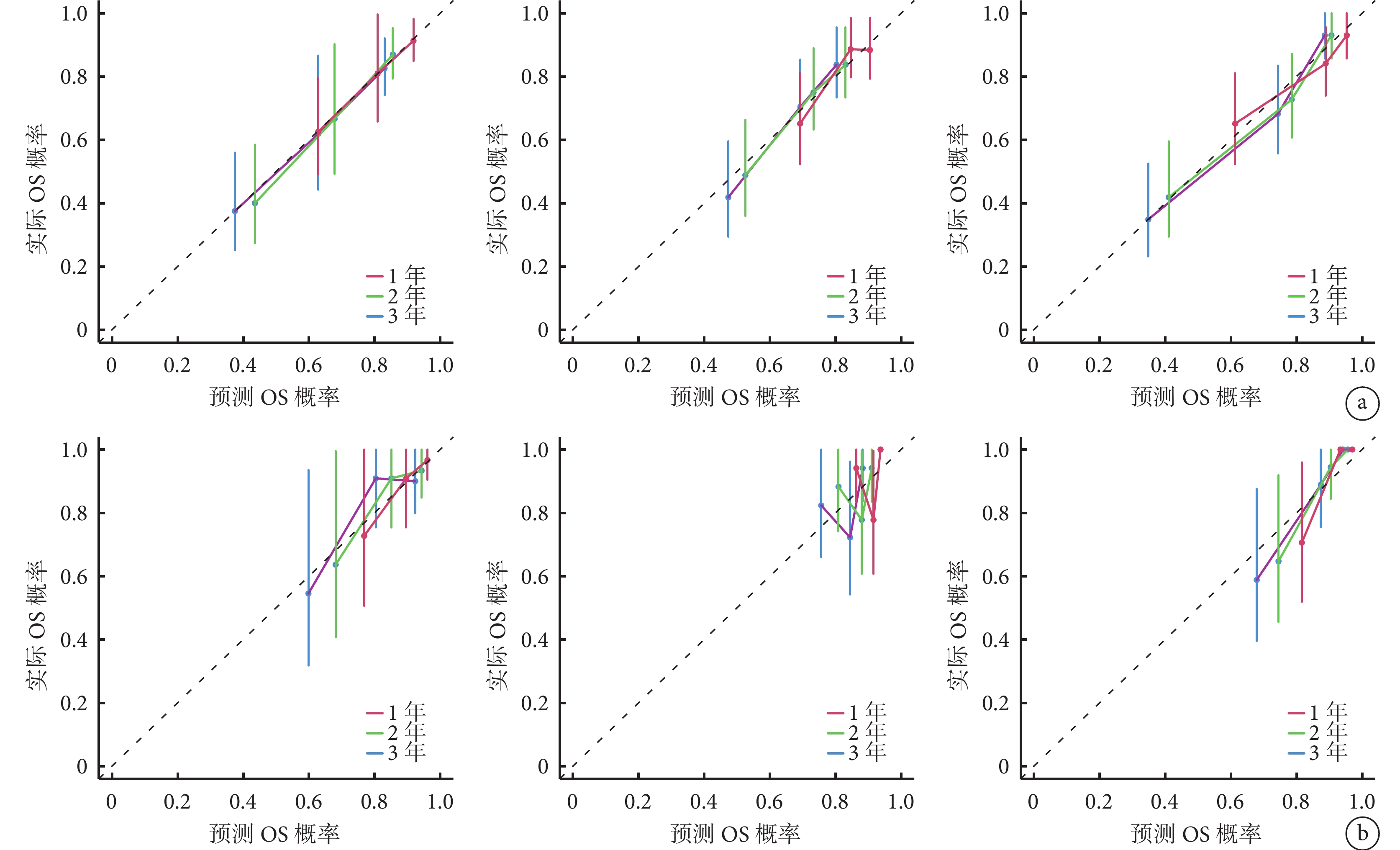 圖7
訓練集和測試集中3種模型的校準曲線
圖7
訓練集和測試集中3種模型的校準曲線
從左至右依次為臨床模型、影像組學模型、綜合模型 a. 訓練集;b. 測試集
Figure7. Calibration curves of 3 models in the training set and testing setFrom left to right for clinical model, radiomics model, and C-R model, respectively a. Training set; b. Testing set
2.4 列線圖的構建與驗證
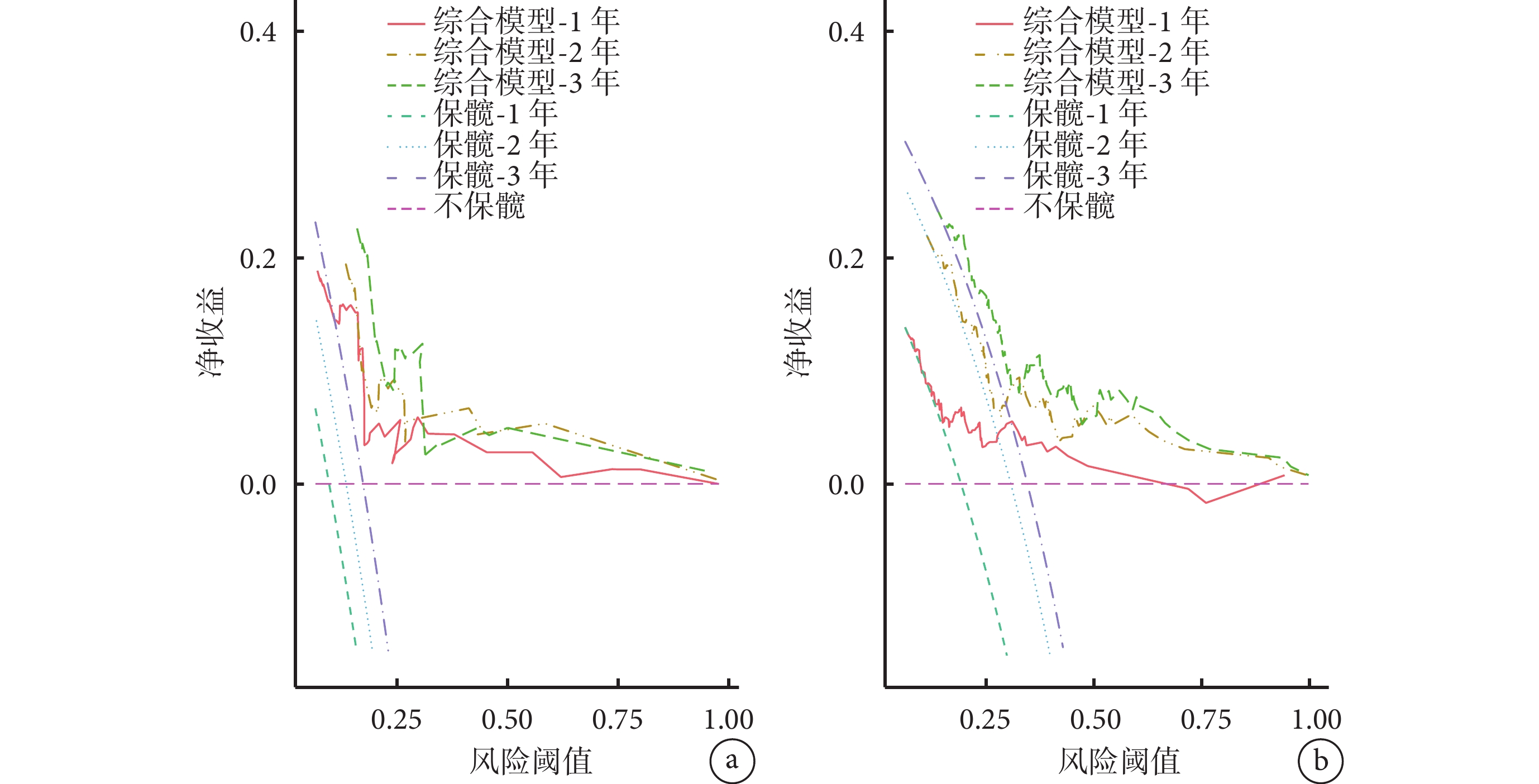
使用列線圖對綜合模型進行可視化,可見較低的Rad-scores、術后不再接觸致病因素和JIC分型中B型及C1型患者,其術后1、2、3年的股骨頭累積生存率較高。決策曲線分析結果顯示,在預測同一年的生存概率時,綜合模型的總凈收益均高于單一預測因子的臨床模型和影像組學模型,在訓練集和測試集中的趨勢相似,能在較大概率閾值范圍內帶給患者更多凈獲益。見圖8、9。
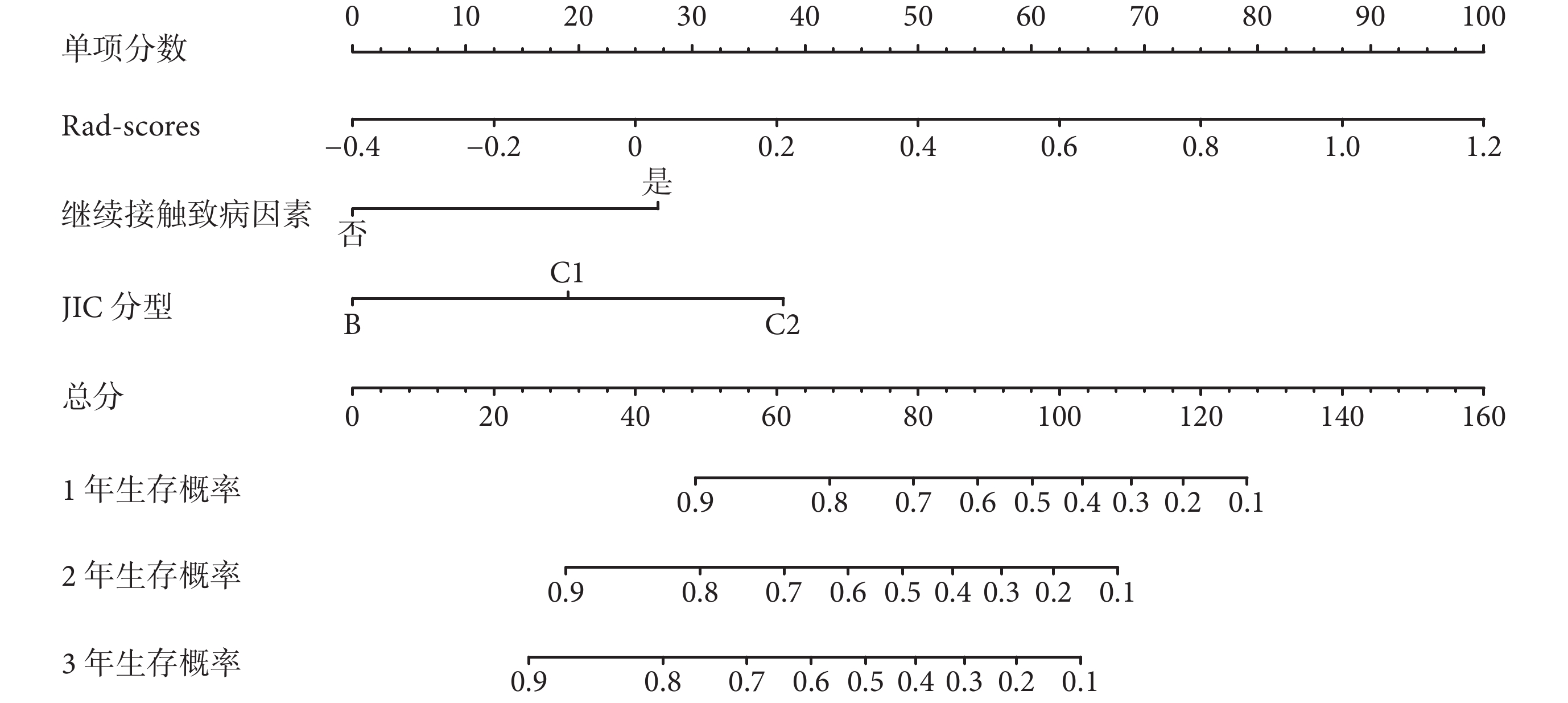 圖8
基于綜合模型構建的列線圖
Figure8.
Nomograms of the C-R model
圖8
基于綜合模型構建的列線圖
Figure8.
Nomograms of the C-R model
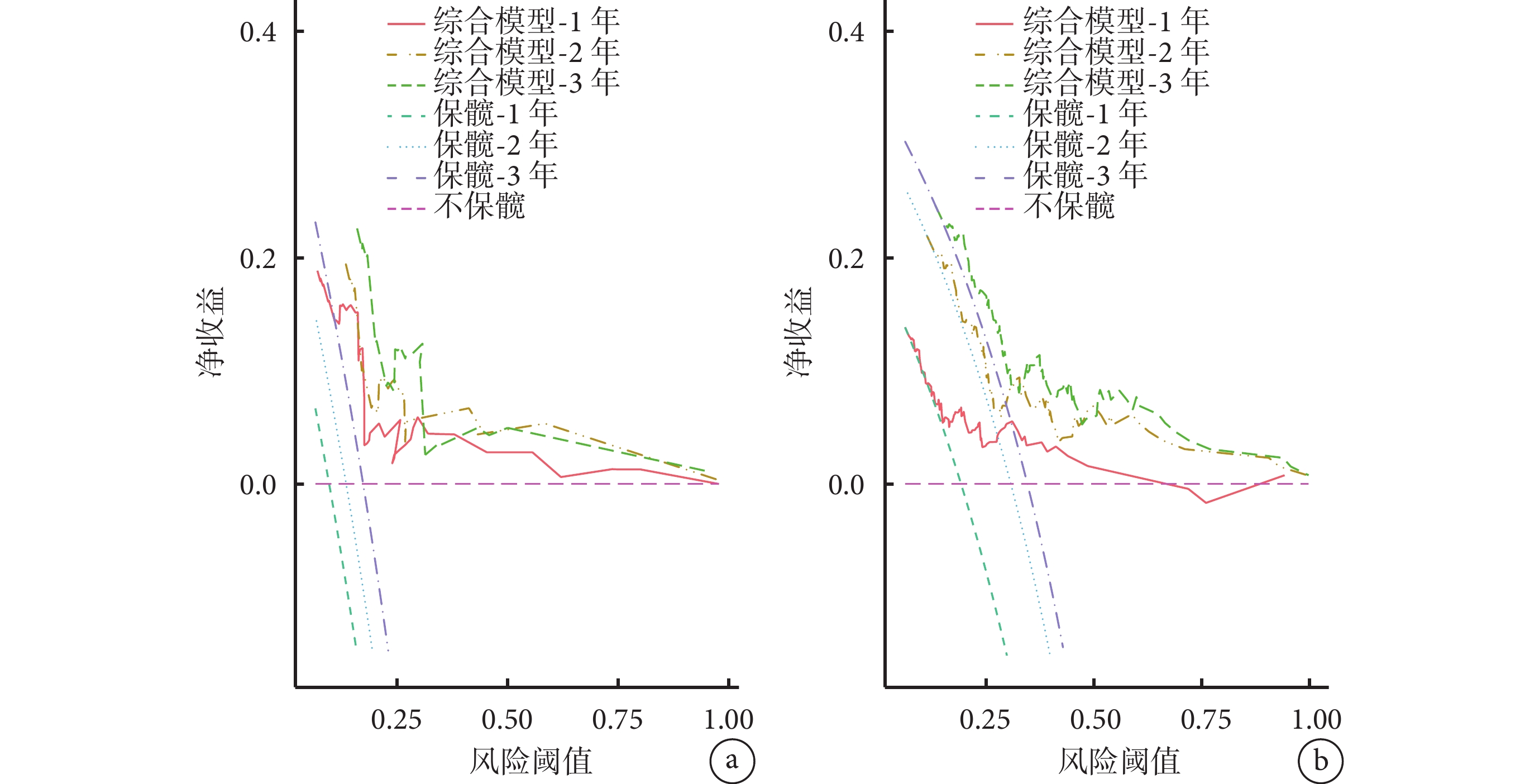 圖9
訓練集和測試集中綜合模型的決策曲線分析
圖9
訓練集和測試集中綜合模型的決策曲線分析
a. 訓練集;b. 測試集
Figure9. Decision curve analysis for C-R model in the training set and testing seta. Training set; b. Testing set
3 討論
目前,保髖成功標準已基本取得共識[16];但是,對于術后何時的股骨頭狀態能界定保髖成敗,尚無明確定論。既往研究多以末次隨訪時結果來評估保髖療效,但這種方法并不合適。對于尋求保髖治療的絕大多數患者而言,接受保髖的主要目的在于延緩初次THA時間,而非完全、徹底地避免THA。一方面,若以末次隨訪時間點來計,是對保髖療效過分苛求,相當一部分患者雖然最終仍置換關節,但實現了股骨頭較長時間的生存,末次隨訪結果不適合用于評定保髖療效,更不能作為是否建議接受保髖手術的依據。另一方面,保髖術后需要3個月免負重期,短期隨訪難以體現保髖療效和價值,也難以體現患者滿意度。因此,選擇合適時間點對于評估保髖療效、判斷患者是否應接受保髖手術十分重要。本團隊前期研究表明[17],股骨頭塌陷患者保髖失敗多出現在術后2~3年,3年后股骨頭生存時間相對穩定。本研究中,僅有8髖在3年后出現失敗,總體進展平緩,3年時保髖成功率與末次隨訪時相當,與既往研究相符。因此我們選擇術后3年的股骨頭狀態作為評判保髖成敗的依據,通過篩選與療效高度相關的風險因素構建決策模型。
本研究中,我們將影像組學應用于保髖領域,通過對CT圖像的壞死區進行勾畫、特征提取、降維及驗證后,篩選出與療效相關的13個影像組學特征。其中4個特征的相關性系數較大,分為以下兩類:① 描述ROI三維大小和形狀的Shape特征-Elongation,顯示了ROI形狀中兩個最大主要成分之間的關系;② 基于灰度共生矩陣GLCM、灰度依賴矩陣GLDM和灰度大小區域矩陣GLSZM的紋理特征,包括平均灰度強度、大依賴低灰度強調和大區域高灰度強調,反映了壞死區的灰度強度特點。這些特征從微觀層面體現了壞死區范圍、大小、局部信號強度與保髖療效的相關性關系。
Erivan等[18]研究發現,消除致病因素能顯著提高保守治療ONFH的存活率;Zhu等[19]的研究也證實術后繼續使用糖皮質激素將明顯增加股骨頭塌陷(≥3 mm)發生風險。與文獻報道一致,本研究中,單因素、多因素Cox回歸分析顯示術后繼續接觸致病因素是影響保髖療效的獨立預后因素。結合列線圖可以發現,術后不再接觸致病因素能提高患者術后3年內的股骨頭累積生存率。根據患者的原發病類型,我們建議激素性ONFH患者在原發病基本得到控制、不再使用激素后再接受保髖手術;創傷性ONFH患者應注意防護,避免進行易摔倒、骨折的高風險活動;酒精性ONFH患者則應完全戒酒;而對于特發性ONFH患者,也應進行相關宣教,調整生活習慣,避免暴露于已知的致病因素。
JIC分型是另一個影響NVBG保髖療效的獨立預測因子,它反映了壞死區范圍和外側柱受累程度。ONFH壞死區的范圍和位置是公認的影響股骨頭預后因素,前外側柱完整性對維持股骨頭功能起著重要作用[20-21]。既往研究認為,壞死區范圍<30%、局限于股骨頭中部、塌陷度<2 mm的患者保髖療效更好[22-23]。本研究中我們發現,JIC C2型患者術后股骨頭累積生存率低于B型及C1型患者,這可能與壞死區范圍過大,外側柱累及程度更重、完整性遭到破壞等有關。因此,對于壞死區主要位于股骨頭中間柱及內側柱,而外側柱較為完整的患者,接受NVBG保髖治療的獲益度將更高。
基于以上預測因子所構建的3種模型中,綜合模型的性能在訓練集和測試集中均優于預測因子單一的臨床模型和影像組學模型,具有較高的特異度和敏感度。影像組學從微觀層面,應用大量定量成像特征來全面量化局部壞死區,這些特征可能反映壞死區在細胞水平上的變化,并提供壞死區微環境的詳細信息,與視覺特征形成互補;而臨床預測因子則從宏觀層面,整體評估ONFH患者的身體狀況、生活習慣及理化檢驗指標。綜合模型整合兩者優勢,局部和整體、微觀與宏觀有機結合,多模態分析保髖療效,因此極大提高了預測準確率。同時,通過列線圖形式將綜合模型可視化,對預測因子進行量化,在臨床上可實現對NVBG保髖療效較好患者的早期識別。
但本研究亦存在一定局限性:① 本研究為單中心、回顧性研究,納入病例數量較少,需要進一步行多中心、大樣本、前瞻性研究驗證。② 目前尚無合適的算法實現對ONFH壞死區的自動分割,因而本研究采用交互式方法人工手動分割三維圖像,工作量大且穩定性欠佳,后續可考慮引入深度學習網絡以提高工作效率、減小人為誤差。③ 本研究重點在于通過對保髖療效模型的構建,指導保髖與否的臨床決策,并未深入探討具體保髖術式的選擇,后期需補充完善相關模型,以更好地輔助臨床決策。
綜上述,CT影像組學聯合臨床資料所構建的預測模型和列線圖,是一種可視量化的、有效的保髖決策方法,能在術前預測NVBG的保髖療效,具備較高的應用價值,能為治療方案的制定提供新的依據。
利益沖突 在課題研究和文章撰寫過程中不存在利益沖突;經費支持沒有影響文章觀點和對研究數據客觀結果的統計分析及其報道
倫理聲明 研究方案經南京中醫藥大學附屬醫院倫理委員會批準(2023NL-001-01)
作者貢獻聲明 杜斌、孫光權:研究設計;劉鋅、陳浩:研究實施;薛鵬、席洪鐘、何帥:數據收集整理及統計分析;劉鋅:文章撰寫(起草文章、對文章的知識性內容作批評性審閱);杜斌:經費支持
股骨頭壞死(osteonecrosis of the femoral head,ONFH)是一種起病隱匿、進展迅速的功能毀滅性疾病[1],一旦進展到股骨頭塌陷、髖關節炎等ONFH晚期,人工全髖關節置換術(total hip arthroplasty,THA)將成為患者唯一治療手段[2-3]。然而,過早接受THA將面臨手術相關并發癥和假體耐久性不足等問題[4]。因此,對于中青年患者,在ONFH早期選擇合適保髖手術以保留股骨頭并延遲初次置換時間,具有重要臨床意義[2-3,5]。但是相對于THA,保髖手術療效不確切,不同術式間的保髖成功率存在差異[6-8],相當一部分患者保髖術后早期即發生失敗,無疑增加了時間和經濟成本。因此,如何在術前預測保髖手術療效、評估患者是否適合保髖手術,進而選擇合理保髖策略,以降低術后股骨頭塌陷風險、提高保髖成功率,逐漸成為保髖研究領域的新焦點。
目前,保髖策略需要綜合考慮患者的臨床癥狀、體征及影像學資料,其中髖關節CT能較為準確顯示壞死區大小、硬化帶范圍等信息[9-10],是臨床制定治療方案的重要參考依據[11]。但是,不同醫生對壞死分期、部位及范圍的診斷存在主觀差異,并且大量深層次影像信息難以通過肉眼直接主觀提取、量化和充分利用。隨著醫學人工智能技術的飛速發展,“影像組學”的概念逐漸興起,作為一種新興的醫學影像方法[12],它通過使用算法或統計分析工具從診斷圖像中捕獲目標區域的明顯表型差異,所提取出的影像學特征可以提供肉眼分析之外的大量信息,能敏感地確定不同部位間形態和功能的微妙異質性,因此在診斷和預后預測領域得到廣泛應用[13-15]。然而,既往將影像組學應用于骨科尤其是保髖領域的相關研究較少。
本研究以非血管化植骨(non-vascularized bone grafting,NVBG)這一經典保髖術式為例,嘗試應用影像組學方法提取患者的CT影像學特征,與臨床資料相結合,構建一種可視量化且有效的保髖策略評估方法,以期為治療方案的制定提供參考。
1 資料與方法
1.1 研究對象
納入標準:① 經術中病理證實為ONFH;② 采用NVBG進行保髖治療;③ 無其他保髖手術治療史;④ 隨訪時間3年以上且隨訪資料完整。排除標準:① 未遵術后3個月內免負重醫囑、提前下地負重者;② CT圖像質量較差,無法進行影像組學分析者。
根據納排標準,篩選2009年6月—2019年6月于南京中醫藥大學附屬醫院接受NVBG進行保髖治療的153例(182髖)ONFH患者納入研究,按7∶3比例隨機分為訓練集(130髖)和測試集(52髖)。兩組患者性別、年齡、身體質量指數(body mass index,BMI)、病程、患側側別、病因、是否繼續接觸致病因素、國際骨循環協會(ARCO)分期、日本骨壞死研究會(JIC)分型以及術前Harris評分、ALP、D-二聚體(D-dimer,D-D)、中性粒細胞(nutrophils,NEUT)百分比、α-L-巖藻糖苷酶(α-L-fucosidase,AFU)等基線資料比較差異均無統計學意義(P>0.05)。見表1。
1.2 實驗方法
將術后行THA或髖關節出現明顯疼痛和活動受限、術后Harris評分<90分及影像學出現股骨頭進行性塌陷設為生存終點;根據術后3年隨訪時是否出現上述結果定義保髖成敗。以2022年6月作為隨訪終點,計算術側股骨頭生存率和生存時間,采用Kaplan-Meier生存曲線進行分析。本研究流程圖見圖1。
 圖1
研究流程圖
Figure1.
Flowchart of the study
圖1
研究流程圖
Figure1.
Flowchart of the study
1.2.1 病灶分割及影像學特征提取
所有患者術前均接受雙髖關節CT平掃(荷蘭飛利浦公司128排Brilliance CT或美國通用公司64排LightSpeed VCT),從PCAS系統中獲取圖像。掃描參數:管電壓120~140 kV,管電流220~680 mA,曝光時間250~800 ms,層厚1.0~3.0 mm,層間距1.0~3.0 mm,重建矩陣512×512。將CT圖像以DICOM格式導入免費開放獲取的軟件3D Slicer(https://www.slicer.org,V5.0.2)中,按照1 mm×1 mm×1 mm體素大小、1~64灰度值進行標準化處理。將股骨頭星芒征缺失、負重區骨小梁缺失斷裂及硬化帶包繞囊變區等密度異常的壞死區域定義為感興趣區(region of interesting,ROI)。首先由1名具有10年以上工作經驗的影像科醫師,于骨窗(窗寬1 500 HU,窗位400 U)手動分割勾勒冠狀位、矢狀位和軸位的ROI;再由1名高年資ONFH專科醫師加以修正,最終生成三維ROI(圖2)。使用“Pyradiomics”插件對每個ROI進行影像組學特征提取,該插件能自動從每個ROI中提取851個特征值,包括18個直方圖強度特征、14個形狀特征、75個紋理特征(24個灰度共生矩陣、14個灰度依賴矩陣、16個灰度行程矩陣、16個灰度區域大小矩陣、5個鄰域灰度差矩陣)和744個小波特征,所有提取的影像學特征值均進行Z-score標準化。
 圖2
于CT圖像骨窗手動勾畫壞死區ROI示意圖
圖2
于CT圖像骨窗手動勾畫壞死區ROI示意圖
a~c. 冠狀位、矢狀位、軸位骨窗CT圖;d. 生成的壞死區三維ROI
Figure2. Schematic diagram of ROI segmented and outlined by manual mode in the bone window of CT imagesa-c. CT images in the bone window in coronal, sagittal, and axial positions; d. Three-dimensional ROI of necrotic area generated from them
1.2.2 特征篩選
對患者的臨床資料和影像組學特征進行降維和篩選。在訓練集中,使用“glmnet”軟件包進行最小絕對收縮和選擇算子(least absolute shrinkage and selection operator,LASSO)回歸降維,通過十折交叉驗證確定最優log(λ)以篩選影像組學特征,根據篩選出的特征所對應的LASSO權重系數構建影像組學標簽,并計算所有患髖的影像組學評分(Rad-scores);收集并記錄文獻報道中與保髖療效相關的風險因素,使用單因素、多因素Cox回歸分析從中篩選臨床預測因子,使用“survminer”軟件包進行Cox回歸分析,評價影像組學評分和臨床預測因子的價值。
1.2.3 保髖決策模型的構建與評價
根據所提取的特征,以保髖成敗作為結局變量,在訓練集中分別構建3種保髖決策模型。根據患者的Rad-scores構建保髖療效的影像組學模型,使用臨床預測因子構建臨床模型,使用臨床預測因子和Rad-scores聯合構建綜合模型。在訓練集及測試集中對3種模型的預測效能進行評價、驗證,使用“pROC”軟件包繪制3種模型的受試者工作特征(receiver operating characteristic curve,ROC)曲線,計算曲線下面積(area under curve,AUC),采用DeLong檢驗比較AUC,根據C-index、敏感度、特異度和校準曲線評估各模型的性能。為了給臨床醫生提供一種保髖決策的定量工具,以預測術后股骨頭的生存概率,使用“rms”和“hdnom”軟件包構建列線圖對最佳模型進行可視化,并使用“rmda”和“ggDCA”軟件包繪制決策曲線分析該列線圖的臨床效用。
1.3 統計學方法
采用SPSS26.0、R軟件(版本號 4.1.2)和RStudio軟件(版本號1.2.5042)進行分析。計量資料行正態性檢驗,符合正態分布的數據以均數±標準差表示,訓練集和測試集間比較采用獨立樣本t檢驗;不符合正態分布的數據以M(Q1,Q3)表示,組間比較采用Mann-Whitney U檢驗;計數資料組間比較采用χ2檢驗。檢驗水準取雙側α=0.05。
2 結果
2.1 隨訪結果
術后3年隨訪時,128髖功能良好,未進行關節置換,保髖成功率為70.33%; Kaplan-Meier生存曲線示,36個月后股骨頭生存率基本穩定。末次隨訪時120髖保髖成功,保髖成功率65.93%,生存時間(65.56±43.27)個月。見圖3。
 圖3
股骨頭生存率的Kaplan-Meier曲線分析
Figure3.
Kaplan-Meier curve analysis of the survival rate of femoral head
圖3
股骨頭生存率的Kaplan-Meier曲線分析
Figure3.
Kaplan-Meier curve analysis of the survival rate of femoral head
2.2 特征篩選
訓練集中對患者臨床特征進行單因素及多因素Cox回歸分析結果示,術后繼續接觸致病因素、JIC分型是影響保髖療效的獨立預測因子(P<0.05)。見表2、3。以LASSO進行回歸降維,經交叉驗證確定最優log(λ)為–3.00,最終將851個特征降維為13個非零系數的特征(圖4),包括3個原始圖像特征以及10個經小波變換采用高、低通濾波器處理后重新計算獲得的高階特征,并根據這些特征所對應的權重系數構建Rad-scores。在訓練集中,Cox回歸分析顯示Rad-scores、JIC分型、術后是否繼續接觸致病因素與保髖療效顯著相關,Rad-scores較低、術后不再接觸致病因素、JIC分型中B型及C1型患者的保髖成功率較高(P<0.05)。見圖5。
 圖4
以LASSO算法篩選的判斷保髖成敗的影像組學特征
圖4
以LASSO算法篩選的判斷保髖成敗的影像組學特征
a. 回歸系數圖;b. 交叉驗證圖
Figure4. Radiomics features selected by LASSO to determine the hip preservation efficacya. Regression coefficient plot; b. Cross-validation plot
 圖5
訓練集患者影像組學評分和臨床預測因子的Cox回歸分析
圖5
訓練集患者影像組學評分和臨床預測因子的Cox回歸分析
a. Rad-scores;b. JIC分型;c. 繼續接觸致病因素
Figure5. Cox regression survival analysis of imaging omics scores and clinical predictors for patients in the training seta. Rad-scores; b. JIC staging; c. Exposure to risk factors
2.3 模型的構建與驗證
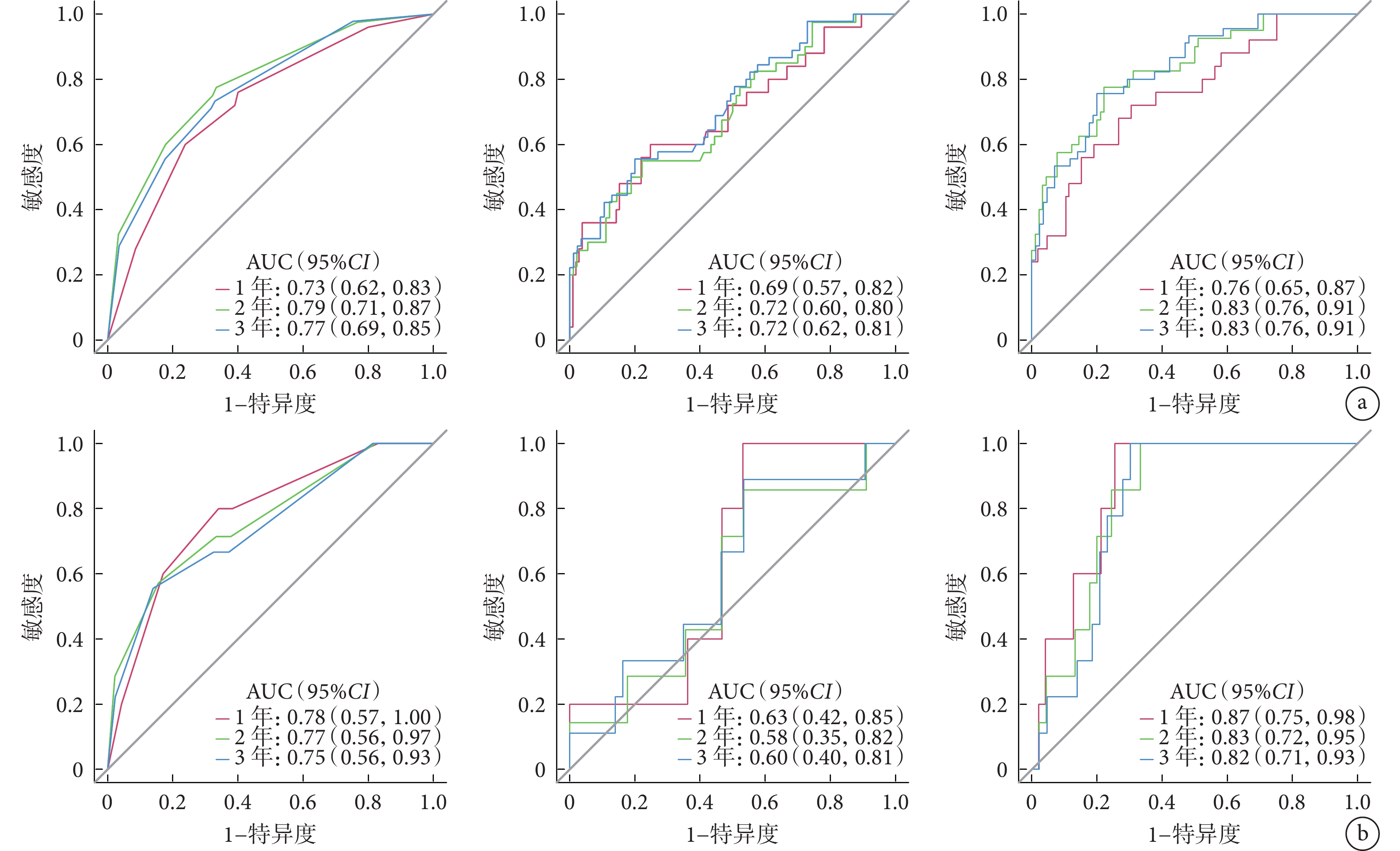
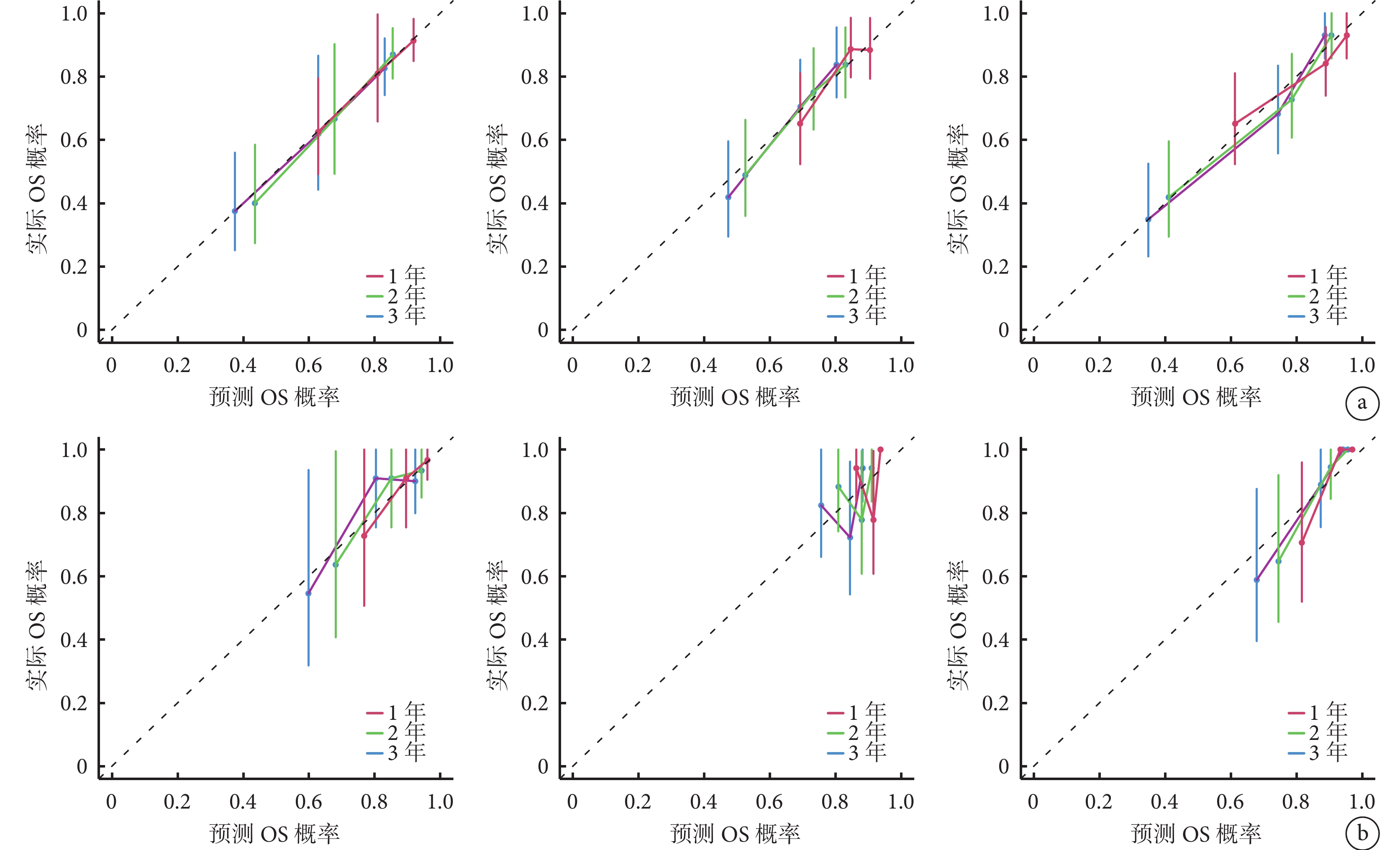
訓練集和測試集中3種模型預測術后1~3年保髖療效的性能及ROC曲線和校準曲線結果顯示,綜合模型的AUC均大于臨床模型和影像組學模型,差異有統計學意義(P<0.05);結合校準曲線,綜合模型的預測值和實際觀察值之間均顯示出良好一致性。結合C-Index、敏感度和特異度評估,綜合模型的預測性能最優。見表4,圖6、7。
 圖6
訓練集和測試集中3種模型的ROC曲線
圖6
訓練集和測試集中3種模型的ROC曲線
從左至右依次為臨床模型、影像組學模型、綜合模型 a. 訓練集;b. 測試集
Figure6. ROC curves of 3 models in the training set and testing setFrom left to right for clinical model, radiomics model, and C-R model, respectively a. Training set; b. Testing set
 圖7
訓練集和測試集中3種模型的校準曲線
圖7
訓練集和測試集中3種模型的校準曲線
從左至右依次為臨床模型、影像組學模型、綜合模型 a. 訓練集;b. 測試集
Figure7. Calibration curves of 3 models in the training set and testing setFrom left to right for clinical model, radiomics model, and C-R model, respectively a. Training set; b. Testing set
2.4 列線圖的構建與驗證
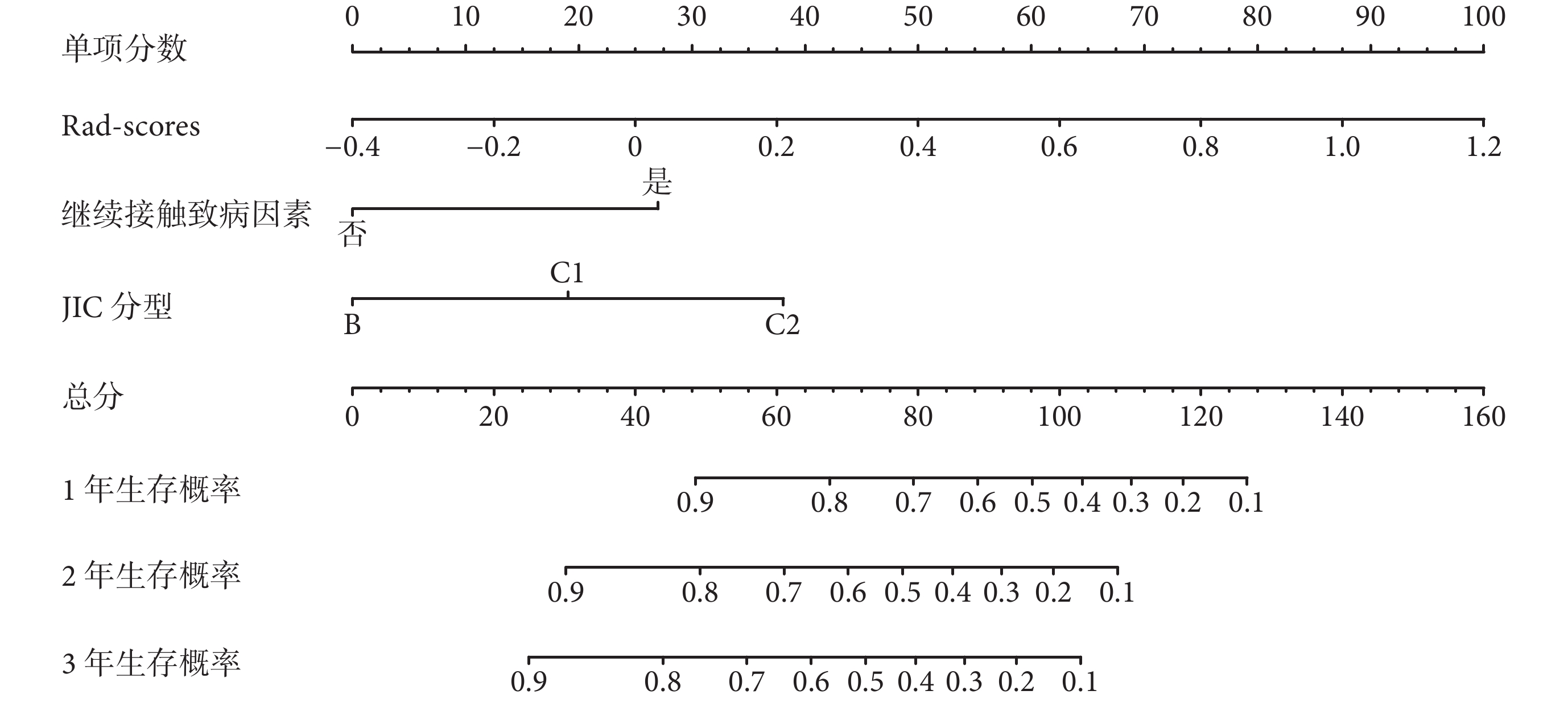
使用列線圖對綜合模型進行可視化,可見較低的Rad-scores、術后不再接觸致病因素和JIC分型中B型及C1型患者,其術后1、2、3年的股骨頭累積生存率較高。決策曲線分析結果顯示,在預測同一年的生存概率時,綜合模型的總凈收益均高于單一預測因子的臨床模型和影像組學模型,在訓練集和測試集中的趨勢相似,能在較大概率閾值范圍內帶給患者更多凈獲益。見圖8、9。
 圖8
基于綜合模型構建的列線圖
Figure8.
Nomograms of the C-R model
圖8
基于綜合模型構建的列線圖
Figure8.
Nomograms of the C-R model
 圖9
訓練集和測試集中綜合模型的決策曲線分析
圖9
訓練集和測試集中綜合模型的決策曲線分析
a. 訓練集;b. 測試集
Figure9. Decision curve analysis for C-R model in the training set and testing seta. Training set; b. Testing set
3 討論
目前,保髖成功標準已基本取得共識[16];但是,對于術后何時的股骨頭狀態能界定保髖成敗,尚無明確定論。既往研究多以末次隨訪時結果來評估保髖療效,但這種方法并不合適。對于尋求保髖治療的絕大多數患者而言,接受保髖的主要目的在于延緩初次THA時間,而非完全、徹底地避免THA。一方面,若以末次隨訪時間點來計,是對保髖療效過分苛求,相當一部分患者雖然最終仍置換關節,但實現了股骨頭較長時間的生存,末次隨訪結果不適合用于評定保髖療效,更不能作為是否建議接受保髖手術的依據。另一方面,保髖術后需要3個月免負重期,短期隨訪難以體現保髖療效和價值,也難以體現患者滿意度。因此,選擇合適時間點對于評估保髖療效、判斷患者是否應接受保髖手術十分重要。本團隊前期研究表明[17],股骨頭塌陷患者保髖失敗多出現在術后2~3年,3年后股骨頭生存時間相對穩定。本研究中,僅有8髖在3年后出現失敗,總體進展平緩,3年時保髖成功率與末次隨訪時相當,與既往研究相符。因此我們選擇術后3年的股骨頭狀態作為評判保髖成敗的依據,通過篩選與療效高度相關的風險因素構建決策模型。
本研究中,我們將影像組學應用于保髖領域,通過對CT圖像的壞死區進行勾畫、特征提取、降維及驗證后,篩選出與療效相關的13個影像組學特征。其中4個特征的相關性系數較大,分為以下兩類:① 描述ROI三維大小和形狀的Shape特征-Elongation,顯示了ROI形狀中兩個最大主要成分之間的關系;② 基于灰度共生矩陣GLCM、灰度依賴矩陣GLDM和灰度大小區域矩陣GLSZM的紋理特征,包括平均灰度強度、大依賴低灰度強調和大區域高灰度強調,反映了壞死區的灰度強度特點。這些特征從微觀層面體現了壞死區范圍、大小、局部信號強度與保髖療效的相關性關系。
Erivan等[18]研究發現,消除致病因素能顯著提高保守治療ONFH的存活率;Zhu等[19]的研究也證實術后繼續使用糖皮質激素將明顯增加股骨頭塌陷(≥3 mm)發生風險。與文獻報道一致,本研究中,單因素、多因素Cox回歸分析顯示術后繼續接觸致病因素是影響保髖療效的獨立預后因素。結合列線圖可以發現,術后不再接觸致病因素能提高患者術后3年內的股骨頭累積生存率。根據患者的原發病類型,我們建議激素性ONFH患者在原發病基本得到控制、不再使用激素后再接受保髖手術;創傷性ONFH患者應注意防護,避免進行易摔倒、骨折的高風險活動;酒精性ONFH患者則應完全戒酒;而對于特發性ONFH患者,也應進行相關宣教,調整生活習慣,避免暴露于已知的致病因素。
JIC分型是另一個影響NVBG保髖療效的獨立預測因子,它反映了壞死區范圍和外側柱受累程度。ONFH壞死區的范圍和位置是公認的影響股骨頭預后因素,前外側柱完整性對維持股骨頭功能起著重要作用[20-21]。既往研究認為,壞死區范圍<30%、局限于股骨頭中部、塌陷度<2 mm的患者保髖療效更好[22-23]。本研究中我們發現,JIC C2型患者術后股骨頭累積生存率低于B型及C1型患者,這可能與壞死區范圍過大,外側柱累及程度更重、完整性遭到破壞等有關。因此,對于壞死區主要位于股骨頭中間柱及內側柱,而外側柱較為完整的患者,接受NVBG保髖治療的獲益度將更高。
基于以上預測因子所構建的3種模型中,綜合模型的性能在訓練集和測試集中均優于預測因子單一的臨床模型和影像組學模型,具有較高的特異度和敏感度。影像組學從微觀層面,應用大量定量成像特征來全面量化局部壞死區,這些特征可能反映壞死區在細胞水平上的變化,并提供壞死區微環境的詳細信息,與視覺特征形成互補;而臨床預測因子則從宏觀層面,整體評估ONFH患者的身體狀況、生活習慣及理化檢驗指標。綜合模型整合兩者優勢,局部和整體、微觀與宏觀有機結合,多模態分析保髖療效,因此極大提高了預測準確率。同時,通過列線圖形式將綜合模型可視化,對預測因子進行量化,在臨床上可實現對NVBG保髖療效較好患者的早期識別。
但本研究亦存在一定局限性:① 本研究為單中心、回顧性研究,納入病例數量較少,需要進一步行多中心、大樣本、前瞻性研究驗證。② 目前尚無合適的算法實現對ONFH壞死區的自動分割,因而本研究采用交互式方法人工手動分割三維圖像,工作量大且穩定性欠佳,后續可考慮引入深度學習網絡以提高工作效率、減小人為誤差。③ 本研究重點在于通過對保髖療效模型的構建,指導保髖與否的臨床決策,并未深入探討具體保髖術式的選擇,后期需補充完善相關模型,以更好地輔助臨床決策。
綜上述,CT影像組學聯合臨床資料所構建的預測模型和列線圖,是一種可視量化的、有效的保髖決策方法,能在術前預測NVBG的保髖療效,具備較高的應用價值,能為治療方案的制定提供新的依據。
利益沖突 在課題研究和文章撰寫過程中不存在利益沖突;經費支持沒有影響文章觀點和對研究數據客觀結果的統計分析及其報道
倫理聲明 研究方案經南京中醫藥大學附屬醫院倫理委員會批準(2023NL-001-01)
作者貢獻聲明 杜斌、孫光權:研究設計;劉鋅、陳浩:研究實施;薛鵬、席洪鐘、何帥:數據收集整理及統計分析;劉鋅:文章撰寫(起草文章、對文章的知識性內容作批評性審閱);杜斌:經費支持