目前經導管介入治療主動脈弓縮窄已成為一線治療方案,主要在放射線引導下進行。但放射線暴露會造成對患者及醫護人員潛在的損害,且依賴大型放射線設備,帶來了諸多限制。本文首次報道單純超聲引導主動脈縮窄支架置入術治療27歲育齡期女性患者的病例,出院后患者主動脈縮窄處壓差降至18 mm Hg,手術效果良好。
引用本文: 常鈞科, 魏培堅, 盧耀星, 張鳳文, 房芳, 王闖世, 王首正, 歐陽文斌, 萬俊義, 潘湘斌. 單純超聲引導支架置入術治療主動脈縮窄一例. 中國胸心血管外科臨床雜志, 2024, 31(2): 325-328. doi: 10.7507/1007-4848.202311022 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
1982年Singer等[1]報道了首例經導管球囊擴張成形術治療主動脈縮窄(coarctation of the aorta,CoA),經過數十年的發展后,目前經導管介入治療已在主動脈縮窄患者中廣泛應用[2],主要在放射線引導下完成。放射線引導下經導管介入治療CoA一方面由于依賴大型放射線設備限制了這一術式在基層醫院的開展,另一方面由于放射線禁忌導致部分患者如育齡期女性無法接受合適治療。而近年來單純超聲引導下介入治療諸如房間隔缺損和動脈導管未閉等簡單先天性心臟病(先心病)已證實治療效果良好,而在此我們報道1例在單純超聲引導下行CoA支架置入術治療CoA育齡期女性患者的病例
臨床資料 患者,女,27歲,因“發現心臟雜音3年余”入住中國醫學科學院阜外醫院深圳醫院。患者3年余前體檢發現心臟雜音,檢查心臟超聲心動圖提示降主動脈縮窄,無胸悶、氣促、頭暈、頭痛等不適,自測收縮壓180 mm Hg (1 mm Hg=0.133 kPa)以上,患者為行單純超聲引導介入治療CoA于我院門診就診,門診以“主動脈縮窄”于2023年2月13日收入我院。患者自發病以來精神食欲可,睡眠可,二便如常,雙下肢不水腫,體重無明顯變化。既往10余年前有甲狀腺功能亢進手術治療史。
入院后體格檢查:左上肢血壓172/97 mm Hg,心率60次/min,律齊,胸骨左緣第2肋間可聞及3級收縮期吹風樣雜音,腹平軟,肝脾肋下未觸及,雙下肢無水腫。經胸超聲心動圖示:降主動脈縮窄(4 mm),狹窄處流速增快,5.0 m/s,壓差100 mm Hg;主動脈瓣葉呈二葉式,右冠瓣、左冠瓣融合,瓣葉開放稍受限,輕度反流;左心房大、二尖瓣輕-中度反流,左心室射血分數(LVEF):62%。全主動脈計算機斷層血管造影(computed tomography angiography,CTA)顯示:CoA、胸主動脈側枝血管開放(主動脈弓降部局部變窄,最窄處約7 mm,距離左鎖骨下動脈開口約24 mm,其后管腔擴張,直徑約27 mm,并可見發出三支側枝血管,管徑3~5 mm,較粗側枝血管向上沿脊柱旁走行)(圖1a),左鎖骨下動脈近端擴張(直徑約13 mm,中遠段管徑7 mm),升主動脈、主動脈弓、腹主動脈及骼動脈管腔未見明顯狹窄或擴張,管腔內未見明顯內膜片及雙腔征。主動脈瓣瓣葉增厚,二葉主動脈瓣。患者“CoA”診斷明確,有手術指征,由于該患者系育齡期女性,結合患者治療意愿,經心臟團隊進一步評估后擬在單純超聲引導下行CoA支架置入術。
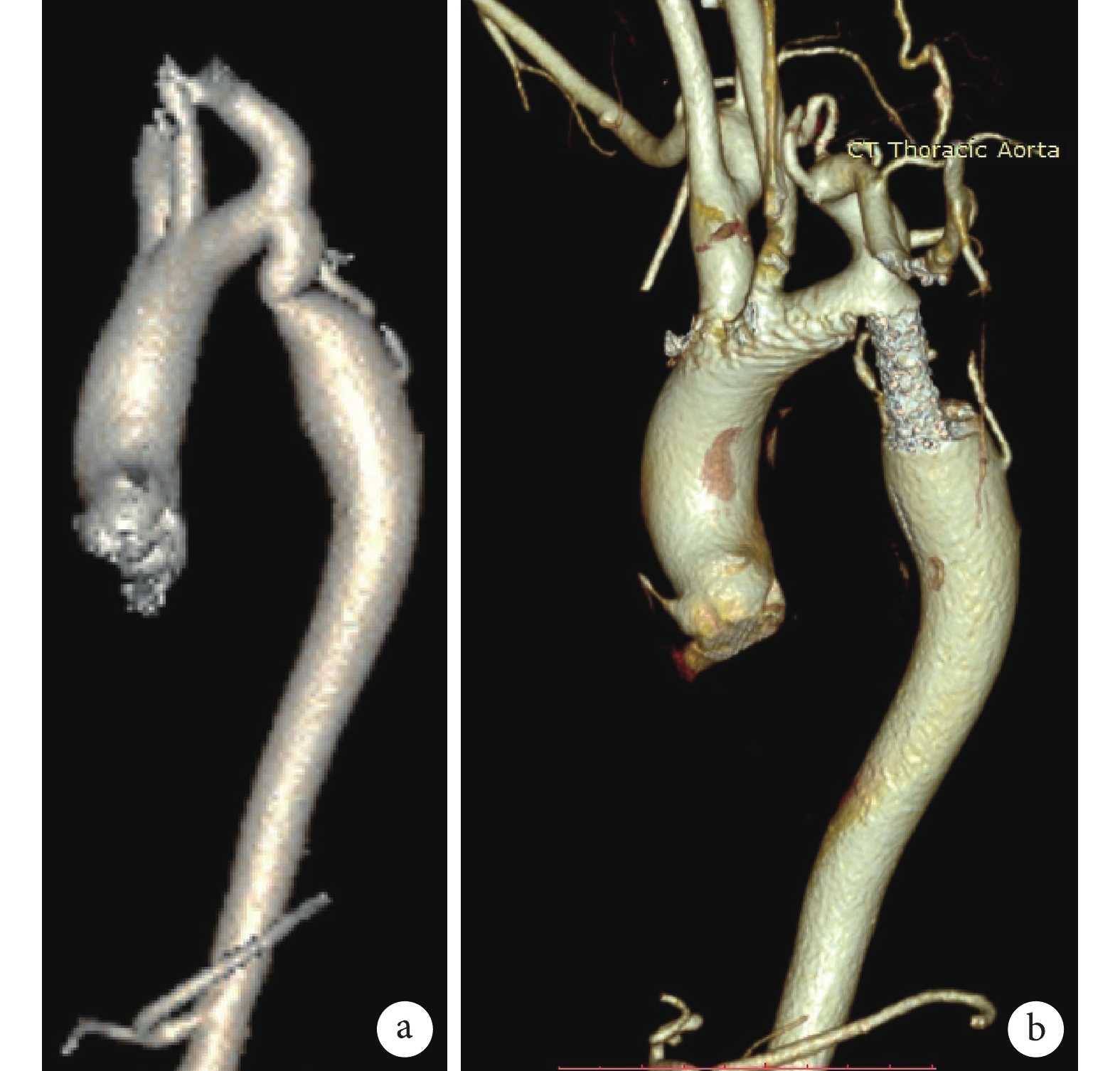 圖1
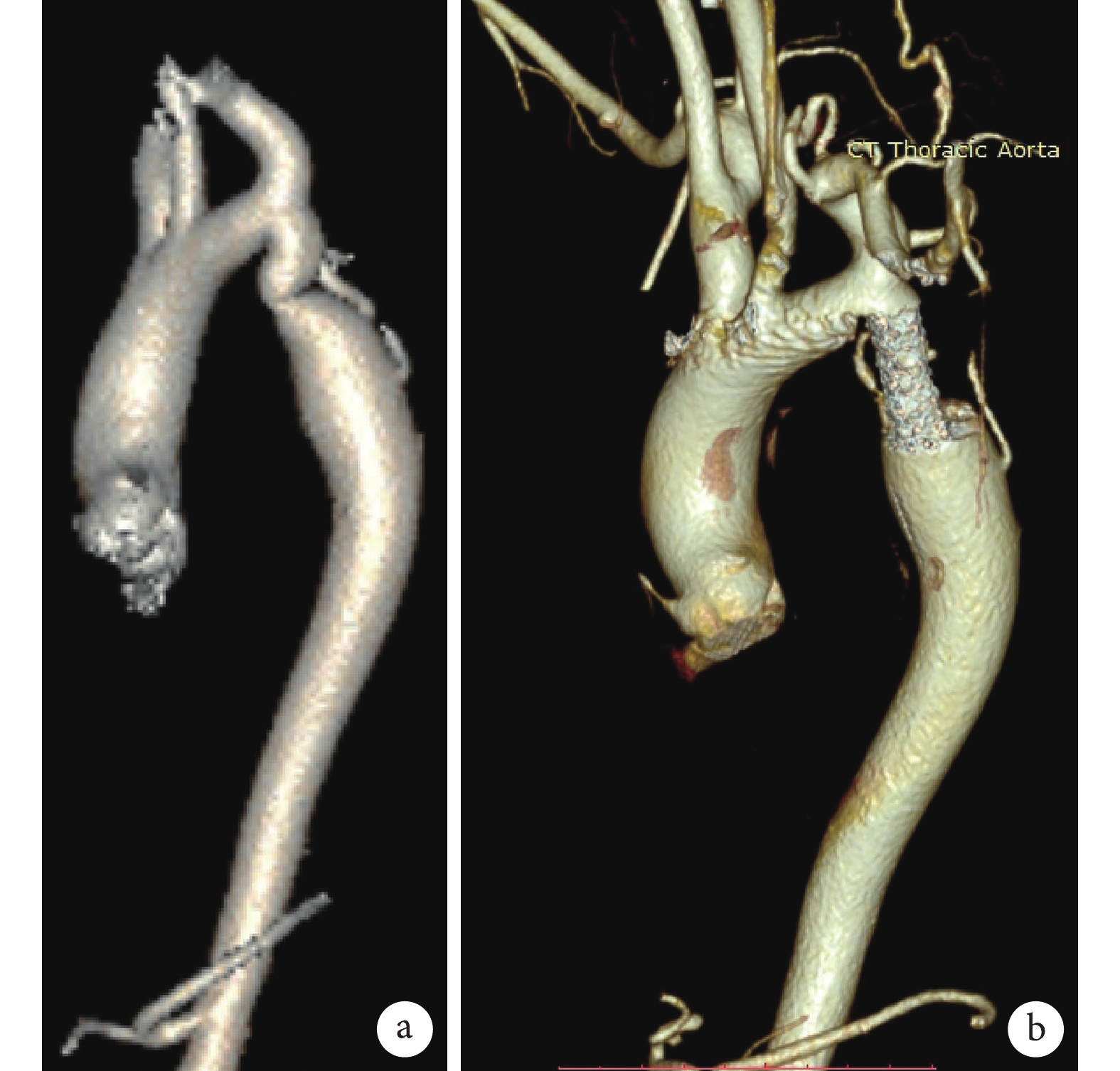
CTA全主動脈三維容積重建
圖1
CTA全主動脈三維容積重建
a:介入前降主動脈縮窄;b:降主動脈支架位置及形態良好
手術在手術室進行,患者取仰臥位,全身麻醉后插入食管超聲備用。常規消毒、鋪巾,穿刺右股動脈,測量穿刺點到胸骨左側第2肋間(主動脈弓)的距離,標記為工作距離。按工作距離插入Luandquit超硬導絲,在食管超聲引導下將超硬導絲通過主動脈縮窄段,進入升主動脈內,沿導絲送入MPA2導管,撤出超硬導絲,沿MPA2導管送入超聲引導專用導絲,其頭部膨脹為菱形,超聲可以準確定位其位置。固定導絲,退出MPA2導管及6F動脈鞘,置入COOK12F輸送鞘。選擇NuMed 16 mm BIB球囊及3.9 cm CP覆膜支架,將支架裝載于球囊上,沿導絲將支架及球囊置入輸送鞘,球囊頂端緊貼導絲頭端的膨大部分,在超聲引導下通過膨大的導絲頭端準確定位支架起始處,調整位置滿意后置入NuMed 16 mm BIB球囊導管擴張狹窄部位,撤出球囊導管后置入NuMed 3.9 cm CP外膨脹支架,再次測壓,左上肢動脈壓104/56 mm Hg。經管道超聲提示CoA處血流速度2.6 m/s,壓差26 mm Hg,測得腹主動脈頻譜明顯改善,CoA處支架位置及形態良好(圖2),血流通暢。撤除導管、導絲及動脈鞘,穿刺點壓力止血器加壓固定。本次手術時間2 h。介入治療術后采用口服阿司匹林腸溶片100 mg(1次/d)行抗凝治療,介入治療后1 d轉出監護室,復查超聲心動圖示:降主動脈流速稍快,2.2 m/s,壓差19 mm Hg。CTA提示主動脈弓降部見金屬支架影,最窄處約13 mm,支架形態完整,內腔通暢(圖1b);升主動脈、主動脈弓管腔未見明顯狹窄或擴張。住院時間4 d。
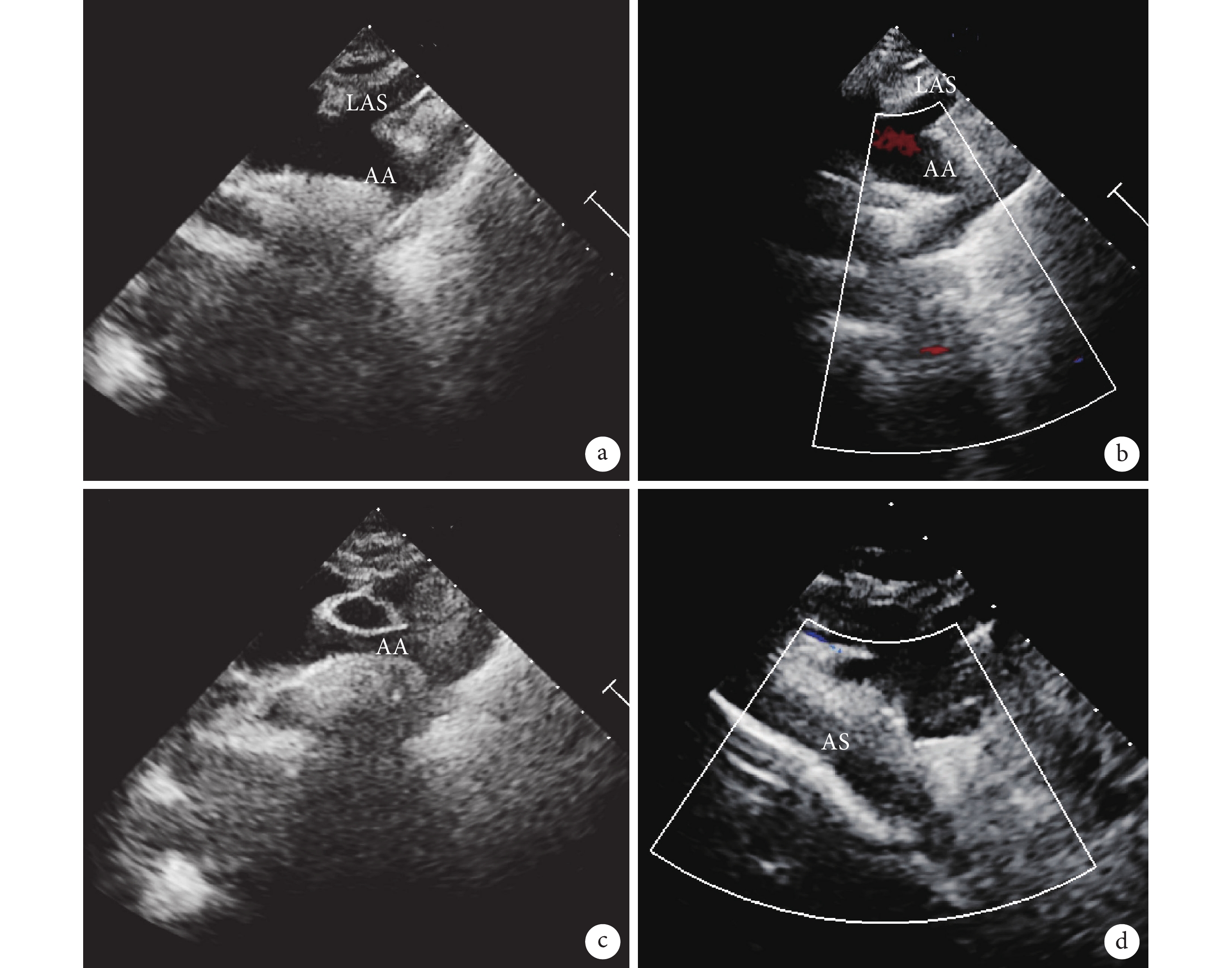 圖2
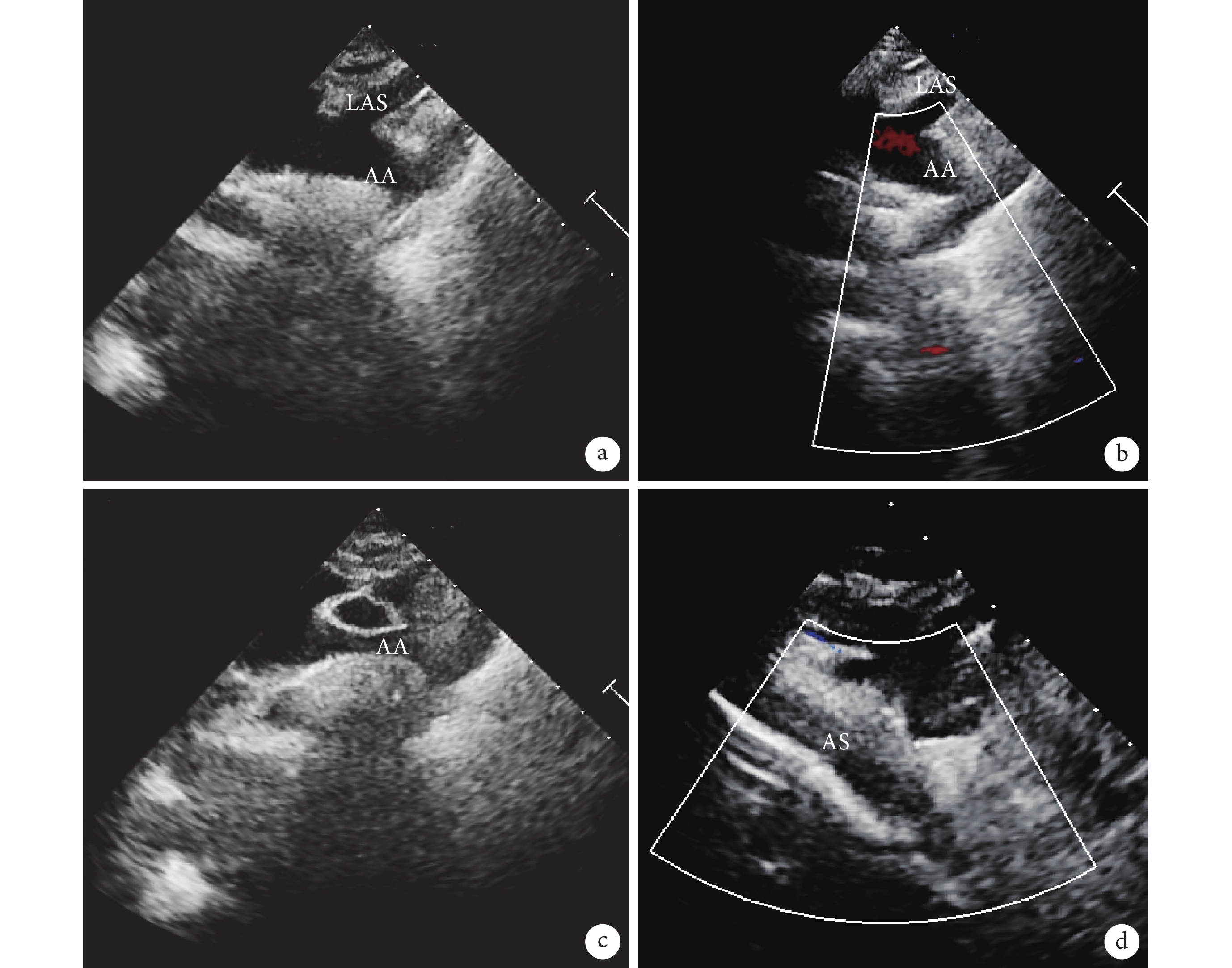
單純經食管超聲心動圖引導主動脈縮窄支架植入術
圖2
單純經食管超聲心動圖引導主動脈縮窄支架植入術
a:術前顯示主動脈弓降部縮窄;b:術前導管經股動脈到達縮窄處;c:超聲專用引導導絲通過狹窄處進入升主動脈,超聲顯示其紡錘形頭部;d:支架釋放;AA:主動脈弓;LSA:左鎖骨上動脈;AS:主動脈支架
隨訪及轉歸:出院后患者左上肢血壓115/76 mm Hg,患者無頭暈、間歇性跛行等癥狀。術后1個月復查超聲心動圖:降主動脈流速稍增快,2.1 m/s,壓差18 mm Hg,主動脈瓣前向血流稍快,峰速3.0 m/s,壓差36 mm Hg,輕度反流;二尖瓣輕度反流,三尖瓣輕度反流。
本研究經中國醫學科學院阜外醫院深圳醫院醫學倫理委員會批準,并已獲得患者的知情同意,并簽署知情同意書。
討論 CoA是一種較為常見的先天性血管畸形,發生率占所有先天性心臟缺陷的5%~8%[3],可通過外科矯治或介入治療。既往研究[4-5]表明,與外科治療相比。介入治療可顯著降低夾層、動脈瘤形成等并發癥的發生率。因此目前介入治療已經成為單純CoA的優先治療選項,但均在放射線引導下完成,具有相當的局限性,限制了其進一步推廣應用。以CoA患者為例,未經治療的CoA會增加妊娠期高血壓、子癇前期,甚至導致主動脈狹窄處破裂或發生夾層的風險[6-7],因此妊娠期患者最好于育齡期先行矯治治療。而針對妊娠期甚至育齡期女性患者,應盡可能規避輻射暴露風險以保證母胎安全。故而在本例中我們選擇為這一育齡期女性CoA患者實施純超聲引導CoA支架植入術。事實上,近年來非放射線引導經皮介入技術快速發展,目前已有文獻[8-13]報道在單純超聲引導下完成諸如房間隔缺損封堵和室間隔缺損封堵等多種簡單先心病以及瓣膜病介入治療的良好效果,其一方面更好地保障了患者及醫護人員的健康安全,另一方面也有助于其在基層醫院開展。國內暫無單純超聲引導下CoA介入治療相關報道,且在相關指南與專家共識[14-15]中均以放射線下介入治療為主。故本例是單純超聲引導技術在CoA介入治療的首次應用,也是單純超聲引導體系下的一次成功探索與嘗試,豐富了CoA患者的治療選項,更大程度地保障患者的獲益。
因經食管超聲心動圖(transesophageal echocardiography,TEE)的探頭位于食管或胃底內,可從心臟的后方向前觀察主動脈,主動脈位于超聲束的近場,可提供質量極佳的聲窗,而經胸超聲心動圖顯露主動脈走行圖像質量較差,故在本例中我們選擇通過TEE指導CoA支架置入。此外,TEE可實現術中實時監測球囊與支架的擴張,第一時間發現是否導致主動脈破裂、夾層等嚴重并發癥以利于及時處置。因導絲顯影不佳,在本例中我們還使用了超聲引導專用導絲,其頭部膨脹為菱形,能有效提高顯影效果,定位導絲位置。如無超聲引導專用導絲使用超硬導絲也可完成手術,但需要在置入導絲前測量并標記工作距離,即在術前先測量主動脈弓(約胸骨左側第2肋間)至外周血管穿刺點的距離,并由術者用手指測量法在導管上標記相應距離,當導管進入體內到達該距離后,即可旋轉導管,方便超聲探查導管的位置,并可防止導管插入過深,損傷主動脈及心臟組織。盡管術中主動脈破裂或穿孔較少見,一旦發現導絲或導管已經偏離主動脈及弓部途徑,應維持導管在原位,并抽吸導管內回血。如確定主動脈已穿孔,立即配血,密切監護呼吸及循環狀態,行急診開胸手術。
本文為單純超聲引導下CoA介入治療的首次報道,避免了電離輻射和使用造影劑,理論上可擴大介入治療CoA的適用人群,如嬰幼兒、育齡期和妊娠期女性、造影劑過敏及腎功能不全患者等。此外,目前已有研究[16-19]報道放射線下球囊擴張術治療兒童CoA以及一站式介入治療合并其他先心病的CoA患者,這亦是將來開展單純超聲引導下CoA介入治療的發展方向。
利益沖突:無。
作者貢獻:魏培堅、常鈞科負責數據收集、論文撰寫;盧耀星負責患者圍手術期管理、隨訪;張鳳文、房芳、王闖世負責論文審閱與修改,王首正、歐陽文斌負責參與手術與論文審閱;潘湘斌、萬俊義負責主刀手術、論文審閱。
1982年Singer等[1]報道了首例經導管球囊擴張成形術治療主動脈縮窄(coarctation of the aorta,CoA),經過數十年的發展后,目前經導管介入治療已在主動脈縮窄患者中廣泛應用[2],主要在放射線引導下完成。放射線引導下經導管介入治療CoA一方面由于依賴大型放射線設備限制了這一術式在基層醫院的開展,另一方面由于放射線禁忌導致部分患者如育齡期女性無法接受合適治療。而近年來單純超聲引導下介入治療諸如房間隔缺損和動脈導管未閉等簡單先天性心臟病(先心病)已證實治療效果良好,而在此我們報道1例在單純超聲引導下行CoA支架置入術治療CoA育齡期女性患者的病例
臨床資料 患者,女,27歲,因“發現心臟雜音3年余”入住中國醫學科學院阜外醫院深圳醫院。患者3年余前體檢發現心臟雜音,檢查心臟超聲心動圖提示降主動脈縮窄,無胸悶、氣促、頭暈、頭痛等不適,自測收縮壓180 mm Hg (1 mm Hg=0.133 kPa)以上,患者為行單純超聲引導介入治療CoA于我院門診就診,門診以“主動脈縮窄”于2023年2月13日收入我院。患者自發病以來精神食欲可,睡眠可,二便如常,雙下肢不水腫,體重無明顯變化。既往10余年前有甲狀腺功能亢進手術治療史。
入院后體格檢查:左上肢血壓172/97 mm Hg,心率60次/min,律齊,胸骨左緣第2肋間可聞及3級收縮期吹風樣雜音,腹平軟,肝脾肋下未觸及,雙下肢無水腫。經胸超聲心動圖示:降主動脈縮窄(4 mm),狹窄處流速增快,5.0 m/s,壓差100 mm Hg;主動脈瓣葉呈二葉式,右冠瓣、左冠瓣融合,瓣葉開放稍受限,輕度反流;左心房大、二尖瓣輕-中度反流,左心室射血分數(LVEF):62%。全主動脈計算機斷層血管造影(computed tomography angiography,CTA)顯示:CoA、胸主動脈側枝血管開放(主動脈弓降部局部變窄,最窄處約7 mm,距離左鎖骨下動脈開口約24 mm,其后管腔擴張,直徑約27 mm,并可見發出三支側枝血管,管徑3~5 mm,較粗側枝血管向上沿脊柱旁走行)(圖1a),左鎖骨下動脈近端擴張(直徑約13 mm,中遠段管徑7 mm),升主動脈、主動脈弓、腹主動脈及骼動脈管腔未見明顯狹窄或擴張,管腔內未見明顯內膜片及雙腔征。主動脈瓣瓣葉增厚,二葉主動脈瓣。患者“CoA”診斷明確,有手術指征,由于該患者系育齡期女性,結合患者治療意愿,經心臟團隊進一步評估后擬在單純超聲引導下行CoA支架置入術。
 圖1
CTA全主動脈三維容積重建
圖1
CTA全主動脈三維容積重建
a:介入前降主動脈縮窄;b:降主動脈支架位置及形態良好
手術在手術室進行,患者取仰臥位,全身麻醉后插入食管超聲備用。常規消毒、鋪巾,穿刺右股動脈,測量穿刺點到胸骨左側第2肋間(主動脈弓)的距離,標記為工作距離。按工作距離插入Luandquit超硬導絲,在食管超聲引導下將超硬導絲通過主動脈縮窄段,進入升主動脈內,沿導絲送入MPA2導管,撤出超硬導絲,沿MPA2導管送入超聲引導專用導絲,其頭部膨脹為菱形,超聲可以準確定位其位置。固定導絲,退出MPA2導管及6F動脈鞘,置入COOK12F輸送鞘。選擇NuMed 16 mm BIB球囊及3.9 cm CP覆膜支架,將支架裝載于球囊上,沿導絲將支架及球囊置入輸送鞘,球囊頂端緊貼導絲頭端的膨大部分,在超聲引導下通過膨大的導絲頭端準確定位支架起始處,調整位置滿意后置入NuMed 16 mm BIB球囊導管擴張狹窄部位,撤出球囊導管后置入NuMed 3.9 cm CP外膨脹支架,再次測壓,左上肢動脈壓104/56 mm Hg。經管道超聲提示CoA處血流速度2.6 m/s,壓差26 mm Hg,測得腹主動脈頻譜明顯改善,CoA處支架位置及形態良好(圖2),血流通暢。撤除導管、導絲及動脈鞘,穿刺點壓力止血器加壓固定。本次手術時間2 h。介入治療術后采用口服阿司匹林腸溶片100 mg(1次/d)行抗凝治療,介入治療后1 d轉出監護室,復查超聲心動圖示:降主動脈流速稍快,2.2 m/s,壓差19 mm Hg。CTA提示主動脈弓降部見金屬支架影,最窄處約13 mm,支架形態完整,內腔通暢(圖1b);升主動脈、主動脈弓管腔未見明顯狹窄或擴張。住院時間4 d。
 圖2
單純經食管超聲心動圖引導主動脈縮窄支架植入術
圖2
單純經食管超聲心動圖引導主動脈縮窄支架植入術
a:術前顯示主動脈弓降部縮窄;b:術前導管經股動脈到達縮窄處;c:超聲專用引導導絲通過狹窄處進入升主動脈,超聲顯示其紡錘形頭部;d:支架釋放;AA:主動脈弓;LSA:左鎖骨上動脈;AS:主動脈支架
隨訪及轉歸:出院后患者左上肢血壓115/76 mm Hg,患者無頭暈、間歇性跛行等癥狀。術后1個月復查超聲心動圖:降主動脈流速稍增快,2.1 m/s,壓差18 mm Hg,主動脈瓣前向血流稍快,峰速3.0 m/s,壓差36 mm Hg,輕度反流;二尖瓣輕度反流,三尖瓣輕度反流。
本研究經中國醫學科學院阜外醫院深圳醫院醫學倫理委員會批準,并已獲得患者的知情同意,并簽署知情同意書。
討論 CoA是一種較為常見的先天性血管畸形,發生率占所有先天性心臟缺陷的5%~8%[3],可通過外科矯治或介入治療。既往研究[4-5]表明,與外科治療相比。介入治療可顯著降低夾層、動脈瘤形成等并發癥的發生率。因此目前介入治療已經成為單純CoA的優先治療選項,但均在放射線引導下完成,具有相當的局限性,限制了其進一步推廣應用。以CoA患者為例,未經治療的CoA會增加妊娠期高血壓、子癇前期,甚至導致主動脈狹窄處破裂或發生夾層的風險[6-7],因此妊娠期患者最好于育齡期先行矯治治療。而針對妊娠期甚至育齡期女性患者,應盡可能規避輻射暴露風險以保證母胎安全。故而在本例中我們選擇為這一育齡期女性CoA患者實施純超聲引導CoA支架植入術。事實上,近年來非放射線引導經皮介入技術快速發展,目前已有文獻[8-13]報道在單純超聲引導下完成諸如房間隔缺損封堵和室間隔缺損封堵等多種簡單先心病以及瓣膜病介入治療的良好效果,其一方面更好地保障了患者及醫護人員的健康安全,另一方面也有助于其在基層醫院開展。國內暫無單純超聲引導下CoA介入治療相關報道,且在相關指南與專家共識[14-15]中均以放射線下介入治療為主。故本例是單純超聲引導技術在CoA介入治療的首次應用,也是單純超聲引導體系下的一次成功探索與嘗試,豐富了CoA患者的治療選項,更大程度地保障患者的獲益。
因經食管超聲心動圖(transesophageal echocardiography,TEE)的探頭位于食管或胃底內,可從心臟的后方向前觀察主動脈,主動脈位于超聲束的近場,可提供質量極佳的聲窗,而經胸超聲心動圖顯露主動脈走行圖像質量較差,故在本例中我們選擇通過TEE指導CoA支架置入。此外,TEE可實現術中實時監測球囊與支架的擴張,第一時間發現是否導致主動脈破裂、夾層等嚴重并發癥以利于及時處置。因導絲顯影不佳,在本例中我們還使用了超聲引導專用導絲,其頭部膨脹為菱形,能有效提高顯影效果,定位導絲位置。如無超聲引導專用導絲使用超硬導絲也可完成手術,但需要在置入導絲前測量并標記工作距離,即在術前先測量主動脈弓(約胸骨左側第2肋間)至外周血管穿刺點的距離,并由術者用手指測量法在導管上標記相應距離,當導管進入體內到達該距離后,即可旋轉導管,方便超聲探查導管的位置,并可防止導管插入過深,損傷主動脈及心臟組織。盡管術中主動脈破裂或穿孔較少見,一旦發現導絲或導管已經偏離主動脈及弓部途徑,應維持導管在原位,并抽吸導管內回血。如確定主動脈已穿孔,立即配血,密切監護呼吸及循環狀態,行急診開胸手術。
本文為單純超聲引導下CoA介入治療的首次報道,避免了電離輻射和使用造影劑,理論上可擴大介入治療CoA的適用人群,如嬰幼兒、育齡期和妊娠期女性、造影劑過敏及腎功能不全患者等。此外,目前已有研究[16-19]報道放射線下球囊擴張術治療兒童CoA以及一站式介入治療合并其他先心病的CoA患者,這亦是將來開展單純超聲引導下CoA介入治療的發展方向。
利益沖突:無。
作者貢獻:魏培堅、常鈞科負責數據收集、論文撰寫;盧耀星負責患者圍手術期管理、隨訪;張鳳文、房芳、王闖世負責論文審閱與修改,王首正、歐陽文斌負責參與手術與論文審閱;潘湘斌、萬俊義負責主刀手術、論文審閱。