永存左上腔靜脈(persistent left superior vena cava,PLSVC)伴右上腔靜脈(superior vena cava,SVC)缺失,也稱為孤立性永存左上腔靜脈(isolated persistent left superior vena cava,iPLSVC),是一種相對罕見的先天性體靜脈畸形。iPLSVC一般無癥狀,但會給全植入式靜脈輸液港(totally implantable venous access port,TIVAP)植入帶來臨床困難。我們報道1例41歲、需要新輔助化療聯合免疫治療的男性食管癌患者,在插入TIVAP前,通過多普勒超聲、計算機斷層掃描(computed tomography,CT)和血管三維重建,發現為PLSVC,右側SVC缺失。我們選擇左側入路,以左側鎖骨上窩胸鎖乳突肌鎖骨頭外側切跡作為穿刺點,導管尖端距頸根部穿刺點21.5 cm, 尖端位于PLSVC和右心房的交界處,也就是擴張的冠狀靜脈竇處。輸液港植入術順利,患者術后接受兩周期新輔助化療聯合免疫治療,術后為預防冠狀靜脈竇及上腔靜脈內血栓形成行抗凝治療,帶港期間無導管相關重大并發癥。
引用本文: 曾志凱, 鄒國穩, 喻本桐. 經孤立性永存左上腔靜脈植入靜脈輸液港一例. 中國胸心血管外科臨床雜志, 2024, 31(4): 639-642. doi: 10.7507/1007-4848.202312010 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
永存左上腔靜脈(persistent left superior vena cava,PLSVC)是一種先天性體靜脈變異體,是最常見的胸腔靜脈畸形,普通人群中發生率為0.3%~0.5%[1-5]。約10%的PLSVC合并右上腔靜脈(superior vena cava,SVC)缺如,稱為孤立性PLSVC[6-10]。這是一種極其罕見的靜脈異常。根據解剖特征和SVC返回方式,PLSVC常分為4種類型:Ⅰ型:PLSVC流入冠狀靜脈竇伴右SVC缺如,占10%~20%;Ⅱ型:無交通支的雙側SVC,占50%~60%;Ⅲ型:有交通支的雙側SVC,占25%~30%;Ⅳ型:PLSVC直接流入左心房,未經過冠狀靜脈竇,占10%~20%[5, 11]。 我們報道的這例為孤立性PLSVC,屬于PLSVCⅠ型。一般來說,PLSVC無癥狀,通常是體檢行胸部增強CT或在放置中心靜脈通路裝置時意外發現。
需要長期但間歇性使用靜脈通路的患者非常適合放置全植入式靜脈輸液港(totally implantable venous access port,TIVAP),這些患者通常每周或每月接受化療或輸血治療。TIVAP一般選擇右側入路,但另外一些患者由于皮膚感染、創傷或右側胸壁腫瘤和心靜脈回流的解剖變異等原因,不能在右側入路植入皮下裝置。本例中心靜脈畸形的食管癌患者就是選擇左側入路植入TIVAP,以左側鎖骨上窩胸鎖乳突肌鎖骨頭外側切跡作為穿刺點置入導管,導管尖端置于擴張的冠狀靜脈竇處,也就是孤立性PLSVC進入右心房的開口處。隨著生活水平提高,患者對改善生活質量的要求越來越高,對于大部分癌癥患者來說,輸液港可以明顯提高其生活質量。由于輸液港、心臟起搏器等中心靜脈通路設備在臨床中的普及,越來越多的臨床醫生可能在工作中遇見心臟靜脈回流的解剖變異。故而在植入中心靜脈通路裝置前,醫生對患者中心靜脈有無畸形應進行常規評估,且應具備這一基本能力,以避免血管損傷等不必要的嚴重并發癥。
臨床資料 患者,男,41歲,食管癌,因進行性吞咽困難1個月入院。在植入TIVAP之前發現他同時是一個孤立性PLSVC患者。食管計算機斷層掃描(computed tomography,CT)、超聲電子胃鏡檢查及病理活檢明確診斷為食管癌。據Machevin-Surugue等[12-13]報道,冠狀靜脈竇擴張的患者有75%以上存在PLSVC,此患者心臟多普勒超聲顯示冠狀靜脈竇擴張(圖1),提示其存在PLSVC可能。患者的胸部增強CT掃描顯示,右頭臂靜脈經無名靜脈流入左SVC, PLSVC經冠狀靜脈竇流入右心房,異常的左奇靜脈在降主動脈旁上升,流入PLSVC(圖2a~c)。術前我們進行了血管的三維重建,從前部可見左側SVC,但右側SVC缺如。右無名靜脈與左無名靜脈合并匯入左側SVC,左側 SVC 從心臟左后方與擴張的冠狀靜脈竇匯合,注入右心房(圖2d~f)。所有檢查均顯示患者為罕見的PLSVC合并右SVC缺如,即Ⅰ型 PLSVC。由于食管癌臨床分期為Ⅱ期(T3N0M0),術前需要進行新輔助化療聯合免疫治療。我們決定在數字減影血管造影(digital subtraction angiography,DSA)引導下植入靜脈輸液港。手術方式選擇左側入路,以左側鎖骨上窩胸鎖乳突肌鎖骨頭外側切跡作為穿刺點,導管尖端深度為21.5 cm(距頸根部穿刺點),位于擴張的冠狀靜脈竇處。皮下囊袋植入于左側胸肌筋膜上,在鎖骨下2 cm處。為預防靜脈血栓形成和心臟并發癥,患者術后接受華法林或皮下低分子肝素抗凝治療。術后患者復查胸部X線片,導管尖端位于脊柱正中線左側約1.5 cm處(圖3)。患者術后行新輔助化療聯合免疫治療兩周期,無明顯的導管相關并發癥。
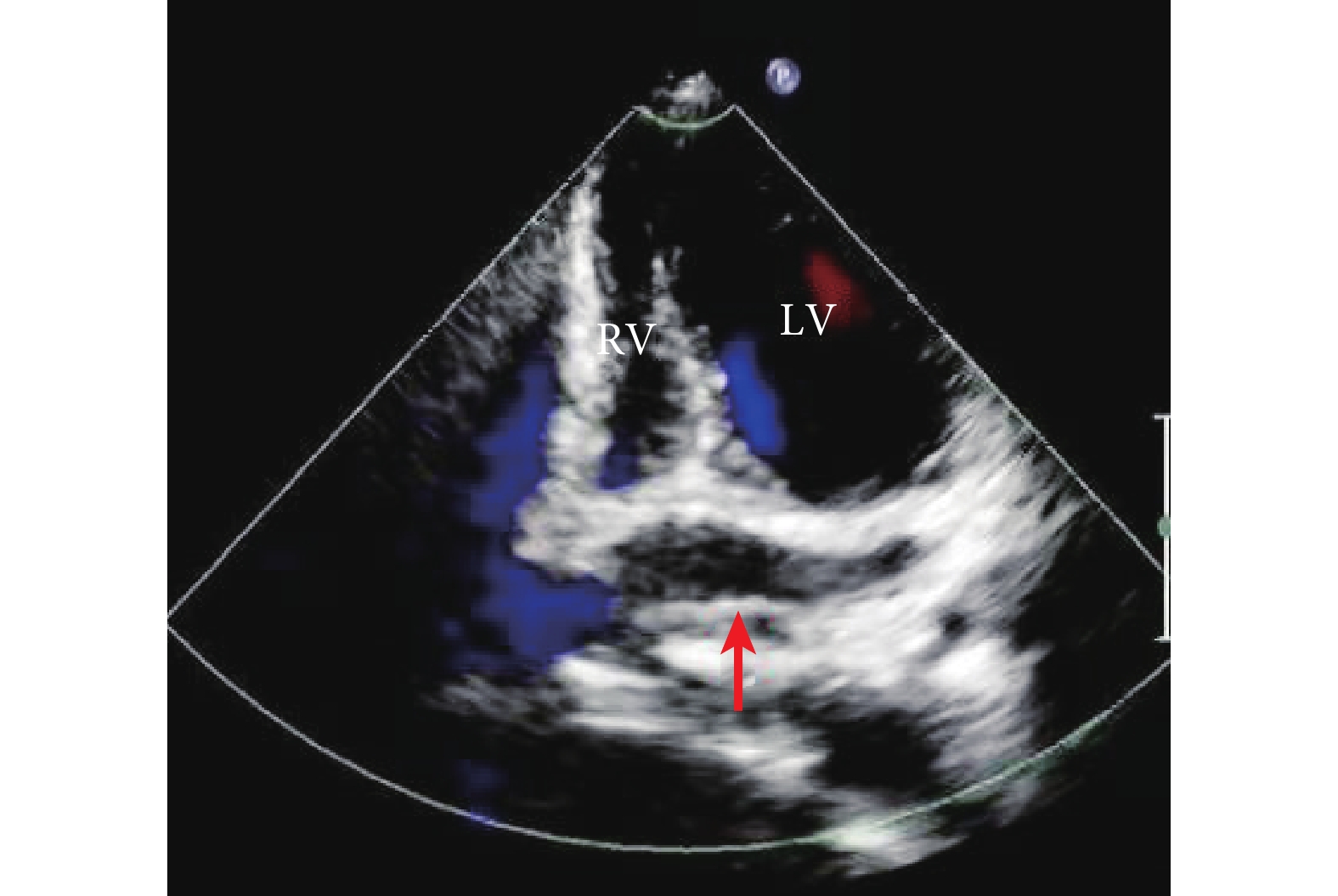 圖1
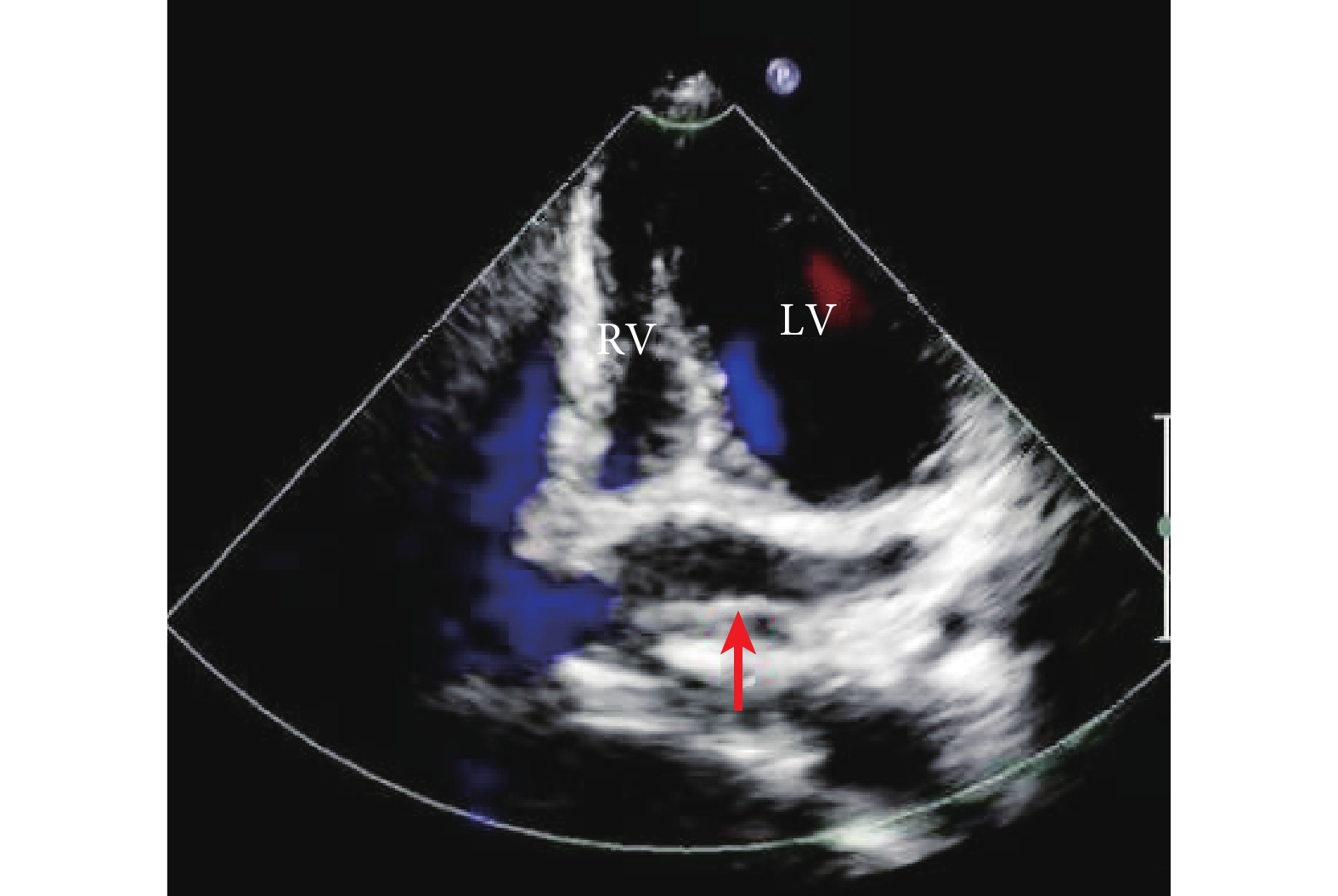
心臟多普勒超聲顯示冠狀靜脈竇擴張(紅色箭頭)
圖1
心臟多普勒超聲顯示冠狀靜脈竇擴張(紅色箭頭)
LV:左心室;RV:右心室
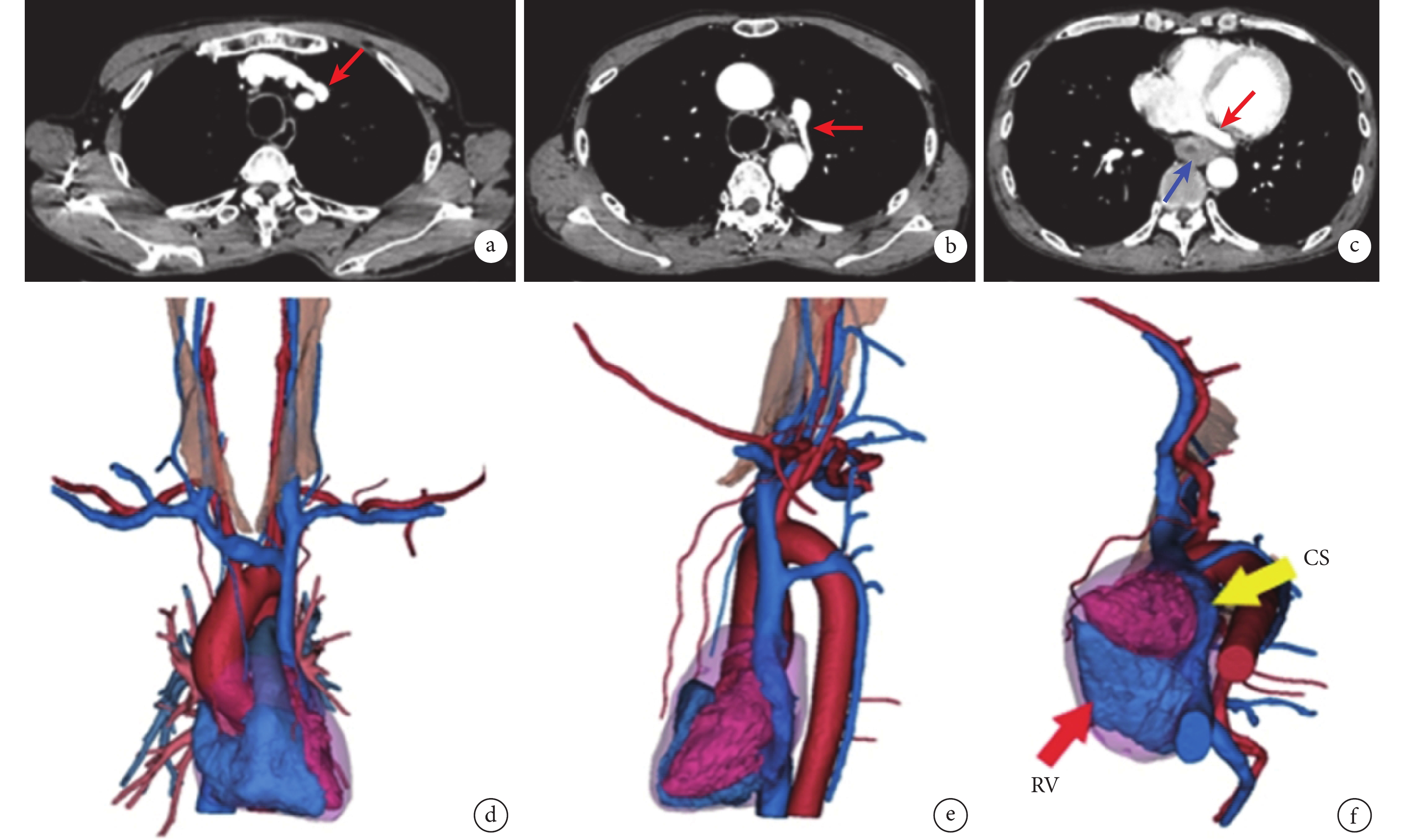 圖2
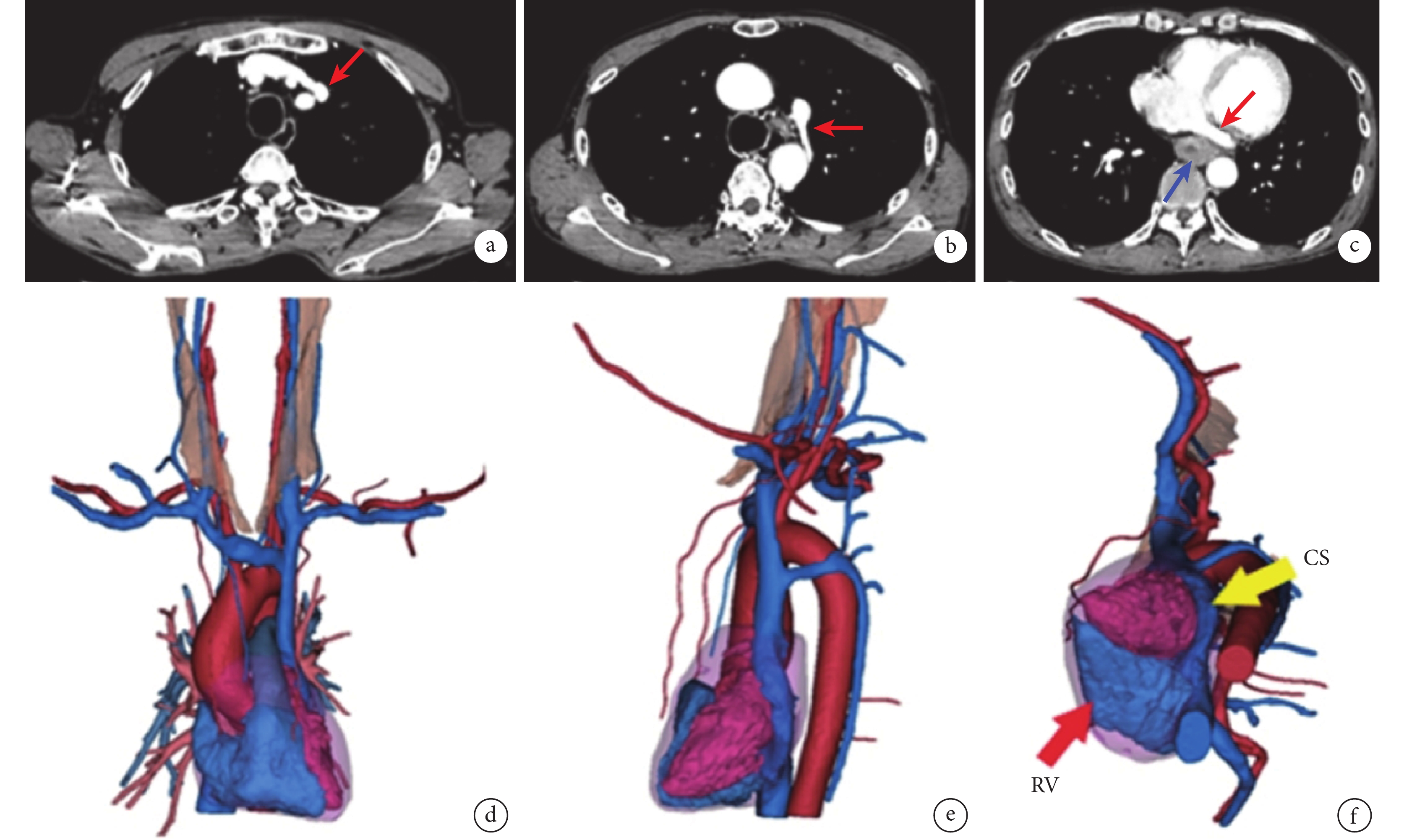
患者胸部增強CT和血管三維重建
圖2
患者胸部增強CT和血管三維重建
a:右無名靜脈匯入左上腔靜脈;b:左側奇靜脈匯入永存左上腔靜脈;c:左上腔靜脈最后匯入擴張的冠狀靜脈竇(紅色箭頭處),食管癌病灶(藍色箭頭處)位于冠狀靜脈竇后方;d:血管三維重建提示: 從前部可見左上腔靜脈,伴右側上腔靜脈缺如,右頭臂靜脈經無名靜脈流入左上腔靜脈;e:左側奇靜脈匯入永存左上腔靜脈;f :左側上腔靜脈從心臟左后方與擴張的冠狀靜脈竇(黃色箭頭處)匯合,注入右心房( 紅色箭頭處)
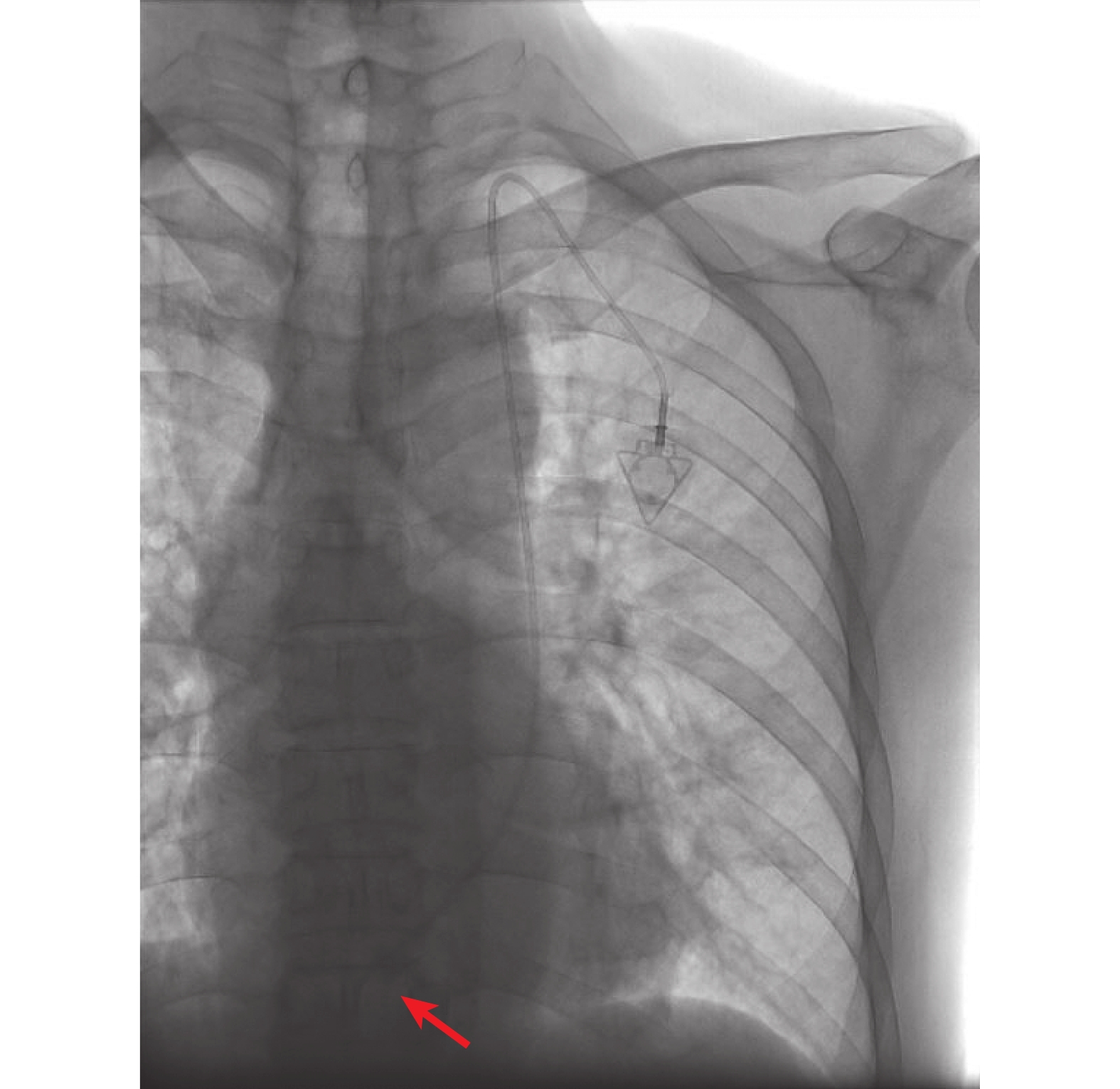 圖3
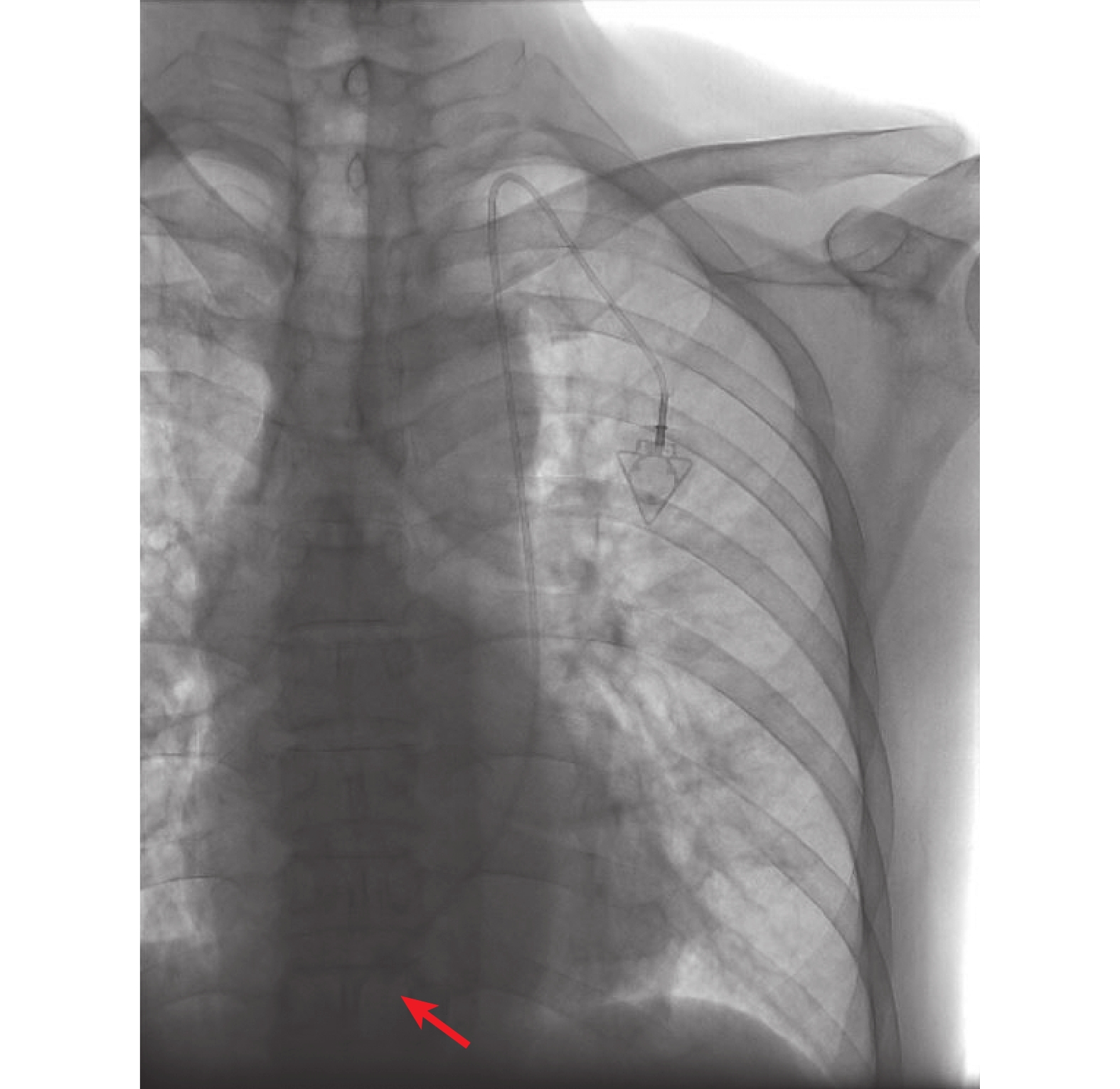
術后胸部X線片示,導管尖端(紅色箭頭處)位于脊柱正中線左側約1.5 cm
圖3
術后胸部X線片示,導管尖端(紅色箭頭處)位于脊柱正中線左側約1.5 cm
討論 人左SVC起源于胚胎期第3周的原始靜脈竇的左角。隨著胚胎左側無名靜脈的發育,左居維葉管和前主靜脈閉塞,左SVC逐漸退化形成馬歇爾韌帶;右居維葉管和前主靜脈發育形成右SVC。如果左前主靜脈未退化,則左SVC為永久性的;如果右居維葉管和前主靜脈退化,則右SVC缺失[5, 7, 14-18]。靜脈輸液港植入術是一種越來越常見的手術,外科醫生應該對患者的靜脈解剖結構有透徹的了解。胸部CT和心臟多普勒超聲可以顯示PLSVC與肺動脈、主動脈、無名靜脈之間的空間關系,對了解患者的靜脈解剖有重要幫助。
綜上所述,對于需要靜脈輸液港植入的患者,術前應進行胸部CT或心臟多普勒超聲檢查,并充分了解患者的心臟靜脈回流情況。通過以上檢查,可以減少先天性靜脈畸形患者植入中心靜脈裝置時的并發癥,防止導管植入錯誤的血管或血管損傷。此外,目前對于孤立性PLSVC植入TIVAP導管尖端的最佳位置和深度尚未達成共識。將導管尖端置入冠狀靜脈竇是否會增加血栓形成和心律失常等心臟相關并發癥的風險,目前仍缺乏足夠的循證醫學證據。本例在植入導管半年時間內,持續行抗凝治療,無明顯血栓并發癥發生。
目前國內外僅見少量的孤立性PLSVC的血管畸形報告[11,19-20],而在這種靜脈畸形的患者中施行輸液港植入術尚未見報道,我們屬于首次報道。這些先天性靜脈異常在中心靜脈通路裝置的植入過程中具有重要臨床意義,對于特殊先天性靜脈畸形患者,選擇常規右側入路可能會導致血管損傷和誤入,在植入靜脈港前,外科醫生應全面了解患者的靜脈回流以及其他先天性心臟異常,以確定植入路徑、導管尖端的位置和深度。
利益沖突:無。
作者貢獻:曾志凱負責論文設計、初稿撰寫,數據整理和分析;鄒國穩、喻本桐負責論文審閱與修改。
永存左上腔靜脈(persistent left superior vena cava,PLSVC)是一種先天性體靜脈變異體,是最常見的胸腔靜脈畸形,普通人群中發生率為0.3%~0.5%[1-5]。約10%的PLSVC合并右上腔靜脈(superior vena cava,SVC)缺如,稱為孤立性PLSVC[6-10]。這是一種極其罕見的靜脈異常。根據解剖特征和SVC返回方式,PLSVC常分為4種類型:Ⅰ型:PLSVC流入冠狀靜脈竇伴右SVC缺如,占10%~20%;Ⅱ型:無交通支的雙側SVC,占50%~60%;Ⅲ型:有交通支的雙側SVC,占25%~30%;Ⅳ型:PLSVC直接流入左心房,未經過冠狀靜脈竇,占10%~20%[5, 11]。 我們報道的這例為孤立性PLSVC,屬于PLSVCⅠ型。一般來說,PLSVC無癥狀,通常是體檢行胸部增強CT或在放置中心靜脈通路裝置時意外發現。
需要長期但間歇性使用靜脈通路的患者非常適合放置全植入式靜脈輸液港(totally implantable venous access port,TIVAP),這些患者通常每周或每月接受化療或輸血治療。TIVAP一般選擇右側入路,但另外一些患者由于皮膚感染、創傷或右側胸壁腫瘤和心靜脈回流的解剖變異等原因,不能在右側入路植入皮下裝置。本例中心靜脈畸形的食管癌患者就是選擇左側入路植入TIVAP,以左側鎖骨上窩胸鎖乳突肌鎖骨頭外側切跡作為穿刺點置入導管,導管尖端置于擴張的冠狀靜脈竇處,也就是孤立性PLSVC進入右心房的開口處。隨著生活水平提高,患者對改善生活質量的要求越來越高,對于大部分癌癥患者來說,輸液港可以明顯提高其生活質量。由于輸液港、心臟起搏器等中心靜脈通路設備在臨床中的普及,越來越多的臨床醫生可能在工作中遇見心臟靜脈回流的解剖變異。故而在植入中心靜脈通路裝置前,醫生對患者中心靜脈有無畸形應進行常規評估,且應具備這一基本能力,以避免血管損傷等不必要的嚴重并發癥。
臨床資料 患者,男,41歲,食管癌,因進行性吞咽困難1個月入院。在植入TIVAP之前發現他同時是一個孤立性PLSVC患者。食管計算機斷層掃描(computed tomography,CT)、超聲電子胃鏡檢查及病理活檢明確診斷為食管癌。據Machevin-Surugue等[12-13]報道,冠狀靜脈竇擴張的患者有75%以上存在PLSVC,此患者心臟多普勒超聲顯示冠狀靜脈竇擴張(圖1),提示其存在PLSVC可能。患者的胸部增強CT掃描顯示,右頭臂靜脈經無名靜脈流入左SVC, PLSVC經冠狀靜脈竇流入右心房,異常的左奇靜脈在降主動脈旁上升,流入PLSVC(圖2a~c)。術前我們進行了血管的三維重建,從前部可見左側SVC,但右側SVC缺如。右無名靜脈與左無名靜脈合并匯入左側SVC,左側 SVC 從心臟左后方與擴張的冠狀靜脈竇匯合,注入右心房(圖2d~f)。所有檢查均顯示患者為罕見的PLSVC合并右SVC缺如,即Ⅰ型 PLSVC。由于食管癌臨床分期為Ⅱ期(T3N0M0),術前需要進行新輔助化療聯合免疫治療。我們決定在數字減影血管造影(digital subtraction angiography,DSA)引導下植入靜脈輸液港。手術方式選擇左側入路,以左側鎖骨上窩胸鎖乳突肌鎖骨頭外側切跡作為穿刺點,導管尖端深度為21.5 cm(距頸根部穿刺點),位于擴張的冠狀靜脈竇處。皮下囊袋植入于左側胸肌筋膜上,在鎖骨下2 cm處。為預防靜脈血栓形成和心臟并發癥,患者術后接受華法林或皮下低分子肝素抗凝治療。術后患者復查胸部X線片,導管尖端位于脊柱正中線左側約1.5 cm處(圖3)。患者術后行新輔助化療聯合免疫治療兩周期,無明顯的導管相關并發癥。
 圖1
心臟多普勒超聲顯示冠狀靜脈竇擴張(紅色箭頭)
圖1
心臟多普勒超聲顯示冠狀靜脈竇擴張(紅色箭頭)
LV:左心室;RV:右心室
 圖2
患者胸部增強CT和血管三維重建
圖2
患者胸部增強CT和血管三維重建
a:右無名靜脈匯入左上腔靜脈;b:左側奇靜脈匯入永存左上腔靜脈;c:左上腔靜脈最后匯入擴張的冠狀靜脈竇(紅色箭頭處),食管癌病灶(藍色箭頭處)位于冠狀靜脈竇后方;d:血管三維重建提示: 從前部可見左上腔靜脈,伴右側上腔靜脈缺如,右頭臂靜脈經無名靜脈流入左上腔靜脈;e:左側奇靜脈匯入永存左上腔靜脈;f :左側上腔靜脈從心臟左后方與擴張的冠狀靜脈竇(黃色箭頭處)匯合,注入右心房( 紅色箭頭處)
 圖3
術后胸部X線片示,導管尖端(紅色箭頭處)位于脊柱正中線左側約1.5 cm
圖3
術后胸部X線片示,導管尖端(紅色箭頭處)位于脊柱正中線左側約1.5 cm
討論 人左SVC起源于胚胎期第3周的原始靜脈竇的左角。隨著胚胎左側無名靜脈的發育,左居維葉管和前主靜脈閉塞,左SVC逐漸退化形成馬歇爾韌帶;右居維葉管和前主靜脈發育形成右SVC。如果左前主靜脈未退化,則左SVC為永久性的;如果右居維葉管和前主靜脈退化,則右SVC缺失[5, 7, 14-18]。靜脈輸液港植入術是一種越來越常見的手術,外科醫生應該對患者的靜脈解剖結構有透徹的了解。胸部CT和心臟多普勒超聲可以顯示PLSVC與肺動脈、主動脈、無名靜脈之間的空間關系,對了解患者的靜脈解剖有重要幫助。
綜上所述,對于需要靜脈輸液港植入的患者,術前應進行胸部CT或心臟多普勒超聲檢查,并充分了解患者的心臟靜脈回流情況。通過以上檢查,可以減少先天性靜脈畸形患者植入中心靜脈裝置時的并發癥,防止導管植入錯誤的血管或血管損傷。此外,目前對于孤立性PLSVC植入TIVAP導管尖端的最佳位置和深度尚未達成共識。將導管尖端置入冠狀靜脈竇是否會增加血栓形成和心律失常等心臟相關并發癥的風險,目前仍缺乏足夠的循證醫學證據。本例在植入導管半年時間內,持續行抗凝治療,無明顯血栓并發癥發生。
目前國內外僅見少量的孤立性PLSVC的血管畸形報告[11,19-20],而在這種靜脈畸形的患者中施行輸液港植入術尚未見報道,我們屬于首次報道。這些先天性靜脈異常在中心靜脈通路裝置的植入過程中具有重要臨床意義,對于特殊先天性靜脈畸形患者,選擇常規右側入路可能會導致血管損傷和誤入,在植入靜脈港前,外科醫生應全面了解患者的靜脈回流以及其他先天性心臟異常,以確定植入路徑、導管尖端的位置和深度。
利益沖突:無。
作者貢獻:曾志凱負責論文設計、初稿撰寫,數據整理和分析;鄒國穩、喻本桐負責論文審閱與修改。