版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
白塞氏病(Beh?et’s disease,BD)于1937年由Hulusi Behcet醫師首次描述[1],后來被定義為一種病因不明的慢性、復發性全身炎癥性疾病[2],可累及多個系統,包括心血管、肺部、神經、關節及胃腸道等。不同地區和種族的患病率和臨床表現差異很大。BD引起的心血管受累少見但危及生命,需要積極的外科手術干預,文獻[3]報道這類患者的發病率為7%~38%。心血管受累的臨床表現多種多樣,包括亞臨床癥狀、靜脈血栓形成[4]、動脈病變伴有動脈瘤或動脈閉塞、急性心肌梗死、瓣膜功能障礙和心室血栓形成等[5-6]。
由于死亡率高且術后并發癥發生率高,如瓣周漏、復發性動脈瘤(伴或不伴破裂)[7],導致外科治療BD合并心血管損害一直具有挑戰性。既往研究[8-9]報道了BD復發性黏膜損害、皮膚損害和腸道損害,但迄今為止較少有研究關注BD患者的心血管損害,以及外科治療同期抗炎和免疫抑制治療,特別是在心血管手術前接受抗炎和免疫抑制治療。目前,術后抗炎和免疫抑制可改善術后并發癥并減少心血管再手術已達成共識[10],然而,術前免疫抑制治療對BD的獲益尚不清楚。
因此,本研究描述了合并心血管損害且需手術治療的BD患者的臨床特點,并評估了影響并發癥發生的危險因素及術前免疫抑制治療的有效性。
1 資料與方法
1.1 臨床資料和分組
回顧性分析2012—2021年廣東省人民醫院因BD心血管受累行心血管手術患者。納入標準:診斷為BD合并心血管病變并且接受心血管手術患者。排除標準:考慮為疑似BD但最終未確診患者;明確診斷BD合并心血管受累但未達到手術指征患者。根據術前是否接受免疫抑制治療將患者分為免疫抑制組和非免疫抑制組。
從電子檔案中收集患者的人口學特征、臨床特征、手術數據及臨床預后,收集術前紅細胞沉降率(erythrocyte sedimentation rate,ESR)、C反應蛋白、肝腎功能指標、風濕免疫指標等實驗室檢查結果。術后并發癥定義為死亡、經超聲心動圖或冠狀動脈造影證實的任何室間隔夾層、動脈瘤(有或無破裂)、血栓形成、動脈內漏、瓣周漏、瓣周膿腫、感染性心內膜炎、人工材料感染、敗血癥、急性BD復發、瓣膜脫垂。每次手術后的并發癥均記錄為與患者最近一次手術相關。隨訪數據包括死亡和非心血管再次手術及上述其他并發癥(如瓣周漏等),通過查看門診就診記錄和電話問卷收集。
1.2 診斷標準
BD的診斷根據國際BD標準(international criteria for Beh?et’s disease,ICBD)[11]和日本疾病研究委員會修訂的BD完全型和不完全型診斷標準[12],或術中病理活檢。BD相關心血管病變的診斷由心臟超聲科、心臟外科、病理科和風濕科醫師根據超聲心動圖、手術和/或病理學表現共同評估。
1.3 手術方法及術前免疫抑制治療
采用胸骨正中切口,在低溫體外循環下行瓣膜置換和/或主動脈根部置換、升主動脈置換、主動脈弓置換、其他同期瓣膜手術。
通過監測ESR等炎癥指標變化和臨床表現評估和調整藥物。多學科醫療小組共同協作行術前管理并決定手術時機。術前免疫抑制治療在手術前1 d逐漸減少并停止使用。兩組患者在手術后均接受免疫抑制治療。
1.4 統計學分析
所有統計分析均采用SPSS 26.0軟件。連續變量以中位數(上下四分位數)[M(P25,P75)]表示,組間比較采用Mann-Whitney U檢驗。分類變量以頻數和百分比表示,組間比較采用Fisher確切概率法。采用Kaplan-Meier生存曲線進行生存分析,計算手術治療后并發癥的累積概率。采用單因素分析探討術后并發癥的危險因素。雙側檢驗水準α=0.05。
1.5 倫理審查
本研究經廣東省人民醫院倫理委員會批準(批準號:KY2024-044),除死亡外,其余患者均獲得患者知情同意。
2 結果
共納入28例BD患者,其中1例術前免疫抑制患者和1例非免疫抑制患者在我院接受第1次心臟手術后,分別于術后第3年和8年因瓣周漏再次于我院接受聯合術前免疫抑制的二次心臟手術。我院因術后隨訪心血管并發癥而進行的任何心血管再手術均視為新的手術病例,因此共納入30例次心血管手術。6例患者入院時無典型的BD癥狀或體征,但術中病理活檢符合白塞氏血管炎,術后隨即確診。免疫抑制組共15例手術,非免疫抑制組15例手術。
與非免疫抑制組相比,免疫抑制組疾病持續時間(確診BD到手術時間)更長(P=0.001),術前診斷率更高(P=0.017)且ESR更低(P=0.046)。兩組患者的性別、確診時和手術時的年齡、既往心血管手術史、心血管受累情況、其他實驗室檢查、體外循環時間和主動脈阻斷時間等差異均無統計學意義(P>0.05)。所有患者心血管病變類型,包括瓣膜反流28例(93.3%)、升主動脈擴張15例(50.0%)、動脈瘤5例(16.7%)、感染性心內膜炎3例(10.0%)。
患者的術前超聲特征表現為:24例重度主動脈瓣反流(85.7%),13例主動脈根部冗余(46.4%),3例主動脈瓣周漏(10.7%),8例右冠瓣脫垂(28.6%),3例無冠瓣脫垂(10.7%),2例左冠瓣脫垂(7.14%),1例右心室血栓(3.6%),3例主動脈-左心室分流(10.7%),1例左冠狀動脈-右心房分流(3.6%)。所有患者的平均左心室舒張末期內徑為(60.04±10.02)mm,左心室收縮末期內徑為(42.42±8.95)mm,左心室射血分數為54.29%±9.72%,升主動脈直徑為(34.83±7.39)mm,室間隔厚度為(9.88±1.79)mm。患者的基線和手術資料見表1。
藥物治療中位時間為10(3~28)d。30例次手術的手術方式、術前免疫抑制情況和臨床結果見附件。
免疫抑制組患者住院期間并發癥發生率低于非免疫抑制組(13.3% vs. 53.3%,P=0.008),主要并發癥為敗血癥(13.3% vs. 6.7%,P=0.540)。術前免疫抑制組患者中有1例(6.7%)因低心排血量綜合征合并膿毒癥院內死亡,非免疫抑制組患者無院內死亡病例,兩組間差異無統計學意義(P=1.000)。
其余患者出院后均獲得隨訪,中位隨訪時間為38.7(15.1,57.3)個月,術前免疫抑制組與非免疫抑制組隨訪時間差異無統計學意義[33.6(5.9,53.3)個月vs. 51.7(19.2,60.0)個月,P=0.287];見表2。隨訪期間,免疫抑制組患者3例(21.4%)死亡,非免疫抑制組患者1例(6.7%)死亡。log-rank檢驗顯示兩組長期生存率差異無統計學意義(26.7% vs. 6.7%,P=0.158);見圖1。
 圖1
兩組患者術后Kaplan-Meier生存曲線(P=0.158)
圖1
兩組患者術后Kaplan-Meier生存曲線(P=0.158)
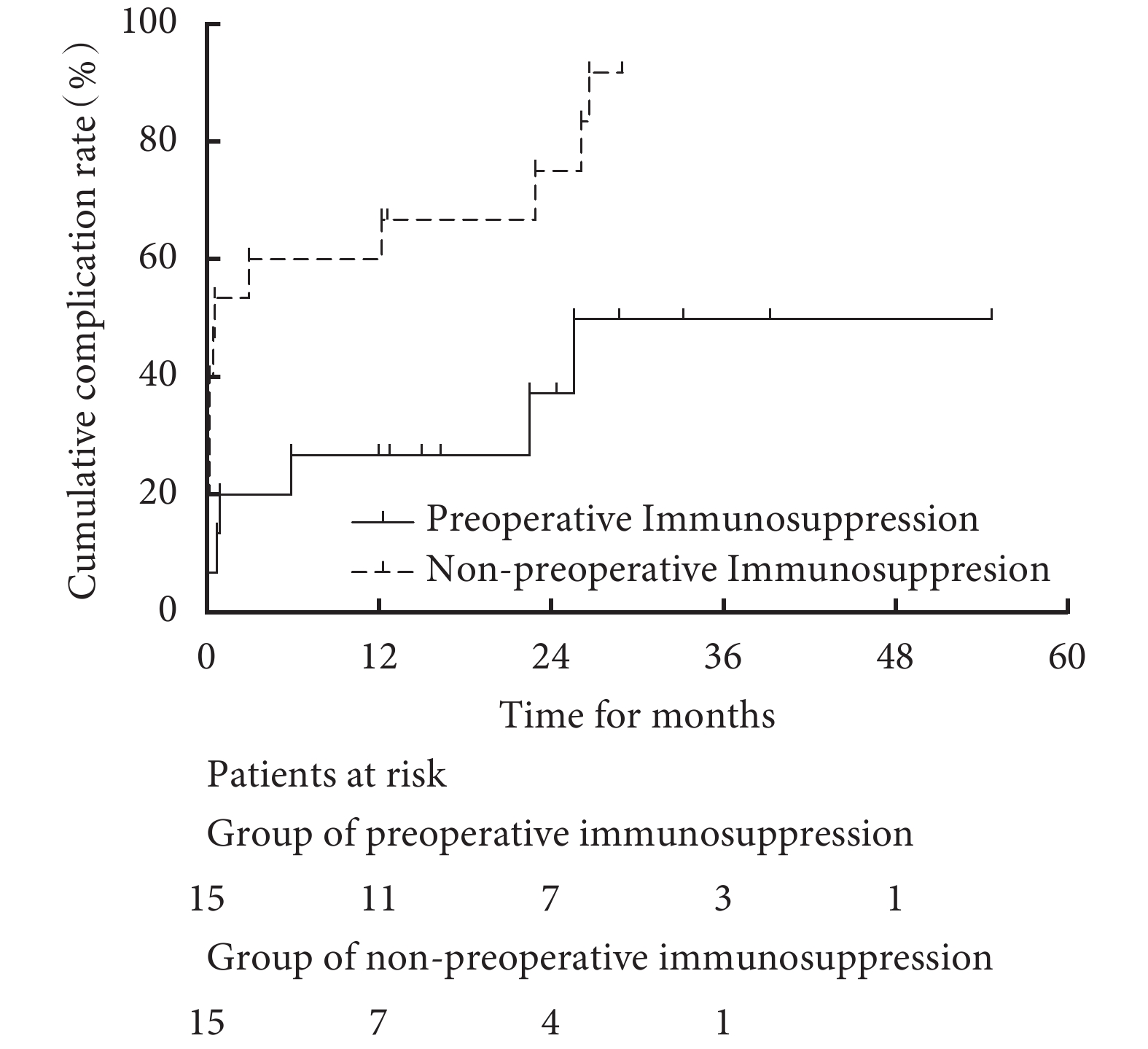
19例出現術后并發癥的心血管BD患者中,術后瓣周漏共5例,兩組差異無統計學意義(13.3% vs. 20.0%,P=1.000),其中有2例瓣周漏患者在我院接受心血管再次手術。經log-rank檢驗,免疫抑制組的累積并發癥發生率低于非免疫抑制組(P=0.013);見圖2。免疫抑制組與非免疫抑制組術后1個月(20% vs. 53%,P=0.058)、1年(27% vs. 60%,P=0.065)累計并發癥發生率差異無統計學意義,術后3年兩組累計并發癥發生率差異有統計學意義(47% vs. 92%,P=0.002)。
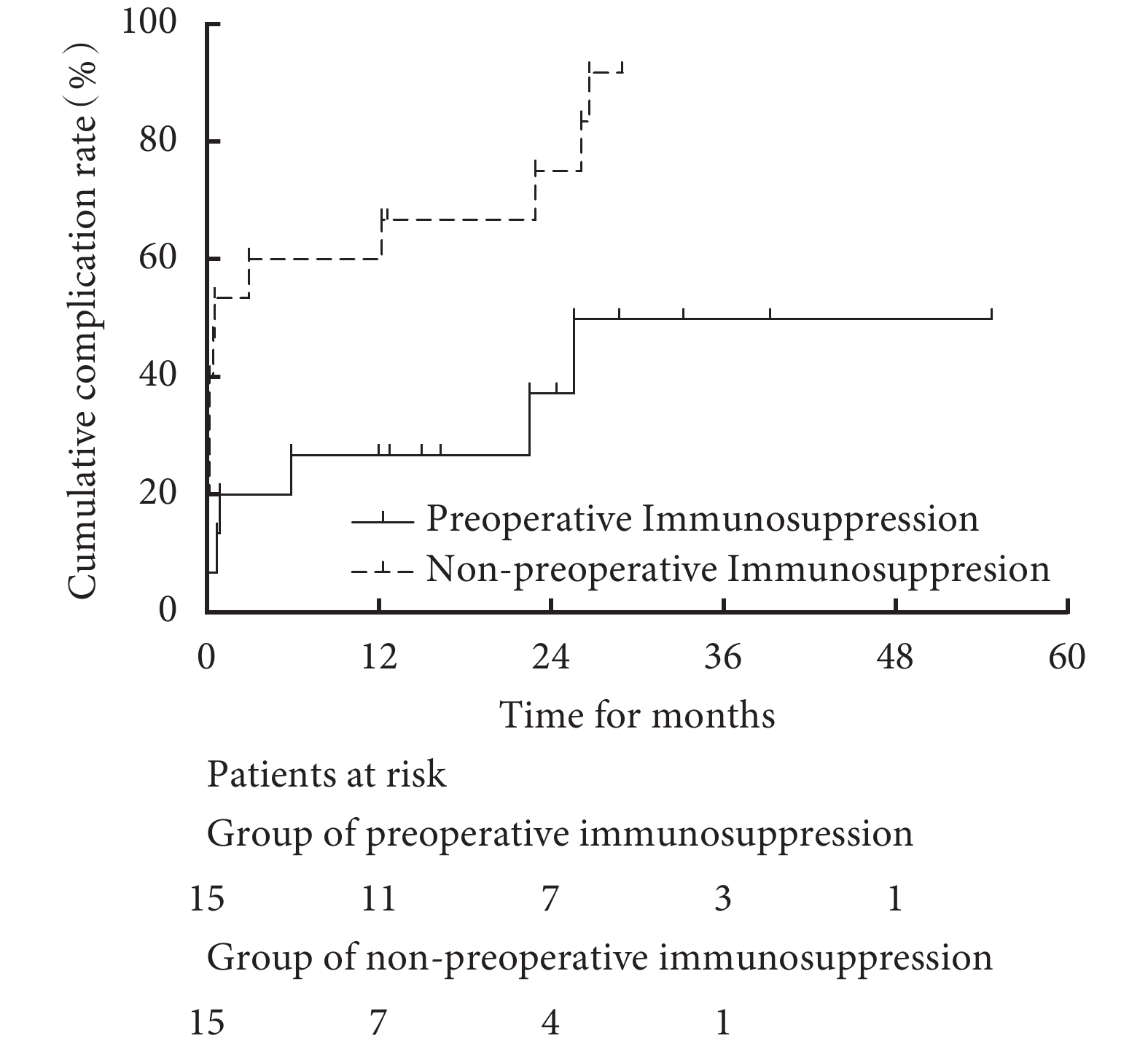 圖2
兩組患者的術后并發癥累積發生率(P=0.013)
圖2
兩組患者的術后并發癥累積發生率(P=0.013)
對兩組BD患者心臟外科術后并發癥的危險因素進行分析,結果顯示,高CRP、類風濕因子、天冬氨酸轉氨酶、手術年齡<30歲或>50歲、術前無免疫抑制治療是術后并發癥的危險因素;見表3。
3 討論
本研究總結了接受心臟外科手術的BD患者的臨床特征和預后,對于該疾病早期診斷尤為重要。本研究隊列中患者的臨床表現多樣,部分患者的心血管表現先于BD的典型癥狀出現[8-9,13],因此心血管醫師可能會漏掉BD的術前診斷,有時只能通過超聲心動圖發現BD特征,特別是在ICBD發布之前,這強調了超聲心動圖在早期識別BD中的診斷價值。既往研究[14-15]表明,主動脈瓣尖延長和環周假性動脈瘤改變是BD的影像學特征。BD心血管受累患者的手術結局及并發癥受許多因素影響,術前診斷是其中一個重要因素。在本研究隊列中,6例術前漏診的BD患者均在術后出現并發癥,2例出現瓣周漏,1例患者在我院接受二次主動脈瓣置換術。本研究中早期隊列未進行術前免疫抑制治療的患者比例較高,可能是由早期術前診斷率較低導致。ICBD的應用提高了該類患者的BD術前診斷,更適用于評估可疑BD伴嚴重主動脈瓣反流患者[16]。
BD累及心血管的主要特征包括主動脈瓣嚴重反流、主動脈瓣脫垂和動脈瘤樣改變。此外,瓣周腫塊的存在被廣泛認為是BD的主要特征,甚至導致自發性夾層進入室間隔[17]。結合本研究病例,當超聲提示瓣膜或冠狀竇動脈瘤樣改變(圖3a),甚至有動脈瘤脫垂導致左心室流出道阻塞時,應高度懷疑BD。心內血栓是BD的一種罕見表現,超聲檢查可發現附著于心房或心室內的高回聲、均勻、局部或固定結構,血栓最常見于心室,其次是右心房,左心房較少見[18]。在心室內血栓伴或不伴肺栓塞的病例中,若無血栓栓塞高危因素,則應高度懷疑BD可能,結合臨床病史或通過手術標本的病理檢查來確診[18]。在本研究收集的病例中,某患者在心內血栓切除2年后再次出現右心室腫塊(超聲懷疑心室內血栓可能性大)(圖3b)。當觀察到主動脈根部冗余、動脈瘤樣改變時,鑒別BD和感染性心內膜炎非常重要。BD表現出無菌性動脈瘤樣改變,而感染性心內膜炎更常表現為感染性贅生物,且兩者的臨床表現、病原學及術中病理檢查有顯著差異。在BD和感染性心內膜炎的早期鑒別診斷中,經驗豐富的心臟超聲科醫師可提供很大幫助。在極少數情況下,BD患者也可能表現為冠狀動脈瘤,當患者主訴胸痛且超聲或冠狀動脈CT血管造影提示冠狀動脈瘤時,早期診斷和治療至關重要[19]。超聲心動圖仍然是診斷心內結構的最佳成像方式,尤其應警惕與BD相關的各種超聲表現,一旦出現這些特征,經食管超聲心動圖在檢測主動脈瓣受累、升主動脈假性動脈瘤的延伸以及心室夾層等方面具有明顯優勢。
 圖3
白塞氏病患者的超聲心動圖特征
圖3
白塞氏病患者的超聲心動圖特征
a:右冠狀竇動脈瘤(白色箭頭);b:心內血栓去除2年后出現右心室腫塊(血栓可能性大);LA:左心房;LV:左心室;RA:右心房;RV:右心室
本研究單因素分析提示,高CRP和類風濕因子、術前無免疫抑制治療是術后并發癥的危險因素。類風濕因子作為炎性疾病活動期的預測因子,與BD活動期的關系尚不明確。而既往研究[20]表明,ESR和CRP等反映疾病活動期的炎癥指標水平,有助于確定手術時機并預測免疫治療的有效性,并且對不良預后有較高的預測價值。術前應用免疫抑制劑可降低ESR水平,術后持續抗炎和免疫抑制劑治療以及ESR動態監測是改善預后的必要條件[20]。本研究單因素分析中,手術年齡<30歲或>50歲作為可能是預防術后并發癥的保護因素,目前并無相關研究證實,但有研究[21-22]表明BD所致心血管損害的患者年齡越小,其余生需要進行心血管手術以及發生再次手術等并發癥的可能性越大。
外科手術治療可挽救生命,但因其術后并發癥如瓣周漏和心血管再手術發生率高而具有挑戰性[23-24]。本研究顯示術后并發癥較為常見,住院期間、術后1個月、1年、3年并發癥累計發生率分別為33%、37%、43%和73%,瓣周漏是最常見的并發癥(33.3%)。對這類患者術中切除的血管壁和主動脈瓣進行病理學檢查,表現為急性大面積內皮細胞丟失,伴有纖維蛋白沉積和中性粒細胞、漿細胞和淋巴組織細胞混合的密集浸潤[15,23]。過度的血管反應性和由此產生的炎癥導致嚴重的術后并發癥,包括出血、假體裂開、感染、血栓形成和移植物失敗等[3],因此,圍術期免疫抑制治療可以控制炎癥反應以減少術后并發癥。有研究[16]表明,當BD患者進行主動脈瓣置換時,術前免疫抑制治療可能降低術后并發癥發生率及死亡率。在本隊列中,術前接受免疫抑制治療患者相較于未接受免疫抑制治療患者預后有明顯改善,可驗證這一結論,并且后者相較于前者在病理特征中表現出更嚴重的主動脈和瓣膜炎癥反應(圖4)。若手術患者處于炎癥活動期,將人工假體縫合到發炎的主動脈根部可能會導致假體裂開而出現術后早期瓣周漏,對于此類患者圍術期免疫抑制治療可通過抑制主動脈根部及瓣膜炎癥來減少術后瓣周漏發生。在本研究中,術前免疫抑制組瓣周漏發生率相較于非免疫抑制組更低。有研究[24]證實,使用預制的帶瓣管道或同種移植物行主動脈根部置換術聯合術后免疫抑制治療可減少術后瓣周漏,該術式可能是避免人工瓣膜裂開的更優選擇。在本隊列中7例手術行主動脈根部置換術,術后出現1例瓣周漏,19例行主動脈瓣置換術,術后出現5例瓣周漏,主動脈根部置換術后瓣周漏發生率更低,但差異無統計學意義(P=0.226)。綜上所述,圍術期免疫抑制治療是有必要的,特別是術前免疫抑制治療可能帶來手術預后獲益,對于部分心功能不全患者,術前應用正性肌力藥物和利尿劑穩定心血管癥狀可為術前免疫抑制治療提供條件,但對于術前危急狀態患者,為行術前免疫抑制治療而推遲手術并不可行,此時術后免疫抑制治療顯得尤為重要。
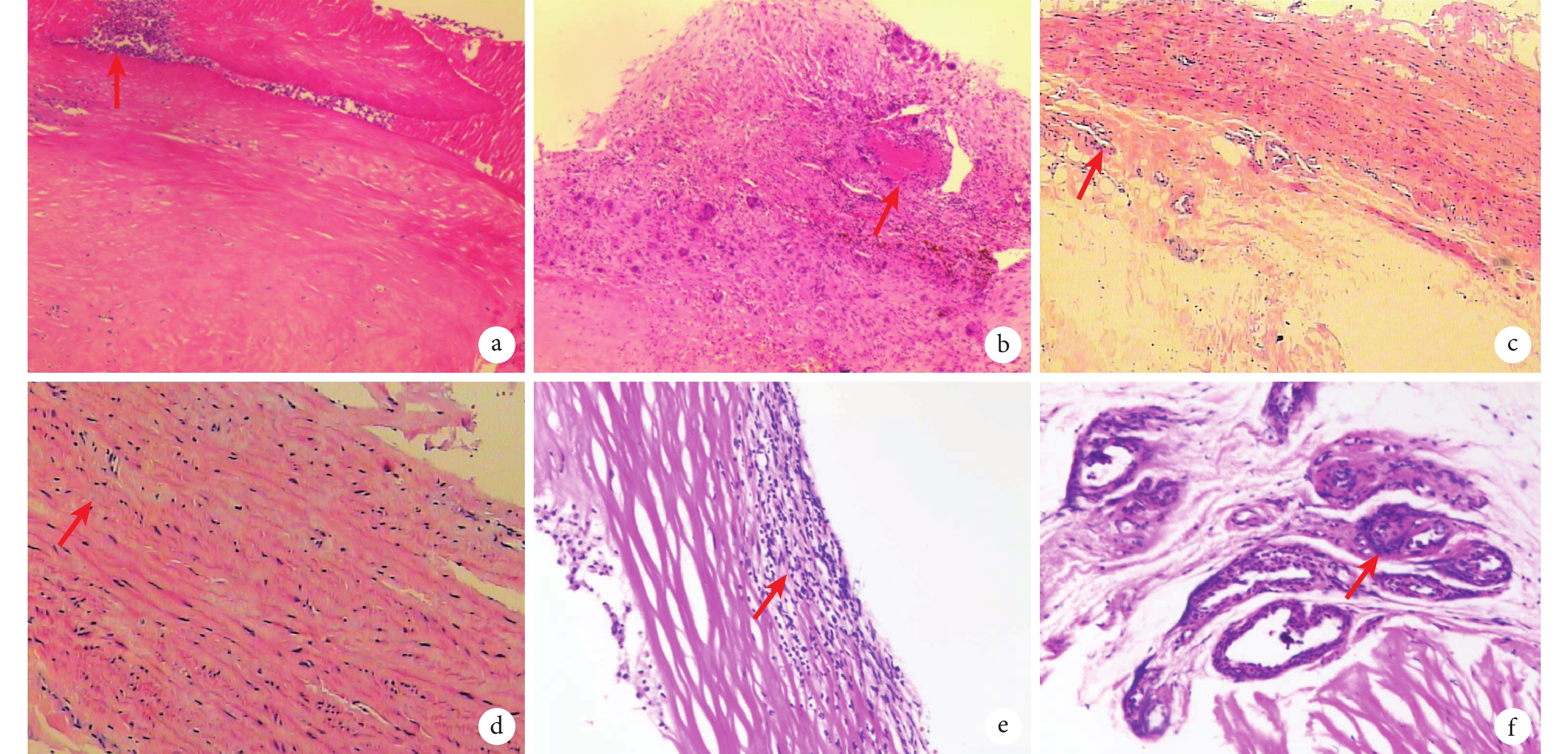 圖4
白塞氏病累及主動脈壁和瓣膜
圖4
白塞氏病累及主動脈壁和瓣膜
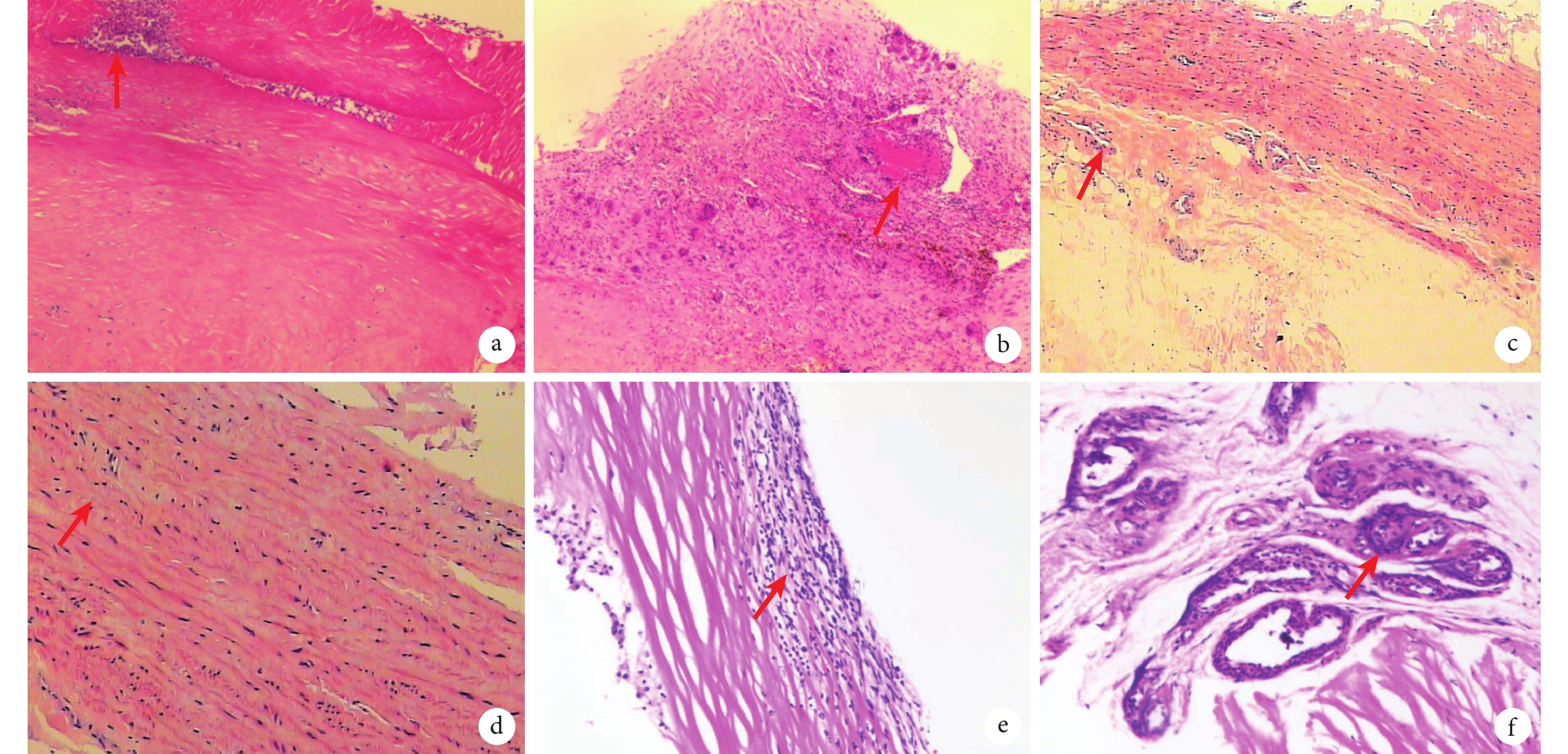
a:廣泛內皮細胞損傷伴纖維蛋白沉積;b:未接受術前免疫抑制治療的患者,急性內皮炎伴內皮脫落(箭頭),多發性炎癥細胞浸潤,壞死及含鐵血黃素沉積;觀察到混合多核巨細胞、中性粒細胞和淋巴細胞密集浸潤,與感染性心內膜炎特征相似;c~d:接受術前免疫抑制治療的患者,主動脈壁表現為內皮缺失,炎癥細胞浸潤和纖維蛋白沉積較少;e:術前接受高劑量免疫抑制治療的患者,新生血管出現明顯透明變性和嚴重炎癥反應(f,箭頭)
本研究中有1例患者術前給予大劑量免疫抑制劑治療,但術后病理仍表現出瓣膜和大血管免疫炎癥的極度惡化(圖4e~f),且最終預后較差。該患者自確診BD后接受免疫抑制治療,但治療并不規律,疾病控制欠佳。待BD進展處于急性活動期后采用大劑量免疫抑制治療,此時心臟超聲提示新發感染性心內膜炎,并突發急性左心衰竭予以無創輔助通氣后接受急診手術,術后BD炎癥和全身感染狀態仍無法得到有效控制,最終導致預后不良。因此我們認為合并心血管病變的BD患者,在接受免疫抑制治療的同時應盡早進行心血管受累評估,手術指征明確時及時行手術干預,避免BD炎癥狀態反復和感染風險增加導致病情惡化從而影響預后。
本研究顯示術前免疫抑制治療能明顯降低術后并發癥發生率,但免疫抑制劑的使用也可能導致術后傷口延遲愈合、感染風險增加等[25]。本研究中,術前免疫抑制組雖然圍術期敗血癥發生率較高,但與非免疫抑制組相比差異無統計學意義,考慮可能與術前不同免疫抑制劑方案引發的圍術期感染風險增加程度不一有關,如上述患者術前行大劑量免疫抑制治療導致并發感染心內膜炎。另有研究[16]證實,術前潑尼松聯合環磷酰胺免疫抑制治療可有效減少術后瓣周漏和再次手術,但術前使用潑尼松龍和秋水仙堿方案的效果未得到證實[26],因此術前免疫抑制治療的藥物方案和藥物劑量對減少術后瓣周漏及再次手術并發癥方面的獲益以及對增加圍術期感染的風險均相關,這凸顯了多學科合作和個體化決策的重要性,需要未來更大樣本量及更詳細的術前免疫抑制治療方案研究進一步證實。
本研究的局限性:本研究為回顧性研究,且樣本量較小。其次,各組間手術方式存在一定異質性。此外,非免疫抑制組中早期患者比例較高,可能存在偏倚。因此,雖然本研究通過有限樣本量患者證明了術前使用免疫抑制劑的優越性,但未來需要更大規模的臨床試驗驗證該研究結果。
手術治療可挽救合并心血管損害BD患者的生命,但術后并發癥尤其是瓣周漏發生率較高。盡早發現BD患者的心血管損害,并在術前接受免疫抑制治療聯合及時的外科干預可能會減少此類患者的術后并發癥。
利益沖突:無。
作者貢獻:陳帆宇負責實施研究,文章撰寫、審閱及指導;葉蘭心負責數據收集、統計分析,文章撰寫;徐子研負責數據收集、統計分析,作圖,文章撰寫;陳歐迪、卿洪琨負責實施研究,文章審閱;甘禮溪負責數據收集,文章審閱及指導;王維騰負責收集數據,設計指導及實施研究;李欣負責實施研究,指導研究方向及研究設計,技術支持;崔陽負責實施研究,設計免疫抑制方案,技術支持;簡旭華負責實施研究,指導研究方向及研究設計,技術支持,文章審閱及指導。
白塞氏病(Beh?et’s disease,BD)于1937年由Hulusi Behcet醫師首次描述[1],后來被定義為一種病因不明的慢性、復發性全身炎癥性疾病[2],可累及多個系統,包括心血管、肺部、神經、關節及胃腸道等。不同地區和種族的患病率和臨床表現差異很大。BD引起的心血管受累少見但危及生命,需要積極的外科手術干預,文獻[3]報道這類患者的發病率為7%~38%。心血管受累的臨床表現多種多樣,包括亞臨床癥狀、靜脈血栓形成[4]、動脈病變伴有動脈瘤或動脈閉塞、急性心肌梗死、瓣膜功能障礙和心室血栓形成等[5-6]。
由于死亡率高且術后并發癥發生率高,如瓣周漏、復發性動脈瘤(伴或不伴破裂)[7],導致外科治療BD合并心血管損害一直具有挑戰性。既往研究[8-9]報道了BD復發性黏膜損害、皮膚損害和腸道損害,但迄今為止較少有研究關注BD患者的心血管損害,以及外科治療同期抗炎和免疫抑制治療,特別是在心血管手術前接受抗炎和免疫抑制治療。目前,術后抗炎和免疫抑制可改善術后并發癥并減少心血管再手術已達成共識[10],然而,術前免疫抑制治療對BD的獲益尚不清楚。
因此,本研究描述了合并心血管損害且需手術治療的BD患者的臨床特點,并評估了影響并發癥發生的危險因素及術前免疫抑制治療的有效性。
1 資料與方法
1.1 臨床資料和分組
回顧性分析2012—2021年廣東省人民醫院因BD心血管受累行心血管手術患者。納入標準:診斷為BD合并心血管病變并且接受心血管手術患者。排除標準:考慮為疑似BD但最終未確診患者;明確診斷BD合并心血管受累但未達到手術指征患者。根據術前是否接受免疫抑制治療將患者分為免疫抑制組和非免疫抑制組。
從電子檔案中收集患者的人口學特征、臨床特征、手術數據及臨床預后,收集術前紅細胞沉降率(erythrocyte sedimentation rate,ESR)、C反應蛋白、肝腎功能指標、風濕免疫指標等實驗室檢查結果。術后并發癥定義為死亡、經超聲心動圖或冠狀動脈造影證實的任何室間隔夾層、動脈瘤(有或無破裂)、血栓形成、動脈內漏、瓣周漏、瓣周膿腫、感染性心內膜炎、人工材料感染、敗血癥、急性BD復發、瓣膜脫垂。每次手術后的并發癥均記錄為與患者最近一次手術相關。隨訪數據包括死亡和非心血管再次手術及上述其他并發癥(如瓣周漏等),通過查看門診就診記錄和電話問卷收集。
1.2 診斷標準
BD的診斷根據國際BD標準(international criteria for Beh?et’s disease,ICBD)[11]和日本疾病研究委員會修訂的BD完全型和不完全型診斷標準[12],或術中病理活檢。BD相關心血管病變的診斷由心臟超聲科、心臟外科、病理科和風濕科醫師根據超聲心動圖、手術和/或病理學表現共同評估。
1.3 手術方法及術前免疫抑制治療
采用胸骨正中切口,在低溫體外循環下行瓣膜置換和/或主動脈根部置換、升主動脈置換、主動脈弓置換、其他同期瓣膜手術。
通過監測ESR等炎癥指標變化和臨床表現評估和調整藥物。多學科醫療小組共同協作行術前管理并決定手術時機。術前免疫抑制治療在手術前1 d逐漸減少并停止使用。兩組患者在手術后均接受免疫抑制治療。
1.4 統計學分析
所有統計分析均采用SPSS 26.0軟件。連續變量以中位數(上下四分位數)[M(P25,P75)]表示,組間比較采用Mann-Whitney U檢驗。分類變量以頻數和百分比表示,組間比較采用Fisher確切概率法。采用Kaplan-Meier生存曲線進行生存分析,計算手術治療后并發癥的累積概率。采用單因素分析探討術后并發癥的危險因素。雙側檢驗水準α=0.05。
1.5 倫理審查
本研究經廣東省人民醫院倫理委員會批準(批準號:KY2024-044),除死亡外,其余患者均獲得患者知情同意。
2 結果
共納入28例BD患者,其中1例術前免疫抑制患者和1例非免疫抑制患者在我院接受第1次心臟手術后,分別于術后第3年和8年因瓣周漏再次于我院接受聯合術前免疫抑制的二次心臟手術。我院因術后隨訪心血管并發癥而進行的任何心血管再手術均視為新的手術病例,因此共納入30例次心血管手術。6例患者入院時無典型的BD癥狀或體征,但術中病理活檢符合白塞氏血管炎,術后隨即確診。免疫抑制組共15例手術,非免疫抑制組15例手術。
與非免疫抑制組相比,免疫抑制組疾病持續時間(確診BD到手術時間)更長(P=0.001),術前診斷率更高(P=0.017)且ESR更低(P=0.046)。兩組患者的性別、確診時和手術時的年齡、既往心血管手術史、心血管受累情況、其他實驗室檢查、體外循環時間和主動脈阻斷時間等差異均無統計學意義(P>0.05)。所有患者心血管病變類型,包括瓣膜反流28例(93.3%)、升主動脈擴張15例(50.0%)、動脈瘤5例(16.7%)、感染性心內膜炎3例(10.0%)。
患者的術前超聲特征表現為:24例重度主動脈瓣反流(85.7%),13例主動脈根部冗余(46.4%),3例主動脈瓣周漏(10.7%),8例右冠瓣脫垂(28.6%),3例無冠瓣脫垂(10.7%),2例左冠瓣脫垂(7.14%),1例右心室血栓(3.6%),3例主動脈-左心室分流(10.7%),1例左冠狀動脈-右心房分流(3.6%)。所有患者的平均左心室舒張末期內徑為(60.04±10.02)mm,左心室收縮末期內徑為(42.42±8.95)mm,左心室射血分數為54.29%±9.72%,升主動脈直徑為(34.83±7.39)mm,室間隔厚度為(9.88±1.79)mm。患者的基線和手術資料見表1。
藥物治療中位時間為10(3~28)d。30例次手術的手術方式、術前免疫抑制情況和臨床結果見附件。
免疫抑制組患者住院期間并發癥發生率低于非免疫抑制組(13.3% vs. 53.3%,P=0.008),主要并發癥為敗血癥(13.3% vs. 6.7%,P=0.540)。術前免疫抑制組患者中有1例(6.7%)因低心排血量綜合征合并膿毒癥院內死亡,非免疫抑制組患者無院內死亡病例,兩組間差異無統計學意義(P=1.000)。
其余患者出院后均獲得隨訪,中位隨訪時間為38.7(15.1,57.3)個月,術前免疫抑制組與非免疫抑制組隨訪時間差異無統計學意義[33.6(5.9,53.3)個月vs. 51.7(19.2,60.0)個月,P=0.287];見表2。隨訪期間,免疫抑制組患者3例(21.4%)死亡,非免疫抑制組患者1例(6.7%)死亡。log-rank檢驗顯示兩組長期生存率差異無統計學意義(26.7% vs. 6.7%,P=0.158);見圖1。
 圖1
兩組患者術后Kaplan-Meier生存曲線(P=0.158)
圖1
兩組患者術后Kaplan-Meier生存曲線(P=0.158)
19例出現術后并發癥的心血管BD患者中,術后瓣周漏共5例,兩組差異無統計學意義(13.3% vs. 20.0%,P=1.000),其中有2例瓣周漏患者在我院接受心血管再次手術。經log-rank檢驗,免疫抑制組的累積并發癥發生率低于非免疫抑制組(P=0.013);見圖2。免疫抑制組與非免疫抑制組術后1個月(20% vs. 53%,P=0.058)、1年(27% vs. 60%,P=0.065)累計并發癥發生率差異無統計學意義,術后3年兩組累計并發癥發生率差異有統計學意義(47% vs. 92%,P=0.002)。
 圖2
兩組患者的術后并發癥累積發生率(P=0.013)
圖2
兩組患者的術后并發癥累積發生率(P=0.013)
對兩組BD患者心臟外科術后并發癥的危險因素進行分析,結果顯示,高CRP、類風濕因子、天冬氨酸轉氨酶、手術年齡<30歲或>50歲、術前無免疫抑制治療是術后并發癥的危險因素;見表3。
3 討論
本研究總結了接受心臟外科手術的BD患者的臨床特征和預后,對于該疾病早期診斷尤為重要。本研究隊列中患者的臨床表現多樣,部分患者的心血管表現先于BD的典型癥狀出現[8-9,13],因此心血管醫師可能會漏掉BD的術前診斷,有時只能通過超聲心動圖發現BD特征,特別是在ICBD發布之前,這強調了超聲心動圖在早期識別BD中的診斷價值。既往研究[14-15]表明,主動脈瓣尖延長和環周假性動脈瘤改變是BD的影像學特征。BD心血管受累患者的手術結局及并發癥受許多因素影響,術前診斷是其中一個重要因素。在本研究隊列中,6例術前漏診的BD患者均在術后出現并發癥,2例出現瓣周漏,1例患者在我院接受二次主動脈瓣置換術。本研究中早期隊列未進行術前免疫抑制治療的患者比例較高,可能是由早期術前診斷率較低導致。ICBD的應用提高了該類患者的BD術前診斷,更適用于評估可疑BD伴嚴重主動脈瓣反流患者[16]。
BD累及心血管的主要特征包括主動脈瓣嚴重反流、主動脈瓣脫垂和動脈瘤樣改變。此外,瓣周腫塊的存在被廣泛認為是BD的主要特征,甚至導致自發性夾層進入室間隔[17]。結合本研究病例,當超聲提示瓣膜或冠狀竇動脈瘤樣改變(圖3a),甚至有動脈瘤脫垂導致左心室流出道阻塞時,應高度懷疑BD。心內血栓是BD的一種罕見表現,超聲檢查可發現附著于心房或心室內的高回聲、均勻、局部或固定結構,血栓最常見于心室,其次是右心房,左心房較少見[18]。在心室內血栓伴或不伴肺栓塞的病例中,若無血栓栓塞高危因素,則應高度懷疑BD可能,結合臨床病史或通過手術標本的病理檢查來確診[18]。在本研究收集的病例中,某患者在心內血栓切除2年后再次出現右心室腫塊(超聲懷疑心室內血栓可能性大)(圖3b)。當觀察到主動脈根部冗余、動脈瘤樣改變時,鑒別BD和感染性心內膜炎非常重要。BD表現出無菌性動脈瘤樣改變,而感染性心內膜炎更常表現為感染性贅生物,且兩者的臨床表現、病原學及術中病理檢查有顯著差異。在BD和感染性心內膜炎的早期鑒別診斷中,經驗豐富的心臟超聲科醫師可提供很大幫助。在極少數情況下,BD患者也可能表現為冠狀動脈瘤,當患者主訴胸痛且超聲或冠狀動脈CT血管造影提示冠狀動脈瘤時,早期診斷和治療至關重要[19]。超聲心動圖仍然是診斷心內結構的最佳成像方式,尤其應警惕與BD相關的各種超聲表現,一旦出現這些特征,經食管超聲心動圖在檢測主動脈瓣受累、升主動脈假性動脈瘤的延伸以及心室夾層等方面具有明顯優勢。
 圖3
白塞氏病患者的超聲心動圖特征
圖3
白塞氏病患者的超聲心動圖特征
a:右冠狀竇動脈瘤(白色箭頭);b:心內血栓去除2年后出現右心室腫塊(血栓可能性大);LA:左心房;LV:左心室;RA:右心房;RV:右心室
本研究單因素分析提示,高CRP和類風濕因子、術前無免疫抑制治療是術后并發癥的危險因素。類風濕因子作為炎性疾病活動期的預測因子,與BD活動期的關系尚不明確。而既往研究[20]表明,ESR和CRP等反映疾病活動期的炎癥指標水平,有助于確定手術時機并預測免疫治療的有效性,并且對不良預后有較高的預測價值。術前應用免疫抑制劑可降低ESR水平,術后持續抗炎和免疫抑制劑治療以及ESR動態監測是改善預后的必要條件[20]。本研究單因素分析中,手術年齡<30歲或>50歲作為可能是預防術后并發癥的保護因素,目前并無相關研究證實,但有研究[21-22]表明BD所致心血管損害的患者年齡越小,其余生需要進行心血管手術以及發生再次手術等并發癥的可能性越大。
外科手術治療可挽救生命,但因其術后并發癥如瓣周漏和心血管再手術發生率高而具有挑戰性[23-24]。本研究顯示術后并發癥較為常見,住院期間、術后1個月、1年、3年并發癥累計發生率分別為33%、37%、43%和73%,瓣周漏是最常見的并發癥(33.3%)。對這類患者術中切除的血管壁和主動脈瓣進行病理學檢查,表現為急性大面積內皮細胞丟失,伴有纖維蛋白沉積和中性粒細胞、漿細胞和淋巴組織細胞混合的密集浸潤[15,23]。過度的血管反應性和由此產生的炎癥導致嚴重的術后并發癥,包括出血、假體裂開、感染、血栓形成和移植物失敗等[3],因此,圍術期免疫抑制治療可以控制炎癥反應以減少術后并發癥。有研究[16]表明,當BD患者進行主動脈瓣置換時,術前免疫抑制治療可能降低術后并發癥發生率及死亡率。在本隊列中,術前接受免疫抑制治療患者相較于未接受免疫抑制治療患者預后有明顯改善,可驗證這一結論,并且后者相較于前者在病理特征中表現出更嚴重的主動脈和瓣膜炎癥反應(圖4)。若手術患者處于炎癥活動期,將人工假體縫合到發炎的主動脈根部可能會導致假體裂開而出現術后早期瓣周漏,對于此類患者圍術期免疫抑制治療可通過抑制主動脈根部及瓣膜炎癥來減少術后瓣周漏發生。在本研究中,術前免疫抑制組瓣周漏發生率相較于非免疫抑制組更低。有研究[24]證實,使用預制的帶瓣管道或同種移植物行主動脈根部置換術聯合術后免疫抑制治療可減少術后瓣周漏,該術式可能是避免人工瓣膜裂開的更優選擇。在本隊列中7例手術行主動脈根部置換術,術后出現1例瓣周漏,19例行主動脈瓣置換術,術后出現5例瓣周漏,主動脈根部置換術后瓣周漏發生率更低,但差異無統計學意義(P=0.226)。綜上所述,圍術期免疫抑制治療是有必要的,特別是術前免疫抑制治療可能帶來手術預后獲益,對于部分心功能不全患者,術前應用正性肌力藥物和利尿劑穩定心血管癥狀可為術前免疫抑制治療提供條件,但對于術前危急狀態患者,為行術前免疫抑制治療而推遲手術并不可行,此時術后免疫抑制治療顯得尤為重要。
 圖4
白塞氏病累及主動脈壁和瓣膜
圖4
白塞氏病累及主動脈壁和瓣膜
a:廣泛內皮細胞損傷伴纖維蛋白沉積;b:未接受術前免疫抑制治療的患者,急性內皮炎伴內皮脫落(箭頭),多發性炎癥細胞浸潤,壞死及含鐵血黃素沉積;觀察到混合多核巨細胞、中性粒細胞和淋巴細胞密集浸潤,與感染性心內膜炎特征相似;c~d:接受術前免疫抑制治療的患者,主動脈壁表現為內皮缺失,炎癥細胞浸潤和纖維蛋白沉積較少;e:術前接受高劑量免疫抑制治療的患者,新生血管出現明顯透明變性和嚴重炎癥反應(f,箭頭)
本研究中有1例患者術前給予大劑量免疫抑制劑治療,但術后病理仍表現出瓣膜和大血管免疫炎癥的極度惡化(圖4e~f),且最終預后較差。該患者自確診BD后接受免疫抑制治療,但治療并不規律,疾病控制欠佳。待BD進展處于急性活動期后采用大劑量免疫抑制治療,此時心臟超聲提示新發感染性心內膜炎,并突發急性左心衰竭予以無創輔助通氣后接受急診手術,術后BD炎癥和全身感染狀態仍無法得到有效控制,最終導致預后不良。因此我們認為合并心血管病變的BD患者,在接受免疫抑制治療的同時應盡早進行心血管受累評估,手術指征明確時及時行手術干預,避免BD炎癥狀態反復和感染風險增加導致病情惡化從而影響預后。
本研究顯示術前免疫抑制治療能明顯降低術后并發癥發生率,但免疫抑制劑的使用也可能導致術后傷口延遲愈合、感染風險增加等[25]。本研究中,術前免疫抑制組雖然圍術期敗血癥發生率較高,但與非免疫抑制組相比差異無統計學意義,考慮可能與術前不同免疫抑制劑方案引發的圍術期感染風險增加程度不一有關,如上述患者術前行大劑量免疫抑制治療導致并發感染心內膜炎。另有研究[16]證實,術前潑尼松聯合環磷酰胺免疫抑制治療可有效減少術后瓣周漏和再次手術,但術前使用潑尼松龍和秋水仙堿方案的效果未得到證實[26],因此術前免疫抑制治療的藥物方案和藥物劑量對減少術后瓣周漏及再次手術并發癥方面的獲益以及對增加圍術期感染的風險均相關,這凸顯了多學科合作和個體化決策的重要性,需要未來更大樣本量及更詳細的術前免疫抑制治療方案研究進一步證實。
本研究的局限性:本研究為回顧性研究,且樣本量較小。其次,各組間手術方式存在一定異質性。此外,非免疫抑制組中早期患者比例較高,可能存在偏倚。因此,雖然本研究通過有限樣本量患者證明了術前使用免疫抑制劑的優越性,但未來需要更大規模的臨床試驗驗證該研究結果。
手術治療可挽救合并心血管損害BD患者的生命,但術后并發癥尤其是瓣周漏發生率較高。盡早發現BD患者的心血管損害,并在術前接受免疫抑制治療聯合及時的外科干預可能會減少此類患者的術后并發癥。
利益沖突:無。
作者貢獻:陳帆宇負責實施研究,文章撰寫、審閱及指導;葉蘭心負責數據收集、統計分析,文章撰寫;徐子研負責數據收集、統計分析,作圖,文章撰寫;陳歐迪、卿洪琨負責實施研究,文章審閱;甘禮溪負責數據收集,文章審閱及指導;王維騰負責收集數據,設計指導及實施研究;李欣負責實施研究,指導研究方向及研究設計,技術支持;崔陽負責實施研究,設計免疫抑制方案,技術支持;簡旭華負責實施研究,指導研究方向及研究設計,技術支持,文章審閱及指導。