版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
胰十二指腸切除術(pancreatoduodenectomy,PD)是治療胰頭部及壺腹周圍腫瘤,尤其是惡性腫瘤的主要術式,已被臨床應用90余年。PD手術需要全部或部分切除5~6個臟器,并將胰腺、膽道和胃分別與腸道吻合從而完成消化道重建,手術過程復雜,對患者創傷極大。近40年來,對于術前懷疑胰頭部良性、交界性以及低度惡性腫瘤性病變的患者,在保障根治的前提下,如何盡可能保留更多的器官、保持較好的消化功能、保障患者術后較高的生活質量,是胰腺外科醫生不斷追求探索的問題。基于此,1972年Beger等[1]首次報道了保留十二指腸的胰頭切除術(duodenum-preserving pancreatic head resection,DPPHR),主要用于慢性胰頭炎的治療,該術式能在完整切除病灶的同時盡可能保證患者的正常消化道解剖結構。近年來,隨著微創外科技術的蓬勃發展和“膜解剖”理論基礎在臨床的廣泛應用,華中科技大學同濟醫學院附屬同濟醫院膽胰外科(下文簡稱“本中心”)首次提出了腹腔鏡下保留十二指腸的全胰頭膜內切除術(intracapsular approach used in laparoscopic duodenum-preserving total pancreatic head resection,LDPPHRt)。本研究回顧性收集了本中心2020年4月至2024年6月期間完成的LDPPHRt患者的臨床資料,分析術前、術中及術后恢復情況并進行經驗總結。
1 資料和方案
1.1 研究對象
回顧性收集本中心2020年4月至2024年6月期間完成的所有LDPPHRt患者的臨床資料。
1.2 LDPPHRt術前準備
術前完善常規檢驗,包括血常規、肝腎功能、凝血功能等。所有患者術前均行上腹部薄層增強CT或增強MRI檢查,提示胰頭部良性、交界性或低度惡性腫瘤性病變,排除了遠處轉移,且具備明顯手術指征。利用CT或MRI的三維重建排除了重要血管和膽總管胰腺段受侵,并根據檢查結果決定是否需要完善超聲內鏡檢查及穿刺活檢。對于合并顯著胰腺炎、胰腺纖維化或高度懷疑惡性病變的患者,均不適宜實施該術式。
LDPPHRt遵循加速康復外科原則:術前6 h禁食、2 h禁飲,留置尿管,術前不常規留置胃管及機械性灌腸。
1.3 手術方法
采用氣管插管、全身麻醉。患者采用仰臥分腿位,根據手術需要可調整為頭高腳低、左右傾斜等體位。臍下做小切口,穿刺針建立人工氣腹,CO2氣腹壓≤12 mmHg(1 mmHg=0.133 kpa),氣腹壓根據患者麻醉檢測情況做適當調整。Trocar布局一般采用5孔法、V字形分布(圖1a)。
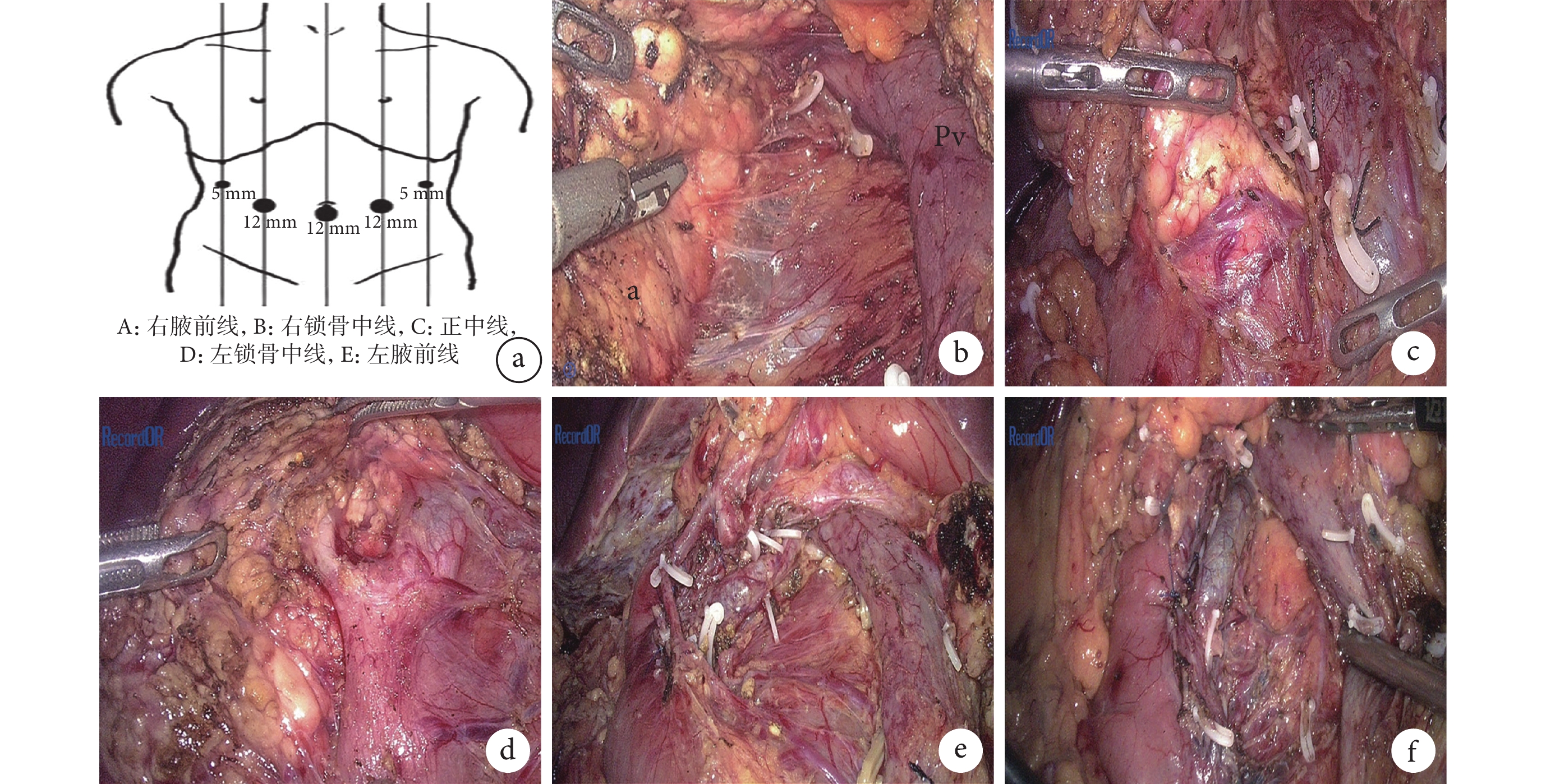 圖1
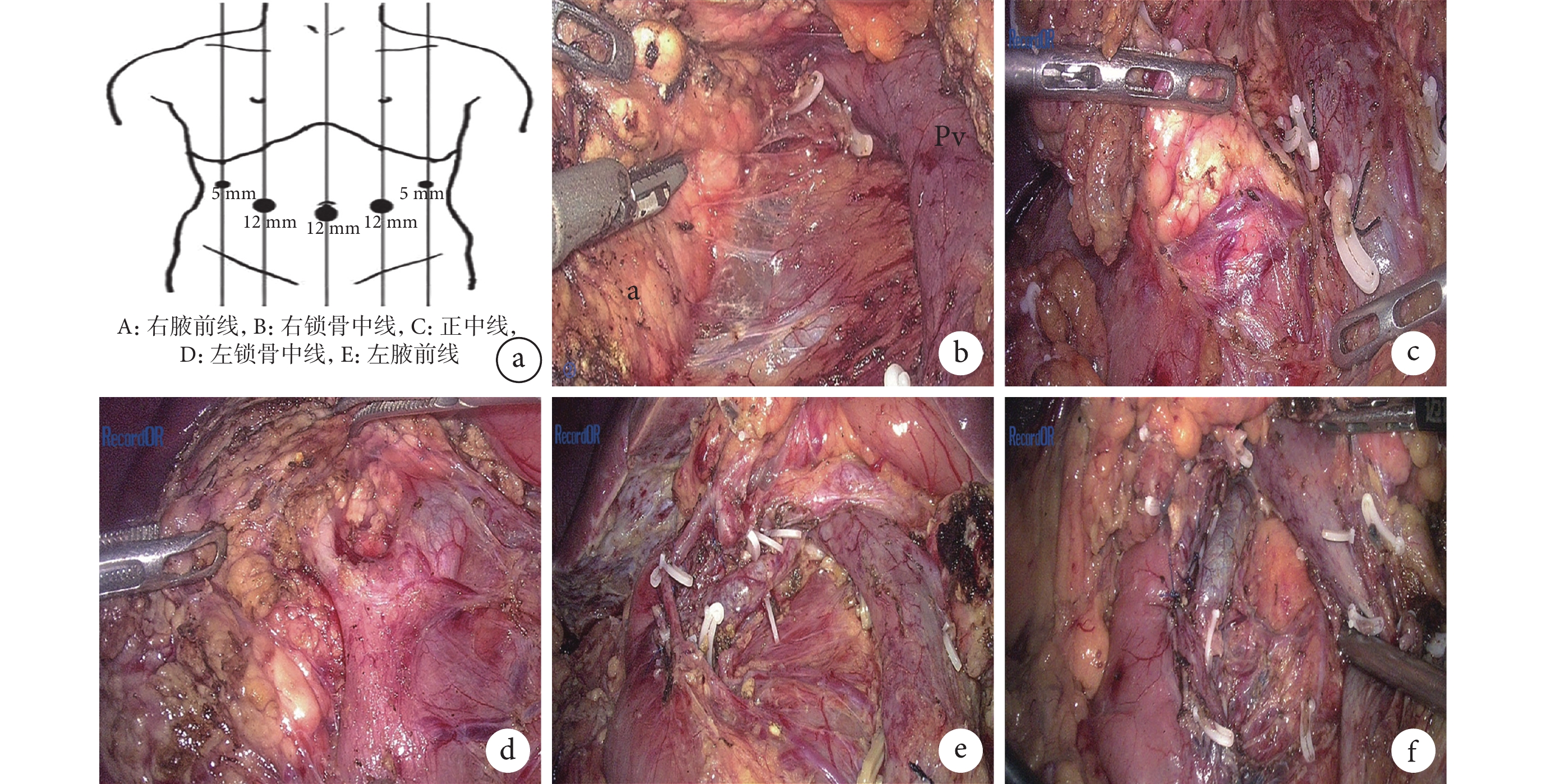
示LDPPHRt的Trocar布局圖及術中圖片
圖1
示LDPPHRt的Trocar布局圖及術中圖片
a:Trocar布局圖;b:胰腺包膜;c:分離胰腺鉤突;d:分離膽總管和壺腹部;e:分離并保護胰十二指腸動脈弓;f:修補十二指腸降部漿肌層
探查整個腹腔后打開胃結腸韌帶,降低結腸肝屈,沿橫結腸系膜前葉和胰頭十二指腸的間隙分離,必要時可離斷副右結腸靜脈、胃網膜右靜脈等匯入胃結腸干(Henle’s trunk)的分支靜脈以及主干,充分顯露胰頭十二指腸,不常規打開Kocker切口。
于胰頸部下緣分離顯露腸系膜上靜脈,沿腸系膜上靜脈正上方離斷胰腺,剪刀剪斷主胰管,胰腺上緣無需解剖分離肝總動脈和胃十二指腸動脈。在腹腔鏡放大效應下,可清晰看到胰腺表面有一層薄薄的包膜(圖1b)。在由胰頭下緣、十二指腸第三段和腸系膜上靜脈右側壁組成的三角形區域內打開胰腺包膜,沿胰腺實質和包膜間隙精細分離,分離過程中無需刻意顯露胰十二指腸下動靜脈,只離斷由包膜上血管發出的穿通進入胰腺實質的分支血管,由此將胰腺鉤突從腸系膜上靜脈后方分離出來(圖1c)。然后繼續沿胰腺實質和包膜的間隙由下向上、由左向右分離,直至將胰頭下緣從十二指腸第三段完全分開,并顯露膽總管左側壁。
將膽總管和壺腹部從胰腺實質內分離出來并保持其結構和血供的完整性,這是本術式的關鍵。通過顯露胰十二指腸上后靜脈來定位膽總管,在間隙內分離胰腺實質時可順勢將該靜脈保護并留置在包膜內,由上向下分離膽總管直至壺腹部,于壺腹部找到主胰管匯入點,結扎并離斷主胰管(圖1d)。從十二指腸球部和降部開始沿包膜間隙分離胰腺實質,注意保護好胰十二指腸動脈前弓和后弓,尤其是后弓(圖1e)。由于十二指腸降部和胰腺聯系緊密,缺乏固有的間隙,分離過程難免會損傷十二指腸漿肌層,可予以修補成形(圖1f)。對于個別膽總管被胰腺完全包裹的患者,可先沿十二指腸和胰腺間隙分離并找到壺腹部,由下向上分離膽總管,必要時可予以懸吊牽拉以方便顯露和分離。至此,整個胰頭部連同腫瘤被完整切除,切除組織送快速冰凍病理學檢查以了解標本性質。
距離屈氏韌帶約15 cm處離斷空腸,于結腸后系膜裂孔處將遠端空腸上提行胰腸吻合,采用植入式胰腸吻合[2],距胰腸吻合口45 cm處行腸腸吻合。胰腸吻合口前后方各放置引流管1根。
1.4 術后治療
術后給予心電監護、鼻導管吸氧、二代頭孢抗生素、補液、靜脈營養支持等,常規給予生長抑素抑制胰酶分泌,恢復進食后停止。術后第1、3、5、7天連續監測腹腔引流液淀粉酶情況,若淀粉酶<500 U/L且顏色清亮,予以拔除引流管。
1.5 觀察指標及評價標準
觀察指標:① 手術情況;② 術后情況及并發癥情況。
評價標準:根據中華醫學會外科學分會胰腺外科學組的標準定義胰腺術后胰瘺、膽瘺、胃排空延遲、術后出血等并發癥。
2 結果
本研究共納入75例LDPPHRt患者,其具體臨床病理資料見表1。
本組患者的術后首次下床時間、首次進食流質食物時間、術后住院時間等術后結果,以及術后病理結果見表1。術后發生并發癥18例(24.0%),其中B級胰瘺6例(8.0%)、術后出血5例(6.7%)、膽瘺4例(5.3%)、乳糜瘺2例(2.7%)、術后胃排空延遲4例(5.3%)、腹腔感染2例(2.7%)、肺部感染1例(1.3%)以及切口感染2例(2.7%)。術后30 d內再入院2例(2.7%),均為胰瘺患者,經保守治療及B超引導下穿刺置管引流后好轉出院;無術后90 d內死亡病例。
3 討論
微創化和保留器官功能是現代外科發展的趨勢。傳統的PD手術切除范圍大、重建復雜,患者的遠期生活質量可能受到不良影響。因此,對于胰頭部良性、交界性以及低度惡性腫瘤性病變患者,尤其是年輕患者,實施PD手術對于醫生和患者而言都是極大的挑戰。DPPHR的提出改善了這一現狀,該術式保留了術后胰腺內外分泌功能,提高了患者的遠期生活質量。最早期,DPPHR用于治療慢性胰腺炎,該術式大部分切除胰頭部炎性腫塊,解除其對膽總管和十二指腸的壓迫,僅保留十二指腸內側的部分胰腺組織,從而緩解疼痛癥狀,延緩慢性胰腺炎的進展。該術式逐漸衍生了Frey手術[3]、Berne手術[4]、Imaizumi手術[5]。直到Takada等[6]提出沿十二指腸內側完整切除胰頭,保留胰十二指腸動脈后弓、膽總管、膽囊以及十二指腸乳頭,由于該術式保留了十二指腸血供,避免了胰頭部胰腺組織剩余,提高了腫瘤的根治性,DPPHR才逐步由胰頭大部分切除演化為胰頭全切除,手術指征也由慢性胰腺炎過渡到胰頭部良性、交界性以及低度惡性腫瘤性病變。
近年來,“膜解剖”理論從基礎解剖學角度為臨床手術層面的研究提供了可能。2007年,Gockel等[7]從解剖學角度闡述了胰腺存在系膜結構,并提出了胰腺系膜的概念。該系膜位于胰頭后方、腸系膜上動脈右側,并從胰腺頭頸部及鉤突后方延伸至腹主動脈及下腔靜脈表面。之后Adham等[8]也提出了胰腺系膜三角的概念,該區域的前界是腸系膜上靜脈和門靜脈的后壁,后界位于腹主動脈及下腔靜脈前壁,內界是腹腔干右緣和腸系膜上動脈。與此同時,也有學者[9, 10]對胰后是否存在胰腺系膜提出了質疑,認為該區域缺乏明顯纖維鞘樣結構的存在,不符合“系膜”這一概念。
隨著科學技術的發展,以腹腔鏡技術為代表的微創外科日新月異,其具有視野清晰、操作精細的優勢,極大地推動了腹腔鏡下保留十二指腸的胰頭切除術(laparoscopic duodenum-preserving pancreatic head resection,LDPPHR)的可行性,同時也提高了安全性。本中心在“膜解剖”理論基礎的指導下,以腹腔鏡手術為平臺,在前期臨床實踐中發現胰腺表面存在一層薄薄的包膜,胰頭腹側為前包膜,背側為后包膜,等同于Gockel等[7]提出的胰腺系膜,而胰頭周圍主要血管弓和膽總管均走行于包膜外。因此,從胰頭前壁打開胰腺包膜,在包膜內完整切除胰頭組織,完整保留包膜的后壁及兩側壁,無須刻意游離保留血管弓,僅離斷其發出的進入胰腺實質的穿通支血管,原則上保留了胰十二指腸前后血管弓的完整性,該思想即LDPPHRt的理論基礎。本研究通過回顧性分析本中心開展的LDPPHRt患者的臨床資料,證實該術式是安全可行的。
盡管這幾年腹腔鏡胰腺外科手術得到了迅速發展,腹腔鏡下胰十二指腸切除術、胰體尾切除術等已廣泛開展于國內外各胰腺外科中心,但LDPPHR仍處于探索初期,其手術指征、短期并發癥、長期預后等問題值得高度關注。
3.1 適應證和禁忌證
LDPPHR的適應證理論上與開腹DPPHR一致,主要用于胰頭部良性、交界性以及低度惡性腫瘤性病變,如漿液性囊腺瘤、黏液性囊腺瘤、實性假乳頭狀腫瘤、胰腺神經內分泌腫瘤、導管內乳頭狀黏液瘤等[11]。但因腹腔鏡手術的技術難度更大,其適應證的選擇應更加嚴格。對于合并急慢性胰腺炎、胰腺纖維化的患者,由于反復炎癥導致正常的胰腺包膜結構被破壞,同時新生血管的形成也大大增加了手術難度,因此,此類患者不適合行LDPPHR,嚴重時甚至是手術禁忌證。
近來隨著腹腔鏡下胰腺局部切除術的流行以及胰管外科理念的興起,越來越多的患者被實施腹腔鏡下胰腺局部切除術及胰管修復整形,導致LDPPHR的適應證越來越窄。根據本中心經驗,對于胰頭部良性、交界性以及低度惡性腫瘤性病變患者,如果腫瘤直徑≤5 cm、腫瘤邊界較清晰且腫瘤和主胰管距離不太近,優先選擇行腹腔鏡下胰腺局部切除術;如果腫瘤體積過大、邊界不清或和主胰管距離過近容易導致損傷,可選擇行LDPPHR;如果合并顯著胰腺炎、胰腺纖維化或術中懷疑惡變,可直接行腹腔鏡下胰十二指腸切除術。
LDPPHR的禁忌證除包括開腹DPPHR的禁忌證外,還包括患者一般情況較差無法耐受氣腹;各種原因導致的腹腔粘連、無法有效建立氣腹;因腫瘤壓迫引起的顯著胰腺炎。
3.2 短期并發癥
文獻[12, 13]報道,開腹DPPHR的圍手術期并發癥發生率為39.5%~81.5%,主要有胰瘺、膽瘺、腹腔出血、腹腔感染、胃排空延遲等。而關于LDPPHR的報道相對較少,且病例數有限。Cao等[14]報道了12例患者行LDPPHR,2例發生胰瘺,2例發生膽瘺,并發癥發生率為33.3%;Cai等[15]報道了24例患者行LDPPHR,11例發生并發癥,并發癥發生率為45.8%,其中包括1例B級胰瘺,3例發生膽瘺。Hong等[16]報道了22例患者行LDPPHR,7例發生并發癥。本中心前期報道的30例患者行LDPPHRt,8例發生并發癥,并發癥發生率為26.7%,其中包括7例B級胰瘺和2例術后出血,無圍手術期死亡病例[17]。由此可見,在選擇合適病例的前提下,LDPPHR具有和開腹手術相同的安全性,且腹腔鏡手術對患者創傷更小,有利于術后恢復,患者受益更大。
3.3 長期預后
無論是開腹還是腹腔鏡手術,DPPHR都追求保器官、保功能,但不能以犧牲腫瘤學安全性為代價。為檢驗該術式的腫瘤學安全性,Beger等[18]通過系統綜述的形式,對14項于2010年以后發表的對比DPPHR和PD療效的研究進行了meta分析,共計納入367例DPPHR和533例PD,平均隨訪45.8個月,結果發現DPPHR組和PD組的吻合口復發率分別為0.86%和1.7%,殘余胰腺的復發率分別為1.5%和2.2%,差異沒有明顯統計學意義。
DPPHR的核心目標是保障患者的長期生活質量。有文獻[19-22]報道DPPHR在改善患者術后生活質量方面具有一定優勢,但這些研究的樣本量較小、對于混雜因素的控制較差。2017年,Diener等[23]開展了一項RCT,共納入115例DPPHR和111例PD患者,并以歐洲癌癥患者生活質量量表QLQ-C30進行客觀評價。結果發現,2組患者的生活質量結果的差異沒有統計學意義。本中心近期也開展了1項系統綜述和meta分析[24]以比較DPPHR和PD手術患者的長期生活質量和生存情況。一共納入了6項RCT和6項非隨機對照研究,共包括456 例DPPHR 和520例 PD。結果表明,2組患者的QLQ-C30總分差異沒有統計學意義,但在疲勞感、惡心嘔吐、腹瀉等消化道癥狀,以及失眠等單項指標方面,DPPHR顯著優于PD手術[24]。
綜上所述,LDPPHR在圍手術期并發癥及長期預后方面具有一定優勢,在術前選擇合適的適應證前提下,該術式值得廣泛推廣應用。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:徐盟負責臨床資料收集、數據分析及撰寫稿件;喬梁、袁天協助數據收集及數據分析;朱峰負責方案設計、研究過程管理和稿件的修改。
倫理聲明:本研究已通過華中科技大學同濟醫學院附屬同濟醫院的倫理審核批準(批文編號:TJ-IRB20180512)。
胰十二指腸切除術(pancreatoduodenectomy,PD)是治療胰頭部及壺腹周圍腫瘤,尤其是惡性腫瘤的主要術式,已被臨床應用90余年。PD手術需要全部或部分切除5~6個臟器,并將胰腺、膽道和胃分別與腸道吻合從而完成消化道重建,手術過程復雜,對患者創傷極大。近40年來,對于術前懷疑胰頭部良性、交界性以及低度惡性腫瘤性病變的患者,在保障根治的前提下,如何盡可能保留更多的器官、保持較好的消化功能、保障患者術后較高的生活質量,是胰腺外科醫生不斷追求探索的問題。基于此,1972年Beger等[1]首次報道了保留十二指腸的胰頭切除術(duodenum-preserving pancreatic head resection,DPPHR),主要用于慢性胰頭炎的治療,該術式能在完整切除病灶的同時盡可能保證患者的正常消化道解剖結構。近年來,隨著微創外科技術的蓬勃發展和“膜解剖”理論基礎在臨床的廣泛應用,華中科技大學同濟醫學院附屬同濟醫院膽胰外科(下文簡稱“本中心”)首次提出了腹腔鏡下保留十二指腸的全胰頭膜內切除術(intracapsular approach used in laparoscopic duodenum-preserving total pancreatic head resection,LDPPHRt)。本研究回顧性收集了本中心2020年4月至2024年6月期間完成的LDPPHRt患者的臨床資料,分析術前、術中及術后恢復情況并進行經驗總結。
1 資料和方案
1.1 研究對象
回顧性收集本中心2020年4月至2024年6月期間完成的所有LDPPHRt患者的臨床資料。
1.2 LDPPHRt術前準備
術前完善常規檢驗,包括血常規、肝腎功能、凝血功能等。所有患者術前均行上腹部薄層增強CT或增強MRI檢查,提示胰頭部良性、交界性或低度惡性腫瘤性病變,排除了遠處轉移,且具備明顯手術指征。利用CT或MRI的三維重建排除了重要血管和膽總管胰腺段受侵,并根據檢查結果決定是否需要完善超聲內鏡檢查及穿刺活檢。對于合并顯著胰腺炎、胰腺纖維化或高度懷疑惡性病變的患者,均不適宜實施該術式。
LDPPHRt遵循加速康復外科原則:術前6 h禁食、2 h禁飲,留置尿管,術前不常規留置胃管及機械性灌腸。
1.3 手術方法
采用氣管插管、全身麻醉。患者采用仰臥分腿位,根據手術需要可調整為頭高腳低、左右傾斜等體位。臍下做小切口,穿刺針建立人工氣腹,CO2氣腹壓≤12 mmHg(1 mmHg=0.133 kpa),氣腹壓根據患者麻醉檢測情況做適當調整。Trocar布局一般采用5孔法、V字形分布(圖1a)。
 圖1
示LDPPHRt的Trocar布局圖及術中圖片
圖1
示LDPPHRt的Trocar布局圖及術中圖片
a:Trocar布局圖;b:胰腺包膜;c:分離胰腺鉤突;d:分離膽總管和壺腹部;e:分離并保護胰十二指腸動脈弓;f:修補十二指腸降部漿肌層
探查整個腹腔后打開胃結腸韌帶,降低結腸肝屈,沿橫結腸系膜前葉和胰頭十二指腸的間隙分離,必要時可離斷副右結腸靜脈、胃網膜右靜脈等匯入胃結腸干(Henle’s trunk)的分支靜脈以及主干,充分顯露胰頭十二指腸,不常規打開Kocker切口。
于胰頸部下緣分離顯露腸系膜上靜脈,沿腸系膜上靜脈正上方離斷胰腺,剪刀剪斷主胰管,胰腺上緣無需解剖分離肝總動脈和胃十二指腸動脈。在腹腔鏡放大效應下,可清晰看到胰腺表面有一層薄薄的包膜(圖1b)。在由胰頭下緣、十二指腸第三段和腸系膜上靜脈右側壁組成的三角形區域內打開胰腺包膜,沿胰腺實質和包膜間隙精細分離,分離過程中無需刻意顯露胰十二指腸下動靜脈,只離斷由包膜上血管發出的穿通進入胰腺實質的分支血管,由此將胰腺鉤突從腸系膜上靜脈后方分離出來(圖1c)。然后繼續沿胰腺實質和包膜的間隙由下向上、由左向右分離,直至將胰頭下緣從十二指腸第三段完全分開,并顯露膽總管左側壁。
將膽總管和壺腹部從胰腺實質內分離出來并保持其結構和血供的完整性,這是本術式的關鍵。通過顯露胰十二指腸上后靜脈來定位膽總管,在間隙內分離胰腺實質時可順勢將該靜脈保護并留置在包膜內,由上向下分離膽總管直至壺腹部,于壺腹部找到主胰管匯入點,結扎并離斷主胰管(圖1d)。從十二指腸球部和降部開始沿包膜間隙分離胰腺實質,注意保護好胰十二指腸動脈前弓和后弓,尤其是后弓(圖1e)。由于十二指腸降部和胰腺聯系緊密,缺乏固有的間隙,分離過程難免會損傷十二指腸漿肌層,可予以修補成形(圖1f)。對于個別膽總管被胰腺完全包裹的患者,可先沿十二指腸和胰腺間隙分離并找到壺腹部,由下向上分離膽總管,必要時可予以懸吊牽拉以方便顯露和分離。至此,整個胰頭部連同腫瘤被完整切除,切除組織送快速冰凍病理學檢查以了解標本性質。
距離屈氏韌帶約15 cm處離斷空腸,于結腸后系膜裂孔處將遠端空腸上提行胰腸吻合,采用植入式胰腸吻合[2],距胰腸吻合口45 cm處行腸腸吻合。胰腸吻合口前后方各放置引流管1根。
1.4 術后治療
術后給予心電監護、鼻導管吸氧、二代頭孢抗生素、補液、靜脈營養支持等,常規給予生長抑素抑制胰酶分泌,恢復進食后停止。術后第1、3、5、7天連續監測腹腔引流液淀粉酶情況,若淀粉酶<500 U/L且顏色清亮,予以拔除引流管。
1.5 觀察指標及評價標準
觀察指標:① 手術情況;② 術后情況及并發癥情況。
評價標準:根據中華醫學會外科學分會胰腺外科學組的標準定義胰腺術后胰瘺、膽瘺、胃排空延遲、術后出血等并發癥。
2 結果
本研究共納入75例LDPPHRt患者,其具體臨床病理資料見表1。
本組患者的術后首次下床時間、首次進食流質食物時間、術后住院時間等術后結果,以及術后病理結果見表1。術后發生并發癥18例(24.0%),其中B級胰瘺6例(8.0%)、術后出血5例(6.7%)、膽瘺4例(5.3%)、乳糜瘺2例(2.7%)、術后胃排空延遲4例(5.3%)、腹腔感染2例(2.7%)、肺部感染1例(1.3%)以及切口感染2例(2.7%)。術后30 d內再入院2例(2.7%),均為胰瘺患者,經保守治療及B超引導下穿刺置管引流后好轉出院;無術后90 d內死亡病例。
3 討論
微創化和保留器官功能是現代外科發展的趨勢。傳統的PD手術切除范圍大、重建復雜,患者的遠期生活質量可能受到不良影響。因此,對于胰頭部良性、交界性以及低度惡性腫瘤性病變患者,尤其是年輕患者,實施PD手術對于醫生和患者而言都是極大的挑戰。DPPHR的提出改善了這一現狀,該術式保留了術后胰腺內外分泌功能,提高了患者的遠期生活質量。最早期,DPPHR用于治療慢性胰腺炎,該術式大部分切除胰頭部炎性腫塊,解除其對膽總管和十二指腸的壓迫,僅保留十二指腸內側的部分胰腺組織,從而緩解疼痛癥狀,延緩慢性胰腺炎的進展。該術式逐漸衍生了Frey手術[3]、Berne手術[4]、Imaizumi手術[5]。直到Takada等[6]提出沿十二指腸內側完整切除胰頭,保留胰十二指腸動脈后弓、膽總管、膽囊以及十二指腸乳頭,由于該術式保留了十二指腸血供,避免了胰頭部胰腺組織剩余,提高了腫瘤的根治性,DPPHR才逐步由胰頭大部分切除演化為胰頭全切除,手術指征也由慢性胰腺炎過渡到胰頭部良性、交界性以及低度惡性腫瘤性病變。
近年來,“膜解剖”理論從基礎解剖學角度為臨床手術層面的研究提供了可能。2007年,Gockel等[7]從解剖學角度闡述了胰腺存在系膜結構,并提出了胰腺系膜的概念。該系膜位于胰頭后方、腸系膜上動脈右側,并從胰腺頭頸部及鉤突后方延伸至腹主動脈及下腔靜脈表面。之后Adham等[8]也提出了胰腺系膜三角的概念,該區域的前界是腸系膜上靜脈和門靜脈的后壁,后界位于腹主動脈及下腔靜脈前壁,內界是腹腔干右緣和腸系膜上動脈。與此同時,也有學者[9, 10]對胰后是否存在胰腺系膜提出了質疑,認為該區域缺乏明顯纖維鞘樣結構的存在,不符合“系膜”這一概念。
隨著科學技術的發展,以腹腔鏡技術為代表的微創外科日新月異,其具有視野清晰、操作精細的優勢,極大地推動了腹腔鏡下保留十二指腸的胰頭切除術(laparoscopic duodenum-preserving pancreatic head resection,LDPPHR)的可行性,同時也提高了安全性。本中心在“膜解剖”理論基礎的指導下,以腹腔鏡手術為平臺,在前期臨床實踐中發現胰腺表面存在一層薄薄的包膜,胰頭腹側為前包膜,背側為后包膜,等同于Gockel等[7]提出的胰腺系膜,而胰頭周圍主要血管弓和膽總管均走行于包膜外。因此,從胰頭前壁打開胰腺包膜,在包膜內完整切除胰頭組織,完整保留包膜的后壁及兩側壁,無須刻意游離保留血管弓,僅離斷其發出的進入胰腺實質的穿通支血管,原則上保留了胰十二指腸前后血管弓的完整性,該思想即LDPPHRt的理論基礎。本研究通過回顧性分析本中心開展的LDPPHRt患者的臨床資料,證實該術式是安全可行的。
盡管這幾年腹腔鏡胰腺外科手術得到了迅速發展,腹腔鏡下胰十二指腸切除術、胰體尾切除術等已廣泛開展于國內外各胰腺外科中心,但LDPPHR仍處于探索初期,其手術指征、短期并發癥、長期預后等問題值得高度關注。
3.1 適應證和禁忌證
LDPPHR的適應證理論上與開腹DPPHR一致,主要用于胰頭部良性、交界性以及低度惡性腫瘤性病變,如漿液性囊腺瘤、黏液性囊腺瘤、實性假乳頭狀腫瘤、胰腺神經內分泌腫瘤、導管內乳頭狀黏液瘤等[11]。但因腹腔鏡手術的技術難度更大,其適應證的選擇應更加嚴格。對于合并急慢性胰腺炎、胰腺纖維化的患者,由于反復炎癥導致正常的胰腺包膜結構被破壞,同時新生血管的形成也大大增加了手術難度,因此,此類患者不適合行LDPPHR,嚴重時甚至是手術禁忌證。
近來隨著腹腔鏡下胰腺局部切除術的流行以及胰管外科理念的興起,越來越多的患者被實施腹腔鏡下胰腺局部切除術及胰管修復整形,導致LDPPHR的適應證越來越窄。根據本中心經驗,對于胰頭部良性、交界性以及低度惡性腫瘤性病變患者,如果腫瘤直徑≤5 cm、腫瘤邊界較清晰且腫瘤和主胰管距離不太近,優先選擇行腹腔鏡下胰腺局部切除術;如果腫瘤體積過大、邊界不清或和主胰管距離過近容易導致損傷,可選擇行LDPPHR;如果合并顯著胰腺炎、胰腺纖維化或術中懷疑惡變,可直接行腹腔鏡下胰十二指腸切除術。
LDPPHR的禁忌證除包括開腹DPPHR的禁忌證外,還包括患者一般情況較差無法耐受氣腹;各種原因導致的腹腔粘連、無法有效建立氣腹;因腫瘤壓迫引起的顯著胰腺炎。
3.2 短期并發癥
文獻[12, 13]報道,開腹DPPHR的圍手術期并發癥發生率為39.5%~81.5%,主要有胰瘺、膽瘺、腹腔出血、腹腔感染、胃排空延遲等。而關于LDPPHR的報道相對較少,且病例數有限。Cao等[14]報道了12例患者行LDPPHR,2例發生胰瘺,2例發生膽瘺,并發癥發生率為33.3%;Cai等[15]報道了24例患者行LDPPHR,11例發生并發癥,并發癥發生率為45.8%,其中包括1例B級胰瘺,3例發生膽瘺。Hong等[16]報道了22例患者行LDPPHR,7例發生并發癥。本中心前期報道的30例患者行LDPPHRt,8例發生并發癥,并發癥發生率為26.7%,其中包括7例B級胰瘺和2例術后出血,無圍手術期死亡病例[17]。由此可見,在選擇合適病例的前提下,LDPPHR具有和開腹手術相同的安全性,且腹腔鏡手術對患者創傷更小,有利于術后恢復,患者受益更大。
3.3 長期預后
無論是開腹還是腹腔鏡手術,DPPHR都追求保器官、保功能,但不能以犧牲腫瘤學安全性為代價。為檢驗該術式的腫瘤學安全性,Beger等[18]通過系統綜述的形式,對14項于2010年以后發表的對比DPPHR和PD療效的研究進行了meta分析,共計納入367例DPPHR和533例PD,平均隨訪45.8個月,結果發現DPPHR組和PD組的吻合口復發率分別為0.86%和1.7%,殘余胰腺的復發率分別為1.5%和2.2%,差異沒有明顯統計學意義。
DPPHR的核心目標是保障患者的長期生活質量。有文獻[19-22]報道DPPHR在改善患者術后生活質量方面具有一定優勢,但這些研究的樣本量較小、對于混雜因素的控制較差。2017年,Diener等[23]開展了一項RCT,共納入115例DPPHR和111例PD患者,并以歐洲癌癥患者生活質量量表QLQ-C30進行客觀評價。結果發現,2組患者的生活質量結果的差異沒有統計學意義。本中心近期也開展了1項系統綜述和meta分析[24]以比較DPPHR和PD手術患者的長期生活質量和生存情況。一共納入了6項RCT和6項非隨機對照研究,共包括456 例DPPHR 和520例 PD。結果表明,2組患者的QLQ-C30總分差異沒有統計學意義,但在疲勞感、惡心嘔吐、腹瀉等消化道癥狀,以及失眠等單項指標方面,DPPHR顯著優于PD手術[24]。
綜上所述,LDPPHR在圍手術期并發癥及長期預后方面具有一定優勢,在術前選擇合適的適應證前提下,該術式值得廣泛推廣應用。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:徐盟負責臨床資料收集、數據分析及撰寫稿件;喬梁、袁天協助數據收集及數據分析;朱峰負責方案設計、研究過程管理和稿件的修改。
倫理聲明:本研究已通過華中科技大學同濟醫學院附屬同濟醫院的倫理審核批準(批文編號:TJ-IRB20180512)。