版權信息: ?四川大學華西醫院華西期刊社《中國循證醫學雜志》版權所有,未經授權不得轉載、改編
以腸桿菌(肺炎克雷伯菌、大腸埃希菌等)和非發酵菌(如鮑曼不動桿菌、銅綠假單胞菌等)為代表的革蘭氏陰性菌是醫院感染的重要致病菌[1]。近些年隨著抗菌藥物的廣泛使用,多重耐藥革蘭陰性菌(MDR-GNB)的臨床檢出率快速升高,其表現為對多種抗菌藥物耐藥(對抗菌譜內3類及以上藥物不敏感),可供選擇的藥物很少。根據耐藥程度可進一步分為多重耐藥(MDR)、泛耐藥(XDR)、全耐藥(PDR)及耐碳青霉烯類(CR)革蘭陰性菌。一旦發生MDR-GNB感染,可能使普通感染變得難以或無法被治愈,導致感染部位癥狀加重甚至進展為膿毒血癥,嚴重影響抗菌治療的效果及患者預后[2]。
遺憾的是,目前臨床對于MDR-GNB感染的最佳治療方案尚未確定[3]。綜合現有研究資料,國內外研究者大多推崇以碳青霉烯類、多黏菌素(國外采用黏菌素)、替加環素、舒巴坦為主的聯用方案,此外一些新藥的研發也為耐藥菌感染提供了治療選擇。但迄今為止,還沒有基于強有力證據的診療指南來證實單一治療或聯合治療的優勢及各方案的臨床偏向[4]。由于耐藥菌感染相關的隨機對照試驗(RCT)數量較少、樣本量較小,各臨床研究間存在較大異質性導致部分研究的臨床數據相互矛盾,因此想要推薦出更有效的初始治療策略具有一定難度。而網狀Meta分析(NMA)通過全面的資料收集和定量分析,可快速獲得非直接比較的藥物療效和安全性評價結果,比普通Meta分析更有優勢[5]。鑒于此本研究擬采用NMA方法全面比較多種抗菌用藥方案對MDR-GNB感染的抗菌效果并進行最優概率排序,以期為MDR-GNB感染的臨床用藥選擇提供循證依據。
1 資料與方法
1.1 納入與排除標準
1.1.1 研究類型
本研究擬收集不同抗菌用藥方案治療MDR-GNB感染的抗菌療效和安全性的臨床研究。由于相關RCT數量較少,且普遍排除耐藥菌感染及患有嚴重疾病、合并癥的患者群體,因此補充納入隊列研究以彌補數據分析的局限性。本研究遵照PRISMA系統評價聲明[5]的要求。
1.1.2 研究對象
為用藥前已確診患有MDR-GNB感染的成年患者。
1.1.3 干預措施
多種用藥方案,劑型、劑量不限。
1.1.4 結局指標
臨床有效率、細菌清除率、全因死亡率(28天死亡率)。臨床有效定義為治療結束時感染體征和癥狀的消除、實驗室指標的好轉,細菌清除定義為初始治療后的培養陽性轉陰性,以上評價指標根據衛生部《抗菌藥物臨床研究指導原則》判定。
1.1.5 排除標準
① 排除兒童、妊娠及哺乳期婦女;② 排除針對腎衰、癌癥患者的研究;③ 排除敏感菌感染;④ 排除比較藥物不同用法(如給藥途徑、劑量等)的研究;⑤ 排除干預措施不具體、缺少數據(如結局指標等)的研究。
1.2 文獻檢索策略
計算機檢索PubMed、Cochrane Library、Web of Science、ClinicalTrials、CNKI、WanFang Data、中華醫學期刊全文數據庫,檢索時限從建庫至2023年2月。中文檢索詞包括:多重耐藥、泛耐藥、耐碳青霉烯、腸桿菌、鮑曼不動桿菌、銅綠假單胞菌、感染、碳青霉烯類、多黏菌素、四環素類、β內酰胺類、氨基糖苷類、喹諾酮類、β內酰胺類/酶抑制劑、有效性、療效、安全性等。英文檢索詞包括:drug resistance、carbapenems resistance、enterobacteriaceae、acinetobacter、pseudomonas、infection、carbapenem、colistin、tetracyclines、β-lactams、aminoglycosides、quinolones、sulbactam、cure、response、mortality等。
1.3 文獻篩選與資料提取
由2名研究者獨立篩選文獻、提取資料并交叉核對。如有分歧,則通過討論或與第三方協商解決。資料提取內容包括:作者、年份、研究類型、干預細節(如治療方案、劑量、治療持續時間等)、患者特征(包括年齡、性別、國家/地區等)和結局指標(療效、死亡率)。
1.4 納入研究的偏倚風險評價
RCT采用RoB2隨機對照試驗Cochrane偏倚風險評估工具評價文獻質量,觀察性研究使用ROBINS-I非隨機干預研究的偏倚風險工具進行評價。
1.5 統計分析
采用Stata 18軟件完成網狀Meta分析的數據處理及圖表繪制,檢驗水準為α=0.05。采用比值比(OR)為效應分析指標,并提供其95%可信區間(CI)。① 繪制各抗菌藥物方案全面比較的證據網絡圖;② 繪制各用藥方案兩兩直接比較的森林圖;③ 采用環內不一致性檢驗(不一致性因子IF,越接近0,表明直接比較與間接比較結果越一致)和節點拆分檢驗(Z檢驗)評估證據網絡內的一致性;④ 采用I2統計量進行異質性檢驗;⑤ 繪制漏斗圖和Egger檢驗評估發表偏倚;⑥ 根據不一致性檢驗選擇采用一致性模型或不一致性模型,繪制累積曲線下面積圖(SUCRA)和等級概率排序表。
2 結果
2.1 文獻檢索流程及結果
共檢索到6 447篇文獻,經逐層篩選后,最終納入64項研究,其中9項為RCT,55項為隊列研究,分別來自中國、韓國、美國、印度、歐洲等國家或地區,感染類型以肺炎、血流感染為主。文獻檢索流程及結果詳見附件圖1。
2.2 納入研究的基本特征
納入研究的基本特征見表1。共涉及12種抗菌藥物方案:碳青霉烯類+多黏菌素(CB+PL)、碳青霉烯類+替加環素(CB+TG)、碳青霉烯類+其他β內酰胺類/組合劑(CB+β-LAC/MIX)、碳青霉烯類+喹諾酮類(CB+QN)、碳青霉烯類+氨基糖苷類(CB+AG)、碳青霉烯類+其他藥物(CB+OTH)、多黏菌素+替加環素(PL+TG)、多黏菌素+β內酰胺類/組合劑(PL+β-LAC/MIX)、替加環素+β內酰胺類/組合劑(TG+β-LAC/MIX)、單藥療法、其他二聯用法、三聯療法。
2.3 偏倚風險評價結果
9項RCT研究中僅1項為低偏倚風險,8項中、高風險,主要原因在于未采用雙盲法,部分研究存在失訪情況(附件圖2)。55項隊列研究中分別在混雜偏倚、干預分類偏倚和實施偏倚方面存在較高風險(附件表1)。
2.4 網狀關系
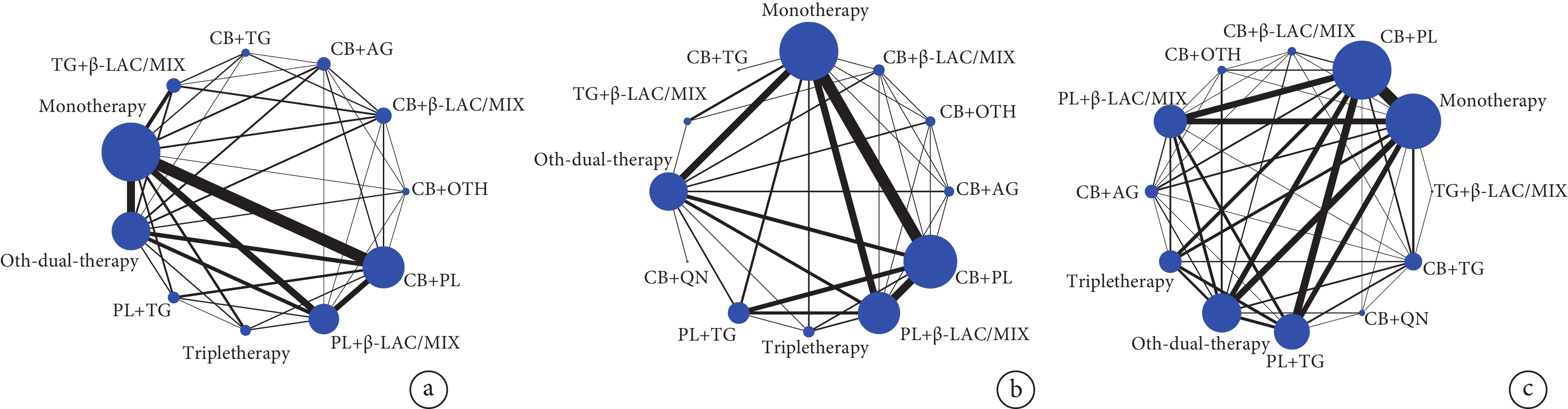
網絡圖直觀展現了12種抗菌用藥方案間現有的研究數量情況(圖1),其中單藥、多黏菌素+碳青霉烯類、其他二聯療法、多黏菌素+β內酰胺類或組合劑、多黏菌素+替加環素這5種聯用方案的網絡節點較大、其間連線較粗,相關研究較多。
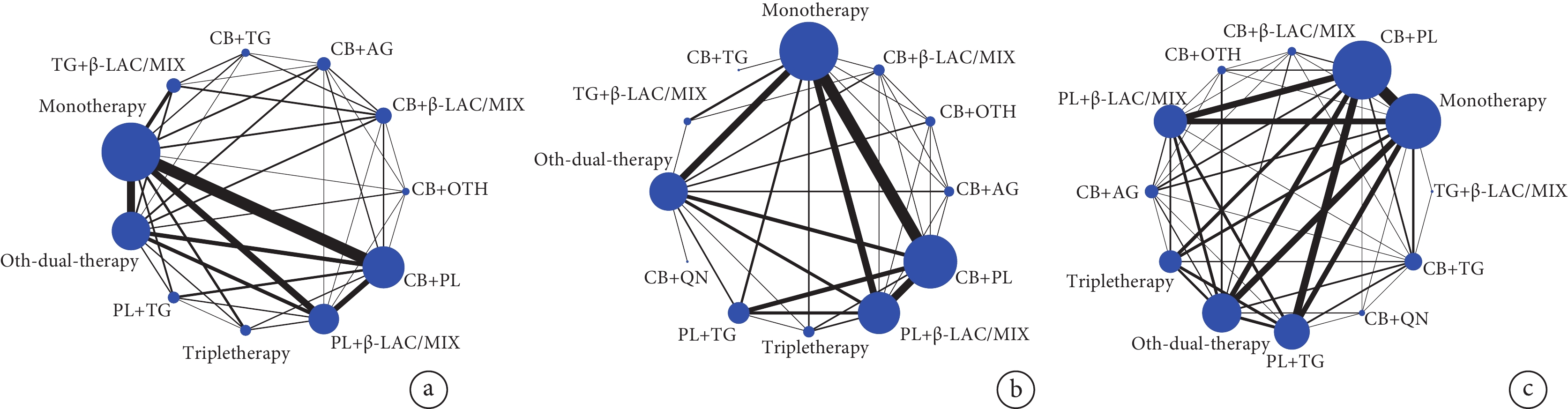 圖1
12種抗菌用藥方案的網絡關系圖
圖1
12種抗菌用藥方案的網絡關系圖
a:臨床有效率;b:細菌清除率;c:28天死亡率。
2.5 方法學檢驗結果
網絡全局一致性檢驗:兩兩比較森林圖顯示在臨床有效率、細菌清除率、28天死亡率方面,12種用藥方案中任意兩種的直接比較效應量(藍線)、間接比較擬合效應量(綠線)、直接比較與間接比較的合并效應量(紅線)之間不存在統計學差異(P均>0.05),證據網絡整體符合一致性假設,可采用一致性模型進行分析(附件圖3)。
網絡局部一致性檢驗:通過對每3個節點組成的閉合三角環進行環內不一致性檢驗,臨床有效率組共形成67個閉合三角環,不一致性檢驗統計量IF介于0.006~2.596之間,有4個三角環的95%CI不包括0,說明存在環內不一致性。細菌清除率組共形成54個閉合三角環,IF介于0.057~2.910,所有環符合一致性假設。28天死亡率組共形成97個閉合三角環,IF介于0.027~3.887,3個環內存在不一致性(附件表2、表3、表4)。另外,針對網絡中每個節點的局部一致性再次采用節點拆分法進行驗證,結果顯示三組均存在局部不一致性(P<0.05)(附件表5、表6、表7)。綜上,臨床有效率組、細菌清除率組、28天死亡率組均存在局部不一致性,但不影響全局,可采用一致性模型進行網狀Meta分析。
臨床有效率、細菌清除率、28天死亡率的各研究間異質性均較小(I2<50%),可進行網狀Meta分析。
2.6 網狀Meta分析結果
2.6.1 累積曲線下面積圖(SUCRA)
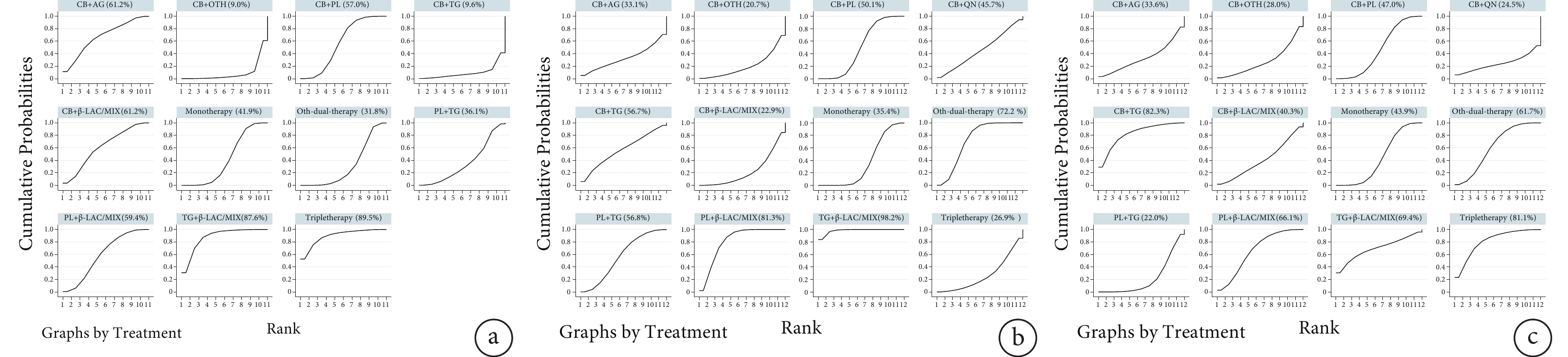
臨床有效率、細菌清除率為有利指標,曲線下面積SUCRA值越大越好;28天死亡率為有害指標,SUCRA值越小越好。12種抗菌用藥方案對于MDR-GNB感染,臨床療效前5名中有3個含β內酰胺類/組合劑,2個含碳青霉烯類,說明以β內酰胺類/組合劑或碳青霉烯類為基礎的聯用有益于提高耐藥菌感染治療的臨床療效。細菌學療效前5名中有3個含替加環素,2個含β內酰胺類/組合劑,說明以替加環素或β內酰胺類/組合劑為基礎的聯用方案對細菌清除率的提高可能有輔助效果。28天死亡風險的比較中,含碳青霉烯類的藥物組合在低死亡風險前5名中占4個,說明碳青霉烯類藥物總體安全性高,聯用該類藥物出現不良結局的概率較小。另外研究結果也提示了碳青霉烯類+替加環素、三聯療法、替加環素+β內酰胺類/組合劑、多黏菌素+β內酰胺類/組合劑這4種用藥方案盡管在臨床療效、細菌學療效中排名靠前,死亡風險卻較高。另外,在以碳青霉烯類為基礎的聯用組合中,碳青霉烯類聯用氨基糖苷類、β內酰胺類/組合劑、多黏菌素的臨床療效排名較為靠前,而聯用替加環素、多黏菌素、喹諾酮類的細菌學療效排名靠前(圖2、附件表8)。
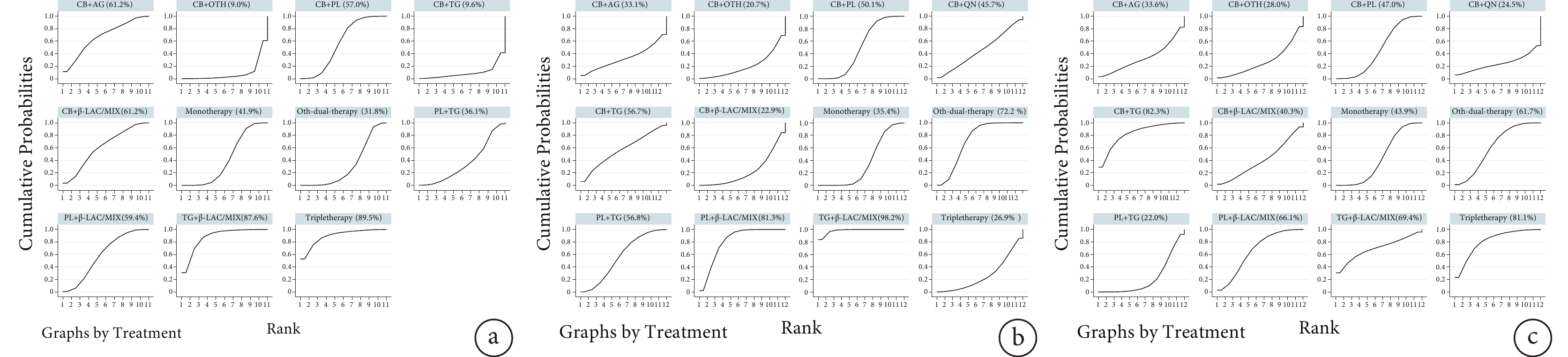 圖2
12種抗菌用藥方案的累積曲線下面積圖
圖2
12種抗菌用藥方案的累積曲線下面積圖
a:臨床有效率;b:細菌清除率;c:28天死亡率。
2.6.2 等級概率排序情況
見附件圖3。① 各抗菌用藥方案臨床療效的比較顯示,三聯療法顯著優于碳青霉烯類+替加環素[OR=5.30(1.13,24.94)]和碳青霉烯類+其他藥物[OR=4.46(1.41,14.06)]。替加環素+其他β內酰胺類/組合劑顯著優于其他二聯用法[OR=2.03(1.11,3.69)]、各種單藥[OR=1.83(1.06,3.17)]、碳青霉烯類+替加環素[OR=4.75(1.16,19.45)]、碳青霉烯類+其他藥物[OR=3.99(1.47,10.88)]。多黏菌素+β內酰胺類/組合劑顯著優于碳青霉烯類+其他藥物[OR=2.55(1.02,6.36)],碳青霉烯類+多黏菌素顯著優于碳青霉烯類+其他藥物[OR=2.45(1.03,5.87)](P<0.05)。② 細菌清除率的比較顯示,替加環素+其他β內酰胺類/組合劑顯著優于三聯療法[OR=4.22 (1.57,11.34)]、多黏菌素+替加環素[OR=2.63(1.24,5.58)]、其他二聯用法[OR=2.17(1.18,4.00)]、各種單藥[OR=3.37(1.94,5.85)]、碳青霉烯類+其他β內酰胺類/組合劑[OR=4.56(1.78,11.65)]、碳青霉烯類+喹諾酮類[OR=3.10(1.02,9.44)]、碳青霉烯類+多黏菌素[OR=2.89(1.59,5.25)]、碳青霉烯類+其他藥物[OR=5.26(1.50,18.39)]這8種組合。而多黏菌素+β內酰胺類/組合劑顯著優于各種單藥[OR=1.83(1.24,2.71)]、碳青霉烯類+其他β內酰胺類/組合劑[OR=2.47(1.05,5.85)]、碳青霉烯類+多黏菌素[OR=1.57(1.07,2.30)]。其他二聯用法顯著優于各單藥用法[OR=1.55(1.11,2.17)](P<0.05)。③28天死亡率的比較顯示,三聯療法的死亡風險顯著高于多黏菌素+替加環素[OR=1.81(1.04,3.16)](P<0.05),其余各組無統計學差異。
2.6.3 發表偏倚
納入的研究大致集中于三角區內,以中線為軸對稱分布,基本不存在發表偏倚(見附件圖4)。Egger檢驗顯示臨床有效率組、細菌清除率組存在發表偏倚可能性小(P均>0.05),但28天死亡率組可能存在發表偏倚(P=0.014)。
3 討論
本研究對MDR-GNB感染患者抗菌藥物聯用方案的臨床療效、細菌學療效、死亡風險進行了網狀Meta分析,共收集了9篇RCT研究,55篇隊列研究,有3項主要成果:其一,MDR-GNB感染患者若采用以β內酰胺類/組合劑或碳青霉烯類為基礎的聯用,有可能獲得較好臨床治療效果;而采用以替加環素或β內酰胺類/組合劑為基礎的聯用,有可能獲得較優的微生物表現。其二,本研究篩選出了幾種可與碳青霉烯類聯用,以提高抗MDR-GNB感染效果的抗菌用藥方案,臨床療效排名靠前的是碳青霉烯類聯用氨基糖苷類、β內酰胺類/組合劑、多黏菌素,而細菌學療效排名靠前的是碳青霉烯類聯用替加環素、多黏菌素、喹諾酮類;大部分含碳青霉烯組合都可降低死亡風險。其三,在其他不含碳青霉烯類的聯用組合中,三聯療法、替加環素+β內酰胺類/組合劑臨床療效較優,而替加環素+β內酰胺類/組合劑、多黏菌素+β內酰胺類/組合劑的細菌學療效可能較優。
本研究結果顯示碳青霉烯類+多黏菌素的臨床療效顯著優于碳青霉烯類+其他藥物(OR=2.45,聯用其他β內酰胺類、四環素類等),并且其臨床或微生物表現及死亡率都優于各種單藥用法(包括多黏菌素、替加環素、碳青霉烯類單藥),與文獻報道一致[19,28]。體外研究與臨床試驗提示,碳青霉烯類+多黏菌素的聯合可產生協同作用(增加約75%)[70],并有助于防止對多黏菌素耐藥的菌株出現[6]。以上結果表明碳青霉烯類+多黏菌素在MDR-GNB感染的治療中具有一定價值,可排在聯用選擇的優先行列中,但由于多黏菌素具有一定腎毒性[6-8],因此宜根據患者具體情況考慮是否需要采用碳青霉烯類+多黏菌素的方案。
根據SUCRA排序可知(表2),碳青霉烯類+β內酰胺類/組合劑盡管在MDR-GNB細菌清除以及降低28天死亡率方面的表現并不突出,但可獲得較高臨床有效率(排名第四)。本研究納入的β內酰胺類/組合劑主要指舒巴坦類,體外研究顯示碳青霉烯類與氨芐西林/舒巴坦的協同作用約為42%[70]。有研究指出舒巴坦類對耐碳青霉烯鮑曼不動桿菌感染的治療效果較多黏菌素更好[71]。因此,本研究結果提示舒巴坦類可作為與碳青霉烯類聯用抗MDR-GNB感染(尤其是鮑曼不動桿菌感染)的推薦選擇之一。
另外,碳青霉烯類+替加環素雖然具有較優的細菌學療效(排名第五),但其28天死亡率在各組中最高,與文獻報道一致[24,68]。在體外研究中,替加環素、多粘菌素對MDR-GNB有較高敏感性,并且對耐碳青霉烯類革蘭氏陰性菌也呈現敏感[54,68],同時替加環素還可與碳青霉烯類產生協同作用(約50%)[70],因此也受到廣泛關注。但在臨床研究中,文獻報道替加環素單藥治療MDR-GNB感染具有較高的全因死亡率,分析原因可能與替加環素的血藥濃度不足有關[72]。綜合考慮其細菌學療效與死亡風險,本研究提示以碳青霉烯類+替加環素治療MDR-GNB感染時,建議監測兩藥血藥濃度,以避免無法真正將細菌學的抗菌效果反映為患者的臨床治愈表現。
碳青霉烯類、氨基糖苷類、喹諾酮類屬于廣譜抗菌藥物,常用于各種革蘭陰性菌感染的治療[46]。本研究結果顯示碳青霉烯類+氨基糖苷類是碳青霉烯類的各組合中治療MDR-GNB感染的最優方案,其臨床療效僅次于三聯療法和替加環素+β內酰胺類/組合劑(位列第三),并且與三聯療法相比碳青霉烯類+氨基糖苷類或喹諾酮類具有更低的28天死亡率和更優的細菌學效果。體外研究顯示,碳青霉烯類藥物可與氨基糖苷類、喹諾酮類聯合產生協同(增強)作用,協同比例約為:40%~50%、15%~30%[70]。因此,氨基糖苷類、喹諾酮類可能依然是與碳青霉烯類聯用的較優選擇。
與此前國外網狀Meta分析結果相同[73,74],本研究顯示三聯療法的臨床有效率排名第一,并且顯著優于碳青霉烯類+替加環素(OR=5.30)和碳青霉烯類+其他藥物(OR=4.46)。然而其28天死亡風險排名第二,且顯著高于多黏菌素+替加環素(OR=1.81),提示三聯療法可能具有較好的療效但可能易造成其他損害而增加死亡風險,因此綜合考慮其臨床療效和安全性,本研究不優先推薦采用三聯療法作為治療選擇。
國內專家共識指出MDR-GNB感染的重癥患者具有使用碳青霉烯類藥物的指征,但推薦采用聯合用法以增加殺菌效果[75-76]。對于不耐碳青霉烯類(MIC≤8 μg/ml)的MDR-GNB感染,采用含碳青霉烯類的聯合方案被認為比不含碳青霉烯的聯合方案具有更高的治療成功率[77-78]。而當菌株對碳青霉烯類的MIC>8 μg/ml時,不再建議選用含碳青霉烯類的聯合用藥方案[5]。鑒于此,本研究為碳青霉烯類治療MDR-GNB感染提供了思路和統計學意義上的方案推薦,但建議臨床用藥時應考慮患者感染部位、患者的肝腎功能及合并癥、細菌最低抑菌濃度(MIC)和耐藥機制等進行綜合考慮以選擇抗菌藥物。
多黏菌素和替加環素是目前MDR-GNB感染治療中的熱點藥物,從圖3證據網絡圖可見,有關多黏菌素和替加環素的各聯用方案(包括碳青霉烯類+多黏菌素)受到較多研究者的關注。在不含碳青霉烯類的其他抗菌用藥方案中,替加環素+β內酰胺類/組合劑、多黏菌素+β內酰胺類/組合劑細菌清除率分別位列第一和第二,并且都顯著優于其他多種抗菌用藥方案,而在臨床療效方面也有不錯的表現;而多黏菌素+替加環素以及其他二聯用法也具有較好的細菌學表現,但臨床療效和死亡風險不佳。此外,臨床療效前5名中有3個含β內酰胺類/組合劑,細菌學療效前5名中有2個含β內酰胺類/組合劑,有3個含替加環素,反映出β內酰胺類/組合劑在MDR-GNB感染的治療中具有一定的優勢,而替加環素的微生物清除效果較突出。綜上,本研究提示多黏菌素、替加環素、β內酰胺類/組合劑的聯合用藥可用于碳青霉烯類使用無效的MDR-GNB治療中,但可能具有更高的28天死亡風險。
綜上,本研究主要的優勢是納入了大量的MDR-GNB相關臨床研究資料,比較了多種抗菌用藥方案,可為MDR-GNB感染的抗菌藥物的選擇提供參考;同時,針對碳青霉烯類藥物進行了詳細分組,對碳青霉烯類在臨床上的用藥決策具有更大的價值。但也存在一些不足之處,主要有3方面:① 由于細菌耐藥性檢測具有滯后性,且耐藥菌比例較低,難以開展相關前瞻性RCT研究,因此本次收集到的RCT研究數量較少,且大多未能實現雙盲法和分配隱藏,雖然補充納入了大量臨床觀察性研究,但可能存在混雜因素、實施因素等影響干預研究結論。對此,我們將持謹慎態度進行結果的解釋,并確保方法學檢驗符合相關要求,但未來仍需要更多高質量的RCT研究驗證本研究結果。② 由于不同研究中對細菌耐藥性的定義存在偏差,因此本研究選擇采用多重耐藥(MDR)這一最大范圍,涵蓋了廣泛耐藥(XDR)、耐碳青霉烯類(CR)細菌,未來有必要根據耐藥程度進行進一步的亞組分析。③ 本研究未考慮不同感染部位的療效差異,使得該研究結論可靠性下降,其中納入的文獻主要為肺炎、血流感染等,因此對于顱內感染或其他部位感染的參考意義減弱。④ 由于文獻中干預措施存在差異,本研究未比較每種藥物的有效劑量、給藥途徑和用藥時間,因此有待更多臨床研究的開展予以補充。
綜上所述,在既往研究中,MDR-GNB感染抗菌藥物的選擇仍存在爭議。鑒于此,本研究納入64篇臨床研究進行網狀Meta分析,結果提示臨床面臨MDR-GNB感染時,采用以β內酰胺類/組合劑、碳青霉烯類、替加環素為基礎的聯用方案可能有益于提高治療耐藥菌感染的臨床療效和細菌學療效,但上述結論尚待更多高質量臨床研究予以驗證。
以腸桿菌(肺炎克雷伯菌、大腸埃希菌等)和非發酵菌(如鮑曼不動桿菌、銅綠假單胞菌等)為代表的革蘭氏陰性菌是醫院感染的重要致病菌[1]。近些年隨著抗菌藥物的廣泛使用,多重耐藥革蘭陰性菌(MDR-GNB)的臨床檢出率快速升高,其表現為對多種抗菌藥物耐藥(對抗菌譜內3類及以上藥物不敏感),可供選擇的藥物很少。根據耐藥程度可進一步分為多重耐藥(MDR)、泛耐藥(XDR)、全耐藥(PDR)及耐碳青霉烯類(CR)革蘭陰性菌。一旦發生MDR-GNB感染,可能使普通感染變得難以或無法被治愈,導致感染部位癥狀加重甚至進展為膿毒血癥,嚴重影響抗菌治療的效果及患者預后[2]。
遺憾的是,目前臨床對于MDR-GNB感染的最佳治療方案尚未確定[3]。綜合現有研究資料,國內外研究者大多推崇以碳青霉烯類、多黏菌素(國外采用黏菌素)、替加環素、舒巴坦為主的聯用方案,此外一些新藥的研發也為耐藥菌感染提供了治療選擇。但迄今為止,還沒有基于強有力證據的診療指南來證實單一治療或聯合治療的優勢及各方案的臨床偏向[4]。由于耐藥菌感染相關的隨機對照試驗(RCT)數量較少、樣本量較小,各臨床研究間存在較大異質性導致部分研究的臨床數據相互矛盾,因此想要推薦出更有效的初始治療策略具有一定難度。而網狀Meta分析(NMA)通過全面的資料收集和定量分析,可快速獲得非直接比較的藥物療效和安全性評價結果,比普通Meta分析更有優勢[5]。鑒于此本研究擬采用NMA方法全面比較多種抗菌用藥方案對MDR-GNB感染的抗菌效果并進行最優概率排序,以期為MDR-GNB感染的臨床用藥選擇提供循證依據。
1 資料與方法
1.1 納入與排除標準
1.1.1 研究類型
本研究擬收集不同抗菌用藥方案治療MDR-GNB感染的抗菌療效和安全性的臨床研究。由于相關RCT數量較少,且普遍排除耐藥菌感染及患有嚴重疾病、合并癥的患者群體,因此補充納入隊列研究以彌補數據分析的局限性。本研究遵照PRISMA系統評價聲明[5]的要求。
1.1.2 研究對象
為用藥前已確診患有MDR-GNB感染的成年患者。
1.1.3 干預措施
多種用藥方案,劑型、劑量不限。
1.1.4 結局指標
臨床有效率、細菌清除率、全因死亡率(28天死亡率)。臨床有效定義為治療結束時感染體征和癥狀的消除、實驗室指標的好轉,細菌清除定義為初始治療后的培養陽性轉陰性,以上評價指標根據衛生部《抗菌藥物臨床研究指導原則》判定。
1.1.5 排除標準
① 排除兒童、妊娠及哺乳期婦女;② 排除針對腎衰、癌癥患者的研究;③ 排除敏感菌感染;④ 排除比較藥物不同用法(如給藥途徑、劑量等)的研究;⑤ 排除干預措施不具體、缺少數據(如結局指標等)的研究。
1.2 文獻檢索策略
計算機檢索PubMed、Cochrane Library、Web of Science、ClinicalTrials、CNKI、WanFang Data、中華醫學期刊全文數據庫,檢索時限從建庫至2023年2月。中文檢索詞包括:多重耐藥、泛耐藥、耐碳青霉烯、腸桿菌、鮑曼不動桿菌、銅綠假單胞菌、感染、碳青霉烯類、多黏菌素、四環素類、β內酰胺類、氨基糖苷類、喹諾酮類、β內酰胺類/酶抑制劑、有效性、療效、安全性等。英文檢索詞包括:drug resistance、carbapenems resistance、enterobacteriaceae、acinetobacter、pseudomonas、infection、carbapenem、colistin、tetracyclines、β-lactams、aminoglycosides、quinolones、sulbactam、cure、response、mortality等。
1.3 文獻篩選與資料提取
由2名研究者獨立篩選文獻、提取資料并交叉核對。如有分歧,則通過討論或與第三方協商解決。資料提取內容包括:作者、年份、研究類型、干預細節(如治療方案、劑量、治療持續時間等)、患者特征(包括年齡、性別、國家/地區等)和結局指標(療效、死亡率)。
1.4 納入研究的偏倚風險評價
RCT采用RoB2隨機對照試驗Cochrane偏倚風險評估工具評價文獻質量,觀察性研究使用ROBINS-I非隨機干預研究的偏倚風險工具進行評價。
1.5 統計分析
采用Stata 18軟件完成網狀Meta分析的數據處理及圖表繪制,檢驗水準為α=0.05。采用比值比(OR)為效應分析指標,并提供其95%可信區間(CI)。① 繪制各抗菌藥物方案全面比較的證據網絡圖;② 繪制各用藥方案兩兩直接比較的森林圖;③ 采用環內不一致性檢驗(不一致性因子IF,越接近0,表明直接比較與間接比較結果越一致)和節點拆分檢驗(Z檢驗)評估證據網絡內的一致性;④ 采用I2統計量進行異質性檢驗;⑤ 繪制漏斗圖和Egger檢驗評估發表偏倚;⑥ 根據不一致性檢驗選擇采用一致性模型或不一致性模型,繪制累積曲線下面積圖(SUCRA)和等級概率排序表。
2 結果
2.1 文獻檢索流程及結果
共檢索到6 447篇文獻,經逐層篩選后,最終納入64項研究,其中9項為RCT,55項為隊列研究,分別來自中國、韓國、美國、印度、歐洲等國家或地區,感染類型以肺炎、血流感染為主。文獻檢索流程及結果詳見附件圖1。
2.2 納入研究的基本特征
納入研究的基本特征見表1。共涉及12種抗菌藥物方案:碳青霉烯類+多黏菌素(CB+PL)、碳青霉烯類+替加環素(CB+TG)、碳青霉烯類+其他β內酰胺類/組合劑(CB+β-LAC/MIX)、碳青霉烯類+喹諾酮類(CB+QN)、碳青霉烯類+氨基糖苷類(CB+AG)、碳青霉烯類+其他藥物(CB+OTH)、多黏菌素+替加環素(PL+TG)、多黏菌素+β內酰胺類/組合劑(PL+β-LAC/MIX)、替加環素+β內酰胺類/組合劑(TG+β-LAC/MIX)、單藥療法、其他二聯用法、三聯療法。
2.3 偏倚風險評價結果
9項RCT研究中僅1項為低偏倚風險,8項中、高風險,主要原因在于未采用雙盲法,部分研究存在失訪情況(附件圖2)。55項隊列研究中分別在混雜偏倚、干預分類偏倚和實施偏倚方面存在較高風險(附件表1)。
2.4 網狀關系
網絡圖直觀展現了12種抗菌用藥方案間現有的研究數量情況(圖1),其中單藥、多黏菌素+碳青霉烯類、其他二聯療法、多黏菌素+β內酰胺類或組合劑、多黏菌素+替加環素這5種聯用方案的網絡節點較大、其間連線較粗,相關研究較多。
 圖1
12種抗菌用藥方案的網絡關系圖
圖1
12種抗菌用藥方案的網絡關系圖
a:臨床有效率;b:細菌清除率;c:28天死亡率。
2.5 方法學檢驗結果
網絡全局一致性檢驗:兩兩比較森林圖顯示在臨床有效率、細菌清除率、28天死亡率方面,12種用藥方案中任意兩種的直接比較效應量(藍線)、間接比較擬合效應量(綠線)、直接比較與間接比較的合并效應量(紅線)之間不存在統計學差異(P均>0.05),證據網絡整體符合一致性假設,可采用一致性模型進行分析(附件圖3)。
網絡局部一致性檢驗:通過對每3個節點組成的閉合三角環進行環內不一致性檢驗,臨床有效率組共形成67個閉合三角環,不一致性檢驗統計量IF介于0.006~2.596之間,有4個三角環的95%CI不包括0,說明存在環內不一致性。細菌清除率組共形成54個閉合三角環,IF介于0.057~2.910,所有環符合一致性假設。28天死亡率組共形成97個閉合三角環,IF介于0.027~3.887,3個環內存在不一致性(附件表2、表3、表4)。另外,針對網絡中每個節點的局部一致性再次采用節點拆分法進行驗證,結果顯示三組均存在局部不一致性(P<0.05)(附件表5、表6、表7)。綜上,臨床有效率組、細菌清除率組、28天死亡率組均存在局部不一致性,但不影響全局,可采用一致性模型進行網狀Meta分析。
臨床有效率、細菌清除率、28天死亡率的各研究間異質性均較小(I2<50%),可進行網狀Meta分析。
2.6 網狀Meta分析結果
2.6.1 累積曲線下面積圖(SUCRA)
臨床有效率、細菌清除率為有利指標,曲線下面積SUCRA值越大越好;28天死亡率為有害指標,SUCRA值越小越好。12種抗菌用藥方案對于MDR-GNB感染,臨床療效前5名中有3個含β內酰胺類/組合劑,2個含碳青霉烯類,說明以β內酰胺類/組合劑或碳青霉烯類為基礎的聯用有益于提高耐藥菌感染治療的臨床療效。細菌學療效前5名中有3個含替加環素,2個含β內酰胺類/組合劑,說明以替加環素或β內酰胺類/組合劑為基礎的聯用方案對細菌清除率的提高可能有輔助效果。28天死亡風險的比較中,含碳青霉烯類的藥物組合在低死亡風險前5名中占4個,說明碳青霉烯類藥物總體安全性高,聯用該類藥物出現不良結局的概率較小。另外研究結果也提示了碳青霉烯類+替加環素、三聯療法、替加環素+β內酰胺類/組合劑、多黏菌素+β內酰胺類/組合劑這4種用藥方案盡管在臨床療效、細菌學療效中排名靠前,死亡風險卻較高。另外,在以碳青霉烯類為基礎的聯用組合中,碳青霉烯類聯用氨基糖苷類、β內酰胺類/組合劑、多黏菌素的臨床療效排名較為靠前,而聯用替加環素、多黏菌素、喹諾酮類的細菌學療效排名靠前(圖2、附件表8)。
 圖2
12種抗菌用藥方案的累積曲線下面積圖
圖2
12種抗菌用藥方案的累積曲線下面積圖
a:臨床有效率;b:細菌清除率;c:28天死亡率。
2.6.2 等級概率排序情況
見附件圖3。① 各抗菌用藥方案臨床療效的比較顯示,三聯療法顯著優于碳青霉烯類+替加環素[OR=5.30(1.13,24.94)]和碳青霉烯類+其他藥物[OR=4.46(1.41,14.06)]。替加環素+其他β內酰胺類/組合劑顯著優于其他二聯用法[OR=2.03(1.11,3.69)]、各種單藥[OR=1.83(1.06,3.17)]、碳青霉烯類+替加環素[OR=4.75(1.16,19.45)]、碳青霉烯類+其他藥物[OR=3.99(1.47,10.88)]。多黏菌素+β內酰胺類/組合劑顯著優于碳青霉烯類+其他藥物[OR=2.55(1.02,6.36)],碳青霉烯類+多黏菌素顯著優于碳青霉烯類+其他藥物[OR=2.45(1.03,5.87)](P<0.05)。② 細菌清除率的比較顯示,替加環素+其他β內酰胺類/組合劑顯著優于三聯療法[OR=4.22 (1.57,11.34)]、多黏菌素+替加環素[OR=2.63(1.24,5.58)]、其他二聯用法[OR=2.17(1.18,4.00)]、各種單藥[OR=3.37(1.94,5.85)]、碳青霉烯類+其他β內酰胺類/組合劑[OR=4.56(1.78,11.65)]、碳青霉烯類+喹諾酮類[OR=3.10(1.02,9.44)]、碳青霉烯類+多黏菌素[OR=2.89(1.59,5.25)]、碳青霉烯類+其他藥物[OR=5.26(1.50,18.39)]這8種組合。而多黏菌素+β內酰胺類/組合劑顯著優于各種單藥[OR=1.83(1.24,2.71)]、碳青霉烯類+其他β內酰胺類/組合劑[OR=2.47(1.05,5.85)]、碳青霉烯類+多黏菌素[OR=1.57(1.07,2.30)]。其他二聯用法顯著優于各單藥用法[OR=1.55(1.11,2.17)](P<0.05)。③28天死亡率的比較顯示,三聯療法的死亡風險顯著高于多黏菌素+替加環素[OR=1.81(1.04,3.16)](P<0.05),其余各組無統計學差異。
2.6.3 發表偏倚
納入的研究大致集中于三角區內,以中線為軸對稱分布,基本不存在發表偏倚(見附件圖4)。Egger檢驗顯示臨床有效率組、細菌清除率組存在發表偏倚可能性小(P均>0.05),但28天死亡率組可能存在發表偏倚(P=0.014)。
3 討論
本研究對MDR-GNB感染患者抗菌藥物聯用方案的臨床療效、細菌學療效、死亡風險進行了網狀Meta分析,共收集了9篇RCT研究,55篇隊列研究,有3項主要成果:其一,MDR-GNB感染患者若采用以β內酰胺類/組合劑或碳青霉烯類為基礎的聯用,有可能獲得較好臨床治療效果;而采用以替加環素或β內酰胺類/組合劑為基礎的聯用,有可能獲得較優的微生物表現。其二,本研究篩選出了幾種可與碳青霉烯類聯用,以提高抗MDR-GNB感染效果的抗菌用藥方案,臨床療效排名靠前的是碳青霉烯類聯用氨基糖苷類、β內酰胺類/組合劑、多黏菌素,而細菌學療效排名靠前的是碳青霉烯類聯用替加環素、多黏菌素、喹諾酮類;大部分含碳青霉烯組合都可降低死亡風險。其三,在其他不含碳青霉烯類的聯用組合中,三聯療法、替加環素+β內酰胺類/組合劑臨床療效較優,而替加環素+β內酰胺類/組合劑、多黏菌素+β內酰胺類/組合劑的細菌學療效可能較優。
本研究結果顯示碳青霉烯類+多黏菌素的臨床療效顯著優于碳青霉烯類+其他藥物(OR=2.45,聯用其他β內酰胺類、四環素類等),并且其臨床或微生物表現及死亡率都優于各種單藥用法(包括多黏菌素、替加環素、碳青霉烯類單藥),與文獻報道一致[19,28]。體外研究與臨床試驗提示,碳青霉烯類+多黏菌素的聯合可產生協同作用(增加約75%)[70],并有助于防止對多黏菌素耐藥的菌株出現[6]。以上結果表明碳青霉烯類+多黏菌素在MDR-GNB感染的治療中具有一定價值,可排在聯用選擇的優先行列中,但由于多黏菌素具有一定腎毒性[6-8],因此宜根據患者具體情況考慮是否需要采用碳青霉烯類+多黏菌素的方案。
根據SUCRA排序可知(表2),碳青霉烯類+β內酰胺類/組合劑盡管在MDR-GNB細菌清除以及降低28天死亡率方面的表現并不突出,但可獲得較高臨床有效率(排名第四)。本研究納入的β內酰胺類/組合劑主要指舒巴坦類,體外研究顯示碳青霉烯類與氨芐西林/舒巴坦的協同作用約為42%[70]。有研究指出舒巴坦類對耐碳青霉烯鮑曼不動桿菌感染的治療效果較多黏菌素更好[71]。因此,本研究結果提示舒巴坦類可作為與碳青霉烯類聯用抗MDR-GNB感染(尤其是鮑曼不動桿菌感染)的推薦選擇之一。
另外,碳青霉烯類+替加環素雖然具有較優的細菌學療效(排名第五),但其28天死亡率在各組中最高,與文獻報道一致[24,68]。在體外研究中,替加環素、多粘菌素對MDR-GNB有較高敏感性,并且對耐碳青霉烯類革蘭氏陰性菌也呈現敏感[54,68],同時替加環素還可與碳青霉烯類產生協同作用(約50%)[70],因此也受到廣泛關注。但在臨床研究中,文獻報道替加環素單藥治療MDR-GNB感染具有較高的全因死亡率,分析原因可能與替加環素的血藥濃度不足有關[72]。綜合考慮其細菌學療效與死亡風險,本研究提示以碳青霉烯類+替加環素治療MDR-GNB感染時,建議監測兩藥血藥濃度,以避免無法真正將細菌學的抗菌效果反映為患者的臨床治愈表現。
碳青霉烯類、氨基糖苷類、喹諾酮類屬于廣譜抗菌藥物,常用于各種革蘭陰性菌感染的治療[46]。本研究結果顯示碳青霉烯類+氨基糖苷類是碳青霉烯類的各組合中治療MDR-GNB感染的最優方案,其臨床療效僅次于三聯療法和替加環素+β內酰胺類/組合劑(位列第三),并且與三聯療法相比碳青霉烯類+氨基糖苷類或喹諾酮類具有更低的28天死亡率和更優的細菌學效果。體外研究顯示,碳青霉烯類藥物可與氨基糖苷類、喹諾酮類聯合產生協同(增強)作用,協同比例約為:40%~50%、15%~30%[70]。因此,氨基糖苷類、喹諾酮類可能依然是與碳青霉烯類聯用的較優選擇。
與此前國外網狀Meta分析結果相同[73,74],本研究顯示三聯療法的臨床有效率排名第一,并且顯著優于碳青霉烯類+替加環素(OR=5.30)和碳青霉烯類+其他藥物(OR=4.46)。然而其28天死亡風險排名第二,且顯著高于多黏菌素+替加環素(OR=1.81),提示三聯療法可能具有較好的療效但可能易造成其他損害而增加死亡風險,因此綜合考慮其臨床療效和安全性,本研究不優先推薦采用三聯療法作為治療選擇。
國內專家共識指出MDR-GNB感染的重癥患者具有使用碳青霉烯類藥物的指征,但推薦采用聯合用法以增加殺菌效果[75-76]。對于不耐碳青霉烯類(MIC≤8 μg/ml)的MDR-GNB感染,采用含碳青霉烯類的聯合方案被認為比不含碳青霉烯的聯合方案具有更高的治療成功率[77-78]。而當菌株對碳青霉烯類的MIC>8 μg/ml時,不再建議選用含碳青霉烯類的聯合用藥方案[5]。鑒于此,本研究為碳青霉烯類治療MDR-GNB感染提供了思路和統計學意義上的方案推薦,但建議臨床用藥時應考慮患者感染部位、患者的肝腎功能及合并癥、細菌最低抑菌濃度(MIC)和耐藥機制等進行綜合考慮以選擇抗菌藥物。
多黏菌素和替加環素是目前MDR-GNB感染治療中的熱點藥物,從圖3證據網絡圖可見,有關多黏菌素和替加環素的各聯用方案(包括碳青霉烯類+多黏菌素)受到較多研究者的關注。在不含碳青霉烯類的其他抗菌用藥方案中,替加環素+β內酰胺類/組合劑、多黏菌素+β內酰胺類/組合劑細菌清除率分別位列第一和第二,并且都顯著優于其他多種抗菌用藥方案,而在臨床療效方面也有不錯的表現;而多黏菌素+替加環素以及其他二聯用法也具有較好的細菌學表現,但臨床療效和死亡風險不佳。此外,臨床療效前5名中有3個含β內酰胺類/組合劑,細菌學療效前5名中有2個含β內酰胺類/組合劑,有3個含替加環素,反映出β內酰胺類/組合劑在MDR-GNB感染的治療中具有一定的優勢,而替加環素的微生物清除效果較突出。綜上,本研究提示多黏菌素、替加環素、β內酰胺類/組合劑的聯合用藥可用于碳青霉烯類使用無效的MDR-GNB治療中,但可能具有更高的28天死亡風險。
綜上,本研究主要的優勢是納入了大量的MDR-GNB相關臨床研究資料,比較了多種抗菌用藥方案,可為MDR-GNB感染的抗菌藥物的選擇提供參考;同時,針對碳青霉烯類藥物進行了詳細分組,對碳青霉烯類在臨床上的用藥決策具有更大的價值。但也存在一些不足之處,主要有3方面:① 由于細菌耐藥性檢測具有滯后性,且耐藥菌比例較低,難以開展相關前瞻性RCT研究,因此本次收集到的RCT研究數量較少,且大多未能實現雙盲法和分配隱藏,雖然補充納入了大量臨床觀察性研究,但可能存在混雜因素、實施因素等影響干預研究結論。對此,我們將持謹慎態度進行結果的解釋,并確保方法學檢驗符合相關要求,但未來仍需要更多高質量的RCT研究驗證本研究結果。② 由于不同研究中對細菌耐藥性的定義存在偏差,因此本研究選擇采用多重耐藥(MDR)這一最大范圍,涵蓋了廣泛耐藥(XDR)、耐碳青霉烯類(CR)細菌,未來有必要根據耐藥程度進行進一步的亞組分析。③ 本研究未考慮不同感染部位的療效差異,使得該研究結論可靠性下降,其中納入的文獻主要為肺炎、血流感染等,因此對于顱內感染或其他部位感染的參考意義減弱。④ 由于文獻中干預措施存在差異,本研究未比較每種藥物的有效劑量、給藥途徑和用藥時間,因此有待更多臨床研究的開展予以補充。
綜上所述,在既往研究中,MDR-GNB感染抗菌藥物的選擇仍存在爭議。鑒于此,本研究納入64篇臨床研究進行網狀Meta分析,結果提示臨床面臨MDR-GNB感染時,采用以β內酰胺類/組合劑、碳青霉烯類、替加環素為基礎的聯用方案可能有益于提高治療耐藥菌感染的臨床療效和細菌學療效,但上述結論尚待更多高質量臨床研究予以驗證。