引用本文: 周健, 翟鋒, 關宇光, 趙萌, 欒偉, 滕鵬飛, 陳述花, 王靜, 王夢陽, 欒國明. 機器人立體定向手術輔助系統輔助下的立體定向顱內電極置入精準定位致癇灶及切除. 癲癇雜志, 2016, 2(4): 290-295. doi: 10.7507/2096-0247.20160052 復制
版權信息: ?四川大學華西醫院華西期刊社《癲癇雜志》版權所有,未經授權不得轉載、改編
對于藥物難治性癲癇手術前評估最主要的目的有兩個:首先要明確致癇灶是彌漫的還是局限的,如局限具體位置及范圍如何;其次就是致癇灶與功能區之間的關系。術前評估的方法包括非侵襲和侵襲性的檢查方法,非侵襲性的方法如長程視頻頭皮腦電圖(VEEG)、磁共振(MRI)癲癇平掃以及其它一些特殊的影像學檢查,如腦磁圖(Magnetoencephalo-graphy, MEG)、正電子發射斷層掃描(Positron emission tomography, PET)、發作期的單光子發射計算機斷層掃描(Single photon emission computed tomography, SPECT)和神經心理檢查等[1]。當這些非侵襲性方法不能滿足定位致癇灶以及明確致癇灶與功能區的關系時,就要采取侵襲性檢查方法。目前最主要的侵襲性的檢查方法就是顱內電極置入腦電監測。硬膜下的條狀和柵狀電極置入是我國各癲癇中心常用的方法,它可以反映皮層的放電情況以及通過它來探測功能區的位置,但是它不能監測皮層下和深部結構的放電情況以及癇性放電的傳導,大多數情況下硬膜下電極需要開顱置入,創傷較大,特別是對需要雙側置入的患者,硬膜下電極就更加不適合了。立體定向電極置入技術(Stereoelectroen-cephalography, SEEG)彌補了上述方法的不足,逐漸成為一種常規的侵入性術前評估方法。
回顧性分析我院癲癇中心自2012年3月-2015年6月間采用機器人立體定向手術輔助系統(Robotized stereotactic assistant,ROSA)引導下的SEEG置入的140例藥物難治性癲癇患者,在長程腦電圖監測(VEEG)下進行致癇區定位,大部分患者根據顱內電極監測結果行手術治療,結合術后癲癇控制情況綜合分析SEEG在致癇灶精確定位中的作用。
資料與方法
1 一般資料
收集2012年3月-2015年6月期間我中心診斷為局灶性癲癇并且應用ROSA系統行SEEG置入的癲癇患者140例,年齡3~51歲,電極置入手術時平均年齡為19歲;其中男86例(61.4%),女54例(38.6%)。患者病史1個月~37年不等,平均病史11年。140例患者術前均行頭顱MRI、CT及VEEG檢查,部分患者行MEG和/或PET檢查,顱內電極置入術前均診斷為局灶性藥物難治性癲癇。140例患者中139例順利完成了SEEG置入手術及VEEG監測,1例患者因在電極置入過程中出現顱內出血,終止了顱內電極的置入。另2例置入過程中出血,止血后順利完成SEEG置入手術。71例患者監測后行局灶性手術,且隨訪均為6個月以上。患者一般情況見表 1。
2 術前評估
詳細詢問病史,按照癲癇發作的國際分類標準進行初步的臨床診斷分類。
2.1 顱腦磁共振
140例患者均行顱腦MRI掃描,場強1.5T;掃描除進行常規的T1、T2像掃描外均行T2液體衰減反轉恢復序列(FLAIR)掃描。
2.2 長程視頻腦電監測
所有患者均行32-64導頭皮視頻VEEG監測,監測前不改變所服抗癲癇藥物(AEDs)的種類及劑量。電極安放采用國際10-20系統腦電安裝法。所有患者均捕捉到2次及以上的慣常發作。
3 立體定向顱內電極置入
我院癲癇中心應用ROSA系統進行SEEG置入手術。根據非侵襲檢查的結果,對致癇灶的位置做出合理的假設,劃定致癇灶可能的區域。MRI的掃描需要做雙倍強化的T1掃描,根據MRI掃描數據在計算機上進行電極置入的設計,設計包括電極所需覆蓋的范圍、電極的數量、電極所需達到的靶點以及電極的軌跡;置入電極的部位往往集中在影像學上異常的部位(如果存在)、發作可能起源的結構以及癲癇性放電可能傳導的路徑。電極的置入角度可以與矢狀位垂直的也可以任意角度(圖 1)。電極置入手術在全麻下進行,麻醉清醒后進行VEEG監測。
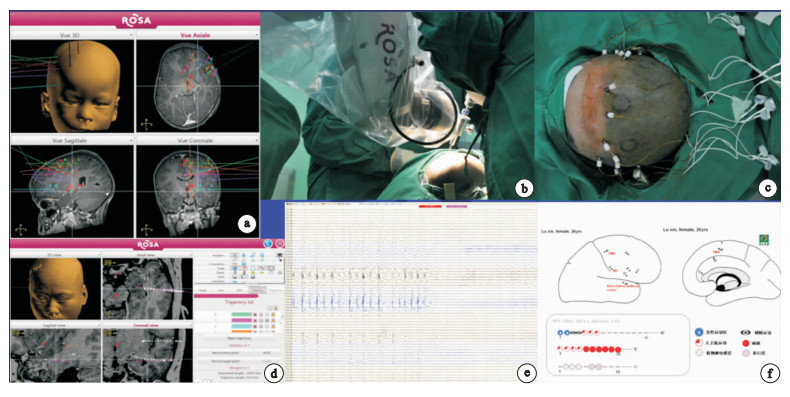
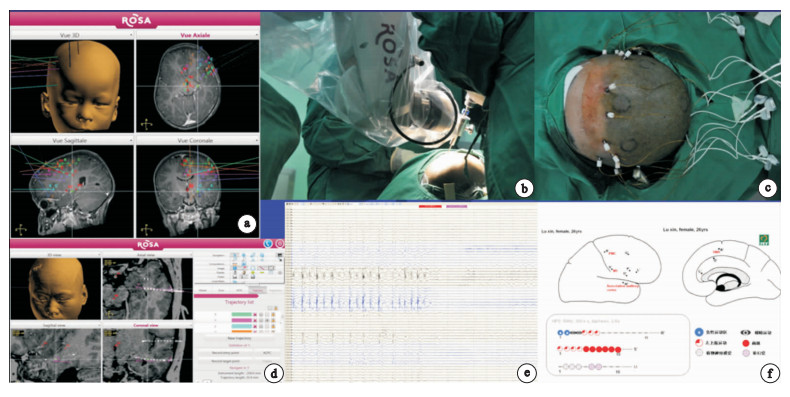 圖1
電極置入及監測程序a.電極置入手術前行MRI掃描及手術計劃,確定電極置入的范圍、電極數量和電極軌跡;b.注冊后按手術計劃在ROSA設備輔助下行SEEG置入;c.電極置入完成后狀態,電極帽固定在導向螺絲上,防止腦脊液外露,電極可以雙側、以任意角度進行置入;d.電極置入術后,行CT掃描,將CT信息與術前MRI信息進行融合,顯示電極各觸電的位置以及與相應腦組織結構之間的關系;e.電極置入后發作期EEG,顯示癇性放電的起源以及可能的傳導順序;f.對相關電極各觸點進行功能mapping,了解對應的組織結構的功能情況
Figure1.
Electrodes implantation a. Underwent MRI before electrode implantation, formulate surgical plan, determine the range, number and track of electrode implantation; b. After registered, operate stereotactic surgery belonging to the plan with the ROSA-assisted equipment; c. The completion status of electrode implantation, the electrode cap was fixed on the guide screws in order to prevent cerebrospinal fluid exposed. Electrodes can be implanted bilaterally and at an arbitrary angle; d. After electrode implantation, underwent CT scan, combine the CT information with the preoperative MRI information, showed the relationship between the position of each electrode of electric shock and the corresponding brain structure; e. EEG during the onset after electrode implantation, showed the origin of epileptic discharge and possible conduction order; f. Functional mapping of related electrode, to understand the function of corresponding structure
圖1
電極置入及監測程序a.電極置入手術前行MRI掃描及手術計劃,確定電極置入的范圍、電極數量和電極軌跡;b.注冊后按手術計劃在ROSA設備輔助下行SEEG置入;c.電極置入完成后狀態,電極帽固定在導向螺絲上,防止腦脊液外露,電極可以雙側、以任意角度進行置入;d.電極置入術后,行CT掃描,將CT信息與術前MRI信息進行融合,顯示電極各觸電的位置以及與相應腦組織結構之間的關系;e.電極置入后發作期EEG,顯示癇性放電的起源以及可能的傳導順序;f.對相關電極各觸點進行功能mapping,了解對應的組織結構的功能情況
Figure1.
Electrodes implantation a. Underwent MRI before electrode implantation, formulate surgical plan, determine the range, number and track of electrode implantation; b. After registered, operate stereotactic surgery belonging to the plan with the ROSA-assisted equipment; c. The completion status of electrode implantation, the electrode cap was fixed on the guide screws in order to prevent cerebrospinal fluid exposed. Electrodes can be implanted bilaterally and at an arbitrary angle; d. After electrode implantation, underwent CT scan, combine the CT information with the preoperative MRI information, showed the relationship between the position of each electrode of electric shock and the corresponding brain structure; e. EEG during the onset after electrode implantation, showed the origin of epileptic discharge and possible conduction order; f. Functional mapping of related electrode, to understand the function of corresponding structure
4 切除性手術及療效隨訪
根據監測結果選擇不同的手術方式,對不能行局灶性切除的選擇調整AEDs或行神經調控性手術等。手術方式包括局灶性的切除、雙側深部核團電刺激、致癇灶的單純熱灼術、迷走神經刺激術等。術后定期隨訪,療效以Engel標準進行分級。
5 統計學方法
采用SPSS 17.0軟件統計分析手術療效,Engel Ⅰ級和Ⅱ級的(療效滿意)與Engel Ⅲ級和Ⅳ級(不滿意)的例數做對比分析。應用分組配對t檢驗,P值≤0.05為差異有統計學意義。
結果
顱內SEEG置入140例, 其中1例置入電極過程中出血,6個月后再次行電極置入;涉及148次電極置入(其中一次電極置入140例、二次置入7例、三次置入1例)。3例術中出血,1例為開顱硬膜下電極置入、1例止血后完成電極置入手術、1例開顱血腫清除后6個月后再次行ROSA。本組除去開顱硬膜下電極置入1例外共148次電極置入,其中左側55例,電極置入共634根,平均每例12根(11.53);右側54例,電極置入共598根,平均每例11根(11.07);雙側31例,電極置入共371根,平均每例12根(11.96)。140次一次置入,其中左側置入的55例,1例出血(改為硬膜下電極置入),致癇灶明確的49例(89.1%),3例彌漫起始,2例行二次的置入電極(1例明確起始,1例行三次置入電極),右側置入的54例,2例出血(其中1例止血后完成電極置入,1例6個月后再次行電極置入手術),致癇灶明確的48例(88.9%),彌漫起始2例,3例行二次置入電極(二次置入電極后均明確致癇灶);雙側31例,其中致癇灶明確的27例(87.1%,其中4例位于雙側顳葉),2例彌漫起始,2例二次置入電極(二次置入電極后均明確致癇灶)。
二次置入的7例患者,除1例三次置入外,6例均明確致癇灶;三次置入的患者最終仍不能明確致癇灶,彌漫,行迷走神經刺激術(VNS)治療。
置入電極后無腦脊液外漏、顱內血腫、電極折斷和死亡病例發生,2例出現頭皮感染(1.43%)。電極置入及監測程序見圖 1,置入后情況見表 2。
行致癇灶切除并且隨訪時間超過6個月的共71例,其中Engel Ⅰ級56例(78.9%),Ⅱ級2例(2.8%),Ⅲ級3例(4.2%),Ⅳ級10例(14.1%)。滿意率為81.7%,不滿意18.3%,兩組比較具有統計學差異(P<0.05)。
討論
1 顱內電極置入是最主要的侵襲性檢查方法
對于難治性癲癇侵襲性檢查,我國目前多家癲癇中心應用的方法就是開顱硬膜下電極置入,包括硬膜下的條狀電極、柵狀電極以及與深部電極的聯合應用。它可以反映皮層的放電情況以及通過它來探測功能區的位置,但它不能監測皮層下和深部結構的放電情況以及癇性放電的傳導,另外在大多數情況下硬膜下電極的置入需要開顱,創傷較大,特別是對需要雙側置入的患者,硬膜下電極就更加不適合了。SEEG彌補了上述方法的不足,對顱內可疑區域,特別是對腦深部區域可以行三維的監測,不但可以監測癇性放電,還可以同時監測癇性放電的傳導。SEEG置入有其標準,總結經驗我們認為:①局灶性癲癇;②不能明確致癇灶的位置及范圍;③不能明確致癇灶與功能性皮層之間的解剖關系。以上三點是所有顱內電極置入都需遵循的標準,SEEG置入的入選標準除了要遵循上述標準外,具有以下四點之一的就應該考慮應用該方法:①存在深部起源的可能性并且這些部位應用硬膜下電極無法達到,如眶額回后部、扣帶回、半球內側以及溝回的深部等;②以往手術失敗的病例(包括切除性的癲癇手術和硬膜下電極置入性手術);③需要對雙側進行監測的;④ MRI陰性的。而且這四點恰恰又是硬膜下電極置入的相對禁忌證。本組140例患者中,23例(16.43%)為MRI陰性;美國克利夫蘭癲癇中心Jorge Gonzalez-Martinez教授報道的100例行SEEG置入的患者中MRI表現陰性的比例較高,有28例[2]。MRI表現陰性的情況下往往需要電極覆蓋較大范圍,SEEG置入手術無需開顱,創傷小,即便置入電極后致癇灶仍不能明確,也是種相對可逆的檢查手段。本組18例既往有手術病史,有手術病史的患者絕大多數情況下硬膜(如果存在)會與腦組織粘連嚴重,不適合開顱硬膜下電極置入。需要雙側置入的31例,91例懷疑有深部放電起源。
頭皮存在感染性病灶或者在電極置入區域存在顱骨缺損的以及擬置入區域有顱骨修補材料和/或人工硬膜材料的均為SEEG置入的禁忌證。另外,如果MRI顯示擬置入電極區域血管阻礙了電極置入并且無法調整電極的置入軌跡時,應考慮及時放棄該手術。
2 癇性放電起源的檢出率及治療性手術效果
本組140例中除1例在置入過程中出現顱內出血而終止電極置入手術外,139例患者均順利完成了置入和立體定向的深部電極VEEG監測,有130例明確了致癇灶的位置,9例致癇灶的位置仍然不清,致癇灶精確定位率達92.9%(130/140)。該比率與其他文獻報道的相似,Jorge Gonzalez-Martinez報道的100例SEEG置入手術,其中4例癇性放電的起源不明確,致癇灶的檢出率為96%[2];Cossu等[3]報道211例患者中明確癇性放電起源的有204例,占96.7%。也有文獻報道,傳統的硬膜下電極能明確癇性放電起源的比率可高達99.2%[4]。雖然致癇灶檢出率很高,但切除后手術療效卻并不很理想。有報道行局灶性切除并且隨訪時間超過12個月的90例患者,其中不再發作的有61例,占67.8%[2];另一些報道認為,切除手術效果不佳還與MRI是否陰性相關,認為MRI陰性的患者效果差,手術后無發作率最低可達18%[5, 6]。還有文獻認為,手術的療效還與致癇灶的位置有關,顳葉外致癇灶的手術效果明顯低于致癇灶位于顳葉的手術效果[7-9]。但Jorge Gonzalez-Martinez等研究認為癲癇的手術療效與MRI是否陰性以及是否為顳葉手術均無關系[2]。Aileen Mc Gonigal等報道100例行SEEG置入的患者,其中MRI陰性43例,陽性57例,電極置入后致癇灶的檢出率分別為95%(41/43)和96%(55/57),MRI陰性和陽性患者行局灶性切除后隨訪1~2年的無發作率分別為55%和53%,也無明顯區別[10]。本組71例行局灶性手術且手術后隨訪時間均超過6個月,其中Engel Ⅰ級56例(78.9%)、Ⅱ級2例(2.8%)、 Ⅲ級3例(4.2%)、Ⅳ級10例(14.1%),滿意率為81.7%。我們的切除手術效果明顯優于其他文獻報道,原因可能如下:① MRI陰性相對少,僅有23例,占患者總數的16.4%;②隨訪時間短,切除性手術療效的規律為隨著時間的延長(可能會在一定的時間范圍內)手術效果逐漸下降,術后6個月隨訪,時間相對較短;③入選標準相對嚴格,在電極置入前,對電極所要置入的范圍和部位都有很清晰的預判;④多次的電極置入,本組有7例在首次電極置入監測后仍不能明確癇性放電的起源,均進行了再次的電極置入,6例最終監測到了癇性放電的起源。
3 并發癥
本組有5例患者出現了并發癥,發生率為3.57%。其中3例在電極置入過程中出現顱內出血,顱內出血的幾率為2.14%,140例共置入電極1 603根,每根電極出血的幾率為0.19%。置入電極后無腦脊液外漏、顱內血腫、電極折斷和死亡病例發生;2例出現頭皮感染,感染率為1.4%(2/139),保守治療后感染治愈。美國克利夫蘭癲癇中心Jorge Gonzalez-Martinez報道100例SEEG置入手術,其中出現了顱內血腫的有3例,發生率為3%(每根電極的出血幾率為0.2%),均保守治療在2周后痊愈,無其他并發癥[2]。Cossu等報道了200例患者的研究經驗,總并發癥發生率為5.6%,其中顱內血腫的發生率為1.0%[3]。不同的文獻也均報道顱內出血是SEEG置入過程中最為常見的并發癥[11-13]。不同的文獻報道硬膜下電極置入的并發癥發生率為0%~26%[14-16],其中最主要的并發癥為血腫及感染。楊崖超等報道112例硬膜下電極置入患者,其中術后腦膿腫2例,硬膜下血腫1例,其他并發癥還包括腦脊液漏和一過性胃腸道反應如嘔吐等[17]。也有研究發現SEEG和硬膜下皮層電極監測在手術結果方面差異不大,但是SEEG具有更少的出血和感染并發癥,是一種安全有效的顱內電極監測方式[18]。Gompel等報道198例顱內電極置人,出現5例感染,6例血腫,發生幾率分別2.5%和3.0%[19]。Fountas和Smith報道185例,術后血腫5例,感染2例,一過性失語2例, 血腫及感染的發生率分別為2.7%和1.1%[20]。還有報道稱,因為有深部的操作,所以其永久并發癥發生率要高于硬膜下電極置入的發生率[21, 22]。本組回顧性病例手術后隨訪時間較短,還不能得出相應的結論,但我們發現SEEG置入的并發癥發生率低于開顱硬膜下電極置入,且硬膜下電極與SEEG置入的手術操作不同以及電極放置的位置不同(一個是硬膜下皮層表面,一個是由皮層到腦深部結構),導致了兩種手術并發癥也不盡相同。因兩者的手術適應證不盡相同,為互相補充的兩種電極置入手段,故單純比較兩者手術后并發癥的幾率意義不大。
SEEG置入手術是一種安全、對致癇灶檢出率高的有創檢查方法,是對傳統的開顱硬膜下電極置入手術的一個有益的補充,特別是ROSA引導的置入方法,手術操作更加簡便并且無需安裝頭架,很好的指導臨床癇灶精確切除。
對于藥物難治性癲癇手術前評估最主要的目的有兩個:首先要明確致癇灶是彌漫的還是局限的,如局限具體位置及范圍如何;其次就是致癇灶與功能區之間的關系。術前評估的方法包括非侵襲和侵襲性的檢查方法,非侵襲性的方法如長程視頻頭皮腦電圖(VEEG)、磁共振(MRI)癲癇平掃以及其它一些特殊的影像學檢查,如腦磁圖(Magnetoencephalo-graphy, MEG)、正電子發射斷層掃描(Positron emission tomography, PET)、發作期的單光子發射計算機斷層掃描(Single photon emission computed tomography, SPECT)和神經心理檢查等[1]。當這些非侵襲性方法不能滿足定位致癇灶以及明確致癇灶與功能區的關系時,就要采取侵襲性檢查方法。目前最主要的侵襲性的檢查方法就是顱內電極置入腦電監測。硬膜下的條狀和柵狀電極置入是我國各癲癇中心常用的方法,它可以反映皮層的放電情況以及通過它來探測功能區的位置,但是它不能監測皮層下和深部結構的放電情況以及癇性放電的傳導,大多數情況下硬膜下電極需要開顱置入,創傷較大,特別是對需要雙側置入的患者,硬膜下電極就更加不適合了。立體定向電極置入技術(Stereoelectroen-cephalography, SEEG)彌補了上述方法的不足,逐漸成為一種常規的侵入性術前評估方法。
回顧性分析我院癲癇中心自2012年3月-2015年6月間采用機器人立體定向手術輔助系統(Robotized stereotactic assistant,ROSA)引導下的SEEG置入的140例藥物難治性癲癇患者,在長程腦電圖監測(VEEG)下進行致癇區定位,大部分患者根據顱內電極監測結果行手術治療,結合術后癲癇控制情況綜合分析SEEG在致癇灶精確定位中的作用。
資料與方法
1 一般資料
收集2012年3月-2015年6月期間我中心診斷為局灶性癲癇并且應用ROSA系統行SEEG置入的癲癇患者140例,年齡3~51歲,電極置入手術時平均年齡為19歲;其中男86例(61.4%),女54例(38.6%)。患者病史1個月~37年不等,平均病史11年。140例患者術前均行頭顱MRI、CT及VEEG檢查,部分患者行MEG和/或PET檢查,顱內電極置入術前均診斷為局灶性藥物難治性癲癇。140例患者中139例順利完成了SEEG置入手術及VEEG監測,1例患者因在電極置入過程中出現顱內出血,終止了顱內電極的置入。另2例置入過程中出血,止血后順利完成SEEG置入手術。71例患者監測后行局灶性手術,且隨訪均為6個月以上。患者一般情況見表 1。
2 術前評估
詳細詢問病史,按照癲癇發作的國際分類標準進行初步的臨床診斷分類。
2.1 顱腦磁共振
140例患者均行顱腦MRI掃描,場強1.5T;掃描除進行常規的T1、T2像掃描外均行T2液體衰減反轉恢復序列(FLAIR)掃描。
2.2 長程視頻腦電監測
所有患者均行32-64導頭皮視頻VEEG監測,監測前不改變所服抗癲癇藥物(AEDs)的種類及劑量。電極安放采用國際10-20系統腦電安裝法。所有患者均捕捉到2次及以上的慣常發作。
3 立體定向顱內電極置入
我院癲癇中心應用ROSA系統進行SEEG置入手術。根據非侵襲檢查的結果,對致癇灶的位置做出合理的假設,劃定致癇灶可能的區域。MRI的掃描需要做雙倍強化的T1掃描,根據MRI掃描數據在計算機上進行電極置入的設計,設計包括電極所需覆蓋的范圍、電極的數量、電極所需達到的靶點以及電極的軌跡;置入電極的部位往往集中在影像學上異常的部位(如果存在)、發作可能起源的結構以及癲癇性放電可能傳導的路徑。電極的置入角度可以與矢狀位垂直的也可以任意角度(圖 1)。電極置入手術在全麻下進行,麻醉清醒后進行VEEG監測。
 圖1
電極置入及監測程序a.電極置入手術前行MRI掃描及手術計劃,確定電極置入的范圍、電極數量和電極軌跡;b.注冊后按手術計劃在ROSA設備輔助下行SEEG置入;c.電極置入完成后狀態,電極帽固定在導向螺絲上,防止腦脊液外露,電極可以雙側、以任意角度進行置入;d.電極置入術后,行CT掃描,將CT信息與術前MRI信息進行融合,顯示電極各觸電的位置以及與相應腦組織結構之間的關系;e.電極置入后發作期EEG,顯示癇性放電的起源以及可能的傳導順序;f.對相關電極各觸點進行功能mapping,了解對應的組織結構的功能情況
Figure1.
Electrodes implantation a. Underwent MRI before electrode implantation, formulate surgical plan, determine the range, number and track of electrode implantation; b. After registered, operate stereotactic surgery belonging to the plan with the ROSA-assisted equipment; c. The completion status of electrode implantation, the electrode cap was fixed on the guide screws in order to prevent cerebrospinal fluid exposed. Electrodes can be implanted bilaterally and at an arbitrary angle; d. After electrode implantation, underwent CT scan, combine the CT information with the preoperative MRI information, showed the relationship between the position of each electrode of electric shock and the corresponding brain structure; e. EEG during the onset after electrode implantation, showed the origin of epileptic discharge and possible conduction order; f. Functional mapping of related electrode, to understand the function of corresponding structure
圖1
電極置入及監測程序a.電極置入手術前行MRI掃描及手術計劃,確定電極置入的范圍、電極數量和電極軌跡;b.注冊后按手術計劃在ROSA設備輔助下行SEEG置入;c.電極置入完成后狀態,電極帽固定在導向螺絲上,防止腦脊液外露,電極可以雙側、以任意角度進行置入;d.電極置入術后,行CT掃描,將CT信息與術前MRI信息進行融合,顯示電極各觸電的位置以及與相應腦組織結構之間的關系;e.電極置入后發作期EEG,顯示癇性放電的起源以及可能的傳導順序;f.對相關電極各觸點進行功能mapping,了解對應的組織結構的功能情況
Figure1.
Electrodes implantation a. Underwent MRI before electrode implantation, formulate surgical plan, determine the range, number and track of electrode implantation; b. After registered, operate stereotactic surgery belonging to the plan with the ROSA-assisted equipment; c. The completion status of electrode implantation, the electrode cap was fixed on the guide screws in order to prevent cerebrospinal fluid exposed. Electrodes can be implanted bilaterally and at an arbitrary angle; d. After electrode implantation, underwent CT scan, combine the CT information with the preoperative MRI information, showed the relationship between the position of each electrode of electric shock and the corresponding brain structure; e. EEG during the onset after electrode implantation, showed the origin of epileptic discharge and possible conduction order; f. Functional mapping of related electrode, to understand the function of corresponding structure
4 切除性手術及療效隨訪
根據監測結果選擇不同的手術方式,對不能行局灶性切除的選擇調整AEDs或行神經調控性手術等。手術方式包括局灶性的切除、雙側深部核團電刺激、致癇灶的單純熱灼術、迷走神經刺激術等。術后定期隨訪,療效以Engel標準進行分級。
5 統計學方法
采用SPSS 17.0軟件統計分析手術療效,Engel Ⅰ級和Ⅱ級的(療效滿意)與Engel Ⅲ級和Ⅳ級(不滿意)的例數做對比分析。應用分組配對t檢驗,P值≤0.05為差異有統計學意義。
結果
顱內SEEG置入140例, 其中1例置入電極過程中出血,6個月后再次行電極置入;涉及148次電極置入(其中一次電極置入140例、二次置入7例、三次置入1例)。3例術中出血,1例為開顱硬膜下電極置入、1例止血后完成電極置入手術、1例開顱血腫清除后6個月后再次行ROSA。本組除去開顱硬膜下電極置入1例外共148次電極置入,其中左側55例,電極置入共634根,平均每例12根(11.53);右側54例,電極置入共598根,平均每例11根(11.07);雙側31例,電極置入共371根,平均每例12根(11.96)。140次一次置入,其中左側置入的55例,1例出血(改為硬膜下電極置入),致癇灶明確的49例(89.1%),3例彌漫起始,2例行二次的置入電極(1例明確起始,1例行三次置入電極),右側置入的54例,2例出血(其中1例止血后完成電極置入,1例6個月后再次行電極置入手術),致癇灶明確的48例(88.9%),彌漫起始2例,3例行二次置入電極(二次置入電極后均明確致癇灶);雙側31例,其中致癇灶明確的27例(87.1%,其中4例位于雙側顳葉),2例彌漫起始,2例二次置入電極(二次置入電極后均明確致癇灶)。
二次置入的7例患者,除1例三次置入外,6例均明確致癇灶;三次置入的患者最終仍不能明確致癇灶,彌漫,行迷走神經刺激術(VNS)治療。
置入電極后無腦脊液外漏、顱內血腫、電極折斷和死亡病例發生,2例出現頭皮感染(1.43%)。電極置入及監測程序見圖 1,置入后情況見表 2。
行致癇灶切除并且隨訪時間超過6個月的共71例,其中Engel Ⅰ級56例(78.9%),Ⅱ級2例(2.8%),Ⅲ級3例(4.2%),Ⅳ級10例(14.1%)。滿意率為81.7%,不滿意18.3%,兩組比較具有統計學差異(P<0.05)。
討論
1 顱內電極置入是最主要的侵襲性檢查方法
對于難治性癲癇侵襲性檢查,我國目前多家癲癇中心應用的方法就是開顱硬膜下電極置入,包括硬膜下的條狀電極、柵狀電極以及與深部電極的聯合應用。它可以反映皮層的放電情況以及通過它來探測功能區的位置,但它不能監測皮層下和深部結構的放電情況以及癇性放電的傳導,另外在大多數情況下硬膜下電極的置入需要開顱,創傷較大,特別是對需要雙側置入的患者,硬膜下電極就更加不適合了。SEEG彌補了上述方法的不足,對顱內可疑區域,特別是對腦深部區域可以行三維的監測,不但可以監測癇性放電,還可以同時監測癇性放電的傳導。SEEG置入有其標準,總結經驗我們認為:①局灶性癲癇;②不能明確致癇灶的位置及范圍;③不能明確致癇灶與功能性皮層之間的解剖關系。以上三點是所有顱內電極置入都需遵循的標準,SEEG置入的入選標準除了要遵循上述標準外,具有以下四點之一的就應該考慮應用該方法:①存在深部起源的可能性并且這些部位應用硬膜下電極無法達到,如眶額回后部、扣帶回、半球內側以及溝回的深部等;②以往手術失敗的病例(包括切除性的癲癇手術和硬膜下電極置入性手術);③需要對雙側進行監測的;④ MRI陰性的。而且這四點恰恰又是硬膜下電極置入的相對禁忌證。本組140例患者中,23例(16.43%)為MRI陰性;美國克利夫蘭癲癇中心Jorge Gonzalez-Martinez教授報道的100例行SEEG置入的患者中MRI表現陰性的比例較高,有28例[2]。MRI表現陰性的情況下往往需要電極覆蓋較大范圍,SEEG置入手術無需開顱,創傷小,即便置入電極后致癇灶仍不能明確,也是種相對可逆的檢查手段。本組18例既往有手術病史,有手術病史的患者絕大多數情況下硬膜(如果存在)會與腦組織粘連嚴重,不適合開顱硬膜下電極置入。需要雙側置入的31例,91例懷疑有深部放電起源。
頭皮存在感染性病灶或者在電極置入區域存在顱骨缺損的以及擬置入區域有顱骨修補材料和/或人工硬膜材料的均為SEEG置入的禁忌證。另外,如果MRI顯示擬置入電極區域血管阻礙了電極置入并且無法調整電極的置入軌跡時,應考慮及時放棄該手術。
2 癇性放電起源的檢出率及治療性手術效果
本組140例中除1例在置入過程中出現顱內出血而終止電極置入手術外,139例患者均順利完成了置入和立體定向的深部電極VEEG監測,有130例明確了致癇灶的位置,9例致癇灶的位置仍然不清,致癇灶精確定位率達92.9%(130/140)。該比率與其他文獻報道的相似,Jorge Gonzalez-Martinez報道的100例SEEG置入手術,其中4例癇性放電的起源不明確,致癇灶的檢出率為96%[2];Cossu等[3]報道211例患者中明確癇性放電起源的有204例,占96.7%。也有文獻報道,傳統的硬膜下電極能明確癇性放電起源的比率可高達99.2%[4]。雖然致癇灶檢出率很高,但切除后手術療效卻并不很理想。有報道行局灶性切除并且隨訪時間超過12個月的90例患者,其中不再發作的有61例,占67.8%[2];另一些報道認為,切除手術效果不佳還與MRI是否陰性相關,認為MRI陰性的患者效果差,手術后無發作率最低可達18%[5, 6]。還有文獻認為,手術的療效還與致癇灶的位置有關,顳葉外致癇灶的手術效果明顯低于致癇灶位于顳葉的手術效果[7-9]。但Jorge Gonzalez-Martinez等研究認為癲癇的手術療效與MRI是否陰性以及是否為顳葉手術均無關系[2]。Aileen Mc Gonigal等報道100例行SEEG置入的患者,其中MRI陰性43例,陽性57例,電極置入后致癇灶的檢出率分別為95%(41/43)和96%(55/57),MRI陰性和陽性患者行局灶性切除后隨訪1~2年的無發作率分別為55%和53%,也無明顯區別[10]。本組71例行局灶性手術且手術后隨訪時間均超過6個月,其中Engel Ⅰ級56例(78.9%)、Ⅱ級2例(2.8%)、 Ⅲ級3例(4.2%)、Ⅳ級10例(14.1%),滿意率為81.7%。我們的切除手術效果明顯優于其他文獻報道,原因可能如下:① MRI陰性相對少,僅有23例,占患者總數的16.4%;②隨訪時間短,切除性手術療效的規律為隨著時間的延長(可能會在一定的時間范圍內)手術效果逐漸下降,術后6個月隨訪,時間相對較短;③入選標準相對嚴格,在電極置入前,對電極所要置入的范圍和部位都有很清晰的預判;④多次的電極置入,本組有7例在首次電極置入監測后仍不能明確癇性放電的起源,均進行了再次的電極置入,6例最終監測到了癇性放電的起源。
3 并發癥
本組有5例患者出現了并發癥,發生率為3.57%。其中3例在電極置入過程中出現顱內出血,顱內出血的幾率為2.14%,140例共置入電極1 603根,每根電極出血的幾率為0.19%。置入電極后無腦脊液外漏、顱內血腫、電極折斷和死亡病例發生;2例出現頭皮感染,感染率為1.4%(2/139),保守治療后感染治愈。美國克利夫蘭癲癇中心Jorge Gonzalez-Martinez報道100例SEEG置入手術,其中出現了顱內血腫的有3例,發生率為3%(每根電極的出血幾率為0.2%),均保守治療在2周后痊愈,無其他并發癥[2]。Cossu等報道了200例患者的研究經驗,總并發癥發生率為5.6%,其中顱內血腫的發生率為1.0%[3]。不同的文獻也均報道顱內出血是SEEG置入過程中最為常見的并發癥[11-13]。不同的文獻報道硬膜下電極置入的并發癥發生率為0%~26%[14-16],其中最主要的并發癥為血腫及感染。楊崖超等報道112例硬膜下電極置入患者,其中術后腦膿腫2例,硬膜下血腫1例,其他并發癥還包括腦脊液漏和一過性胃腸道反應如嘔吐等[17]。也有研究發現SEEG和硬膜下皮層電極監測在手術結果方面差異不大,但是SEEG具有更少的出血和感染并發癥,是一種安全有效的顱內電極監測方式[18]。Gompel等報道198例顱內電極置人,出現5例感染,6例血腫,發生幾率分別2.5%和3.0%[19]。Fountas和Smith報道185例,術后血腫5例,感染2例,一過性失語2例, 血腫及感染的發生率分別為2.7%和1.1%[20]。還有報道稱,因為有深部的操作,所以其永久并發癥發生率要高于硬膜下電極置入的發生率[21, 22]。本組回顧性病例手術后隨訪時間較短,還不能得出相應的結論,但我們發現SEEG置入的并發癥發生率低于開顱硬膜下電極置入,且硬膜下電極與SEEG置入的手術操作不同以及電極放置的位置不同(一個是硬膜下皮層表面,一個是由皮層到腦深部結構),導致了兩種手術并發癥也不盡相同。因兩者的手術適應證不盡相同,為互相補充的兩種電極置入手段,故單純比較兩者手術后并發癥的幾率意義不大。
SEEG置入手術是一種安全、對致癇灶檢出率高的有創檢查方法,是對傳統的開顱硬膜下電極置入手術的一個有益的補充,特別是ROSA引導的置入方法,手術操作更加簡便并且無需安裝頭架,很好的指導臨床癇灶精確切除。