國內外學者對鎳鈦合金血管支架的力學性能進行了多方面的研究,關于不同釋放尺度下的髂靜脈支架力學性能的研究尚未見報道。利用有限元法,對自主研發的三款鎳鈦合金髂靜脈支架力學性能進行研究,揭示支架直徑(12、14、16 mm)與不同釋放尺度(80%、90%)對其強度、疲勞壽命和靜脈壁生物力學性能影響的規律。研究結果顯示,不同直徑的支架隨著釋放尺度的增加,支架彈性應變、血管壁等效應力和疲勞強度的安全系數均有減小的趨勢,危險截面發生在支架連接桿圓弧處。通過 30 天、60 天和 90 天的動物實驗,對 12 頭豬的髂靜脈建立狹窄的血管模型,植入研發的髂靜脈支架,綜合評價支架的安全性和有效性,同時驗證了三款支架的力學性能,為后續產品的型式檢驗及臨床試驗提供了重要的參考依據。
引用本文: 馮海全, 王淑彪, 王永剛, 李曉強, 王曉天. 不同釋放尺度下新型鎳鈦合金髂靜脈支架力學性能和動物實驗研究. 生物醫學工程學雜志, 2019, 36(6): 1024-1031. doi: 10.7507/1001-5515.201807006 復制
版權信息: ?四川大學華西醫院華西期刊社《生物醫學工程學雜志》版權所有,未經授權不得轉載、改編
引言
髂靜脈壓迫綜合征(iliac venous compression syndrome,IVCS)是指由于髂靜脈受壓和(或)存在腔內異常粘連所引起的下肢和盆腔靜脈回流障礙的疾病,是下肢靜脈瓣膜功能不全和淺靜脈曲張的主要原因之一。在臨床治療中,對病變狹窄大于 50% 以上的 IVCS 患者,均建議進行支架植入手術[1]。然而目前,在臨床上對于髂靜脈病變使用的支架均是專為動脈設計的支架。
用于治療 IVCS 的支架的早期經驗全部是基于波士頓科學公司的 Wallstent 支架。該支架是由不銹鋼絲編織而成的管狀結構,盡管表現好于預期,但是在特定的髂-腔解剖條件下有一定的局限性,大約有 25% 的支架需要糾正支架內再狹窄或支架受壓。近年來,臨床以 Luminexx 支架(Bard 公司,美國)和 Smart control 支架(Cordis 公司,美國)最為常用,兩種支架是由激光雕刻切割形成,膨脹后支架短縮小、柔順性好,易于定位,是目前常用于髂靜脈部位的支架。但是,Luminexx 支架和 Smart control 支架均為動脈專用支架。目前,國內臨床上用于治療 IVCS 的支架也是以動脈支架為主,但是髂靜脈支架植入術的適應證和治療目的與動脈支架有諸多不同。冠狀動脈狹窄是粥樣硬化所致,當狹窄到一定程度就會導致心肌缺血。髂靜脈狹窄是髂靜脈受壓或存在腔內異常粘連結構所引起的下肢和盆腔靜脈回流障礙性疾病,其發病原因與解剖位置有關,右髂總動脈跨越左髂總靜脈的前方,左髂總靜脈處于腰骶椎的生理性前凸和右髂總動脈之間,受前后夾擠形成狹窄。因此,研究一種符合髂靜脈解剖特點的專用支架具有重要的臨床意義和良好的應用前景。
支架植入人體后,在血管脈流的長期作用下,可能會出現支架變形、移位、疲勞斷裂等導致失效。很多報道中顯示,支架植入人體后發生斷裂的現象較為頻繁[2-3]。因此,在血管支架的研發過程中金屬支架的疲勞強度是需要考慮的重要因素之一。在測定鎳鈦合金支架疲勞強度的實驗方面,早期研究人員對鎳鈦合金支架進行了單一方式的疲勞測試[4]。Harrison 等[5]測試了 V 型鎳鈦合金支架的彎曲疲勞行為,結果表明隨著平均應變的增加,應力變化幅度減小,從而疲勞壽命增加。Tolomeo 等[6]對相變溫度點在 28℃ 左右的鎳鈦合金支架進行了拉伸疲勞實驗。近幾年,Marrey[7]利用美國 Bose 公司研制的加速疲勞試驗機,模擬支架在血管內的工作狀態,驗證了支架 10 年疲勞壽命。在國內,趙振心等[8]對鎳鈦合金血管支架進行有限元分析和疲勞性能測試,評價了鎳鈦合金支架的疲勞強度。李建軍等[9]利用疲勞圖譜研究不同圓弧段尺寸對鎳鈦合金支架疲勞特性的影響,發現鎳鈦合金支架的疲勞性能與圓弧段尺寸密切相關。易沛林[10]利用有限元技術模擬分析了兩種不同支架結構的軸向力學性能和疲勞性能,得出有限元分析技術可以方便地對鎳鈦合金支架及其作用的生理環境進行模擬。
本文主要研究了自主研發的三款鎳鈦合金髂靜脈支架在不同釋放尺度下的力學性能和動物實驗。通過繪制支架疲勞極限應變線圖以及計算出支架動態安全系數,總結出不同釋放尺度對鎳鈦合金髂靜脈支架疲勞強度的影響,并結合動物實驗驗證了其安全性和有效性,為鎳鈦合金髂靜脈支架的研發和臨床應用提供科學的參考依據。
1 材料與方法
1.1 材料模型
材料模型采用 ABAQUS 軟件中專用的超彈性材料模塊,根據該模塊設置鎳鈦合金應力—應變關系。支架材料的應力—應變關系是通過對鎳鈦合金試件進行拉伸卸載實驗后得到的。實驗設備為日本 SHIMADZU 制 DSS-500 數字式萬能拉壓實驗機。應變信號采集器為日本 KYOWA 電工的 DBU-120 型信號采集器。載荷使用日本 KYOWA 電工的 PCD-300B 型傳感器以 100 Hz 的頻率進行數據采集。試件使用與支架成分相同且經過相同熱處理的直徑 0.5 mm、長度 100 mm 的 NiTi 合金絲材。實驗測試速度為 12.7 mm/min,環境溫度為 25 oC。先進行定量的壓縮后再進行拉伸試驗,每組樣品測試 3 次。分析時取其平均值作為材料力學性能參數,得到支架模擬的材料屬性。測試的 NiTi 合金絲的彈性模量 E = 80 GPa,泊松比 0.3,抗拉強度 1 290 MPa,屈服強度 390~610 MPa,延伸率 0.147。實驗結果為公稱應力應變值,考慮到材料在實際拉伸過程中的形變,通過公式(1)和(2)得到材料真實應力應變值:
 |
 |
式中, 、
、 為公稱應力與應變;
為公稱應力與應變; 、
、 為材料的真實應力與應變。將材料的真實應力應變輸入到 ABAQUS 中作為支架材料的力學性能參數。
為材料的真實應力與應變。將材料的真實應力應變輸入到 ABAQUS 中作為支架材料的力學性能參數。
1.2 支架模型
該新型髂靜脈支架主要通過獨特的結構設計治療髂靜脈受壓后引起的下肢和盆腔靜脈回流障礙性疾病,可大大降低血栓發生率。支架的前端設計成較疏的花冠,支架網孔小,提高了髂靜脈支架的遠期通暢率;支架的花冠部分與網孔較小的中央支撐單元連接處設置顯影標記,提高支架的定位及釋放的準確性;同時,通過降低支架的末端支撐單元的支撐力,減少支架對靜脈壁的傷害,可以完全滿足臨床使用要求。支架筋寬為 0.16 mm,壁厚 0.22 mm,花冠開口與軸線相夾 20°,并在花冠與中部、末端各有 3 個顯影標記。支架直徑分別為 12、14、16 mm,長度均為 26 mm,以下稱為支架 L-12、L-14 和 L-16。目前在支架結構設計方面已獲得發明專利 3 項[11-13]。
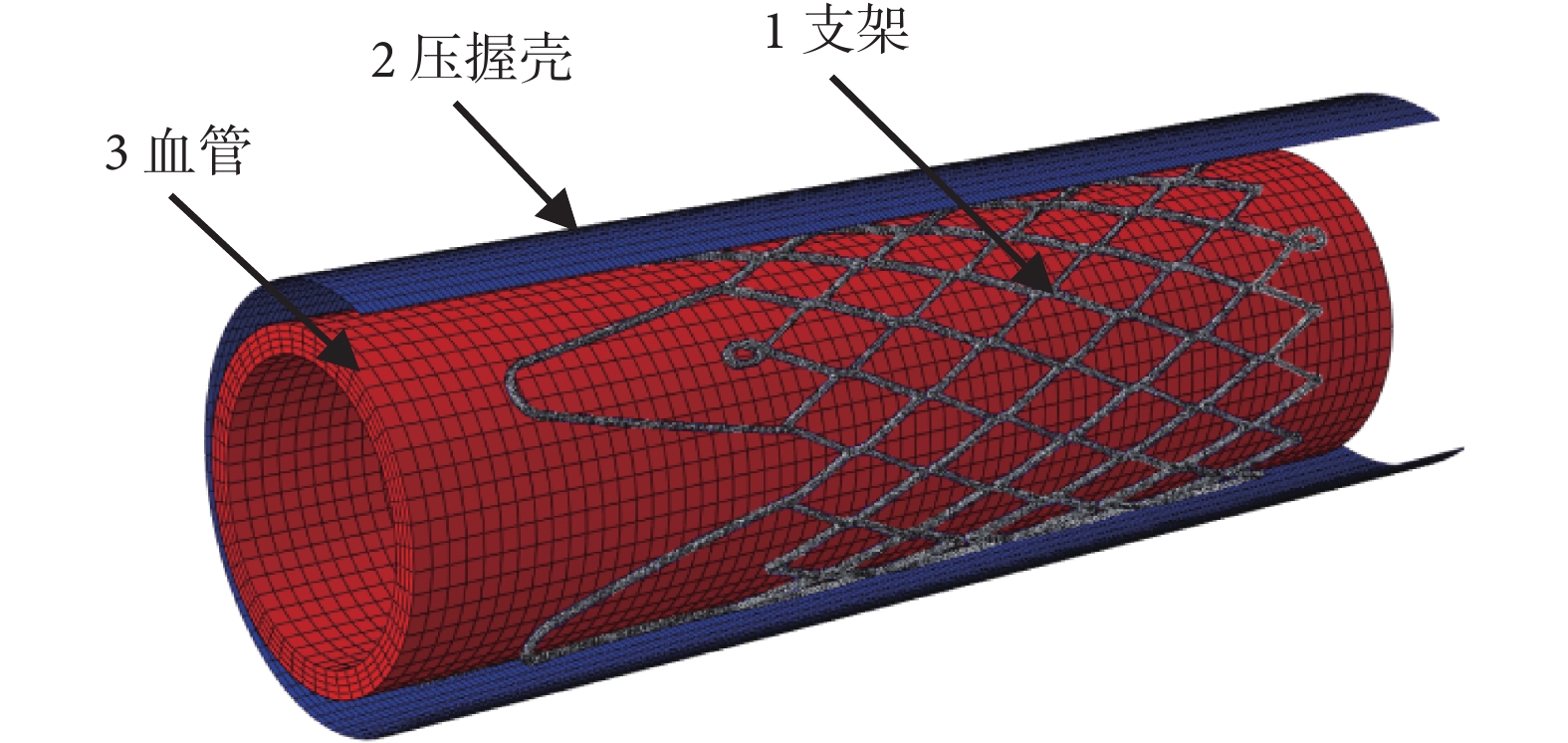
圖 1 為支架、壓握殼和血管導入到 ABAQUS 分析軟件后的系統模型,其中 1、2、3 分別為支架、壓握殼和血管模型。在構造仿真模型時,在有限元軟件 ABAQUS 中通過移動(move)、旋轉(rotate)等功能,使三個模型合理裝配在一起。建立壓握殼時,使其直徑大于支架外徑,確保裝配時壓握殼與支架不接觸。壓握殼和血管應有足夠的長度,保證支架內外圓柱表面上均勻受壓。即在支架大變形過程中,壓握殼和支架(支架被壓握至 3 mm 時),以及支架和血管(支架釋放至血管內時)能實現充分接觸。有限元分析過程中,在圓柱坐標系中先通過壓握殼的徑向位移壓握支架至 3 mm,再分別以不同的釋放尺度(80% 和 90%)使支架釋放至血管內,最后分別對支架和血管內表面施加循環載荷評價支架的疲勞強度。文中結合有關文獻報道設置壓握殼與血管壁為超彈性材料,壓握殼彈性模量為 300 MPa,血管壁彈性模量為 1.75 MPa,泊松比均為 0.499[14-15]。
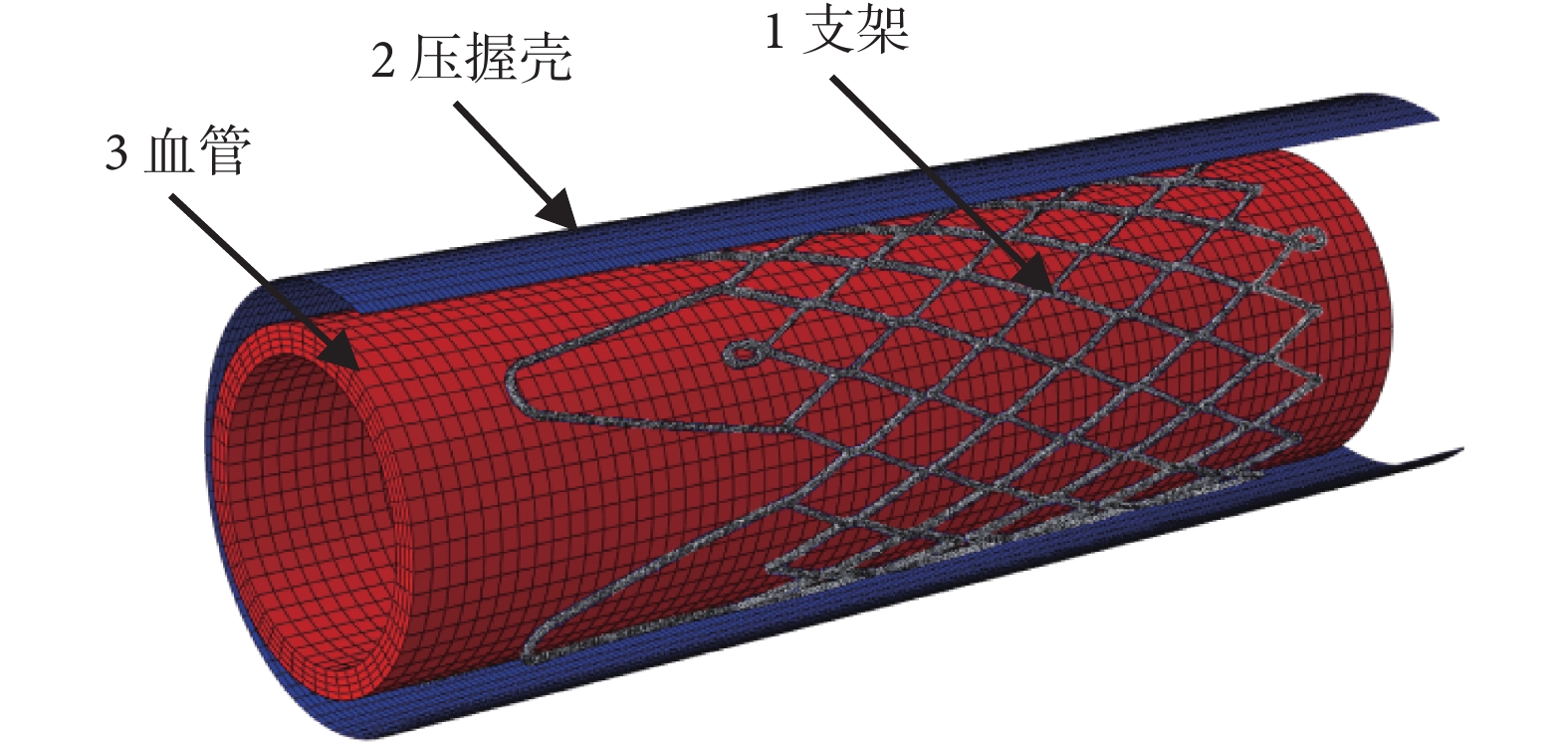 圖1
支架系統模型示意圖
Figure1.
Figure of stent system
圖1
支架系統模型示意圖
Figure1.
Figure of stent system
1.3 載荷定義
支架植入髂靜脈后,受到脈流周期性疲勞載荷作用,分析時通過對支架外表面施加交替變化的作用力來進行模擬。首先在 ABAQUS 分析軟件里建立壓握殼、血管、支架的有限元模型,通過壓握殼的徑向位移使支架壓握至 3 mm,再釋放到不同直徑的血管內。其次對血管和支架施加周期循環載荷模擬人體血管內的脈流循環載荷,即疲勞強度的分析是在支架釋放后進行的。支架承受循環變載荷時應以具有 10 年疲勞壽命為前提。髂靜脈血壓值在 3~9 mm Hg,對應壓力值為 0.000 4~0.001 2 MPa。在有限元計算中為了分析結果的準確性和科學性,模擬的周期加載過程重復多次進行。
1.4 評價指標
髂靜脈支架疲勞強度的評價準則是根據 Pelton 等[16]提出的針對鎳鈦合金材料的疲勞強度評價方法。有限元模型計算結束后,首先從結果文件 odb 中導出支架在動態加載過程中所有節點的最大和最小彈性應變,并且在 EXCEL 表格中分別應用公式(3)和(4)計算支架所有節點的平均應變和應變幅。最后為了對比分析支架在不同釋放尺度下的安全性能,本文分別以公式(5)計算出支架安全系數(SFdynamic)[5]。支架疲勞強度的安全系數計算方法如下:
 |
 |
 |
式中,SFdynamic 為疲勞強度的安全系數,δuts 為延伸率,δε 為疲勞極限,δmax 和 δmin 分別為脈動循環載荷的最大和最小彈性應變,δmean 和 δalt 分別為支架在脈動載荷下的平均應變和應變幅。
1.5 有限元模型
本文應用 ABAQUS 有限元軟件的 Explicit 求解模塊對支架系統進行顯示動態分析,該求解方法可以有效地模擬大變形非線性等問題[17]。髂靜脈支架的植入過程涉及壓握殼、血管與支架之間的非線性耦合作用。利用廣義變分原理和懲罰函數法,以不可侵徹性條件作為接觸問題的動力學及運動學約束條件,建立髂靜脈支架介入耦合系統計算模型的等效形式[18],表示為:
 |
式中,δpc 為接觸問題的總虛功,δ 為變分算子,σji 為柯西應力張量,bi、 分別為體力和面力,vi、
分別為體力和面力,vi、 分別為質點的速度和加速度,ρ 是材料密度,γN、γT 分別為接觸界面的相互侵徹率與相對切向速度,tT 是接觸界面切向面力,P 為接觸界面法相壓力,表示為:
分別為質點的速度和加速度,ρ 是材料密度,γN、γT 分別為接觸界面的相互侵徹率與相對切向速度,tT 是接觸界面切向面力,P 為接觸界面法相壓力,表示為:
 |
式中,β1、β2 為罰參數, 為 Heaviside 分布函數,gN 為接觸界面相互侵徹量,可表示為最近點映射形式:
為 Heaviside 分布函數,gN 為接觸界面相互侵徹量,可表示為最近點映射形式:
 |
式中, 、
、 分別代表主控體 A 與從屬體 B 接觸界面質點的歐拉坐標,?、
分別代表主控體 A 與從屬體 B 接觸界面質點的歐拉坐標,?、 表示相應接觸界面的曲面坐標,t 表示時間。由此,利用非線性有限元方法,建立方程(6)的 Lagrangian 離散格式,通過 Newton-Raphson 隱式迭代格式來求解支架被壓握和釋放過程的有限元方程。
表示相應接觸界面的曲面坐標,t 表示時間。由此,利用非線性有限元方法,建立方程(6)的 Lagrangian 離散格式,通過 Newton-Raphson 隱式迭代格式來求解支架被壓握和釋放過程的有限元方程。
2 有限元分析結果
2.1 支架力學性能
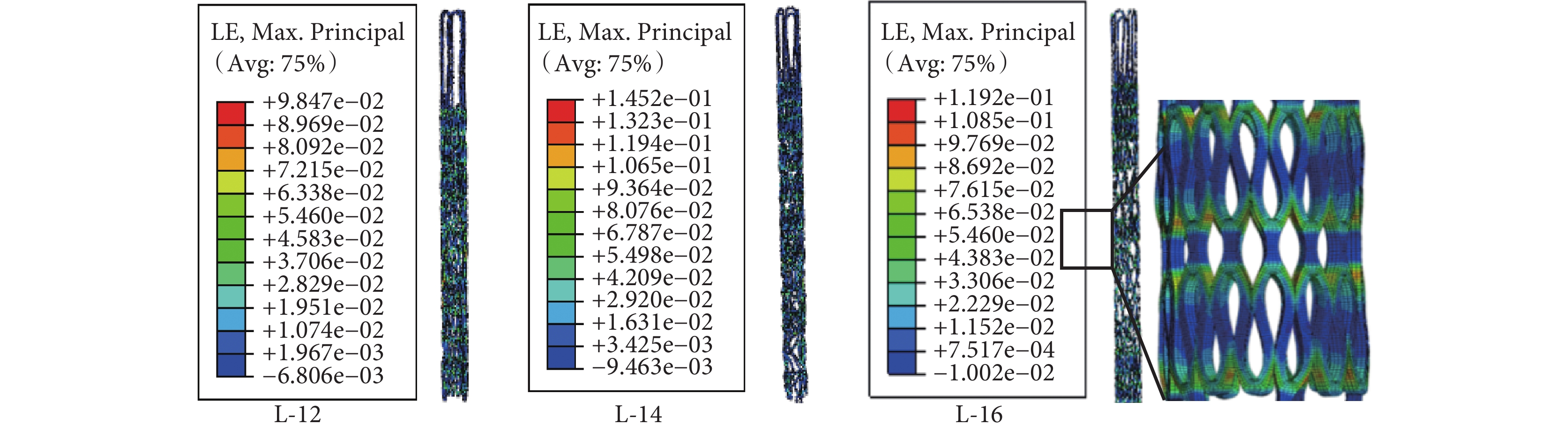
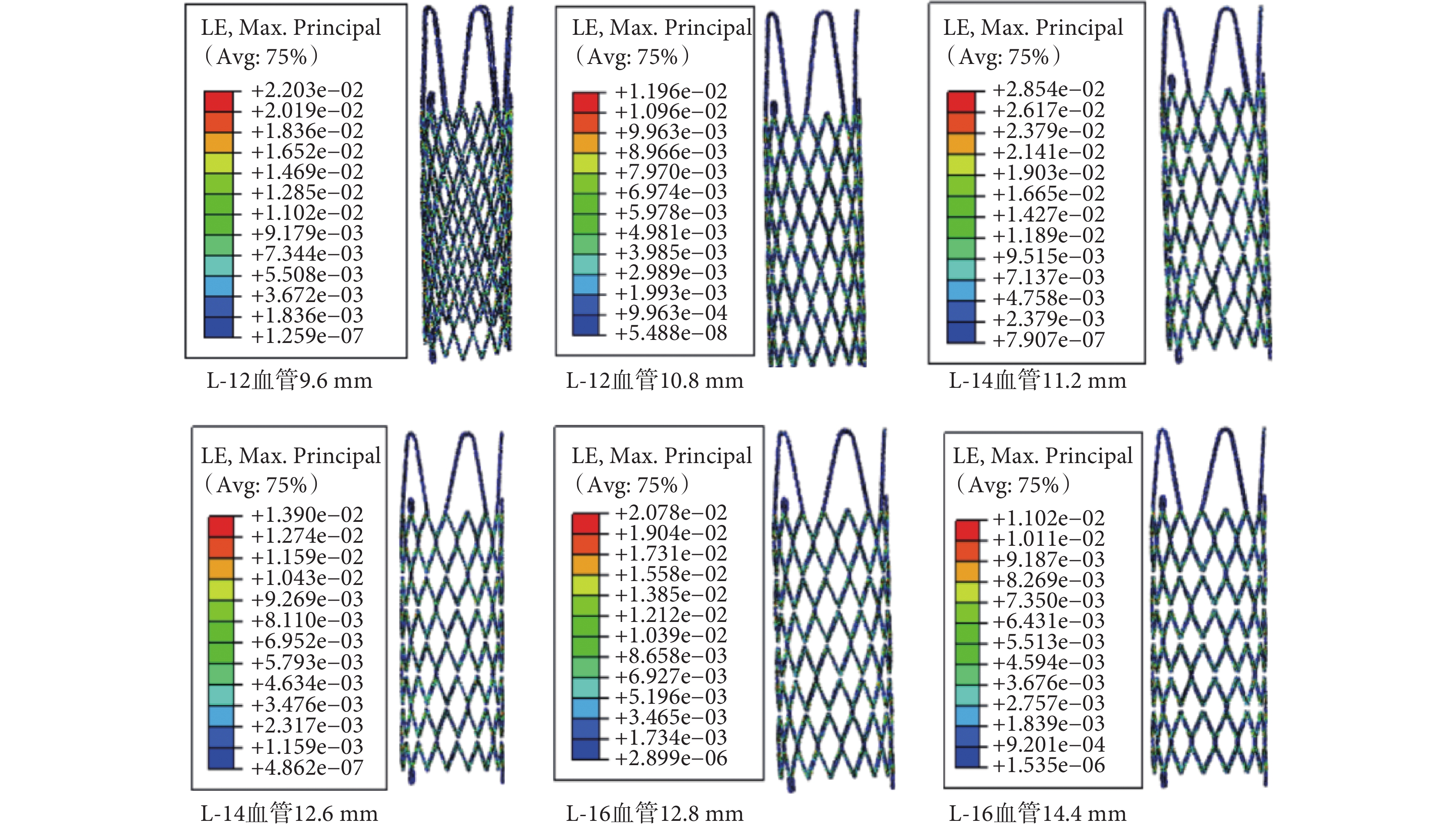
三款支架分別從 12、14、16 mm 壓握至 3 mm 時的彈性應變云圖如圖 2 所示。圖 3 為三款支架在不同釋放尺度(80% 和 90%)下的彈性應變云圖。結果顯示:支架被壓握和釋放時最大應變都發生在支撐體和圓弧段相交區域的內外兩側,并小于材料延伸率 15%。當壓握至 3 mm 時三款支架的應變相差不大,都在 9.8%~14.5%,其中支架 L-14 的應變最大,支架 L-16 次之,支架 L-12 最小;隨著釋放尺度的增大,支架彈性應變呈現遞減的趨勢。如表 1 所示,三款支架 L-12、L-14、L-16 的應變遞減率分別為 45%、52%、48%,其中支架 L-14 最大,支架 L-16 次之,支架 L-12 最小。
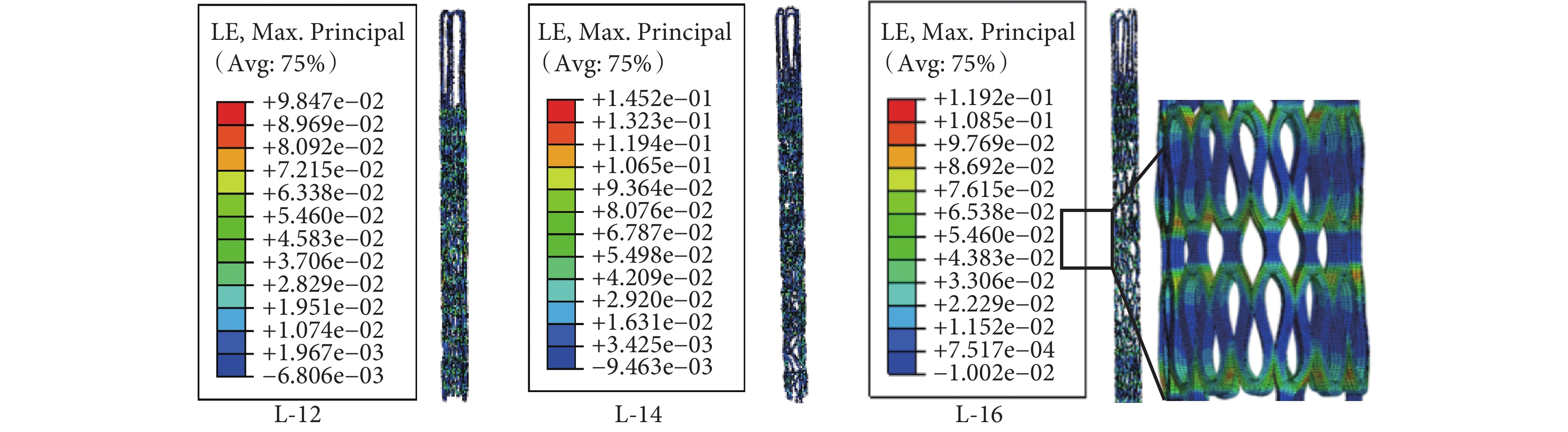 圖2
支架壓握至 DVessel = 3 mm 時的彈性應變云圖
Figure2.
Equivalent transformation strain of the stents at the end of crimping DVessel = 3.0 mm
圖2
支架壓握至 DVessel = 3 mm 時的彈性應變云圖
Figure2.
Equivalent transformation strain of the stents at the end of crimping DVessel = 3.0 mm
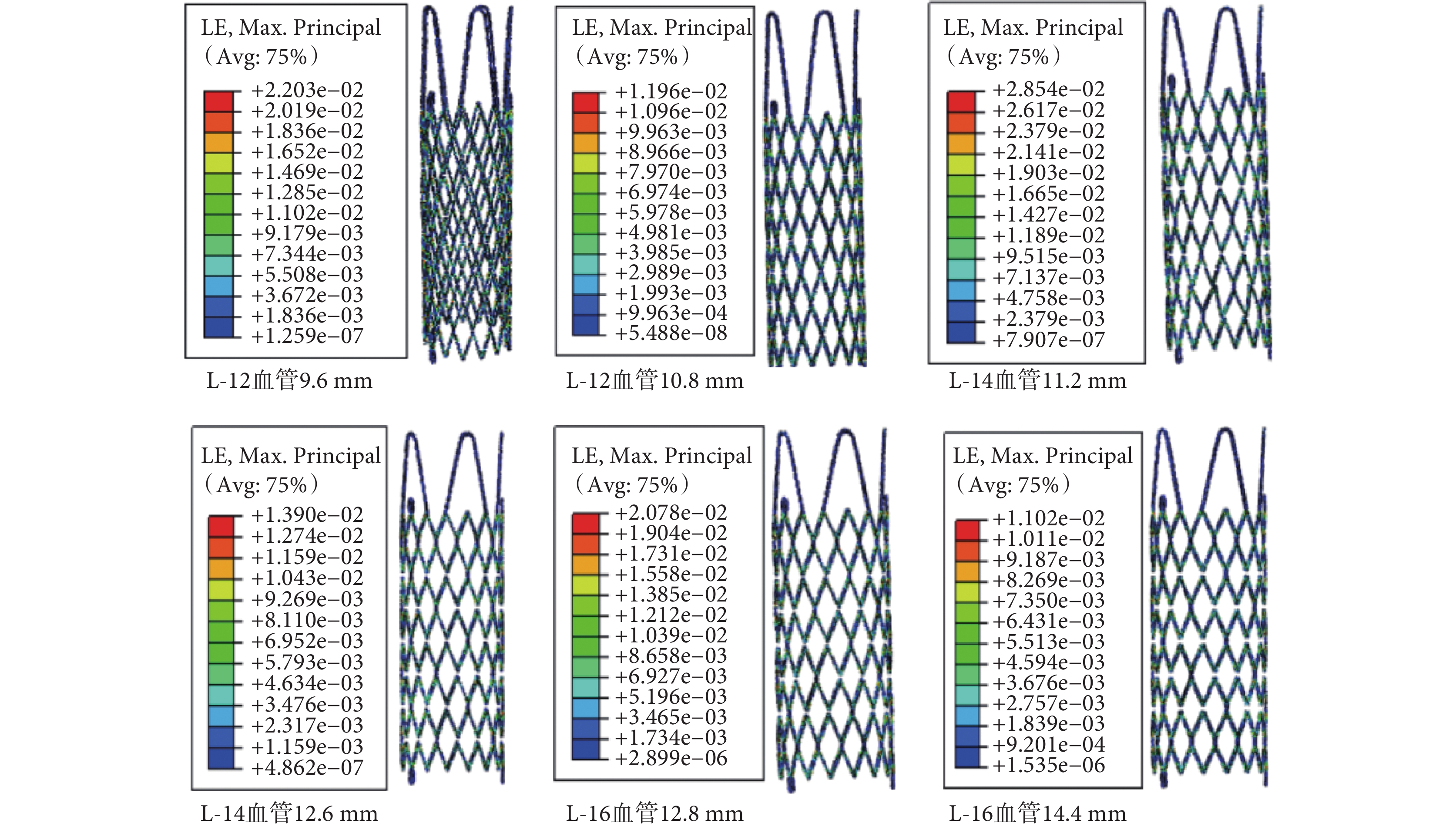 圖3
支架彈性應變云圖
Figure3.
Equivalent transformation strain of the stents
圖3
支架彈性應變云圖
Figure3.
Equivalent transformation strain of the stents
2.2 血管力學性能
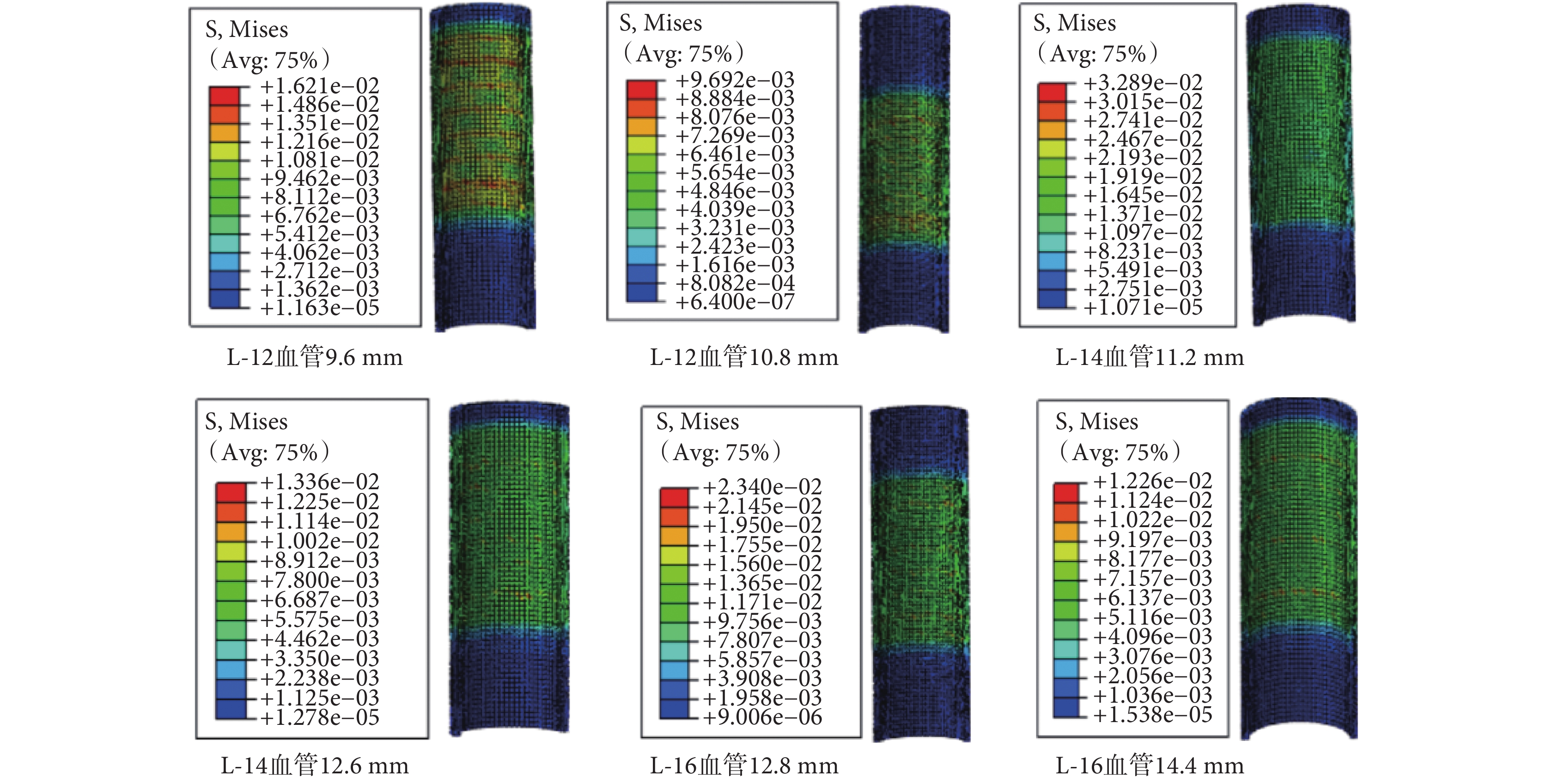
圖 4 為三款支架在不同釋放尺度(80% 和 90%)下對應的血管等效應力云圖。結果顯示,在血管內壁與支架支撐體接觸處有局部的應力集中現象,并隨著支架釋放尺度的增大,血管等效應力呈現減小的趨勢。如表 1 所示,三款支架 L-12、L-14、L-16 對應的血管等效應力遞減率分別為 44%、60%、48%,其中支架 L-14 對應的血管等效應力遞減率最大,支架 L-16 次之,支架 L-12 最小。
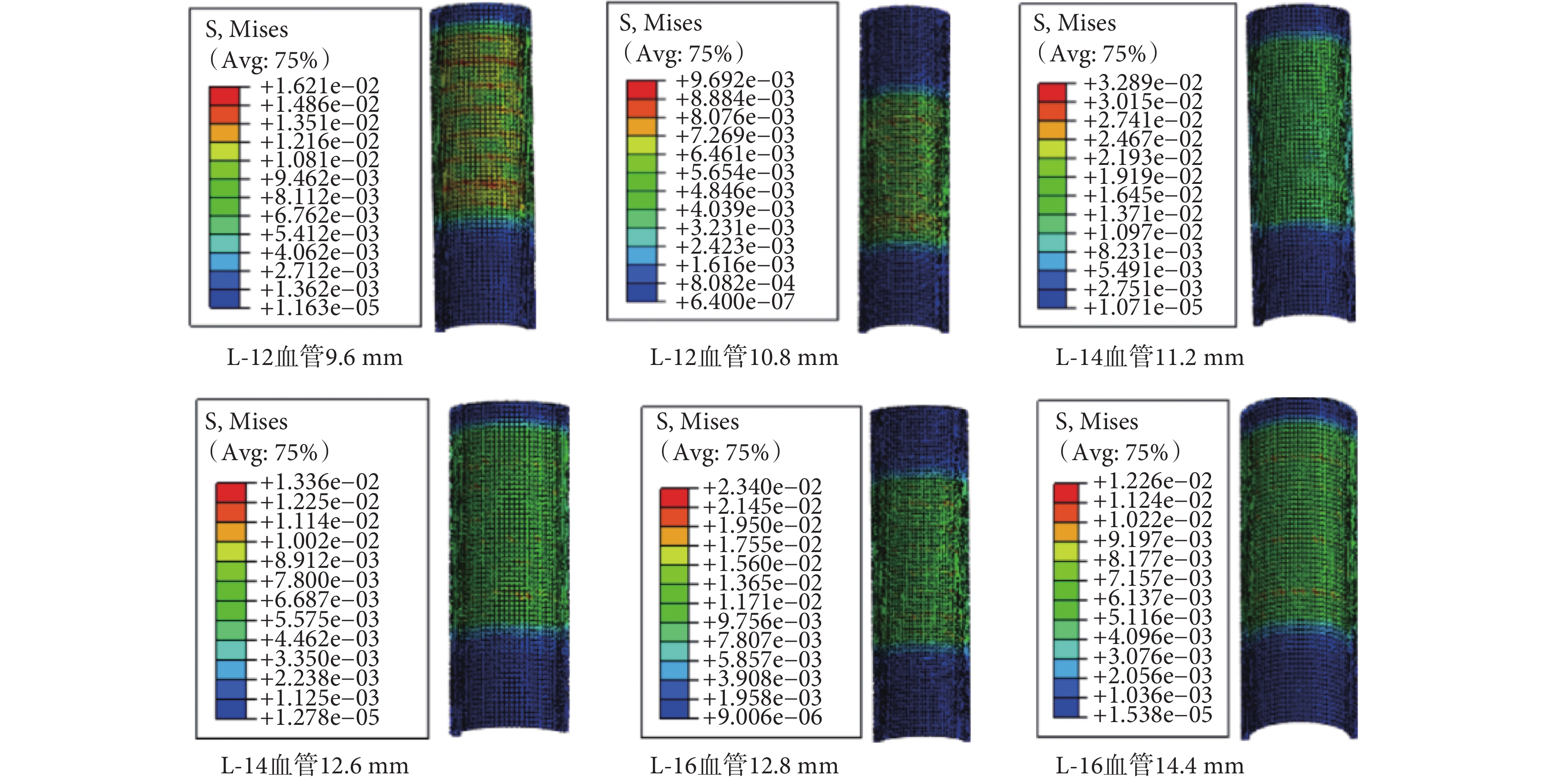 圖4
血管等效應力云圖
Figure4.
Equivalent stress of vessel
圖4
血管等效應力云圖
Figure4.
Equivalent stress of vessel
2.3 支架疲勞強度
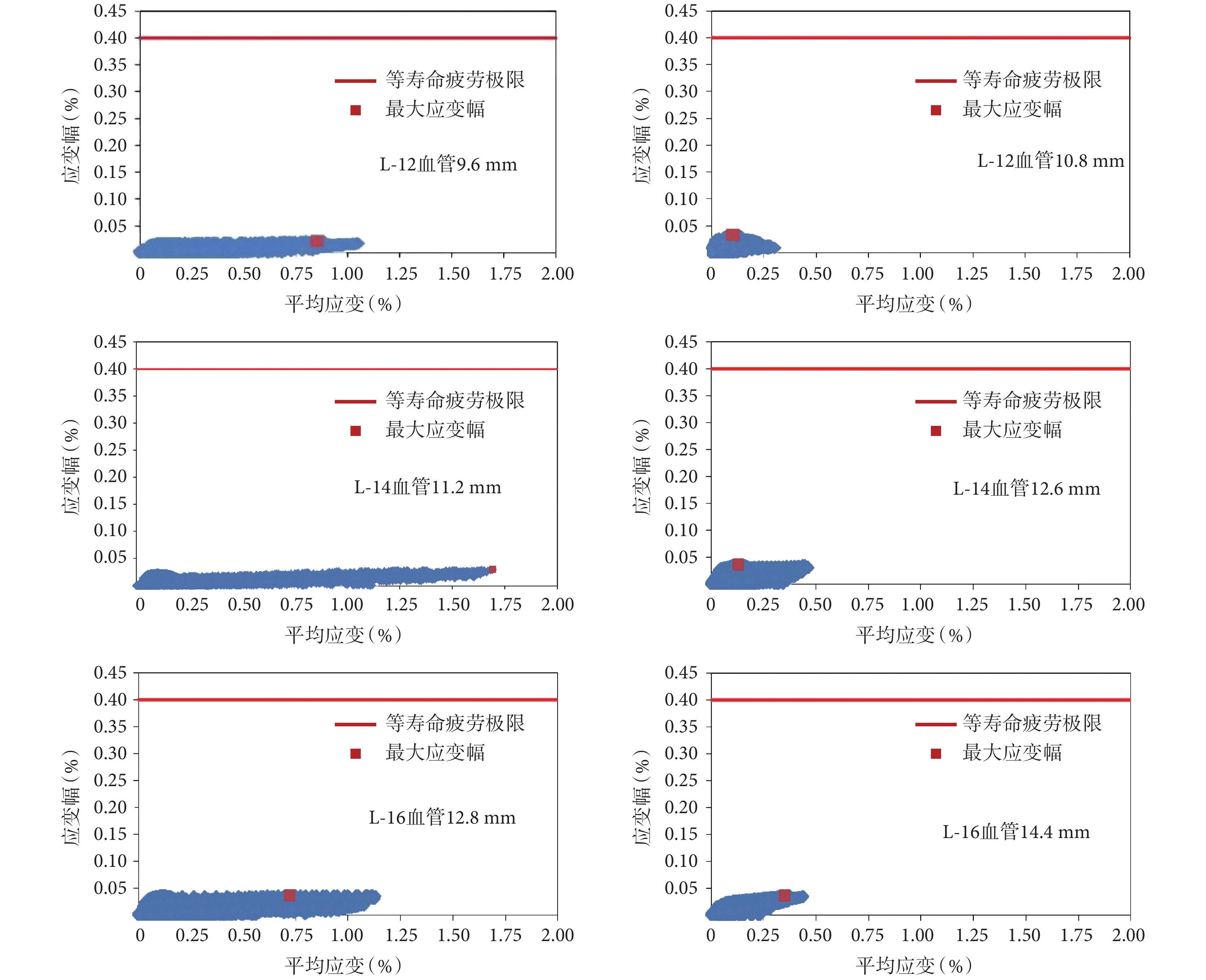
圖 5 是三款支架 L-12、L-14、L-16 在不同釋放尺度(80% 和 90%)下的疲勞極限應變線圖。其中,紅色直線段表示鎳鈦合金支架滿足 10 年壽命的疲勞極限,紅點表示支架在動態加載過程中的最大應變幅。支架所有節點均處于疲勞極限下方,說明均滿足 10 年疲勞壽命的要求。表 2 為三款支架在不同釋放尺度下的力學性能和安全系數計算結果。從支架在不同釋放尺度下的極限應變線圖中可以看出,支架的安全系數均大于 1,說明三款支架結構設計是安全的,滿足強度條件和 10 年疲勞壽命的要求,并且隨著釋放尺度的增大,支架安全系數呈現增大的趨勢。通過對比分析后發現,支架 L-16 在 12.8 mm 血管中釋放時安全性相對較好,而支架 L-12 在 10.8 mm 血管中釋放時安全性相對較差。
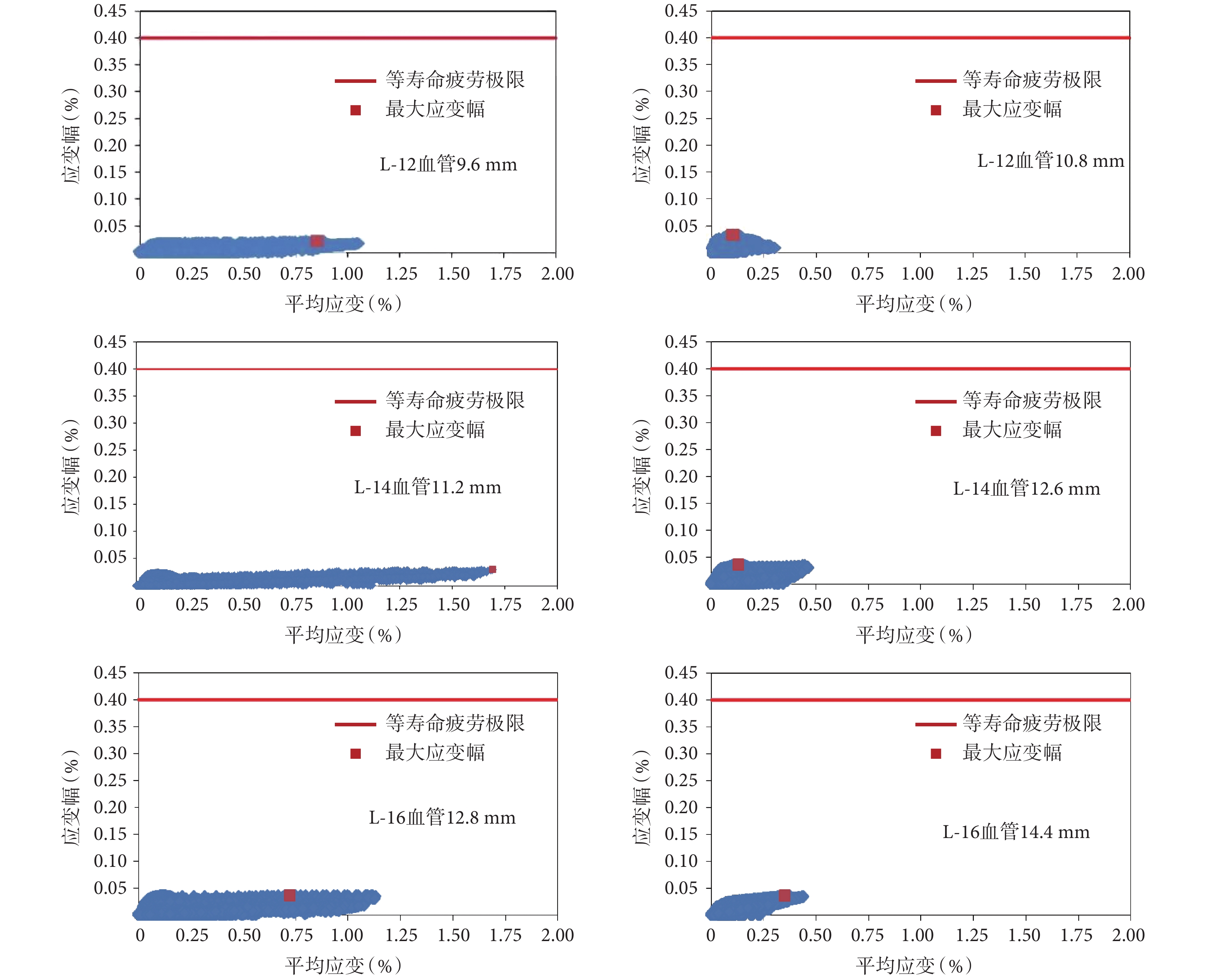 圖5
支架疲勞強度的極限應變線圖
Figure5.
Ultimate strain line diagram of stent fatigue strength
圖5
支架疲勞強度的極限應變線圖
Figure5.
Ultimate strain line diagram of stent fatigue strength
3 動物實驗與討論
3.1 動物實驗
實驗用白豬[生產商:上海甲干生物科技有限公司,生產許可證:SCXK(滬)2015-0005],雌雄不限,體重在 45~65 kg。令實驗豬麻醉后仰臥于手術床并插管,行彩色多普勒超聲檢測雙側髂靜脈及下腔靜脈,在下腹部第一至第三乳頭之間做豎行正中切口,顯露腹主動脈、下腔靜脈下段及左側髂動靜脈,分別用絲線懸吊左髂動脈及左髂靜脈,用慕絲線纏繞左髂靜脈近心端一周,以游標卡尺測量慕絲線,即左髂靜脈周長,根據左髂靜脈周長計算出左髂靜脈直徑及髂靜脈橫截面面積,計算髂靜脈 50% 狹窄的直徑數值,于左髂靜脈匯入下腔靜脈 1~2 cm 及 3~5 cm 處,將 4-0 強生可吸收線雙重纏繞髂靜脈建立狹窄模型[19]。
實驗豬在建立髂靜脈狹窄模型手術后第 30 天,植入該新型髂靜脈支架,觀察支架植入靶血管后的血管順應性、徑向支撐力、支架移位、管腔通暢率、支架內血栓形成、靶血管的炎癥反應及支架內內膜增生等相關指標,綜合評價所研發的髂靜脈支架的安全性和有效性,為后續產品的型式檢驗及臨床試驗提供實驗數據。實驗方案由蘇州大學附屬第二醫院血管外科審核批準,在每只豬的左髂靜脈植入實驗組支架。根據彩色多普勒超聲測量髂靜脈直徑并明確髂靜脈位置,以確保所用支架直徑與所選靜脈參考直徑相一致的比率,支架釋放比率 80%~90% 的血管段為靶血管段。支架植入后再次行數字減影血管造影確認植入成功。
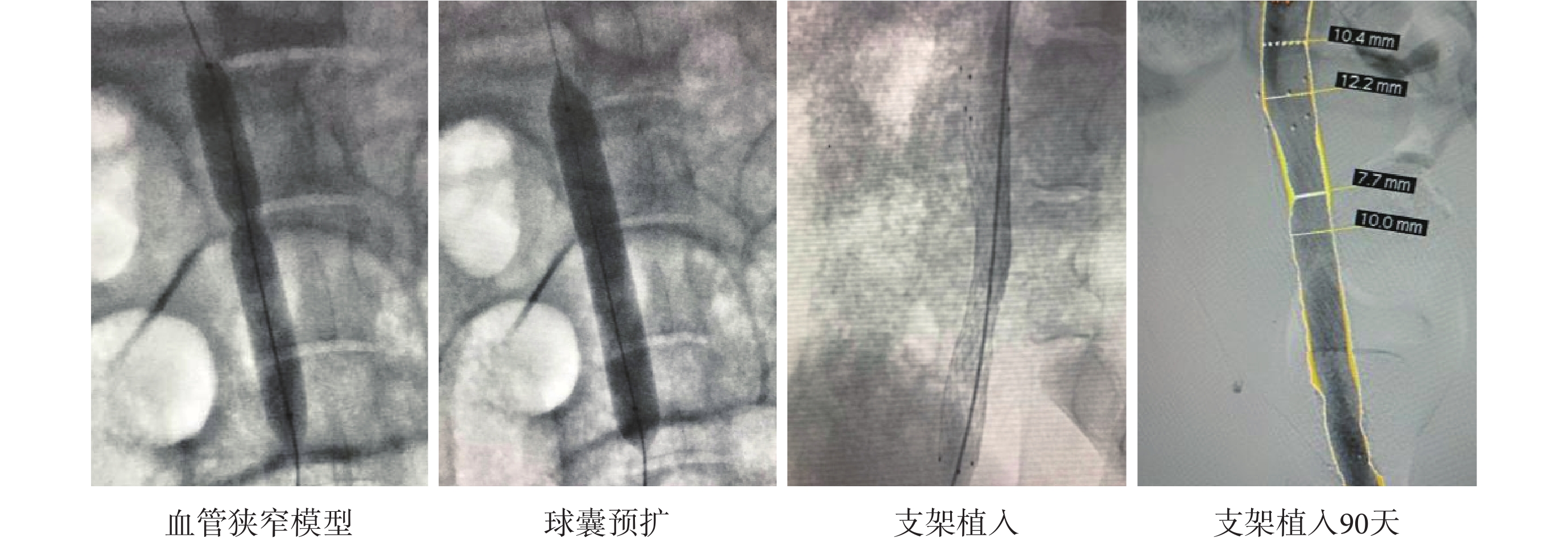
實驗動物在術后 14、30、60 和 90 天復查靜脈造影,主要考察:支架管腔丟失值 = 植入即刻支架管腔直徑 ? 復查時支架管腔直徑;支架管腔丟失率 = 支架管腔丟失值/植入即刻支架管腔直徑。動物實驗不同階段的造影圖片如圖 6 所示。術后對實驗動物進行解剖分析,支架未出現移位、斷裂、裂紋,支撐力良好,血管順應性良好,支架內均未出現再狹窄、血栓形成、靶血管的炎癥反應及內膜增生等現象。結果表明:髂靜脈血管植入支架無裂紋或斷裂等現象,支架結構是安全的,而且未顯著增加手術期并發癥的發生。支架植入后隨訪顯示支架在 90 天隨訪期中并無再狹窄和血栓形成,且支架通暢率均為 100%。動物實驗中所有支架釋放均達到要求,未使用球囊導管行術后再擴張;手術前實驗豬髂靜脈直徑為(8.76 ± 1.29)mm,支架植入術后支架管腔直徑有不同程度的回縮,但均未超過 5%[20](見表 3)。
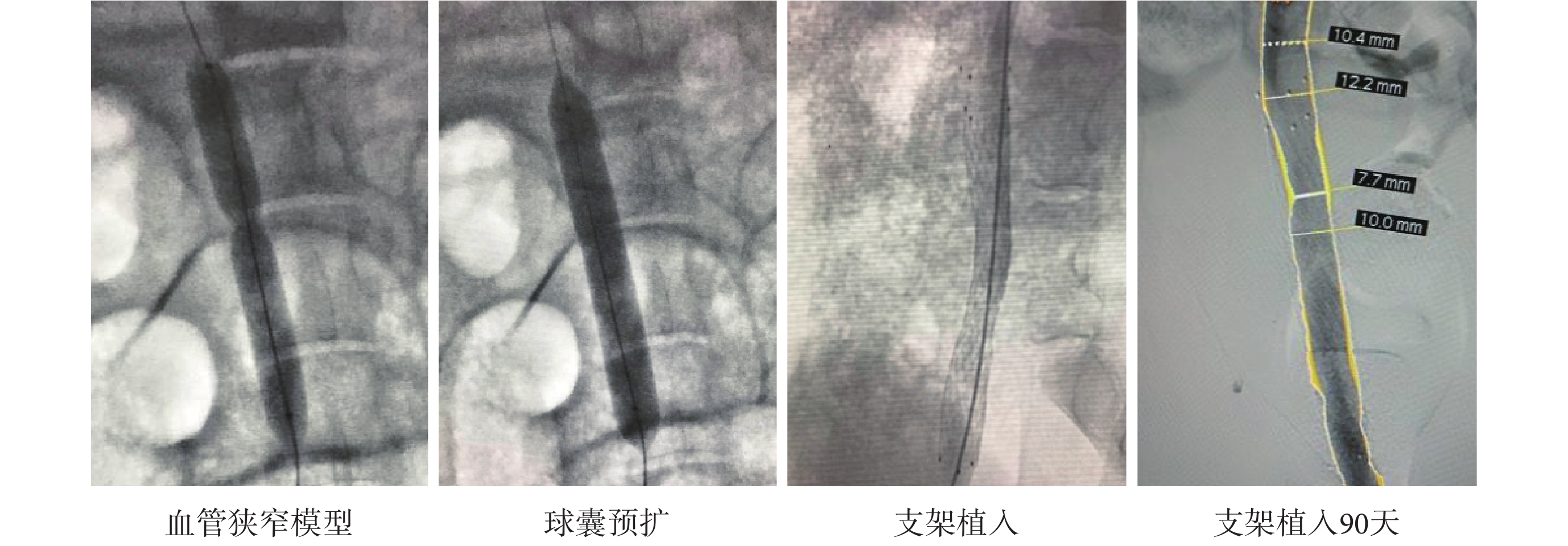 圖6
動物實驗中的髂靜脈造影
Figure6.
Iliac venous angiography in animal test
圖6
動物實驗中的髂靜脈造影
Figure6.
Iliac venous angiography in animal test
3.2 討論
本項目設計的是一款髂靜脈專用支架,系主要用于治療髂靜脈壓迫綜合征的醫療器械。項目組為了適應患者病變部位血管尺寸,設計了三款支架,對比分析在 80%~90% 比例釋放下的力學性能,確認是否達到了設計要求。數值模擬和動物實驗結果顯示,該支架符合不同病變部位的需求,滿足相應的力學性能要求。
支架結構設計方面,主要根據病變部位的特點將支架花冠后面的中央支撐單元的支撐力提高,以更好地解決髂靜脈受壓的問題。獨特的支架結構具有較強的支撐性能和疲勞強度,可以解決髂靜脈受壓后引起的下肢和盆腔靜脈回流障礙性疾病,尤其是可以大大降低血栓發生率。目前該項目完成了結構設計、型式檢驗和動物實驗等工作,正在國內開展臨床試驗研究。
支架前端設計成一定長度和角度的“花冠”狀結構,該結構與主體合為一體切割而成,結構與主體間存在一定銳角,且與主體之間增加了顯影標志。在支架釋放時,“花冠”先行送入下腔靜脈內,可以術中準確定位支架位置,避免較密集網孔的支架主體過多進入下腔靜脈,避免大面積遮蓋對側髂靜脈開口,影響對側髂靜脈血液回流,從而避免不良事件發生。
本研究的不足之處:① 有限元模擬分析時沒有考慮狹窄血管對支架的影響,因此為了真實分析支架的力學性能,有必要建立狹窄血管內支架模型進行評價。② 動物實驗時間較短,一定程度上驗證了支架的安全性,但是實驗不足以證明支架滿足 10 年疲勞壽命的要求,今后需要通過加速疲勞實驗或臨床試驗驗證。③ 動物實驗樣本量較少,需要進行更大量樣本的觀察和統計分析,驗證支架的有效性和可靠性。
4 結論
通過對國產新型鎳鈦合金髂靜脈支架的理論分析和動物實驗發現,釋放尺度對支架的彈性應變、疲勞強度和血管壁等效應力具有一定的影響,為避免或減少血管壁面的損傷、支架內血栓形成以及血管的炎癥反應等,選用合適的支架尺寸和釋放尺度是尤為重要的。動物實驗在一定程度上驗證了該新型髂靜脈支架的有效性和安全性,并驗證了理論分析的正確性和合理性,為臨床試驗與應用提供了重要的參考。
利益沖突聲明:本文全體作者均聲明不存在利益沖突。
引言
髂靜脈壓迫綜合征(iliac venous compression syndrome,IVCS)是指由于髂靜脈受壓和(或)存在腔內異常粘連所引起的下肢和盆腔靜脈回流障礙的疾病,是下肢靜脈瓣膜功能不全和淺靜脈曲張的主要原因之一。在臨床治療中,對病變狹窄大于 50% 以上的 IVCS 患者,均建議進行支架植入手術[1]。然而目前,在臨床上對于髂靜脈病變使用的支架均是專為動脈設計的支架。
用于治療 IVCS 的支架的早期經驗全部是基于波士頓科學公司的 Wallstent 支架。該支架是由不銹鋼絲編織而成的管狀結構,盡管表現好于預期,但是在特定的髂-腔解剖條件下有一定的局限性,大約有 25% 的支架需要糾正支架內再狹窄或支架受壓。近年來,臨床以 Luminexx 支架(Bard 公司,美國)和 Smart control 支架(Cordis 公司,美國)最為常用,兩種支架是由激光雕刻切割形成,膨脹后支架短縮小、柔順性好,易于定位,是目前常用于髂靜脈部位的支架。但是,Luminexx 支架和 Smart control 支架均為動脈專用支架。目前,國內臨床上用于治療 IVCS 的支架也是以動脈支架為主,但是髂靜脈支架植入術的適應證和治療目的與動脈支架有諸多不同。冠狀動脈狹窄是粥樣硬化所致,當狹窄到一定程度就會導致心肌缺血。髂靜脈狹窄是髂靜脈受壓或存在腔內異常粘連結構所引起的下肢和盆腔靜脈回流障礙性疾病,其發病原因與解剖位置有關,右髂總動脈跨越左髂總靜脈的前方,左髂總靜脈處于腰骶椎的生理性前凸和右髂總動脈之間,受前后夾擠形成狹窄。因此,研究一種符合髂靜脈解剖特點的專用支架具有重要的臨床意義和良好的應用前景。
支架植入人體后,在血管脈流的長期作用下,可能會出現支架變形、移位、疲勞斷裂等導致失效。很多報道中顯示,支架植入人體后發生斷裂的現象較為頻繁[2-3]。因此,在血管支架的研發過程中金屬支架的疲勞強度是需要考慮的重要因素之一。在測定鎳鈦合金支架疲勞強度的實驗方面,早期研究人員對鎳鈦合金支架進行了單一方式的疲勞測試[4]。Harrison 等[5]測試了 V 型鎳鈦合金支架的彎曲疲勞行為,結果表明隨著平均應變的增加,應力變化幅度減小,從而疲勞壽命增加。Tolomeo 等[6]對相變溫度點在 28℃ 左右的鎳鈦合金支架進行了拉伸疲勞實驗。近幾年,Marrey[7]利用美國 Bose 公司研制的加速疲勞試驗機,模擬支架在血管內的工作狀態,驗證了支架 10 年疲勞壽命。在國內,趙振心等[8]對鎳鈦合金血管支架進行有限元分析和疲勞性能測試,評價了鎳鈦合金支架的疲勞強度。李建軍等[9]利用疲勞圖譜研究不同圓弧段尺寸對鎳鈦合金支架疲勞特性的影響,發現鎳鈦合金支架的疲勞性能與圓弧段尺寸密切相關。易沛林[10]利用有限元技術模擬分析了兩種不同支架結構的軸向力學性能和疲勞性能,得出有限元分析技術可以方便地對鎳鈦合金支架及其作用的生理環境進行模擬。
本文主要研究了自主研發的三款鎳鈦合金髂靜脈支架在不同釋放尺度下的力學性能和動物實驗。通過繪制支架疲勞極限應變線圖以及計算出支架動態安全系數,總結出不同釋放尺度對鎳鈦合金髂靜脈支架疲勞強度的影響,并結合動物實驗驗證了其安全性和有效性,為鎳鈦合金髂靜脈支架的研發和臨床應用提供科學的參考依據。
1 材料與方法
1.1 材料模型
材料模型采用 ABAQUS 軟件中專用的超彈性材料模塊,根據該模塊設置鎳鈦合金應力—應變關系。支架材料的應力—應變關系是通過對鎳鈦合金試件進行拉伸卸載實驗后得到的。實驗設備為日本 SHIMADZU 制 DSS-500 數字式萬能拉壓實驗機。應變信號采集器為日本 KYOWA 電工的 DBU-120 型信號采集器。載荷使用日本 KYOWA 電工的 PCD-300B 型傳感器以 100 Hz 的頻率進行數據采集。試件使用與支架成分相同且經過相同熱處理的直徑 0.5 mm、長度 100 mm 的 NiTi 合金絲材。實驗測試速度為 12.7 mm/min,環境溫度為 25 oC。先進行定量的壓縮后再進行拉伸試驗,每組樣品測試 3 次。分析時取其平均值作為材料力學性能參數,得到支架模擬的材料屬性。測試的 NiTi 合金絲的彈性模量 E = 80 GPa,泊松比 0.3,抗拉強度 1 290 MPa,屈服強度 390~610 MPa,延伸率 0.147。實驗結果為公稱應力應變值,考慮到材料在實際拉伸過程中的形變,通過公式(1)和(2)得到材料真實應力應變值:
 |
 |
式中, 、
、 為公稱應力與應變;
為公稱應力與應變; 、
、 為材料的真實應力與應變。將材料的真實應力應變輸入到 ABAQUS 中作為支架材料的力學性能參數。
為材料的真實應力與應變。將材料的真實應力應變輸入到 ABAQUS 中作為支架材料的力學性能參數。
1.2 支架模型
該新型髂靜脈支架主要通過獨特的結構設計治療髂靜脈受壓后引起的下肢和盆腔靜脈回流障礙性疾病,可大大降低血栓發生率。支架的前端設計成較疏的花冠,支架網孔小,提高了髂靜脈支架的遠期通暢率;支架的花冠部分與網孔較小的中央支撐單元連接處設置顯影標記,提高支架的定位及釋放的準確性;同時,通過降低支架的末端支撐單元的支撐力,減少支架對靜脈壁的傷害,可以完全滿足臨床使用要求。支架筋寬為 0.16 mm,壁厚 0.22 mm,花冠開口與軸線相夾 20°,并在花冠與中部、末端各有 3 個顯影標記。支架直徑分別為 12、14、16 mm,長度均為 26 mm,以下稱為支架 L-12、L-14 和 L-16。目前在支架結構設計方面已獲得發明專利 3 項[11-13]。
圖 1 為支架、壓握殼和血管導入到 ABAQUS 分析軟件后的系統模型,其中 1、2、3 分別為支架、壓握殼和血管模型。在構造仿真模型時,在有限元軟件 ABAQUS 中通過移動(move)、旋轉(rotate)等功能,使三個模型合理裝配在一起。建立壓握殼時,使其直徑大于支架外徑,確保裝配時壓握殼與支架不接觸。壓握殼和血管應有足夠的長度,保證支架內外圓柱表面上均勻受壓。即在支架大變形過程中,壓握殼和支架(支架被壓握至 3 mm 時),以及支架和血管(支架釋放至血管內時)能實現充分接觸。有限元分析過程中,在圓柱坐標系中先通過壓握殼的徑向位移壓握支架至 3 mm,再分別以不同的釋放尺度(80% 和 90%)使支架釋放至血管內,最后分別對支架和血管內表面施加循環載荷評價支架的疲勞強度。文中結合有關文獻報道設置壓握殼與血管壁為超彈性材料,壓握殼彈性模量為 300 MPa,血管壁彈性模量為 1.75 MPa,泊松比均為 0.499[14-15]。
 圖1
支架系統模型示意圖
Figure1.
Figure of stent system
圖1
支架系統模型示意圖
Figure1.
Figure of stent system
1.3 載荷定義
支架植入髂靜脈后,受到脈流周期性疲勞載荷作用,分析時通過對支架外表面施加交替變化的作用力來進行模擬。首先在 ABAQUS 分析軟件里建立壓握殼、血管、支架的有限元模型,通過壓握殼的徑向位移使支架壓握至 3 mm,再釋放到不同直徑的血管內。其次對血管和支架施加周期循環載荷模擬人體血管內的脈流循環載荷,即疲勞強度的分析是在支架釋放后進行的。支架承受循環變載荷時應以具有 10 年疲勞壽命為前提。髂靜脈血壓值在 3~9 mm Hg,對應壓力值為 0.000 4~0.001 2 MPa。在有限元計算中為了分析結果的準確性和科學性,模擬的周期加載過程重復多次進行。
1.4 評價指標
髂靜脈支架疲勞強度的評價準則是根據 Pelton 等[16]提出的針對鎳鈦合金材料的疲勞強度評價方法。有限元模型計算結束后,首先從結果文件 odb 中導出支架在動態加載過程中所有節點的最大和最小彈性應變,并且在 EXCEL 表格中分別應用公式(3)和(4)計算支架所有節點的平均應變和應變幅。最后為了對比分析支架在不同釋放尺度下的安全性能,本文分別以公式(5)計算出支架安全系數(SFdynamic)[5]。支架疲勞強度的安全系數計算方法如下:
 |
 |
 |
式中,SFdynamic 為疲勞強度的安全系數,δuts 為延伸率,δε 為疲勞極限,δmax 和 δmin 分別為脈動循環載荷的最大和最小彈性應變,δmean 和 δalt 分別為支架在脈動載荷下的平均應變和應變幅。
1.5 有限元模型
本文應用 ABAQUS 有限元軟件的 Explicit 求解模塊對支架系統進行顯示動態分析,該求解方法可以有效地模擬大變形非線性等問題[17]。髂靜脈支架的植入過程涉及壓握殼、血管與支架之間的非線性耦合作用。利用廣義變分原理和懲罰函數法,以不可侵徹性條件作為接觸問題的動力學及運動學約束條件,建立髂靜脈支架介入耦合系統計算模型的等效形式[18],表示為:
 |
式中,δpc 為接觸問題的總虛功,δ 為變分算子,σji 為柯西應力張量,bi、 分別為體力和面力,vi、
分別為體力和面力,vi、 分別為質點的速度和加速度,ρ 是材料密度,γN、γT 分別為接觸界面的相互侵徹率與相對切向速度,tT 是接觸界面切向面力,P 為接觸界面法相壓力,表示為:
分別為質點的速度和加速度,ρ 是材料密度,γN、γT 分別為接觸界面的相互侵徹率與相對切向速度,tT 是接觸界面切向面力,P 為接觸界面法相壓力,表示為:
 |
式中,β1、β2 為罰參數, 為 Heaviside 分布函數,gN 為接觸界面相互侵徹量,可表示為最近點映射形式:
為 Heaviside 分布函數,gN 為接觸界面相互侵徹量,可表示為最近點映射形式:
 |
式中, 、
、 分別代表主控體 A 與從屬體 B 接觸界面質點的歐拉坐標,?、
分別代表主控體 A 與從屬體 B 接觸界面質點的歐拉坐標,?、 表示相應接觸界面的曲面坐標,t 表示時間。由此,利用非線性有限元方法,建立方程(6)的 Lagrangian 離散格式,通過 Newton-Raphson 隱式迭代格式來求解支架被壓握和釋放過程的有限元方程。
表示相應接觸界面的曲面坐標,t 表示時間。由此,利用非線性有限元方法,建立方程(6)的 Lagrangian 離散格式,通過 Newton-Raphson 隱式迭代格式來求解支架被壓握和釋放過程的有限元方程。
2 有限元分析結果
2.1 支架力學性能
三款支架分別從 12、14、16 mm 壓握至 3 mm 時的彈性應變云圖如圖 2 所示。圖 3 為三款支架在不同釋放尺度(80% 和 90%)下的彈性應變云圖。結果顯示:支架被壓握和釋放時最大應變都發生在支撐體和圓弧段相交區域的內外兩側,并小于材料延伸率 15%。當壓握至 3 mm 時三款支架的應變相差不大,都在 9.8%~14.5%,其中支架 L-14 的應變最大,支架 L-16 次之,支架 L-12 最小;隨著釋放尺度的增大,支架彈性應變呈現遞減的趨勢。如表 1 所示,三款支架 L-12、L-14、L-16 的應變遞減率分別為 45%、52%、48%,其中支架 L-14 最大,支架 L-16 次之,支架 L-12 最小。
 圖2
支架壓握至 DVessel = 3 mm 時的彈性應變云圖
Figure2.
Equivalent transformation strain of the stents at the end of crimping DVessel = 3.0 mm
圖2
支架壓握至 DVessel = 3 mm 時的彈性應變云圖
Figure2.
Equivalent transformation strain of the stents at the end of crimping DVessel = 3.0 mm
 圖3
支架彈性應變云圖
Figure3.
Equivalent transformation strain of the stents
圖3
支架彈性應變云圖
Figure3.
Equivalent transformation strain of the stents
2.2 血管力學性能
圖 4 為三款支架在不同釋放尺度(80% 和 90%)下對應的血管等效應力云圖。結果顯示,在血管內壁與支架支撐體接觸處有局部的應力集中現象,并隨著支架釋放尺度的增大,血管等效應力呈現減小的趨勢。如表 1 所示,三款支架 L-12、L-14、L-16 對應的血管等效應力遞減率分別為 44%、60%、48%,其中支架 L-14 對應的血管等效應力遞減率最大,支架 L-16 次之,支架 L-12 最小。
 圖4
血管等效應力云圖
Figure4.
Equivalent stress of vessel
圖4
血管等效應力云圖
Figure4.
Equivalent stress of vessel
2.3 支架疲勞強度
圖 5 是三款支架 L-12、L-14、L-16 在不同釋放尺度(80% 和 90%)下的疲勞極限應變線圖。其中,紅色直線段表示鎳鈦合金支架滿足 10 年壽命的疲勞極限,紅點表示支架在動態加載過程中的最大應變幅。支架所有節點均處于疲勞極限下方,說明均滿足 10 年疲勞壽命的要求。表 2 為三款支架在不同釋放尺度下的力學性能和安全系數計算結果。從支架在不同釋放尺度下的極限應變線圖中可以看出,支架的安全系數均大于 1,說明三款支架結構設計是安全的,滿足強度條件和 10 年疲勞壽命的要求,并且隨著釋放尺度的增大,支架安全系數呈現增大的趨勢。通過對比分析后發現,支架 L-16 在 12.8 mm 血管中釋放時安全性相對較好,而支架 L-12 在 10.8 mm 血管中釋放時安全性相對較差。
 圖5
支架疲勞強度的極限應變線圖
Figure5.
Ultimate strain line diagram of stent fatigue strength
圖5
支架疲勞強度的極限應變線圖
Figure5.
Ultimate strain line diagram of stent fatigue strength
3 動物實驗與討論
3.1 動物實驗
實驗用白豬[生產商:上海甲干生物科技有限公司,生產許可證:SCXK(滬)2015-0005],雌雄不限,體重在 45~65 kg。令實驗豬麻醉后仰臥于手術床并插管,行彩色多普勒超聲檢測雙側髂靜脈及下腔靜脈,在下腹部第一至第三乳頭之間做豎行正中切口,顯露腹主動脈、下腔靜脈下段及左側髂動靜脈,分別用絲線懸吊左髂動脈及左髂靜脈,用慕絲線纏繞左髂靜脈近心端一周,以游標卡尺測量慕絲線,即左髂靜脈周長,根據左髂靜脈周長計算出左髂靜脈直徑及髂靜脈橫截面面積,計算髂靜脈 50% 狹窄的直徑數值,于左髂靜脈匯入下腔靜脈 1~2 cm 及 3~5 cm 處,將 4-0 強生可吸收線雙重纏繞髂靜脈建立狹窄模型[19]。
實驗豬在建立髂靜脈狹窄模型手術后第 30 天,植入該新型髂靜脈支架,觀察支架植入靶血管后的血管順應性、徑向支撐力、支架移位、管腔通暢率、支架內血栓形成、靶血管的炎癥反應及支架內內膜增生等相關指標,綜合評價所研發的髂靜脈支架的安全性和有效性,為后續產品的型式檢驗及臨床試驗提供實驗數據。實驗方案由蘇州大學附屬第二醫院血管外科審核批準,在每只豬的左髂靜脈植入實驗組支架。根據彩色多普勒超聲測量髂靜脈直徑并明確髂靜脈位置,以確保所用支架直徑與所選靜脈參考直徑相一致的比率,支架釋放比率 80%~90% 的血管段為靶血管段。支架植入后再次行數字減影血管造影確認植入成功。
實驗動物在術后 14、30、60 和 90 天復查靜脈造影,主要考察:支架管腔丟失值 = 植入即刻支架管腔直徑 ? 復查時支架管腔直徑;支架管腔丟失率 = 支架管腔丟失值/植入即刻支架管腔直徑。動物實驗不同階段的造影圖片如圖 6 所示。術后對實驗動物進行解剖分析,支架未出現移位、斷裂、裂紋,支撐力良好,血管順應性良好,支架內均未出現再狹窄、血栓形成、靶血管的炎癥反應及內膜增生等現象。結果表明:髂靜脈血管植入支架無裂紋或斷裂等現象,支架結構是安全的,而且未顯著增加手術期并發癥的發生。支架植入后隨訪顯示支架在 90 天隨訪期中并無再狹窄和血栓形成,且支架通暢率均為 100%。動物實驗中所有支架釋放均達到要求,未使用球囊導管行術后再擴張;手術前實驗豬髂靜脈直徑為(8.76 ± 1.29)mm,支架植入術后支架管腔直徑有不同程度的回縮,但均未超過 5%[20](見表 3)。
 圖6
動物實驗中的髂靜脈造影
Figure6.
Iliac venous angiography in animal test
圖6
動物實驗中的髂靜脈造影
Figure6.
Iliac venous angiography in animal test
3.2 討論
本項目設計的是一款髂靜脈專用支架,系主要用于治療髂靜脈壓迫綜合征的醫療器械。項目組為了適應患者病變部位血管尺寸,設計了三款支架,對比分析在 80%~90% 比例釋放下的力學性能,確認是否達到了設計要求。數值模擬和動物實驗結果顯示,該支架符合不同病變部位的需求,滿足相應的力學性能要求。
支架結構設計方面,主要根據病變部位的特點將支架花冠后面的中央支撐單元的支撐力提高,以更好地解決髂靜脈受壓的問題。獨特的支架結構具有較強的支撐性能和疲勞強度,可以解決髂靜脈受壓后引起的下肢和盆腔靜脈回流障礙性疾病,尤其是可以大大降低血栓發生率。目前該項目完成了結構設計、型式檢驗和動物實驗等工作,正在國內開展臨床試驗研究。
支架前端設計成一定長度和角度的“花冠”狀結構,該結構與主體合為一體切割而成,結構與主體間存在一定銳角,且與主體之間增加了顯影標志。在支架釋放時,“花冠”先行送入下腔靜脈內,可以術中準確定位支架位置,避免較密集網孔的支架主體過多進入下腔靜脈,避免大面積遮蓋對側髂靜脈開口,影響對側髂靜脈血液回流,從而避免不良事件發生。
本研究的不足之處:① 有限元模擬分析時沒有考慮狹窄血管對支架的影響,因此為了真實分析支架的力學性能,有必要建立狹窄血管內支架模型進行評價。② 動物實驗時間較短,一定程度上驗證了支架的安全性,但是實驗不足以證明支架滿足 10 年疲勞壽命的要求,今后需要通過加速疲勞實驗或臨床試驗驗證。③ 動物實驗樣本量較少,需要進行更大量樣本的觀察和統計分析,驗證支架的有效性和可靠性。
4 結論
通過對國產新型鎳鈦合金髂靜脈支架的理論分析和動物實驗發現,釋放尺度對支架的彈性應變、疲勞強度和血管壁等效應力具有一定的影響,為避免或減少血管壁面的損傷、支架內血栓形成以及血管的炎癥反應等,選用合適的支架尺寸和釋放尺度是尤為重要的。動物實驗在一定程度上驗證了該新型髂靜脈支架的有效性和安全性,并驗證了理論分析的正確性和合理性,為臨床試驗與應用提供了重要的參考。
利益沖突聲明:本文全體作者均聲明不存在利益沖突。