針對適形貼壁支架“適形”和“可行”的矛盾,探究不同平滑設計方案對支架力學行為和貼壁效果的影響。基于三維投影方法,對投影區域用最小二乘法進行擬合(擬合階數1~6分別對應模型1~6),達到對適形貼壁支架平滑的效果。模擬6組支架在斑塊鈣化程度不同的狹窄血管中的壓握、擴張過程,分析了彎曲剛度、支架崎嶇度、面積殘余狹窄率、接觸面積分數和接觸體積分數等指標。結果顯示,彎曲剛度、支架崎嶇度、面積殘余狹窄率、接觸面積分數和接觸體積分數均隨擬合階數的增加呈上升趨勢。其中模型1的接觸面積分數和接觸體積分數最小,未完全鈣化斑塊環境中分別為77.63%和83.49%,完全鈣化斑塊環境中分別為72.86%和82.21%,“適形”性最差;模型5和6的支架崎嶇度的值較為接近,分別為32.15%和32.38%,制造和植入的“可行”性最差;模型2、3、4在兩種斑塊環境中具有相近的面積殘余狹窄率。可見,對投影區域用最小二乘法進行2~4階擬合獲得適形貼壁支架較為合理;其中,在完全鈣化環境中,2階擬合獲得的適形貼壁支架性能更好。
引用本文: 孫浩, 陶克怡, 劉昭, 杜田明, 張艷萍, 劉圣文, 馮繼玲, 喬愛科. 適形貼壁支架的“適形”與“可行”結構設計及其力學分析. 生物醫學工程學雜志, 2024, 41(4): 790-797, 806. doi: 10.7507/1001-5515.202403005 復制
版權信息: ?四川大學華西醫院華西期刊社《生物醫學工程學雜志》版權所有,未經授權不得轉載、改編
0 引言
支架貼壁不良(stent malapposition,SM)是經皮冠狀動脈介入術后常發生的現象[1-2],是指支架植入血管后無法有效地附著在血管壁上,存在顯著分離的情況,從而影響治療的效果[3-4]。SM可能會誘發嚴重的并發癥,如晚期血栓(late stent thrombosis,LST)[5-7]和支架內再狹窄(in-stent restenosis,ISR)[8]。不同的支架結構設計會影響支架與血管內壁的貼合程度,從而影響ISR、LST的發生概率。因此,如何設計支架使之在服役過程中貼壁良好,以保證血管的內皮化和重構能夠很好地覆蓋支架是一個重要問題[9]。現有研究對支架結構的設計大都從提升支架力學性能出發,以提高支架和血管幾何的匹配性[10-13]。然而,對在復雜的血管及斑塊形狀下,如何實現“個性化”支架、改善支架與血管壁的貼合情況鮮有研究。
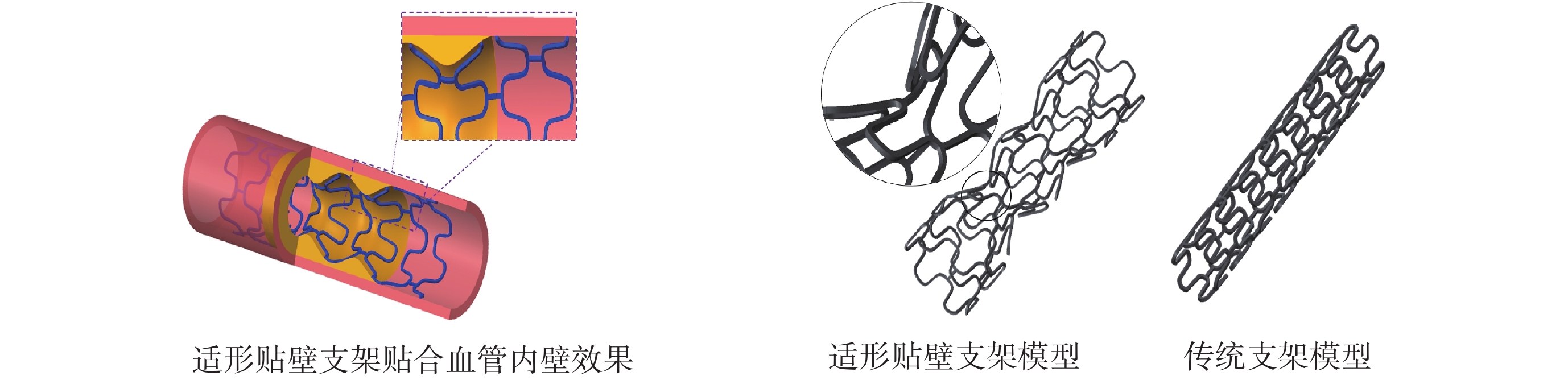
本課題組為了解決支架貼壁不良問題,提出了通過三維投影的方法,可以得到與患者個性化狹窄血管和斑塊形態貼合的適形貼壁支架[4, 14],但是這樣獲得的適形貼壁支架存在著“適形”與“可行”的矛盾。所謂適形就是支架的形狀能適應并貼合血管內壁,貼壁性良好,效果如圖1所示;所謂可行則是易于制造和植入的能力。由于適形貼壁支架相比于傳統的圓筒形支架,形狀更加凹凸不平,直徑不一致,這將使它在激光切割加工時需要厚度更大的工件[15]和更加復雜的制造工藝,影響其制造的可行性,也影響其輸送過程即植入的可行性。所以,不能為了好的貼壁效果即適形性而忽略制造和植入的可行性,而是需要一個折中方案對適形貼壁支架進行合理、適度的平滑處理,兼顧好的貼壁性和支架結構的可行性。
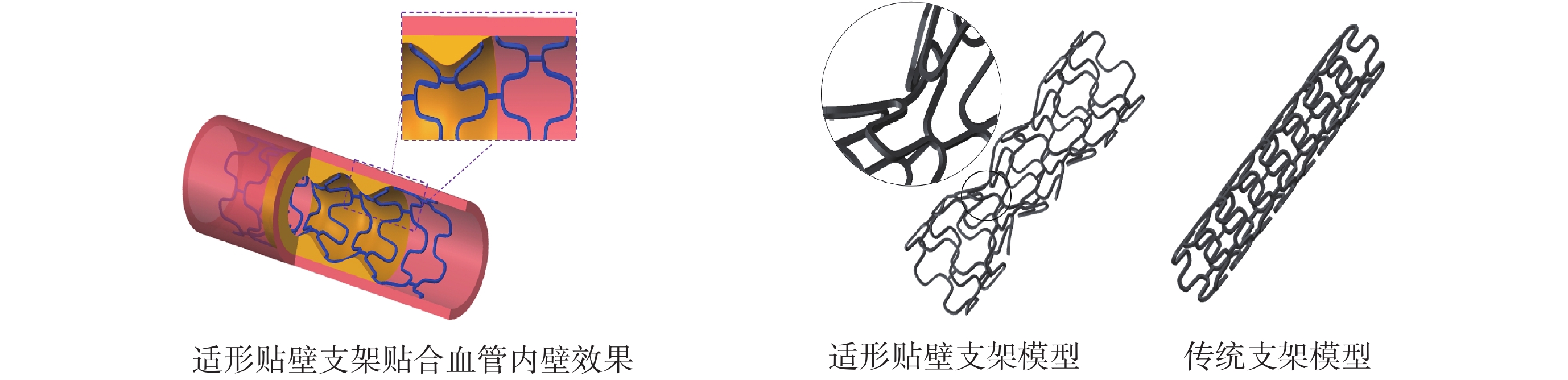 圖1
適形貼壁支架效果圖以及適形貼壁支架與傳統支架結構對比
Figure1.
Schematic of body-fitted stent and structural comparison of body-fitted stent and conventional stent
圖1
適形貼壁支架效果圖以及適形貼壁支架與傳統支架結構對比
Figure1.
Schematic of body-fitted stent and structural comparison of body-fitted stent and conventional stent
1 研究方法
針對適型貼壁支架設計中適形與可行之間的矛盾,本研究解決思路如下:首先構建理想化的狹窄血管模型,通過對適形貼壁支架投影區域進行不同階數的最小二乘法擬合達到對之平滑的效果,然后模擬支架在未完全鈣化和完全鈣化斑塊血管中的壓握、擴張過程,分析相應的評價指標,最終確定合理的平滑方案以兼顧適形和可行的矛盾。
1.1 適形貼壁支架及血管斑塊三維有限元模型的建立
1.1.1 狹窄血管模型構建
使用3D CAD設計軟件SolidWorks 2020(SolidWorks Inc.,美國)構建狹窄血管模型,如圖2所示。將斑塊與血管共軸,采用旋轉的方式建模,壁厚為0.5 mm,最狹窄處直徑為2.4 mm,計算得到狹窄率為49%。為了使支架直徑滿足其在體內輸送的要求,建立理想化圓筒結構的壓握殼,厚度為0.02 mm,直徑和長度根據不同適形貼壁支架進行定義,如圖2所示,采用折疊球囊對支架進行擴張。
 圖2
理想化的冠狀動脈血管-斑塊、壓握殼和球囊模型
Figure2.
Idealized coronary vessel-plaque, crimping shell and balloon models
圖2
理想化的冠狀動脈血管-斑塊、壓握殼和球囊模型
Figure2.
Idealized coronary vessel-plaque, crimping shell and balloon models
1.1.2 適形貼壁支架構建
本文選擇柔順性更好、便于植入的開環支架,采用結構較簡單易于制造的I型連接筋,如圖3所示。使用三維投影的方法構建適形貼壁支架模型,將傳統支架與狹窄血管模型共軸裝配。將支架中心線(三維投影示意圖中綠線)沿管腔徑向投影至狹窄血管內表面上,以投影所得的曲線(三維投影示意圖中貼合狹窄血管內壁的黑線)為掃描路徑,支架支桿的方形截面為掃描輪廓進行掃描,即可獲得完整適形貼壁支架結構。
 圖3
適形貼壁支架三維投影建模方法示意圖
Figure3.
Schematic diagram of the three-dimensional projection modelling method for body-fitted stent
圖3
適形貼壁支架三維投影建模方法示意圖
Figure3.
Schematic diagram of the three-dimensional projection modelling method for body-fitted stent
1.1.3 適形貼壁支架平滑方案的構建
最小二乘法常被用于數據的擬合處理中。本文根據最小二乘法使擬合對象無限接近目標對象的核心思想,將之用于適形貼壁支架的平滑問題,對支架投影區域(包含了斑塊部分和支架兩端覆蓋血管的部分)用最小二乘法多項式擬合。隨著擬合階數的增加,所擬合的效果會越來越接近原始投影區域。不難推測出這樣獲得的適形貼壁支架結構貼壁性即適形性會增加,但其可行性也會降低。所以本文選取將投影區域用1~6階多項式擬合,共得到6組適形貼壁支架結構進行對比,如圖4所示。
 圖4
適形貼壁支架平滑方案
圖4
適形貼壁支架平滑方案
左:支架投影區域和采用最小二乘法擬合達到平滑的效果;右:支架結構,模型1 ~ 6對應最小二乘法擬合階數1 ~ 6
Figure4. Smoothing scheme for body-fitted stentLeft: stent projection area and smoothing achieved by least-squares fitting to the projected region; Right: six groups of stent structures, with models 1 to 6 corresponding to the least squares fitting order from 1 to 6
1.2 材料屬性及網格劃分
選擇生物相容性優良的鈷鉻(CoCr)合金作為支架材料[16],密度為8.5×10-3 g/mm3,楊氏模量為233 GPa,泊松比為0.3,屈服極限為414 MPa,強度極限為933 MPa。球囊則采用熱塑性聚酯材料,楊氏模量為14.5 GPa,泊松比為0.3。此外,設置血管的楊氏模量為1.75 MPa,泊松比為0.3[17]。設計對比實驗,將斑塊設為完全鈣化與未完全鈣化,以探究斑塊鈣化程度對支架力學行為及貼壁效果的影響,實現針對不同病灶的個性化適形貼壁支架平滑方案。如式(1)所示,使用一階Ogden模型描述斑塊的材料屬性[18],具體參數如表1所示。
 |
式中:W是應變能密度函數;αi、μi和Di為材料模型參數;J是彈性體積比;λ是主伸長率。
本研究采用網格劃分軟件HyperMesh 14.0(Altair Engineering,美國)對支架、血管、斑塊、球囊以及壓握殼模型進行網格劃分。為確保高質量的規則網格(雅可比 > 0.7),使用check elems功能進行網格質量檢查,對質量較差的網格進行優化。如圖5所示,支架和斑塊采用4節點線性四面體單元C3D4,血管采用8節點線性減縮積分單元C3D8R。將球囊定義為厚度為0.02 mm的膜材料,并選用了4節點縮減積分膜單元M3D4R。壓握殼采用四節點殼單元S4R。
 圖5
各模型網格劃分示意圖
Figure5.
Schematic diagram of meshing for each model
圖5
各模型網格劃分示意圖
Figure5.
Schematic diagram of meshing for each model
本研究通過加密模型2在完全鈣化環境下的網格,驗證網格獨立性,如表2所示。分析了支架擴張、回彈后支架上的最大von Mises應力的變化。加密后的支架網格與原網格最大von Mises應力值差異約為4.2%,符合網格密度變化導致的解誤差小于5%的合理性標準。因此,采用原網格尺寸對后續組別進行劃分。
1.3 邊界條件及載荷
支架壓握、柔順性分析、擴張-保持-回彈過程的數值模擬,利用有限元分析軟件Abaqus6.14(SIMULIA Inc.,美國)來實現。壓握階段:在壓握殼與支架之間采用硬接觸摩擦,切向摩擦系數為0.2,在壓握殼外表面施加徑向向內的位移將其壓握至1.1 mm,然后對壓握殼施加徑向向外的位移,使支架自由回彈。之后將壓握后的支架模型及其應力狀態作為柔順性分析的初始狀態。在支架兩端建立參考點,并將參考點與支架的6個支撐筋波峰最外側節點之間創建多點約束,約束為梁,之后在支架兩端的參考點上分別施加大小相同、方向相反的彎矩使支架整體發生均勻彎曲。擴張-保持-回彈階段要將壓握變形的支架與狹窄血管、斑塊及球囊進行裝配,將所有接觸的面之間設置為通用接觸,摩擦系數設置為0.2。擴張階段:固定球囊兩端,對球囊內表面施加1.2 MPa的壓力載荷,持續時間為10 ms,由球囊擴張撐開支架,進而支架擠壓斑塊和血管,擴開狹窄的部位。保持階段:保持此時擴張的穩定狀態,持續時間為2 ms。回彈階段:將對球囊內表面的載荷降低為–0.01 MPa,持續時間為3 ms,支架在血管和斑塊徑向向內的作用力下發生一定程度的回彈。
2 評價指標
本文主要分析了三個方面的評價指標,分別對應:① 支架基本功能:壓握損傷性能評估、支架柔順性和面積殘余狹窄率;② 支架適形性能:接觸面積分數和接觸體積分數;③ 支架可行性能:支架崎嶇度。
2.1 支架基本功能測試
2.1.1 壓握損傷性能評估
支架在壓握時需合理受力至塑性應變,確保尺寸縮小以進入狹窄血管,同時避免斷裂,保證后續擴張回彈效果,實現治療目標。
2.1.2 支架柔順性
支架柔順性影響其植入病變部位的順暢度以及與血管的適應性[19],用彎曲剛度(EI)反映,如式(2)所示,二者成倒數關系,低彎曲剛度意味著高柔順性,用以評估支架可植入性。
 |
式中,M為支架兩端施加的彎矩, 為支架的旋轉角度,L為壓握后支架的長度。
為支架的旋轉角度,L為壓握后支架的長度。
2.1.3 面積殘余狹窄率
支架擴張后,在血管和斑塊的彈性回縮力的影響下會發生一定的回彈,表現為術后的殘余狹窄。用面積殘余狹窄率(A)來表征支架對狹窄管腔的支撐性能,如式(3)所示。
 |
式中, 為支架植入后最終狀態的最小管腔橫截面積,
為支架植入后最終狀態的最小管腔橫截面積, 為原狹窄血管中正常管腔部分的橫截面積,二者之差是橫截面內的殘余狹窄面積。
為原狹窄血管中正常管腔部分的橫截面積,二者之差是橫截面內的殘余狹窄面積。
2.2 支架適形性能的評價
接觸面積分數(S)和接觸體積分數(V)反映支架在血管中完全釋放后,支架與血管內壁的接觸關系,從面積和體積兩個角度評價支架的貼壁性即適形性,如式(4)和式(5)所示。
 |
式中, 為支架外表面包絡面積與血管接觸部分的面積,
為支架外表面包絡面積與血管接觸部分的面積, 是支架外表面包絡面積的總表面積,二者之差是支架與血管未接觸的面積。
是支架外表面包絡面積的總表面積,二者之差是支架與血管未接觸的面積。
 |
式中, 為支架植入后的支架模型外表面封閉形成實體的體積,
為支架植入后的支架模型外表面封閉形成實體的體積, 為支架植入后對應的血管管腔空間體積,二者之差是支架與血管之間的空隙體積。
為支架植入后對應的血管管腔空間體積,二者之差是支架與血管之間的空隙體積。
接觸面積分數和接觸體積分數兩者取值都在[0, 1]之間,其值越接近1,說明支架的貼壁越好,適形性能越好。
2.3 支架可行性能的評價
適形貼壁支架相比于傳統的圓筒形支架,其形狀貼合于狹窄血管內表面,直徑不一致,導致相應的結構單元也不一致。支架崎嶇度(U)反映適形貼壁支架直徑之間的差異,用來評價支架的可行性,其值越小說明越容易制造、植入越可行,如式(6)所示。
 |
式中, 為適形貼壁支架的最大直徑,
為適形貼壁支架的最大直徑, 為適形貼壁支架的最小直徑,二者之差是支架的大小直徑落差。
為適形貼壁支架的最小直徑,二者之差是支架的大小直徑落差。
支架崎嶇度取值也在[0, 1]之間,越接近于0,說明適形貼壁支架可行性能越好。
3 結果分析
3.1 支架基本功能分析
3.1.1 支架壓握及柔順性分析
壓握階段,支架受徑向向內的作用力,徑向縮短而軸向伸長,高應力集中于支撐筋拐彎處,引發塑性應變。圖6所示為模型4的壓握過程。支架兩端先接觸壓握殼,變形顯著,影響其適形結構。但各模型應力峰值均未超鈷鉻合金強度極限(933 MPa),支架不會發生斷裂,均適用。
 圖6
模型4支架壓握過程
Figure6.
Crimping process for model 4
圖6
模型4支架壓握過程
Figure6.
Crimping process for model 4
通過式(2)計算得出模型1~6的彎曲剛度如表3所示,可以看出模型1的彎曲剛度最小即柔順性最好,模型6的彎曲剛度最大柔順性最差。結果表明,隨著多項式擬合階數的增加,所獲得適形貼壁支架的柔順性隨之下降。
3.1.2 支架支撐性能分析
支架模擬擴張后,得到各支架回彈的模擬結果,如圖7所示。高應力區域主要在血管狹窄處附近,對于每個支架單元,高應力區域集中在支架的支撐筋轉彎處,6組模型應力變化趨勢基本相同。支架應力峰值均未超過強度極限933 MPa,不會發生斷裂,這表明6組均能適用并對狹窄病變部位起到一定的治療效果。
 圖7
在未完全鈣化斑塊及完全鈣化斑塊模型中的支架回彈后的應力云圖
Figure7.
Stress contour of stents after recoiling in the incompletely calcified plaque and completely calcified plaque models
圖7
在未完全鈣化斑塊及完全鈣化斑塊模型中的支架回彈后的應力云圖
Figure7.
Stress contour of stents after recoiling in the incompletely calcified plaque and completely calcified plaque models
本研究聚焦于臨床醫生最為關注的殘余狹窄率,初始設為49%。如圖8所示,6組適形貼壁支架在未完全鈣化斑塊中面積殘余狹窄率更低,支撐性能表現更佳。因為完全鈣化斑塊硬度大,支架回彈多,支撐減弱。同種斑塊下,擬合階數增加則殘余狹窄率升高,支撐性能下降。因高擬合階數使支架更貼合血管,波環與支撐筋延長,會加劇回彈。故在完全鈣化斑塊中,為保證支撐性能,宜選擇低擬合階數的支架。
 圖8
支架植入后的面積殘余狹窄率
Figure8.
Area residual stenosis ratio after stent implantation
圖8
支架植入后的面積殘余狹窄率
Figure8.
Area residual stenosis ratio after stent implantation
3.2 支架的適形性能分析
3.2.1 接觸面積分數
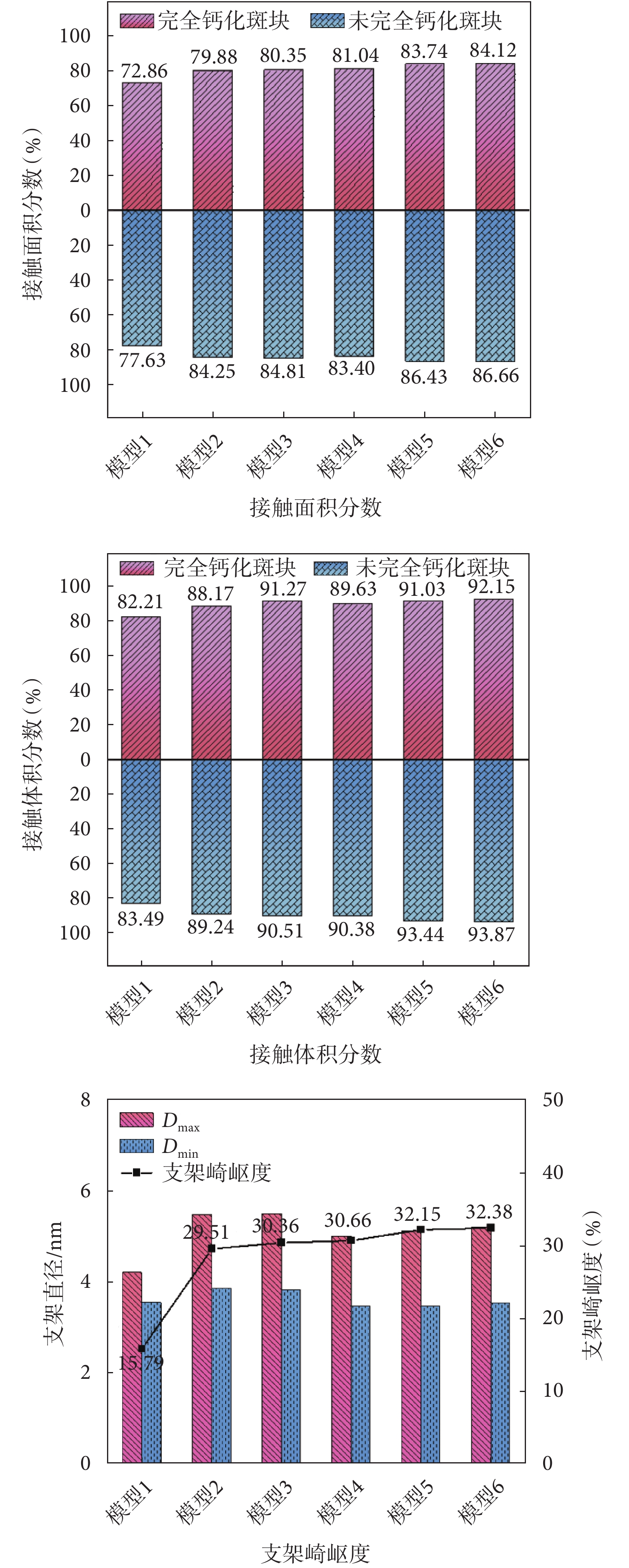
如圖9所示,6組適形貼壁支架的接觸面積分數隨擬合階數增加而升高,適形性增強。模型1接觸面積最小,適形性最差。模型1與2差別最大,在未完全鈣化斑塊環境相差約6.62%,完全鈣化斑塊環境相差約7.02%,因模型1相比其他模型呈錐形,更不適形。
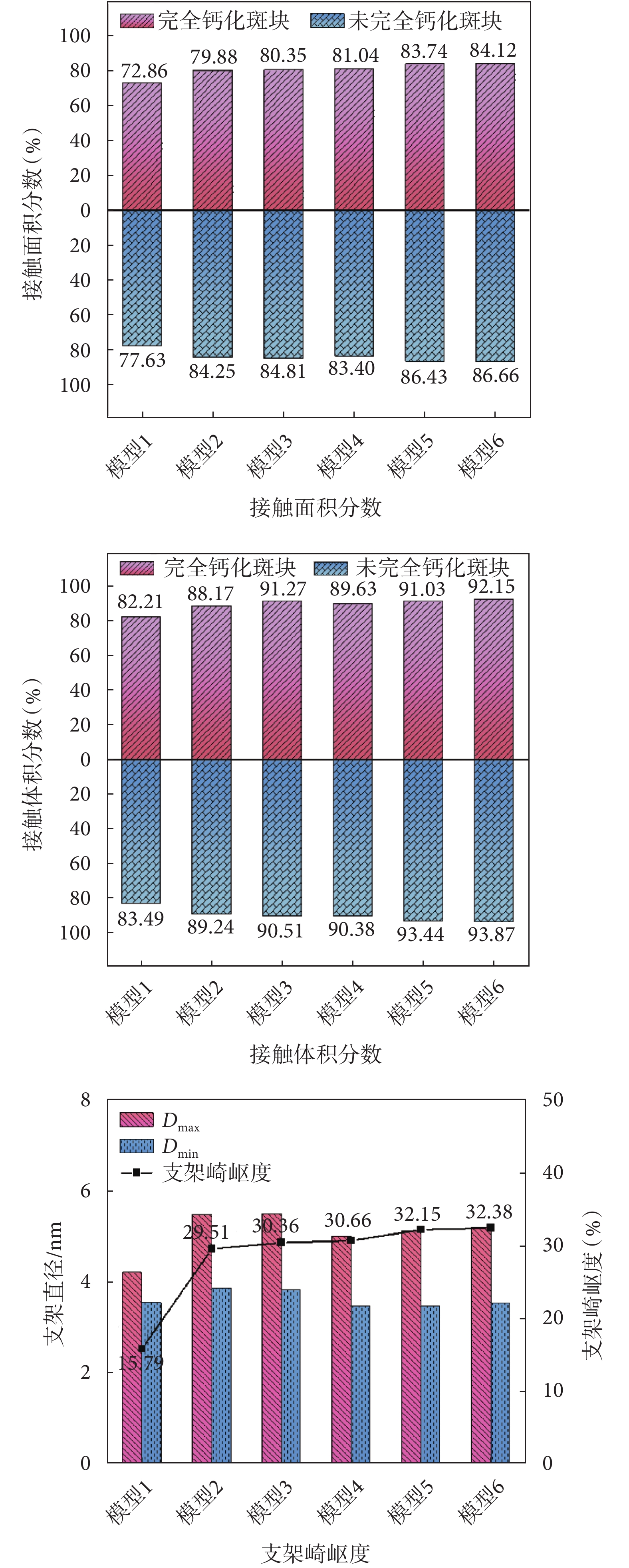 圖9
適形貼壁支架適形和可行相應指標
Figure9.
Corresponding evaluation indices for fitness and feasibility of body-fitted stent
圖9
適形貼壁支架適形和可行相應指標
Figure9.
Corresponding evaluation indices for fitness and feasibility of body-fitted stent
3.2.2 接觸體積分數
如圖9所示,6組適形貼壁支架的接觸體積分數在相同的斑塊環境中,隨著擬合階數的增加,也整體呈上升趨勢,與接觸面積分數展現的結果一致。
3.3 支架的可行性能分析
6組適形貼壁支架崎嶇度的變化如圖9所示。可以看出模型1最大直徑與最小直徑的差別最小,模型5和6的最大直徑與最小直徑差值明顯大于其他模型。模型1~6的支架崎嶇度呈上升趨勢,說明隨著擬合階數的增加,支架的崎嶇度升高,即可行性下降。
4 討論
本文所構建的6組適形貼壁支架在壓握過程中無斷裂失效現象[14],符合預期,與現有支架力學研究相吻合[20-21]。模型1至6的彎曲剛度遞增,顯示柔順性隨擬合階數增加而遞減,可將其連接筋增加圓弧形設計以提升其柔順性[22]。同時,隨著擬合階數的遞增,支撐性能呈現下降趨勢,且在完全鈣化斑塊環境中表現略差,故建議選擇低擬合階數的支架并加粗支桿以提高支撐性能[23]。另外,投影后所得的適形貼壁支架無論是波環還是連接筋都會變長,以達到適形的效果[14]。而這些結構長度增加,支架的徑向回彈率也隨之增大[24]。因此,為提高適形貼壁支架的支撐性能,在投影時可將支架波環結構對應病變最狹窄處。
臨床上基于光學相干斷層掃描技術分析支架管腔面積[25]和支架貼壁不良的體積來評價貼壁效果[26]。本研究引入接觸面積分數與接觸體積分數,從面積和體積兩個維度綜合評價支架貼壁效果即適形性,更加客觀合理。此外,針對適形貼壁支架直徑不一的結構特點,本文提出崎嶇度指標,合理評估其可行性。
本研究是通過對二維投影區域進行最小二乘法擬合來對適形貼壁支架進行平滑處理的,未來可考慮利用患者影像數據進行三維模型構建,以更好地平衡支架的適形性與可行性。同時,為客觀便捷地評估支架適形與可行性能的匹配度,需進一步探討如何將接觸面積分數、接觸體積分數及支架崎嶇度綜合為一個整體評價指標。
本研究采用了理想化的直筒型周向對稱血管-斑塊模型進行模擬分析,但這種方法存在一定局限性,主要體現在未充分考量血管彎曲角度、斑塊不對稱性等因素對適形貼壁支架設計中適形與可行之間矛盾的影響。在以往的適形貼壁支架研究[14, 27]中,已深入探討了支架在彎曲且具有不對稱斑塊血管環境中的力學表現,以及對貼壁不良問題的改善情況。在針對非對稱狹窄血管和具有偏心率的斑塊進行處理時,適形貼壁支架的獲取是將傳統支架折彎至其中心線與狹窄血管的剩余管腔中心線重合后再進行投影。這樣在后續投影時,就能保證垂直于剩余管腔中心線同一截面上的傳統支架到狹窄血管內表面的距離相等,從而保證了所得適形貼壁支架網孔的周向對稱性。本文作為探討支架適形和可行問題的基礎性研究,重點關注了其中最基本的問題,試圖從方法和理念上進行初步的研究和驗證;而考慮復雜個性化的模型將大大增加研究內容的范圍,分散本文焦點。因此,本研究對模型做了簡化。在下一步研究中,可根據患者病變部位血管的具體特征,包括彎曲角度、斑塊的不對稱性、偏心率等幾何參數,以及斑塊的非均勻性、各向異性等物理特性,對病變部位進行科學的分類。基于這些分類,構建幾大類適形貼壁支架的平滑策略,旨在更有效地平衡適形貼壁支架的適形性和可行性之間的矛盾,提升其個性化應用和臨床效用價值。
5 結論
本文構建了6組支架模型,模型1~6分別對應將支架投影區域進行1~6階擬合。在相同的斑塊環境下,支撐性能從模型1~模型6呈下降趨勢。在完全鈣化斑塊環境中,為了得到較好的支撐性能,最好選取擬合階數低的適形貼壁支架。在相同斑塊環境中,從模型1到模型6的貼壁性能基本呈上升趨勢,且支架崎嶇度也呈上升趨勢。模型1的接觸面積分數和接觸體積分數都是最小的,說明其適形最差。從支架崎嶇度的角度來說,模型5和模型6的值遠大于其他模型,這表明其制造和植入的可行性最差。綜上所述,對投影區域用最小二乘法進行2~4階擬合獲得的適形貼壁支架較為合理;另外,在完全鈣化環境里,將投影區域用2階擬合獲得的適形貼壁支架性能更好。
重要聲明
利益沖突聲明:本文全體作者均聲明不存在利益沖突。
作者貢獻聲明:孫浩負責有限元仿真分析和論文撰寫;陶克怡、劉昭主要負責方案設計;杜田明、張艷萍和劉圣文主要負責提供實驗指導和論文審閱修訂;馮繼玲和喬愛科主要負責總體指導和審定論文最終版本。
0 引言
支架貼壁不良(stent malapposition,SM)是經皮冠狀動脈介入術后常發生的現象[1-2],是指支架植入血管后無法有效地附著在血管壁上,存在顯著分離的情況,從而影響治療的效果[3-4]。SM可能會誘發嚴重的并發癥,如晚期血栓(late stent thrombosis,LST)[5-7]和支架內再狹窄(in-stent restenosis,ISR)[8]。不同的支架結構設計會影響支架與血管內壁的貼合程度,從而影響ISR、LST的發生概率。因此,如何設計支架使之在服役過程中貼壁良好,以保證血管的內皮化和重構能夠很好地覆蓋支架是一個重要問題[9]。現有研究對支架結構的設計大都從提升支架力學性能出發,以提高支架和血管幾何的匹配性[10-13]。然而,對在復雜的血管及斑塊形狀下,如何實現“個性化”支架、改善支架與血管壁的貼合情況鮮有研究。
本課題組為了解決支架貼壁不良問題,提出了通過三維投影的方法,可以得到與患者個性化狹窄血管和斑塊形態貼合的適形貼壁支架[4, 14],但是這樣獲得的適形貼壁支架存在著“適形”與“可行”的矛盾。所謂適形就是支架的形狀能適應并貼合血管內壁,貼壁性良好,效果如圖1所示;所謂可行則是易于制造和植入的能力。由于適形貼壁支架相比于傳統的圓筒形支架,形狀更加凹凸不平,直徑不一致,這將使它在激光切割加工時需要厚度更大的工件[15]和更加復雜的制造工藝,影響其制造的可行性,也影響其輸送過程即植入的可行性。所以,不能為了好的貼壁效果即適形性而忽略制造和植入的可行性,而是需要一個折中方案對適形貼壁支架進行合理、適度的平滑處理,兼顧好的貼壁性和支架結構的可行性。
 圖1
適形貼壁支架效果圖以及適形貼壁支架與傳統支架結構對比
Figure1.
Schematic of body-fitted stent and structural comparison of body-fitted stent and conventional stent
圖1
適形貼壁支架效果圖以及適形貼壁支架與傳統支架結構對比
Figure1.
Schematic of body-fitted stent and structural comparison of body-fitted stent and conventional stent
1 研究方法
針對適型貼壁支架設計中適形與可行之間的矛盾,本研究解決思路如下:首先構建理想化的狹窄血管模型,通過對適形貼壁支架投影區域進行不同階數的最小二乘法擬合達到對之平滑的效果,然后模擬支架在未完全鈣化和完全鈣化斑塊血管中的壓握、擴張過程,分析相應的評價指標,最終確定合理的平滑方案以兼顧適形和可行的矛盾。
1.1 適形貼壁支架及血管斑塊三維有限元模型的建立
1.1.1 狹窄血管模型構建
使用3D CAD設計軟件SolidWorks 2020(SolidWorks Inc.,美國)構建狹窄血管模型,如圖2所示。將斑塊與血管共軸,采用旋轉的方式建模,壁厚為0.5 mm,最狹窄處直徑為2.4 mm,計算得到狹窄率為49%。為了使支架直徑滿足其在體內輸送的要求,建立理想化圓筒結構的壓握殼,厚度為0.02 mm,直徑和長度根據不同適形貼壁支架進行定義,如圖2所示,采用折疊球囊對支架進行擴張。
 圖2
理想化的冠狀動脈血管-斑塊、壓握殼和球囊模型
Figure2.
Idealized coronary vessel-plaque, crimping shell and balloon models
圖2
理想化的冠狀動脈血管-斑塊、壓握殼和球囊模型
Figure2.
Idealized coronary vessel-plaque, crimping shell and balloon models
1.1.2 適形貼壁支架構建
本文選擇柔順性更好、便于植入的開環支架,采用結構較簡單易于制造的I型連接筋,如圖3所示。使用三維投影的方法構建適形貼壁支架模型,將傳統支架與狹窄血管模型共軸裝配。將支架中心線(三維投影示意圖中綠線)沿管腔徑向投影至狹窄血管內表面上,以投影所得的曲線(三維投影示意圖中貼合狹窄血管內壁的黑線)為掃描路徑,支架支桿的方形截面為掃描輪廓進行掃描,即可獲得完整適形貼壁支架結構。
 圖3
適形貼壁支架三維投影建模方法示意圖
Figure3.
Schematic diagram of the three-dimensional projection modelling method for body-fitted stent
圖3
適形貼壁支架三維投影建模方法示意圖
Figure3.
Schematic diagram of the three-dimensional projection modelling method for body-fitted stent
1.1.3 適形貼壁支架平滑方案的構建
最小二乘法常被用于數據的擬合處理中。本文根據最小二乘法使擬合對象無限接近目標對象的核心思想,將之用于適形貼壁支架的平滑問題,對支架投影區域(包含了斑塊部分和支架兩端覆蓋血管的部分)用最小二乘法多項式擬合。隨著擬合階數的增加,所擬合的效果會越來越接近原始投影區域。不難推測出這樣獲得的適形貼壁支架結構貼壁性即適形性會增加,但其可行性也會降低。所以本文選取將投影區域用1~6階多項式擬合,共得到6組適形貼壁支架結構進行對比,如圖4所示。
 圖4
適形貼壁支架平滑方案
圖4
適形貼壁支架平滑方案
左:支架投影區域和采用最小二乘法擬合達到平滑的效果;右:支架結構,模型1 ~ 6對應最小二乘法擬合階數1 ~ 6
Figure4. Smoothing scheme for body-fitted stentLeft: stent projection area and smoothing achieved by least-squares fitting to the projected region; Right: six groups of stent structures, with models 1 to 6 corresponding to the least squares fitting order from 1 to 6
1.2 材料屬性及網格劃分
選擇生物相容性優良的鈷鉻(CoCr)合金作為支架材料[16],密度為8.5×10-3 g/mm3,楊氏模量為233 GPa,泊松比為0.3,屈服極限為414 MPa,強度極限為933 MPa。球囊則采用熱塑性聚酯材料,楊氏模量為14.5 GPa,泊松比為0.3。此外,設置血管的楊氏模量為1.75 MPa,泊松比為0.3[17]。設計對比實驗,將斑塊設為完全鈣化與未完全鈣化,以探究斑塊鈣化程度對支架力學行為及貼壁效果的影響,實現針對不同病灶的個性化適形貼壁支架平滑方案。如式(1)所示,使用一階Ogden模型描述斑塊的材料屬性[18],具體參數如表1所示。
 |
式中:W是應變能密度函數;αi、μi和Di為材料模型參數;J是彈性體積比;λ是主伸長率。
本研究采用網格劃分軟件HyperMesh 14.0(Altair Engineering,美國)對支架、血管、斑塊、球囊以及壓握殼模型進行網格劃分。為確保高質量的規則網格(雅可比 > 0.7),使用check elems功能進行網格質量檢查,對質量較差的網格進行優化。如圖5所示,支架和斑塊采用4節點線性四面體單元C3D4,血管采用8節點線性減縮積分單元C3D8R。將球囊定義為厚度為0.02 mm的膜材料,并選用了4節點縮減積分膜單元M3D4R。壓握殼采用四節點殼單元S4R。
 圖5
各模型網格劃分示意圖
Figure5.
Schematic diagram of meshing for each model
圖5
各模型網格劃分示意圖
Figure5.
Schematic diagram of meshing for each model
本研究通過加密模型2在完全鈣化環境下的網格,驗證網格獨立性,如表2所示。分析了支架擴張、回彈后支架上的最大von Mises應力的變化。加密后的支架網格與原網格最大von Mises應力值差異約為4.2%,符合網格密度變化導致的解誤差小于5%的合理性標準。因此,采用原網格尺寸對后續組別進行劃分。
1.3 邊界條件及載荷
支架壓握、柔順性分析、擴張-保持-回彈過程的數值模擬,利用有限元分析軟件Abaqus6.14(SIMULIA Inc.,美國)來實現。壓握階段:在壓握殼與支架之間采用硬接觸摩擦,切向摩擦系數為0.2,在壓握殼外表面施加徑向向內的位移將其壓握至1.1 mm,然后對壓握殼施加徑向向外的位移,使支架自由回彈。之后將壓握后的支架模型及其應力狀態作為柔順性分析的初始狀態。在支架兩端建立參考點,并將參考點與支架的6個支撐筋波峰最外側節點之間創建多點約束,約束為梁,之后在支架兩端的參考點上分別施加大小相同、方向相反的彎矩使支架整體發生均勻彎曲。擴張-保持-回彈階段要將壓握變形的支架與狹窄血管、斑塊及球囊進行裝配,將所有接觸的面之間設置為通用接觸,摩擦系數設置為0.2。擴張階段:固定球囊兩端,對球囊內表面施加1.2 MPa的壓力載荷,持續時間為10 ms,由球囊擴張撐開支架,進而支架擠壓斑塊和血管,擴開狹窄的部位。保持階段:保持此時擴張的穩定狀態,持續時間為2 ms。回彈階段:將對球囊內表面的載荷降低為–0.01 MPa,持續時間為3 ms,支架在血管和斑塊徑向向內的作用力下發生一定程度的回彈。
2 評價指標
本文主要分析了三個方面的評價指標,分別對應:① 支架基本功能:壓握損傷性能評估、支架柔順性和面積殘余狹窄率;② 支架適形性能:接觸面積分數和接觸體積分數;③ 支架可行性能:支架崎嶇度。
2.1 支架基本功能測試
2.1.1 壓握損傷性能評估
支架在壓握時需合理受力至塑性應變,確保尺寸縮小以進入狹窄血管,同時避免斷裂,保證后續擴張回彈效果,實現治療目標。
2.1.2 支架柔順性
支架柔順性影響其植入病變部位的順暢度以及與血管的適應性[19],用彎曲剛度(EI)反映,如式(2)所示,二者成倒數關系,低彎曲剛度意味著高柔順性,用以評估支架可植入性。
 |
式中,M為支架兩端施加的彎矩, 為支架的旋轉角度,L為壓握后支架的長度。
為支架的旋轉角度,L為壓握后支架的長度。
2.1.3 面積殘余狹窄率
支架擴張后,在血管和斑塊的彈性回縮力的影響下會發生一定的回彈,表現為術后的殘余狹窄。用面積殘余狹窄率(A)來表征支架對狹窄管腔的支撐性能,如式(3)所示。
 |
式中, 為支架植入后最終狀態的最小管腔橫截面積,
為支架植入后最終狀態的最小管腔橫截面積, 為原狹窄血管中正常管腔部分的橫截面積,二者之差是橫截面內的殘余狹窄面積。
為原狹窄血管中正常管腔部分的橫截面積,二者之差是橫截面內的殘余狹窄面積。
2.2 支架適形性能的評價
接觸面積分數(S)和接觸體積分數(V)反映支架在血管中完全釋放后,支架與血管內壁的接觸關系,從面積和體積兩個角度評價支架的貼壁性即適形性,如式(4)和式(5)所示。
 |
式中, 為支架外表面包絡面積與血管接觸部分的面積,
為支架外表面包絡面積與血管接觸部分的面積, 是支架外表面包絡面積的總表面積,二者之差是支架與血管未接觸的面積。
是支架外表面包絡面積的總表面積,二者之差是支架與血管未接觸的面積。
 |
式中, 為支架植入后的支架模型外表面封閉形成實體的體積,
為支架植入后的支架模型外表面封閉形成實體的體積, 為支架植入后對應的血管管腔空間體積,二者之差是支架與血管之間的空隙體積。
為支架植入后對應的血管管腔空間體積,二者之差是支架與血管之間的空隙體積。
接觸面積分數和接觸體積分數兩者取值都在[0, 1]之間,其值越接近1,說明支架的貼壁越好,適形性能越好。
2.3 支架可行性能的評價
適形貼壁支架相比于傳統的圓筒形支架,其形狀貼合于狹窄血管內表面,直徑不一致,導致相應的結構單元也不一致。支架崎嶇度(U)反映適形貼壁支架直徑之間的差異,用來評價支架的可行性,其值越小說明越容易制造、植入越可行,如式(6)所示。
 |
式中, 為適形貼壁支架的最大直徑,
為適形貼壁支架的最大直徑, 為適形貼壁支架的最小直徑,二者之差是支架的大小直徑落差。
為適形貼壁支架的最小直徑,二者之差是支架的大小直徑落差。
支架崎嶇度取值也在[0, 1]之間,越接近于0,說明適形貼壁支架可行性能越好。
3 結果分析
3.1 支架基本功能分析
3.1.1 支架壓握及柔順性分析
壓握階段,支架受徑向向內的作用力,徑向縮短而軸向伸長,高應力集中于支撐筋拐彎處,引發塑性應變。圖6所示為模型4的壓握過程。支架兩端先接觸壓握殼,變形顯著,影響其適形結構。但各模型應力峰值均未超鈷鉻合金強度極限(933 MPa),支架不會發生斷裂,均適用。
 圖6
模型4支架壓握過程
Figure6.
Crimping process for model 4
圖6
模型4支架壓握過程
Figure6.
Crimping process for model 4
通過式(2)計算得出模型1~6的彎曲剛度如表3所示,可以看出模型1的彎曲剛度最小即柔順性最好,模型6的彎曲剛度最大柔順性最差。結果表明,隨著多項式擬合階數的增加,所獲得適形貼壁支架的柔順性隨之下降。
3.1.2 支架支撐性能分析
支架模擬擴張后,得到各支架回彈的模擬結果,如圖7所示。高應力區域主要在血管狹窄處附近,對于每個支架單元,高應力區域集中在支架的支撐筋轉彎處,6組模型應力變化趨勢基本相同。支架應力峰值均未超過強度極限933 MPa,不會發生斷裂,這表明6組均能適用并對狹窄病變部位起到一定的治療效果。
 圖7
在未完全鈣化斑塊及完全鈣化斑塊模型中的支架回彈后的應力云圖
Figure7.
Stress contour of stents after recoiling in the incompletely calcified plaque and completely calcified plaque models
圖7
在未完全鈣化斑塊及完全鈣化斑塊模型中的支架回彈后的應力云圖
Figure7.
Stress contour of stents after recoiling in the incompletely calcified plaque and completely calcified plaque models
本研究聚焦于臨床醫生最為關注的殘余狹窄率,初始設為49%。如圖8所示,6組適形貼壁支架在未完全鈣化斑塊中面積殘余狹窄率更低,支撐性能表現更佳。因為完全鈣化斑塊硬度大,支架回彈多,支撐減弱。同種斑塊下,擬合階數增加則殘余狹窄率升高,支撐性能下降。因高擬合階數使支架更貼合血管,波環與支撐筋延長,會加劇回彈。故在完全鈣化斑塊中,為保證支撐性能,宜選擇低擬合階數的支架。
 圖8
支架植入后的面積殘余狹窄率
Figure8.
Area residual stenosis ratio after stent implantation
圖8
支架植入后的面積殘余狹窄率
Figure8.
Area residual stenosis ratio after stent implantation
3.2 支架的適形性能分析
3.2.1 接觸面積分數
如圖9所示,6組適形貼壁支架的接觸面積分數隨擬合階數增加而升高,適形性增強。模型1接觸面積最小,適形性最差。模型1與2差別最大,在未完全鈣化斑塊環境相差約6.62%,完全鈣化斑塊環境相差約7.02%,因模型1相比其他模型呈錐形,更不適形。
 圖9
適形貼壁支架適形和可行相應指標
Figure9.
Corresponding evaluation indices for fitness and feasibility of body-fitted stent
圖9
適形貼壁支架適形和可行相應指標
Figure9.
Corresponding evaluation indices for fitness and feasibility of body-fitted stent
3.2.2 接觸體積分數
如圖9所示,6組適形貼壁支架的接觸體積分數在相同的斑塊環境中,隨著擬合階數的增加,也整體呈上升趨勢,與接觸面積分數展現的結果一致。
3.3 支架的可行性能分析
6組適形貼壁支架崎嶇度的變化如圖9所示。可以看出模型1最大直徑與最小直徑的差別最小,模型5和6的最大直徑與最小直徑差值明顯大于其他模型。模型1~6的支架崎嶇度呈上升趨勢,說明隨著擬合階數的增加,支架的崎嶇度升高,即可行性下降。
4 討論
本文所構建的6組適形貼壁支架在壓握過程中無斷裂失效現象[14],符合預期,與現有支架力學研究相吻合[20-21]。模型1至6的彎曲剛度遞增,顯示柔順性隨擬合階數增加而遞減,可將其連接筋增加圓弧形設計以提升其柔順性[22]。同時,隨著擬合階數的遞增,支撐性能呈現下降趨勢,且在完全鈣化斑塊環境中表現略差,故建議選擇低擬合階數的支架并加粗支桿以提高支撐性能[23]。另外,投影后所得的適形貼壁支架無論是波環還是連接筋都會變長,以達到適形的效果[14]。而這些結構長度增加,支架的徑向回彈率也隨之增大[24]。因此,為提高適形貼壁支架的支撐性能,在投影時可將支架波環結構對應病變最狹窄處。
臨床上基于光學相干斷層掃描技術分析支架管腔面積[25]和支架貼壁不良的體積來評價貼壁效果[26]。本研究引入接觸面積分數與接觸體積分數,從面積和體積兩個維度綜合評價支架貼壁效果即適形性,更加客觀合理。此外,針對適形貼壁支架直徑不一的結構特點,本文提出崎嶇度指標,合理評估其可行性。
本研究是通過對二維投影區域進行最小二乘法擬合來對適形貼壁支架進行平滑處理的,未來可考慮利用患者影像數據進行三維模型構建,以更好地平衡支架的適形性與可行性。同時,為客觀便捷地評估支架適形與可行性能的匹配度,需進一步探討如何將接觸面積分數、接觸體積分數及支架崎嶇度綜合為一個整體評價指標。
本研究采用了理想化的直筒型周向對稱血管-斑塊模型進行模擬分析,但這種方法存在一定局限性,主要體現在未充分考量血管彎曲角度、斑塊不對稱性等因素對適形貼壁支架設計中適形與可行之間矛盾的影響。在以往的適形貼壁支架研究[14, 27]中,已深入探討了支架在彎曲且具有不對稱斑塊血管環境中的力學表現,以及對貼壁不良問題的改善情況。在針對非對稱狹窄血管和具有偏心率的斑塊進行處理時,適形貼壁支架的獲取是將傳統支架折彎至其中心線與狹窄血管的剩余管腔中心線重合后再進行投影。這樣在后續投影時,就能保證垂直于剩余管腔中心線同一截面上的傳統支架到狹窄血管內表面的距離相等,從而保證了所得適形貼壁支架網孔的周向對稱性。本文作為探討支架適形和可行問題的基礎性研究,重點關注了其中最基本的問題,試圖從方法和理念上進行初步的研究和驗證;而考慮復雜個性化的模型將大大增加研究內容的范圍,分散本文焦點。因此,本研究對模型做了簡化。在下一步研究中,可根據患者病變部位血管的具體特征,包括彎曲角度、斑塊的不對稱性、偏心率等幾何參數,以及斑塊的非均勻性、各向異性等物理特性,對病變部位進行科學的分類。基于這些分類,構建幾大類適形貼壁支架的平滑策略,旨在更有效地平衡適形貼壁支架的適形性和可行性之間的矛盾,提升其個性化應用和臨床效用價值。
5 結論
本文構建了6組支架模型,模型1~6分別對應將支架投影區域進行1~6階擬合。在相同的斑塊環境下,支撐性能從模型1~模型6呈下降趨勢。在完全鈣化斑塊環境中,為了得到較好的支撐性能,最好選取擬合階數低的適形貼壁支架。在相同斑塊環境中,從模型1到模型6的貼壁性能基本呈上升趨勢,且支架崎嶇度也呈上升趨勢。模型1的接觸面積分數和接觸體積分數都是最小的,說明其適形最差。從支架崎嶇度的角度來說,模型5和模型6的值遠大于其他模型,這表明其制造和植入的可行性最差。綜上所述,對投影區域用最小二乘法進行2~4階擬合獲得的適形貼壁支架較為合理;另外,在完全鈣化環境里,將投影區域用2階擬合獲得的適形貼壁支架性能更好。
重要聲明
利益沖突聲明:本文全體作者均聲明不存在利益沖突。
作者貢獻聲明:孫浩負責有限元仿真分析和論文撰寫;陶克怡、劉昭主要負責方案設計;杜田明、張艷萍和劉圣文主要負責提供實驗指導和論文審閱修訂;馮繼玲和喬愛科主要負責總體指導和審定論文最終版本。