引用本文: 盧娟, 鄔步云, 邢昌贏, 毛慧娟. 急性腎損傷患者連續性腎臟替代治療中早期液體超負荷變化和死亡的關系. 華西醫學, 2024, 39(7): 1048-1055. doi: 10.7507/1002-0179.202405239 復制
版權信息: ?四川大學華西醫院華西期刊社《華西醫學》版權所有,未經授權不得轉載、改編
急性腎損傷(acute kidney injury, AKI)是入住重癥監護病房(intensive care unit, ICU)患者常見的臨床綜合征,發生率可達 50%~60%[1],與短期死亡風險增加和長期不良預后獨立相關[2-4]。AKI 患者目前管理是通過改善血流動力學,清除潛在腎損傷物質,當合并高鉀血癥、代謝性酸中毒等嚴重并發癥時可應用腎臟替代治療[5]。腎臟替代治療是嚴重 AKI 時治療的主流方式,其中 75% 的 ICU 患者使用連續性腎臟替代治療(continuous renal replacement therapy, CRRT)[1]。相比間斷透析,CRRT 與透析依賴減少相關[6-7],因此 CRRT 被認為是 ICU 中 AKI 患者首選腎臟替代治療模式。CRRT 是一種緩慢連續清除體內溶質和液體的體外血液凈化方式[8]。既往研究表明液體超負荷與 AKI 的發病率、死亡率和腎功能恢復降低獨立相關[9-13]。但作為嚴重 AKI 患者容量管理的主要手段,CRRT 容量管理是維持液體平衡還是積極超濾尚不確定。觀察性分析表明 CRRT 期間的液體負平衡與改善的臨床結局相關[14-16]。但既往研究采用液體平衡作為容量管理評估手段存在一些缺點,包括未校正患者體重,且少有體重標準化的液體平衡變化比例與預后的關系。因此本研究通過回顧性隊列研究分析體重標準化的液體平衡變化與接受 CRRT 的 AKI 患者 28 d 死亡率之間的關系。
1 對象與方法
1.1 研究對象
利用 MIMIC-IV(Medical Information Mart for Intensive Care-IV)數據庫 0.4 版中的數據進行回顧性隊列研究[17]。MIMIC-IV 記錄了 2008 年—2019 年美國 Beth Israel Deaconess 醫療中心 ICU
1.2 資料收集
通過 PostgreSQL(version 12)中的結構化查詢語言從 MIMIC-IV 數據庫中提取每例患者的數據,提取的資料包括人口統計學特征(年齡、性別、種族、身高、入院體重、入院類型和 ICU 類型)、并發癥(高血壓、糖尿病、慢性腎病、慢性心力衰竭、癌癥和查爾森合并癥指數評分)、入院第 1 天的疾病嚴重程度[牛津急性疾病嚴重程度評分(Oxford Acute Sickness Severity Score, OASIS)]、CRRT 前序貫器官衰竭評估(Sequential Organ Failure Assessment, SOFA)評分、CRRT 前血管活性強心藥物評分(Vasoactive-inotropic Score, VIS)、實驗室檢查、生命體征、CRRT 數據(包括 CRRT 設置、超濾數據、液體平衡和從 ICU 入院到 CRRT 的時間間隔)和臨床結果等。
1.3 暴露因素與結局
暴露變量為 CRRT 啟動后 48 h 液體超負荷改變比例(proportion of change of fluid overload, ΔFO%),其定義為體重標準化的液體入量與出量之差。由于潛在的非線性關系,分析時將暴露變量按四分位數分組(按照從小至大分別稱為 Q1、Q2、Q3、Q4 組),死亡風險最低組在分析中用作參考。研究終點為 28 d 死亡率。
1.4 統計學方法
連續性變量采用中位數(下四分位數,上四分位數)表示,4 組間比較采用 Kruskal-Wallis H 秩和檢驗。分類變量采用例數和/或百分比表示,4 組間采用 χ2 檢驗或 Fisher 確切概率法。兩兩比較使用 Bonferroni 校正。本研究未估計樣本量,納入了數據庫中所有符合條件的受試者。由于缺失數據可能會偏離分析結果,本研究使用多重插值法對體質量指數的缺失數據進行處理。
使用廣義可加線性回歸模型分析連續性變量 ΔFO% 與 28 d 死亡率的關系;使用對數秩檢驗分析四分位分組間生存曲線差異,組間比較使用 Benjamini-Hochberg 校正;因不滿足 Cox 模型比例風險假設,故使用單因素和多因素 logistic 回歸分析 ΔFO% 四分位分組與 28 d 死亡率的關系,計算比值比(odds ratio, OR)及 95% 置信區間(confidence interval, CI),多因素模型校正變量包括有臨床意義或單因素分析有統計學意義的人口統計學特征、基礎疾病、入院情況、CRRT 前情況和 CRRT 持續時間。使用 R 4.3.1 軟件進行統計分析。雙側檢驗水準 α=0.05。
2 結果
2.1 一般資料
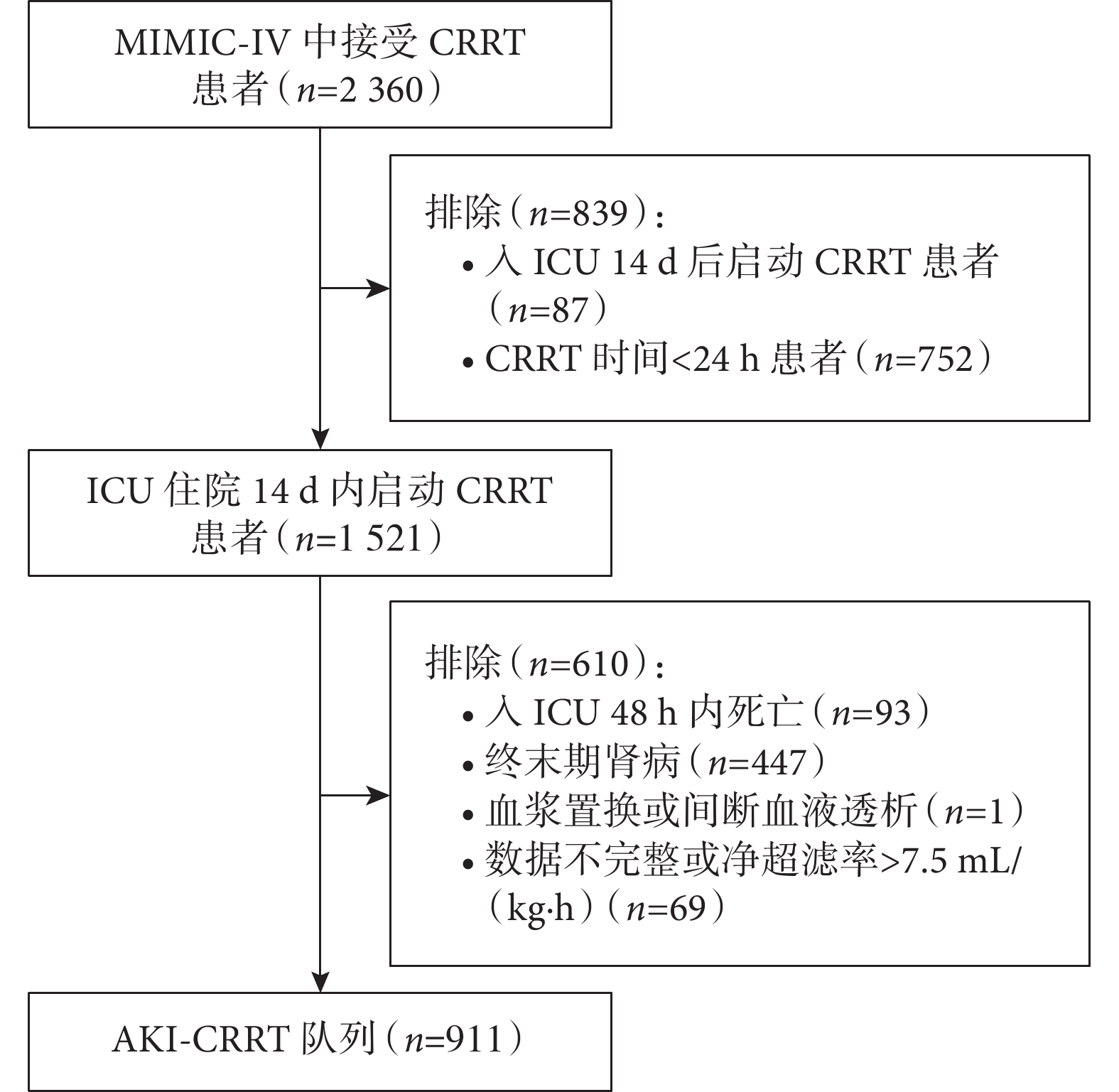
根據納入與排除標準,本研究納入 911 例患者(圖1)。研究人群年齡 63(52,73)歲,男性占 60.0%(547 例);白人 586 例(64.3%),黑人 72 例(7.9%),其他種族 253 例(27.8%);體質量指數 32.2(27.6,37.7) kg/m2;基線肌酐 0.9(0.7,1.1) mg/dL;372 例(40.8%)進行手術,286 例(31.4%)來自心血管 ICU;既往慢性腎臟病 372 例(40.8%),充血性心力衰竭 362 例(39.7%);查爾森合并癥指數評分 3(2,5)分;入院 OASIS 評分 46(38,51)分,VIS 評分 0.8(0,2.4)分,SOFA 評分 13(10,15)分;CRRT 前少尿 498 例(54.7%),膿毒癥 611 例(67.1%),機械通氣 673 例(73.9%),使用血管加壓藥物 605 例(66.4%),使用強心藥物 86 例(9.4%)。
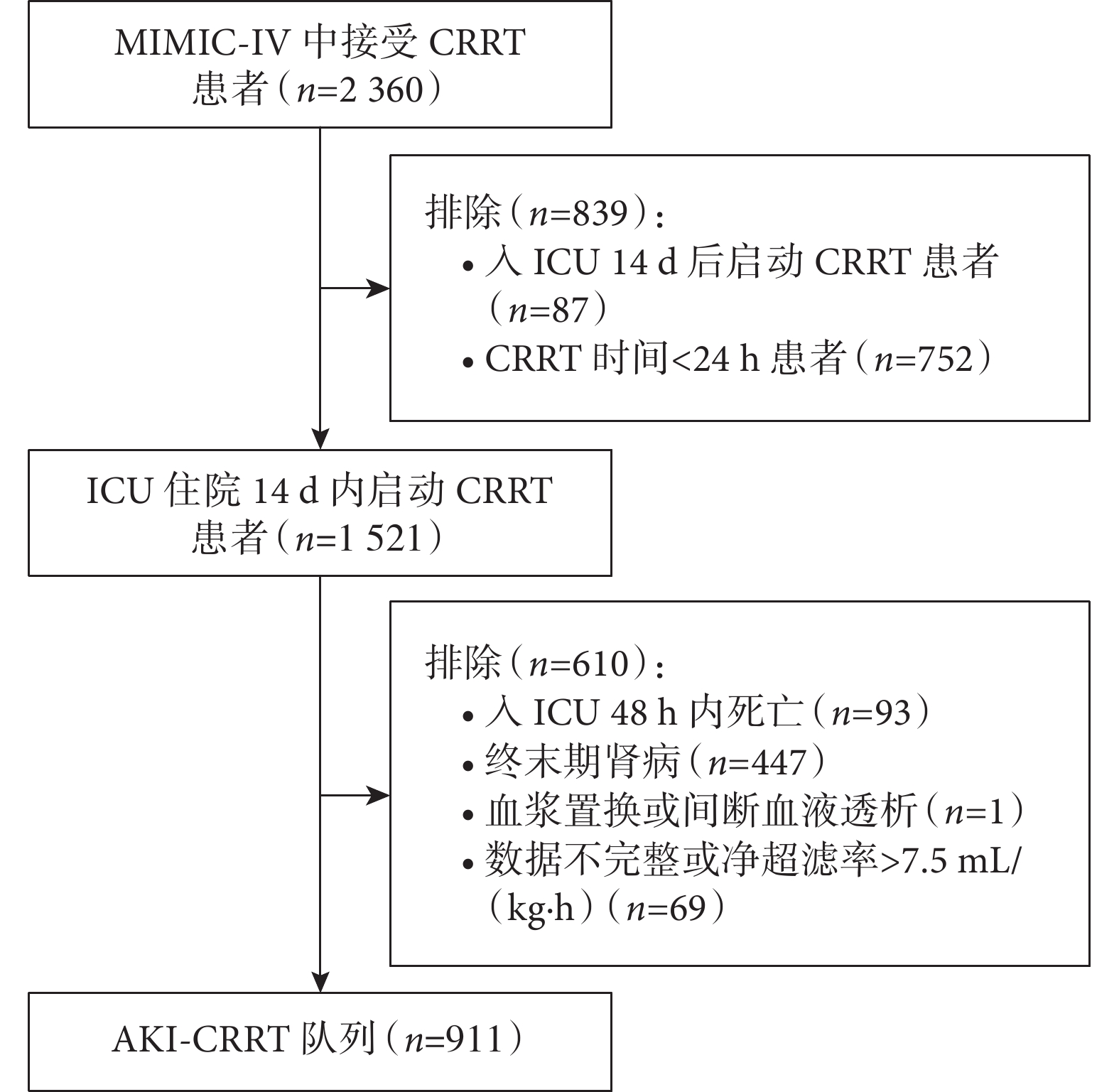 圖1
患者篩選流程圖
圖1
患者篩選流程圖
CRRT:連續性腎臟替代治療;ICU:重癥監護病房;AKI:急性腎損傷
入院到 CRRT 啟動前累計液體負荷比例為 0.07(0.02,0.13)。CRRT 模式中,濾過模式 67 例(7.4%),透析模式 10 例(1.1%),透析濾過模式 826 例(90.7%),單純超濾 8 例(0.9%)。CRRT 劑量為 25.6(21.6,289.0)mL/(kg·h),CRRT 抗凝方式中,枸櫞酸抗凝 568 例(62.3%),肝素抗凝 72 例(7.9%),枸櫞酸+肝素抗凝 24 例(2.6%),無抗凝 247 例(27.1%)。CRRT 持續時間為 124(71,236) h。
2.2 暴露因素與結局
研究人群的 ΔFO% 為 ?3.27%(?6.03%,0.01%),28 d 死亡率為 40.1%(365/911)。對研究人群按 ΔFO% 行四分位數分組,其基線數據見表1。總體來說,CRRT 首個 48 h 的 ΔFO% 越大,其人群病情嚴重度評分越高,血管活性用藥越多,代謝性酸中毒越嚴重,入院到 CRRT 啟動時間越短,凈超濾速度越大。4 組間 CRRT 模式、抗凝方式和持續時間差異無統計學意義(P>0.05)。4 組 28 d 死亡率分別為 36.0%、31.3%、43.9% 和 49.1%,差異有統計學意義(P<0.05),見表2。相比死亡組,生存者的中位 ΔFO% 更低[?3.69%(?6.34%,?0.50%) vs. ?2.35%(?5.76%,1.05%);中位數差=?1.39%,95%CI(?1.98%,?0.64%),P<0.001]。
2.3 暴露因素與結局的關系
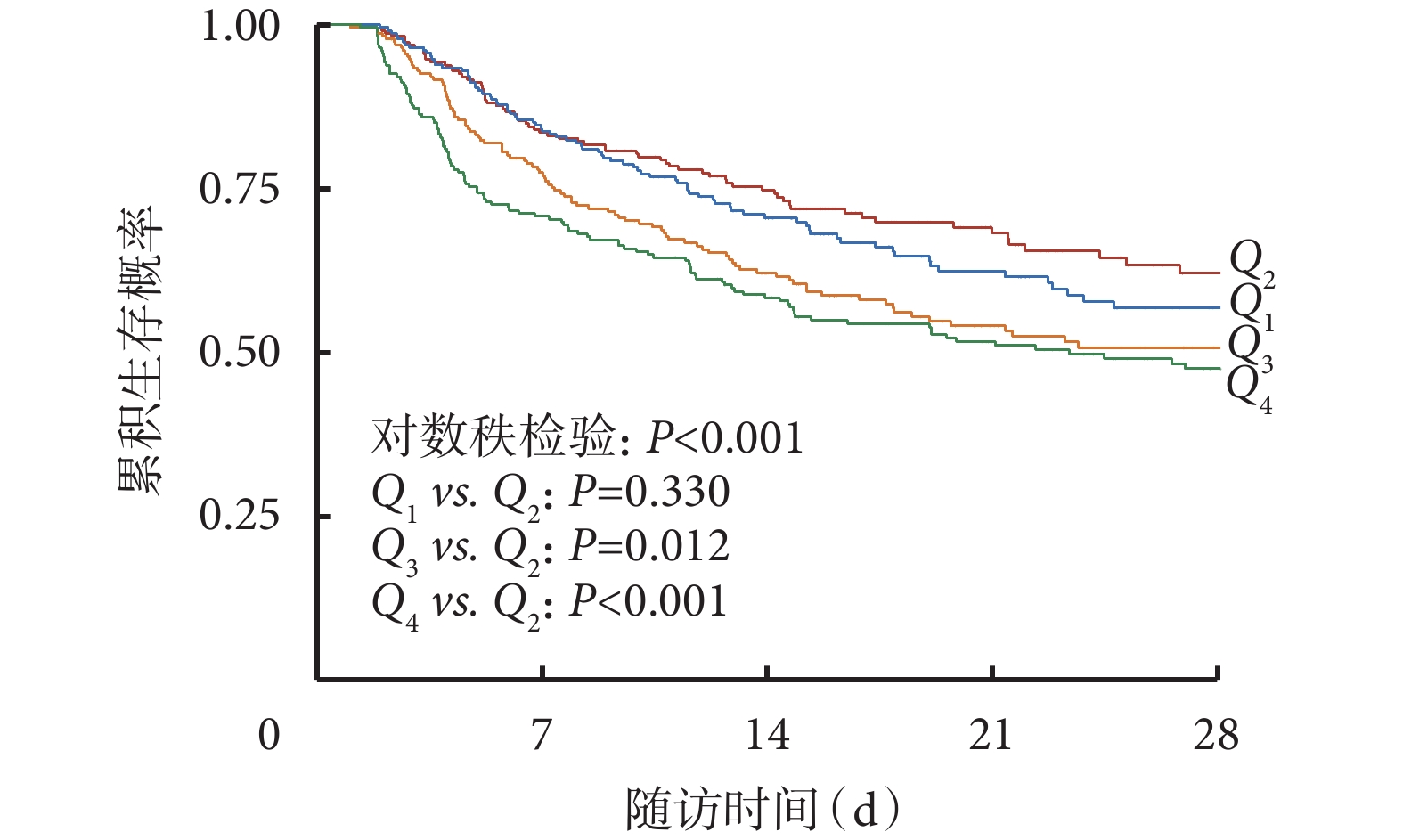
生存分析顯示,CRRT 啟動后 48 h 的 ΔFO% 四分位分組間的生存曲線差異有統計學意義(P<0.001)。其中 Q1 組與 Q2 組差異無統計學意義(P>0.05),Q3 組和 Q4 組相比 Q2 組死亡風險均增高(P<0.05)。見圖2。
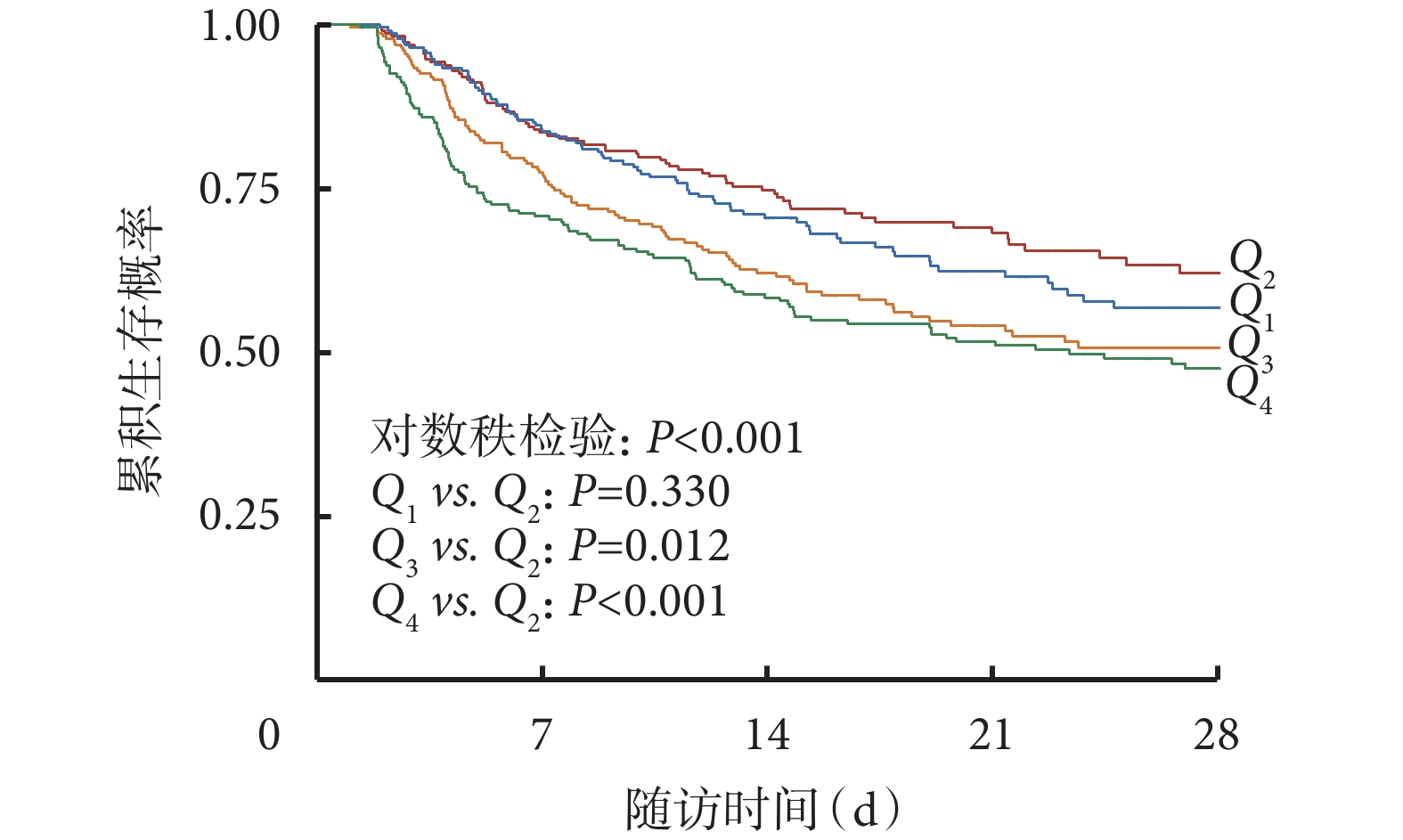 圖2
按 CRRT 48 h 內 ΔFO% 四分位分組患者 Kaplan-Meier 生存曲線分析
圖2
按 CRRT 48 h 內 ΔFO% 四分位分組患者 Kaplan-Meier 生存曲線分析
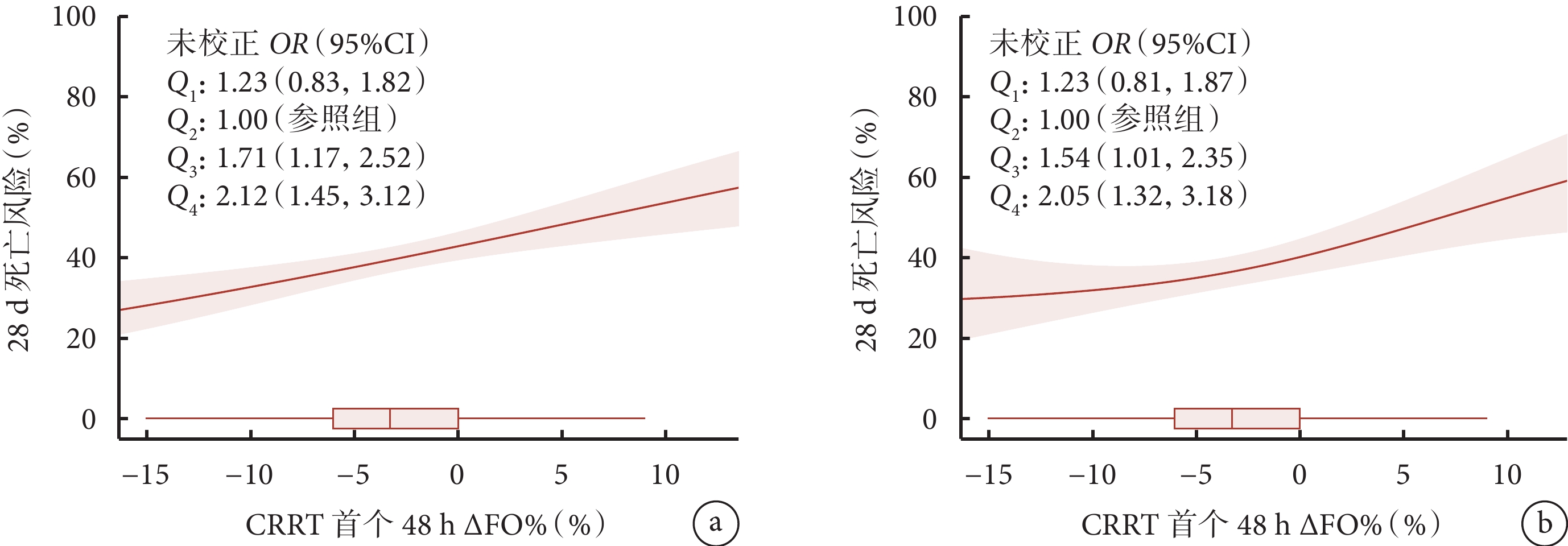
廣義可加線性回歸模型顯示 CRRT 啟動后 48 h 的 ΔFO% 與 28 d 死亡呈線性關系,但在校正其他變量后,CRRT 啟動后 48 h 的 ΔFO% 與 28 d 死亡呈 J 型曲線關系(圖3)。未校正 logistic 回歸結果顯示,與 Q2 組相比,Q1 組的死亡風險差異無統計學意義(P>0.05),但 Q3 組和 Q4 組的 28 d 死亡率均顯著增高(P<0.05)。在校正其他混淆因素后,關系仍然成立(表3)。
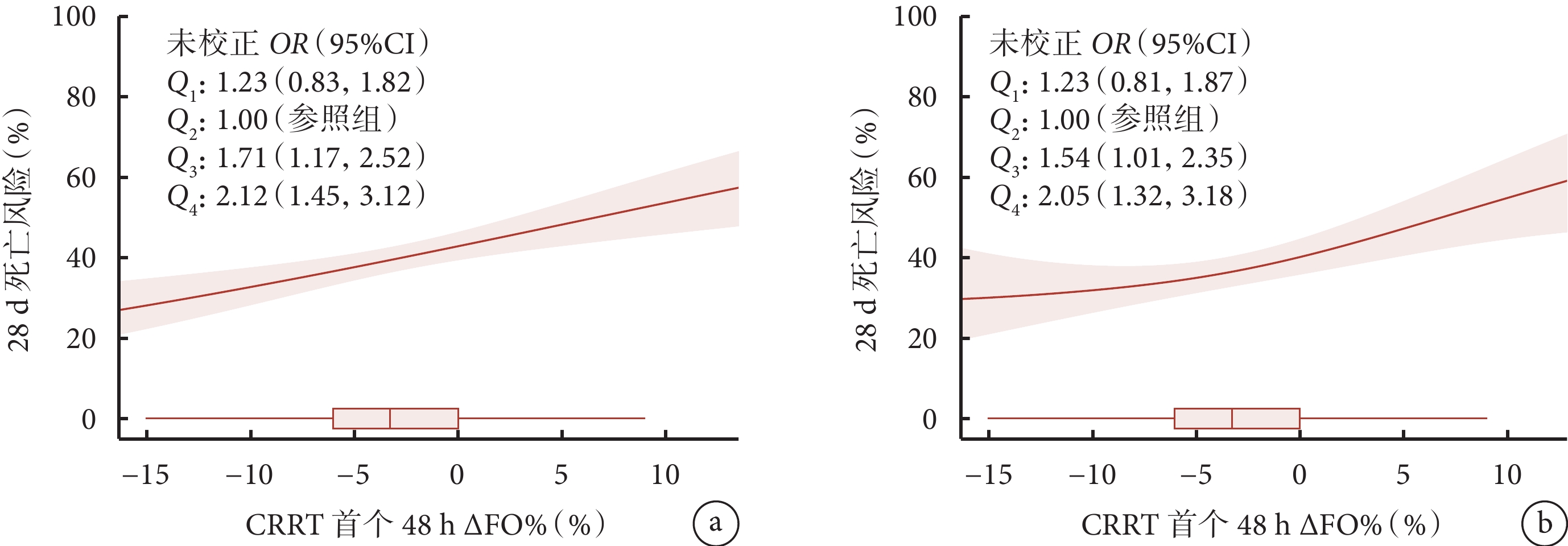 圖3
CRRT 48 h 內 ΔFO% 與 28 d 死亡率關系
圖3
CRRT 48 h 內 ΔFO% 與 28 d 死亡率關系
a. 48 h ΔFO% 與 28 d 死亡風險關系(未校正),使用廣義可加線性模型得到;ΔFO% 的中位數、四分位數和 95% 置信區間使用箱式圖表示;b. 48 h ΔFO% 與 28 d 死亡風險關系(校正)。CRRT:連續性腎臟替代治療;ΔFO%:液體超負荷改變比例
分析第 1 個 24 h 和第 2 個 24 h 內 ΔFO% 與 28 d 死亡率關系,發現 CRRT 啟動后第 1 個 24 h ΔFO% 四分位分組與 28 d 死亡率無統計學關聯(表3)。但 CRRT 啟動后第 2 個 24 h ΔFO% 與 28 d 死亡呈線性關系(表3),即 ΔFO% 越正,死亡率越高[每增加 1% 的 OR=1.10,95%CI(1.04,1.16),P<0.001]。
交互作用分析顯示,心血管 ICU 與入 ICU 至 CRRT 天數與暴露存在交互作用,心血管 ICU 患者中暴露與結局關聯[OR=1.09,95%CI(1.03,1.15)]強于非心血管 ICU[OR=1.03,95%CI(1.00,1.07)],入 ICU 至 CRRT 天數短的患者中暴露與結局關聯[OR=1.08,95%CI(1.04,1.13)]強于長的患者[OR=1.01,95%CI(0.97,1.05)]。
3 討論
CRRT 是重癥患者的主要腎臟替代治療方式,其核心任務之一是維持患者的容量平衡。但是目前關于 CRRT 啟動后早期的容量變化情況與 28 d 死亡率之間的關系并無定論。本研究顯示在需進行 CRRT 的 AKI 患者中,CRRT 啟動后 48 h 內 ΔFO%≥?3.27% 與 28 d 死亡風險增高獨立相關。進一步分析顯示 CRRT 啟動后首個 24 h 內 ΔFO% 與死亡率關系無統計學意義,而第 2 個 24 h 內的 ΔFO% 與死亡率顯著相關。這種關系提示第 1 個 24 h CRRT 液體管理目標并不需要強制液體負平衡,而第 2 個 24 h CRRT 液體管理目標應該要求液體負平衡。這與休克的“ROSE”理論(復蘇-優化-穩定-撤減)[18]是相符的。
目前觀察性研究證實接受 CRRT 的危重患者的容量超負荷與不良結局有關。Woodward 等[19]發現,在需要 CRRT 的 AKI 危重患者中,超過 10% 的液體負荷百分比與 90 d 內主要腎臟不良事件的風險更高相關,包括死亡率的上升和腎臟恢復率的下降。類似地,Jhee 等[20]發現,CRRT 啟動后 24 h 和 72 h 累積液體平衡的增加與 CRRT 開始后的 7 d 和 28 d 死亡率顯著相關。目前也有多項觀察性研究支持負的液體平衡與更好的預后顯著相關。Neyra 等[15]發現生存組較之非生存組有著更負的液體平衡,且 CRRT 開始后目標液體平衡與實際液體平衡之間的差距百分比與住院死亡率獨立相關。孫治平等[16]發現液體負平衡組患者 60 d 死亡率相比正平衡組更低(40% vs. 67%,P=0.036)。在對重癥 AKI 患者 CRRT 的 RENAL 試驗的二次分析中,幸存者的 ICU 住院期間的平均日液體平衡為 ?234 mL,而非幸存者的為 +560 mL;此外,負的平均日液體平衡與 90 d 死亡風險的降低以及無透析天數和無住院天數的增加獨立相關[14]。Naorungroj 等[21]也發現,CRRT 啟動后早期更明顯的每小時負的液體平衡與降低 ICU 死亡率有關。本研究也支持負的 ΔFO%(最低死亡風險四分位組 ΔFO% 為 –6.03%~–3.27%)與更好預后相關,但是迄今為止還沒有隨機臨床試驗在接受 CRRT 的危重患者中探索液體清除和生存之間的因果關系。
上述多項研究支持與正的液體平衡相比,接受 CRRT 的危重癥患者負的液體平衡與更好的預后相關。負的液體平衡與改善預后的原因可以用 ROSE 四階段模型來解釋[18, 22]。通常 CRRT 開始時,大多患者處于優化或穩定階段,接近于液體零平衡。而存活的患者多數能進入到穩定和去復蘇階段,即通過 CRRT 支持出現液體負平衡。而死亡患者通常持續處于復蘇和優化階段,無法進入下一階段以迎來負的液體平衡,這就導致了正的液體平衡與死亡率上升相關的現象出現。本研究顯示在需 CRRT 的 AKI 患者中,CRRT 啟動后 48 h 內 ΔFO%≥?3.27% 與 28 d 死亡風險增高獨立相關,但是更大的 ΔFO% 并沒有顯著改善預后。這與 2020 年的一項研究結果一致,該研究顯示時間平均每小時液體平衡在 18.5 至 ?33 mL/h 之間較>18.5 mL/h 死亡風險降低,<?33 mL/h 組死亡風險并未顯著下降[21]。這提示容量負荷減輕可能減少死亡風險,但進一步減少容量并不能進一步改善預后。然而,觀察性研究可能會被這樣一個事實所混淆,即液體只能在對液體清除有耐受能力的患者中清除,體液平衡陽性也是危重癥嚴重程度的標志。因此,可能是對液體清除的耐受性和調節液體穩態的能力與更好的臨床結局相關,而非液體清除本身[22]。這表明耐受液體清除的能力和隨之而來的負液平衡是更好的生理儲備的標志。
本研究也提示更負的 ΔFO%(<–6.03%)并不能進一步改善預后,這可能與該人群液體負荷過重或凈超濾率過大相關。需 CRRT 的 AKI 患者液體負荷越重,死亡風險越高[9-13];而積極 CRRT 減輕液體負荷可能并不能完全逆轉預后。另外,更負的液體負荷改變需要更大的凈超濾率,而過大的凈超濾率則增加低血壓、低灌注發生,增加患者死亡風險[23-24]。另外交互作用分析顯示 CRRT 期間液體負荷改變在心血管 ICU 人群與入 ICU 至 CRRT 天數短的患者中更顯著,提示了容量負荷在心功能衰竭人群中具有更重要的作用。
本研究顯示,CRRT 啟動后第 2 個 24 h ΔFO% 與 28 d 死亡率線性相關,但第 1 個 24 h 關系 ΔFO% 與 28 d 死亡率關系不顯著。這種相關性不一致也可以用 ROSE 模型進行解釋[18, 22]。CRRT 起始后第 1 個 24 h 患者多數處于復蘇或優化階段,可能需要液體正平衡保持充足的血流灌注。因此第 1 個 24 h ΔFO% 與 28 d 死亡率關系不顯著。但是 CRRT 啟動后第 2 個 24 h 病情好轉的患者已處于穩定或撤減階段,可以耐受液體負平衡;而病情持續不好轉的患者仍處于復蘇或優化階段,仍需要更多的液體正平衡。這種時間不同 CRRT ΔFO% 與預后關系的不一致提示,第 1 個 24 h CRRT 液體管理目標并不需要強制液體負平衡,而第 2 個 24 h CRRT 液體管理目標應該要求液體負平衡。
本研究也存在一些局限性:首先該研究是單中心回顧性隊列研究,研究人群存在一定異質性,研究結果能否外推到其他人群尚有待進一步證實。其次,雖然本研究對模型進行了多方面的校正,但仍存在未校正的混雜因素。未來需采用大型隨機對照研究來驗證 CRRT 不同的液體平衡策略與預后的關系,以指導臨床 CRRT 液體管理策略。
綜上,在需 CRRT 的 AKI 患者中,CRRT 啟動后 48 h 內 ΔFO%≥?3.27% 與 28 d 死亡風險增高獨立相關,但 ΔFO%<?6.03% 并不與更好的預后相關。CRRT 啟動后第 2 個 24 h ΔFO% 與 28 d 死亡率線性相關,但第 1 個 24 h ΔFO% 與 28 d 死亡率關系不顯著,這提示 CRRT 液體管理目標應該動態變化,即第 1 個 24 h CRRT 液體管理目標并不需要強制液體負平衡,而第 2 個 24 h CRRT 液體管理目標應該要求液體負平衡。
利益沖突:所有作者聲明不存在利益沖突。
急性腎損傷(acute kidney injury, AKI)是入住重癥監護病房(intensive care unit, ICU)患者常見的臨床綜合征,發生率可達 50%~60%[1],與短期死亡風險增加和長期不良預后獨立相關[2-4]。AKI 患者目前管理是通過改善血流動力學,清除潛在腎損傷物質,當合并高鉀血癥、代謝性酸中毒等嚴重并發癥時可應用腎臟替代治療[5]。腎臟替代治療是嚴重 AKI 時治療的主流方式,其中 75% 的 ICU 患者使用連續性腎臟替代治療(continuous renal replacement therapy, CRRT)[1]。相比間斷透析,CRRT 與透析依賴減少相關[6-7],因此 CRRT 被認為是 ICU 中 AKI 患者首選腎臟替代治療模式。CRRT 是一種緩慢連續清除體內溶質和液體的體外血液凈化方式[8]。既往研究表明液體超負荷與 AKI 的發病率、死亡率和腎功能恢復降低獨立相關[9-13]。但作為嚴重 AKI 患者容量管理的主要手段,CRRT 容量管理是維持液體平衡還是積極超濾尚不確定。觀察性分析表明 CRRT 期間的液體負平衡與改善的臨床結局相關[14-16]。但既往研究采用液體平衡作為容量管理評估手段存在一些缺點,包括未校正患者體重,且少有體重標準化的液體平衡變化比例與預后的關系。因此本研究通過回顧性隊列研究分析體重標準化的液體平衡變化與接受 CRRT 的 AKI 患者 28 d 死亡率之間的關系。
1 對象與方法
1.1 研究對象
利用 MIMIC-IV(Medical Information Mart for Intensive Care-IV)數據庫 0.4 版中的數據進行回顧性隊列研究[17]。MIMIC-IV 記錄了 2008 年—2019 年美國 Beth Israel Deaconess 醫療中心 ICU
1.2 資料收集
通過 PostgreSQL(version 12)中的結構化查詢語言從 MIMIC-IV 數據庫中提取每例患者的數據,提取的資料包括人口統計學特征(年齡、性別、種族、身高、入院體重、入院類型和 ICU 類型)、并發癥(高血壓、糖尿病、慢性腎病、慢性心力衰竭、癌癥和查爾森合并癥指數評分)、入院第 1 天的疾病嚴重程度[牛津急性疾病嚴重程度評分(Oxford Acute Sickness Severity Score, OASIS)]、CRRT 前序貫器官衰竭評估(Sequential Organ Failure Assessment, SOFA)評分、CRRT 前血管活性強心藥物評分(Vasoactive-inotropic Score, VIS)、實驗室檢查、生命體征、CRRT 數據(包括 CRRT 設置、超濾數據、液體平衡和從 ICU 入院到 CRRT 的時間間隔)和臨床結果等。
1.3 暴露因素與結局
暴露變量為 CRRT 啟動后 48 h 液體超負荷改變比例(proportion of change of fluid overload, ΔFO%),其定義為體重標準化的液體入量與出量之差。由于潛在的非線性關系,分析時將暴露變量按四分位數分組(按照從小至大分別稱為 Q1、Q2、Q3、Q4 組),死亡風險最低組在分析中用作參考。研究終點為 28 d 死亡率。
1.4 統計學方法
連續性變量采用中位數(下四分位數,上四分位數)表示,4 組間比較采用 Kruskal-Wallis H 秩和檢驗。分類變量采用例數和/或百分比表示,4 組間采用 χ2 檢驗或 Fisher 確切概率法。兩兩比較使用 Bonferroni 校正。本研究未估計樣本量,納入了數據庫中所有符合條件的受試者。由于缺失數據可能會偏離分析結果,本研究使用多重插值法對體質量指數的缺失數據進行處理。
使用廣義可加線性回歸模型分析連續性變量 ΔFO% 與 28 d 死亡率的關系;使用對數秩檢驗分析四分位分組間生存曲線差異,組間比較使用 Benjamini-Hochberg 校正;因不滿足 Cox 模型比例風險假設,故使用單因素和多因素 logistic 回歸分析 ΔFO% 四分位分組與 28 d 死亡率的關系,計算比值比(odds ratio, OR)及 95% 置信區間(confidence interval, CI),多因素模型校正變量包括有臨床意義或單因素分析有統計學意義的人口統計學特征、基礎疾病、入院情況、CRRT 前情況和 CRRT 持續時間。使用 R 4.3.1 軟件進行統計分析。雙側檢驗水準 α=0.05。
2 結果
2.1 一般資料
根據納入與排除標準,本研究納入 911 例患者(圖1)。研究人群年齡 63(52,73)歲,男性占 60.0%(547 例);白人 586 例(64.3%),黑人 72 例(7.9%),其他種族 253 例(27.8%);體質量指數 32.2(27.6,37.7) kg/m2;基線肌酐 0.9(0.7,1.1) mg/dL;372 例(40.8%)進行手術,286 例(31.4%)來自心血管 ICU;既往慢性腎臟病 372 例(40.8%),充血性心力衰竭 362 例(39.7%);查爾森合并癥指數評分 3(2,5)分;入院 OASIS 評分 46(38,51)分,VIS 評分 0.8(0,2.4)分,SOFA 評分 13(10,15)分;CRRT 前少尿 498 例(54.7%),膿毒癥 611 例(67.1%),機械通氣 673 例(73.9%),使用血管加壓藥物 605 例(66.4%),使用強心藥物 86 例(9.4%)。
 圖1
患者篩選流程圖
圖1
患者篩選流程圖
CRRT:連續性腎臟替代治療;ICU:重癥監護病房;AKI:急性腎損傷
入院到 CRRT 啟動前累計液體負荷比例為 0.07(0.02,0.13)。CRRT 模式中,濾過模式 67 例(7.4%),透析模式 10 例(1.1%),透析濾過模式 826 例(90.7%),單純超濾 8 例(0.9%)。CRRT 劑量為 25.6(21.6,289.0)mL/(kg·h),CRRT 抗凝方式中,枸櫞酸抗凝 568 例(62.3%),肝素抗凝 72 例(7.9%),枸櫞酸+肝素抗凝 24 例(2.6%),無抗凝 247 例(27.1%)。CRRT 持續時間為 124(71,236) h。
2.2 暴露因素與結局
研究人群的 ΔFO% 為 ?3.27%(?6.03%,0.01%),28 d 死亡率為 40.1%(365/911)。對研究人群按 ΔFO% 行四分位數分組,其基線數據見表1。總體來說,CRRT 首個 48 h 的 ΔFO% 越大,其人群病情嚴重度評分越高,血管活性用藥越多,代謝性酸中毒越嚴重,入院到 CRRT 啟動時間越短,凈超濾速度越大。4 組間 CRRT 模式、抗凝方式和持續時間差異無統計學意義(P>0.05)。4 組 28 d 死亡率分別為 36.0%、31.3%、43.9% 和 49.1%,差異有統計學意義(P<0.05),見表2。相比死亡組,生存者的中位 ΔFO% 更低[?3.69%(?6.34%,?0.50%) vs. ?2.35%(?5.76%,1.05%);中位數差=?1.39%,95%CI(?1.98%,?0.64%),P<0.001]。
2.3 暴露因素與結局的關系
生存分析顯示,CRRT 啟動后 48 h 的 ΔFO% 四分位分組間的生存曲線差異有統計學意義(P<0.001)。其中 Q1 組與 Q2 組差異無統計學意義(P>0.05),Q3 組和 Q4 組相比 Q2 組死亡風險均增高(P<0.05)。見圖2。
 圖2
按 CRRT 48 h 內 ΔFO% 四分位分組患者 Kaplan-Meier 生存曲線分析
圖2
按 CRRT 48 h 內 ΔFO% 四分位分組患者 Kaplan-Meier 生存曲線分析
廣義可加線性回歸模型顯示 CRRT 啟動后 48 h 的 ΔFO% 與 28 d 死亡呈線性關系,但在校正其他變量后,CRRT 啟動后 48 h 的 ΔFO% 與 28 d 死亡呈 J 型曲線關系(圖3)。未校正 logistic 回歸結果顯示,與 Q2 組相比,Q1 組的死亡風險差異無統計學意義(P>0.05),但 Q3 組和 Q4 組的 28 d 死亡率均顯著增高(P<0.05)。在校正其他混淆因素后,關系仍然成立(表3)。
 圖3
CRRT 48 h 內 ΔFO% 與 28 d 死亡率關系
圖3
CRRT 48 h 內 ΔFO% 與 28 d 死亡率關系
a. 48 h ΔFO% 與 28 d 死亡風險關系(未校正),使用廣義可加線性模型得到;ΔFO% 的中位數、四分位數和 95% 置信區間使用箱式圖表示;b. 48 h ΔFO% 與 28 d 死亡風險關系(校正)。CRRT:連續性腎臟替代治療;ΔFO%:液體超負荷改變比例
分析第 1 個 24 h 和第 2 個 24 h 內 ΔFO% 與 28 d 死亡率關系,發現 CRRT 啟動后第 1 個 24 h ΔFO% 四分位分組與 28 d 死亡率無統計學關聯(表3)。但 CRRT 啟動后第 2 個 24 h ΔFO% 與 28 d 死亡呈線性關系(表3),即 ΔFO% 越正,死亡率越高[每增加 1% 的 OR=1.10,95%CI(1.04,1.16),P<0.001]。
交互作用分析顯示,心血管 ICU 與入 ICU 至 CRRT 天數與暴露存在交互作用,心血管 ICU 患者中暴露與結局關聯[OR=1.09,95%CI(1.03,1.15)]強于非心血管 ICU[OR=1.03,95%CI(1.00,1.07)],入 ICU 至 CRRT 天數短的患者中暴露與結局關聯[OR=1.08,95%CI(1.04,1.13)]強于長的患者[OR=1.01,95%CI(0.97,1.05)]。
3 討論
CRRT 是重癥患者的主要腎臟替代治療方式,其核心任務之一是維持患者的容量平衡。但是目前關于 CRRT 啟動后早期的容量變化情況與 28 d 死亡率之間的關系并無定論。本研究顯示在需進行 CRRT 的 AKI 患者中,CRRT 啟動后 48 h 內 ΔFO%≥?3.27% 與 28 d 死亡風險增高獨立相關。進一步分析顯示 CRRT 啟動后首個 24 h 內 ΔFO% 與死亡率關系無統計學意義,而第 2 個 24 h 內的 ΔFO% 與死亡率顯著相關。這種關系提示第 1 個 24 h CRRT 液體管理目標并不需要強制液體負平衡,而第 2 個 24 h CRRT 液體管理目標應該要求液體負平衡。這與休克的“ROSE”理論(復蘇-優化-穩定-撤減)[18]是相符的。
目前觀察性研究證實接受 CRRT 的危重患者的容量超負荷與不良結局有關。Woodward 等[19]發現,在需要 CRRT 的 AKI 危重患者中,超過 10% 的液體負荷百分比與 90 d 內主要腎臟不良事件的風險更高相關,包括死亡率的上升和腎臟恢復率的下降。類似地,Jhee 等[20]發現,CRRT 啟動后 24 h 和 72 h 累積液體平衡的增加與 CRRT 開始后的 7 d 和 28 d 死亡率顯著相關。目前也有多項觀察性研究支持負的液體平衡與更好的預后顯著相關。Neyra 等[15]發現生存組較之非生存組有著更負的液體平衡,且 CRRT 開始后目標液體平衡與實際液體平衡之間的差距百分比與住院死亡率獨立相關。孫治平等[16]發現液體負平衡組患者 60 d 死亡率相比正平衡組更低(40% vs. 67%,P=0.036)。在對重癥 AKI 患者 CRRT 的 RENAL 試驗的二次分析中,幸存者的 ICU 住院期間的平均日液體平衡為 ?234 mL,而非幸存者的為 +560 mL;此外,負的平均日液體平衡與 90 d 死亡風險的降低以及無透析天數和無住院天數的增加獨立相關[14]。Naorungroj 等[21]也發現,CRRT 啟動后早期更明顯的每小時負的液體平衡與降低 ICU 死亡率有關。本研究也支持負的 ΔFO%(最低死亡風險四分位組 ΔFO% 為 –6.03%~–3.27%)與更好預后相關,但是迄今為止還沒有隨機臨床試驗在接受 CRRT 的危重患者中探索液體清除和生存之間的因果關系。
上述多項研究支持與正的液體平衡相比,接受 CRRT 的危重癥患者負的液體平衡與更好的預后相關。負的液體平衡與改善預后的原因可以用 ROSE 四階段模型來解釋[18, 22]。通常 CRRT 開始時,大多患者處于優化或穩定階段,接近于液體零平衡。而存活的患者多數能進入到穩定和去復蘇階段,即通過 CRRT 支持出現液體負平衡。而死亡患者通常持續處于復蘇和優化階段,無法進入下一階段以迎來負的液體平衡,這就導致了正的液體平衡與死亡率上升相關的現象出現。本研究顯示在需 CRRT 的 AKI 患者中,CRRT 啟動后 48 h 內 ΔFO%≥?3.27% 與 28 d 死亡風險增高獨立相關,但是更大的 ΔFO% 并沒有顯著改善預后。這與 2020 年的一項研究結果一致,該研究顯示時間平均每小時液體平衡在 18.5 至 ?33 mL/h 之間較>18.5 mL/h 死亡風險降低,<?33 mL/h 組死亡風險并未顯著下降[21]。這提示容量負荷減輕可能減少死亡風險,但進一步減少容量并不能進一步改善預后。然而,觀察性研究可能會被這樣一個事實所混淆,即液體只能在對液體清除有耐受能力的患者中清除,體液平衡陽性也是危重癥嚴重程度的標志。因此,可能是對液體清除的耐受性和調節液體穩態的能力與更好的臨床結局相關,而非液體清除本身[22]。這表明耐受液體清除的能力和隨之而來的負液平衡是更好的生理儲備的標志。
本研究也提示更負的 ΔFO%(<–6.03%)并不能進一步改善預后,這可能與該人群液體負荷過重或凈超濾率過大相關。需 CRRT 的 AKI 患者液體負荷越重,死亡風險越高[9-13];而積極 CRRT 減輕液體負荷可能并不能完全逆轉預后。另外,更負的液體負荷改變需要更大的凈超濾率,而過大的凈超濾率則增加低血壓、低灌注發生,增加患者死亡風險[23-24]。另外交互作用分析顯示 CRRT 期間液體負荷改變在心血管 ICU 人群與入 ICU 至 CRRT 天數短的患者中更顯著,提示了容量負荷在心功能衰竭人群中具有更重要的作用。
本研究顯示,CRRT 啟動后第 2 個 24 h ΔFO% 與 28 d 死亡率線性相關,但第 1 個 24 h 關系 ΔFO% 與 28 d 死亡率關系不顯著。這種相關性不一致也可以用 ROSE 模型進行解釋[18, 22]。CRRT 起始后第 1 個 24 h 患者多數處于復蘇或優化階段,可能需要液體正平衡保持充足的血流灌注。因此第 1 個 24 h ΔFO% 與 28 d 死亡率關系不顯著。但是 CRRT 啟動后第 2 個 24 h 病情好轉的患者已處于穩定或撤減階段,可以耐受液體負平衡;而病情持續不好轉的患者仍處于復蘇或優化階段,仍需要更多的液體正平衡。這種時間不同 CRRT ΔFO% 與預后關系的不一致提示,第 1 個 24 h CRRT 液體管理目標并不需要強制液體負平衡,而第 2 個 24 h CRRT 液體管理目標應該要求液體負平衡。
本研究也存在一些局限性:首先該研究是單中心回顧性隊列研究,研究人群存在一定異質性,研究結果能否外推到其他人群尚有待進一步證實。其次,雖然本研究對模型進行了多方面的校正,但仍存在未校正的混雜因素。未來需采用大型隨機對照研究來驗證 CRRT 不同的液體平衡策略與預后的關系,以指導臨床 CRRT 液體管理策略。
綜上,在需 CRRT 的 AKI 患者中,CRRT 啟動后 48 h 內 ΔFO%≥?3.27% 與 28 d 死亡風險增高獨立相關,但 ΔFO%<?6.03% 并不與更好的預后相關。CRRT 啟動后第 2 個 24 h ΔFO% 與 28 d 死亡率線性相關,但第 1 個 24 h ΔFO% 與 28 d 死亡率關系不顯著,這提示 CRRT 液體管理目標應該動態變化,即第 1 個 24 h CRRT 液體管理目標并不需要強制液體負平衡,而第 2 個 24 h CRRT 液體管理目標應該要求液體負平衡。
利益沖突:所有作者聲明不存在利益沖突。