圍手術期機械通氣與肺損傷和術后肺部并發癥風險增加相關,但目前就如何在手術患者機械通氣期間提供最佳肺保護這一關鍵臨床問題尚缺乏共識,有必要制定適合我國麻醉醫生應用的圍手術期機械通氣專家共識以更好地指導臨床實踐。四川大學華西醫院組織成都醫學會麻醉專業委員會和重慶市醫學會麻醉專科分會專家提出關于圍手術期機械通氣的若干問題,對現有文獻進行回顧并征求專家意見,最后采用改良德爾菲法建立了該專家共識,制定出 28 條具有中-高級證據質量的推薦。
引用本文: 成都醫學會麻醉專業委員會, 重慶市醫學會麻醉專科分會,. 成人非心胸手術圍手術期機械通氣專家共識. 華西醫學, 2024, 39(11): 1679-1690. doi: 10.7507/1002-0179.202410028 復制
版權信息: ?四川大學華西醫院華西期刊社《華西醫學》版權所有,未經授權不得轉載、改編
我國每年手術近 0.8 億人次[1],其中絕大多數須在術中接受全身麻醉下的機械通氣支持。圍手術期機械通氣可能造成通氣和氣體交換機制受損、局部和全身炎癥反應等而增加術中肺損傷和術后肺部并發癥(postoperative pulmonary complication, PPC)風險[2-3]。研究報道,在接受非心胸手術患者中,肺部感染、肺不張、低氧血癥和呼吸衰竭等 PPC 發生率為 11%~59%[4-5]。圍手術期肺保護性通氣策略已被證實是降低 PPC 的有效措施,相關國際專家共識于 2019 年發布[6]。然而,國內調查性研究顯示,我國麻醉醫生對肺保護性通氣策略的理論認識與臨床實踐存在差異[7-8]。隨著近年來新的臨床證據不斷涌現,有必要制定適合我國麻醉醫生應用的圍手術期機械通氣專家共識,以更好地指導臨床實踐。本專家共識基于當前臨床證據,為成人非心胸手術提供圍手術期機械通氣的臨床實踐推薦。
1 共識制定過程
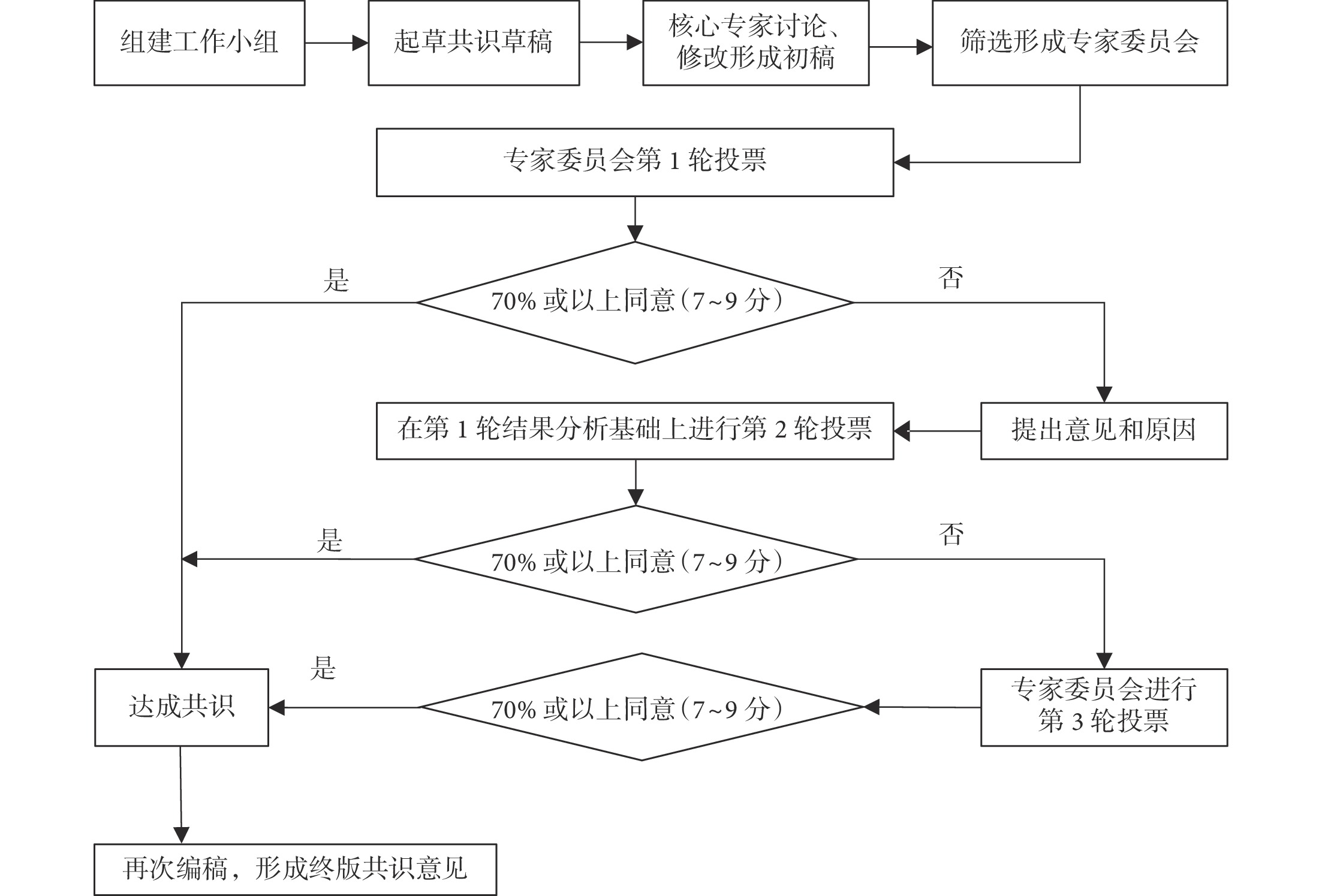
本共識制定采用改良德爾菲調查法。第 1 步:由四川大學華西醫院余海教授牽頭組建工作小組,該小組包含 3 名主任醫師和 2 名主治醫師,他們來自知名三級甲等醫院心胸麻醉和普外麻醉專業,并且都有超過 10 年的臨床麻醉經驗。工作小組起草了圍手術期機械通氣領域需要達成專家共識的臨床問題,并由 8 名來自成渝地區知名麻醉學教授/主任醫師組成的核心專家團隊進行開放式討論,最終篩選出 18 個擬納入共識的臨床問題。第 2 步:工作小組依據 PICO[研究對象(Participants)、干預措施(Interventions)、對照(Comparisons)和結局(Outcomes)]原則,對每一個問題進行系統的研究證據檢索和總結,形成共識初稿。第 3 步:成都醫學會麻醉專業委員會和重慶市醫學會麻醉專科分會遴選推舉 20 名成員組成專家委員會,推舉標準:在圍手術期機械通氣/麻醉學領域具有豐富經驗以及權威性的專家學者。由專家委員會對共識初稿進行匿名投票并反饋。共識投票方法:參考 Likert 9 級量表,不同意為 1~3 分,不確定為 4~6 分,同意為 7~9 分(1~6 分需給出理由或建議)。證據分級和推薦:按照 GRADE 評分進行總結和評估[9]。根據質量等級,證據被標注為高、中、低和極低,隨后予以推薦強度分級。第 4 步:經過 2 輪匿名反饋調查,每條共識投票同意率>70% 即可納入共識。第 5 步:通過 1 輪專家組集體討論后形成終版共識。具體流程見圖1。
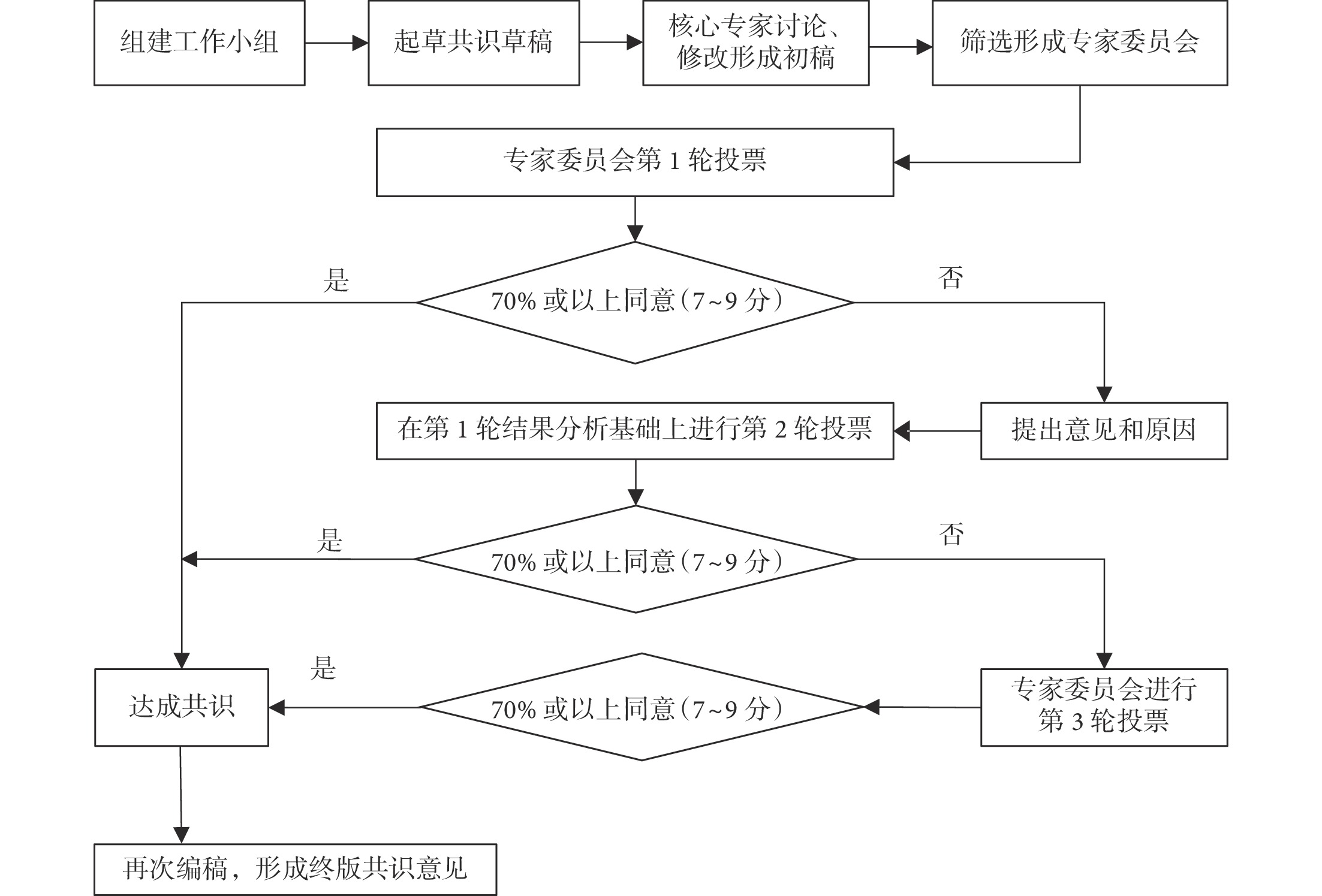 圖1
專家共識制定流程
圖1
專家共識制定流程
2 共識內容
本共識共形成 28 條關于成人非心胸手術圍手術期機械通氣管理的共識意見(表1)。
2.1 圍手術期機械通氣相關肺損傷的風險評估
圍手術期機械通氣相關肺損傷主要包括容積傷、氣壓傷、萎陷傷、生物傷和剪切傷,其臨床特征為 PPC 風險增加[10-11]:① 容積傷:機械通氣誘發的容積傷來源于高潮氣量通氣,導致肺泡破裂和嚴重氣體外漏(如縱隔氣腫和皮下氣腫);② 氣壓傷:機械通氣導致的氣壓傷來源于肺泡壓或跨肺壓而非氣道壓,高氣道壓力本身并不會導致機械通氣相關肺損傷;③ 萎陷傷:肺泡周期性的塌陷所造成的損傷;④ 生物傷:指局部或廣泛的生物反應,如激活促炎和促損傷的細胞因子級聯反應;⑤ 剪切傷:由于肺泡通氣不均勻產生的區域力學差異誘發了額外的機械應力產生的肺損傷。
2.1.1 危險因素
全面的病史和體格檢查是評估 PPC 風險的關鍵,建議已經建立電子信息化系統的醫療單位將 PPC 危險因素評估量表嵌入術前訪視電子信息化系統。
機械通氣相關肺損傷風險因素包括[6, 12-15]:① 一般狀況:年齡>50 歲,吸煙,美國麻醉醫師協會分級>Ⅱ級,體質量指數>40 kg/m2;② 合并癥:睡眠呼吸暫停綜合征,呼吸系統感染,慢性阻塞性肺疾病(慢阻肺),間質性肺疾病,控制不良的支氣管哮喘,肺高壓,充血性心力衰竭,低白蛋白血癥(血白蛋白<30 g/L),貧血(血紅蛋白<100 g/L),血清尿素氮>300 g/L,以及術前脈搏血氧飽和度(pulse oxygen saturation, SpO2)≤95%;③ 手術因素:手術部位(大血管、上腹部、頭頸及神經外科手術),預計手術時長>2 h 和急診手術。
2.1.2 個體化的優化策略
基于術前 PPC 危險因素評估的優化策略包括[13]:① 改善心肺功能狀態;② 營養支持,糾正貧血、低蛋白血癥;③ 術前教育,包括戒煙 4 周和呼吸功能鍛煉;④ 多學科討論。
2.2 麻醉誘導階段的通氣方法建議
2.2.1 患者體位
麻醉誘導時仰臥位可導致腹部臟器向頭側移位,從而迫使膈肌上移。與仰臥位相比,頭高位可提高給氧去氮的效能,延長呼吸暫停的安全時間[16-17]。尤其是對于肥胖患者,30° 頭高位與仰臥位相比可有效減少功能殘氣量的降低[18]。
2.2.2 誘導期間預充氧
在麻醉誘導時進行預充氧可增加氧儲備。維持呼氣末氧濃度>90% 的高效預充氧是氣管插管過程中預防低氧血癥的關鍵[19]。肺活量呼吸法在至少 10 L/min 的新鮮氣流量下可實現快速預充氧[20]。Nimmagadda 等[21]研究顯示,采用 100% 吸入氧濃度(fraction of inspiratory oxygen, FiO2)進行預充氧時,在 10 L/min 新鮮氣流量下進行 1 min 8 次肺活量呼吸和在 5 L/min 新鮮氣流量下進行 3 min 正常潮氣量呼吸同樣有效。預充氧最重要的潛在并發癥是吸收性肺不張,麻醉誘導后肺不張發生率高達 90%[19]。麻醉誘導以 80% FiO2 預充氧可減少肺不張[22],但會縮短呼吸暫停的安全時間。臨床醫生必須權衡肺不張與呼吸暫停的安全時間縮短的相對風險。對于肥胖患者,與常規面罩預充氧相比,高流量鼻導管吸氧可延長呼吸暫停的安全時間[23]。
2.2.3 誘導期間通氣
麻醉誘導期間可采用手動或機械控制行面罩正壓通氣,必要時可采用雙人正壓通氣。在面罩通氣期間聯合呼氣末正壓(positive end-expiratory pressure, PEEP)可延長呼吸暫停的安全時間,改善氧合[24]。然而,PEEP 的應用或氣道峰壓(peak pressure, Ppeak)>15 cm H2O(1 cm H2O=0.098 kPa)可能會增加胃進氣風險[25-26]。與單獨使用面罩相比,頭高位高流量鼻導管(high-flow nasal cannula, HFNC)可有效延長呼吸暫停的安全時間[27]。該技術可改善二氧化碳清除和增強氧合,但存在胃進氣的風險[28-29]。HFNC 適用于頭頸手術中面罩通氣受限的患者等[30]。誘導期間可根據氣道通暢度置入鼻或口咽通氣裝置來緩解上氣道梗阻,但如果患者存在以下情況則禁忌使用:① 口腔及上下頜骨創傷、咽部氣道占位性病變、喉頭水腫、哮喘、門齒有折斷或脫落危險、頻繁嘔吐;② 鼻息肉、鼻出血傾向、鼻外傷、鼻腔畸形、鼻腔炎癥、明顯的鼻中隔偏曲、凝血功能異常、顱底骨折、腦脊液耳鼻漏等。
2.3 術中機械通氣策略
2.3.1 常用的肺保護性通氣策略
針對機械通氣誘導肺損傷的一系列通氣設置優化措施稱為肺保護性通氣策略。肺保護性通氣策略是改善全身麻醉后肺部結局的有效措施,相比于傳統的通氣方式可減少機械通氣相關肺損傷、改善肺功能、降低 PPC 發生率和死亡率[31]。
① 經典的肺保護性通氣策略主要包含小潮氣量、適當的 PEEP、肺復張和低平臺壓等(詳見 2.3.3~2.3.5 節描述)。
② 肺開放通氣策略[32]:肺開放通氣是一種結合了小潮氣量、肺復張和個體化 PEEP 滴定的聯合策略。該策略強調盡可能打開塌陷的肺泡和維持其復張。
③ 驅動壓導向通氣策略[33]:驅動壓是促使肺泡開放的壓力,代表肺實質在整個吸氣過程中受到的壓力。驅動壓是氣道平臺壓(plateau pressure, Pplat)與 PEEP 的差值(Pplat–PEEP),<13 cm H2O 可降低 PPC 發生風險。
④ 機械功率導向通氣策略:機械功率是呼吸機維持通氣所做的功,是傳遞給呼吸系統和肺的能量總和。機械功率(J/min)計算為 0.098×RR×VT×[PEEP+(Pplat–PEEP)/2+(Ppeak–Pplat)],其中 RR 表示呼吸頻率,VT 表示潮氣量。較高的機械功率與患者術后呼吸衰竭發生率、死亡率有關,但目前暫缺乏機械功率最佳值的證據[34]。
2.3.2 術中機械通氣的通氣模式
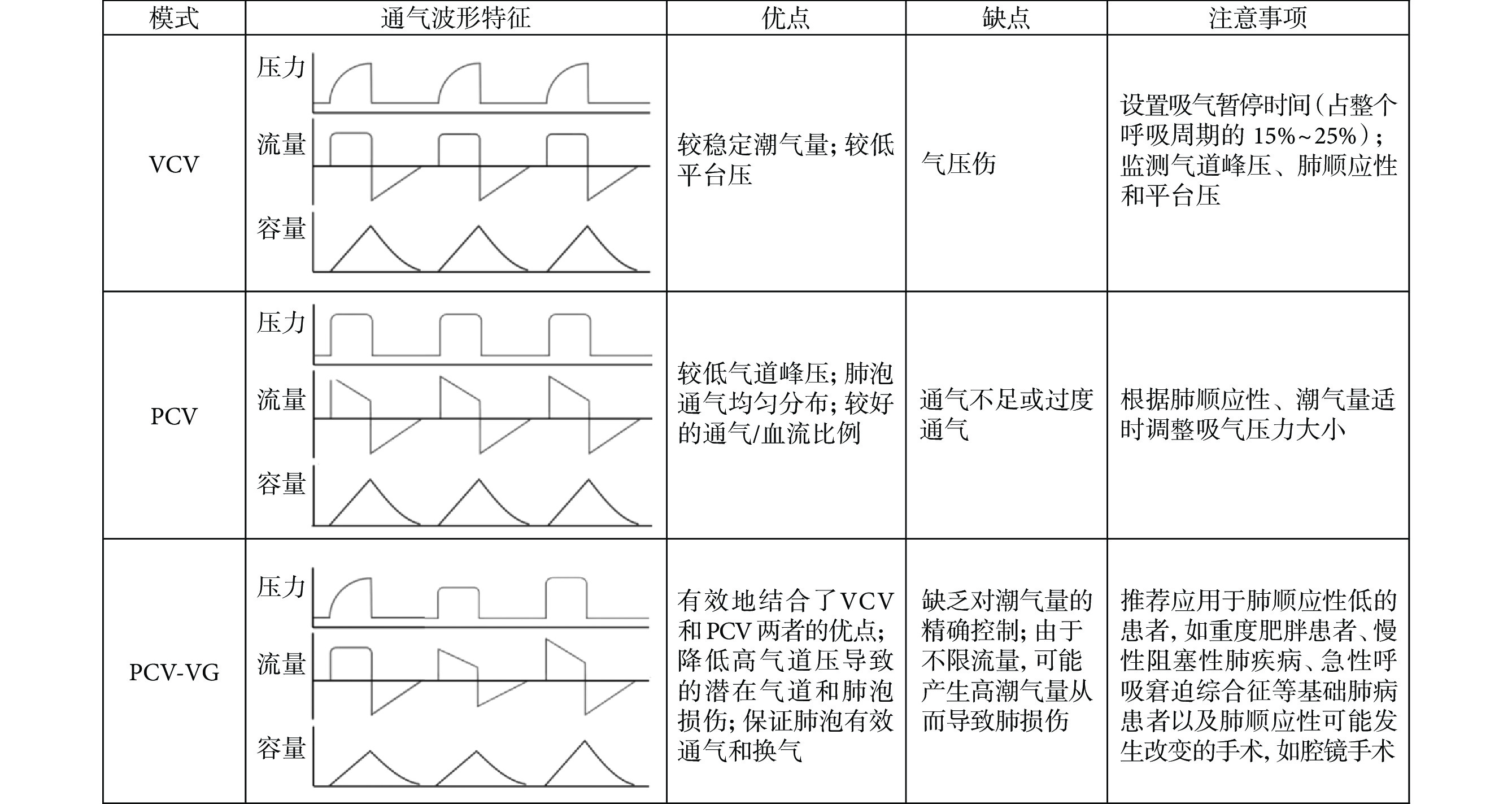
目前常用的術中機械通氣模式包括容量控制通氣(volume-controlled ventilation, VCV)、壓力控制通氣(pressure-controlled ventilation, PCV)、壓力控制-容量保證通氣(pressure-control with volume guaranteed ventilation, PCV-VG)。VCV 也稱容量限制通氣或容量循環通氣,呼吸機以恒定流量傳送潮氣量。在 PCV 模式下,呼吸機可在吸氣相維持恒定壓力,同時流量逐漸降低。PCV-VG 具有 PCV 的優勢,同時根據患者肺順應性的變化保障設置的最低潮氣量。雖然研究發現 PCV 和 PCV-VG 模式下 Ppeak 更低、肺順應性更好,但由于臨床結局的相似性,實現肺保護性通氣的最佳通氣模式選擇尚無定論[35-36]。近期的研究發現,在接受腹部手術和心胸手術的患者中,通氣方式的選擇并未降低 PPC 風險[37-38]。常用的通氣模式特點見圖2。
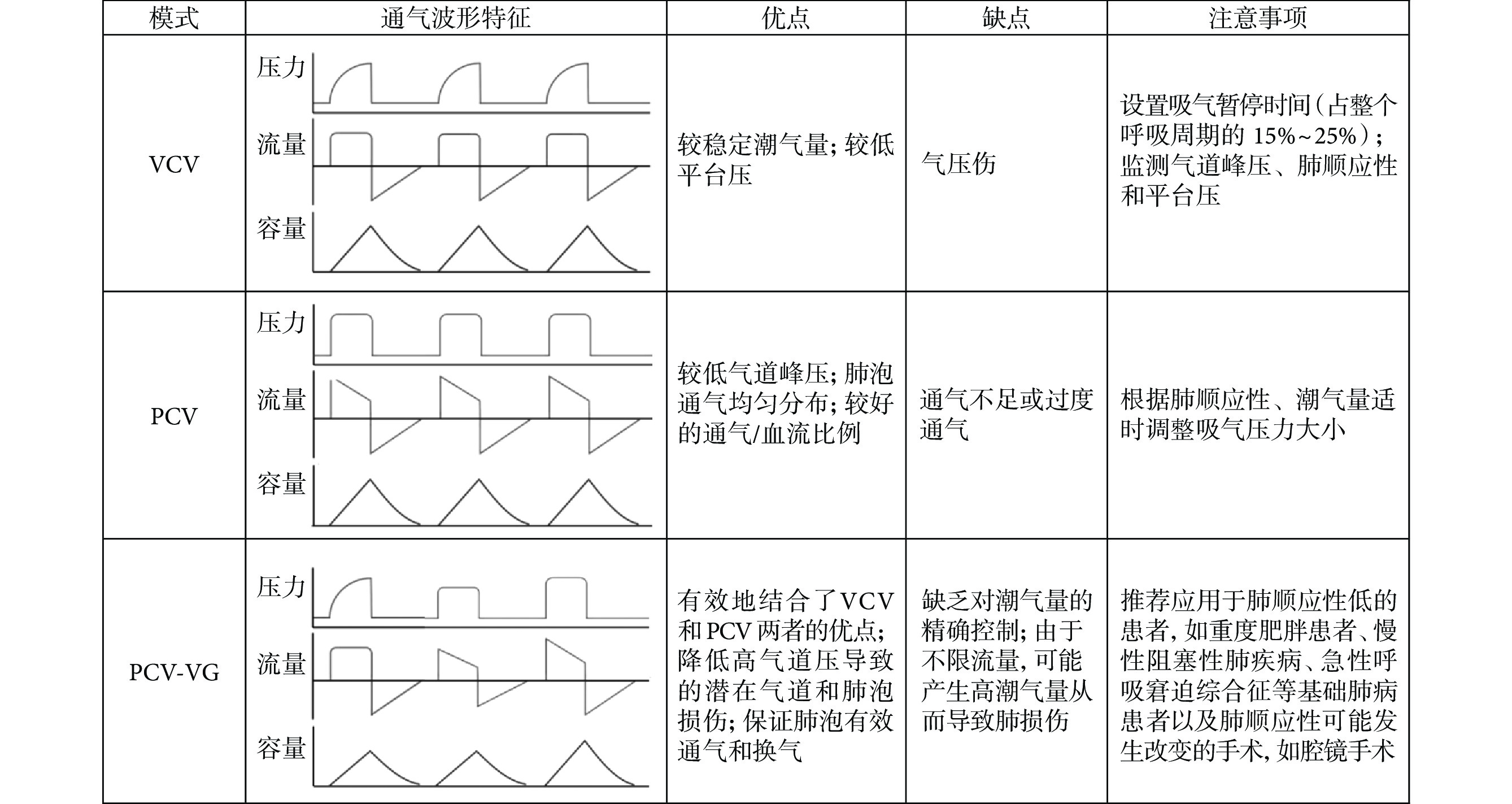 圖2
常用的通氣模式特點
圖2
常用的通氣模式特點
VCV:容量控制通氣;PCV:壓力控制通氣;PCV-VG:壓力控制-容量保證通氣
2.3.3 術中機械通氣的潮氣量
術中以小潮氣量(6~8 mL/kg)通氣是肺保護性通氣策略的重要組成部分。多項高質量研究證實,設定小潮氣量通氣能減少肺擴張傷和肺部感染等 PPC[39-40]。但需要注意的是,在小潮氣量通氣期間,應聯合 PEEP 和肺復張來改善肺順應性和防止肺不張[11]。
肺容積主要由性別和身高決定,建議以患者的預測體重來確定潮氣量[41]。推薦的預測體重公式為男性:50.0+0.905×(身高–152.4),女性:45.5+0.905×(身高–152.4)[42]。為方便應用,可將公式簡化為 0.91×(身高–152.4)+50/45.5。
2.3.4 術中機械通氣的 PEEP
PEEP 是指在機械通氣呼氣末時維持一定水平的正壓,使肺泡壓高于大氣壓。PEEP 可通過增加肺再通氣、促塌陷肺區域開放、增加氣體交換面積和減少肺內分流從而提高氧合。
多項研究表明 5~10 cm H2O 水平的 PEEP 可以優化通氣生理、改善肺功能和降低肺不張風險[31, 39],過低(≤2 cm H2O)或過高(≥12 cm H2O)的 PEEP 則無益[43-44],但其最佳水平沒有定論。推薦個體化的 PEEP 滴定,即根據驅動壓、動脈氧分壓、氧合指數、SpO2、肺順應性和/或肺超聲來調整[45]。滴定個體化 PEEP 水平采用遞增法,從 2 cm H2O 開始,每次呼吸周期遞增 2 cm H2O,在觀測到最低驅動壓、最佳氧合、最高順應性或最少肺不張時獲得個體化 PEEP 水平,如有條件,可在床旁肺超聲或胸電阻抗成像技術(electrical impedance tomography, EIT)監測下進行[46-50]。個體化 PEEP 滴定受限于各醫學中心設備和麻醉醫生掌握程度。以驅動壓為導向的 PEEP 滴定法提示大部分手術患者的最佳 PEEP 范圍為 5~8 cm H2O。基于現有的臨床證據,建議可應用 5~8 cm H2O PEEP,且應在低氧、氧合指數下降或肺順應性降低時予以個體化滴定調整。PEEP 滴定或高水平 PEEP 維持期間需關注其對循環的負面影響,通常表現為低血壓。
2.3.5 術中機械通氣的肺復張策略
肺復張指對于接受機械通氣的患者應用持續增加或維持較高的短暫正壓通氣使塌陷肺泡擴張,從而改善局部通氣、促進肺泡再灌注和增大有效通氣區域,達到逆轉肺不張和提高氧合的目的。
現有證據表明,對于非肥胖患者,肺復張的持續正壓應達到 30~40 cm H2O,對于肥胖患者須達到 40~45 cm H2O[51-53]。在實施肺復張時,應保持能維持 SpO2≥90% 的最低 FiO2 即可。肺復張可通過手控或機控兩種方法完成,更推薦機控通氣下的肺復張以達到均勻擴張肺泡和降低血流動力學紊亂風險的目的。手控肺復張指在麻醉機手控狀態下調節逸氣閥到 30~40 cm H2O 后,持續擠壓儲氣囊維持 15~30 s。機控肺復張包括 VCV 和 PCV 模式下的操作,需先設置吸呼比為 1∶1、呼吸頻率 6~8 次/min 和峰壓限制為 45 cm H2O。VCV 模式下,PEEP 設置 10~12 cm H2O,潮氣量從 6~8 mL/kg 開始,每 3~6 次呼吸增加 4 mL/kg,直至達到平臺壓 30~40 cm H2O,維持 3~6 次呼吸后完成肺復張,如潮氣量達到麻醉機上限仍無法實現目標平臺壓,則增加 PEEP。PCV 模式下,吸氣壓力從 15~20 cm H2O 開始,每 3~6 次呼吸 PEEP 增加 5 cm H2O,直至達到平臺壓 30~40 cm H2O,維持 3~6 次呼吸后完成肺復張[44, 53-54]。
肺復張的實施節點和頻率目前沒有定論,研究發現每小時進行肺復張并不降低 PPC 風險[44]。推薦至少在氣管插管后和氣管拔管前各進行 1 次。如術中出現氧合下降,應在排除通氣不足、分泌物阻塞等原因后進行 1~2 次肺復張,以排除和治療肺不張引起的低氧血癥。
肺復張策略對于肺泡再灌注的效果可通過壓力-容量曲線、氧合指數、床旁肺超聲或/和 EIT 監測[55-56]。在肺復張結束后應立即恢復小潮氣量和 PEEP 設置。肺復張可導致靜脈回流受阻、右心房壓升高和心排出量下降,特別是在機體容量欠缺的時候。因此在進行肺復張時,應密切關注血壓的波動,在血壓明顯降低時應暫停操作[57]。
2.3.6 術中機械通氣的吸呼比、呼吸頻率和呼氣末二氧化碳分壓(end-tidal carbon dioxide, ETCO2)
吸呼比推薦常規設置為 1∶2,這與正常呼吸生理相似。有數項研究表明,延長吸氣時間的等比通氣(吸呼比 1∶1)可改善腔鏡手術中的氧合、減少生理性呼吸死腔、降低 Ppeak 和 Pplat[58-61]。其潛在機制是吸氣時間延長可升高平均氣道力,吸氣流量減慢致氣體在肺內分布改善,以及由于呼氣時間短而產生內源性 PEEP。因此,在腔鏡手術等特殊手術人群,可以根據情況適當延長吸氣時間。Meta 分析顯示,反比通氣[吸呼比(1~4)∶1]可降低 Ppeak 和改善動態順應性[62],但應根據臨床情況采用。
機械通氣中呼吸頻率推薦常規設置為 8~12 次/min,并調整以維持正常的 ETCO2 水平。在聯合小潮氣量通氣的腔鏡手術中,為避免 ETCO2 過高,可能需要較快的呼吸頻率(12~18 次/min)。為避免快呼吸頻率導致的呼吸疊加和內源性 PEEP 過高,不建議呼吸頻率超過 18~20 次/min。
2.3.7 術中機械通氣的 FiO2 和新鮮氣流量
術中超出生理范圍的過量氧供應不僅對肺有直接毒性作用,還會促心肺腦血管收縮、炎癥反應和氧化應激[63-65]。高 FiO2 與肺不張等 PPC 風險增高相關,并可能增高術后死亡率[66-67]。30%~50% FiO2 可降低手術患者術后肺不張風險[68-70]。推薦在沒有低氧血癥的情況下,維持術中 FiO2≤40%。
常規新鮮氣流量為 1~2 L/min,在部分吸入麻醉和小兒麻醉中可能用到低新鮮氣流量(1 L/min),不建議常規應用高新鮮氣流量(≥3 L/min)。
2.3.8 術中通氣相關的監測建議
① 呼吸動力學監測:良好的呼吸動力學監測可以改善患者肺順應性和氧合。建議術中持續監測重要呼吸參數,包括潮氣量、Ppeak、Pplat、吸呼比和肺順應性,如有條件可監測平均氣道壓、壓力-容量曲線等。
② 呼氣末二氧化碳的監測:建議術中連續監測 ETCO2 的數值和波形,不僅可判斷氣管導管的位置,還反映肺通氣和肺血流,其正常值為 35~45 mm Hg(1 mm Hg=0.133 kPa)。
③ FiO2 監測:全身麻醉期間應常規監測 FiO2,具體見 2.3.7。
④ 氧合指數監測:術中監測 SpO2 的同時,對某些患者還需要進行氧合指數的監測,正常值應≥300 mm Hg。如果術中出現低于 300 mm Hg 的狀況,應快速進行病因分析和對癥處理。由于氧合指數受溫度、貧血、內環境等影響,需要綜合考慮分析。
⑤ 床旁肺超聲:圍手術期肺不張病變范圍和程度較輕,胸部 X 線片不易診斷,而診斷肺不張的金標準胸部 CT 依賴于特定的場所和設備,在手術中難以實現。肺超聲對圍手術期肺不張的診斷準確率與 CT 相似度約為 90%[71],能夠在術中實時監測肺不張、胸腔積液、氣胸等重要征象[72],可在減少射線暴露的情況下指導機械通氣。建議在有條件的醫療單位,麻醉醫師應接受肺超聲技術系統培訓。
⑥ EIT:EIT 是一種床旁、無創、無輻射的肺通氣監測技術,主要原理是根據肺組織的生物導電性因含氣量不同而存在差異的原理,通過局部電極感應呼吸過程中胸腔生物電阻抗變化,再利用相應的成像算法監測肺不同區域內通氣功能的狀態。EIT 還可用于指導實時肺復張、個體化 PEEP 設定和確立最佳通氣策略[46, 73]。
⑦ 通氣血流比(ventilation/perfusion ratio, V/Q)監測:術中 V/Q 失調可能會增加非心臟大手術的患者術后 PPC 風險,但是由于床旁評估 V/Q 的自動肺參數估計技術依賴特殊設備,臨床應用尚存在一定困難[74]。
2.4 麻醉蘇醒期通氣相關建議
麻醉蘇醒期指從手術結束時停止使用麻醉藥和輔助藥物后,意識呼吸逐漸恢復的時期。氣管拔管前患者需經歷從機械通氣到自主呼吸的轉換,這過程中通氣模式的選擇有間歇手控輔助通氣、機控通氣、同步間歇指令通氣(synchronized intermittent mandatory ventilation, SIMV)和壓力支持通氣(pressure support ventilation, PSV)模式等。對于全身麻醉患者的蘇醒期氣管拔管前機械通氣模式,目前尚無定論。SIMV 模式在機控呼吸與自主呼吸同步的基礎上提供設定的呼吸頻率和潮氣量,可與 PCV、PSV 模式同時應用。PSV 模式可單獨應用于已有自主呼吸的患者來提供壓力輔助通氣。SIMV 和 PSV 均可減少呼吸功、抵消麻醉藥物的呼吸抑制作用,以及在撤機前進行支持通氣。為促進帶管順應和減少不均勻通氣導致的肺不張等,我們建議如有條件,應在蘇醒階段采用 SIMV(無論有無自主呼吸)或 PSV(有自主呼吸)[75-76],否則仍繼續機控通氣。氣管拔管前應避免通過中斷通氣讓二氧化碳蓄積刺激自主呼吸恢復,因為呼吸暫停與肺泡塌陷相關,可能引起肺不張。
建議麻醉蘇醒階段氣管拔管前進行輔助給氧,以預防氣管拔管后低氧。但是,氣管拔管前即使短暫地給予高 FiO2 也可能產生吸收性肺不張[77]。因此,根據目前的證據,我們建議避免在氣管拔管前應用高 FiO2,30%~40% FiO2 即能在提供保證氧合的同時減少肺不張[68, 77-78]。
拔管時維持 30° 頭高位可顯著降低上腹部手術患者術后低氧血癥的發生[79]。推薦常規通過鼻導管吸入低流量氧氣(2~3 L/min,FiO2≤40%)行常規氧療維持 SpO2 ≥95%。
對低氧血癥高風險患者和肥胖患者,建議蘇醒期機控通氣時常規給予 PEEP,氣管拔管后給予持續氣道正壓通氣和 HFNC 氧療以改善氧合和降低低氧血癥風險[80-84]。有研究建議對 PPC 高風險患者實施無創間歇正壓通氣,但該技術并未降低 PPC 發生率[85],此結論尚存在爭議[86]。
近年,有研究提出采用無創的 SpO2/FiO2 比作為低氧血癥篩查的評估。SpO2/FiO2 和氧合指數具有良好的相關性,當 SpO2/FiO2<370 可能需要轉入重癥監護病房;SpO2/FiO2 在 370~450 需要進一步的臨床評估和動脈血氣檢查;SpO2/FiO2>450 時,可轉入普通病房[87]。需要注意的是,術后蘇醒期不同的吸氧裝置可達的氧濃度不同,具體參照表2[88]。
2.5 特殊患者通氣建議
2.5.1 肥胖患者的通氣建議
肥胖患者的呼吸系統順應性降低、膈肌升高、肺活量下降、肺容量減少伴肺不張增加、小氣道閉合、阻力增加,并存在較高的腹內壓導致限制性通氣障礙,因此是 PPC 發病的高危人群。研究證實肺保護性通氣策略可減少肥胖患者的通氣相關肺損傷[89]。研究指出術中維持≥10 cm H2O 的 PEEP 可以顯著降低肥胖患者 PPC 的發生率[90],但最佳 PEEP 值尚無定論,設置 PEEP 可能需要個體化,并根據患者和手術情況進行調整[44, 91]。肥胖患者還應該適當提高呼吸頻率,因為肥胖患者的二氧化碳產生過多,會繼發于高耗氧量,引起呼吸功增加[92]。
2.5.2 合并常見呼吸系統疾病患者的通氣建議
① 支氣管哮喘/支氣管痙攣。支氣管哮喘患者在圍手術期發生支氣管痙攣的風險高達 4.2%[93]。研究表明,手術前近 3 個月內未控制的哮喘患者術后死亡率是健康患者的 2 倍,術后肺炎發生率為健康患者的 3 倍[94]。建議對合并哮喘患者的呼吸功能和哮喘控制情況進行準確的臨床評估,并根據患者哮喘控制情況、手術緊急程度、術前干預方案等評估哮喘患者在全身麻醉中發生支氣管痙攣的危險程度,以制定相應的麻醉計劃。術中一旦發生支氣管痙攣,應立即消除刺激因素、加深麻醉、給予 β2 受體激動劑等。機械通氣中應注意提供足夠長的呼氣時間以避免內源性 PEEP,這可以通過使用比平時更小的潮氣量來實現[95]。此外,目前尚無證據支持任一通氣模式在哮喘患者中的應用,但應用 VCV 模式時可直接監測 Ppeak 和 Pplat[96],必要時手控通氣以克服氣道阻力所致的通氣不足。
② 慢阻肺。慢阻肺是一種以持續性氣流受限為病理特征的呼吸系統疾病,是 PPC 的獨立危險因素。對于慢阻肺患者需綜合手術緊急程度和患者病情制定麻醉方案,盡可能避免氣管插管的全身麻醉,必要時可進行多學科討論。此類患者術中最優通氣模式的選擇尚無定論,目前認為 PCV-VG 模式可降低肺氣壓傷風險、有利于術后肺功能恢復[97-98]。術中通氣推薦如下:A. 推薦慢阻肺患者采用小潮氣量(6~8 mL/kg 預測體重)通氣以減少機械通氣相關肺損傷和預防過度通氣[99]。B. 在機械通氣過程中,允許充分的呼氣,建議選擇較低的呼吸頻率,如 6~10 次/min。C. 在血液動力學穩定的人群中,允許適當的高碳酸血癥。在降低呼吸頻率、允許性高碳酸血癥、調節吸呼比等更基本的干預措施仍無法改善患者氧合時,可在有豐富經驗的上級醫師指導下適當提高吸氣峰壓[100]。D. 對慢阻肺患者應用 PEEP 可在呼氣末保持小氣道開放,改善與呼吸肌的相互作用和減少呼吸做功。E. 建議對于慢阻肺患者,外源性 PEEP 應接近 80%~85% 或等于可測得的內源性 PEEP 值[100]。但在臨床工作中,內源性 PEEP 值的測定存在困難,建議采用個體化 PEEP 設定。有條件的單位可以采用 EIT 指導確定 PEEP 水平。
③ 急性肺損傷(acute lung injury, ALI)/急性呼吸窘迫綜合征(acute respiratory distress syndrome, ARDS)。ALI/ARDS 是由多種因素誘導全身系統炎性疾病的肺部表現。肺保護性通氣是治療 ARDS 的有效手段,應早期給予小潮氣量(6 mL/kg)、PEEP>5 cm H2O 并維持平臺壓<30 cm H2O,有條件的情況下應個體化設置 PEEP。肺復張操作應謹慎使用,注意其對循環的影響[101]。對于 ALI/ARDS 患者術中機械通氣的設定,證據有限,建議參照 ARDS 管理指南的推薦[101]。
2.5.3 俯臥位患者的通氣建議
俯臥位患者的胸腔壓力分布更均勻,重度依賴區肺泡更容易張開,且俯臥位減少縱隔和心臟對背側組織的壓力,利于肺復張。對于俯臥位患者,建議給予肺保護性通氣(小潮氣量、5 cm H2O PEEP 和肺復張)可降低氣壓傷風險、減少肺部炎癥和改善術后氧合的同時不增加心血管事件[102-103]。此外,有研究表明 PCV 模式更有利于降低短期術后白細胞介素-6 和 C 反應蛋白水平及術后 PPC 的發生率[104],可能提供更理想的通氣參數[105]。
2.5.4 頭低足高位患者的通氣建議
頭低足高位(Trendelenburg)手術時,患者的腹腔臟器向頭端移動造成腹內壓增高,導致膈肌上移、胸內壓升高、肺泡擴張受限和氣道阻力增大等。推薦采用肺保護性通氣策略以改善術中氧合和減少機械通氣相關肺損傷[106]。另外可以考慮稍高水平 PEEP(>10 cm H2O)有利于減少肺不張[107],但須保持循環穩定。
3 小結
圍手術期肺保護性通氣策略可降低 PPC 風險,改善患者預后。本專家共識共形成 28 條關于成人非心胸手術圍手術期機械通氣的具有中-高級證據質量和專家強烈支持的推薦和聲明,是針對這一領域臨床證據的更新。本專家共識總結并評價了最新圍手術期機械通氣管理策略,對成人非心胸手術患者圍手術期機械通氣臨床實踐極具參考價值。
執筆人:孫琪榮(四川大學華西醫院),李雪霏(四川大學華西醫院),崔宇(電子科技大學附屬成都市婦女兒童中心醫院)
專家名單(按姓氏漢語拼音排序):
成都醫學會麻醉專業委員會專家名單:陳峰(都江堰市人民醫院),陳軍(彭州市人民醫院),鄧婉欣(成都市龍泉驛區第一人民醫院),丁孝東(四川天府新區人民醫院),董蜀華(成都醫學院),杜智(成都市新津區人民醫院),范丹(四川省人民醫院),付強(成都市第三人民醫院),郭浪濤(成都市婦女兒童中心醫院),何斌(成都大學附屬醫院),何崎(成都體育學院附屬體育醫院),吉陽(四川大學華西口腔醫院),賈飛(成都市錦江區婦幼保健院),姜春玲(四川大學華西醫院),亢平(成都市公共衛生臨床醫療中心),李德遠(金堂縣第一人民醫院),李佳(成都市中西醫結合醫院),李軍祥(成都市郫都區人民醫院),李俊芳(蒲江縣人民醫院),李茜(四川大學華西醫院),李祥奎(四川省人民醫院),李曉強(四川大學華西醫院),李永榮(四川華美紫馨醫學美容醫院),劉建波(大邑縣人民醫院),劉琉(成都中醫藥大學附屬醫院),劉永峰(邛崍市醫療中心醫院),羅東(四川大學華西第二醫院),羅化全(崇州市中醫醫院),羅小偉(成都市新都區中醫醫院),歐珊(成都市中西醫結合醫院),齊鵬亮(成都市第六人民醫院),舒家云(成都新都區人民醫院),孫燕(成都市第二人民醫院),孫陽陽(中國人民解放軍西部戰區總醫院),唐東(西藏自治區人民政府駐成都辦事處醫院),唐勇(四川錦欣婦女兒童醫院),陶勇(成都市雙流區第一人民醫院),王麗(成都醫學院第一附屬醫院),王雄(成都大學附屬醫院),王宇(三六三醫院),魏新川(四川大學華西第二醫院),溫開蘭(四川省人民醫院),肖勝(成都市武侯區人民醫院),謝先豐(成都市第二人民醫院),楊岸(簡陽市人民醫院),姚富(四川省骨科醫院),易明亮(成都市第五人民醫院),余海(四川大學華西醫院),袁川(成都市雙流區中醫醫院),張涵(崇州市人民醫院),張科(核工業四一六醫院),趙澤宇(四川省八一康復中心),鐘惠(成都市第七人民醫院),周激(成都新麗美醫療美容醫院),鄒江(四川省腫瘤醫院)
重慶市醫學會麻醉專科分會專家名單:白福海(陸軍軍醫大學第二附屬醫院),曹俊(重慶醫科大學附屬第一醫院),陳朝華(重慶市銅梁區人民醫院),陳理紅(重慶市第九人民醫院),陳力勇(陸軍特色醫學中心),程璐(重慶市秀山土家族苗族自治縣人民醫院),程鵬(重慶市涪陵中心醫院),杜權(重慶醫科大學附屬第二醫院),杜耘(重慶市人民醫院),杜智勇(陸軍軍醫大學第二附屬醫院),方平(重慶市沙坪壩區人民醫院),傅洪(重慶市急救醫療中心),顧健騰(陸軍軍醫大學第一附屬醫院),黃河(重慶醫科大學附屬第二醫院),江春秀(重慶市人民醫院),雷曉峰(重慶市婦幼保健院),李皓(重慶市云陽縣人民醫院),李洪(陸軍軍醫大學第二附屬醫院),李劍(重慶市合川區人民醫院),李明(重慶市長壽區人民醫院),李月(重慶市黔江中心醫院),劉紅亮(重慶大學附屬腫瘤醫院),劉娟(重慶市奉節縣人民醫院),魯開智(陸軍軍醫大學第一附屬醫院),欒國會(重慶市綦江區人民醫院),閔蘇(重慶醫科大學附屬第一醫院),甯交琳(陸軍軍醫大學第一附屬醫院),彭明清(重慶醫科大學附屬永川醫院),冉興(重慶市潼南區人民醫院),饒傳華(重慶市江津區中心醫院),阮定紅(重慶市大足區人民醫院),邵青(重慶市紅十字會醫院(江北區人民醫院),石先倫(重慶市巴南區人民醫院),王艷冰(重慶市璧山區人民醫院),王震(陸軍特色醫學中心),魏珂(重慶醫科大學附屬第一醫院),先見(重慶市墊江縣人民醫院),謝冕(重慶市中醫院),徐穎(重慶醫科大學附屬兒童醫院),許月明(陸軍第九五八醫院),閆紅(陸軍特色醫學中心),楊仕超(重慶市南川區人民醫院),楊天德(陸軍軍醫大學第二附屬醫院),楊廷軍(重慶市石柱土家族自治縣人民醫院),葉茂(重慶醫科大學附屬兒童醫院),易斌(陸軍軍醫大學第一附屬醫院),余云明(重慶大學附屬三峽醫院),郁蔥(重慶醫科大學附屬口腔醫院),張雪飛(重慶市第五人民醫院),趙敏(重慶市武隆區人民醫院),趙衛兵(重慶市公共衛生醫療救治中心),鄭彬武(重慶市榮昌區人民醫院),鄭曉鑄(重慶市渝北區人民醫院),鐘河江(重慶市西區醫院),朱長江(重慶市九龍坡區人民醫院)
利益沖突:所有作者聲明不存在利益沖突。
我國每年手術近 0.8 億人次[1],其中絕大多數須在術中接受全身麻醉下的機械通氣支持。圍手術期機械通氣可能造成通氣和氣體交換機制受損、局部和全身炎癥反應等而增加術中肺損傷和術后肺部并發癥(postoperative pulmonary complication, PPC)風險[2-3]。研究報道,在接受非心胸手術患者中,肺部感染、肺不張、低氧血癥和呼吸衰竭等 PPC 發生率為 11%~59%[4-5]。圍手術期肺保護性通氣策略已被證實是降低 PPC 的有效措施,相關國際專家共識于 2019 年發布[6]。然而,國內調查性研究顯示,我國麻醉醫生對肺保護性通氣策略的理論認識與臨床實踐存在差異[7-8]。隨著近年來新的臨床證據不斷涌現,有必要制定適合我國麻醉醫生應用的圍手術期機械通氣專家共識,以更好地指導臨床實踐。本專家共識基于當前臨床證據,為成人非心胸手術提供圍手術期機械通氣的臨床實踐推薦。
1 共識制定過程
本共識制定采用改良德爾菲調查法。第 1 步:由四川大學華西醫院余海教授牽頭組建工作小組,該小組包含 3 名主任醫師和 2 名主治醫師,他們來自知名三級甲等醫院心胸麻醉和普外麻醉專業,并且都有超過 10 年的臨床麻醉經驗。工作小組起草了圍手術期機械通氣領域需要達成專家共識的臨床問題,并由 8 名來自成渝地區知名麻醉學教授/主任醫師組成的核心專家團隊進行開放式討論,最終篩選出 18 個擬納入共識的臨床問題。第 2 步:工作小組依據 PICO[研究對象(Participants)、干預措施(Interventions)、對照(Comparisons)和結局(Outcomes)]原則,對每一個問題進行系統的研究證據檢索和總結,形成共識初稿。第 3 步:成都醫學會麻醉專業委員會和重慶市醫學會麻醉專科分會遴選推舉 20 名成員組成專家委員會,推舉標準:在圍手術期機械通氣/麻醉學領域具有豐富經驗以及權威性的專家學者。由專家委員會對共識初稿進行匿名投票并反饋。共識投票方法:參考 Likert 9 級量表,不同意為 1~3 分,不確定為 4~6 分,同意為 7~9 分(1~6 分需給出理由或建議)。證據分級和推薦:按照 GRADE 評分進行總結和評估[9]。根據質量等級,證據被標注為高、中、低和極低,隨后予以推薦強度分級。第 4 步:經過 2 輪匿名反饋調查,每條共識投票同意率>70% 即可納入共識。第 5 步:通過 1 輪專家組集體討論后形成終版共識。具體流程見圖1。
 圖1
專家共識制定流程
圖1
專家共識制定流程
2 共識內容
本共識共形成 28 條關于成人非心胸手術圍手術期機械通氣管理的共識意見(表1)。
2.1 圍手術期機械通氣相關肺損傷的風險評估
圍手術期機械通氣相關肺損傷主要包括容積傷、氣壓傷、萎陷傷、生物傷和剪切傷,其臨床特征為 PPC 風險增加[10-11]:① 容積傷:機械通氣誘發的容積傷來源于高潮氣量通氣,導致肺泡破裂和嚴重氣體外漏(如縱隔氣腫和皮下氣腫);② 氣壓傷:機械通氣導致的氣壓傷來源于肺泡壓或跨肺壓而非氣道壓,高氣道壓力本身并不會導致機械通氣相關肺損傷;③ 萎陷傷:肺泡周期性的塌陷所造成的損傷;④ 生物傷:指局部或廣泛的生物反應,如激活促炎和促損傷的細胞因子級聯反應;⑤ 剪切傷:由于肺泡通氣不均勻產生的區域力學差異誘發了額外的機械應力產生的肺損傷。
2.1.1 危險因素
全面的病史和體格檢查是評估 PPC 風險的關鍵,建議已經建立電子信息化系統的醫療單位將 PPC 危險因素評估量表嵌入術前訪視電子信息化系統。
機械通氣相關肺損傷風險因素包括[6, 12-15]:① 一般狀況:年齡>50 歲,吸煙,美國麻醉醫師協會分級>Ⅱ級,體質量指數>40 kg/m2;② 合并癥:睡眠呼吸暫停綜合征,呼吸系統感染,慢性阻塞性肺疾病(慢阻肺),間質性肺疾病,控制不良的支氣管哮喘,肺高壓,充血性心力衰竭,低白蛋白血癥(血白蛋白<30 g/L),貧血(血紅蛋白<100 g/L),血清尿素氮>300 g/L,以及術前脈搏血氧飽和度(pulse oxygen saturation, SpO2)≤95%;③ 手術因素:手術部位(大血管、上腹部、頭頸及神經外科手術),預計手術時長>2 h 和急診手術。
2.1.2 個體化的優化策略
基于術前 PPC 危險因素評估的優化策略包括[13]:① 改善心肺功能狀態;② 營養支持,糾正貧血、低蛋白血癥;③ 術前教育,包括戒煙 4 周和呼吸功能鍛煉;④ 多學科討論。
2.2 麻醉誘導階段的通氣方法建議
2.2.1 患者體位
麻醉誘導時仰臥位可導致腹部臟器向頭側移位,從而迫使膈肌上移。與仰臥位相比,頭高位可提高給氧去氮的效能,延長呼吸暫停的安全時間[16-17]。尤其是對于肥胖患者,30° 頭高位與仰臥位相比可有效減少功能殘氣量的降低[18]。
2.2.2 誘導期間預充氧
在麻醉誘導時進行預充氧可增加氧儲備。維持呼氣末氧濃度>90% 的高效預充氧是氣管插管過程中預防低氧血癥的關鍵[19]。肺活量呼吸法在至少 10 L/min 的新鮮氣流量下可實現快速預充氧[20]。Nimmagadda 等[21]研究顯示,采用 100% 吸入氧濃度(fraction of inspiratory oxygen, FiO2)進行預充氧時,在 10 L/min 新鮮氣流量下進行 1 min 8 次肺活量呼吸和在 5 L/min 新鮮氣流量下進行 3 min 正常潮氣量呼吸同樣有效。預充氧最重要的潛在并發癥是吸收性肺不張,麻醉誘導后肺不張發生率高達 90%[19]。麻醉誘導以 80% FiO2 預充氧可減少肺不張[22],但會縮短呼吸暫停的安全時間。臨床醫生必須權衡肺不張與呼吸暫停的安全時間縮短的相對風險。對于肥胖患者,與常規面罩預充氧相比,高流量鼻導管吸氧可延長呼吸暫停的安全時間[23]。
2.2.3 誘導期間通氣
麻醉誘導期間可采用手動或機械控制行面罩正壓通氣,必要時可采用雙人正壓通氣。在面罩通氣期間聯合呼氣末正壓(positive end-expiratory pressure, PEEP)可延長呼吸暫停的安全時間,改善氧合[24]。然而,PEEP 的應用或氣道峰壓(peak pressure, Ppeak)>15 cm H2O(1 cm H2O=0.098 kPa)可能會增加胃進氣風險[25-26]。與單獨使用面罩相比,頭高位高流量鼻導管(high-flow nasal cannula, HFNC)可有效延長呼吸暫停的安全時間[27]。該技術可改善二氧化碳清除和增強氧合,但存在胃進氣的風險[28-29]。HFNC 適用于頭頸手術中面罩通氣受限的患者等[30]。誘導期間可根據氣道通暢度置入鼻或口咽通氣裝置來緩解上氣道梗阻,但如果患者存在以下情況則禁忌使用:① 口腔及上下頜骨創傷、咽部氣道占位性病變、喉頭水腫、哮喘、門齒有折斷或脫落危險、頻繁嘔吐;② 鼻息肉、鼻出血傾向、鼻外傷、鼻腔畸形、鼻腔炎癥、明顯的鼻中隔偏曲、凝血功能異常、顱底骨折、腦脊液耳鼻漏等。
2.3 術中機械通氣策略
2.3.1 常用的肺保護性通氣策略
針對機械通氣誘導肺損傷的一系列通氣設置優化措施稱為肺保護性通氣策略。肺保護性通氣策略是改善全身麻醉后肺部結局的有效措施,相比于傳統的通氣方式可減少機械通氣相關肺損傷、改善肺功能、降低 PPC 發生率和死亡率[31]。
① 經典的肺保護性通氣策略主要包含小潮氣量、適當的 PEEP、肺復張和低平臺壓等(詳見 2.3.3~2.3.5 節描述)。
② 肺開放通氣策略[32]:肺開放通氣是一種結合了小潮氣量、肺復張和個體化 PEEP 滴定的聯合策略。該策略強調盡可能打開塌陷的肺泡和維持其復張。
③ 驅動壓導向通氣策略[33]:驅動壓是促使肺泡開放的壓力,代表肺實質在整個吸氣過程中受到的壓力。驅動壓是氣道平臺壓(plateau pressure, Pplat)與 PEEP 的差值(Pplat–PEEP),<13 cm H2O 可降低 PPC 發生風險。
④ 機械功率導向通氣策略:機械功率是呼吸機維持通氣所做的功,是傳遞給呼吸系統和肺的能量總和。機械功率(J/min)計算為 0.098×RR×VT×[PEEP+(Pplat–PEEP)/2+(Ppeak–Pplat)],其中 RR 表示呼吸頻率,VT 表示潮氣量。較高的機械功率與患者術后呼吸衰竭發生率、死亡率有關,但目前暫缺乏機械功率最佳值的證據[34]。
2.3.2 術中機械通氣的通氣模式
目前常用的術中機械通氣模式包括容量控制通氣(volume-controlled ventilation, VCV)、壓力控制通氣(pressure-controlled ventilation, PCV)、壓力控制-容量保證通氣(pressure-control with volume guaranteed ventilation, PCV-VG)。VCV 也稱容量限制通氣或容量循環通氣,呼吸機以恒定流量傳送潮氣量。在 PCV 模式下,呼吸機可在吸氣相維持恒定壓力,同時流量逐漸降低。PCV-VG 具有 PCV 的優勢,同時根據患者肺順應性的變化保障設置的最低潮氣量。雖然研究發現 PCV 和 PCV-VG 模式下 Ppeak 更低、肺順應性更好,但由于臨床結局的相似性,實現肺保護性通氣的最佳通氣模式選擇尚無定論[35-36]。近期的研究發現,在接受腹部手術和心胸手術的患者中,通氣方式的選擇并未降低 PPC 風險[37-38]。常用的通氣模式特點見圖2。
 圖2
常用的通氣模式特點
圖2
常用的通氣模式特點
VCV:容量控制通氣;PCV:壓力控制通氣;PCV-VG:壓力控制-容量保證通氣
2.3.3 術中機械通氣的潮氣量
術中以小潮氣量(6~8 mL/kg)通氣是肺保護性通氣策略的重要組成部分。多項高質量研究證實,設定小潮氣量通氣能減少肺擴張傷和肺部感染等 PPC[39-40]。但需要注意的是,在小潮氣量通氣期間,應聯合 PEEP 和肺復張來改善肺順應性和防止肺不張[11]。
肺容積主要由性別和身高決定,建議以患者的預測體重來確定潮氣量[41]。推薦的預測體重公式為男性:50.0+0.905×(身高–152.4),女性:45.5+0.905×(身高–152.4)[42]。為方便應用,可將公式簡化為 0.91×(身高–152.4)+50/45.5。
2.3.4 術中機械通氣的 PEEP
PEEP 是指在機械通氣呼氣末時維持一定水平的正壓,使肺泡壓高于大氣壓。PEEP 可通過增加肺再通氣、促塌陷肺區域開放、增加氣體交換面積和減少肺內分流從而提高氧合。
多項研究表明 5~10 cm H2O 水平的 PEEP 可以優化通氣生理、改善肺功能和降低肺不張風險[31, 39],過低(≤2 cm H2O)或過高(≥12 cm H2O)的 PEEP 則無益[43-44],但其最佳水平沒有定論。推薦個體化的 PEEP 滴定,即根據驅動壓、動脈氧分壓、氧合指數、SpO2、肺順應性和/或肺超聲來調整[45]。滴定個體化 PEEP 水平采用遞增法,從 2 cm H2O 開始,每次呼吸周期遞增 2 cm H2O,在觀測到最低驅動壓、最佳氧合、最高順應性或最少肺不張時獲得個體化 PEEP 水平,如有條件,可在床旁肺超聲或胸電阻抗成像技術(electrical impedance tomography, EIT)監測下進行[46-50]。個體化 PEEP 滴定受限于各醫學中心設備和麻醉醫生掌握程度。以驅動壓為導向的 PEEP 滴定法提示大部分手術患者的最佳 PEEP 范圍為 5~8 cm H2O。基于現有的臨床證據,建議可應用 5~8 cm H2O PEEP,且應在低氧、氧合指數下降或肺順應性降低時予以個體化滴定調整。PEEP 滴定或高水平 PEEP 維持期間需關注其對循環的負面影響,通常表現為低血壓。
2.3.5 術中機械通氣的肺復張策略
肺復張指對于接受機械通氣的患者應用持續增加或維持較高的短暫正壓通氣使塌陷肺泡擴張,從而改善局部通氣、促進肺泡再灌注和增大有效通氣區域,達到逆轉肺不張和提高氧合的目的。
現有證據表明,對于非肥胖患者,肺復張的持續正壓應達到 30~40 cm H2O,對于肥胖患者須達到 40~45 cm H2O[51-53]。在實施肺復張時,應保持能維持 SpO2≥90% 的最低 FiO2 即可。肺復張可通過手控或機控兩種方法完成,更推薦機控通氣下的肺復張以達到均勻擴張肺泡和降低血流動力學紊亂風險的目的。手控肺復張指在麻醉機手控狀態下調節逸氣閥到 30~40 cm H2O 后,持續擠壓儲氣囊維持 15~30 s。機控肺復張包括 VCV 和 PCV 模式下的操作,需先設置吸呼比為 1∶1、呼吸頻率 6~8 次/min 和峰壓限制為 45 cm H2O。VCV 模式下,PEEP 設置 10~12 cm H2O,潮氣量從 6~8 mL/kg 開始,每 3~6 次呼吸增加 4 mL/kg,直至達到平臺壓 30~40 cm H2O,維持 3~6 次呼吸后完成肺復張,如潮氣量達到麻醉機上限仍無法實現目標平臺壓,則增加 PEEP。PCV 模式下,吸氣壓力從 15~20 cm H2O 開始,每 3~6 次呼吸 PEEP 增加 5 cm H2O,直至達到平臺壓 30~40 cm H2O,維持 3~6 次呼吸后完成肺復張[44, 53-54]。
肺復張的實施節點和頻率目前沒有定論,研究發現每小時進行肺復張并不降低 PPC 風險[44]。推薦至少在氣管插管后和氣管拔管前各進行 1 次。如術中出現氧合下降,應在排除通氣不足、分泌物阻塞等原因后進行 1~2 次肺復張,以排除和治療肺不張引起的低氧血癥。
肺復張策略對于肺泡再灌注的效果可通過壓力-容量曲線、氧合指數、床旁肺超聲或/和 EIT 監測[55-56]。在肺復張結束后應立即恢復小潮氣量和 PEEP 設置。肺復張可導致靜脈回流受阻、右心房壓升高和心排出量下降,特別是在機體容量欠缺的時候。因此在進行肺復張時,應密切關注血壓的波動,在血壓明顯降低時應暫停操作[57]。
2.3.6 術中機械通氣的吸呼比、呼吸頻率和呼氣末二氧化碳分壓(end-tidal carbon dioxide, ETCO2)
吸呼比推薦常規設置為 1∶2,這與正常呼吸生理相似。有數項研究表明,延長吸氣時間的等比通氣(吸呼比 1∶1)可改善腔鏡手術中的氧合、減少生理性呼吸死腔、降低 Ppeak 和 Pplat[58-61]。其潛在機制是吸氣時間延長可升高平均氣道力,吸氣流量減慢致氣體在肺內分布改善,以及由于呼氣時間短而產生內源性 PEEP。因此,在腔鏡手術等特殊手術人群,可以根據情況適當延長吸氣時間。Meta 分析顯示,反比通氣[吸呼比(1~4)∶1]可降低 Ppeak 和改善動態順應性[62],但應根據臨床情況采用。
機械通氣中呼吸頻率推薦常規設置為 8~12 次/min,并調整以維持正常的 ETCO2 水平。在聯合小潮氣量通氣的腔鏡手術中,為避免 ETCO2 過高,可能需要較快的呼吸頻率(12~18 次/min)。為避免快呼吸頻率導致的呼吸疊加和內源性 PEEP 過高,不建議呼吸頻率超過 18~20 次/min。
2.3.7 術中機械通氣的 FiO2 和新鮮氣流量
術中超出生理范圍的過量氧供應不僅對肺有直接毒性作用,還會促心肺腦血管收縮、炎癥反應和氧化應激[63-65]。高 FiO2 與肺不張等 PPC 風險增高相關,并可能增高術后死亡率[66-67]。30%~50% FiO2 可降低手術患者術后肺不張風險[68-70]。推薦在沒有低氧血癥的情況下,維持術中 FiO2≤40%。
常規新鮮氣流量為 1~2 L/min,在部分吸入麻醉和小兒麻醉中可能用到低新鮮氣流量(1 L/min),不建議常規應用高新鮮氣流量(≥3 L/min)。
2.3.8 術中通氣相關的監測建議
① 呼吸動力學監測:良好的呼吸動力學監測可以改善患者肺順應性和氧合。建議術中持續監測重要呼吸參數,包括潮氣量、Ppeak、Pplat、吸呼比和肺順應性,如有條件可監測平均氣道壓、壓力-容量曲線等。
② 呼氣末二氧化碳的監測:建議術中連續監測 ETCO2 的數值和波形,不僅可判斷氣管導管的位置,還反映肺通氣和肺血流,其正常值為 35~45 mm Hg(1 mm Hg=0.133 kPa)。
③ FiO2 監測:全身麻醉期間應常規監測 FiO2,具體見 2.3.7。
④ 氧合指數監測:術中監測 SpO2 的同時,對某些患者還需要進行氧合指數的監測,正常值應≥300 mm Hg。如果術中出現低于 300 mm Hg 的狀況,應快速進行病因分析和對癥處理。由于氧合指數受溫度、貧血、內環境等影響,需要綜合考慮分析。
⑤ 床旁肺超聲:圍手術期肺不張病變范圍和程度較輕,胸部 X 線片不易診斷,而診斷肺不張的金標準胸部 CT 依賴于特定的場所和設備,在手術中難以實現。肺超聲對圍手術期肺不張的診斷準確率與 CT 相似度約為 90%[71],能夠在術中實時監測肺不張、胸腔積液、氣胸等重要征象[72],可在減少射線暴露的情況下指導機械通氣。建議在有條件的醫療單位,麻醉醫師應接受肺超聲技術系統培訓。
⑥ EIT:EIT 是一種床旁、無創、無輻射的肺通氣監測技術,主要原理是根據肺組織的生物導電性因含氣量不同而存在差異的原理,通過局部電極感應呼吸過程中胸腔生物電阻抗變化,再利用相應的成像算法監測肺不同區域內通氣功能的狀態。EIT 還可用于指導實時肺復張、個體化 PEEP 設定和確立最佳通氣策略[46, 73]。
⑦ 通氣血流比(ventilation/perfusion ratio, V/Q)監測:術中 V/Q 失調可能會增加非心臟大手術的患者術后 PPC 風險,但是由于床旁評估 V/Q 的自動肺參數估計技術依賴特殊設備,臨床應用尚存在一定困難[74]。
2.4 麻醉蘇醒期通氣相關建議
麻醉蘇醒期指從手術結束時停止使用麻醉藥和輔助藥物后,意識呼吸逐漸恢復的時期。氣管拔管前患者需經歷從機械通氣到自主呼吸的轉換,這過程中通氣模式的選擇有間歇手控輔助通氣、機控通氣、同步間歇指令通氣(synchronized intermittent mandatory ventilation, SIMV)和壓力支持通氣(pressure support ventilation, PSV)模式等。對于全身麻醉患者的蘇醒期氣管拔管前機械通氣模式,目前尚無定論。SIMV 模式在機控呼吸與自主呼吸同步的基礎上提供設定的呼吸頻率和潮氣量,可與 PCV、PSV 模式同時應用。PSV 模式可單獨應用于已有自主呼吸的患者來提供壓力輔助通氣。SIMV 和 PSV 均可減少呼吸功、抵消麻醉藥物的呼吸抑制作用,以及在撤機前進行支持通氣。為促進帶管順應和減少不均勻通氣導致的肺不張等,我們建議如有條件,應在蘇醒階段采用 SIMV(無論有無自主呼吸)或 PSV(有自主呼吸)[75-76],否則仍繼續機控通氣。氣管拔管前應避免通過中斷通氣讓二氧化碳蓄積刺激自主呼吸恢復,因為呼吸暫停與肺泡塌陷相關,可能引起肺不張。
建議麻醉蘇醒階段氣管拔管前進行輔助給氧,以預防氣管拔管后低氧。但是,氣管拔管前即使短暫地給予高 FiO2 也可能產生吸收性肺不張[77]。因此,根據目前的證據,我們建議避免在氣管拔管前應用高 FiO2,30%~40% FiO2 即能在提供保證氧合的同時減少肺不張[68, 77-78]。
拔管時維持 30° 頭高位可顯著降低上腹部手術患者術后低氧血癥的發生[79]。推薦常規通過鼻導管吸入低流量氧氣(2~3 L/min,FiO2≤40%)行常規氧療維持 SpO2 ≥95%。
對低氧血癥高風險患者和肥胖患者,建議蘇醒期機控通氣時常規給予 PEEP,氣管拔管后給予持續氣道正壓通氣和 HFNC 氧療以改善氧合和降低低氧血癥風險[80-84]。有研究建議對 PPC 高風險患者實施無創間歇正壓通氣,但該技術并未降低 PPC 發生率[85],此結論尚存在爭議[86]。
近年,有研究提出采用無創的 SpO2/FiO2 比作為低氧血癥篩查的評估。SpO2/FiO2 和氧合指數具有良好的相關性,當 SpO2/FiO2<370 可能需要轉入重癥監護病房;SpO2/FiO2 在 370~450 需要進一步的臨床評估和動脈血氣檢查;SpO2/FiO2>450 時,可轉入普通病房[87]。需要注意的是,術后蘇醒期不同的吸氧裝置可達的氧濃度不同,具體參照表2[88]。
2.5 特殊患者通氣建議
2.5.1 肥胖患者的通氣建議
肥胖患者的呼吸系統順應性降低、膈肌升高、肺活量下降、肺容量減少伴肺不張增加、小氣道閉合、阻力增加,并存在較高的腹內壓導致限制性通氣障礙,因此是 PPC 發病的高危人群。研究證實肺保護性通氣策略可減少肥胖患者的通氣相關肺損傷[89]。研究指出術中維持≥10 cm H2O 的 PEEP 可以顯著降低肥胖患者 PPC 的發生率[90],但最佳 PEEP 值尚無定論,設置 PEEP 可能需要個體化,并根據患者和手術情況進行調整[44, 91]。肥胖患者還應該適當提高呼吸頻率,因為肥胖患者的二氧化碳產生過多,會繼發于高耗氧量,引起呼吸功增加[92]。
2.5.2 合并常見呼吸系統疾病患者的通氣建議
① 支氣管哮喘/支氣管痙攣。支氣管哮喘患者在圍手術期發生支氣管痙攣的風險高達 4.2%[93]。研究表明,手術前近 3 個月內未控制的哮喘患者術后死亡率是健康患者的 2 倍,術后肺炎發生率為健康患者的 3 倍[94]。建議對合并哮喘患者的呼吸功能和哮喘控制情況進行準確的臨床評估,并根據患者哮喘控制情況、手術緊急程度、術前干預方案等評估哮喘患者在全身麻醉中發生支氣管痙攣的危險程度,以制定相應的麻醉計劃。術中一旦發生支氣管痙攣,應立即消除刺激因素、加深麻醉、給予 β2 受體激動劑等。機械通氣中應注意提供足夠長的呼氣時間以避免內源性 PEEP,這可以通過使用比平時更小的潮氣量來實現[95]。此外,目前尚無證據支持任一通氣模式在哮喘患者中的應用,但應用 VCV 模式時可直接監測 Ppeak 和 Pplat[96],必要時手控通氣以克服氣道阻力所致的通氣不足。
② 慢阻肺。慢阻肺是一種以持續性氣流受限為病理特征的呼吸系統疾病,是 PPC 的獨立危險因素。對于慢阻肺患者需綜合手術緊急程度和患者病情制定麻醉方案,盡可能避免氣管插管的全身麻醉,必要時可進行多學科討論。此類患者術中最優通氣模式的選擇尚無定論,目前認為 PCV-VG 模式可降低肺氣壓傷風險、有利于術后肺功能恢復[97-98]。術中通氣推薦如下:A. 推薦慢阻肺患者采用小潮氣量(6~8 mL/kg 預測體重)通氣以減少機械通氣相關肺損傷和預防過度通氣[99]。B. 在機械通氣過程中,允許充分的呼氣,建議選擇較低的呼吸頻率,如 6~10 次/min。C. 在血液動力學穩定的人群中,允許適當的高碳酸血癥。在降低呼吸頻率、允許性高碳酸血癥、調節吸呼比等更基本的干預措施仍無法改善患者氧合時,可在有豐富經驗的上級醫師指導下適當提高吸氣峰壓[100]。D. 對慢阻肺患者應用 PEEP 可在呼氣末保持小氣道開放,改善與呼吸肌的相互作用和減少呼吸做功。E. 建議對于慢阻肺患者,外源性 PEEP 應接近 80%~85% 或等于可測得的內源性 PEEP 值[100]。但在臨床工作中,內源性 PEEP 值的測定存在困難,建議采用個體化 PEEP 設定。有條件的單位可以采用 EIT 指導確定 PEEP 水平。
③ 急性肺損傷(acute lung injury, ALI)/急性呼吸窘迫綜合征(acute respiratory distress syndrome, ARDS)。ALI/ARDS 是由多種因素誘導全身系統炎性疾病的肺部表現。肺保護性通氣是治療 ARDS 的有效手段,應早期給予小潮氣量(6 mL/kg)、PEEP>5 cm H2O 并維持平臺壓<30 cm H2O,有條件的情況下應個體化設置 PEEP。肺復張操作應謹慎使用,注意其對循環的影響[101]。對于 ALI/ARDS 患者術中機械通氣的設定,證據有限,建議參照 ARDS 管理指南的推薦[101]。
2.5.3 俯臥位患者的通氣建議
俯臥位患者的胸腔壓力分布更均勻,重度依賴區肺泡更容易張開,且俯臥位減少縱隔和心臟對背側組織的壓力,利于肺復張。對于俯臥位患者,建議給予肺保護性通氣(小潮氣量、5 cm H2O PEEP 和肺復張)可降低氣壓傷風險、減少肺部炎癥和改善術后氧合的同時不增加心血管事件[102-103]。此外,有研究表明 PCV 模式更有利于降低短期術后白細胞介素-6 和 C 反應蛋白水平及術后 PPC 的發生率[104],可能提供更理想的通氣參數[105]。
2.5.4 頭低足高位患者的通氣建議
頭低足高位(Trendelenburg)手術時,患者的腹腔臟器向頭端移動造成腹內壓增高,導致膈肌上移、胸內壓升高、肺泡擴張受限和氣道阻力增大等。推薦采用肺保護性通氣策略以改善術中氧合和減少機械通氣相關肺損傷[106]。另外可以考慮稍高水平 PEEP(>10 cm H2O)有利于減少肺不張[107],但須保持循環穩定。
3 小結
圍手術期肺保護性通氣策略可降低 PPC 風險,改善患者預后。本專家共識共形成 28 條關于成人非心胸手術圍手術期機械通氣的具有中-高級證據質量和專家強烈支持的推薦和聲明,是針對這一領域臨床證據的更新。本專家共識總結并評價了最新圍手術期機械通氣管理策略,對成人非心胸手術患者圍手術期機械通氣臨床實踐極具參考價值。
執筆人:孫琪榮(四川大學華西醫院),李雪霏(四川大學華西醫院),崔宇(電子科技大學附屬成都市婦女兒童中心醫院)
專家名單(按姓氏漢語拼音排序):
成都醫學會麻醉專業委員會專家名單:陳峰(都江堰市人民醫院),陳軍(彭州市人民醫院),鄧婉欣(成都市龍泉驛區第一人民醫院),丁孝東(四川天府新區人民醫院),董蜀華(成都醫學院),杜智(成都市新津區人民醫院),范丹(四川省人民醫院),付強(成都市第三人民醫院),郭浪濤(成都市婦女兒童中心醫院),何斌(成都大學附屬醫院),何崎(成都體育學院附屬體育醫院),吉陽(四川大學華西口腔醫院),賈飛(成都市錦江區婦幼保健院),姜春玲(四川大學華西醫院),亢平(成都市公共衛生臨床醫療中心),李德遠(金堂縣第一人民醫院),李佳(成都市中西醫結合醫院),李軍祥(成都市郫都區人民醫院),李俊芳(蒲江縣人民醫院),李茜(四川大學華西醫院),李祥奎(四川省人民醫院),李曉強(四川大學華西醫院),李永榮(四川華美紫馨醫學美容醫院),劉建波(大邑縣人民醫院),劉琉(成都中醫藥大學附屬醫院),劉永峰(邛崍市醫療中心醫院),羅東(四川大學華西第二醫院),羅化全(崇州市中醫醫院),羅小偉(成都市新都區中醫醫院),歐珊(成都市中西醫結合醫院),齊鵬亮(成都市第六人民醫院),舒家云(成都新都區人民醫院),孫燕(成都市第二人民醫院),孫陽陽(中國人民解放軍西部戰區總醫院),唐東(西藏自治區人民政府駐成都辦事處醫院),唐勇(四川錦欣婦女兒童醫院),陶勇(成都市雙流區第一人民醫院),王麗(成都醫學院第一附屬醫院),王雄(成都大學附屬醫院),王宇(三六三醫院),魏新川(四川大學華西第二醫院),溫開蘭(四川省人民醫院),肖勝(成都市武侯區人民醫院),謝先豐(成都市第二人民醫院),楊岸(簡陽市人民醫院),姚富(四川省骨科醫院),易明亮(成都市第五人民醫院),余海(四川大學華西醫院),袁川(成都市雙流區中醫醫院),張涵(崇州市人民醫院),張科(核工業四一六醫院),趙澤宇(四川省八一康復中心),鐘惠(成都市第七人民醫院),周激(成都新麗美醫療美容醫院),鄒江(四川省腫瘤醫院)
重慶市醫學會麻醉專科分會專家名單:白福海(陸軍軍醫大學第二附屬醫院),曹俊(重慶醫科大學附屬第一醫院),陳朝華(重慶市銅梁區人民醫院),陳理紅(重慶市第九人民醫院),陳力勇(陸軍特色醫學中心),程璐(重慶市秀山土家族苗族自治縣人民醫院),程鵬(重慶市涪陵中心醫院),杜權(重慶醫科大學附屬第二醫院),杜耘(重慶市人民醫院),杜智勇(陸軍軍醫大學第二附屬醫院),方平(重慶市沙坪壩區人民醫院),傅洪(重慶市急救醫療中心),顧健騰(陸軍軍醫大學第一附屬醫院),黃河(重慶醫科大學附屬第二醫院),江春秀(重慶市人民醫院),雷曉峰(重慶市婦幼保健院),李皓(重慶市云陽縣人民醫院),李洪(陸軍軍醫大學第二附屬醫院),李劍(重慶市合川區人民醫院),李明(重慶市長壽區人民醫院),李月(重慶市黔江中心醫院),劉紅亮(重慶大學附屬腫瘤醫院),劉娟(重慶市奉節縣人民醫院),魯開智(陸軍軍醫大學第一附屬醫院),欒國會(重慶市綦江區人民醫院),閔蘇(重慶醫科大學附屬第一醫院),甯交琳(陸軍軍醫大學第一附屬醫院),彭明清(重慶醫科大學附屬永川醫院),冉興(重慶市潼南區人民醫院),饒傳華(重慶市江津區中心醫院),阮定紅(重慶市大足區人民醫院),邵青(重慶市紅十字會醫院(江北區人民醫院),石先倫(重慶市巴南區人民醫院),王艷冰(重慶市璧山區人民醫院),王震(陸軍特色醫學中心),魏珂(重慶醫科大學附屬第一醫院),先見(重慶市墊江縣人民醫院),謝冕(重慶市中醫院),徐穎(重慶醫科大學附屬兒童醫院),許月明(陸軍第九五八醫院),閆紅(陸軍特色醫學中心),楊仕超(重慶市南川區人民醫院),楊天德(陸軍軍醫大學第二附屬醫院),楊廷軍(重慶市石柱土家族自治縣人民醫院),葉茂(重慶醫科大學附屬兒童醫院),易斌(陸軍軍醫大學第一附屬醫院),余云明(重慶大學附屬三峽醫院),郁蔥(重慶醫科大學附屬口腔醫院),張雪飛(重慶市第五人民醫院),趙敏(重慶市武隆區人民醫院),趙衛兵(重慶市公共衛生醫療救治中心),鄭彬武(重慶市榮昌區人民醫院),鄭曉鑄(重慶市渝北區人民醫院),鐘河江(重慶市西區醫院),朱長江(重慶市九龍坡區人民醫院)
利益沖突:所有作者聲明不存在利益沖突。