報道1例乳腺癌肺轉移32歲女性患者,以單發純磨玻璃結節(ground-glass opacity,GGO)病變為表現。雖然術前診斷不準確,但患者接受了合理的術前檢查和手術治療。由于不同的治療策略和目的,區分非典型轉移瘤與原發癌是至關重要的。因此,如果在CT上發現新的GGO,有惡性腫瘤史的患者應考慮有轉移可能性。此外,應適當縮短CT隨訪間隔,根據多學科團隊建議進行術前檢查和手術治療。
引用本文: 敬濤, 宋鐵牛, 魏小平, 馮海明, 張少博, 王成, 蔣鵬, 李斌. 單發純磨玻璃結節為表現的肺轉移癌一例. 中國胸心血管外科臨床雜志, 2024, 31(3): 485-488. doi: 10.7507/1007-4848.202207003 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
隨著健康體檢意識的增強和低劑量螺旋CT應用的增多,磨玻璃結節(ground-glass opacity,GGO)的檢出率逐年增高[1],尤其是純GGO極少表現為轉移瘤。肺是乳腺癌常見的轉移部位,可表現為單發或多發結節、淋巴管炎或彌漫性間質增厚[2]。然而,GGO是一種罕見的肺轉移形態,可能被誤診為早期肺腺癌、間質性肺炎或病毒感染等,如果我們不能區分原發或轉移性病變,就無法制定準確的治療策略。GGO是一種非特異性的影像學表現,見于許多涉及不同臨床疾病的病理過程。GGO在影像上可表現為肺泡腔變實改變,也可表現為肺間質改變、肺泡壁內細胞數量增加、液體增多等。除了早期肺腺癌或不典型腺瘤樣增生外,GGO可能是肺部病毒感染(如COVID-19)、肺水腫伴間質積液、斑片狀肺實質水腫或間質性疾病的表現[3],但很少表現為轉移癌。實體惡性腫瘤的肺轉移類型通常為多發結節或腫塊、淋巴管炎或彌漫性間質增厚[2],而表現為單發GGO較為少見。本文報道1例乳腺癌肺轉移表現為單發GGO患者。
臨床資料 患者,女,32歲,2018年10月發現右側乳腺包塊,乳腺CT示右側乳房外上象限見 21 mm×20 mm腫塊,周圍呈不規則狀、毛刺樣改變(圖1a),行B超引導下腫瘤及腋窩淋巴結穿刺,穿刺病理示乳腺浸潤性導管癌(圖2a~b),免疫組化結果(圖2c~d):雌激素受體(ER,>80%強+),孕激素受體(PR,20%弱-中等+),人表皮生長因子受體2(CerbB2,2+),拓撲異構酶Ⅱ(Top-2,2+),細胞角蛋白5(CK5,–),E-鈣粘蛋白(E-Cadherin,+),Ki-67(>20%),P120(胞膜+),P63(–),雌激素調節蛋白(pS2,–);Fish檢測HER-2為陰性。腋窩淋巴結可見腺癌細胞轉移。全身檢查(頭、胸、腹CT,骨掃描)未見遠處轉移,給予2個周期多西他賽+表柔比星+環磷酰胺新輔助化療1個月后,行保留乳頭乳暈右側乳腺腺體切除術+腋窩淋巴結采樣+乳腺假體植入術。術后繼續給予多西他賽+表柔比星+環磷酰胺方案術后輔助化療4個周期,2019年7月采用亮丙瑞林+阿那曲唑內分泌治療并每3個月復查。2021年7月胸部CT未見肺部異常病灶(圖1b),而5個月后胸部CT發現右肺下葉后基底段純GGO,大小20 mm×22 mm×20 mm(圖1c),縱隔淋巴結未見明顯增大,術前考慮早期肺腺癌可能性大,頭顱磁共振成像、腹部CT及全身骨顯像未見轉移,B超檢查腋窩及頸部未見增大淋巴結。2022年1月行胸腔鏡肺段切除術,術中病理檢查回報乳腺癌肺轉移,遂行縱隔淋巴結采樣術。術后病理為肺浸潤性導管癌侵犯,切緣未見癌殘留,脈管腔內見瘤栓(圖3a~b),免疫組化染色(圖3c~d):細胞角蛋白7(CK7,–),細胞角蛋白20(CK20,–),絨毛蛋白(Villin,–),轉錄因子GATA3(+),乳腺珠蛋白(Mammaglobin,–),甲狀腺轉錄因子-1(TTF-1,–),P40(–),突觸素(Syn,–),Ki-67(30%+),2、4、7、8、9、10、12組淋巴結見癌轉移;患者術后1個月給予白蛋白紫杉醇300 mg+卡培他濱1.5 g維持化療中,2022年7月復查胸部CT(圖1d),RECIST評分為病情穩定。
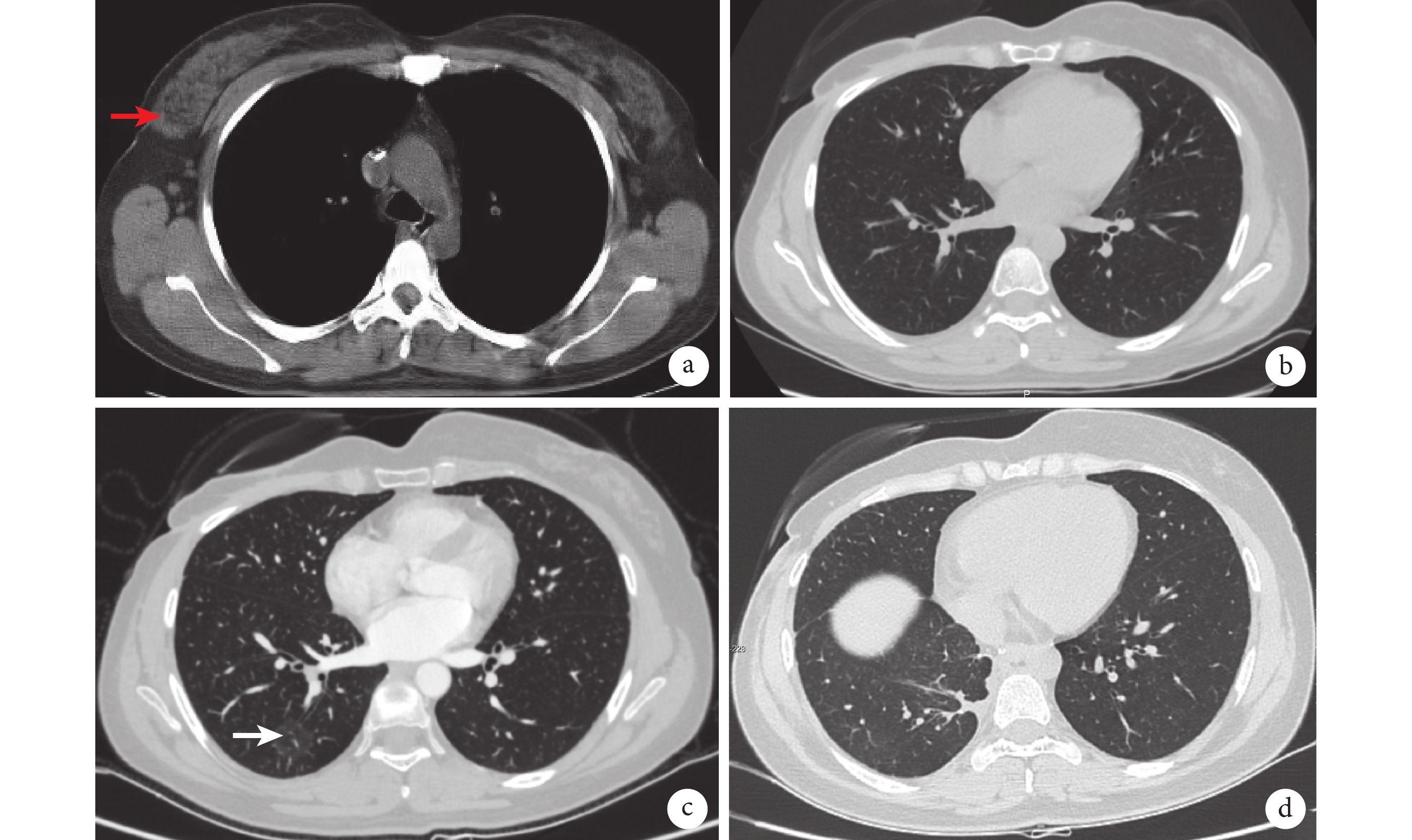 圖1
乳腺 CT
圖1
乳腺 CT
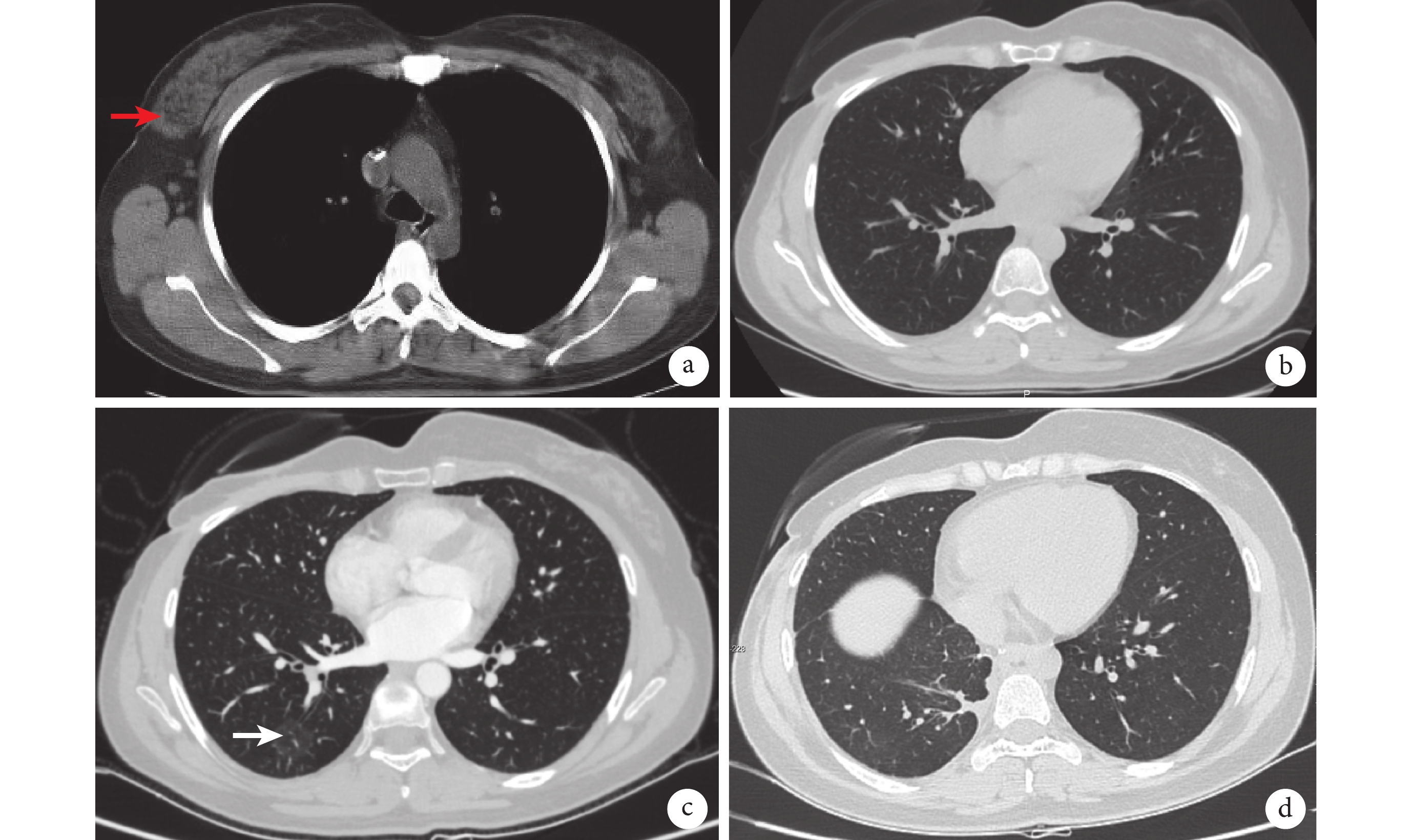
a:乳腺外上象限可見大小約 21 mm×20 mm 低密度腫塊影(紅色箭頭);b:乳腺癌術后 25 個月復查胸部 CT 未見異常;c:乳腺癌術后31個月的胸部 CT 可見右肺下葉純磨玻璃結節影(白色箭頭);d:胸腔鏡肺段切除術后復查
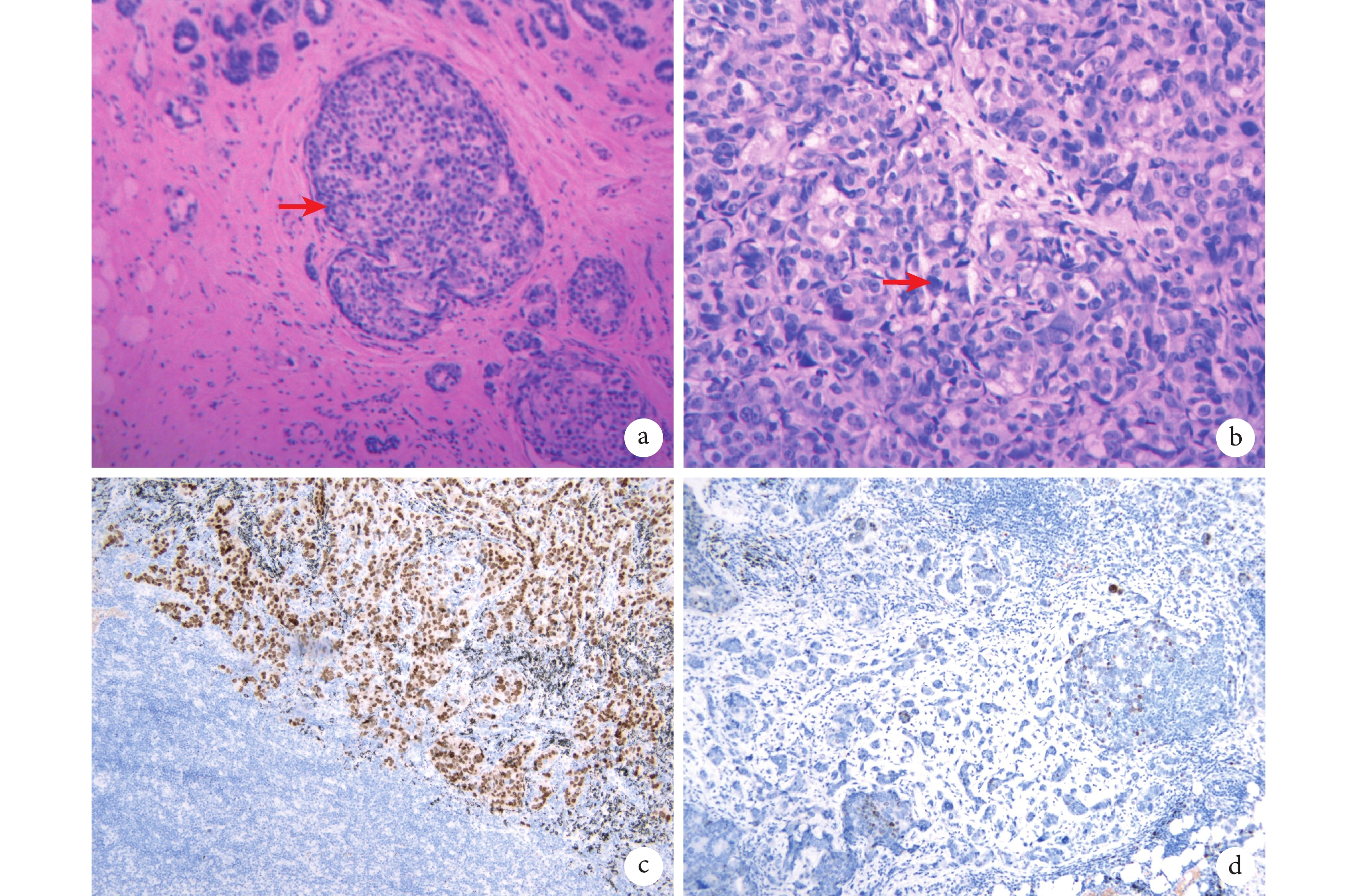 圖2
術前穿刺病理和免疫組化結果
圖2
術前穿刺病理和免疫組化結果
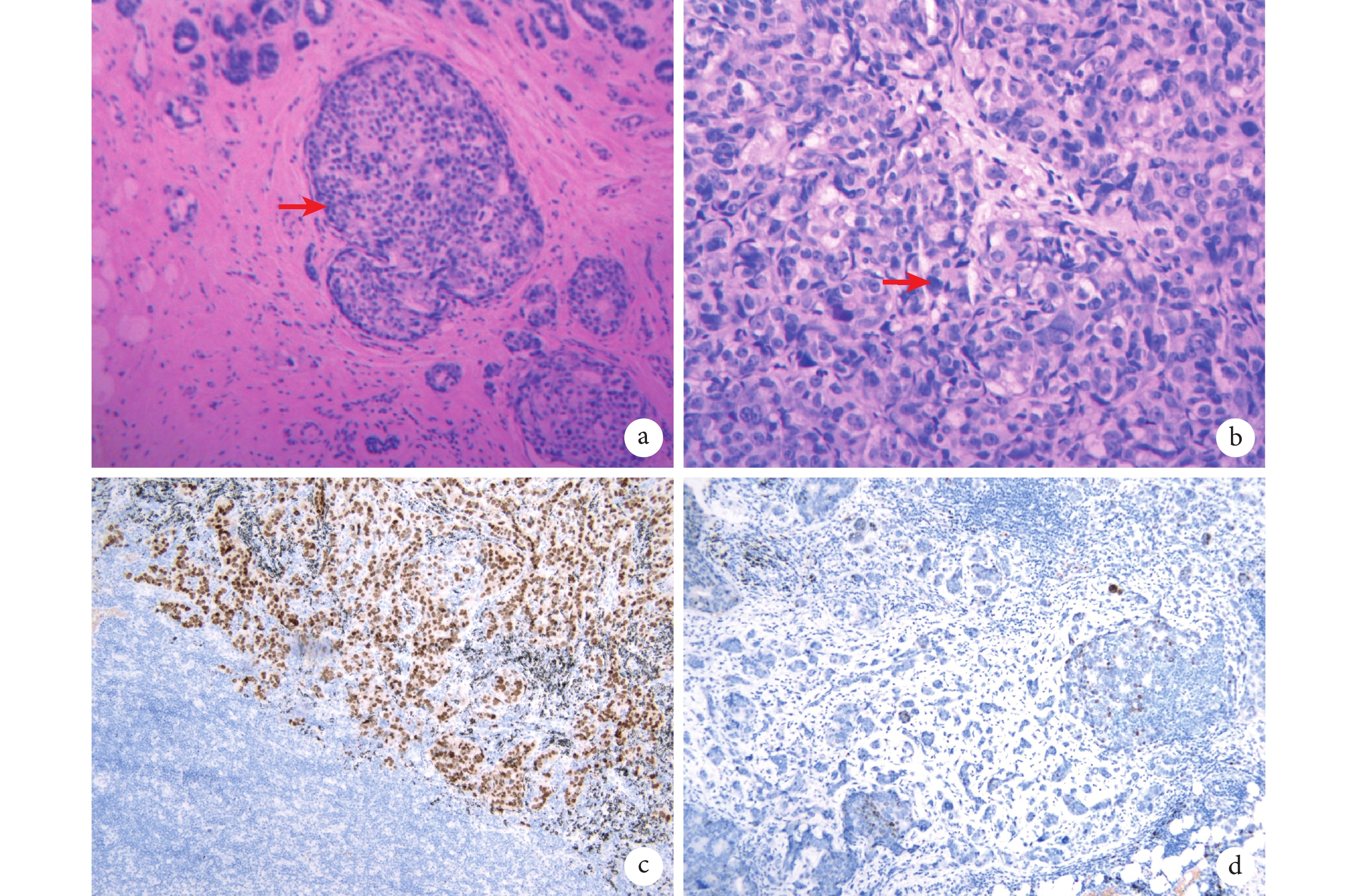
a:癌細胞充滿乳腺導管(紅色箭頭,HE 染色,×100);b:核大深染癌細胞的聚集(紅色箭頭,HE 染色,×200);c:雌激素受體免疫組化結果;d:細胞角蛋白免疫組化結果;HE:蘇木素-伊紅
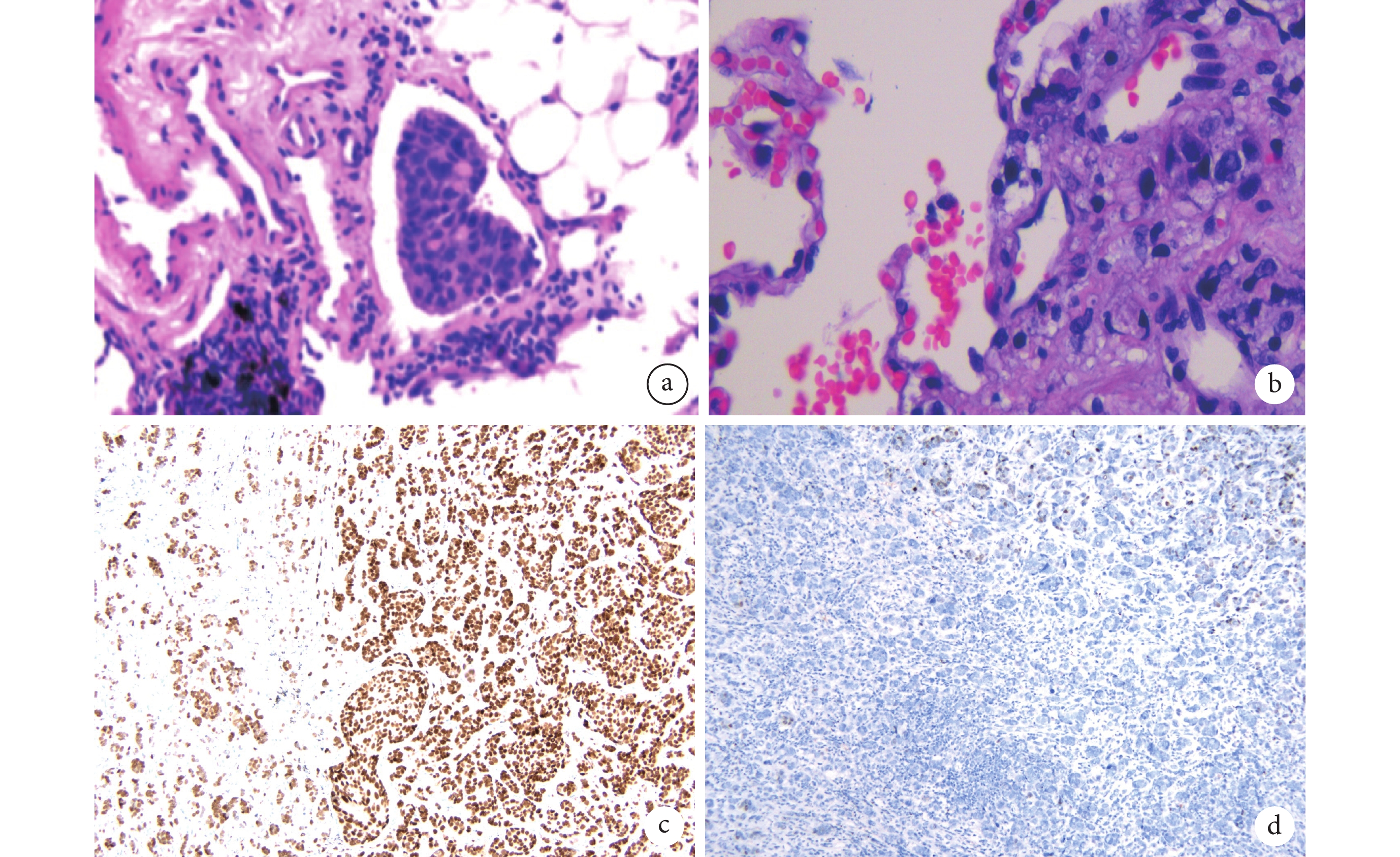 圖3
術中病理檢查和免疫組化結果
圖3
術中病理檢查和免疫組化結果
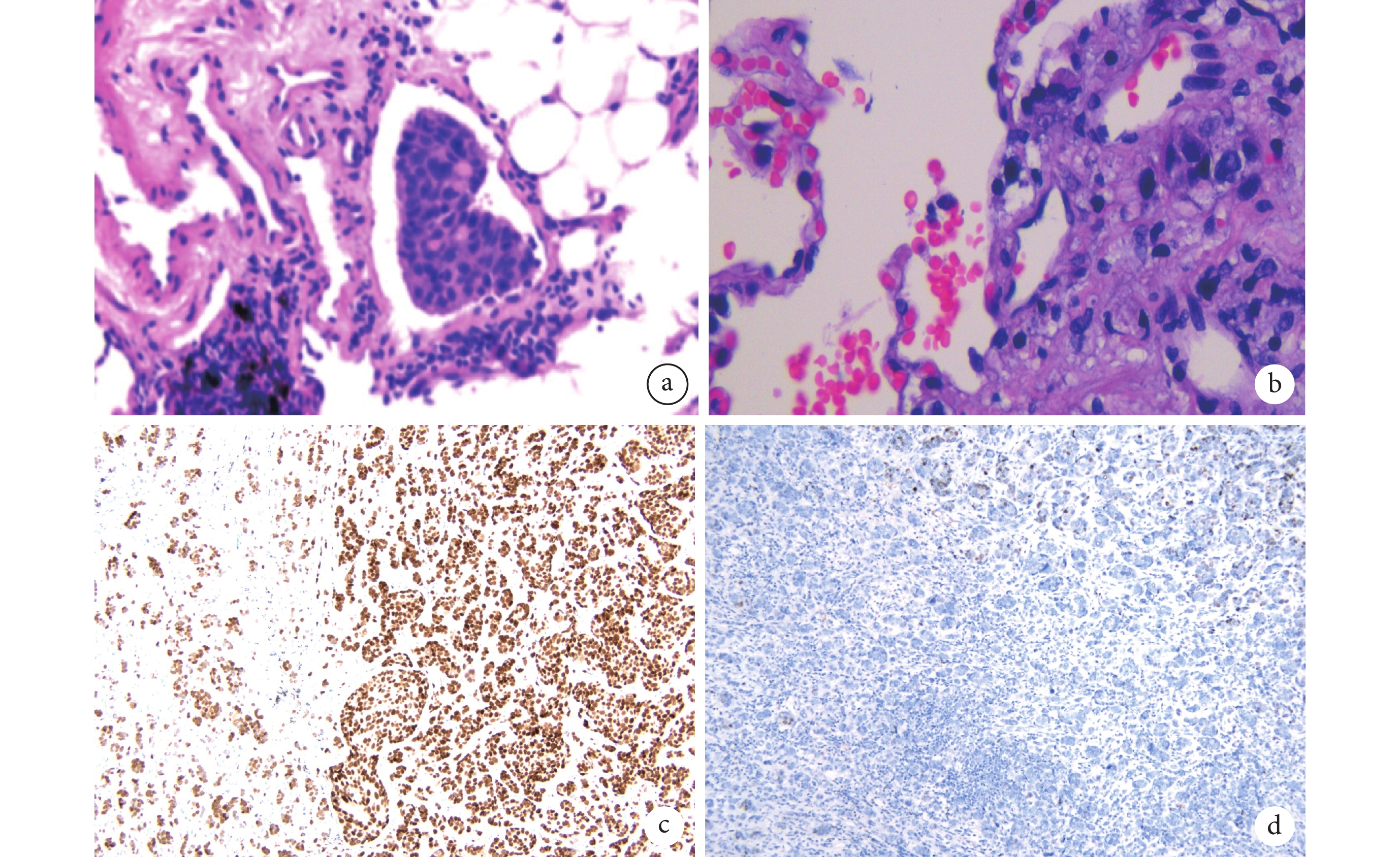
a:癌細胞貼壁樣生長于肺泡空間,肺泡腔內可見癌巢(HE 染色,×200);b:可見異型細胞、核分裂象(HE 染色,×400);c:轉錄因子GATA3免疫組化結果;d:細胞角蛋白7免疫組化結果;HE:蘇木素-伊紅
討論 截至目前,我們在中國知網、萬方、維普數據庫尚未檢索到肺部轉移瘤在CT上表現為單發純GGO的中文文獻報道。2001年有學者[4]報道1例胰腺癌肺轉移CT表現為磨玻璃形態;日本Okita等[5]報道1例鼻腔內黑色素瘤肺部轉移性GGO,黑色素瘤細胞沿增厚的肺泡壁呈鱗狀增生,類似細支氣管肺泡癌。這2項報道中,肺部病變均為多發GGO而非單發,伴有實性成分而非純GGO。韓國學者[6]2013年報道1例乳腺癌新輔助化療期間胸部CT顯示雙肺胸膜下斑片狀磨玻璃樣滲出影,伴有發燒癥狀,胸腔鏡肺活檢表明為乳腺癌肺轉移,與本篇報道的純GGO影像學表現不同。2020年日本學者[7]報道1例乳腺惡性葉狀腫瘤術后31個月發現肺部典型GGO,隨訪后結節增大,手術切除后病理為乳腺惡性葉狀腫瘤肺轉移,其形態與本篇報道較為相似。
在肺腺癌中,GGO是非侵襲性或惰性病變,具有良好的預后[8]。初次發現的GGO根據不同的大小、實性成分占比,其隨訪時間不同,必要時,應開展包括放射腫瘤學、外科和介入的多學科評估[9-11],且GGO患者術前不推薦頭顱磁共振成像[12]、腹部CT[13]以及骨掃描檢查[14]。與此相反的是,肺轉移瘤患者需要盡快治療,在多種實體惡性腫瘤中,無論有沒有縱隔淋巴結轉移,手術切除可增加單發的肺轉移瘤患者的生存獲益[15-18]。并且,對于既往有惡性腫瘤病史的GGO患者,如果不能確定為肺原發病變的情況下,頭顱增強磁共振成像、骨掃描或者 PET/CT是有必要的。在本例中,乳腺癌術后隨診檢查中發現單發純GGO,術前考慮為非典型腺瘤樣增生或原位腺癌,行胸腔鏡下聯合肺段切除+縱隔淋巴結采樣,術中病理檢查提示為乳腺癌肺轉移,幸運的是該患者術前進行了全身檢查,未發現其他病灶,但意外的是,肺門淋巴結和縱隔淋巴結陽性,這在術前CT檢查中未能發現。
原發性GGO與轉移性結節的手術原則不同[19]。原發性GGO的主要手術方式是肺段切除術或聯合肺段切除術+縱隔淋巴結采樣,此術式可以保留更多的肺功能,其總生存率與肺葉切除術的生存率差異無統計學意義[20]。而對于肺單發轉移瘤而言,手術的基本原則是盡可能完整切除轉移灶、盡量多地保留肺組織,以提高患者生存率以及改善生存質量。對于外周轉移灶,楔形切除是足夠的,對于深部的轉移灶無法行楔形切除術的可行解剖性切除,肺段切除是選擇之一[17, 21]。但縱隔淋巴結采樣或清掃是否可提高總生存率存在爭議,尚無定論[21]。
隨著抗腫瘤藥物的研發和治療手段的多樣化,腫瘤患者的生存時間不斷延長,在腫瘤的治療過程中出現肺轉移瘤的機會必將增多,在GGO檢出率增高的背景下,以GGO為表現形式的轉移癌值得警惕。在有惡性腫瘤病史的患者中,發現單發純GGO應考慮轉移瘤的可能性,應縮短隨訪時間。如果隨訪中結節進行性增大,應鼓勵患者完善全身檢查后盡早手術,根據術中冰凍病理檢查結果決定淋巴結切除方式。
本文報道一個非常罕見的肺轉移性腫瘤的CT表現,即純GGO。存在惡性腫瘤病史的患者治療后出現GGO,應考慮肺轉移性瘤的可能性,應縮短隨訪時間。對于單發、手術可切除遠處轉移瘤應盡早手術切除,術前全身檢查以排除其他器官轉移,根據術中冰凍病理檢查結果決定淋巴結切除方式。在腫瘤治療中,多學科團隊對罕見病例制定合理的治療策略具有一定的幫助。
利益沖突:無。
作者貢獻:敬濤、宋鐵牛負責起草、撰寫、修改文章;敬濤、魏小平、王成負責手術規劃、操作;馮海明、張少博負責術前資料收集、術后隨訪;王成、蔣鵬、李斌負責文章修改、校審。
隨著健康體檢意識的增強和低劑量螺旋CT應用的增多,磨玻璃結節(ground-glass opacity,GGO)的檢出率逐年增高[1],尤其是純GGO極少表現為轉移瘤。肺是乳腺癌常見的轉移部位,可表現為單發或多發結節、淋巴管炎或彌漫性間質增厚[2]。然而,GGO是一種罕見的肺轉移形態,可能被誤診為早期肺腺癌、間質性肺炎或病毒感染等,如果我們不能區分原發或轉移性病變,就無法制定準確的治療策略。GGO是一種非特異性的影像學表現,見于許多涉及不同臨床疾病的病理過程。GGO在影像上可表現為肺泡腔變實改變,也可表現為肺間質改變、肺泡壁內細胞數量增加、液體增多等。除了早期肺腺癌或不典型腺瘤樣增生外,GGO可能是肺部病毒感染(如COVID-19)、肺水腫伴間質積液、斑片狀肺實質水腫或間質性疾病的表現[3],但很少表現為轉移癌。實體惡性腫瘤的肺轉移類型通常為多發結節或腫塊、淋巴管炎或彌漫性間質增厚[2],而表現為單發GGO較為少見。本文報道1例乳腺癌肺轉移表現為單發GGO患者。
臨床資料 患者,女,32歲,2018年10月發現右側乳腺包塊,乳腺CT示右側乳房外上象限見 21 mm×20 mm腫塊,周圍呈不規則狀、毛刺樣改變(圖1a),行B超引導下腫瘤及腋窩淋巴結穿刺,穿刺病理示乳腺浸潤性導管癌(圖2a~b),免疫組化結果(圖2c~d):雌激素受體(ER,>80%強+),孕激素受體(PR,20%弱-中等+),人表皮生長因子受體2(CerbB2,2+),拓撲異構酶Ⅱ(Top-2,2+),細胞角蛋白5(CK5,–),E-鈣粘蛋白(E-Cadherin,+),Ki-67(>20%),P120(胞膜+),P63(–),雌激素調節蛋白(pS2,–);Fish檢測HER-2為陰性。腋窩淋巴結可見腺癌細胞轉移。全身檢查(頭、胸、腹CT,骨掃描)未見遠處轉移,給予2個周期多西他賽+表柔比星+環磷酰胺新輔助化療1個月后,行保留乳頭乳暈右側乳腺腺體切除術+腋窩淋巴結采樣+乳腺假體植入術。術后繼續給予多西他賽+表柔比星+環磷酰胺方案術后輔助化療4個周期,2019年7月采用亮丙瑞林+阿那曲唑內分泌治療并每3個月復查。2021年7月胸部CT未見肺部異常病灶(圖1b),而5個月后胸部CT發現右肺下葉后基底段純GGO,大小20 mm×22 mm×20 mm(圖1c),縱隔淋巴結未見明顯增大,術前考慮早期肺腺癌可能性大,頭顱磁共振成像、腹部CT及全身骨顯像未見轉移,B超檢查腋窩及頸部未見增大淋巴結。2022年1月行胸腔鏡肺段切除術,術中病理檢查回報乳腺癌肺轉移,遂行縱隔淋巴結采樣術。術后病理為肺浸潤性導管癌侵犯,切緣未見癌殘留,脈管腔內見瘤栓(圖3a~b),免疫組化染色(圖3c~d):細胞角蛋白7(CK7,–),細胞角蛋白20(CK20,–),絨毛蛋白(Villin,–),轉錄因子GATA3(+),乳腺珠蛋白(Mammaglobin,–),甲狀腺轉錄因子-1(TTF-1,–),P40(–),突觸素(Syn,–),Ki-67(30%+),2、4、7、8、9、10、12組淋巴結見癌轉移;患者術后1個月給予白蛋白紫杉醇300 mg+卡培他濱1.5 g維持化療中,2022年7月復查胸部CT(圖1d),RECIST評分為病情穩定。
 圖1
乳腺 CT
圖1
乳腺 CT
a:乳腺外上象限可見大小約 21 mm×20 mm 低密度腫塊影(紅色箭頭);b:乳腺癌術后 25 個月復查胸部 CT 未見異常;c:乳腺癌術后31個月的胸部 CT 可見右肺下葉純磨玻璃結節影(白色箭頭);d:胸腔鏡肺段切除術后復查
 圖2
術前穿刺病理和免疫組化結果
圖2
術前穿刺病理和免疫組化結果
a:癌細胞充滿乳腺導管(紅色箭頭,HE 染色,×100);b:核大深染癌細胞的聚集(紅色箭頭,HE 染色,×200);c:雌激素受體免疫組化結果;d:細胞角蛋白免疫組化結果;HE:蘇木素-伊紅
 圖3
術中病理檢查和免疫組化結果
圖3
術中病理檢查和免疫組化結果
a:癌細胞貼壁樣生長于肺泡空間,肺泡腔內可見癌巢(HE 染色,×200);b:可見異型細胞、核分裂象(HE 染色,×400);c:轉錄因子GATA3免疫組化結果;d:細胞角蛋白7免疫組化結果;HE:蘇木素-伊紅
討論 截至目前,我們在中國知網、萬方、維普數據庫尚未檢索到肺部轉移瘤在CT上表現為單發純GGO的中文文獻報道。2001年有學者[4]報道1例胰腺癌肺轉移CT表現為磨玻璃形態;日本Okita等[5]報道1例鼻腔內黑色素瘤肺部轉移性GGO,黑色素瘤細胞沿增厚的肺泡壁呈鱗狀增生,類似細支氣管肺泡癌。這2項報道中,肺部病變均為多發GGO而非單發,伴有實性成分而非純GGO。韓國學者[6]2013年報道1例乳腺癌新輔助化療期間胸部CT顯示雙肺胸膜下斑片狀磨玻璃樣滲出影,伴有發燒癥狀,胸腔鏡肺活檢表明為乳腺癌肺轉移,與本篇報道的純GGO影像學表現不同。2020年日本學者[7]報道1例乳腺惡性葉狀腫瘤術后31個月發現肺部典型GGO,隨訪后結節增大,手術切除后病理為乳腺惡性葉狀腫瘤肺轉移,其形態與本篇報道較為相似。
在肺腺癌中,GGO是非侵襲性或惰性病變,具有良好的預后[8]。初次發現的GGO根據不同的大小、實性成分占比,其隨訪時間不同,必要時,應開展包括放射腫瘤學、外科和介入的多學科評估[9-11],且GGO患者術前不推薦頭顱磁共振成像[12]、腹部CT[13]以及骨掃描檢查[14]。與此相反的是,肺轉移瘤患者需要盡快治療,在多種實體惡性腫瘤中,無論有沒有縱隔淋巴結轉移,手術切除可增加單發的肺轉移瘤患者的生存獲益[15-18]。并且,對于既往有惡性腫瘤病史的GGO患者,如果不能確定為肺原發病變的情況下,頭顱增強磁共振成像、骨掃描或者 PET/CT是有必要的。在本例中,乳腺癌術后隨診檢查中發現單發純GGO,術前考慮為非典型腺瘤樣增生或原位腺癌,行胸腔鏡下聯合肺段切除+縱隔淋巴結采樣,術中病理檢查提示為乳腺癌肺轉移,幸運的是該患者術前進行了全身檢查,未發現其他病灶,但意外的是,肺門淋巴結和縱隔淋巴結陽性,這在術前CT檢查中未能發現。
原發性GGO與轉移性結節的手術原則不同[19]。原發性GGO的主要手術方式是肺段切除術或聯合肺段切除術+縱隔淋巴結采樣,此術式可以保留更多的肺功能,其總生存率與肺葉切除術的生存率差異無統計學意義[20]。而對于肺單發轉移瘤而言,手術的基本原則是盡可能完整切除轉移灶、盡量多地保留肺組織,以提高患者生存率以及改善生存質量。對于外周轉移灶,楔形切除是足夠的,對于深部的轉移灶無法行楔形切除術的可行解剖性切除,肺段切除是選擇之一[17, 21]。但縱隔淋巴結采樣或清掃是否可提高總生存率存在爭議,尚無定論[21]。
隨著抗腫瘤藥物的研發和治療手段的多樣化,腫瘤患者的生存時間不斷延長,在腫瘤的治療過程中出現肺轉移瘤的機會必將增多,在GGO檢出率增高的背景下,以GGO為表現形式的轉移癌值得警惕。在有惡性腫瘤病史的患者中,發現單發純GGO應考慮轉移瘤的可能性,應縮短隨訪時間。如果隨訪中結節進行性增大,應鼓勵患者完善全身檢查后盡早手術,根據術中冰凍病理檢查結果決定淋巴結切除方式。
本文報道一個非常罕見的肺轉移性腫瘤的CT表現,即純GGO。存在惡性腫瘤病史的患者治療后出現GGO,應考慮肺轉移性瘤的可能性,應縮短隨訪時間。對于單發、手術可切除遠處轉移瘤應盡早手術切除,術前全身檢查以排除其他器官轉移,根據術中冰凍病理檢查結果決定淋巴結切除方式。在腫瘤治療中,多學科團隊對罕見病例制定合理的治療策略具有一定的幫助。
利益沖突:無。
作者貢獻:敬濤、宋鐵牛負責起草、撰寫、修改文章;敬濤、魏小平、王成負責手術規劃、操作;馮海明、張少博負責術前資料收集、術后隨訪;王成、蔣鵬、李斌負責文章修改、校審。