引用本文: 徐旖煒, 周密, 朱嘉希, 康磊, 葉曉峰, 裘佳培, 李海清, 王哲, 陳安清, 趙強. 姑息性手術與單純藥物治療繼發性非缺血性二尖瓣反流的回顧性隊列研究. 中國胸心血管外科臨床雜志, 2024, 31(7): 1000-1006. doi: 10.7507/1007-4848.202301024 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
繼發性二尖瓣反流并不是由二尖瓣結構本身病變引起,而是由二尖瓣瓣環擴大或左心室擴大、腱索拴系引起[1-2]。最常見的病因是缺血性心肌病、擴張型心肌病或心房顫動(房顫),二尖瓣反流既是左心室擴大的結果,同時反流也會增加左心室前負荷從而進一步加速左心室擴大,兩者互為因果。有研究[3-6]表明心力衰竭患者在標準藥物治療的基礎上如果合并輕度二尖瓣反流,4年內心源性死亡率為6%;若合并中度繼發性二尖瓣反流,死亡率為43%;合并重度繼發性二尖瓣反流,死亡率達45%。可見標準藥物治療對于合并中度及以上繼發性二尖瓣反流的患者效果有限[7]。理論上糾正二尖瓣反流可以打破惡性循環、延緩左心室擴大的進展速度。有研究[8]證實在缺血性心肌病中,糾正繼發性二尖瓣反流能改善患者預后,但對于繼發性非缺血性二尖瓣反流的循證依據還較少,本研究旨在進一步探討二尖瓣手術對于繼發性非缺血性二尖瓣反流的治療效果。
1 資料與方法
1.1 臨床資料和分組
本研究為回顧性隊列研究。研究對象為2009—2019年上海交通大學醫學院附屬瑞金醫院心臟外科收治的繼發性非缺血性二尖瓣反流患者。納入標準:(1)繼發性非缺血性二尖瓣反流患者;(2)中度及以上二尖瓣反流;(3)左心室射血分數(left ventricular ejection fraction,LVEF)<40%。排除標準:(1)原發性二尖瓣病變;(2)合并冠狀動脈粥樣硬化性心臟病(冠心病);(3)合并主動脈瓣及大血管病變且需手術治療;(4)既往心臟手術史;(5)合并急性心力衰竭。給予多巴酚丁胺25 μg/(kg·min)后LVEF較基礎值改善>15%判定為試驗結果陽性[9]。將多巴酚丁胺負荷試驗結果陽性患者分為手術組和藥物組,其中手術組患者接受姑息性二尖瓣手術,包括二尖瓣置換術和成形術,術后接受指南推薦的心力衰竭最大化的藥物治療(guideline-directed medical therapy,GDMT),而藥物組患者僅接受GDMT。
1.2 資料收集
收集患者的年齡、性別、歐洲心臟手術風險評估系統(European System for Cardiac Operative Risk Evaluation,EuroSCORE)Ⅱ評分(預測死亡率)、高血壓史、糖尿病史、慢性阻塞性肺疾病史、慢性腎臟病史、卒中史、紐約心臟協會(New York Heart Association,NYHA)心功能分級、心臟超聲二尖瓣反流程度、左心房內徑、左心室舒張末期內徑、肺動脈收縮壓。
1.3 評價指標
研究終點為全因死亡、心力衰竭再住院、心臟移植的復合終點。心力衰竭再住院定義為有心力衰竭癥狀并在住院期間使用靜脈利尿劑。定期評估患者NYHA心功能分級,出院后1年心臟超聲評估二尖瓣反流程度及各項心臟超聲參數。
1.4 二尖瓣手術
對于手術組患者,在全身麻醉氣管插管后行胸骨正中切口進胸,予升主動脈上下腔靜脈插管建立體外循環。心肌保護策略為:升主動脈根部順行性灌注+冠狀靜脈竇逆行性灌注4∶1冷血停搏液,心臟表面置冰泥,手術過程中每半小時予間斷順行性灌注或逆行性灌注冷血停搏液,開放前予順行性灌注低溫冷血。術中采用二尖瓣修復或置換由主刀醫生根據自身經驗決定。二尖瓣修復均采用單純人工瓣環植入術,瓣環尺寸選擇較常規小1~2號。二尖瓣置換患者盡可能保留瓣葉及瓣下結構,盡可能采用生物瓣,瓣膜大小較常規選用小1~2號瓣膜。人工瓣膜用間斷褥式帶墊縫合固定。
1.5 藥物治療
對于所有患者,排除禁忌后均給予GDMT,包括β受體阻滯劑、醛固酮拮抗劑、血管緊張素轉換酶抑制劑及血管緊張素Ⅱ受體拮抗劑、血管緊張素受體腦啡肽酶抑制劑。術后二尖瓣修復和二尖瓣生物瓣置換患者抗凝方案為華法林抗凝3個月,二尖瓣機械瓣置換患者抗凝方案為終身華法林抗凝,合并房顫患者亦終身華法林抗凝。
1.6 隨訪
患者每半年進行門診或電話隨訪,隨訪內容包括生存情況、心力衰竭再住院、心臟移植、NYHA心功能分級,術后1年門診隨訪心臟超聲。末次隨訪時間為2020年12月。如患者1年內出現終點事件,選用終點事件發生前最近一次心臟超聲結果進行統計。
1.7 統計學分析
采用IBM SPSS Statistics 16.0軟件進行統計分析。符合正態分布的計量資料采用均數±標準差( ±s)描述,組間比較采用獨立樣本t檢驗。非正態分布的計量資料采用中位數(M)和范圍描述。計數資料用頻數和百分比(%)描述,組間比較采用四格表χ2檢驗。生存比較采用Kaplan-Meier法及log-rank分析。P≤0.05為差異有統計學意義。
±s)描述,組間比較采用獨立樣本t檢驗。非正態分布的計量資料采用中位數(M)和范圍描述。計數資料用頻數和百分比(%)描述,組間比較采用四格表χ2檢驗。生存比較采用Kaplan-Meier法及log-rank分析。P≤0.05為差異有統計學意義。
1.8 倫理審查
本研究已通過上海交通大學醫學院附屬瑞金醫院倫理委員會批準,批件編號:(2023)臨倫審第(216)號。
2 結果
2.1 術前資料
初步納入154例繼發性非缺血性二尖瓣反流患者,反流原因均為擴張型心肌病,不包括退行性、風濕性、感染性、先天性等原發性二尖瓣反流,和冠心病所致的繼發性缺血性二尖瓣反流。排除63例LVEF≥40%的患者。91例LVEF<40%患者進行了多巴酚丁胺負荷試驗。
最終41例患者納入研究,其中男28例、女 13 例,平均年齡(55.5±11.1)歲。手術組25例、藥物組16例。兩組年齡、性別、EuroSCOREⅡ評分、NYHA心功能分級、LVEF、左心房內徑、左心室舒張末期內徑、肺動脈收縮壓、二尖瓣反流程度、糖尿病史、慢性阻塞性肺疾病史、慢性腎功能不全史和卒中史差異無統計學意義(P>0.05)。手術組高血壓史患者比例較高(P=0.03)。兩組患者基線資料基本匹配;見表1。
 ±s/例(%)]
±s/例(%)]
2.2 手術情況
在行二尖瓣手術的25例患者中,6例(24.0%)行二尖瓣成形術,19例(76.0%)行二尖瓣置換術,所有二尖瓣成形術均為單純瓣環植入,未處理瓣葉及瓣下結構。在二尖瓣置換組中,12例(63.2%)植入生物瓣,7例(36.3%)植入機械瓣,所有換瓣患者均保留了部分瓣葉及瓣下結構,其中4例(21.1%)保留了二尖瓣后葉,15例(78.9%)前后葉均保留。在同期手術方面,12例(48.0%)同期行三尖瓣成形,3例(12.0%)同期行房顫消融,1例(5.3%)同期行心臟再同步化治療;見表2。
2.3 隨訪結果
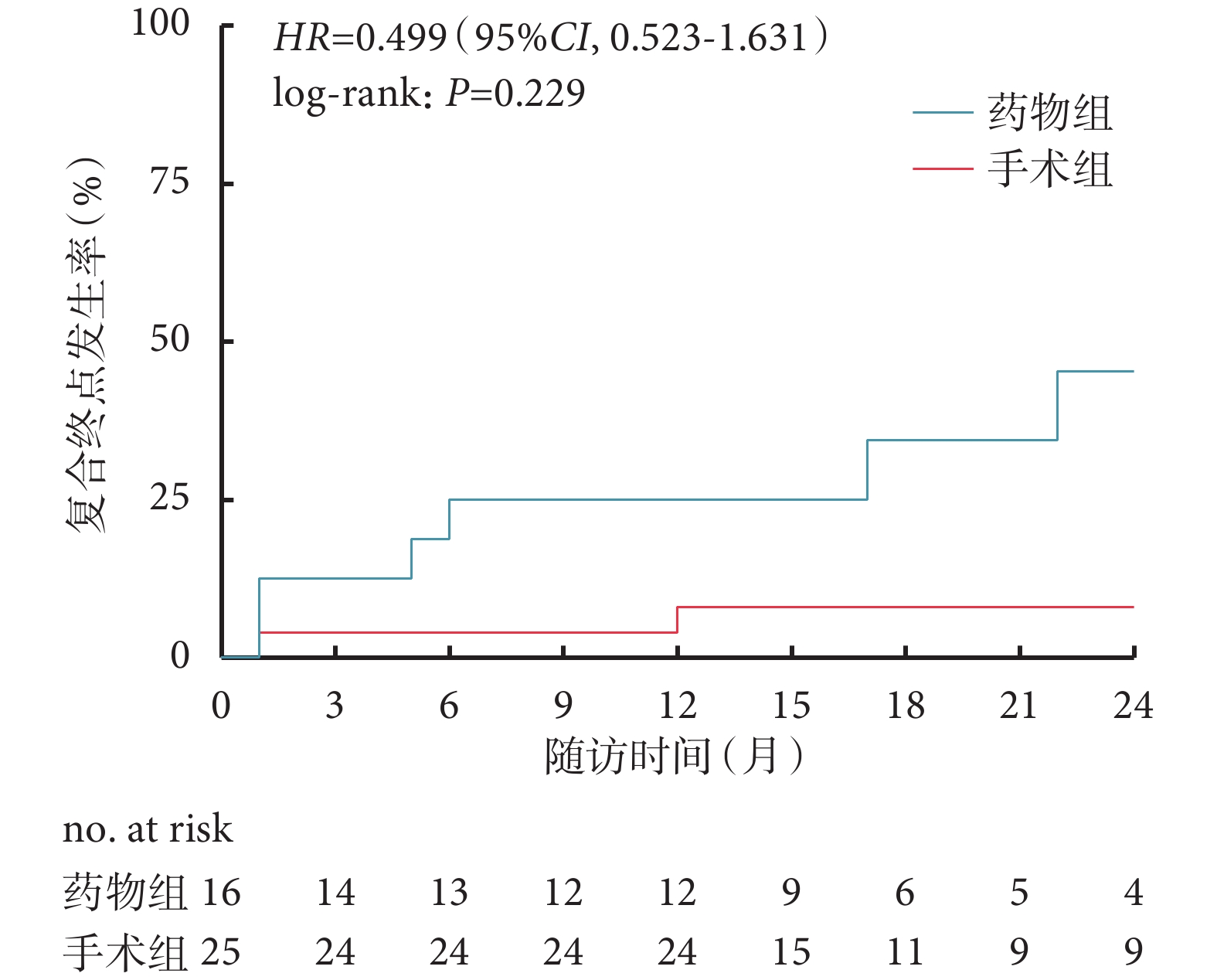
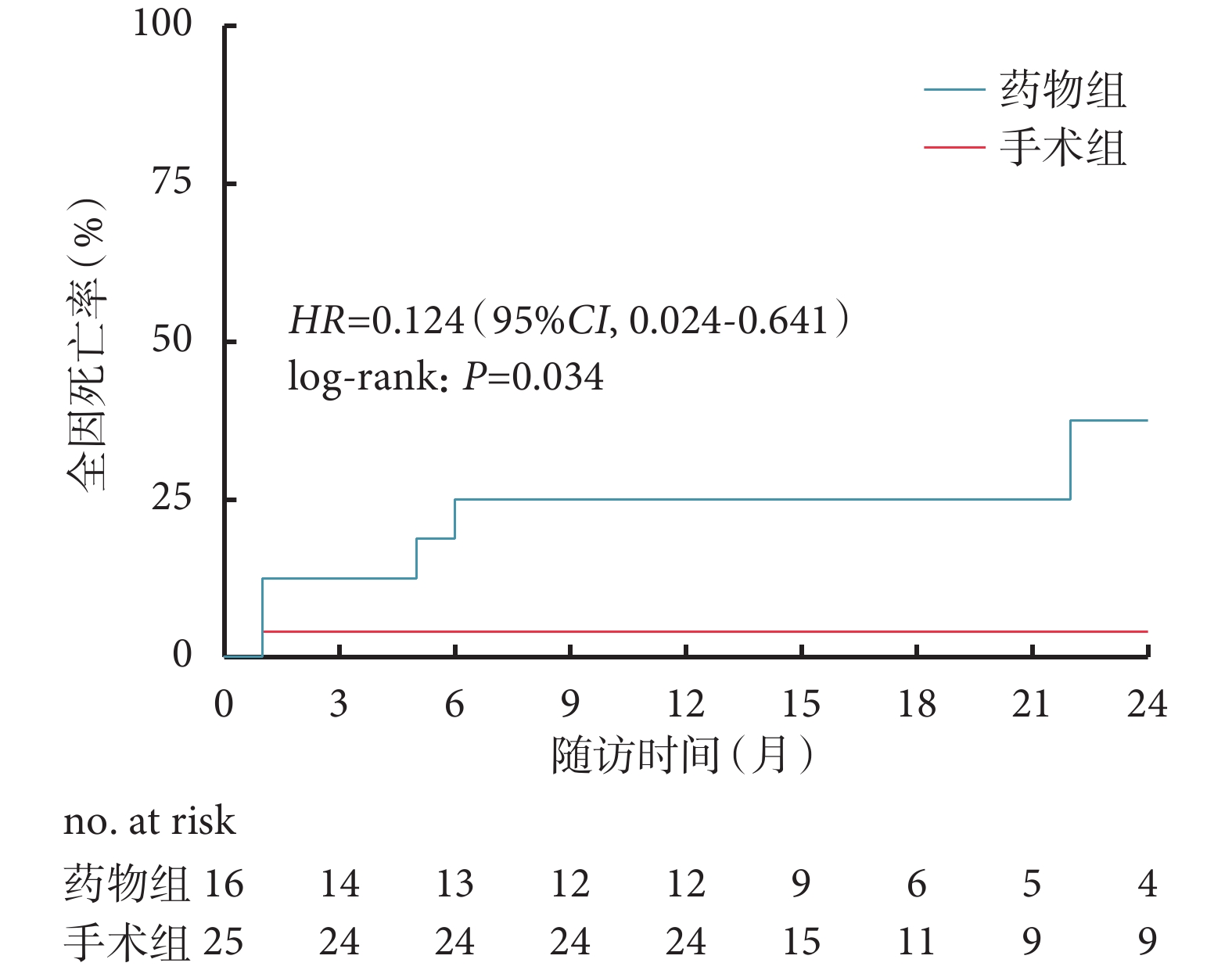
所有患者均獲得隨訪,中位隨訪16(1~96)個月。隨訪期間手術組死亡1例(4.0%),死因為圍術期腦血管意外合并肺部感染,藥物組死亡5例(31.3%),均為心源性死亡;手術組心力衰竭再住院4例(16.0%),藥物組7例(43.8%);藥物組有1例隨訪期間接受了心臟移植(6.3%),手術組無心臟移植病例;兩組復合終點發生率差異無統計學意義[HR=0.499,95%CI(0.523,1.631),P=0.229];見圖1。手術組1年復合終點發生率為8.0%,藥物組為25.0%(P=0.13)。手術組全因死亡率低于藥物組[HR=0.124,95%CI(0.024,0.641),P=0.034];見圖2。手術組1年全因死亡率為4.0%,藥物組為25.0%(P=0.04)。
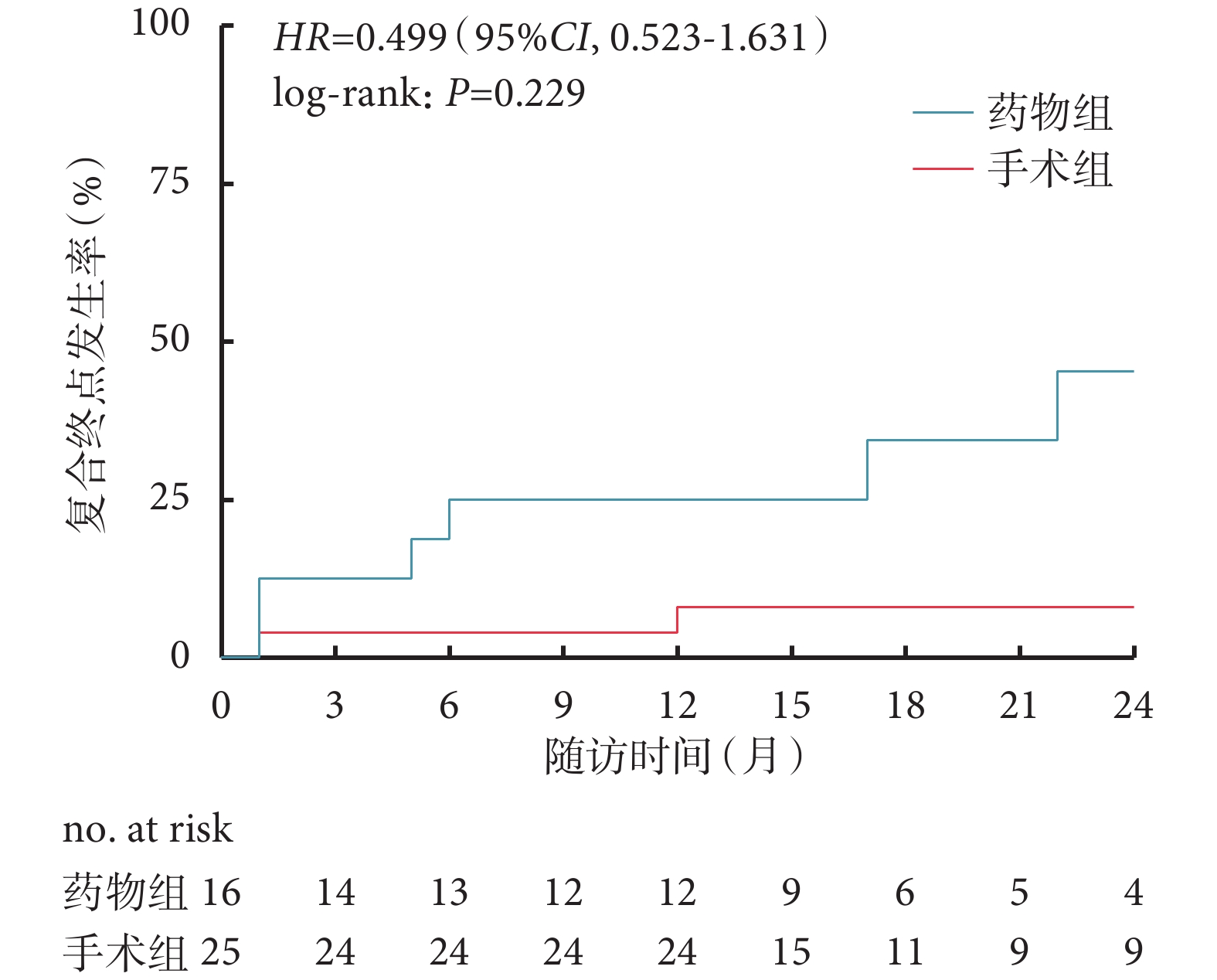 圖1
兩組復合終點(全因死亡、心力衰竭再住院、心臟移植)發生率比較
圖1
兩組復合終點(全因死亡、心力衰竭再住院、心臟移植)發生率比較
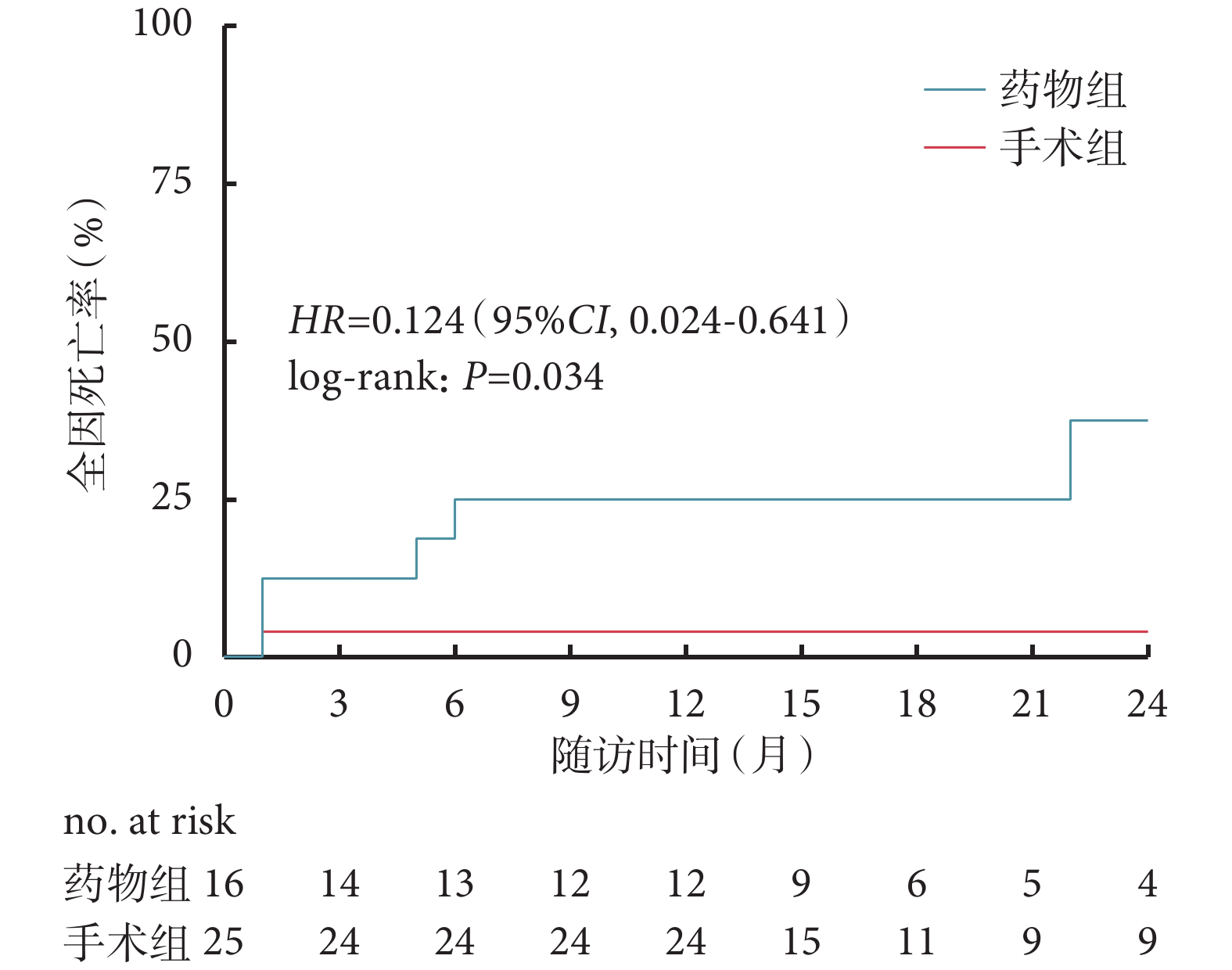 圖2
兩組全因死亡率比較
圖2
兩組全因死亡率比較
兩組長期抗心力衰竭藥物使用情況:大部分患者接受了最佳藥物治療,兩組藥物使用差異無統計學意義(P>0.05);見表3。
隨訪時心功能:藥物組NYHA Ⅰ~Ⅱ級占18.8%,手術組占68.0%,手術組心功能優于藥物組(P<0.01)。藥物組隨訪時心功能分級與術前水平差異無統計學意義(P=0.14),手術組心功能較術前明顯改善(P<0.01);見表4。
1年隨訪時心臟超聲結果:藥物組12.5%的患者為無或輕度二尖瓣反流,18.8%的患者為中度反流,68.8%的患者為重度反流,與術前水平差異無統計學意義(P=0.14);手術組52.0%的患者無二尖瓣反流,48.0%的患者為輕微至輕度反流,無中、重度反流患者,較藥物組明顯改善(P<0.01),與術前二尖瓣反流程度相比也明顯改善(P<0.01);見表4。
1年隨訪時心臟超聲結果:手術組LVEF改善5.5%±8.1%,藥物組改善6.9%±6.4%(P=0.66)。手術組左心房內徑縮小(4.1±3.9)mm,藥物組縮小(4.8±3.7)mm(P=0.66)。手術組左心室舒張末期內徑縮小(4.3±4.3)mm,藥物組縮小(3.4±3.4)mm(P=0.60)。手術組肺動脈收縮壓下降(10.6±11.1)mm Hg(1 mm Hg=0.133 kPa),藥物組下降(8.5±15.6)mm Hg(P=0.73);見表5。
 ±s)
±s)
3 討論
盡管心力衰竭的治療方法在不斷進步,但其仍嚴重威脅著患者生命安全。美國心力衰竭的死亡率為53/100 000~92/100 000[10]。而在所有心力衰竭患者中,合并繼發性二尖瓣關閉不全的患者生存和生活質量會進一步惡化,有研究[11-14]表明合并繼發性二尖瓣反流的心力衰竭患者全因死亡率(HR=4.696)和心力衰竭住院率(HR=7.676)都較不合并二尖瓣反流的患者要高。
治療繼發性二尖瓣反流目前常用的方法有藥物治療、二尖瓣姑息性手術(包括外科二尖瓣手術和介入二尖瓣手術)、心臟移植等。其中藥物治療的效果非常有限,根據Agricola等[7]的研究,在合并二尖瓣反流的心功能低下患者中,藥物治療4年的生存率僅為53%。心臟移植是有效的根治性治療手段,但受限于供體的短缺尚無法廣泛開展。至于姑息性二尖瓣手術,理論上消除繼發性二尖瓣反流可以降低左心室前負荷,從而打破二尖瓣反流與左心室擴大之間的惡性循環,但循證上仍缺乏相關證據。
對于缺血性心肌病引起的重度二尖瓣反流患者,已有不少研究[15-16]證實干預二尖瓣可以獲益,趙強團隊[17]也證實非移植外科治療對于缺血性心功能不全安全有效。2021年歐洲心臟病學會(ESC)瓣膜指南[18]提出:如果冠狀動脈旁路移植術合并重度二尖瓣關閉不全,建議同期干預二尖瓣,但是對于非缺血性心肌病導致的繼發性二尖瓣反流患者,二尖瓣干預的效果如何,目前尚缺乏相關數據,單純干預二尖瓣的獲益、風險都有待進一步評估。Chung等[19]的研究比較了特發性擴張型心肌病中行二尖瓣手術和GDMT的效果(全因死亡或心室輔助裝置植入率),二尖瓣手術相對更好一些。
近年來介入二尖瓣技術日趨成熟,根據COAPT研究[20]結果,經導管二尖瓣成形較藥物治療可以降低全因死亡率,但是該研究入組時并未區分缺血性還是非缺血性心功能不全。這兩種病因導致心功能受損的機制是不同的,缺血性心肌病患者常常因心室壁局部活動異常而導致心功能不全,乳頭肌牽拉也常常是非對稱性的,而非缺血性心肌病往往是心室肌肉的普遍性活動異常、心室普遍擴張。
本研究關注了繼發性二尖瓣反流合并LVEF降低的人群,并剔除了其中缺血性二尖瓣反流的患者。鑒于二尖瓣外科手術圍術期的潛在風險,我們并不推薦所有非缺血性繼發性二尖瓣反流都接受二尖瓣外科手術。左心室收縮功能儲備低下可能與心肌纖維化相關,可能導致死亡率上升,也更快地進展到需要心臟移植[21-25]。本研究剔除了多巴酚丁胺負荷試驗結果陰性的患者,因為我們認為這些患者更適合在一段時間后接受心臟移植,在移植前行姑息性二尖瓣手術可能弊大于利。
兩組術前一般情況、二尖瓣反流程度和心功能狀態基本匹配。兩組高血壓史差異有統計學意義,可能與樣本量較小及高血壓史患者比例較低相關。手術過程中為了預防術后低心排血量綜合征,我們在所有患者中盡可能保留瓣膜及瓣下結構。手術組圍術期有1例患者術后出現腦血管意外,長期機械通氣后并發感染死亡,為非心源性死亡。16個月的隨訪中,手術組較藥物組在生存上有顯著獲益,除外圍術期1例非心源性死亡,手術組后續沒有死亡病例,藥物治療組有5例患者死亡,均為心源性死亡。根據心臟超聲隨訪結果,外科手術有效消除了二尖瓣反流,手術組左心房、左心室較術前縮小合并LVEF提高、肺動脈收縮壓下降,但其改善程度較藥物組并沒有顯著差異。Wu等[26]也發現,在低LVEF合并二尖瓣反流的患者中手術糾正二尖瓣反流,術后左心房、左心室大小與藥物組差異無統計學意義。Chung等[19]的研究也有類似結果,二尖瓣手術改善了擴張型心肌病的生存預后,但與非手術組相比,并沒有發現左心室、左心房和其他心臟超聲參數的顯著優勢。中重度二尖瓣反流患者的LVEF往往會被高估,而藥物組1年隨訪時二尖瓣反流較重,可能是導致兩組LVEF無明顯差別的原因,在LVEF值相似時,手術組二尖瓣反流較輕,相對前向血流也較多,這種獲益也體現在兩組的生存差異上。
本研究的不足之處在于該研究是回顧性研究,證據力度有欠缺。其次該研究為單中心研究,樣本量有限。
綜上,我們認為對于有一定心臟收縮功能儲備的繼發性非缺血性二尖瓣反流,行姑息性外科二尖瓣手術能夠改善生存、提高生活質量。
利益沖突:無。
作者貢獻:徐旖煒參與研究設計、手術、數據收集、文章撰寫;周密參與研究設計、手術、文章撰寫及修改;朱嘉希、康磊、葉曉峰、裘佳培、李海清、王哲、陳安清參與手術及資料收集;趙強參與研究設計、手術、文章修改及審核。
繼發性二尖瓣反流并不是由二尖瓣結構本身病變引起,而是由二尖瓣瓣環擴大或左心室擴大、腱索拴系引起[1-2]。最常見的病因是缺血性心肌病、擴張型心肌病或心房顫動(房顫),二尖瓣反流既是左心室擴大的結果,同時反流也會增加左心室前負荷從而進一步加速左心室擴大,兩者互為因果。有研究[3-6]表明心力衰竭患者在標準藥物治療的基礎上如果合并輕度二尖瓣反流,4年內心源性死亡率為6%;若合并中度繼發性二尖瓣反流,死亡率為43%;合并重度繼發性二尖瓣反流,死亡率達45%。可見標準藥物治療對于合并中度及以上繼發性二尖瓣反流的患者效果有限[7]。理論上糾正二尖瓣反流可以打破惡性循環、延緩左心室擴大的進展速度。有研究[8]證實在缺血性心肌病中,糾正繼發性二尖瓣反流能改善患者預后,但對于繼發性非缺血性二尖瓣反流的循證依據還較少,本研究旨在進一步探討二尖瓣手術對于繼發性非缺血性二尖瓣反流的治療效果。
1 資料與方法
1.1 臨床資料和分組
本研究為回顧性隊列研究。研究對象為2009—2019年上海交通大學醫學院附屬瑞金醫院心臟外科收治的繼發性非缺血性二尖瓣反流患者。納入標準:(1)繼發性非缺血性二尖瓣反流患者;(2)中度及以上二尖瓣反流;(3)左心室射血分數(left ventricular ejection fraction,LVEF)<40%。排除標準:(1)原發性二尖瓣病變;(2)合并冠狀動脈粥樣硬化性心臟病(冠心病);(3)合并主動脈瓣及大血管病變且需手術治療;(4)既往心臟手術史;(5)合并急性心力衰竭。給予多巴酚丁胺25 μg/(kg·min)后LVEF較基礎值改善>15%判定為試驗結果陽性[9]。將多巴酚丁胺負荷試驗結果陽性患者分為手術組和藥物組,其中手術組患者接受姑息性二尖瓣手術,包括二尖瓣置換術和成形術,術后接受指南推薦的心力衰竭最大化的藥物治療(guideline-directed medical therapy,GDMT),而藥物組患者僅接受GDMT。
1.2 資料收集
收集患者的年齡、性別、歐洲心臟手術風險評估系統(European System for Cardiac Operative Risk Evaluation,EuroSCORE)Ⅱ評分(預測死亡率)、高血壓史、糖尿病史、慢性阻塞性肺疾病史、慢性腎臟病史、卒中史、紐約心臟協會(New York Heart Association,NYHA)心功能分級、心臟超聲二尖瓣反流程度、左心房內徑、左心室舒張末期內徑、肺動脈收縮壓。
1.3 評價指標
研究終點為全因死亡、心力衰竭再住院、心臟移植的復合終點。心力衰竭再住院定義為有心力衰竭癥狀并在住院期間使用靜脈利尿劑。定期評估患者NYHA心功能分級,出院后1年心臟超聲評估二尖瓣反流程度及各項心臟超聲參數。
1.4 二尖瓣手術
對于手術組患者,在全身麻醉氣管插管后行胸骨正中切口進胸,予升主動脈上下腔靜脈插管建立體外循環。心肌保護策略為:升主動脈根部順行性灌注+冠狀靜脈竇逆行性灌注4∶1冷血停搏液,心臟表面置冰泥,手術過程中每半小時予間斷順行性灌注或逆行性灌注冷血停搏液,開放前予順行性灌注低溫冷血。術中采用二尖瓣修復或置換由主刀醫生根據自身經驗決定。二尖瓣修復均采用單純人工瓣環植入術,瓣環尺寸選擇較常規小1~2號。二尖瓣置換患者盡可能保留瓣葉及瓣下結構,盡可能采用生物瓣,瓣膜大小較常規選用小1~2號瓣膜。人工瓣膜用間斷褥式帶墊縫合固定。
1.5 藥物治療
對于所有患者,排除禁忌后均給予GDMT,包括β受體阻滯劑、醛固酮拮抗劑、血管緊張素轉換酶抑制劑及血管緊張素Ⅱ受體拮抗劑、血管緊張素受體腦啡肽酶抑制劑。術后二尖瓣修復和二尖瓣生物瓣置換患者抗凝方案為華法林抗凝3個月,二尖瓣機械瓣置換患者抗凝方案為終身華法林抗凝,合并房顫患者亦終身華法林抗凝。
1.6 隨訪
患者每半年進行門診或電話隨訪,隨訪內容包括生存情況、心力衰竭再住院、心臟移植、NYHA心功能分級,術后1年門診隨訪心臟超聲。末次隨訪時間為2020年12月。如患者1年內出現終點事件,選用終點事件發生前最近一次心臟超聲結果進行統計。
1.7 統計學分析
采用IBM SPSS Statistics 16.0軟件進行統計分析。符合正態分布的計量資料采用均數±標準差( ±s)描述,組間比較采用獨立樣本t檢驗。非正態分布的計量資料采用中位數(M)和范圍描述。計數資料用頻數和百分比(%)描述,組間比較采用四格表χ2檢驗。生存比較采用Kaplan-Meier法及log-rank分析。P≤0.05為差異有統計學意義。
±s)描述,組間比較采用獨立樣本t檢驗。非正態分布的計量資料采用中位數(M)和范圍描述。計數資料用頻數和百分比(%)描述,組間比較采用四格表χ2檢驗。生存比較采用Kaplan-Meier法及log-rank分析。P≤0.05為差異有統計學意義。
1.8 倫理審查
本研究已通過上海交通大學醫學院附屬瑞金醫院倫理委員會批準,批件編號:(2023)臨倫審第(216)號。
2 結果
2.1 術前資料
初步納入154例繼發性非缺血性二尖瓣反流患者,反流原因均為擴張型心肌病,不包括退行性、風濕性、感染性、先天性等原發性二尖瓣反流,和冠心病所致的繼發性缺血性二尖瓣反流。排除63例LVEF≥40%的患者。91例LVEF<40%患者進行了多巴酚丁胺負荷試驗。
最終41例患者納入研究,其中男28例、女 13 例,平均年齡(55.5±11.1)歲。手術組25例、藥物組16例。兩組年齡、性別、EuroSCOREⅡ評分、NYHA心功能分級、LVEF、左心房內徑、左心室舒張末期內徑、肺動脈收縮壓、二尖瓣反流程度、糖尿病史、慢性阻塞性肺疾病史、慢性腎功能不全史和卒中史差異無統計學意義(P>0.05)。手術組高血壓史患者比例較高(P=0.03)。兩組患者基線資料基本匹配;見表1。
 ±s/例(%)]
±s/例(%)]
2.2 手術情況
在行二尖瓣手術的25例患者中,6例(24.0%)行二尖瓣成形術,19例(76.0%)行二尖瓣置換術,所有二尖瓣成形術均為單純瓣環植入,未處理瓣葉及瓣下結構。在二尖瓣置換組中,12例(63.2%)植入生物瓣,7例(36.3%)植入機械瓣,所有換瓣患者均保留了部分瓣葉及瓣下結構,其中4例(21.1%)保留了二尖瓣后葉,15例(78.9%)前后葉均保留。在同期手術方面,12例(48.0%)同期行三尖瓣成形,3例(12.0%)同期行房顫消融,1例(5.3%)同期行心臟再同步化治療;見表2。
2.3 隨訪結果
所有患者均獲得隨訪,中位隨訪16(1~96)個月。隨訪期間手術組死亡1例(4.0%),死因為圍術期腦血管意外合并肺部感染,藥物組死亡5例(31.3%),均為心源性死亡;手術組心力衰竭再住院4例(16.0%),藥物組7例(43.8%);藥物組有1例隨訪期間接受了心臟移植(6.3%),手術組無心臟移植病例;兩組復合終點發生率差異無統計學意義[HR=0.499,95%CI(0.523,1.631),P=0.229];見圖1。手術組1年復合終點發生率為8.0%,藥物組為25.0%(P=0.13)。手術組全因死亡率低于藥物組[HR=0.124,95%CI(0.024,0.641),P=0.034];見圖2。手術組1年全因死亡率為4.0%,藥物組為25.0%(P=0.04)。
 圖1
兩組復合終點(全因死亡、心力衰竭再住院、心臟移植)發生率比較
圖1
兩組復合終點(全因死亡、心力衰竭再住院、心臟移植)發生率比較
 圖2
兩組全因死亡率比較
圖2
兩組全因死亡率比較
兩組長期抗心力衰竭藥物使用情況:大部分患者接受了最佳藥物治療,兩組藥物使用差異無統計學意義(P>0.05);見表3。
隨訪時心功能:藥物組NYHA Ⅰ~Ⅱ級占18.8%,手術組占68.0%,手術組心功能優于藥物組(P<0.01)。藥物組隨訪時心功能分級與術前水平差異無統計學意義(P=0.14),手術組心功能較術前明顯改善(P<0.01);見表4。
1年隨訪時心臟超聲結果:藥物組12.5%的患者為無或輕度二尖瓣反流,18.8%的患者為中度反流,68.8%的患者為重度反流,與術前水平差異無統計學意義(P=0.14);手術組52.0%的患者無二尖瓣反流,48.0%的患者為輕微至輕度反流,無中、重度反流患者,較藥物組明顯改善(P<0.01),與術前二尖瓣反流程度相比也明顯改善(P<0.01);見表4。
1年隨訪時心臟超聲結果:手術組LVEF改善5.5%±8.1%,藥物組改善6.9%±6.4%(P=0.66)。手術組左心房內徑縮小(4.1±3.9)mm,藥物組縮小(4.8±3.7)mm(P=0.66)。手術組左心室舒張末期內徑縮小(4.3±4.3)mm,藥物組縮小(3.4±3.4)mm(P=0.60)。手術組肺動脈收縮壓下降(10.6±11.1)mm Hg(1 mm Hg=0.133 kPa),藥物組下降(8.5±15.6)mm Hg(P=0.73);見表5。
 ±s)
±s)
3 討論
盡管心力衰竭的治療方法在不斷進步,但其仍嚴重威脅著患者生命安全。美國心力衰竭的死亡率為53/100 000~92/100 000[10]。而在所有心力衰竭患者中,合并繼發性二尖瓣關閉不全的患者生存和生活質量會進一步惡化,有研究[11-14]表明合并繼發性二尖瓣反流的心力衰竭患者全因死亡率(HR=4.696)和心力衰竭住院率(HR=7.676)都較不合并二尖瓣反流的患者要高。
治療繼發性二尖瓣反流目前常用的方法有藥物治療、二尖瓣姑息性手術(包括外科二尖瓣手術和介入二尖瓣手術)、心臟移植等。其中藥物治療的效果非常有限,根據Agricola等[7]的研究,在合并二尖瓣反流的心功能低下患者中,藥物治療4年的生存率僅為53%。心臟移植是有效的根治性治療手段,但受限于供體的短缺尚無法廣泛開展。至于姑息性二尖瓣手術,理論上消除繼發性二尖瓣反流可以降低左心室前負荷,從而打破二尖瓣反流與左心室擴大之間的惡性循環,但循證上仍缺乏相關證據。
對于缺血性心肌病引起的重度二尖瓣反流患者,已有不少研究[15-16]證實干預二尖瓣可以獲益,趙強團隊[17]也證實非移植外科治療對于缺血性心功能不全安全有效。2021年歐洲心臟病學會(ESC)瓣膜指南[18]提出:如果冠狀動脈旁路移植術合并重度二尖瓣關閉不全,建議同期干預二尖瓣,但是對于非缺血性心肌病導致的繼發性二尖瓣反流患者,二尖瓣干預的效果如何,目前尚缺乏相關數據,單純干預二尖瓣的獲益、風險都有待進一步評估。Chung等[19]的研究比較了特發性擴張型心肌病中行二尖瓣手術和GDMT的效果(全因死亡或心室輔助裝置植入率),二尖瓣手術相對更好一些。
近年來介入二尖瓣技術日趨成熟,根據COAPT研究[20]結果,經導管二尖瓣成形較藥物治療可以降低全因死亡率,但是該研究入組時并未區分缺血性還是非缺血性心功能不全。這兩種病因導致心功能受損的機制是不同的,缺血性心肌病患者常常因心室壁局部活動異常而導致心功能不全,乳頭肌牽拉也常常是非對稱性的,而非缺血性心肌病往往是心室肌肉的普遍性活動異常、心室普遍擴張。
本研究關注了繼發性二尖瓣反流合并LVEF降低的人群,并剔除了其中缺血性二尖瓣反流的患者。鑒于二尖瓣外科手術圍術期的潛在風險,我們并不推薦所有非缺血性繼發性二尖瓣反流都接受二尖瓣外科手術。左心室收縮功能儲備低下可能與心肌纖維化相關,可能導致死亡率上升,也更快地進展到需要心臟移植[21-25]。本研究剔除了多巴酚丁胺負荷試驗結果陰性的患者,因為我們認為這些患者更適合在一段時間后接受心臟移植,在移植前行姑息性二尖瓣手術可能弊大于利。
兩組術前一般情況、二尖瓣反流程度和心功能狀態基本匹配。兩組高血壓史差異有統計學意義,可能與樣本量較小及高血壓史患者比例較低相關。手術過程中為了預防術后低心排血量綜合征,我們在所有患者中盡可能保留瓣膜及瓣下結構。手術組圍術期有1例患者術后出現腦血管意外,長期機械通氣后并發感染死亡,為非心源性死亡。16個月的隨訪中,手術組較藥物組在生存上有顯著獲益,除外圍術期1例非心源性死亡,手術組后續沒有死亡病例,藥物治療組有5例患者死亡,均為心源性死亡。根據心臟超聲隨訪結果,外科手術有效消除了二尖瓣反流,手術組左心房、左心室較術前縮小合并LVEF提高、肺動脈收縮壓下降,但其改善程度較藥物組并沒有顯著差異。Wu等[26]也發現,在低LVEF合并二尖瓣反流的患者中手術糾正二尖瓣反流,術后左心房、左心室大小與藥物組差異無統計學意義。Chung等[19]的研究也有類似結果,二尖瓣手術改善了擴張型心肌病的生存預后,但與非手術組相比,并沒有發現左心室、左心房和其他心臟超聲參數的顯著優勢。中重度二尖瓣反流患者的LVEF往往會被高估,而藥物組1年隨訪時二尖瓣反流較重,可能是導致兩組LVEF無明顯差別的原因,在LVEF值相似時,手術組二尖瓣反流較輕,相對前向血流也較多,這種獲益也體現在兩組的生存差異上。
本研究的不足之處在于該研究是回顧性研究,證據力度有欠缺。其次該研究為單中心研究,樣本量有限。
綜上,我們認為對于有一定心臟收縮功能儲備的繼發性非缺血性二尖瓣反流,行姑息性外科二尖瓣手術能夠改善生存、提高生活質量。
利益沖突:無。
作者貢獻:徐旖煒參與研究設計、手術、數據收集、文章撰寫;周密參與研究設計、手術、文章撰寫及修改;朱嘉希、康磊、葉曉峰、裘佳培、李海清、王哲、陳安清參與手術及資料收集;趙強參與研究設計、手術、文章修改及審核。