引用本文: 常碩, 張心怡, 黃晟, 范宇欣, 潘湘斌, 王小啟. 新型冠狀病毒感染期行心臟大血管手術的術后管理. 中國胸心血管外科臨床雜志, 2024, 31(7): 967-973. doi: 10.7507/1007-4848.202302024 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
新型冠狀病毒感染(coronavirus disease 2019,COVID-19)流行以來,千萬例以上手術因其取消和推遲[1],國際上不斷推出相應的臨床建議和共識[2]。2022年底,我國開始調整COVID-19管控政策。由于奧密克戎株的高傳染性,許多需要行心臟大血管手術的患者亦大量感染,國內對于COVID-19期行心臟大血管手術的經驗比較匱乏,因此本文通過回顧性分析18例COVID-19期接受心臟外科手術患者的臨床資料,分享我們的術后管理經驗及體會。
1 資料與方法
1.1 臨床資料
選取2022年12月7日—2023年1月5日,入住云南省阜外心血管病醫院,術前COVID-19診斷明確并行心臟大血管手術患者。納入標準:(1)年齡≥18歲;(2)體外循環下行心臟大血管手術患者;(3)依照《新型冠狀病毒感染診療方案(試行第十版)》[3]診斷COVID-19患者。排除標準:(1)其他系統嚴重合并癥;(2)資料不全的患者。
1.2 COVID-19診斷
病原學診斷標準:呼吸道標本(鼻/咽拭子或支氣管分泌物/肺泡灌洗液)新型冠狀病毒核酸和/或抗原檢測陽性。
根據《新型冠狀病毒感染診療方案(試行第十版)》[3],進展為重型/危重型高危人群的高危因素包括:年齡>65歲,尤其是未全程接種新型冠狀病毒疫苗者;有心腦血管疾病(含高血壓)、慢性肺部疾病、糖尿病、慢性肝臟、腎臟疾病,腫瘤等基礎疾病以及維持性透析患者;免疫功能缺陷(如艾滋病患者、長期使用皮質類固醇或其他免疫抑制藥物導致免疫功能減退狀態);肥胖(體重指數≥30 kg/m2);晚期妊娠和圍產期女性;重度吸煙者。
1.3 數據收集內容
1.3.1 常規病史
年齡、性別、體重指數、糖尿病史、高血壓史、高脂血癥史、吸煙史、飲酒史、慢性阻塞性肺疾病史、慢性肝腎功能不全病史。
1.3.2 COVID-19病史
新型冠狀病毒疫苗接種情況(何種疫苗、接種次數、何時完成最后一劑)、診斷COVID-19依據(新型冠狀病毒核酸和/或抗原檢測陽性)、感染期間臨床表現(發熱、咽痛、乏力、咳嗽、心慌、頭痛及四肢疼痛等)、是否服用抗病毒藥物。
1.3.3 手術相關信息
手術名稱、手術時間、手術時長、體外循環時間、主動脈阻斷時間等。
1.3.4 圍術期化驗檢查
常規檢測:血常規、血生化檢測;生物標記物檢測:心肌梗死三項、腦鈉肽、N端腦鈉肽前體、腫瘤標記物。炎癥指標監測:C反應蛋白、炎癥因子、紅細胞沉降率、降鈣素原、鐵蛋白等。凝血全項檢測:凝血四項+D二聚體+纖維蛋白降解產物。氧合指標:經皮氧飽和度、血氣分析。
1.3.5 術后監護情況
機械通氣時間、應用高流量氧療情況、住ICU時間、術后并發癥、術后機械輔助情況、心肌梗死、腦卒中、肺栓塞、急性腎損傷、二次開胸止血、全因死亡、心因性死亡等。
1.4 統計學分析
使用SPSS 24.0軟件和Office Excel 2021軟件進行統計分析和表格繪制。服從正態分布的計量資料以均數±標準差(x±s)描述;不服從正態分布的計量資料以中位數(上下四分位數)[M(P25,P75)]描述。計數資料以頻數和/或百分比(%)描述。
1.5 倫理審查
本研究已通過云南省阜外心血管病醫院倫理委員會審查,批準號:2022-094-01。
2 結果
2.1 基本情況
共納入患者18例,其中男11例(61.1%)、女7例(38.9%),平均年齡(58.1±10.9)歲,平均體重(60.6±12.4)kg。既往高血壓7例、糖尿病5例;既往合并呼吸系統疾病3例(哮喘、慢性阻塞性肺疾病、慢性支氣管炎各1例)、合并慢性腎功能不全2例。急診手術5例(27.8%),擇期手術13例(72.2%);見表1。
2.2 COVID-19情況
本組18例患者均為術前感染新型冠狀病毒(新型冠狀病毒核酸和/或抗原檢測陽性),末次核酸和/或抗原檢測陽性時間距手術時間為1.50(1.00,6.25)d。術前疫苗接種情況:12例(66.7%)患者接種3針疫苗,5例(27.8%)患者接種2針疫苗,1例(5.6%)患者因高血壓控制不佳,從未接種疫苗。術前COVID-19癥狀:發熱16例,咳嗽13例,咽痛10例,呼吸急促1例,無明顯不適癥狀2例。影像學改變:術前出現肺部影像學改變8例,其中肺CT平掃及胸部X線片表現為斑片影3例,肺紋理增粗、紊亂3例,滲出改變2例。全組病例術前均未行抗病毒治療。
繼發感染:全組患者觀察期內,除1例重癥患者(病例12)術后合并真菌感染,其余無任何病例出現院內感染。
2.3 術后轉歸
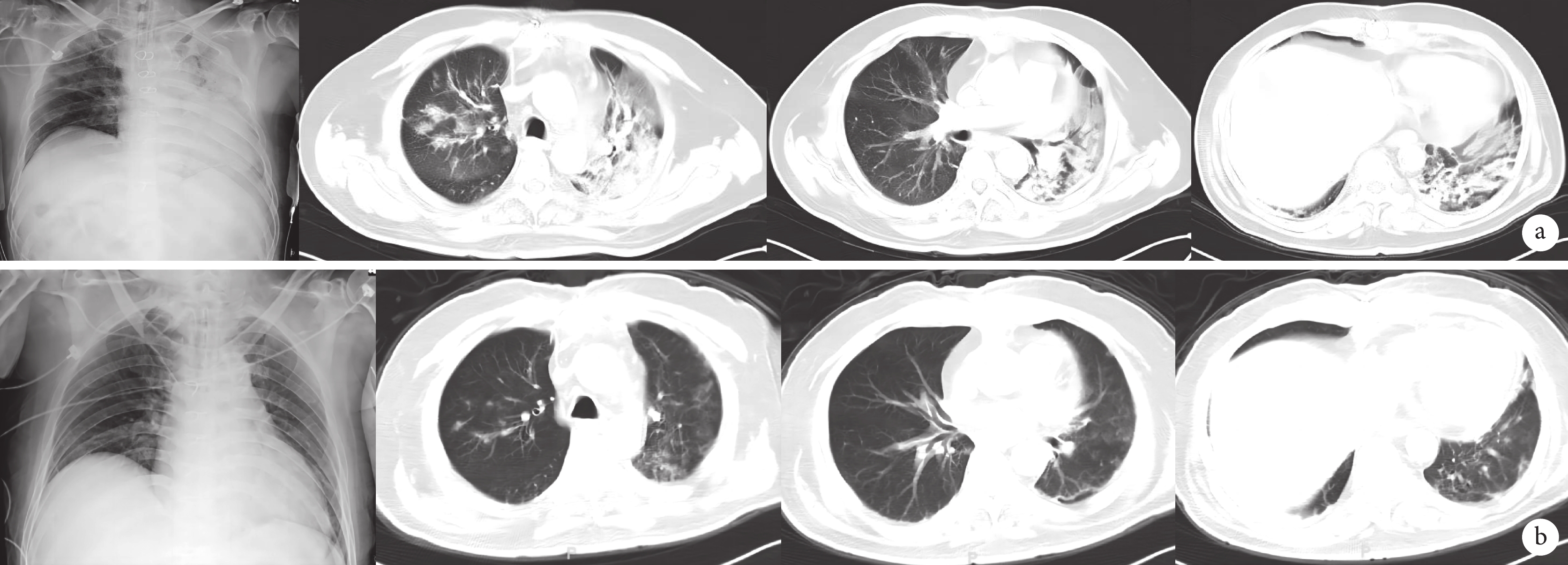
本組患者均順利實施心臟大血管手術,未出現外科相關并發癥。18例患者死亡1例(5.6%),其余患者均好轉。術后3例進展為肺炎:病例5為急性A型主動脈夾層急診手術患者,術前合并重度哮喘,未接種新型冠狀病毒疫苗,入院時呼吸急促,呼吸頻率>30次/min,術前影像學改變最為嚴重,肺部CT表現為雙肺多發片狀密度增高影及斑片、片絮模糊影(圖1),術后兩次撤離有創通氣后均出現哮喘發作狀態,胸部X線片表現為單肺(左側)透光度降低,肺部CT示雙肺多發斑片影、滲出,雙下肺背段實變,行氣管切開后影像學表現有所好轉,但患者出現肝腎功能衰竭、凝血功能紊亂、消化道出血、多臟器功能衰竭死亡。病例12,行冠狀動脈旁路移植手術,術后早期恢復良好,術后第8 d因低氧予高流量氧療,同時因肌酐進行性升高,予持續床旁血液濾過治療,術后第11 d因肺部感染加重,再次氣管插管行有創機械通氣,積極氣管切開、纖維支氣管鏡灌洗、俯臥位通氣及抗病毒治療(奈瑪特韋片/利托那韋片,英文名 Paxlovid)后,影像學明顯改善(圖2);炎癥指標下降,肺部感染得到有效控制。該患者術后常規雙聯抗血小板(阿司匹林+氯吡格雷)治療,病程中發現深靜脈血栓形成,神經系統表現為意識喪失,影像學(頭顱CT及磁共振成像)均未見明顯異常,疑似微血栓形成,經過抗凝治療(肝素泵入維持活化凝血時間 160~180 s,過渡至低分子肝素,再過渡至華法林鼻飼),5 d后蘇醒,進入康復階段。病例17,因圍術期感染新型冠狀病毒,劇烈咳嗽,導致胸骨正中切口愈合不良,行清創手術,術后體溫高、痰液量多、胸部X線片表現為雙下肺斑片影,予Paxlovid抗病毒治療,恢復順利。其余15例患者術后均轉歸良好,無重大并發癥。
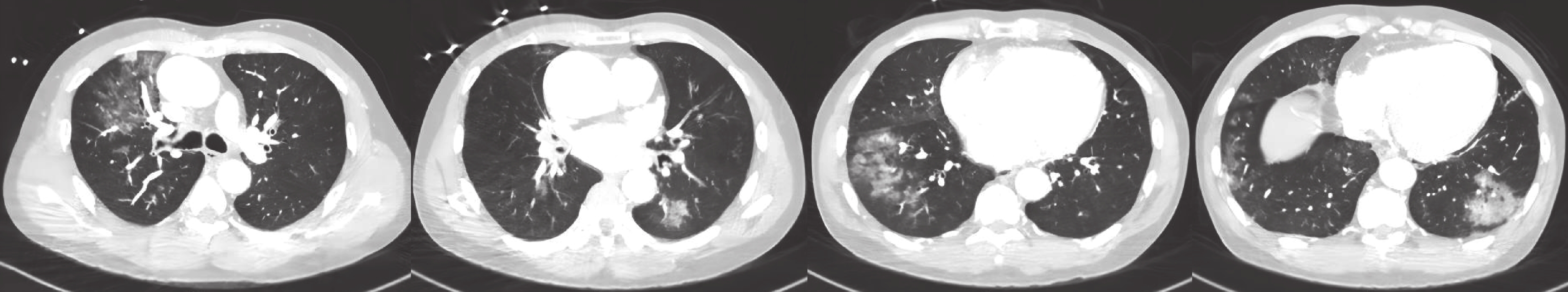
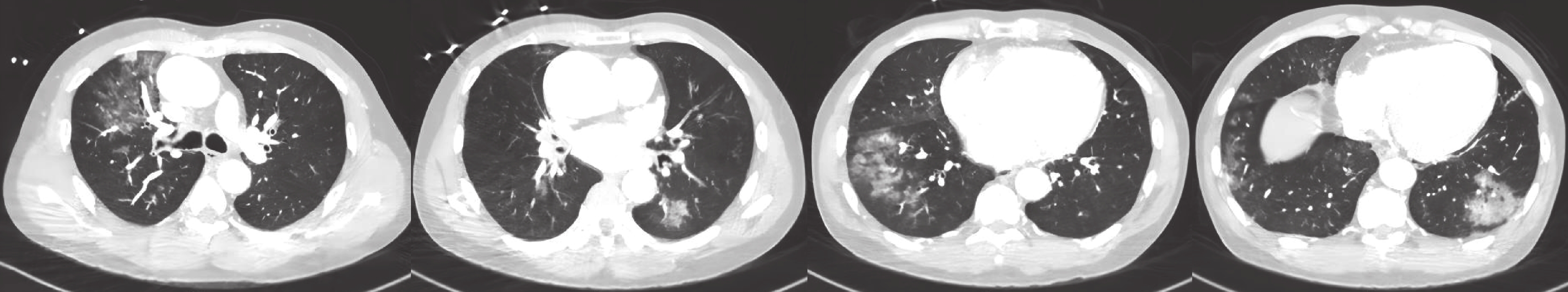 圖1
病例5術前肺部CT表現為雙肺多發片狀密度增高影及斑片、片絮模糊影
圖1
病例5術前肺部CT表現為雙肺多發片狀密度增高影及斑片、片絮模糊影
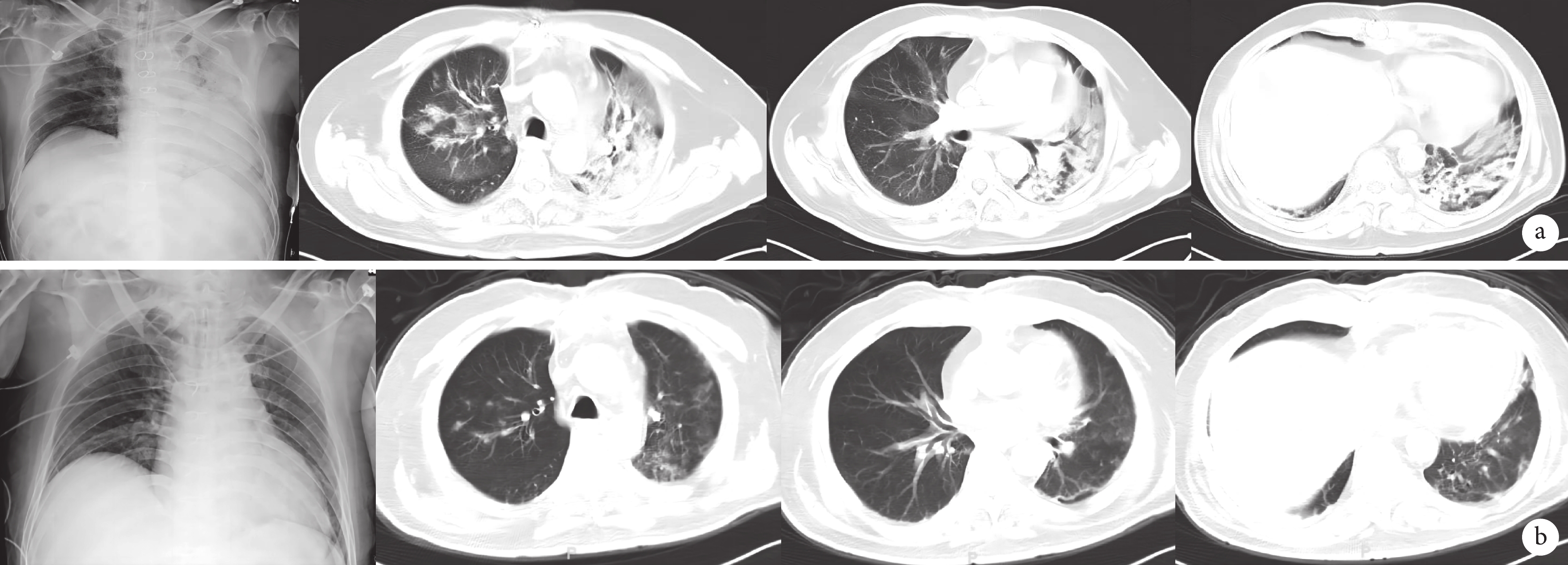 圖2
病例12影像學表現
圖2
病例12影像學表現
a:治療前影像學表現;b:治療后影像學表現
3 討論
本研究中,8例患者術前即出現影像學改變,其中3例擇期手術患者表現為輕度影像學改變,主要為肺紋理增粗、紊亂,無滲出表現,術后恢復順利;另5例急診手術患者,術后均有不同程度機械通氣時間延長,死亡病例(病例5)影像學改變最為嚴重(圖1),且術后肺部病變加重,提示COVID-19合并嚴重影像學改變患者行心臟大血管手術風險較高。
除影像學表現嚴重外,本研究中唯一的死亡病例(病例5)特點非常突出:既往哮喘病史,未注射新型冠狀病毒疫苗,基礎病變重(高血壓、急性A型主動脈夾層);另1例心臟術后重癥肺炎患者(病例 12)術前合并慢性腎功能不全。上述特點均提示:具有高危因素患者,進展為COVID-19急危重癥患者的可能性大大增加,后期病情惡化進展迅速,短時間內即進展為多臟器功能衰竭,臨床診療決策宜盡早實施,重拳猛擊。本組中3例患者接受了抗病毒治療:死亡患者抗病毒治療藥物為阿茲夫定,其他COVID-19治療包括:拖珠單抗、巴瑞替尼、激素;2例存活好轉患者方案為Paxlovid,其中1例聯用巴瑞替尼+激素,另1例肺炎相對較輕,僅以Paxlovid抗病毒治療。通過觀察,我們建議針對COVID-19需行急診心臟大血管手術患者,宜在病程初期積極抗病毒治療,且首選Paxlovid。本組2例氣管切開患者均在氣管切開后發生病情好轉征象,且影像學改善明顯(圖2),因此我們認為,當不可避免進展為急危重癥患者時,宜盡早行氣管切開[4]。俯臥位通氣治療避免了因低氧導致二次氣管插管、縮短機械通氣時間及住ICU時間[5-6]。本組2例重癥肺炎患者均行俯臥位通氣治療,氧合改善明顯。2020年一項研究[7]顯示COVID-19后期繼發細菌感染率約為14.3%,對于行心臟大血管手術者,一旦出現繼發感染,患者的病死率將顯著升高[8],因此繼發感染的防治一定是以預防為主。建議:積極尋找病原學依據,包括痰、血液、支氣管肺泡灌洗液培養等,對于急危重癥患者,可行病原微生物宏基因組檢測,即高通量測序(NGS),以縮短等待病原學結果時間,提早應用敏感抗生素針對性抗感染治療;能以無創通氣或高流量氧療支持,盡量避免氣管插管;積極采取清醒俯臥位; 早期氣管切開(3~5 d內);預防性使用抗生素等。全組患者觀察期內,除1例重癥患者(病例12)術后合并真菌感染,其余無任何病例出現院內感染,分析原因可能與加強感控措施及預防性應用抗菌藥物有關。
本研究中,1例(5.6%)患者術后出現血栓栓塞事件。COVID-19誘發的血栓問題正越來越多受到重視。急性COVID-19患者非常常見靜脈血栓栓塞,包括廣泛深靜脈血栓形成和肺栓塞[9-10],靜脈血栓栓塞在ICU患者中的發生率可達33.3%,即使給予預防性抗凝治療也可能發生[11]。心臟大血管手術后早期患者出血風險較高,但后期可能轉為高凝狀態,再有COVID-19加持,應重視對于此類患者的抗凝治療,以降低血栓發生風險,但同時亦須警惕出血事件的發生。
對于COVID-19患者的心臟大血管外科手術的時機選擇,目前仍沒有共識。近3年來,國外有一些文獻報道,合并COVID-19患者行心外科手術,術后并發癥和住院費用明顯增多[12],認為應根據患者病情的緊急程度決策手術時機[13]:(1)以急性A型主動脈夾層為代表危及生命的急危重癥患者,需急診手術治療;(2)擇期手術患者,建議在COVID-19后至少6~7周才考慮進行手術治療,若患者癥狀加重需急診處理,則盡量采用介入、微創等方式進行治療;(3)對于患有糖尿病、免疫功能低下或住院的有癥狀患者,需要8~10周;(4)患者因COVID-19需要入住ICU,應至少12周后再考慮手術[14]。然而上述研究建議基本基于COVID-19原始毒株或德爾塔毒株,目前流行的奧密克戎毒株毒力較前已有所降低,該毒株流行期間心外科手術的風險需再次評估。
綜上所述,具有高危因素的COVID-19患者(影像學改變嚴重、腎功能不全等),在COVID-19期行心臟大血管手術極有可能快速進展為重癥肺炎,增加手術風險[15]。我們建議:擇期手術患者,術前有肺部影像學改變或合并其他臟器基礎病變患者尤為高危,若病情允許應考慮延遲手術;急診手術患者,接診后盡早抗病毒治療,搶占黃金72 h,術后如發展為重癥肺炎,積極行氣管切開及俯臥位通氣,可能有助于改善患者總體預后。感染中后期聯用激素、白細胞介素-6受體抑制劑、JAK 抑制劑有助于調節免疫,同時也應積極防治院內感染。積極抗凝、抗血小板治療同時也要警惕出血風險。本研究涉及病例數較少,存在較大的局限性,期待國內多中心前瞻性研究提供更多的治療建議。
利益沖突:無。
作者貢獻:常碩醞釀、設計、實施研究,采集、分析、解釋數據,起草文章,對文章的知識性內容作批評性審閱;張心怡采集、分析、解釋數據;黃晟實施研究,采集、分析、解釋數據;范宇欣醞釀和設計研究,采集、分析、解釋數據;潘湘斌醞釀和設計研究,對文章的知識性內容作批評性審閱,獲取研究經費,行政、技術或材料支持,指導研究,對研究有支持性貢獻;王小啟醞釀、設計、實施研究,對文章的知識性內容作批評性審閱,獲取研究經費,行政、技術或材料支持,指導研究,對研究有支持性貢獻。
新型冠狀病毒感染(coronavirus disease 2019,COVID-19)流行以來,千萬例以上手術因其取消和推遲[1],國際上不斷推出相應的臨床建議和共識[2]。2022年底,我國開始調整COVID-19管控政策。由于奧密克戎株的高傳染性,許多需要行心臟大血管手術的患者亦大量感染,國內對于COVID-19期行心臟大血管手術的經驗比較匱乏,因此本文通過回顧性分析18例COVID-19期接受心臟外科手術患者的臨床資料,分享我們的術后管理經驗及體會。
1 資料與方法
1.1 臨床資料
選取2022年12月7日—2023年1月5日,入住云南省阜外心血管病醫院,術前COVID-19診斷明確并行心臟大血管手術患者。納入標準:(1)年齡≥18歲;(2)體外循環下行心臟大血管手術患者;(3)依照《新型冠狀病毒感染診療方案(試行第十版)》[3]診斷COVID-19患者。排除標準:(1)其他系統嚴重合并癥;(2)資料不全的患者。
1.2 COVID-19診斷
病原學診斷標準:呼吸道標本(鼻/咽拭子或支氣管分泌物/肺泡灌洗液)新型冠狀病毒核酸和/或抗原檢測陽性。
根據《新型冠狀病毒感染診療方案(試行第十版)》[3],進展為重型/危重型高危人群的高危因素包括:年齡>65歲,尤其是未全程接種新型冠狀病毒疫苗者;有心腦血管疾病(含高血壓)、慢性肺部疾病、糖尿病、慢性肝臟、腎臟疾病,腫瘤等基礎疾病以及維持性透析患者;免疫功能缺陷(如艾滋病患者、長期使用皮質類固醇或其他免疫抑制藥物導致免疫功能減退狀態);肥胖(體重指數≥30 kg/m2);晚期妊娠和圍產期女性;重度吸煙者。
1.3 數據收集內容
1.3.1 常規病史
年齡、性別、體重指數、糖尿病史、高血壓史、高脂血癥史、吸煙史、飲酒史、慢性阻塞性肺疾病史、慢性肝腎功能不全病史。
1.3.2 COVID-19病史
新型冠狀病毒疫苗接種情況(何種疫苗、接種次數、何時完成最后一劑)、診斷COVID-19依據(新型冠狀病毒核酸和/或抗原檢測陽性)、感染期間臨床表現(發熱、咽痛、乏力、咳嗽、心慌、頭痛及四肢疼痛等)、是否服用抗病毒藥物。
1.3.3 手術相關信息
手術名稱、手術時間、手術時長、體外循環時間、主動脈阻斷時間等。
1.3.4 圍術期化驗檢查
常規檢測:血常規、血生化檢測;生物標記物檢測:心肌梗死三項、腦鈉肽、N端腦鈉肽前體、腫瘤標記物。炎癥指標監測:C反應蛋白、炎癥因子、紅細胞沉降率、降鈣素原、鐵蛋白等。凝血全項檢測:凝血四項+D二聚體+纖維蛋白降解產物。氧合指標:經皮氧飽和度、血氣分析。
1.3.5 術后監護情況
機械通氣時間、應用高流量氧療情況、住ICU時間、術后并發癥、術后機械輔助情況、心肌梗死、腦卒中、肺栓塞、急性腎損傷、二次開胸止血、全因死亡、心因性死亡等。
1.4 統計學分析
使用SPSS 24.0軟件和Office Excel 2021軟件進行統計分析和表格繪制。服從正態分布的計量資料以均數±標準差(x±s)描述;不服從正態分布的計量資料以中位數(上下四分位數)[M(P25,P75)]描述。計數資料以頻數和/或百分比(%)描述。
1.5 倫理審查
本研究已通過云南省阜外心血管病醫院倫理委員會審查,批準號:2022-094-01。
2 結果
2.1 基本情況
共納入患者18例,其中男11例(61.1%)、女7例(38.9%),平均年齡(58.1±10.9)歲,平均體重(60.6±12.4)kg。既往高血壓7例、糖尿病5例;既往合并呼吸系統疾病3例(哮喘、慢性阻塞性肺疾病、慢性支氣管炎各1例)、合并慢性腎功能不全2例。急診手術5例(27.8%),擇期手術13例(72.2%);見表1。
2.2 COVID-19情況
本組18例患者均為術前感染新型冠狀病毒(新型冠狀病毒核酸和/或抗原檢測陽性),末次核酸和/或抗原檢測陽性時間距手術時間為1.50(1.00,6.25)d。術前疫苗接種情況:12例(66.7%)患者接種3針疫苗,5例(27.8%)患者接種2針疫苗,1例(5.6%)患者因高血壓控制不佳,從未接種疫苗。術前COVID-19癥狀:發熱16例,咳嗽13例,咽痛10例,呼吸急促1例,無明顯不適癥狀2例。影像學改變:術前出現肺部影像學改變8例,其中肺CT平掃及胸部X線片表現為斑片影3例,肺紋理增粗、紊亂3例,滲出改變2例。全組病例術前均未行抗病毒治療。
繼發感染:全組患者觀察期內,除1例重癥患者(病例12)術后合并真菌感染,其余無任何病例出現院內感染。
2.3 術后轉歸
本組患者均順利實施心臟大血管手術,未出現外科相關并發癥。18例患者死亡1例(5.6%),其余患者均好轉。術后3例進展為肺炎:病例5為急性A型主動脈夾層急診手術患者,術前合并重度哮喘,未接種新型冠狀病毒疫苗,入院時呼吸急促,呼吸頻率>30次/min,術前影像學改變最為嚴重,肺部CT表現為雙肺多發片狀密度增高影及斑片、片絮模糊影(圖1),術后兩次撤離有創通氣后均出現哮喘發作狀態,胸部X線片表現為單肺(左側)透光度降低,肺部CT示雙肺多發斑片影、滲出,雙下肺背段實變,行氣管切開后影像學表現有所好轉,但患者出現肝腎功能衰竭、凝血功能紊亂、消化道出血、多臟器功能衰竭死亡。病例12,行冠狀動脈旁路移植手術,術后早期恢復良好,術后第8 d因低氧予高流量氧療,同時因肌酐進行性升高,予持續床旁血液濾過治療,術后第11 d因肺部感染加重,再次氣管插管行有創機械通氣,積極氣管切開、纖維支氣管鏡灌洗、俯臥位通氣及抗病毒治療(奈瑪特韋片/利托那韋片,英文名 Paxlovid)后,影像學明顯改善(圖2);炎癥指標下降,肺部感染得到有效控制。該患者術后常規雙聯抗血小板(阿司匹林+氯吡格雷)治療,病程中發現深靜脈血栓形成,神經系統表現為意識喪失,影像學(頭顱CT及磁共振成像)均未見明顯異常,疑似微血栓形成,經過抗凝治療(肝素泵入維持活化凝血時間 160~180 s,過渡至低分子肝素,再過渡至華法林鼻飼),5 d后蘇醒,進入康復階段。病例17,因圍術期感染新型冠狀病毒,劇烈咳嗽,導致胸骨正中切口愈合不良,行清創手術,術后體溫高、痰液量多、胸部X線片表現為雙下肺斑片影,予Paxlovid抗病毒治療,恢復順利。其余15例患者術后均轉歸良好,無重大并發癥。
 圖1
病例5術前肺部CT表現為雙肺多發片狀密度增高影及斑片、片絮模糊影
圖1
病例5術前肺部CT表現為雙肺多發片狀密度增高影及斑片、片絮模糊影
 圖2
病例12影像學表現
圖2
病例12影像學表現
a:治療前影像學表現;b:治療后影像學表現
3 討論
本研究中,8例患者術前即出現影像學改變,其中3例擇期手術患者表現為輕度影像學改變,主要為肺紋理增粗、紊亂,無滲出表現,術后恢復順利;另5例急診手術患者,術后均有不同程度機械通氣時間延長,死亡病例(病例5)影像學改變最為嚴重(圖1),且術后肺部病變加重,提示COVID-19合并嚴重影像學改變患者行心臟大血管手術風險較高。
除影像學表現嚴重外,本研究中唯一的死亡病例(病例5)特點非常突出:既往哮喘病史,未注射新型冠狀病毒疫苗,基礎病變重(高血壓、急性A型主動脈夾層);另1例心臟術后重癥肺炎患者(病例 12)術前合并慢性腎功能不全。上述特點均提示:具有高危因素患者,進展為COVID-19急危重癥患者的可能性大大增加,后期病情惡化進展迅速,短時間內即進展為多臟器功能衰竭,臨床診療決策宜盡早實施,重拳猛擊。本組中3例患者接受了抗病毒治療:死亡患者抗病毒治療藥物為阿茲夫定,其他COVID-19治療包括:拖珠單抗、巴瑞替尼、激素;2例存活好轉患者方案為Paxlovid,其中1例聯用巴瑞替尼+激素,另1例肺炎相對較輕,僅以Paxlovid抗病毒治療。通過觀察,我們建議針對COVID-19需行急診心臟大血管手術患者,宜在病程初期積極抗病毒治療,且首選Paxlovid。本組2例氣管切開患者均在氣管切開后發生病情好轉征象,且影像學改善明顯(圖2),因此我們認為,當不可避免進展為急危重癥患者時,宜盡早行氣管切開[4]。俯臥位通氣治療避免了因低氧導致二次氣管插管、縮短機械通氣時間及住ICU時間[5-6]。本組2例重癥肺炎患者均行俯臥位通氣治療,氧合改善明顯。2020年一項研究[7]顯示COVID-19后期繼發細菌感染率約為14.3%,對于行心臟大血管手術者,一旦出現繼發感染,患者的病死率將顯著升高[8],因此繼發感染的防治一定是以預防為主。建議:積極尋找病原學依據,包括痰、血液、支氣管肺泡灌洗液培養等,對于急危重癥患者,可行病原微生物宏基因組檢測,即高通量測序(NGS),以縮短等待病原學結果時間,提早應用敏感抗生素針對性抗感染治療;能以無創通氣或高流量氧療支持,盡量避免氣管插管;積極采取清醒俯臥位; 早期氣管切開(3~5 d內);預防性使用抗生素等。全組患者觀察期內,除1例重癥患者(病例12)術后合并真菌感染,其余無任何病例出現院內感染,分析原因可能與加強感控措施及預防性應用抗菌藥物有關。
本研究中,1例(5.6%)患者術后出現血栓栓塞事件。COVID-19誘發的血栓問題正越來越多受到重視。急性COVID-19患者非常常見靜脈血栓栓塞,包括廣泛深靜脈血栓形成和肺栓塞[9-10],靜脈血栓栓塞在ICU患者中的發生率可達33.3%,即使給予預防性抗凝治療也可能發生[11]。心臟大血管手術后早期患者出血風險較高,但后期可能轉為高凝狀態,再有COVID-19加持,應重視對于此類患者的抗凝治療,以降低血栓發生風險,但同時亦須警惕出血事件的發生。
對于COVID-19患者的心臟大血管外科手術的時機選擇,目前仍沒有共識。近3年來,國外有一些文獻報道,合并COVID-19患者行心外科手術,術后并發癥和住院費用明顯增多[12],認為應根據患者病情的緊急程度決策手術時機[13]:(1)以急性A型主動脈夾層為代表危及生命的急危重癥患者,需急診手術治療;(2)擇期手術患者,建議在COVID-19后至少6~7周才考慮進行手術治療,若患者癥狀加重需急診處理,則盡量采用介入、微創等方式進行治療;(3)對于患有糖尿病、免疫功能低下或住院的有癥狀患者,需要8~10周;(4)患者因COVID-19需要入住ICU,應至少12周后再考慮手術[14]。然而上述研究建議基本基于COVID-19原始毒株或德爾塔毒株,目前流行的奧密克戎毒株毒力較前已有所降低,該毒株流行期間心外科手術的風險需再次評估。
綜上所述,具有高危因素的COVID-19患者(影像學改變嚴重、腎功能不全等),在COVID-19期行心臟大血管手術極有可能快速進展為重癥肺炎,增加手術風險[15]。我們建議:擇期手術患者,術前有肺部影像學改變或合并其他臟器基礎病變患者尤為高危,若病情允許應考慮延遲手術;急診手術患者,接診后盡早抗病毒治療,搶占黃金72 h,術后如發展為重癥肺炎,積極行氣管切開及俯臥位通氣,可能有助于改善患者總體預后。感染中后期聯用激素、白細胞介素-6受體抑制劑、JAK 抑制劑有助于調節免疫,同時也應積極防治院內感染。積極抗凝、抗血小板治療同時也要警惕出血風險。本研究涉及病例數較少,存在較大的局限性,期待國內多中心前瞻性研究提供更多的治療建議。
利益沖突:無。
作者貢獻:常碩醞釀、設計、實施研究,采集、分析、解釋數據,起草文章,對文章的知識性內容作批評性審閱;張心怡采集、分析、解釋數據;黃晟實施研究,采集、分析、解釋數據;范宇欣醞釀和設計研究,采集、分析、解釋數據;潘湘斌醞釀和設計研究,對文章的知識性內容作批評性審閱,獲取研究經費,行政、技術或材料支持,指導研究,對研究有支持性貢獻;王小啟醞釀、設計、實施研究,對文章的知識性內容作批評性審閱,獲取研究經費,行政、技術或材料支持,指導研究,對研究有支持性貢獻。