引用本文: 馬曉中, 張韶鵬, 白云鵬, 吳振華, 趙豐, 陳慶良, 姜楠. 低劑量吸入性一氧化氮治療孫氏手術術后嚴重低氧血癥療效的回顧性隊列研究. 中國胸心血管外科臨床雜志, 2024, 31(5): 762-767. doi: 10.7507/1007-4848.202310042 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
急性A型主動脈夾層(acute type A aortic dissection,ATAAD)是心血管領域內最危險、致死率最高的疾病類型之一,其發病48 h內死亡率高達50%以上[1]。目前國內治療ATAAD的經典術式仍為孫氏手術,盡管如此,孫氏手術患者在技術成熟的心臟中心仍有7%~10%的死亡率以及較高的術后并發癥發生率[2-3]。術后低氧血癥是ATAAD孫氏手術術后常見的一種并發癥,發生率為30%~50%[4],盡管術后低氧血癥具體的發生機制尚未闡明,但Song等[5]的研究顯示,可能與深低溫停循環、體外循環時間、缺血-再灌注損傷、大量輸庫存血和炎癥反應等因素密切相關,低氧血癥又與肺血管收縮相互因果,進一步導致肺通氣血流比例失調和肺內分流[6]。長時間的低氧血癥不僅會延長住院時間、增加住院費用,還會增加除肺以外臟器的并發癥,甚至增加患者圍手術期死亡率,目前相關的干預治療效果作用有限。一氧化氮(nitric oxide,NO)是一種選擇性肺血管擴張劑,是急性呼吸窘迫綜合征(acute respiratory distress syndrome,ARDS)、肺動脈高壓等疾病的常規治療手段之一,可以明顯改善氧合[7-8]。目前由于缺乏吸入性一氧化氮(inhaled nitric oxide,iNO)治療孫氏手術術后低氧血癥的隨機對照或病例對照研究,本研究回顧性比較低劑量iNO治療與傳統治療孫氏手術術后嚴重低氧血癥的療效和安全性。
1 資料與方法
1.1 臨床資料和分組
所有患者在術前均需進行主動脈CT血管造影(computered tomograhy angiography,CTA)和超聲心動圖檢查,根據主動脈夾層Stanford分型,凡是累及升主動脈的夾層均為Stanford A型主動脈夾層。選取2020年1月—2022年6月我科收治的ATAAD行孫氏手術術后發生嚴重低氧血癥的患者,手術均為同一手術團隊進行。2021年11月之前孫氏手術術后嚴重低氧血癥患者采用的是常規治療(對照組),2021年11月之后我院開始使用低劑量iNO治療(iNO組)。
納入標準:(1)行孫氏手術不除外同期行主動脈根部處理患者;(2)術后6 h內氧合指數(PaO2/FiO2)≤100 mm Hg(1 mm Hg=0.133 kPa)且無氣胸、肺氣腫、心源性肺水腫、胸腔積液及肺不張等原因引起的肺功能不全。排除標準:(1)術前發生嚴重低氧血癥;(2)同期行冠狀動脈搭橋手術、非主動脈瓣位瓣膜手術、肺部手術或合并其他臟器手術;(3)術后72 h內死亡;(4)術后發生腦梗死、截癱。
1.2 治療方法
1.2.1 手術方法
仰臥位,全身麻醉,消毒。前正中切口,劈開胸骨,肝素化,經股動脈、右心房插管建立體外循環,并降體溫,植入左房管。32℃阻斷橫竇,切開主動脈,注停跳液。懸吊外膜,探查主動脈根部,根據情況行主動脈根部重建或成形術。降溫至28℃左右,阻斷頭臂血管,停循環,順行沿無名動脈選擇性腦灌注或者行無名動脈與左頸總動脈雙側腦灌注,于鎖骨下動脈開口降主動脈順行植入術中支架,連續縫合四分支人工血管遠端和降主動脈支架近端,開放循環,再吻合四分支血管近端和主動脈根部,升溫排氣、復跳。依次吻合無名動脈、左頸總動脈、左鎖骨下動脈和人工血管分支。升主動脈持續引流,心率、血壓平穩后減流量停止體外循環,超濾。撤出體外循環管路,魚精蛋白中和肝素,止血,置心表臨時起搏導線、置縱隔、心包(或胸腔)引流管,關胸,手術完畢送入ICU。
1.2.2 對照組治療方法
(1)根據患者的胸部X線片、心臟彩色超聲(彩超)、胸部彩超、血氣分析等檢查,優化呼吸機參數設置,包括潮氣量和呼氣末正壓通氣(positive end expiratory pressure,PEEP)調節;(2)胸腔閉式引流及時干預胸腔積液或氣胸;(3)優化全身容量管理,維持良好的心臟功能;(4)給予甲潑尼龍40 mg、烏司他丁30萬單位靜脈滴注,每日2次,連用3 d;(5)必要時拔管后予以無創通氣支持。
1.2.3 iNO組治療方法
手術完畢送入ICU 6 h內在常規方法基礎上嚴重低氧血癥患者,使用低流量5 ppm iNO治療。應用NO通氣設備(SLE3600 INOSYS,英國)將NO氣體連接于呼吸機進氣管路,吸入流量約20~60 mL/min,調節流量使NO濃度保持體積分數為5 ppm。把監測NO和NO2濃度的氣體流量監測儀(LZK-200,杭州)與呼吸機回氣管路連接,保持NO2濃度≤3 ppm。如果FiO2<0.6,PaO2/FiO2>150 mm Hg能維持6 h以上,則停用iNO。
1.2.4 呼吸機拔管標準
(1)患者可被喚醒,神智清楚,肌力正常,可遵囑配合;(2)自主呼吸測試正常,血氣結果滿意,當FiO2≤0.5、PEEP≤5 cm H2O(1 cm H2O=0.098 kPa)時,PaO2≥80 mm Hg、PaCO2<45 mm Hg;(3)血流動力學穩定,無低心排血量綜合征或心肌缺血征象,或小劑量強心藥物支持[去甲腎上腺素或腎上腺素≤0.05 μg/(kg·min)];(4)無活動性出血,胸腔引流量≤50 mL/h。
1.3 終點事件和術后并發癥
主要終點事件:呼吸機通氣時間;術后住ICU時間;術后氧合指數變化。次要終點事件:院內死亡,術后住院時間,術后72 h引流。術后并發癥:肺感染,敗血癥,急性腎損傷(acute kidney injury,AKI),連續性腎臟替代治療(continuous renal replacement treatment,CRRT),無創通氣,再次開胸探查(出血導致的)。
1.4 相關定義
(1)低氧血癥:PaO2/FiO2≤300 mm Hg;嚴重低氧血癥:PaO2/FiO2≤100 mm Hg;(2)體重指數(body mass index,BMI)≥25 kg/m2為超重;BMI≥28 kg/m2 為肥胖;(3)AKI:在48 h內血清肌酐(Cr)上升0.3 mg/dL(≥26.5 μmol/L);已知或假定腎功能損害發生在7 d之內,Cr上升至>基礎值的1.5倍;尿量<0.5 mL/(kg·h),持續6 h。
1.5 統計學分析
采用SPSS 26.0和GraphPad Prism 5.0進行統計分析及繪圖。正態分布的計量資料以均數±標準差(x±s)描述,兩組間比較采用獨立樣本t檢驗;非正態分布的計量資料采用中位數(上下四分位數)[M(P25,P75)]描述,組間比較采用秩和檢驗。兩組術后多時間點氧合指數比較采用重復測量方差分析。計數資料以例數和率(%)表示,采用χ2 檢驗或Fisher確切概率法。P≤0.05為差異有統計學意義。
1.6 倫理審查
本研究由天津市胸科醫院倫理審查委員會批準(倫理審查批號:2023LW-015)。
2 結果
2.1 兩組術前資料比較
對照組納入54例患者,iNO組納入27例患者。對照組和iNO組基線資料(包括低氧高危因素:年齡、BMI及吸煙史等)差異無統計學意義(P>0.05)。兩組術前白細胞計數、中性粒細胞計數、血紅蛋白、血小板計數、C反應蛋白(C-reactive protein,CRP)水平及氧合指數等術前化驗指標差異均無統計學意義(P>0.05);見表1。
2.2 兩組術中資料比較
對照組和iNO組總體手術時間、體外循環時間、主動脈阻斷時間、停循環時間、術中肛溫等差異均無統計學意義(P>0.05);見表2。
2.3 兩組術后早期資料比較
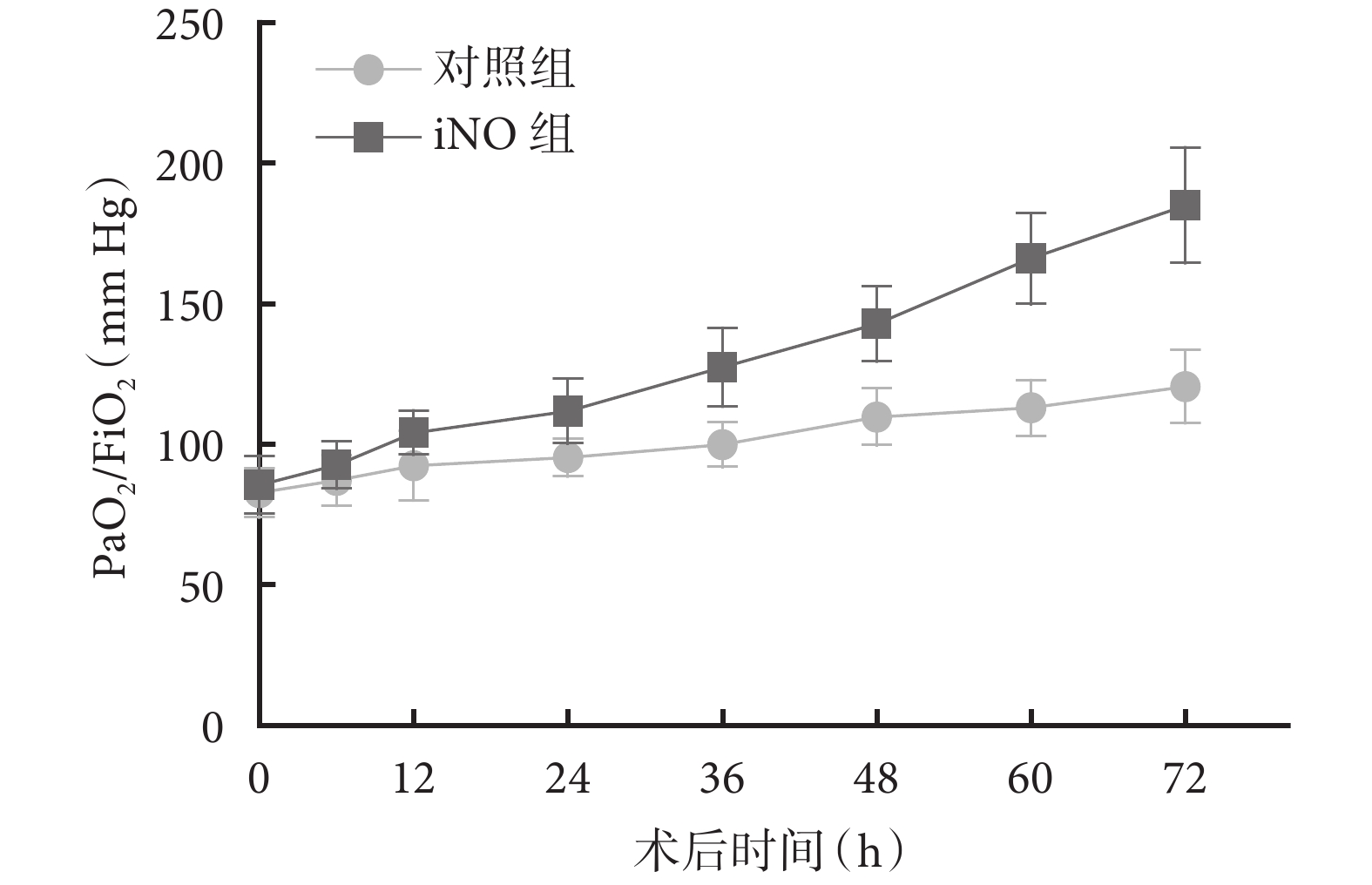
對照組和iNO組患者術后即刻氧合指數分別為(82.77±8.75)mm Hg、(85.59±10.34)mm Hg,兩組差異無統計學意義(P=0.150)。對照組和iNO組呼吸機通氣時間分別為116.5(101.5,141.2)h、93.3(83.7,105.5)h,差異有統計學意義(P<0.001);術后ICU住院時間分別為12.0(10.0,16.0)d、7.0(6.0,9.0)d,差異有統計學意義(P<0.001);兩組患者術后住院時間差異有統計學意義(P<0.001)。兩組院內死亡及術后并發癥方面差異無統計學意義(P>0.05);見表3。術后氧合指數變化見圖1。
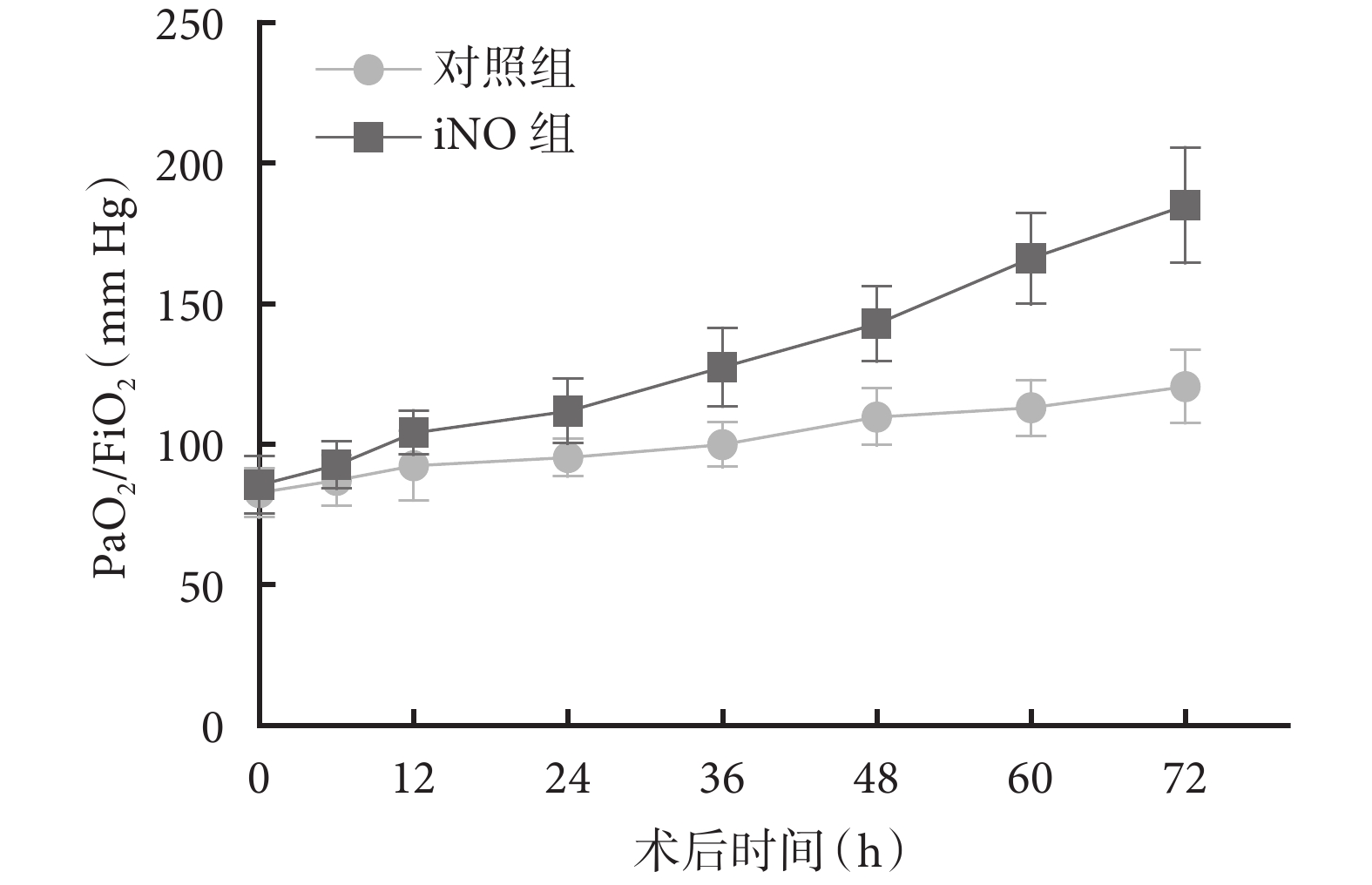 圖1
兩組患者術后氧合指數(PaO2/FiO2)比較
圖1
兩組患者術后氧合指數(PaO2/FiO2)比較
*:重復測量方差分析結果顯示
3 討論
術后嚴重低氧血癥是孫氏手術術后常見的一種并發癥,發生率高達30%~50%,不僅可以明顯延長呼吸機使用時間,還可以顯著增加病死率,與術后不良預后密切相關,影響早期治療效果[6, 9]。術后低氧與深低溫停循環、輸血、炎癥反應及肺損傷等術中因素密切相關,高齡、吸煙史、高BMI和高白細胞計數也是術后發生嚴重低氧血癥的獨立危險因素。本研究中兩組病例平均BMI均>25 kg/m2,白細胞計數和CRP也顯著高于正常值,提示低氧與上述指標密切有關,這和文獻[5, 10-11]報道一致。
Rossaint等[12]首次報道了iNO治療ARDS患者低氧血癥的作用,iNO可以迅速擴張通氣肺泡血管增加血流,改善肺通氣/血流比例,進而提升肺氧合功能。Dellinger等[13]的研究也表明低劑量iNO治療能夠顯著改善ARDS生存患者的肺功能。基于之前我們將NO應用于小兒先天性心臟病低氧的經驗,發現iNO可以明顯改善患者低氧紫紺狀態。在隨后的A型主動脈夾層孫氏手術術后低氧患者應用iNO過程中,發現NO可以顯著改善患者的氧合指數。本研究兩組術后氧合指數均<100 mm Hg,通過調節呼吸機參數,FiO2在0.8~1.0的情況下,肺氧合仍然不理想。吸入NO后,患者氧合指數改善非常迅速,12 h后iNO組顯著高于對照組,在之后的研究時間節點里,也均顯著高于對照組,在72 h時,iNO組氧合指數已接近200 mm Hg,盡管優化呼吸機各參數,包括PEEP的調整,但對照組氧合指數進展非常緩慢,提示這可能與iNO減少肺內分流,優化肺通氣/血流比有關。
有動物實驗[14-15]發現,NO 通過抑制炎癥細胞因子和氧化損傷來改善肺損傷。也有研究[16]顯示,NO在肝移植中具有良好的抗炎效果,在降低術后并發癥發生率起到了關鍵性作用,iNO治療具有較好的術后早期結果可能與其抗炎作用密切相關。既往大量研究[17-19]顯示A型主動脈夾層圍手術期內產生劇烈的炎癥反應,這與我們術前白細胞計數及CRP水平統計結果相吻合。劇烈的全身炎癥反應再加上孫氏手術的打擊,肺功能會進一步受到損害。我們可以看到, iNO組呼吸機使用時間為93.3 h,顯著短于對照組的116.5 h,ICU停留時間以及術后住院時間同樣也有顯著差別,也進一步證實了iNO能縮短機械通氣時間、ICU停留時間以及術后住院時間等。本研究還發現術后院內死亡率對照組(9.3%)高于iNO組(7.4%),但差異無統計學意義,這與Al Sulaiman等[20]的研究結果相似。我們的研究結果顯示心臟術后低氧及時應用NO治療急性肺損傷可以明顯提高氧合指數、顯著縮短患者嚴重低氧血癥的發作時間和降低發作程度,但是并不能改變術后病死率等臨床治療結果,提示孫氏手術術后病死率與低氧血癥相關性不強,主要還是與合并永久性神經功能障礙以及多臟器損害等多因素作用相關[21]。
一項ARDS研究[22]發現NO可以明顯損害腎功能,然而其機制并未闡明。另一項研究[23]也報道了iNO在肺移植患者中對腎功能的影響,但結果顯示iNO并不會使腎功能惡化。最近的臨床試驗[24]同樣證實,在心臟手術期間和之后給予NO氣體可顯著減少術后AKI及溶血。在本研究中,術后兩組 AKI 發生率以及與AKI 相關的CRRT 發生率無顯著差別,這一結果也證實了低劑量NO治療并不會加重腎功能損傷。我們推測,一方面低劑量的iNO可以減小肺血管阻力和右心負荷來增加心臟輸出量,進而腎臟可以得到充分的灌注;另一方面NO直接擴張腎臟血管,降低腎血管阻力,從而保護腎臟功能。目前的氣體檢測儀器具有很好的NO和NO2濃度監測性能,在使用過程中上述氣體的濃度和流量具有良好的穩定性。在隨后的研究中發現iNO在改善氧合的過程中并不與NO濃度呈正相關[25],低劑量的NO治療在其他研究[26-28]中也被證實是安全有效的。NO的另一個副作用是抑制血小板聚集和黏附血管內皮[29-30],導致出血時間延長。我們比較了兩組術后胸腔積液引流量以及因出血導致的再次開胸探查次數,發現組間并無顯著差異,提示低劑量的iNO治療不增加術后出血事件的發生[28]。但是根據我們以往的心臟術后治療經驗,有明確的活動性出血時不建議使用iNO治療。
本研究表明,低劑量iNO治療孫氏手術術后嚴重低氧血癥安全、有效,可以明顯縮短呼吸機使用時間、ICU停留時間和術后住院時間,且不額外增加腎功能損害,在改善患者早期臨床治療結果方面具有重要意義。本研究也存在一些不足,這是一項回顧性研究,樣本量小且來自于單一心臟中心,將來還需要前瞻性的隨機對照研究提供更多的證據。另外本研究還缺少患者的長期隨訪數據,iNO治療對出院患者的影響尚未闡明。
利益沖突:無。
作者貢獻:馬曉中、張韶鵬、白云鵬、陳慶良和姜楠負責課題的研究設計;張韶鵬、吳振華和趙豐負責患者篩選和數據收集及分析;馬曉中、白云鵬負責文章撰寫。
急性A型主動脈夾層(acute type A aortic dissection,ATAAD)是心血管領域內最危險、致死率最高的疾病類型之一,其發病48 h內死亡率高達50%以上[1]。目前國內治療ATAAD的經典術式仍為孫氏手術,盡管如此,孫氏手術患者在技術成熟的心臟中心仍有7%~10%的死亡率以及較高的術后并發癥發生率[2-3]。術后低氧血癥是ATAAD孫氏手術術后常見的一種并發癥,發生率為30%~50%[4],盡管術后低氧血癥具體的發生機制尚未闡明,但Song等[5]的研究顯示,可能與深低溫停循環、體外循環時間、缺血-再灌注損傷、大量輸庫存血和炎癥反應等因素密切相關,低氧血癥又與肺血管收縮相互因果,進一步導致肺通氣血流比例失調和肺內分流[6]。長時間的低氧血癥不僅會延長住院時間、增加住院費用,還會增加除肺以外臟器的并發癥,甚至增加患者圍手術期死亡率,目前相關的干預治療效果作用有限。一氧化氮(nitric oxide,NO)是一種選擇性肺血管擴張劑,是急性呼吸窘迫綜合征(acute respiratory distress syndrome,ARDS)、肺動脈高壓等疾病的常規治療手段之一,可以明顯改善氧合[7-8]。目前由于缺乏吸入性一氧化氮(inhaled nitric oxide,iNO)治療孫氏手術術后低氧血癥的隨機對照或病例對照研究,本研究回顧性比較低劑量iNO治療與傳統治療孫氏手術術后嚴重低氧血癥的療效和安全性。
1 資料與方法
1.1 臨床資料和分組
所有患者在術前均需進行主動脈CT血管造影(computered tomograhy angiography,CTA)和超聲心動圖檢查,根據主動脈夾層Stanford分型,凡是累及升主動脈的夾層均為Stanford A型主動脈夾層。選取2020年1月—2022年6月我科收治的ATAAD行孫氏手術術后發生嚴重低氧血癥的患者,手術均為同一手術團隊進行。2021年11月之前孫氏手術術后嚴重低氧血癥患者采用的是常規治療(對照組),2021年11月之后我院開始使用低劑量iNO治療(iNO組)。
納入標準:(1)行孫氏手術不除外同期行主動脈根部處理患者;(2)術后6 h內氧合指數(PaO2/FiO2)≤100 mm Hg(1 mm Hg=0.133 kPa)且無氣胸、肺氣腫、心源性肺水腫、胸腔積液及肺不張等原因引起的肺功能不全。排除標準:(1)術前發生嚴重低氧血癥;(2)同期行冠狀動脈搭橋手術、非主動脈瓣位瓣膜手術、肺部手術或合并其他臟器手術;(3)術后72 h內死亡;(4)術后發生腦梗死、截癱。
1.2 治療方法
1.2.1 手術方法
仰臥位,全身麻醉,消毒。前正中切口,劈開胸骨,肝素化,經股動脈、右心房插管建立體外循環,并降體溫,植入左房管。32℃阻斷橫竇,切開主動脈,注停跳液。懸吊外膜,探查主動脈根部,根據情況行主動脈根部重建或成形術。降溫至28℃左右,阻斷頭臂血管,停循環,順行沿無名動脈選擇性腦灌注或者行無名動脈與左頸總動脈雙側腦灌注,于鎖骨下動脈開口降主動脈順行植入術中支架,連續縫合四分支人工血管遠端和降主動脈支架近端,開放循環,再吻合四分支血管近端和主動脈根部,升溫排氣、復跳。依次吻合無名動脈、左頸總動脈、左鎖骨下動脈和人工血管分支。升主動脈持續引流,心率、血壓平穩后減流量停止體外循環,超濾。撤出體外循環管路,魚精蛋白中和肝素,止血,置心表臨時起搏導線、置縱隔、心包(或胸腔)引流管,關胸,手術完畢送入ICU。
1.2.2 對照組治療方法
(1)根據患者的胸部X線片、心臟彩色超聲(彩超)、胸部彩超、血氣分析等檢查,優化呼吸機參數設置,包括潮氣量和呼氣末正壓通氣(positive end expiratory pressure,PEEP)調節;(2)胸腔閉式引流及時干預胸腔積液或氣胸;(3)優化全身容量管理,維持良好的心臟功能;(4)給予甲潑尼龍40 mg、烏司他丁30萬單位靜脈滴注,每日2次,連用3 d;(5)必要時拔管后予以無創通氣支持。
1.2.3 iNO組治療方法
手術完畢送入ICU 6 h內在常規方法基礎上嚴重低氧血癥患者,使用低流量5 ppm iNO治療。應用NO通氣設備(SLE3600 INOSYS,英國)將NO氣體連接于呼吸機進氣管路,吸入流量約20~60 mL/min,調節流量使NO濃度保持體積分數為5 ppm。把監測NO和NO2濃度的氣體流量監測儀(LZK-200,杭州)與呼吸機回氣管路連接,保持NO2濃度≤3 ppm。如果FiO2<0.6,PaO2/FiO2>150 mm Hg能維持6 h以上,則停用iNO。
1.2.4 呼吸機拔管標準
(1)患者可被喚醒,神智清楚,肌力正常,可遵囑配合;(2)自主呼吸測試正常,血氣結果滿意,當FiO2≤0.5、PEEP≤5 cm H2O(1 cm H2O=0.098 kPa)時,PaO2≥80 mm Hg、PaCO2<45 mm Hg;(3)血流動力學穩定,無低心排血量綜合征或心肌缺血征象,或小劑量強心藥物支持[去甲腎上腺素或腎上腺素≤0.05 μg/(kg·min)];(4)無活動性出血,胸腔引流量≤50 mL/h。
1.3 終點事件和術后并發癥
主要終點事件:呼吸機通氣時間;術后住ICU時間;術后氧合指數變化。次要終點事件:院內死亡,術后住院時間,術后72 h引流。術后并發癥:肺感染,敗血癥,急性腎損傷(acute kidney injury,AKI),連續性腎臟替代治療(continuous renal replacement treatment,CRRT),無創通氣,再次開胸探查(出血導致的)。
1.4 相關定義
(1)低氧血癥:PaO2/FiO2≤300 mm Hg;嚴重低氧血癥:PaO2/FiO2≤100 mm Hg;(2)體重指數(body mass index,BMI)≥25 kg/m2為超重;BMI≥28 kg/m2 為肥胖;(3)AKI:在48 h內血清肌酐(Cr)上升0.3 mg/dL(≥26.5 μmol/L);已知或假定腎功能損害發生在7 d之內,Cr上升至>基礎值的1.5倍;尿量<0.5 mL/(kg·h),持續6 h。
1.5 統計學分析
采用SPSS 26.0和GraphPad Prism 5.0進行統計分析及繪圖。正態分布的計量資料以均數±標準差(x±s)描述,兩組間比較采用獨立樣本t檢驗;非正態分布的計量資料采用中位數(上下四分位數)[M(P25,P75)]描述,組間比較采用秩和檢驗。兩組術后多時間點氧合指數比較采用重復測量方差分析。計數資料以例數和率(%)表示,采用χ2 檢驗或Fisher確切概率法。P≤0.05為差異有統計學意義。
1.6 倫理審查
本研究由天津市胸科醫院倫理審查委員會批準(倫理審查批號:2023LW-015)。
2 結果
2.1 兩組術前資料比較
對照組納入54例患者,iNO組納入27例患者。對照組和iNO組基線資料(包括低氧高危因素:年齡、BMI及吸煙史等)差異無統計學意義(P>0.05)。兩組術前白細胞計數、中性粒細胞計數、血紅蛋白、血小板計數、C反應蛋白(C-reactive protein,CRP)水平及氧合指數等術前化驗指標差異均無統計學意義(P>0.05);見表1。
2.2 兩組術中資料比較
對照組和iNO組總體手術時間、體外循環時間、主動脈阻斷時間、停循環時間、術中肛溫等差異均無統計學意義(P>0.05);見表2。
2.3 兩組術后早期資料比較
對照組和iNO組患者術后即刻氧合指數分別為(82.77±8.75)mm Hg、(85.59±10.34)mm Hg,兩組差異無統計學意義(P=0.150)。對照組和iNO組呼吸機通氣時間分別為116.5(101.5,141.2)h、93.3(83.7,105.5)h,差異有統計學意義(P<0.001);術后ICU住院時間分別為12.0(10.0,16.0)d、7.0(6.0,9.0)d,差異有統計學意義(P<0.001);兩組患者術后住院時間差異有統計學意義(P<0.001)。兩組院內死亡及術后并發癥方面差異無統計學意義(P>0.05);見表3。術后氧合指數變化見圖1。
 圖1
兩組患者術后氧合指數(PaO2/FiO2)比較
圖1
兩組患者術后氧合指數(PaO2/FiO2)比較
*:重復測量方差分析結果顯示
3 討論
術后嚴重低氧血癥是孫氏手術術后常見的一種并發癥,發生率高達30%~50%,不僅可以明顯延長呼吸機使用時間,還可以顯著增加病死率,與術后不良預后密切相關,影響早期治療效果[6, 9]。術后低氧與深低溫停循環、輸血、炎癥反應及肺損傷等術中因素密切相關,高齡、吸煙史、高BMI和高白細胞計數也是術后發生嚴重低氧血癥的獨立危險因素。本研究中兩組病例平均BMI均>25 kg/m2,白細胞計數和CRP也顯著高于正常值,提示低氧與上述指標密切有關,這和文獻[5, 10-11]報道一致。
Rossaint等[12]首次報道了iNO治療ARDS患者低氧血癥的作用,iNO可以迅速擴張通氣肺泡血管增加血流,改善肺通氣/血流比例,進而提升肺氧合功能。Dellinger等[13]的研究也表明低劑量iNO治療能夠顯著改善ARDS生存患者的肺功能。基于之前我們將NO應用于小兒先天性心臟病低氧的經驗,發現iNO可以明顯改善患者低氧紫紺狀態。在隨后的A型主動脈夾層孫氏手術術后低氧患者應用iNO過程中,發現NO可以顯著改善患者的氧合指數。本研究兩組術后氧合指數均<100 mm Hg,通過調節呼吸機參數,FiO2在0.8~1.0的情況下,肺氧合仍然不理想。吸入NO后,患者氧合指數改善非常迅速,12 h后iNO組顯著高于對照組,在之后的研究時間節點里,也均顯著高于對照組,在72 h時,iNO組氧合指數已接近200 mm Hg,盡管優化呼吸機各參數,包括PEEP的調整,但對照組氧合指數進展非常緩慢,提示這可能與iNO減少肺內分流,優化肺通氣/血流比有關。
有動物實驗[14-15]發現,NO 通過抑制炎癥細胞因子和氧化損傷來改善肺損傷。也有研究[16]顯示,NO在肝移植中具有良好的抗炎效果,在降低術后并發癥發生率起到了關鍵性作用,iNO治療具有較好的術后早期結果可能與其抗炎作用密切相關。既往大量研究[17-19]顯示A型主動脈夾層圍手術期內產生劇烈的炎癥反應,這與我們術前白細胞計數及CRP水平統計結果相吻合。劇烈的全身炎癥反應再加上孫氏手術的打擊,肺功能會進一步受到損害。我們可以看到, iNO組呼吸機使用時間為93.3 h,顯著短于對照組的116.5 h,ICU停留時間以及術后住院時間同樣也有顯著差別,也進一步證實了iNO能縮短機械通氣時間、ICU停留時間以及術后住院時間等。本研究還發現術后院內死亡率對照組(9.3%)高于iNO組(7.4%),但差異無統計學意義,這與Al Sulaiman等[20]的研究結果相似。我們的研究結果顯示心臟術后低氧及時應用NO治療急性肺損傷可以明顯提高氧合指數、顯著縮短患者嚴重低氧血癥的發作時間和降低發作程度,但是并不能改變術后病死率等臨床治療結果,提示孫氏手術術后病死率與低氧血癥相關性不強,主要還是與合并永久性神經功能障礙以及多臟器損害等多因素作用相關[21]。
一項ARDS研究[22]發現NO可以明顯損害腎功能,然而其機制并未闡明。另一項研究[23]也報道了iNO在肺移植患者中對腎功能的影響,但結果顯示iNO并不會使腎功能惡化。最近的臨床試驗[24]同樣證實,在心臟手術期間和之后給予NO氣體可顯著減少術后AKI及溶血。在本研究中,術后兩組 AKI 發生率以及與AKI 相關的CRRT 發生率無顯著差別,這一結果也證實了低劑量NO治療并不會加重腎功能損傷。我們推測,一方面低劑量的iNO可以減小肺血管阻力和右心負荷來增加心臟輸出量,進而腎臟可以得到充分的灌注;另一方面NO直接擴張腎臟血管,降低腎血管阻力,從而保護腎臟功能。目前的氣體檢測儀器具有很好的NO和NO2濃度監測性能,在使用過程中上述氣體的濃度和流量具有良好的穩定性。在隨后的研究中發現iNO在改善氧合的過程中并不與NO濃度呈正相關[25],低劑量的NO治療在其他研究[26-28]中也被證實是安全有效的。NO的另一個副作用是抑制血小板聚集和黏附血管內皮[29-30],導致出血時間延長。我們比較了兩組術后胸腔積液引流量以及因出血導致的再次開胸探查次數,發現組間并無顯著差異,提示低劑量的iNO治療不增加術后出血事件的發生[28]。但是根據我們以往的心臟術后治療經驗,有明確的活動性出血時不建議使用iNO治療。
本研究表明,低劑量iNO治療孫氏手術術后嚴重低氧血癥安全、有效,可以明顯縮短呼吸機使用時間、ICU停留時間和術后住院時間,且不額外增加腎功能損害,在改善患者早期臨床治療結果方面具有重要意義。本研究也存在一些不足,這是一項回顧性研究,樣本量小且來自于單一心臟中心,將來還需要前瞻性的隨機對照研究提供更多的證據。另外本研究還缺少患者的長期隨訪數據,iNO治療對出院患者的影響尚未闡明。
利益沖突:無。
作者貢獻:馬曉中、張韶鵬、白云鵬、陳慶良和姜楠負責課題的研究設計;張韶鵬、吳振華和趙豐負責患者篩選和數據收集及分析;馬曉中、白云鵬負責文章撰寫。