引用本文: 熊遠鵬, 孔小玉, 周世發. 雙硫死亡相關基因與胰腺癌預后及免疫治療的關系探索:基于生物信息學分析. 中國普外基礎與臨床雜志, 2023, 30(11): 1359-1366. doi: 10.7507/1007-9424.202308012 復制
版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
2019年統計結果顯示胰腺癌的發病率與病死率相近,均居全球癌癥死亡第7位[1]。近年來,胰腺癌在外科治療、綜合治療等方面取得了一定進展,但由于胰腺癌早期臨床癥狀并不明顯,且病情進展迅速,多數患者在確診時已發生局部進展或遠處轉移,失去了手術機會,即使患者在早期接受手術切除,90%以上患者也會出現復發,導致其總體5年生存率(僅為10%左右)仍不滿意[2-3]。因此,積極探索胰腺癌的發病機制以及尋求新的有效治療靶點具有重要的臨床意義。2023年Liu等[4]提出存在一種全新的細胞死亡形式—雙硫死亡,在該研究中發現,部分高表達溶質載體家族7成員11(solute carrier family 7 member A11,SLC7A11)的細胞在發生葡萄糖饑餓時將會導致細胞內的二硫化物不斷積聚,并進一步誘導細胞產生二硫化物應激,這使得能夠維持細胞形態的肌動蛋白細胞骨架中的二硫鍵含量升高,促進肌動蛋白絲發生收縮,最終破壞其骨架結構,使細胞發生死亡,這種全新的細胞死亡形式不同于已知的細胞凋亡、自噬、焦亡等方式。現不斷有研究[5-7]結果表明,雙硫死亡在腫瘤發生及發展過程中發揮著重要作用,并且可作為一種全新分子質量靶點。但到目前為止,雙硫死亡在胰腺癌中的作用尚不清楚。因此,本研究通過癌癥基因組圖譜(The Cancer Genome Atlas,TCGA)中的數據識別雙硫死亡的不同聚類特征并確定其亞型,同時分析它與胰腺癌患者的總生存和免疫浸潤的關系,然后通過雙硫死亡相關基因(disulfidptosis-related genes,DRGs)的表達水平進行風險評分,并進一步分析它評估胰腺癌患者預后和腫瘤突變負荷(tumor mutation burden,TMB)的價值。
1 資料與方法
1.1 數據收集
從TCGA(
1.2 鑒定在胰腺癌中突變的DRGs
提取15個DRGs的體細胞突變數據,分別使用R軟件的“maftools”“RCircos”和“RColorBrewer”程序包繪制突變基因的瀑布圖、染色體定位圖和相關性網格圖。
1.3 DRGs的共識聚類分析
采用R軟件的“ConensusClusterPlus”程序包進行一致性的聚類分析,根據聚類效果選擇具有較高聚類穩定性的k值,并以此構建為不同的DRGs亞型。最佳聚類基于以下標準:沒有任何一組的樣本量過小;在累積分布函數(cumulative distribution function,CDF)曲線中觀察到下降坡度減小;聚類后組內相關性增加,組間相關性降低。然后通過R軟件的“survival”程序包分析DRGs不同亞型患者間的總生存情況差異;同時使用R軟件的“pheatmap”程序包繪制DRGs熱圖,以便反映DRGs不同亞型患者間的臨床特征差異。使用主成分分析(principal component analysis,PCA)算法和R軟件的“ggplot2”程序包分析并繪制DRGs不同亞型間胰腺癌患者的分布情況。
1.4 DRGs不同亞型間的腫瘤浸潤性免疫細胞和功能富集分析
從Timer2.0(
1.5 基于DRGs的風險評分
為了定量評估雙硫死亡模式與胰腺癌的關系,引入發生突變的DRGs的風險評分(基于DRGs在每例樣本中的基因表達量不同,根據PCA算法對每例樣本進行的評分即為風險評分)。根據所有樣本風險評分計算均值,根據均值將所有胰腺癌患者分為高風險組(≥均值)和低風險組(<均值),采用Kaplan-Meier法繪制高風險組和低風險組患者的生存曲線。使用R軟件的“ggpubr”程序包繪制箱線圖比較DRGs不同亞型患者的風險評分差異,“ggalluvial”程序包繪制桑基圖展示不同風險、DRGs不同亞型及患者生存狀態之間的關系。
1.6 TMB分析
采用R軟件的“maftools”程序包對含有體細胞突變數據的胰腺癌患者進行分析,以獲得TMB信息,用“maftools”程序包繪制不同風險評分胰腺癌患者的基因突變圖譜,使用箱線圖直觀地展示不同風險組胰腺癌患者的TMB定量差異,并用散點圖進一步展示DRGs不同亞型胰腺癌患者的風險評分與TMB的關系;根據含有體細胞突變數據患者TMB值的均值將患者分為高TMB(≥均值)組和低TMB(<均值)組,再用Kaplan-Meier法繪制高和低TMB患者的總生存曲線,隨后將患者依據風險評分和TMB高低分為4個亞組進行總生存情況比較。
1.7 統計學方法
采用R軟件(4.3.1版本)整理數據,使用包括Kaplan-Meier生存分析和log-rank檢驗進行生存分析。對于正態分布變量使用t檢驗,對于非正態分布變量使用Wilcoxon檢驗。采用Spearman相關性分析評估變量間的相關性。檢驗水準α=0.05。
2 結果
2.1 數據下載情況
從TCGA中下載了177例胰腺癌患者的轉錄組數據和對應患者的臨床信息,其中有161例胰腺癌樣本含有體細胞突變數據。
2.2 DRGs在胰腺癌中的突變情況
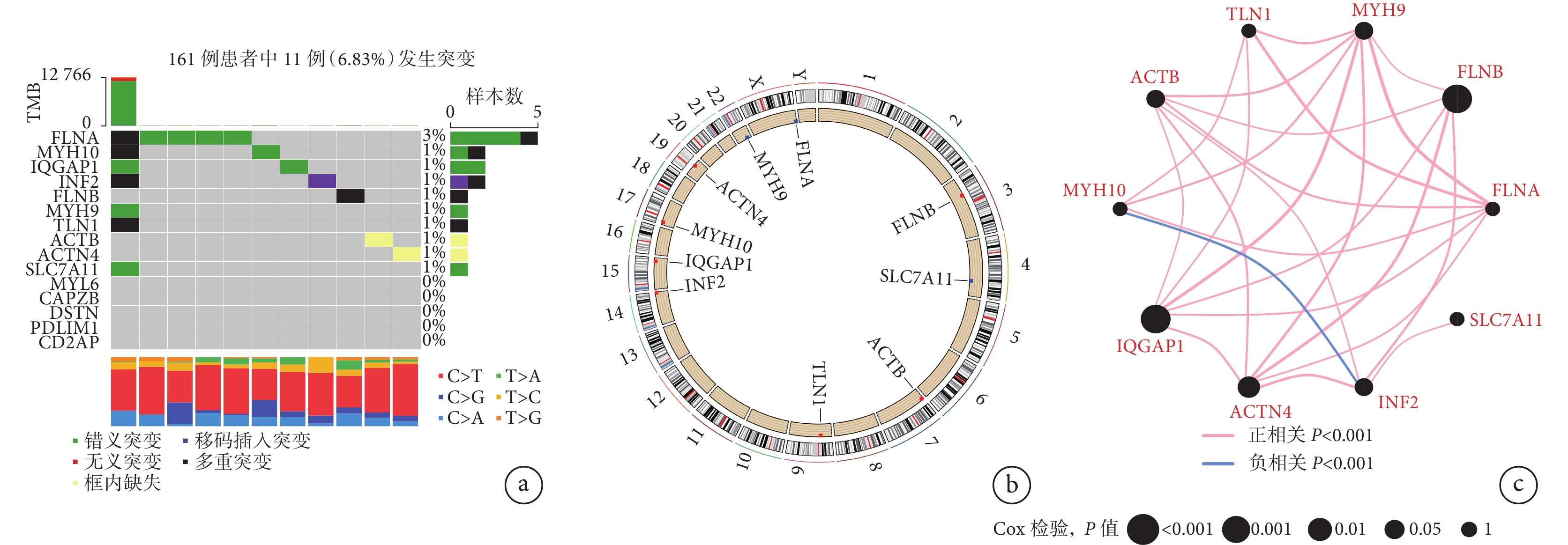
對選擇的15個DRGs在161例含有體細胞突變的胰腺癌樣本中進行分析的結果(圖1a)顯示,其中有11例胰腺癌樣本共10個DRGs(FLNA、MYH10、IQGAP1、INF2、FLNB、MYH9、TLN1、ACTB、ACTN4、SLC7A11)發生了突變,而有5個DRGs(MYL6、CAPZB、DSTN、PDLIM1、CD2AP)未發生突變。發生突變的這10個DRGs在胰腺癌患者染色體上的定位情況見圖1b;發生突變的10個DRGs之間相關性分析結果的網格圖見圖1c,在這10個DRGs中僅MYH10與INF2之間呈負相關(P<0.001),其余DRGs間均呈正相關(P<0.001)。
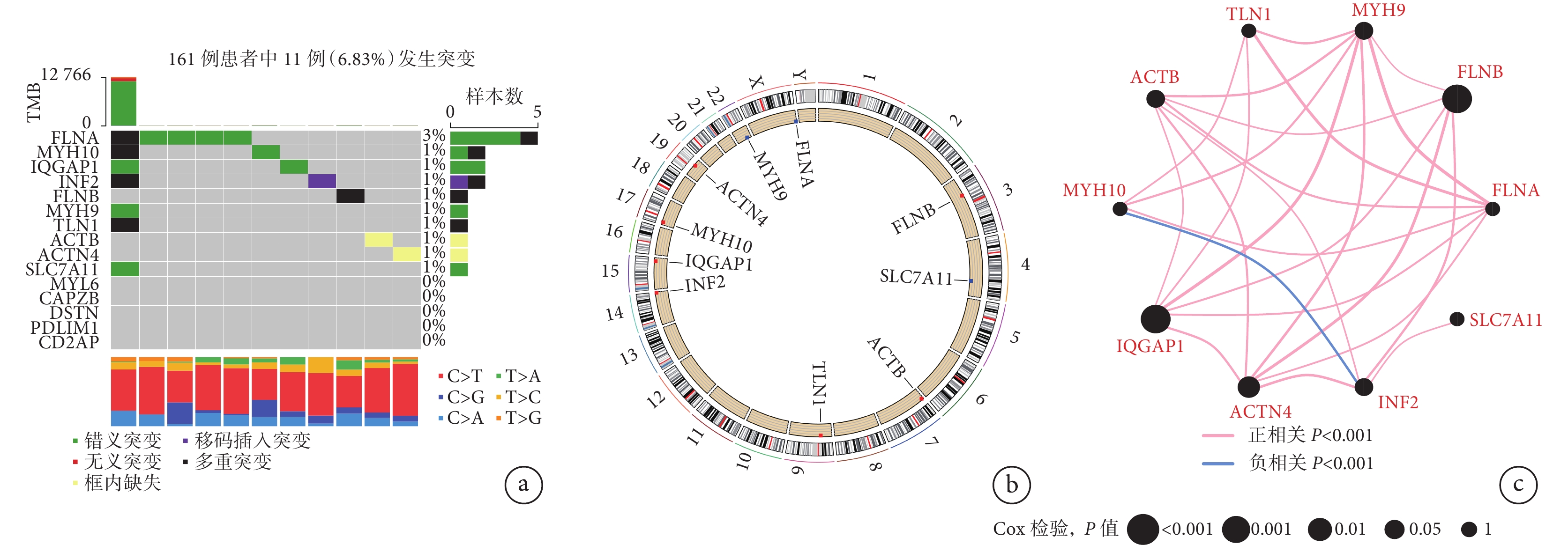 圖1
示DRGs在胰腺癌樣本中的突變情況
圖1
示DRGs在胰腺癌樣本中的突變情況
a:15個DRGs在TCGA中含有體細胞突變數據的161例胰腺癌患者中的突變情況(右側:突變個數最多的基因行柱狀圖;上方:根據樣本中包含的突變個數排序的列柱狀圖;下方:樣本中堿基突變情況的柱狀圖);b:發生突變的10個DRGs在染色體上的定位情況;c:發生突變的10個DRGs相互之間相關性分析結果的網格圖(相關性分析結果掃描圖中二維碼查看)
2.3 胰腺癌中DRGs聚類分析結果
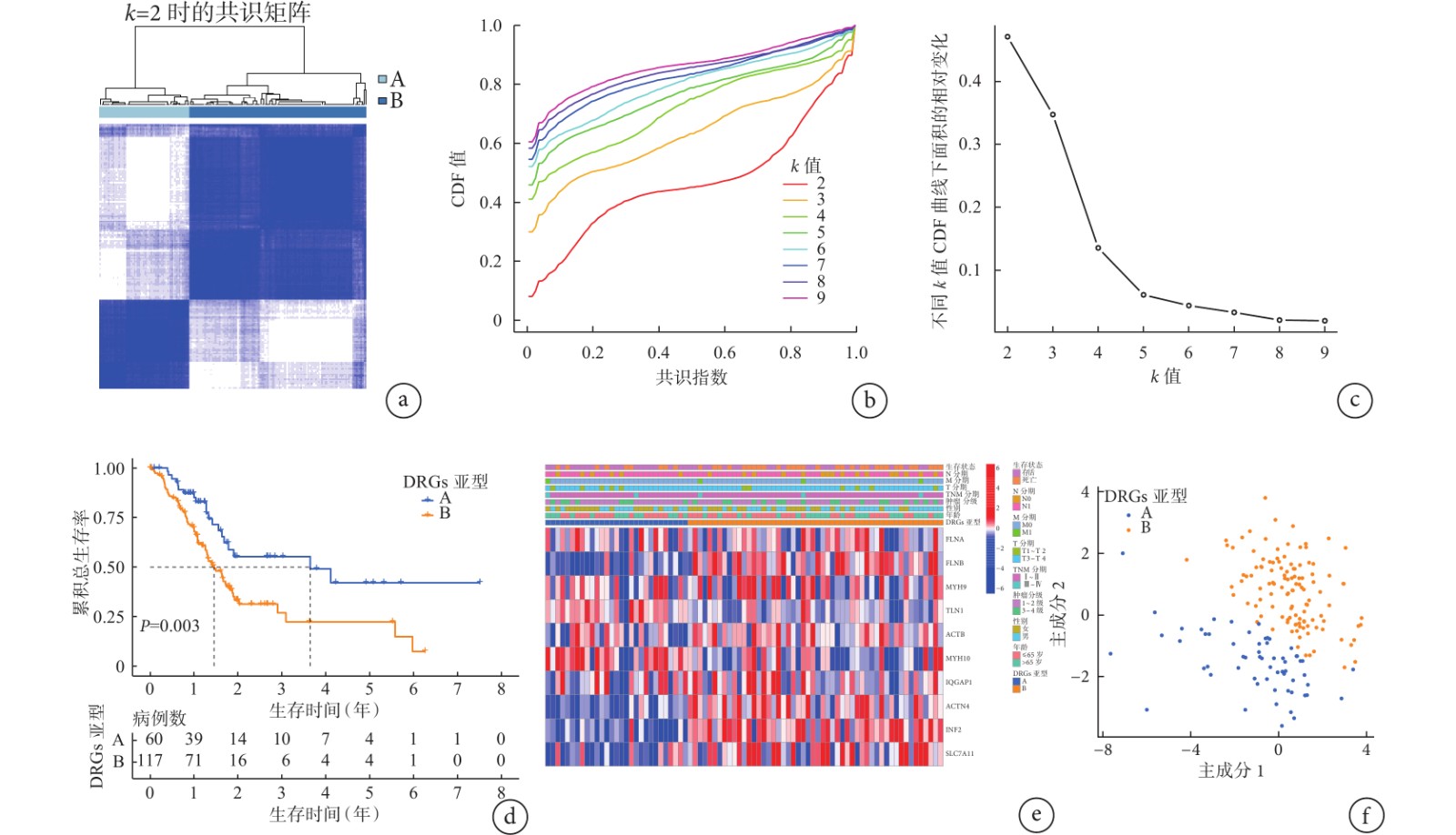
從圖2a~2c的聚類分析結果展示,當k=2時穩定性最佳,得到2個DRGs聚類亞型(A亞型和B亞型),其中A亞型包含60例胰腺癌樣本,B亞型包含117例胰腺癌樣本。進一步繪制A亞型和B亞型胰腺癌患者的Kaplan-Meier生存曲線(圖2d),log-rank檢驗的結果顯示,A亞型胰腺癌患者的生存情況優于B亞型胰腺癌患者(χ2=8.316,P=0.003)。基于TCGA中的不同臨床病理因素繪制的10個突變DRGs的熱圖見圖2e,詳細展示了DRGs在各臨床病理因素中的表達情況,并且提示DRGs在B亞型胰腺癌患者中表達明顯比在A亞型中更為豐富(基因表達越高紅色越深,表達越低藍色越深,在B亞型中紅色居多)。而PCA算法的結果(圖2f)顯示,基于發生突變的這10個DRGs聚類所得到的亞型可以很好地將胰腺癌患者區分開來(每個點代表1例患者,圖中不同亞型患者被明顯分為2個區域內)。
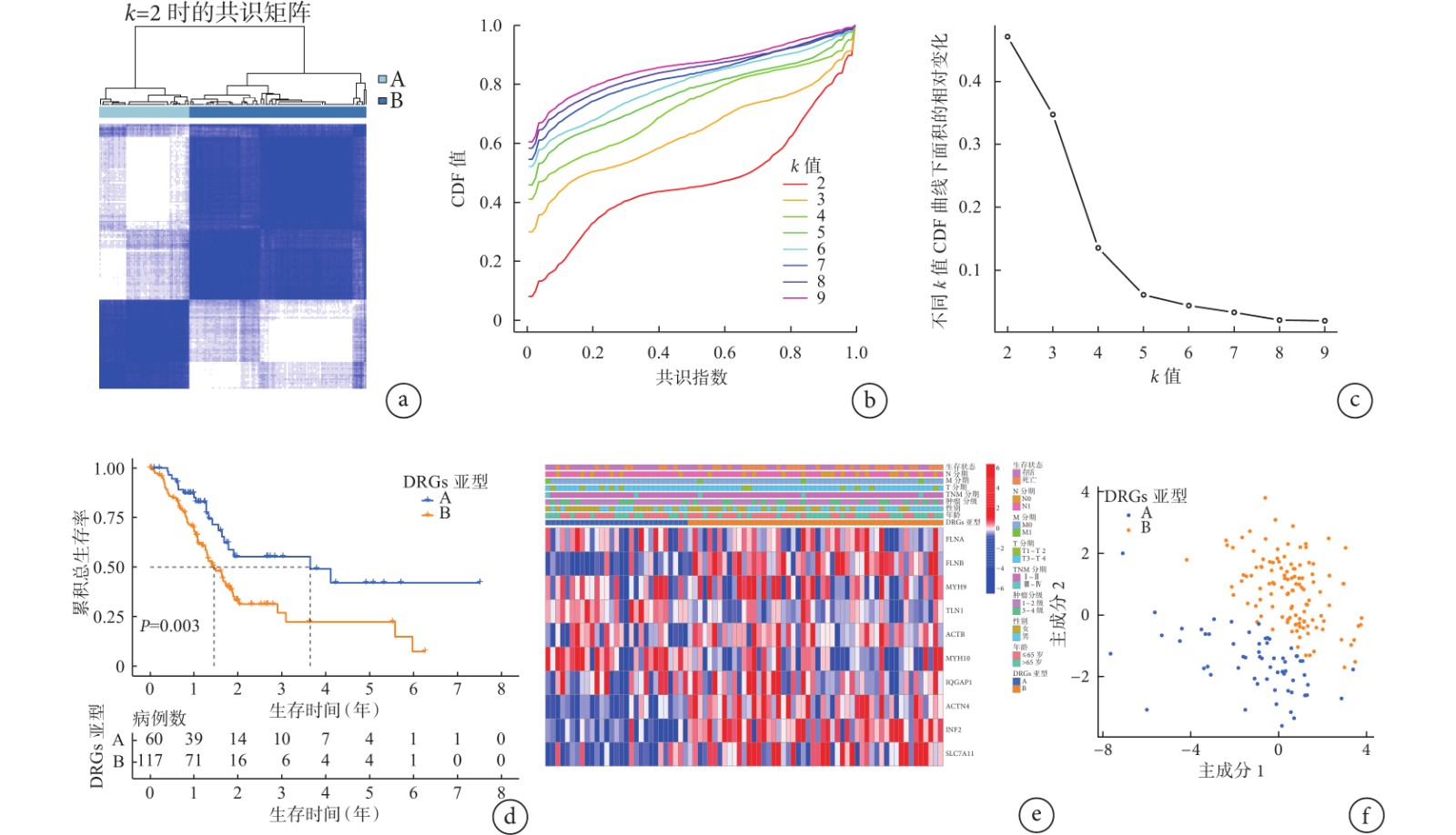 圖2
示DRGs聚類分析結果及不同亞型患者的臨床病理特征
圖2
示DRGs聚類分析結果及不同亞型患者的臨床病理特征
a:最佳
2.4 DRGs不同亞型間腫瘤浸潤性免疫細胞和功能富集分析結果
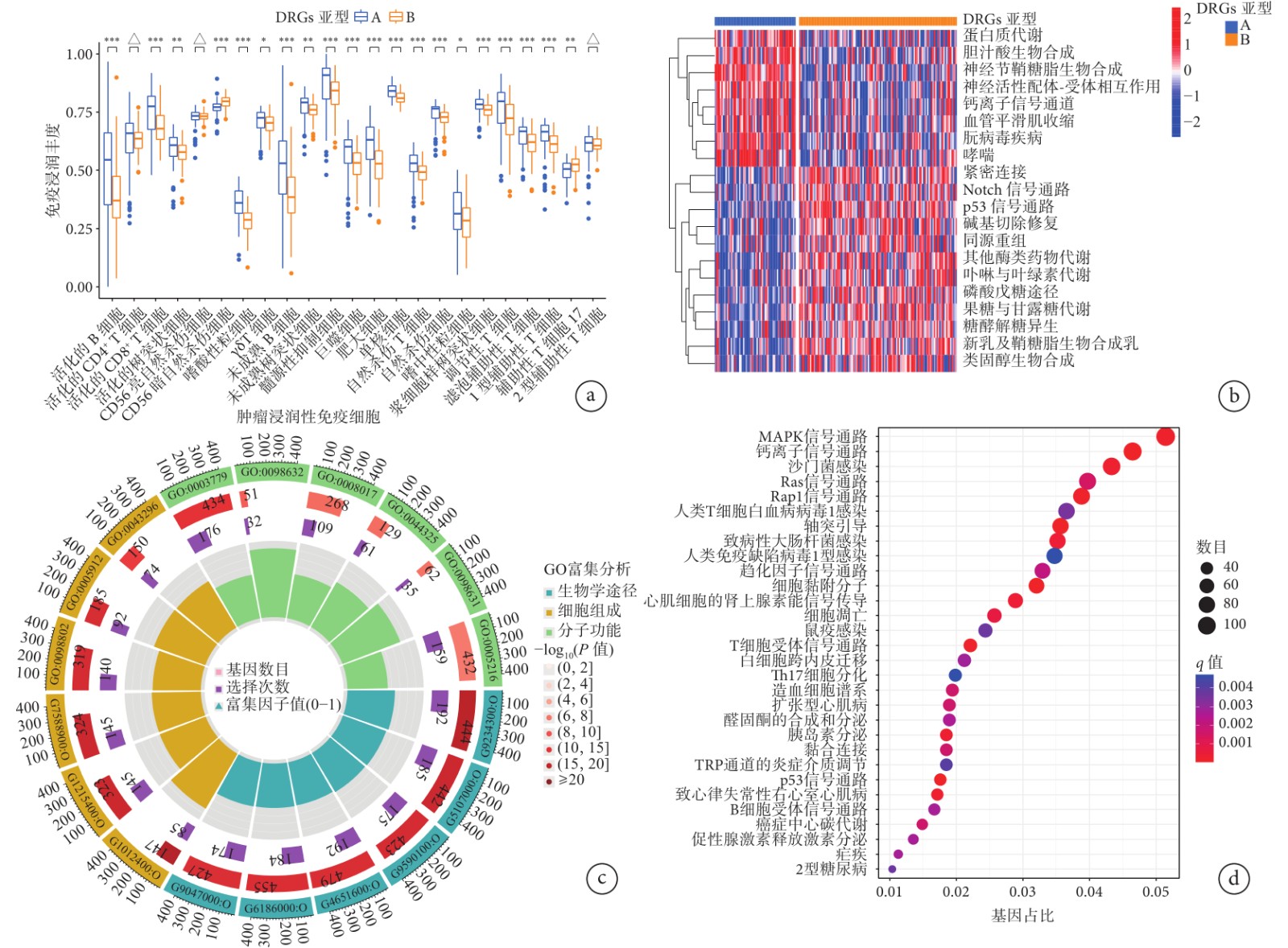
Estimate算法分析結果(圖3a)顯示,23種腫瘤浸潤性免疫細胞中除了活化的CD4+ T細胞、CD56亮自然殺傷細胞和2型輔助性T細胞豐度在DRGs A亞型和B型患者間比較差異無統計學意義(P>0.05)外,其余20種腫瘤浸潤性免疫細胞包括活化的B細胞、活化的CD8+ T細胞、活化的樹突狀細胞、CD56暗自然殺傷細胞、嗜酸性粒細胞、γδ T細胞、未成熟B細胞、未成熟樹突狀細胞、髓源性抑制細胞、巨噬細胞、肥大細胞、單核細胞、自然殺傷T細胞、自然殺傷細胞、嗜中性粒細胞、漿細胞樣樹突狀細胞、調節性T細胞、濾泡輔助性T細胞、1型輔助性T細胞和輔助性T細胞17的豐度在A亞型胰腺癌患者中均高于B亞型患者(P<0.05)。
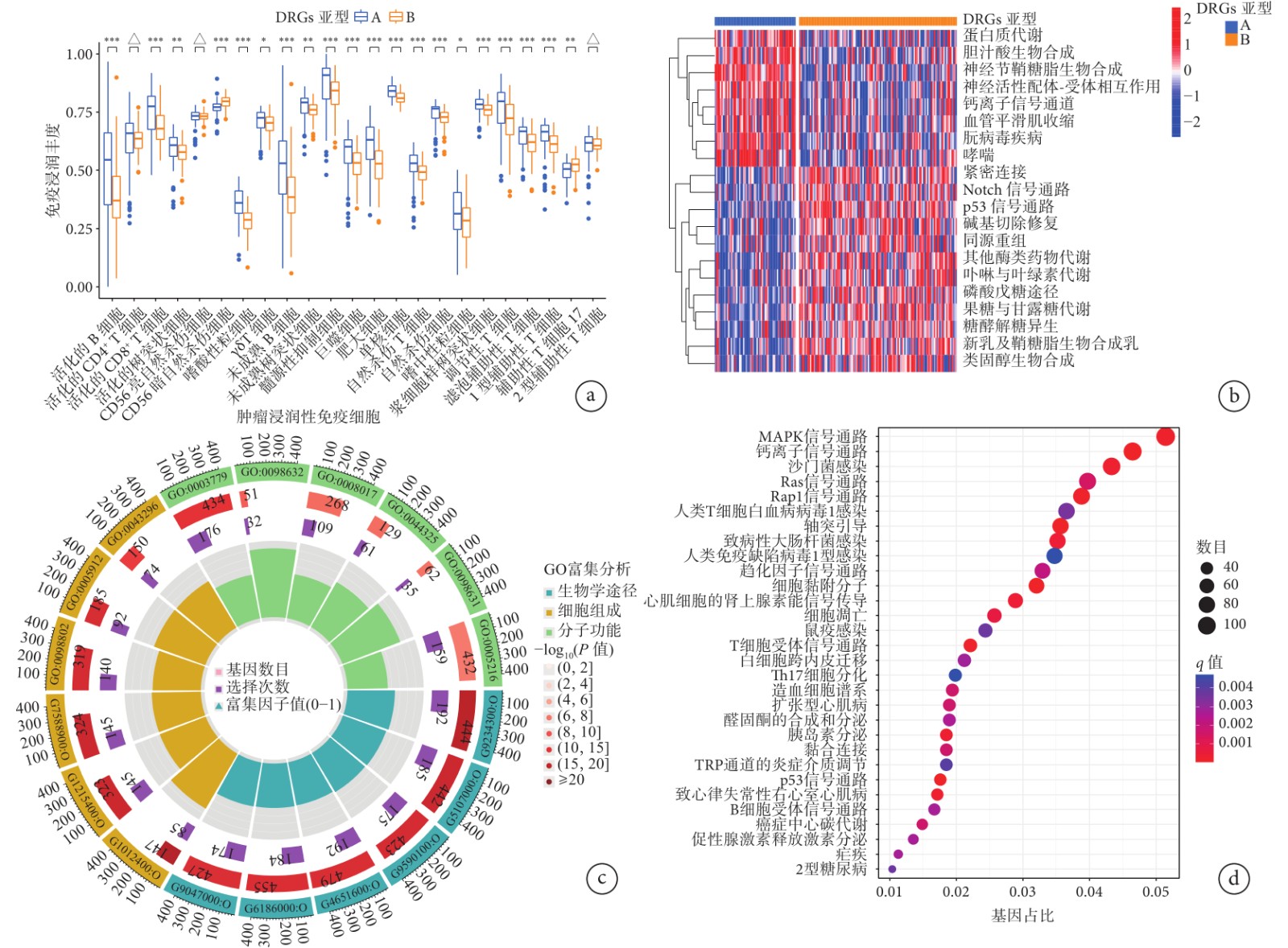 圖3
示基于DRGs亞型的腫瘤免疫細胞浸潤和功能富集分析
圖3
示基于DRGs亞型的腫瘤免疫細胞浸潤和功能富集分析
a:23種腫瘤浸潤性免疫細胞的豐度在A亞型和B亞型胰腺癌患者中比較結果(△:
GSVA結果(圖3b)顯示,A亞型的胰腺癌患者富集的前5個通路主要是蛋白質代謝和膽汁酸生物合成、神經傳導信號通路(神經節鞘糖脂生物合成、神經活性配體-受體相互作用、鈣離子信號通路)。
A亞型和B亞型胰腺癌患者之間共鑒定出7 473個DEGs,這些DEGs的GO富集分析(圖3c)結果顯示,大多數的DEGs主要在生物學途徑中顯著富集;KEGG富集分析(圖3d)結果顯示,這些DEGs主要富集在腫瘤和與免疫相關的信號通路中,如MAPK信號通路[8]、RAS信號通路[9]、T細胞相關信號通路等。
2.5 基于DRGs的風險評分結果
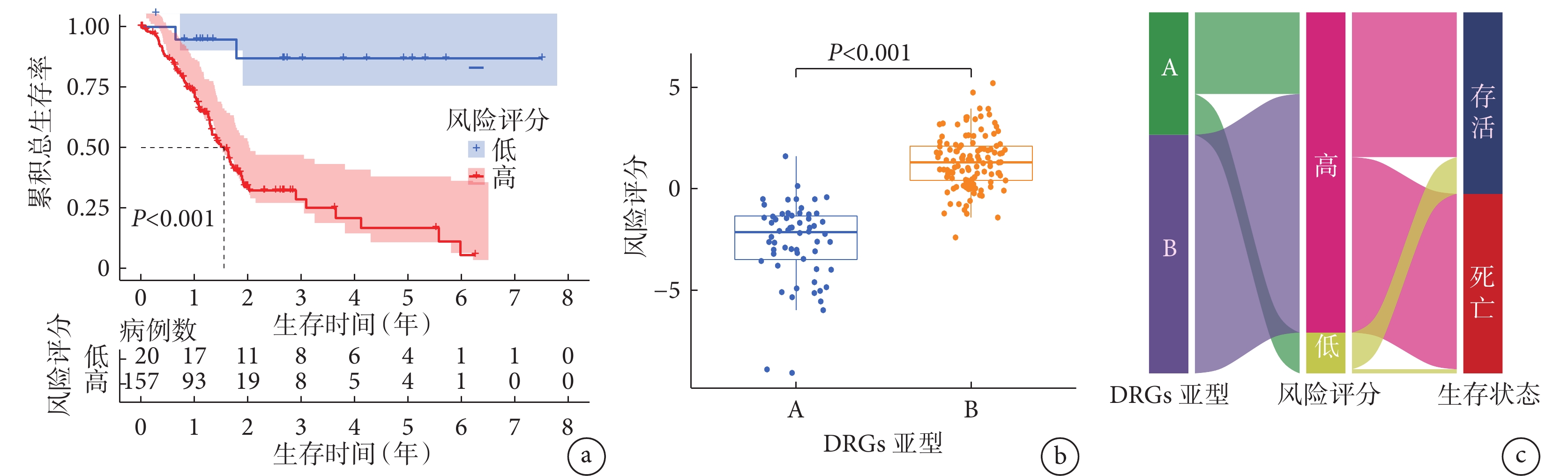
177例胰腺癌患者的風險評分均值為1.921,以此為界分組,高風險組157例,低風險組20例。Kaplan-Meier生存曲線(圖4a)顯示,低風險組的總生存情況優于高風險組(χ2=17.058,P<0.001);箱線圖(圖4b)結果顯示,B亞型患者的風險評分高于A亞型(t=14.031,P<0.001);桑基圖(圖4c)顯示,B亞型胰腺癌患者的風險評分更高及預后更差。
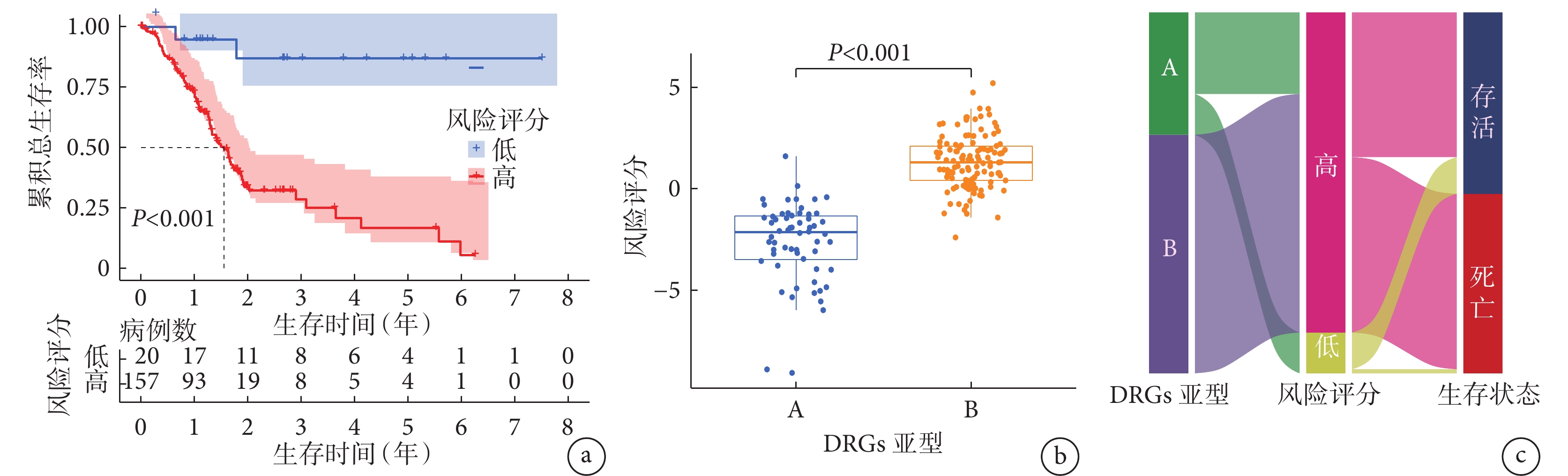 圖4
示基于DRGs的風險評分結果
圖4
示基于DRGs的風險評分結果
a:高風險組和低風險組胰腺癌患者總生存情況的Kaplan-Meier生存曲線;b:DRGs不同亞型胰腺癌患者的風險評分的箱線圖;c:桑基圖顯示DRGs不同亞型、不同風險及生存狀態之間的關系(線條走向代表聯系,節點長度代表患者數目)
2.6 TMB分析結果
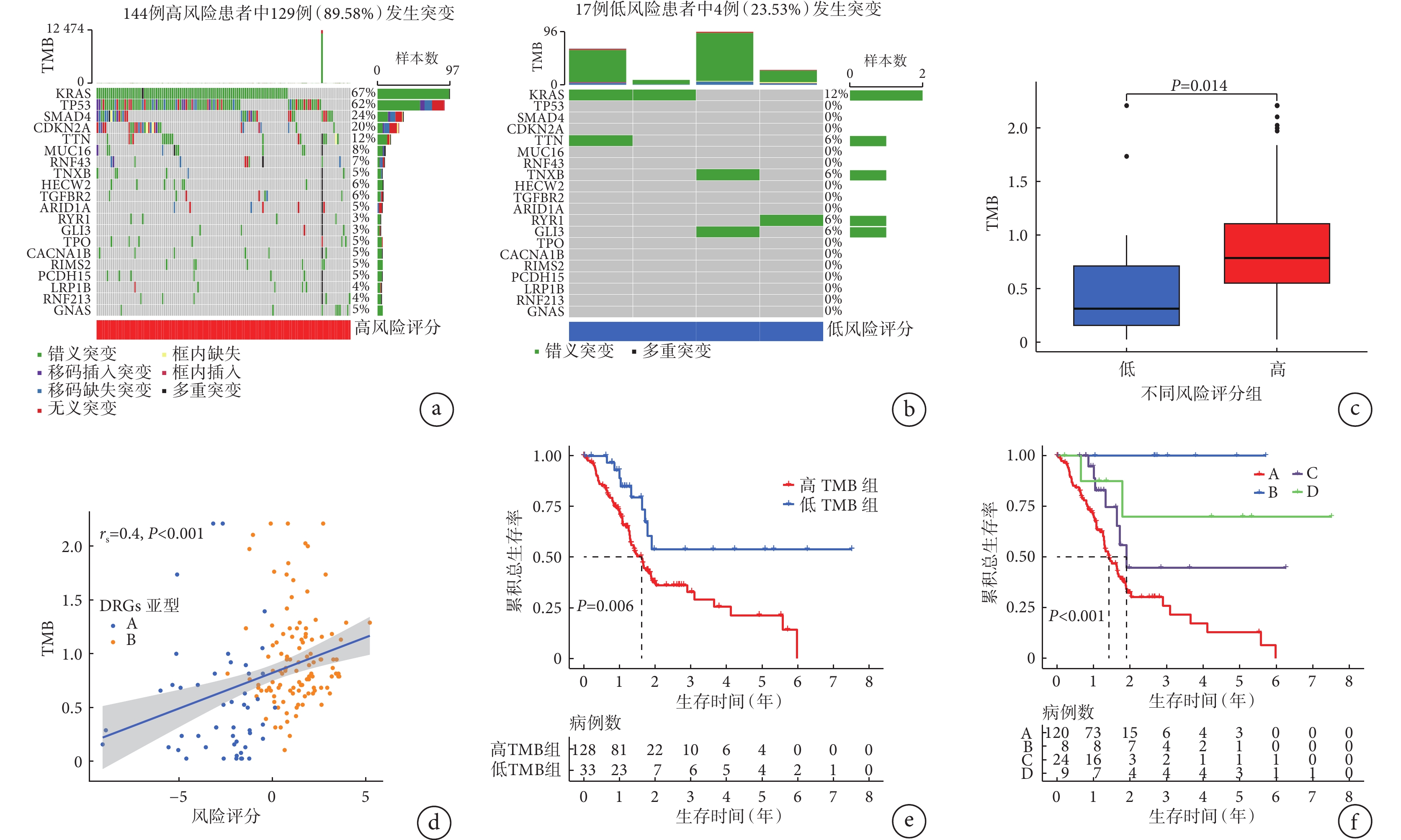
本研究在TCGA中共收集到有161例胰腺癌患者含有體細胞突變數據,其中風險評分為高風險有144例患者、低風險有17例患者,高風險和低風險胰腺癌患者的DEGs突變情況分別見圖5a和圖5b,從圖5a、5b中可見, KRAS、TTN、TNXB、RYR1、GLI3 這 5 個GEGs在高風險和低風險胰腺癌患者中都發生突變;而且箱線圖(圖5c)結果顯示,高風險胰腺癌患者的TMB值較低風險胰腺癌患者更高(t=5.642,P=0.014);相關性分析結果(圖5d)顯示,風險評分與TMB呈現正相關關系(rs=0.4,P<0.001)。161例含有體細胞突變數據胰腺癌患者的TMB均值為2.767,以此為界分組,高TMB組128例、低TMB組33例,Kaplan-Meier法繪制的生存曲線(圖5e)顯示,高TMB組患者的總生存情況較低TMB組患者差(χ2=7.425,P=0.006)。將TMB和風險評分聯合分析總生存情況的差異,結果發現,高TMB伴高風險評分患者、高TMB伴低風險評分患者、低TMB伴高風險評分患者及低TMB伴低風險評分患者的總生存曲線(圖5f)總體比較差異有統計學意義(χ2=11.106,P<0.001),其中高TMB伴低風險評分患者的生存情況最好,而高TMB伴高風險評分患者的生存情況最差。
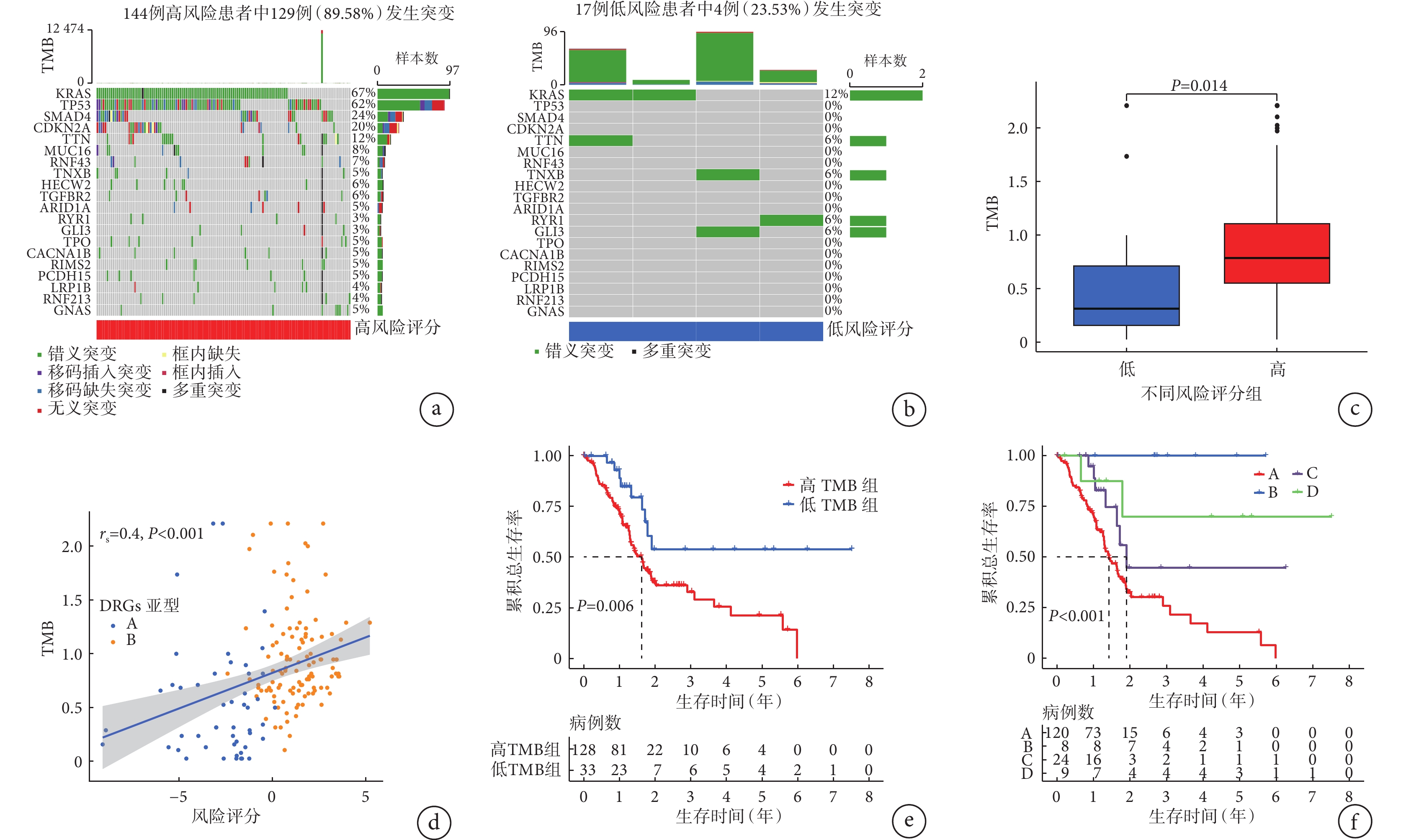 圖5
示TMB分析結果
圖5
示TMB分析結果
a、b:分別為高風險和低風險胰腺癌患者的DEGs突變狀態瀑布圖;c:高風險和低風險組胰腺癌患者間TMB的差異;d:A和B亞型胰腺患者的風險評分與TMB之間的相關性;e:高TMB組和低TMB組的Kaplan-Meier生存曲線;f:不同風險評分和TMB結合的胰腺癌患者的Kaplan-Meier生存曲線(A:高TMB伴高風險評分患者;B:高TMB伴低風險評分患者;C:低TMB伴高風險評分患者;D:低TMB伴低風險評分患者)
3 討論
雙硫死亡可引起一系列氧化還原缺陷和誘導細胞死亡發生,而免疫細胞產生相關免疫反應在很大程度上又需依賴于氧化還原反應的發生[10-11],而且氧化還原狀態是腫瘤發生和發展的重要機制之一[12-13];并且Liu等[4]也指出雙硫死亡與腫瘤有關且報道了DRGs,同時提出誘導雙硫死亡有可能成為腫瘤的有效治療策略。同時有研究[14-16]表明,胰腺癌患者的治療反應和預后與免疫細胞的浸潤狀態有密切聯系。然而目前有關雙硫死亡與胰腺癌免疫相關的研究較為有限。基于此,本研究借助TCGA中的數據對此進行了探索分析。
根據Liu等[4]報道的DRGs,本研究選擇了與雙硫死亡關聯性最強的14個基因外加關鍵基因SCL7A11共15個DRGs,發現其中有10個DRGs發生了突變,其中除了MYH10和INF2這2個DRGs間呈負相關外,其余DRGs相互間均呈正相關,此結果可能提示了不同DRGs間具有一定的協同作用;通過對這10個DRGs進行聚類分型發現它將胰腺癌患者分為了DRGs A和B這2個亞型,發現DRGs在B亞型胰腺癌患者中的表達較在A亞型中更為豐富且B亞型胰腺癌患者的預后較A亞型更差,提示DRGs與胰腺癌患者的不良預后有關。進一步分析發現,免疫浸潤細胞CD8+ T細胞、樹突狀細胞、自然殺傷T細胞、調節性T細胞、輔助T細胞等均在A亞型胰腺癌患者中的浸潤比例更高。以往有研究[17]表明,活化的CD8+ T細胞有助于產生持久有效的抗腫瘤免疫反應;樹突狀細胞和自然殺傷T細胞在體內發揮著重要監測作用,一旦失調則更容易促進胰腺癌的進展[14, 18];而調節性T細胞和輔助T細胞的缺失則會增加抗原呈遞效果的下降,促進免疫逃逸的發生[19]。從本研究結果以及結合文獻報道結果均提示,A亞型胰腺癌患者可能具有更好的預后。此外,GSVA結果提示A亞型胰腺癌患者在代謝和信息傳導相關通路上富集程度更高,而A亞型和B亞型胰腺癌患者之間DEGs的GO富集分析表明大多數的DEGs主要富集于生物過程中,KEGG富集分析的結果進一步提示DEGs主要在腫瘤和免疫相關通路上顯著富集,提示這兩種分子亞型表現出不同的免疫細胞浸潤特征和功能富集途徑,DRGs可能通過刺激信號傳導、調控腫瘤微環境中免疫細胞浸潤等方式影響胰腺癌的發生和發展。
為了進一步確認這10個發生突變的DRGs與患者預后的關系,本研究基于它們的基因表達量引入風險評分,B亞型胰腺癌患者的風險評分較A亞型更高,根據風險評分均值(1.921)將患者分為高風險組和低風險組,高風險患者預后呈現不良狀態。
TMB是評價基因突變頻率高低的指標[20]。腫瘤細胞基因突變頻率高,則細胞表面所攜帶的腫瘤抗原就多,就越容易受到機體免疫系統的攻擊,代表此對免疫治療的效果越好。有研究[21]表明,高TMB的癌癥患者在接受免疫治療時可以獲得較好的預后。本研究分析了高低風險組患者的TMB,其中高風險組有144例患者,低風險組有17例患者,發現 KRAS、TTN、TNXB、RYR1、GLI3 這 5 個DEGs在高和低風險患者中均發生了突變,且在高風險患者中突變頻率明顯更高,這與先前已有的研究[22-26]報道相符,這 5 個DEGs都作為促癌因子存在,并且高 TMB且高風險的胰腺癌患者預后最差,這表明高TMB組胰腺癌患者雖具有預后不良的特性,但對免疫治療可能具有更好的反應,因此建議應盡早使用免疫治療以期帶來更好的預后。
總之,雙硫死亡作為一種新的細胞死亡形式,其基因表達與胰腺癌患者的預后及免疫治療反應密切相關,因此對DRGs展開針對性靶點治療可能為胰腺癌的診療提供一種新的思路。但本研究也存在樣本量不足等問題,還需要使用不同的隊列進行驗證,并且也需要更多的前瞻性臨床研究以及基礎研究來進一步完善并驗證。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:熊遠鵬構思和設計本研究并撰寫文本;孔小玉參與圖片制作;周世發給予技術和寫作指導同時審查論文及編輯。所有作者均審閱了此文稿并同意最終文稿。
倫理聲明:由于本研究的數據來自公共數據庫,因此無需獲得倫理委員會的批準。
2019年統計結果顯示胰腺癌的發病率與病死率相近,均居全球癌癥死亡第7位[1]。近年來,胰腺癌在外科治療、綜合治療等方面取得了一定進展,但由于胰腺癌早期臨床癥狀并不明顯,且病情進展迅速,多數患者在確診時已發生局部進展或遠處轉移,失去了手術機會,即使患者在早期接受手術切除,90%以上患者也會出現復發,導致其總體5年生存率(僅為10%左右)仍不滿意[2-3]。因此,積極探索胰腺癌的發病機制以及尋求新的有效治療靶點具有重要的臨床意義。2023年Liu等[4]提出存在一種全新的細胞死亡形式—雙硫死亡,在該研究中發現,部分高表達溶質載體家族7成員11(solute carrier family 7 member A11,SLC7A11)的細胞在發生葡萄糖饑餓時將會導致細胞內的二硫化物不斷積聚,并進一步誘導細胞產生二硫化物應激,這使得能夠維持細胞形態的肌動蛋白細胞骨架中的二硫鍵含量升高,促進肌動蛋白絲發生收縮,最終破壞其骨架結構,使細胞發生死亡,這種全新的細胞死亡形式不同于已知的細胞凋亡、自噬、焦亡等方式。現不斷有研究[5-7]結果表明,雙硫死亡在腫瘤發生及發展過程中發揮著重要作用,并且可作為一種全新分子質量靶點。但到目前為止,雙硫死亡在胰腺癌中的作用尚不清楚。因此,本研究通過癌癥基因組圖譜(The Cancer Genome Atlas,TCGA)中的數據識別雙硫死亡的不同聚類特征并確定其亞型,同時分析它與胰腺癌患者的總生存和免疫浸潤的關系,然后通過雙硫死亡相關基因(disulfidptosis-related genes,DRGs)的表達水平進行風險評分,并進一步分析它評估胰腺癌患者預后和腫瘤突變負荷(tumor mutation burden,TMB)的價值。
1 資料與方法
1.1 數據收集
從TCGA(
1.2 鑒定在胰腺癌中突變的DRGs
提取15個DRGs的體細胞突變數據,分別使用R軟件的“maftools”“RCircos”和“RColorBrewer”程序包繪制突變基因的瀑布圖、染色體定位圖和相關性網格圖。
1.3 DRGs的共識聚類分析
采用R軟件的“ConensusClusterPlus”程序包進行一致性的聚類分析,根據聚類效果選擇具有較高聚類穩定性的k值,并以此構建為不同的DRGs亞型。最佳聚類基于以下標準:沒有任何一組的樣本量過小;在累積分布函數(cumulative distribution function,CDF)曲線中觀察到下降坡度減小;聚類后組內相關性增加,組間相關性降低。然后通過R軟件的“survival”程序包分析DRGs不同亞型患者間的總生存情況差異;同時使用R軟件的“pheatmap”程序包繪制DRGs熱圖,以便反映DRGs不同亞型患者間的臨床特征差異。使用主成分分析(principal component analysis,PCA)算法和R軟件的“ggplot2”程序包分析并繪制DRGs不同亞型間胰腺癌患者的分布情況。
1.4 DRGs不同亞型間的腫瘤浸潤性免疫細胞和功能富集分析
從Timer2.0(
1.5 基于DRGs的風險評分
為了定量評估雙硫死亡模式與胰腺癌的關系,引入發生突變的DRGs的風險評分(基于DRGs在每例樣本中的基因表達量不同,根據PCA算法對每例樣本進行的評分即為風險評分)。根據所有樣本風險評分計算均值,根據均值將所有胰腺癌患者分為高風險組(≥均值)和低風險組(<均值),采用Kaplan-Meier法繪制高風險組和低風險組患者的生存曲線。使用R軟件的“ggpubr”程序包繪制箱線圖比較DRGs不同亞型患者的風險評分差異,“ggalluvial”程序包繪制桑基圖展示不同風險、DRGs不同亞型及患者生存狀態之間的關系。
1.6 TMB分析
采用R軟件的“maftools”程序包對含有體細胞突變數據的胰腺癌患者進行分析,以獲得TMB信息,用“maftools”程序包繪制不同風險評分胰腺癌患者的基因突變圖譜,使用箱線圖直觀地展示不同風險組胰腺癌患者的TMB定量差異,并用散點圖進一步展示DRGs不同亞型胰腺癌患者的風險評分與TMB的關系;根據含有體細胞突變數據患者TMB值的均值將患者分為高TMB(≥均值)組和低TMB(<均值)組,再用Kaplan-Meier法繪制高和低TMB患者的總生存曲線,隨后將患者依據風險評分和TMB高低分為4個亞組進行總生存情況比較。
1.7 統計學方法
采用R軟件(4.3.1版本)整理數據,使用包括Kaplan-Meier生存分析和log-rank檢驗進行生存分析。對于正態分布變量使用t檢驗,對于非正態分布變量使用Wilcoxon檢驗。采用Spearman相關性分析評估變量間的相關性。檢驗水準α=0.05。
2 結果
2.1 數據下載情況
從TCGA中下載了177例胰腺癌患者的轉錄組數據和對應患者的臨床信息,其中有161例胰腺癌樣本含有體細胞突變數據。
2.2 DRGs在胰腺癌中的突變情況
對選擇的15個DRGs在161例含有體細胞突變的胰腺癌樣本中進行分析的結果(圖1a)顯示,其中有11例胰腺癌樣本共10個DRGs(FLNA、MYH10、IQGAP1、INF2、FLNB、MYH9、TLN1、ACTB、ACTN4、SLC7A11)發生了突變,而有5個DRGs(MYL6、CAPZB、DSTN、PDLIM1、CD2AP)未發生突變。發生突變的這10個DRGs在胰腺癌患者染色體上的定位情況見圖1b;發生突變的10個DRGs之間相關性分析結果的網格圖見圖1c,在這10個DRGs中僅MYH10與INF2之間呈負相關(P<0.001),其余DRGs間均呈正相關(P<0.001)。
 圖1
示DRGs在胰腺癌樣本中的突變情況
圖1
示DRGs在胰腺癌樣本中的突變情況
a:15個DRGs在TCGA中含有體細胞突變數據的161例胰腺癌患者中的突變情況(右側:突變個數最多的基因行柱狀圖;上方:根據樣本中包含的突變個數排序的列柱狀圖;下方:樣本中堿基突變情況的柱狀圖);b:發生突變的10個DRGs在染色體上的定位情況;c:發生突變的10個DRGs相互之間相關性分析結果的網格圖(相關性分析結果掃描圖中二維碼查看)
2.3 胰腺癌中DRGs聚類分析結果
從圖2a~2c的聚類分析結果展示,當k=2時穩定性最佳,得到2個DRGs聚類亞型(A亞型和B亞型),其中A亞型包含60例胰腺癌樣本,B亞型包含117例胰腺癌樣本。進一步繪制A亞型和B亞型胰腺癌患者的Kaplan-Meier生存曲線(圖2d),log-rank檢驗的結果顯示,A亞型胰腺癌患者的生存情況優于B亞型胰腺癌患者(χ2=8.316,P=0.003)。基于TCGA中的不同臨床病理因素繪制的10個突變DRGs的熱圖見圖2e,詳細展示了DRGs在各臨床病理因素中的表達情況,并且提示DRGs在B亞型胰腺癌患者中表達明顯比在A亞型中更為豐富(基因表達越高紅色越深,表達越低藍色越深,在B亞型中紅色居多)。而PCA算法的結果(圖2f)顯示,基于發生突變的這10個DRGs聚類所得到的亞型可以很好地將胰腺癌患者區分開來(每個點代表1例患者,圖中不同亞型患者被明顯分為2個區域內)。
 圖2
示DRGs聚類分析結果及不同亞型患者的臨床病理特征
圖2
示DRGs聚類分析結果及不同亞型患者的臨床病理特征
a:最佳
2.4 DRGs不同亞型間腫瘤浸潤性免疫細胞和功能富集分析結果
Estimate算法分析結果(圖3a)顯示,23種腫瘤浸潤性免疫細胞中除了活化的CD4+ T細胞、CD56亮自然殺傷細胞和2型輔助性T細胞豐度在DRGs A亞型和B型患者間比較差異無統計學意義(P>0.05)外,其余20種腫瘤浸潤性免疫細胞包括活化的B細胞、活化的CD8+ T細胞、活化的樹突狀細胞、CD56暗自然殺傷細胞、嗜酸性粒細胞、γδ T細胞、未成熟B細胞、未成熟樹突狀細胞、髓源性抑制細胞、巨噬細胞、肥大細胞、單核細胞、自然殺傷T細胞、自然殺傷細胞、嗜中性粒細胞、漿細胞樣樹突狀細胞、調節性T細胞、濾泡輔助性T細胞、1型輔助性T細胞和輔助性T細胞17的豐度在A亞型胰腺癌患者中均高于B亞型患者(P<0.05)。
 圖3
示基于DRGs亞型的腫瘤免疫細胞浸潤和功能富集分析
圖3
示基于DRGs亞型的腫瘤免疫細胞浸潤和功能富集分析
a:23種腫瘤浸潤性免疫細胞的豐度在A亞型和B亞型胰腺癌患者中比較結果(△:
GSVA結果(圖3b)顯示,A亞型的胰腺癌患者富集的前5個通路主要是蛋白質代謝和膽汁酸生物合成、神經傳導信號通路(神經節鞘糖脂生物合成、神經活性配體-受體相互作用、鈣離子信號通路)。
A亞型和B亞型胰腺癌患者之間共鑒定出7 473個DEGs,這些DEGs的GO富集分析(圖3c)結果顯示,大多數的DEGs主要在生物學途徑中顯著富集;KEGG富集分析(圖3d)結果顯示,這些DEGs主要富集在腫瘤和與免疫相關的信號通路中,如MAPK信號通路[8]、RAS信號通路[9]、T細胞相關信號通路等。
2.5 基于DRGs的風險評分結果
177例胰腺癌患者的風險評分均值為1.921,以此為界分組,高風險組157例,低風險組20例。Kaplan-Meier生存曲線(圖4a)顯示,低風險組的總生存情況優于高風險組(χ2=17.058,P<0.001);箱線圖(圖4b)結果顯示,B亞型患者的風險評分高于A亞型(t=14.031,P<0.001);桑基圖(圖4c)顯示,B亞型胰腺癌患者的風險評分更高及預后更差。
 圖4
示基于DRGs的風險評分結果
圖4
示基于DRGs的風險評分結果
a:高風險組和低風險組胰腺癌患者總生存情況的Kaplan-Meier生存曲線;b:DRGs不同亞型胰腺癌患者的風險評分的箱線圖;c:桑基圖顯示DRGs不同亞型、不同風險及生存狀態之間的關系(線條走向代表聯系,節點長度代表患者數目)
2.6 TMB分析結果
本研究在TCGA中共收集到有161例胰腺癌患者含有體細胞突變數據,其中風險評分為高風險有144例患者、低風險有17例患者,高風險和低風險胰腺癌患者的DEGs突變情況分別見圖5a和圖5b,從圖5a、5b中可見, KRAS、TTN、TNXB、RYR1、GLI3 這 5 個GEGs在高風險和低風險胰腺癌患者中都發生突變;而且箱線圖(圖5c)結果顯示,高風險胰腺癌患者的TMB值較低風險胰腺癌患者更高(t=5.642,P=0.014);相關性分析結果(圖5d)顯示,風險評分與TMB呈現正相關關系(rs=0.4,P<0.001)。161例含有體細胞突變數據胰腺癌患者的TMB均值為2.767,以此為界分組,高TMB組128例、低TMB組33例,Kaplan-Meier法繪制的生存曲線(圖5e)顯示,高TMB組患者的總生存情況較低TMB組患者差(χ2=7.425,P=0.006)。將TMB和風險評分聯合分析總生存情況的差異,結果發現,高TMB伴高風險評分患者、高TMB伴低風險評分患者、低TMB伴高風險評分患者及低TMB伴低風險評分患者的總生存曲線(圖5f)總體比較差異有統計學意義(χ2=11.106,P<0.001),其中高TMB伴低風險評分患者的生存情況最好,而高TMB伴高風險評分患者的生存情況最差。
 圖5
示TMB分析結果
圖5
示TMB分析結果
a、b:分別為高風險和低風險胰腺癌患者的DEGs突變狀態瀑布圖;c:高風險和低風險組胰腺癌患者間TMB的差異;d:A和B亞型胰腺患者的風險評分與TMB之間的相關性;e:高TMB組和低TMB組的Kaplan-Meier生存曲線;f:不同風險評分和TMB結合的胰腺癌患者的Kaplan-Meier生存曲線(A:高TMB伴高風險評分患者;B:高TMB伴低風險評分患者;C:低TMB伴高風險評分患者;D:低TMB伴低風險評分患者)
3 討論
雙硫死亡可引起一系列氧化還原缺陷和誘導細胞死亡發生,而免疫細胞產生相關免疫反應在很大程度上又需依賴于氧化還原反應的發生[10-11],而且氧化還原狀態是腫瘤發生和發展的重要機制之一[12-13];并且Liu等[4]也指出雙硫死亡與腫瘤有關且報道了DRGs,同時提出誘導雙硫死亡有可能成為腫瘤的有效治療策略。同時有研究[14-16]表明,胰腺癌患者的治療反應和預后與免疫細胞的浸潤狀態有密切聯系。然而目前有關雙硫死亡與胰腺癌免疫相關的研究較為有限。基于此,本研究借助TCGA中的數據對此進行了探索分析。
根據Liu等[4]報道的DRGs,本研究選擇了與雙硫死亡關聯性最強的14個基因外加關鍵基因SCL7A11共15個DRGs,發現其中有10個DRGs發生了突變,其中除了MYH10和INF2這2個DRGs間呈負相關外,其余DRGs相互間均呈正相關,此結果可能提示了不同DRGs間具有一定的協同作用;通過對這10個DRGs進行聚類分型發現它將胰腺癌患者分為了DRGs A和B這2個亞型,發現DRGs在B亞型胰腺癌患者中的表達較在A亞型中更為豐富且B亞型胰腺癌患者的預后較A亞型更差,提示DRGs與胰腺癌患者的不良預后有關。進一步分析發現,免疫浸潤細胞CD8+ T細胞、樹突狀細胞、自然殺傷T細胞、調節性T細胞、輔助T細胞等均在A亞型胰腺癌患者中的浸潤比例更高。以往有研究[17]表明,活化的CD8+ T細胞有助于產生持久有效的抗腫瘤免疫反應;樹突狀細胞和自然殺傷T細胞在體內發揮著重要監測作用,一旦失調則更容易促進胰腺癌的進展[14, 18];而調節性T細胞和輔助T細胞的缺失則會增加抗原呈遞效果的下降,促進免疫逃逸的發生[19]。從本研究結果以及結合文獻報道結果均提示,A亞型胰腺癌患者可能具有更好的預后。此外,GSVA結果提示A亞型胰腺癌患者在代謝和信息傳導相關通路上富集程度更高,而A亞型和B亞型胰腺癌患者之間DEGs的GO富集分析表明大多數的DEGs主要富集于生物過程中,KEGG富集分析的結果進一步提示DEGs主要在腫瘤和免疫相關通路上顯著富集,提示這兩種分子亞型表現出不同的免疫細胞浸潤特征和功能富集途徑,DRGs可能通過刺激信號傳導、調控腫瘤微環境中免疫細胞浸潤等方式影響胰腺癌的發生和發展。
為了進一步確認這10個發生突變的DRGs與患者預后的關系,本研究基于它們的基因表達量引入風險評分,B亞型胰腺癌患者的風險評分較A亞型更高,根據風險評分均值(1.921)將患者分為高風險組和低風險組,高風險患者預后呈現不良狀態。
TMB是評價基因突變頻率高低的指標[20]。腫瘤細胞基因突變頻率高,則細胞表面所攜帶的腫瘤抗原就多,就越容易受到機體免疫系統的攻擊,代表此對免疫治療的效果越好。有研究[21]表明,高TMB的癌癥患者在接受免疫治療時可以獲得較好的預后。本研究分析了高低風險組患者的TMB,其中高風險組有144例患者,低風險組有17例患者,發現 KRAS、TTN、TNXB、RYR1、GLI3 這 5 個DEGs在高和低風險患者中均發生了突變,且在高風險患者中突變頻率明顯更高,這與先前已有的研究[22-26]報道相符,這 5 個DEGs都作為促癌因子存在,并且高 TMB且高風險的胰腺癌患者預后最差,這表明高TMB組胰腺癌患者雖具有預后不良的特性,但對免疫治療可能具有更好的反應,因此建議應盡早使用免疫治療以期帶來更好的預后。
總之,雙硫死亡作為一種新的細胞死亡形式,其基因表達與胰腺癌患者的預后及免疫治療反應密切相關,因此對DRGs展開針對性靶點治療可能為胰腺癌的診療提供一種新的思路。但本研究也存在樣本量不足等問題,還需要使用不同的隊列進行驗證,并且也需要更多的前瞻性臨床研究以及基礎研究來進一步完善并驗證。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:熊遠鵬構思和設計本研究并撰寫文本;孔小玉參與圖片制作;周世發給予技術和寫作指導同時審查論文及編輯。所有作者均審閱了此文稿并同意最終文稿。
倫理聲明:由于本研究的數據來自公共數據庫,因此無需獲得倫理委員會的批準。