引用本文: 任黎蕾, 趙小波, 高硯春, 侯令密. 銅死亡與乳腺癌相關性的研究進展. 中國普外基礎與臨床雜志, 2024, 31(2): 250-256. doi: 10.7507/1007-9424.202309075 復制
版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
乳腺癌(breast cancer)是全世界女性中最普遍的惡性腫瘤。近幾十年來,盡管發現內分泌治療(endocrine therapy,ET)、化療、免疫治療和聯合治療可改善乳腺癌的預后,但乳腺癌異質性和復雜性的特點,對改善乳腺癌的臨床生存期提出了挑戰。
一般來講,細胞死亡分為意外細胞死亡和調節性細胞死亡(regulatory cell death,RCD)。ACD是一個不可控的生物學過程,而RCD具有精確的分子機制和復雜的信號調節途徑。目前已有數十種RCD,其中細胞凋亡、焦亡、自噬、鐵死亡和壞死已被廣泛研究。通過誘導癌細胞死亡是癌癥治療的常見策略。銅死亡作為一種新型細胞死亡方式,是銅誘導的線粒體細胞死亡方式,參與腫瘤的增殖與轉移,在乳腺癌治療中具有重要作用[1]。筆者現就銅死亡及其衍生物在腫瘤進展中的機制及其在乳腺癌中的相關研究進行綜述。
1 銅死亡概述
1.1 銅在銅死亡中的作用
銅是介導細胞功能的酶的重要輔助因子。銅穩態是維持細胞基本功能的保證,體內銅轉運涉及多種銅分子伴侶和銅轉運體。金屬還原酶將細胞外Cu2+ 還原為Cu+,銅轉運蛋白1(copper transport protein,CTR1)將Cu+從細胞外轉移到細胞內,進入細胞內的銅離子通過銅分子伴侶轉運。研究[2]表明,CTR1在黑色素瘤、肝癌、前列腺癌和其他人類癌細胞系中高度表達。2014年Brady等[3]證實了CTR1調控的銅間接調節絲氨酸-蘇氨酸激酶(serine/threonine-protein kinase B-raf,BRAF)/絲裂原活化的細胞外信號調節激酶(mitogen-activated extracellular signal-regulated kinase,MEK)/細胞外信號調節激酶(extracellular signal-regulated kinase,ERK)信號通路,最終抑制腫瘤生長。
銅轉運蛋白質α鏈抗體(ATPase copper transporting alpha polypeptide,ATP7A)和銅轉運蛋白質β鏈抗體(ATPase copper transporting beta polypeptide,ATP7B)是P型銅輸出ATP酶P1B亞家族的兩個成員。研究[4]表明,應用CRISPR/Cas9沉默ATP7A后,賴氨酸氧化酶的活性在乳腺癌和肺癌細胞系中受到抑制,進一步抑制腫瘤細胞的生長和遷移。此外,靶向ATP7A或ATP7B在克服腫瘤細胞對鉑類藥物的耐藥性方面具有廣闊的應用空間[5]。
銅誘導程序性細胞死亡的機制一直備受人們的關注,早在20世紀80年代學者就發現銅會導致細胞死亡,但確切的機制未得到證實[6]。直到Tsvetkov等[7]的研究顯示,在人類細胞中銅依賴性受控細胞死亡是一種不同于已知細胞死亡機制的由銅介導的新型細胞死亡方式,它是通過銅離子與線粒體呼吸中的三羧酸循環(tricarboxylic acid cycle,TCA)中的脂酰化成分直接結合而發生的,導致脂酰化蛋白質聚集和隨后的鐵硫簇蛋白表達下調,進而發生蛋白質毒性應激并導致細胞死亡,該團隊將這種死亡方式命名為銅死亡,但該研究中銅死亡的細胞形態學變化尚未明確,缺乏有效評估銅死亡的方法。細胞中銅的積累可能通過鐵氧還蛋白1(ferredoxin one,FDX1)介導Cu2+還原成Cu+,鐵硫簇蛋白的降解、脂酰化,二氫硫辛酰胺S-乙酰轉移酶(dihydrolipoamide S-acetyltransferase,DLAT)的聚焦來誘導銅死亡[7-8]。
1.2 銅在乳腺癌中的作用
銅是人生命活動中必不可少的微量元素[9]。研究[10-12]發現,與健康人相比,多種癌癥患者的血清和腫瘤組織中的銅含量顯著改變,其在癌癥的發生發展中起到關鍵作用。銅已被證明能促進癌癥進展和轉移過程中至關重要的血管生成,可以激活血管生成因子,如血管生成素、血管內皮生長因子、成纖維細胞生長因子1、白細胞介素1等。乳腺癌的發生與體內微量元素(如Cu、Zn、Se)異常相關[13],微量元素的檢測可能有助于乳腺癌的早期預防和預后[14]。銅也是自噬激酶驅動肺腺癌的重要調節因子[15],且是一種具有高度氧化還原活性的元素,銅的失調會導致活性氧(reaticve oxygen species,ROS)的過量產生。這些過量的ROS可以作為腫瘤轉化發展和轉移形成的前體。Bengtsson等[16]針對1 998例新診斷乳腺癌患者的前瞻性隊列研究是第一項檢查血清銅水平和銅/鋅比值與乳腺癌存活率之間關系的研究,結果發現較高的血清銅/鋅比值與乳腺癌診斷后較差的總體生存率相關。但Jouybari等[17]的薈萃分析不支持銅水平與乳腺癌之間存在關聯,但同時也指出由于原始研究結果的高度異質性,需要設計良好的前瞻性研究來證實這一結論。
1.3 銅死亡的發生機制
銅是諸多生物過程的基礎元素,包括線粒體呼吸、鐵吸收、抗氧化、解毒等過程,銅通常在哺乳動物細胞內維持極低的水平,細胞內銅離子濃度超過維持穩態機制的閾值時,同樣會表現出細胞毒性。在人類細胞中,依賴于銅的受調節的細胞死亡不同于已知的死亡機制,并且銅死亡依賴于線粒體呼吸。之前關于銅誘導的細胞死亡的研究中,大多數學者將銅死亡歸因于銅對線粒體的作用導致ROS的產生[18]。線粒體呼吸可調節銅離子載體誘導的細胞死亡,依賴線粒體呼吸的細胞對銅離子誘導劑的敏感度是依賴糖酵解細胞的1 000倍左右,用線粒體抗氧化劑、脂肪酸和線粒體功能抑制劑處理都會明顯改變細胞對銅離子的敏感性。線粒體解偶聯劑對銅毒性沒有影響,這表明銅誘導的細胞死亡需要線粒體呼吸,而不是三磷酸腺苷(adenosine triphosphate,ATP)。代謝組學研究發現,對銅離子敏感細胞的代謝組學中,與TCA相關的代謝物明顯增多,表明銅誘導的細胞死亡和線粒體代謝緊密相關[7]。總之銅死亡的主要過程依賴于細胞內銅離子的積累,銅離子與TCA的脂酰化成分直接結合導致脂酰化蛋白質聚集,鐵硫簇蛋白失調,進而引發蛋白質毒性應激,并最終導致細胞死亡。
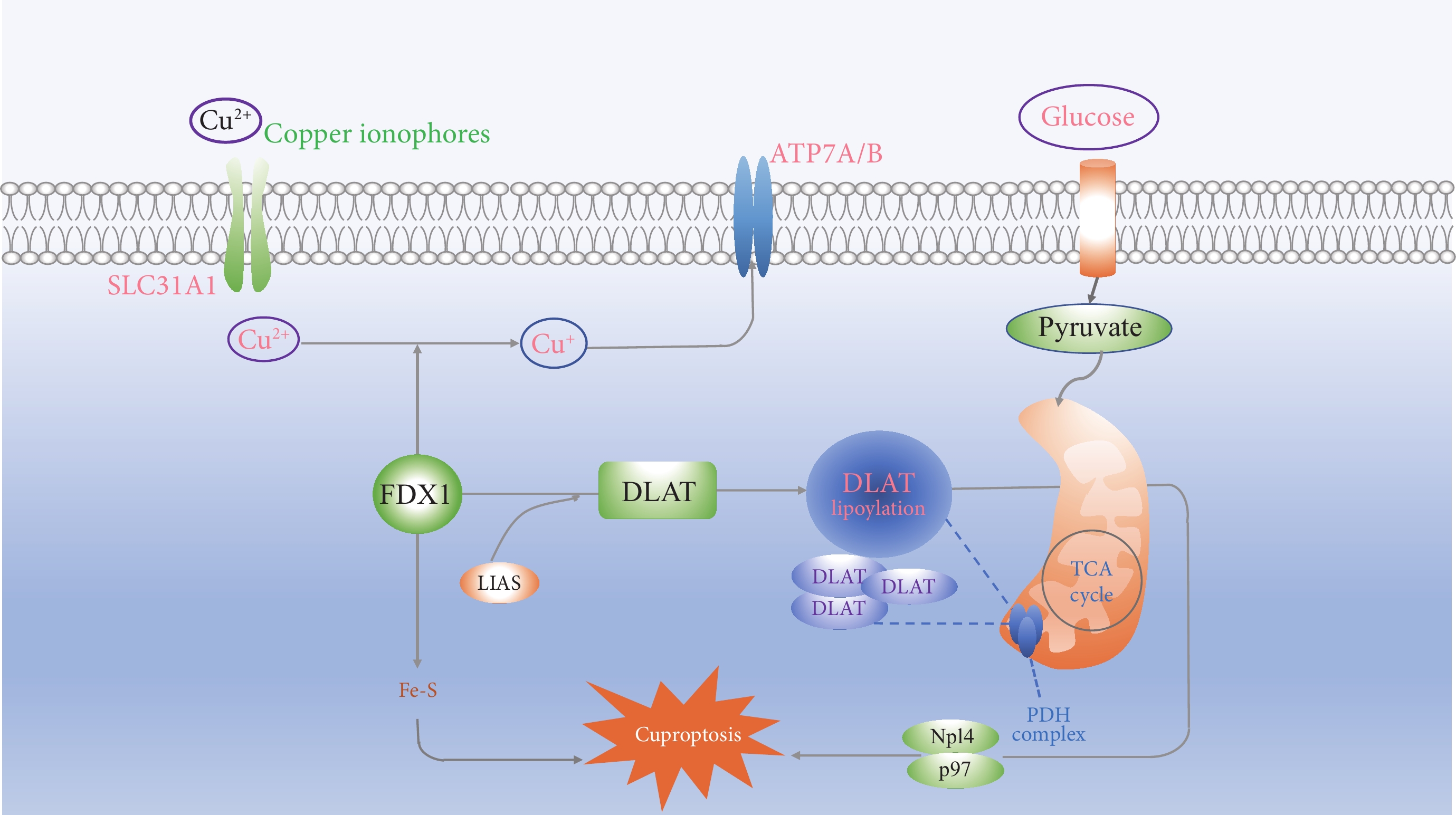
FDX1和脂酰化蛋白的豐度與多種人類腫瘤高度相關,具有高水平脂酰化蛋白的細胞系被證實對銅死亡更加敏感。研究人員[7]進行了全基因組CRISPR-Cas9功能喪失篩選,確定了參與銅離子載體誘導死亡的基因,發現敲除FDX1基因以及6個脂酰化蛋白基因(LIPT1、DLD、LIAS、DLAT、PDHA1、PDHB)可以挽救銅離子對細胞的殺傷作用,認為FDX1是銅離子載體誘導細胞死亡的關鍵介質。FDX1是蛋白質脂酰化的上游調節因子,其缺失導致了蛋白質脂酰化功能的完全喪失,以及細胞內丙酮酸、α-酮戊二酸的積累與琥珀酸的消耗,阻斷了TCA的進行。銅與脂酰化TCA循環蛋白的結合導致DLAT的脂酰化依賴性寡聚化。銅誘導的死亡機制與銅穩態失調的遺傳模型相同,Jiang等[19]經生物信息學方法分析了人FDX1基因的核酸結構,預測了潛在的生物學功能,并探討了乳腺癌銅死亡相關預后特征和調控軸。FDX1、LIAS、DLAT被命名為銅死亡相關基因(Cu death related gene,CRG),在調節銅死亡機制方面發揮重要作用,且銅轉運蛋白CTR1,以及銅轉運酶ATP7A和ATP7B主要參與調節銅濃度的動態平衡,因此CRG和銅轉運蛋白將成為未來癌癥研究的重點,為腫瘤的診斷和治療提供理論支持和參考,其機制見圖1。
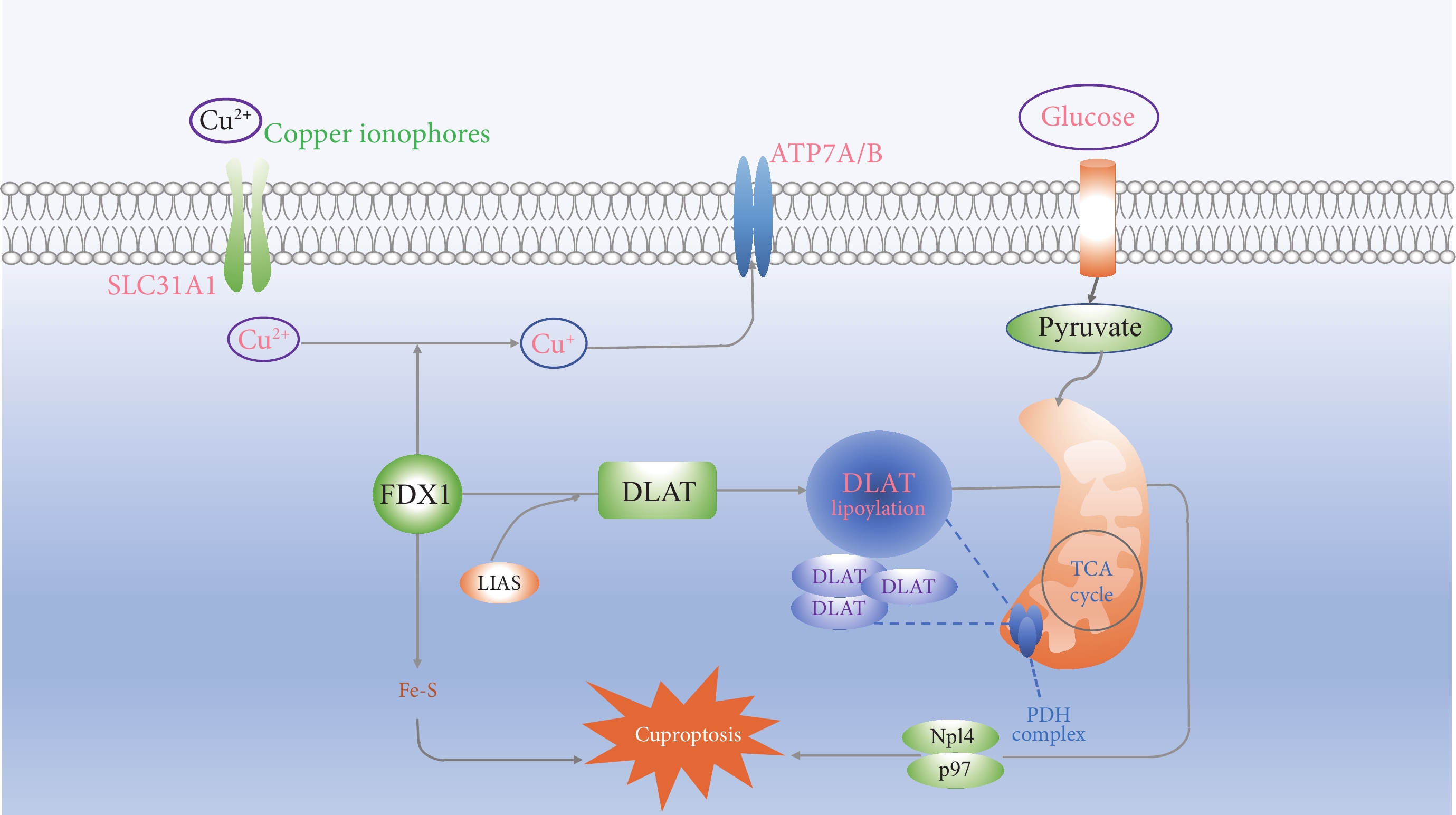 圖1
示銅死亡機制圖
圖1
示銅死亡機制圖
Copper ionophores:銅離子載體;Glucose:葡萄糖;Pyruvate:丙酮酸;Fe-S:鐵硫簇蛋白;DLAT lipoylation:二氫硫辛酰胺S-乙酰轉移酶硫酰化;PDH complex:丙酮酸脫氫酶復合物;TCA cycle:TCA 循環;Cuproptosis:銅死亡
2 CRG與乳腺癌的相關性
大多數癌癥治療的目的是通過殺死癌細胞或阻止癌細胞遷移來減少癌細胞,實現癌細胞減少的最根本途徑是誘導癌細胞死亡,因此,任何類型的細胞死亡對癌癥研究人員都具有重要意義。最近發現的銅死亡將成為癌細胞死亡研究的下一個熱點,探索銅死亡相關調節機制在腫瘤中的作用可增強對腫瘤的認識與治療。
2.1 CRG是乳腺癌的預后指標
溶質載體家族31成員1(solute carrier family 31,SLC31A1)是最近發現的CRG,作為銅轉運蛋白家族基因的一員,SLC31A1與眾多腫瘤發生和預后相關,可能是一種潛在的癌癥關鍵生物標志物和治療靶點[20]。Li等[21]發現CRG SLC31A1是預測乳腺癌診斷、預后和治療反應的潛在指標。劉以原[22]發現SLC31A1在包括乳腺浸潤性癌在內的多種人類腫瘤中呈高水平表達,并且與乳腺浸潤性癌的不良預后呈正相關。
另一研究[23]則證明了丙酮酸脫氫酶E1α亞基(pyruvate dehydrogenase E1 alpha subunit,PDHA1)可作為乳腺癌獨立的預后生物標志物和免疫治療的潛在靶點。Sha等[24]分析發現5個CRG差異表達與三陰性乳腺癌(triple negative breast cancer,TNBC)預后顯著相關,其中ATP7A、二氫硫胺S-琥珀酰基轉移酶(dihydrolipoamide S-succinyltransferase,DLST)、LIAS高表達提示總生存期較差, LIPT1、PDHA1高表達提示預后較好,并發現下調ATP7A的表達水平可顯著抑制TNBC細胞的遷移和增殖能力。此外研究[25]發現,細胞周期蛋白依賴性激酶抑制因子2A(cyclin-dependent kinase inhibitor 2A,CDKN2A)可作為TNBC的預后指標,這為TNBC的免疫治療提供了理論基礎,并為通過誘導鐵死亡和銅死亡來開發新的抗癌治療策略提供了依據,從而為腫瘤治療提供新的方向。
2.2 CRG調控乳腺癌細胞對藥物的敏感性
銅通過抑制腫瘤細胞周期、下調信號通路、克服化療耐藥、抗氧化等誘導細胞死亡,阻斷銅離子流出,使線粒體內銅不斷積累。銅不僅能夠通過誘導銅死亡導致腫瘤細胞死亡,還能克服腫瘤細胞對鉑類藥物耐藥[26]。
腫瘤的特征之一是細胞代謝紊亂。FDX1作為調節銅死亡的相關基因,在調節銅死亡和腫瘤進展中發揮重要作用。在大多數癌癥中FDX1的mRNA和蛋白表達均降低,如乳腺癌、結腸腺癌、肺腺癌、甲狀腺癌等;此外,FDX1的表達與抗腫瘤藥物敏感性和耐藥性相關,基因富集分析顯示FDX1與免疫相關通路、免疫細胞浸潤密切相關[27]。FDX1有望成為未來癌癥治療的潛在靶點和評估預后的生物標志物。SLC31A1最可能的上游非編碼RNA調控機制為LINC00511/miR-29c-3p/SLC31A1調控軸,且SLC31A1的表達水平與免疫細胞浸潤、免疫細胞生物標志物以及免疫檢查點表達水平呈顯著正相關,表明SLC31A1的表達水平可以作為某類藥物敏感性的判斷標準[22]。
3 銅死亡與乳腺癌綜合性治療的相關性
3.1 參與免疫治療
銅穩態與癌癥發展之間的關系仍不夠確切,需要進一步探索驗證其復雜性。Liu等[28]利用腫瘤基因組圖譜計劃(TCGA)數據集經泛癌分析發現,CRG與乳腺癌有關,且乳腺癌樣本的免疫浸潤特征與其他癌癥有顯著差異;LASSO-Cox回歸顯示CRG ATP7B和DLAT富集在細胞周期通路中;CRG得分較低組的免疫激活水平更高,存活概率更高,富含丙酮酸代謝和細胞凋亡相關通路,對化療藥物的敏感性更高;免疫組織化學染色顯示,乳腺癌樣本中 ATP7B 和 DLAT 蛋白表達較高。該研究[28]揭示了銅相關基因對乳腺癌的總體生存率、免疫浸潤、藥物敏感性和代謝譜的潛在影響,這些影響可以預測患者的生存率。這些發現可能有助于拓展乳腺癌治療的深入研究[28]。
有研究[29]揭示了CRG風險模型具有指導TNBC免疫治療的潛在應用前景,認為LIAS是銅死亡的關鍵基因,與腫瘤的發病機制和免疫應答有顯著關系,通過生物信息學平臺探索發現其在乳腺癌中表達下調,而LIAS高表達的乳腺癌患者具有更好的總生存期、無遠處轉移生存期、進展后生存期和無復發生存期。此外LIAS的表達水平與M1巨噬細胞數量呈負相關[30]。Zhang等[31]初步發現了銅死亡相關長鏈非編碼RNAs(long noncoding RNAs,LncRNAs)與抗腫瘤免疫之間的聯系,發現受體激酶酪氨酸、信號轉導和轉錄激活因子(Janus signal transducer and activator of transcription,JAK-STAT)信號通路是參與免疫調節的重要通路,但預后模型需要更多的前瞻性、多中心、真實數據進一步驗證。Zhou等[32]基于NLRP3、LIPT1、PDHA1和DLST的表達構建列線圖模型,將患者分為高風險和低風險亞組,結果發現高風險組與癌基因突變相關,更容易發生免疫逃逸,預后較差。Zhu等[29]建立了CRG相關的風險模型,包含6種預后生物標志物:PTPRN2、SCARB1、SLC37A2、YES1、LY6D、NOTCH3,該研究揭示了銅死亡在TNBC免疫微環境中的重要作用,可能有助于指導個性化免疫治療。
Li等[1]分析公共數據庫后發現,銅死亡評分高的乳腺癌患者生存狀態差,對免疫檢查點抑制劑治療敏感。Li等[33]基于TCGA數據庫收集了乳腺癌患者的資料,使用共聚類方法確定了兩種預后不同的簇,開發了銅死亡相關的預后特征和列線圖,驗證了腫瘤微環境對免疫治療的反應。
Cheng等[25]全面分析了CDKN2A在乳腺癌中的生物學作用和預后價值,發現CDKN2A在乳腺癌中過表達,其上調與DNA的超甲基化顯著相關,此外基因與表觀遺傳改變都參與了乳腺癌的發展,提示調節CDKN2A相關基因的通路或設計新型金屬抗癌藥物誘導銅死亡可能會指導我們為乳腺癌開發新的抗癌治療策略。該研究[25]進一步分析發現CDKN2A的過表達與免疫細胞的增加、趨化因子升高相關,CDKN2A高表達的TNBC患者獲益于免疫治療,并且CDKN2A可能是預測TNBC抗表皮生長因子治療效果的有前景的預測性生物標志物。Guo等[34]的研究建立由9個與銅死亡相關的LncRNAs構建的風險模型,建立了LncRNAs-mRNA共表達網絡,發現ARHGAP28-AS1、LINC01711、LRRC8C-DT、PCAT18和SIAH2-AS1是乳腺癌患者的保護因素,而TDRKH-AS1、SAMMSON、WDFY3-AS2和LINC00393是危險因素;風險評分較低的乳腺癌患者CD8+T細胞浸潤率更高,能獲益于免疫治療。Huang等[23]的研究綜合分析了CRG在乳腺癌中的表達譜和分期特征,發現CDKN2A、PDHA1和LIPT1的表達與乳腺癌的病理分級相關,其中上調的PDHA1與乳腺癌中較短的總生存期和無復發生存期相關,與乳腺癌中的CD4+ 記憶T細胞、巨噬細胞和肥大細胞數量密切相關,為進一步研究PDHA1作為乳腺癌的潛在靶點提供了思路。
Song等[35]全面分析了CRG在腫瘤微環境和免疫治療中的作用,構建與銅死亡相關的基因特征(PGK1、SLC52A2、SEC14L2、RAD23B、SLC16A6、CCL5和MAL2)和評分系統,以預測乳腺癌的總生存期和對免疫治療的反應,發現RAD23B上調的患者對靶向程序性死亡受體1(programmed death receptor 1,PD-1)/程序性死亡-配體1(programmed death receptor 1,PD-L1)軸的免疫檢查點阻斷療法更敏感,為乳腺癌患者的個性化免疫治療提供了參考。
3.2 參與內分泌藥物耐藥
雌激素受體(estrogen receptor,ER)陽性乳腺癌約占臨床乳腺癌患者的80%[36],對ER陽性乳腺癌患者給予ET至關重要。他莫昔芬(tamoxifen,TAM)是主要的ET藥物,但仍有患者因TAM耐藥導致疾病復發和轉移[37]。發現ET新的耐藥機制和確定新的治療靶點一直是近年來乳腺癌研究的重點。很少有研究關注銅穩態和ET的關系,闡明銅死亡在ET耐藥中的潛在作用機制可能會為乳腺癌提供新的治療途徑。Zhang等[38]調查了ER陽性乳腺癌中銅死亡和ET耐藥的潛在關聯,構建了由DLD、DBT、DLAT和ATP7A組成的CRG風險評分,其中DLD對銅死亡至關重要。DLD不僅與ER陽性乳腺癌患者的預后顯著相關,而且與對TAM和氟維司群雙重耐藥的LCC9細胞系和對ET敏感的MCF-7細胞系中miRNA的表達也存在顯著關系,因此推測DLD高水平的表達可能導致銅穩態的失衡。該研究進一步分析了治療靶點,建立了由C6orf99/hsa-miR-370-3p和hsa-miR-432-5p/DLD組成的ceRNA網絡,并確定了一個銅代謝ET耐藥軸,這為深入研究乳腺癌內分泌藥物耐藥的預防和逆轉提供了潛在的靶點[38]。
3.3 調控化療藥物耐藥
銅穩態相關基因和化療耐藥性相關。癌癥中CRG的表達與癌細胞對多種化學物質的敏感性有關,具體耐藥機制因藥物而異。因此,需要進一步探索銅代謝相關細胞死亡在不同耐藥性中的機制。Li等[21]發現SLC31A1拷貝數變異、G2E3-AS1/let-7a-5p軸、CDKN2B-AS1/let-7b-5p通路可能是導致SLC31A1在乳腺癌中過表達的另一種機制,SLC31A1在化療無反應組中明顯上調,可以預測化療藥物的敏感性。此外,Li等[39]使用癌癥免疫圖譜和TCGA數據庫發現SLC31A1與紫杉醇藥物不良反應相關,可能是克服乳腺癌耐藥的新型治療靶點。
4 銅衍生物在乳腺癌治療中的應用
銅死亡機制的發現為未來藥物的研究提供了方向,銅離子載體和銅螯合劑已被用于抗癌治療[40-42]。銅離子載體的作用方式多種多樣,包括DNA相互作用、蛋白酶體抑制和ROS生成[43]。口服銅螯合劑四硫鉬酸鹽(tetrathiomolybdate,TM)經銅耗竭機制、通過抑制復合體Ⅳ的失活和減少線粒體氧化ATP的生成來阻止TNBC的轉移[44]。銅還通過促進腫瘤細胞增殖和血管生成而促進癌癥的發展。因此,銅鰲合劑已在臨床試驗中應用于抑制腫瘤轉移[45]。將銅離子與銅離子載體結合的納米藥物目前正在廣泛研究中,它可以通過銅誘導細胞死亡實現靶向腫瘤的精準治療[46-47]。銅離子載體可能對線粒體代謝水平較高的腫瘤更有效,其他藥物聯合銅離子載體誘導腫瘤高線粒體呼吸狀態也是一個潛在的治療方向[18]。Cui等[48]開發了一種安全的、靶向線粒體的銅消耗納米顆粒(copper depletion nanoparticles,CDN),并在TNBC中進行了測試,結果發現CDN可減少耗氧量和氧化磷酸化,導致代謝轉換為糖酵解,并減少TNBC細胞中ATP的產生。CDN的毒性低于現有的銅螯合劑,有利于剝奪癌細胞線粒體中的銅,而不是全身耗竭,在乳腺癌小鼠模型中,CDN給藥可抑制腫瘤生長并顯著提高存活率[48]。CDN的有效性和安全性表明這種方法具有潛在的臨床相關性。
銅死亡途徑為腫瘤治療帶來新的機遇,而在腫瘤中高效、靶向誘導銅死亡仍然面臨挑戰。雙硫侖(disulfiram,DSF)已被證明能夠誘導銅死亡[7]。DSF與銅離子結合時,增加細胞內銅離子濃度,導致Wnt通路中兩個重要分子β-catenin和C-myc的表達水平降低,從而抑制腫瘤生長。DSF在多種癌癥中具有抗腫瘤活性[49]。臨床研究[50-51]表明,DSF聯合銅可特異性靶向醛脫氫酶(aldehyde dehydro- genase,ALDH),降低腫瘤復發風險。Liu等[52]將DSF/Cu2+負載的MXene納米片涂覆在PD-1過度表達的T細胞膜上,生成CuX-P系統,該系統能識別表達PD-L1的腫瘤細胞并黏附,從而促進腫瘤細胞對CuX-P和PD-L1的內吞。DSF/Cu2+內化并在細胞質中釋放后,PD-L1的表達就會上調。由于腫瘤微環境中存在CuX-P,腫瘤表面補充的PD-L1又會再次與CuX-P結合進行內化。這種反饋循環不斷阻斷和消耗腫瘤表面的PD-L1,促進腫瘤中CuX-P的富集,誘導銅死亡。在TNBC小鼠模型中,給予激光照射CuX-P治療后,激發了強烈的抗腫瘤免疫反應[52]。因此,該研究開發了一種腫瘤靶向生物仿生系統,可對小鼠誘導銅死亡的同時進行光熱療法和免疫療法[52]。
5 銅死亡聯合治療
鹽酸小檗堿在多種類型的癌細胞中具備化療療效,與銅死亡的結合可能會提高抗癌潛力[53-54]。
P53可以抑制糖酵解途徑和促進線粒體呼吸,導致細胞從糖酵解到氧化磷酸化的轉變,提供更多的能量,協調鐵硫簇、銅螯合劑谷胱甘肽(glutathione,GSH)合成的水平,進一步通過提高代謝水平來增加對銅死亡的敏感性,與此同時GSH的氧化還原作用促進了細胞內銅的釋放[55]。
Shen等[56]發現,PTEN敲除后SLC31A1的表達上調,而TFAM敲除后ATP7A水平升高,ATF2敲低后LIPT1被抑制;這表明銅死亡和鐵死亡之間存在較強的相關性,因此推測在癌癥中,銅死亡和鐵死亡調節因子之間存在著相互作用和生物學調控。
6 小結與展望
乳腺癌是一種常見的惡性腫瘤,發病率在女性中居高不下。盡管目前已經了解到很多與乳腺癌發生有關的因素,它仍然是一種具有挑戰性的疾病。隨著醫學技術和研究的不斷進展,我們對于乳腺癌的認識和治療手段也在不斷地提高和完善,對患者生存質量愈加重視并提供個體化干預措施[57]。隨著銅死亡概念的引入,以及銅通過靶向蛋白脂酰化修飾來影響細胞命運的機制的不斷闡明,為開發新的抗腫瘤藥物提供了新思路。銅可能成為具有潛力的抑制癌癥發生的靶點,且既往研究為探索銅死亡和腫瘤的關系提供了充分的依據。銅金屬結合化合物在治療癌癥方面具有巨大的潛力,能夠選擇性靶向癌細胞的新型銅結合化合物備受關注。銅離子載體和銅螯合劑都被認為是抗癌劑,在多種腫瘤中已進行臨床前及臨床研究。銅死亡在乳腺癌治療中的作用也有所突破。盡管銅離子載體目前尚未在臨床中廣泛應用,但銅螯合劑TM、AmphinexTM(ATN-224)在乳腺癌領域已經進入Ⅱ期臨床試驗。
大部分理論研究表明銅離子載體利用氧化應激引起癌細胞的易感性,因此靶向銅死亡可以治療乳腺癌,下一代選擇性銅離子載體應該利用僅能被特定受體識別的靶向單元。然而這些受體僅存在于特定類型的癌細胞中,應該預先評估可能受益的患者群體,比如篩選具有較高線粒體代謝、腫瘤干細胞特性及某些藥物耐藥的癌癥患者,拓展乳腺癌精準治療。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:任黎蕾查閱文獻、設計選題及撰寫文章,趙小波和高硯春對論文寫作進行指導,侯令密對文章及選題設計進行指導。
乳腺癌(breast cancer)是全世界女性中最普遍的惡性腫瘤。近幾十年來,盡管發現內分泌治療(endocrine therapy,ET)、化療、免疫治療和聯合治療可改善乳腺癌的預后,但乳腺癌異質性和復雜性的特點,對改善乳腺癌的臨床生存期提出了挑戰。
一般來講,細胞死亡分為意外細胞死亡和調節性細胞死亡(regulatory cell death,RCD)。ACD是一個不可控的生物學過程,而RCD具有精確的分子機制和復雜的信號調節途徑。目前已有數十種RCD,其中細胞凋亡、焦亡、自噬、鐵死亡和壞死已被廣泛研究。通過誘導癌細胞死亡是癌癥治療的常見策略。銅死亡作為一種新型細胞死亡方式,是銅誘導的線粒體細胞死亡方式,參與腫瘤的增殖與轉移,在乳腺癌治療中具有重要作用[1]。筆者現就銅死亡及其衍生物在腫瘤進展中的機制及其在乳腺癌中的相關研究進行綜述。
1 銅死亡概述
1.1 銅在銅死亡中的作用
銅是介導細胞功能的酶的重要輔助因子。銅穩態是維持細胞基本功能的保證,體內銅轉運涉及多種銅分子伴侶和銅轉運體。金屬還原酶將細胞外Cu2+ 還原為Cu+,銅轉運蛋白1(copper transport protein,CTR1)將Cu+從細胞外轉移到細胞內,進入細胞內的銅離子通過銅分子伴侶轉運。研究[2]表明,CTR1在黑色素瘤、肝癌、前列腺癌和其他人類癌細胞系中高度表達。2014年Brady等[3]證實了CTR1調控的銅間接調節絲氨酸-蘇氨酸激酶(serine/threonine-protein kinase B-raf,BRAF)/絲裂原活化的細胞外信號調節激酶(mitogen-activated extracellular signal-regulated kinase,MEK)/細胞外信號調節激酶(extracellular signal-regulated kinase,ERK)信號通路,最終抑制腫瘤生長。
銅轉運蛋白質α鏈抗體(ATPase copper transporting alpha polypeptide,ATP7A)和銅轉運蛋白質β鏈抗體(ATPase copper transporting beta polypeptide,ATP7B)是P型銅輸出ATP酶P1B亞家族的兩個成員。研究[4]表明,應用CRISPR/Cas9沉默ATP7A后,賴氨酸氧化酶的活性在乳腺癌和肺癌細胞系中受到抑制,進一步抑制腫瘤細胞的生長和遷移。此外,靶向ATP7A或ATP7B在克服腫瘤細胞對鉑類藥物的耐藥性方面具有廣闊的應用空間[5]。
銅誘導程序性細胞死亡的機制一直備受人們的關注,早在20世紀80年代學者就發現銅會導致細胞死亡,但確切的機制未得到證實[6]。直到Tsvetkov等[7]的研究顯示,在人類細胞中銅依賴性受控細胞死亡是一種不同于已知細胞死亡機制的由銅介導的新型細胞死亡方式,它是通過銅離子與線粒體呼吸中的三羧酸循環(tricarboxylic acid cycle,TCA)中的脂酰化成分直接結合而發生的,導致脂酰化蛋白質聚集和隨后的鐵硫簇蛋白表達下調,進而發生蛋白質毒性應激并導致細胞死亡,該團隊將這種死亡方式命名為銅死亡,但該研究中銅死亡的細胞形態學變化尚未明確,缺乏有效評估銅死亡的方法。細胞中銅的積累可能通過鐵氧還蛋白1(ferredoxin one,FDX1)介導Cu2+還原成Cu+,鐵硫簇蛋白的降解、脂酰化,二氫硫辛酰胺S-乙酰轉移酶(dihydrolipoamide S-acetyltransferase,DLAT)的聚焦來誘導銅死亡[7-8]。
1.2 銅在乳腺癌中的作用
銅是人生命活動中必不可少的微量元素[9]。研究[10-12]發現,與健康人相比,多種癌癥患者的血清和腫瘤組織中的銅含量顯著改變,其在癌癥的發生發展中起到關鍵作用。銅已被證明能促進癌癥進展和轉移過程中至關重要的血管生成,可以激活血管生成因子,如血管生成素、血管內皮生長因子、成纖維細胞生長因子1、白細胞介素1等。乳腺癌的發生與體內微量元素(如Cu、Zn、Se)異常相關[13],微量元素的檢測可能有助于乳腺癌的早期預防和預后[14]。銅也是自噬激酶驅動肺腺癌的重要調節因子[15],且是一種具有高度氧化還原活性的元素,銅的失調會導致活性氧(reaticve oxygen species,ROS)的過量產生。這些過量的ROS可以作為腫瘤轉化發展和轉移形成的前體。Bengtsson等[16]針對1 998例新診斷乳腺癌患者的前瞻性隊列研究是第一項檢查血清銅水平和銅/鋅比值與乳腺癌存活率之間關系的研究,結果發現較高的血清銅/鋅比值與乳腺癌診斷后較差的總體生存率相關。但Jouybari等[17]的薈萃分析不支持銅水平與乳腺癌之間存在關聯,但同時也指出由于原始研究結果的高度異質性,需要設計良好的前瞻性研究來證實這一結論。
1.3 銅死亡的發生機制
銅是諸多生物過程的基礎元素,包括線粒體呼吸、鐵吸收、抗氧化、解毒等過程,銅通常在哺乳動物細胞內維持極低的水平,細胞內銅離子濃度超過維持穩態機制的閾值時,同樣會表現出細胞毒性。在人類細胞中,依賴于銅的受調節的細胞死亡不同于已知的死亡機制,并且銅死亡依賴于線粒體呼吸。之前關于銅誘導的細胞死亡的研究中,大多數學者將銅死亡歸因于銅對線粒體的作用導致ROS的產生[18]。線粒體呼吸可調節銅離子載體誘導的細胞死亡,依賴線粒體呼吸的細胞對銅離子誘導劑的敏感度是依賴糖酵解細胞的1 000倍左右,用線粒體抗氧化劑、脂肪酸和線粒體功能抑制劑處理都會明顯改變細胞對銅離子的敏感性。線粒體解偶聯劑對銅毒性沒有影響,這表明銅誘導的細胞死亡需要線粒體呼吸,而不是三磷酸腺苷(adenosine triphosphate,ATP)。代謝組學研究發現,對銅離子敏感細胞的代謝組學中,與TCA相關的代謝物明顯增多,表明銅誘導的細胞死亡和線粒體代謝緊密相關[7]。總之銅死亡的主要過程依賴于細胞內銅離子的積累,銅離子與TCA的脂酰化成分直接結合導致脂酰化蛋白質聚集,鐵硫簇蛋白失調,進而引發蛋白質毒性應激,并最終導致細胞死亡。
FDX1和脂酰化蛋白的豐度與多種人類腫瘤高度相關,具有高水平脂酰化蛋白的細胞系被證實對銅死亡更加敏感。研究人員[7]進行了全基因組CRISPR-Cas9功能喪失篩選,確定了參與銅離子載體誘導死亡的基因,發現敲除FDX1基因以及6個脂酰化蛋白基因(LIPT1、DLD、LIAS、DLAT、PDHA1、PDHB)可以挽救銅離子對細胞的殺傷作用,認為FDX1是銅離子載體誘導細胞死亡的關鍵介質。FDX1是蛋白質脂酰化的上游調節因子,其缺失導致了蛋白質脂酰化功能的完全喪失,以及細胞內丙酮酸、α-酮戊二酸的積累與琥珀酸的消耗,阻斷了TCA的進行。銅與脂酰化TCA循環蛋白的結合導致DLAT的脂酰化依賴性寡聚化。銅誘導的死亡機制與銅穩態失調的遺傳模型相同,Jiang等[19]經生物信息學方法分析了人FDX1基因的核酸結構,預測了潛在的生物學功能,并探討了乳腺癌銅死亡相關預后特征和調控軸。FDX1、LIAS、DLAT被命名為銅死亡相關基因(Cu death related gene,CRG),在調節銅死亡機制方面發揮重要作用,且銅轉運蛋白CTR1,以及銅轉運酶ATP7A和ATP7B主要參與調節銅濃度的動態平衡,因此CRG和銅轉運蛋白將成為未來癌癥研究的重點,為腫瘤的診斷和治療提供理論支持和參考,其機制見圖1。
 圖1
示銅死亡機制圖
圖1
示銅死亡機制圖
Copper ionophores:銅離子載體;Glucose:葡萄糖;Pyruvate:丙酮酸;Fe-S:鐵硫簇蛋白;DLAT lipoylation:二氫硫辛酰胺S-乙酰轉移酶硫酰化;PDH complex:丙酮酸脫氫酶復合物;TCA cycle:TCA 循環;Cuproptosis:銅死亡
2 CRG與乳腺癌的相關性
大多數癌癥治療的目的是通過殺死癌細胞或阻止癌細胞遷移來減少癌細胞,實現癌細胞減少的最根本途徑是誘導癌細胞死亡,因此,任何類型的細胞死亡對癌癥研究人員都具有重要意義。最近發現的銅死亡將成為癌細胞死亡研究的下一個熱點,探索銅死亡相關調節機制在腫瘤中的作用可增強對腫瘤的認識與治療。
2.1 CRG是乳腺癌的預后指標
溶質載體家族31成員1(solute carrier family 31,SLC31A1)是最近發現的CRG,作為銅轉運蛋白家族基因的一員,SLC31A1與眾多腫瘤發生和預后相關,可能是一種潛在的癌癥關鍵生物標志物和治療靶點[20]。Li等[21]發現CRG SLC31A1是預測乳腺癌診斷、預后和治療反應的潛在指標。劉以原[22]發現SLC31A1在包括乳腺浸潤性癌在內的多種人類腫瘤中呈高水平表達,并且與乳腺浸潤性癌的不良預后呈正相關。
另一研究[23]則證明了丙酮酸脫氫酶E1α亞基(pyruvate dehydrogenase E1 alpha subunit,PDHA1)可作為乳腺癌獨立的預后生物標志物和免疫治療的潛在靶點。Sha等[24]分析發現5個CRG差異表達與三陰性乳腺癌(triple negative breast cancer,TNBC)預后顯著相關,其中ATP7A、二氫硫胺S-琥珀酰基轉移酶(dihydrolipoamide S-succinyltransferase,DLST)、LIAS高表達提示總生存期較差, LIPT1、PDHA1高表達提示預后較好,并發現下調ATP7A的表達水平可顯著抑制TNBC細胞的遷移和增殖能力。此外研究[25]發現,細胞周期蛋白依賴性激酶抑制因子2A(cyclin-dependent kinase inhibitor 2A,CDKN2A)可作為TNBC的預后指標,這為TNBC的免疫治療提供了理論基礎,并為通過誘導鐵死亡和銅死亡來開發新的抗癌治療策略提供了依據,從而為腫瘤治療提供新的方向。
2.2 CRG調控乳腺癌細胞對藥物的敏感性
銅通過抑制腫瘤細胞周期、下調信號通路、克服化療耐藥、抗氧化等誘導細胞死亡,阻斷銅離子流出,使線粒體內銅不斷積累。銅不僅能夠通過誘導銅死亡導致腫瘤細胞死亡,還能克服腫瘤細胞對鉑類藥物耐藥[26]。
腫瘤的特征之一是細胞代謝紊亂。FDX1作為調節銅死亡的相關基因,在調節銅死亡和腫瘤進展中發揮重要作用。在大多數癌癥中FDX1的mRNA和蛋白表達均降低,如乳腺癌、結腸腺癌、肺腺癌、甲狀腺癌等;此外,FDX1的表達與抗腫瘤藥物敏感性和耐藥性相關,基因富集分析顯示FDX1與免疫相關通路、免疫細胞浸潤密切相關[27]。FDX1有望成為未來癌癥治療的潛在靶點和評估預后的生物標志物。SLC31A1最可能的上游非編碼RNA調控機制為LINC00511/miR-29c-3p/SLC31A1調控軸,且SLC31A1的表達水平與免疫細胞浸潤、免疫細胞生物標志物以及免疫檢查點表達水平呈顯著正相關,表明SLC31A1的表達水平可以作為某類藥物敏感性的判斷標準[22]。
3 銅死亡與乳腺癌綜合性治療的相關性
3.1 參與免疫治療
銅穩態與癌癥發展之間的關系仍不夠確切,需要進一步探索驗證其復雜性。Liu等[28]利用腫瘤基因組圖譜計劃(TCGA)數據集經泛癌分析發現,CRG與乳腺癌有關,且乳腺癌樣本的免疫浸潤特征與其他癌癥有顯著差異;LASSO-Cox回歸顯示CRG ATP7B和DLAT富集在細胞周期通路中;CRG得分較低組的免疫激活水平更高,存活概率更高,富含丙酮酸代謝和細胞凋亡相關通路,對化療藥物的敏感性更高;免疫組織化學染色顯示,乳腺癌樣本中 ATP7B 和 DLAT 蛋白表達較高。該研究[28]揭示了銅相關基因對乳腺癌的總體生存率、免疫浸潤、藥物敏感性和代謝譜的潛在影響,這些影響可以預測患者的生存率。這些發現可能有助于拓展乳腺癌治療的深入研究[28]。
有研究[29]揭示了CRG風險模型具有指導TNBC免疫治療的潛在應用前景,認為LIAS是銅死亡的關鍵基因,與腫瘤的發病機制和免疫應答有顯著關系,通過生物信息學平臺探索發現其在乳腺癌中表達下調,而LIAS高表達的乳腺癌患者具有更好的總生存期、無遠處轉移生存期、進展后生存期和無復發生存期。此外LIAS的表達水平與M1巨噬細胞數量呈負相關[30]。Zhang等[31]初步發現了銅死亡相關長鏈非編碼RNAs(long noncoding RNAs,LncRNAs)與抗腫瘤免疫之間的聯系,發現受體激酶酪氨酸、信號轉導和轉錄激活因子(Janus signal transducer and activator of transcription,JAK-STAT)信號通路是參與免疫調節的重要通路,但預后模型需要更多的前瞻性、多中心、真實數據進一步驗證。Zhou等[32]基于NLRP3、LIPT1、PDHA1和DLST的表達構建列線圖模型,將患者分為高風險和低風險亞組,結果發現高風險組與癌基因突變相關,更容易發生免疫逃逸,預后較差。Zhu等[29]建立了CRG相關的風險模型,包含6種預后生物標志物:PTPRN2、SCARB1、SLC37A2、YES1、LY6D、NOTCH3,該研究揭示了銅死亡在TNBC免疫微環境中的重要作用,可能有助于指導個性化免疫治療。
Li等[1]分析公共數據庫后發現,銅死亡評分高的乳腺癌患者生存狀態差,對免疫檢查點抑制劑治療敏感。Li等[33]基于TCGA數據庫收集了乳腺癌患者的資料,使用共聚類方法確定了兩種預后不同的簇,開發了銅死亡相關的預后特征和列線圖,驗證了腫瘤微環境對免疫治療的反應。
Cheng等[25]全面分析了CDKN2A在乳腺癌中的生物學作用和預后價值,發現CDKN2A在乳腺癌中過表達,其上調與DNA的超甲基化顯著相關,此外基因與表觀遺傳改變都參與了乳腺癌的發展,提示調節CDKN2A相關基因的通路或設計新型金屬抗癌藥物誘導銅死亡可能會指導我們為乳腺癌開發新的抗癌治療策略。該研究[25]進一步分析發現CDKN2A的過表達與免疫細胞的增加、趨化因子升高相關,CDKN2A高表達的TNBC患者獲益于免疫治療,并且CDKN2A可能是預測TNBC抗表皮生長因子治療效果的有前景的預測性生物標志物。Guo等[34]的研究建立由9個與銅死亡相關的LncRNAs構建的風險模型,建立了LncRNAs-mRNA共表達網絡,發現ARHGAP28-AS1、LINC01711、LRRC8C-DT、PCAT18和SIAH2-AS1是乳腺癌患者的保護因素,而TDRKH-AS1、SAMMSON、WDFY3-AS2和LINC00393是危險因素;風險評分較低的乳腺癌患者CD8+T細胞浸潤率更高,能獲益于免疫治療。Huang等[23]的研究綜合分析了CRG在乳腺癌中的表達譜和分期特征,發現CDKN2A、PDHA1和LIPT1的表達與乳腺癌的病理分級相關,其中上調的PDHA1與乳腺癌中較短的總生存期和無復發生存期相關,與乳腺癌中的CD4+ 記憶T細胞、巨噬細胞和肥大細胞數量密切相關,為進一步研究PDHA1作為乳腺癌的潛在靶點提供了思路。
Song等[35]全面分析了CRG在腫瘤微環境和免疫治療中的作用,構建與銅死亡相關的基因特征(PGK1、SLC52A2、SEC14L2、RAD23B、SLC16A6、CCL5和MAL2)和評分系統,以預測乳腺癌的總生存期和對免疫治療的反應,發現RAD23B上調的患者對靶向程序性死亡受體1(programmed death receptor 1,PD-1)/程序性死亡-配體1(programmed death receptor 1,PD-L1)軸的免疫檢查點阻斷療法更敏感,為乳腺癌患者的個性化免疫治療提供了參考。
3.2 參與內分泌藥物耐藥
雌激素受體(estrogen receptor,ER)陽性乳腺癌約占臨床乳腺癌患者的80%[36],對ER陽性乳腺癌患者給予ET至關重要。他莫昔芬(tamoxifen,TAM)是主要的ET藥物,但仍有患者因TAM耐藥導致疾病復發和轉移[37]。發現ET新的耐藥機制和確定新的治療靶點一直是近年來乳腺癌研究的重點。很少有研究關注銅穩態和ET的關系,闡明銅死亡在ET耐藥中的潛在作用機制可能會為乳腺癌提供新的治療途徑。Zhang等[38]調查了ER陽性乳腺癌中銅死亡和ET耐藥的潛在關聯,構建了由DLD、DBT、DLAT和ATP7A組成的CRG風險評分,其中DLD對銅死亡至關重要。DLD不僅與ER陽性乳腺癌患者的預后顯著相關,而且與對TAM和氟維司群雙重耐藥的LCC9細胞系和對ET敏感的MCF-7細胞系中miRNA的表達也存在顯著關系,因此推測DLD高水平的表達可能導致銅穩態的失衡。該研究進一步分析了治療靶點,建立了由C6orf99/hsa-miR-370-3p和hsa-miR-432-5p/DLD組成的ceRNA網絡,并確定了一個銅代謝ET耐藥軸,這為深入研究乳腺癌內分泌藥物耐藥的預防和逆轉提供了潛在的靶點[38]。
3.3 調控化療藥物耐藥
銅穩態相關基因和化療耐藥性相關。癌癥中CRG的表達與癌細胞對多種化學物質的敏感性有關,具體耐藥機制因藥物而異。因此,需要進一步探索銅代謝相關細胞死亡在不同耐藥性中的機制。Li等[21]發現SLC31A1拷貝數變異、G2E3-AS1/let-7a-5p軸、CDKN2B-AS1/let-7b-5p通路可能是導致SLC31A1在乳腺癌中過表達的另一種機制,SLC31A1在化療無反應組中明顯上調,可以預測化療藥物的敏感性。此外,Li等[39]使用癌癥免疫圖譜和TCGA數據庫發現SLC31A1與紫杉醇藥物不良反應相關,可能是克服乳腺癌耐藥的新型治療靶點。
4 銅衍生物在乳腺癌治療中的應用
銅死亡機制的發現為未來藥物的研究提供了方向,銅離子載體和銅螯合劑已被用于抗癌治療[40-42]。銅離子載體的作用方式多種多樣,包括DNA相互作用、蛋白酶體抑制和ROS生成[43]。口服銅螯合劑四硫鉬酸鹽(tetrathiomolybdate,TM)經銅耗竭機制、通過抑制復合體Ⅳ的失活和減少線粒體氧化ATP的生成來阻止TNBC的轉移[44]。銅還通過促進腫瘤細胞增殖和血管生成而促進癌癥的發展。因此,銅鰲合劑已在臨床試驗中應用于抑制腫瘤轉移[45]。將銅離子與銅離子載體結合的納米藥物目前正在廣泛研究中,它可以通過銅誘導細胞死亡實現靶向腫瘤的精準治療[46-47]。銅離子載體可能對線粒體代謝水平較高的腫瘤更有效,其他藥物聯合銅離子載體誘導腫瘤高線粒體呼吸狀態也是一個潛在的治療方向[18]。Cui等[48]開發了一種安全的、靶向線粒體的銅消耗納米顆粒(copper depletion nanoparticles,CDN),并在TNBC中進行了測試,結果發現CDN可減少耗氧量和氧化磷酸化,導致代謝轉換為糖酵解,并減少TNBC細胞中ATP的產生。CDN的毒性低于現有的銅螯合劑,有利于剝奪癌細胞線粒體中的銅,而不是全身耗竭,在乳腺癌小鼠模型中,CDN給藥可抑制腫瘤生長并顯著提高存活率[48]。CDN的有效性和安全性表明這種方法具有潛在的臨床相關性。
銅死亡途徑為腫瘤治療帶來新的機遇,而在腫瘤中高效、靶向誘導銅死亡仍然面臨挑戰。雙硫侖(disulfiram,DSF)已被證明能夠誘導銅死亡[7]。DSF與銅離子結合時,增加細胞內銅離子濃度,導致Wnt通路中兩個重要分子β-catenin和C-myc的表達水平降低,從而抑制腫瘤生長。DSF在多種癌癥中具有抗腫瘤活性[49]。臨床研究[50-51]表明,DSF聯合銅可特異性靶向醛脫氫酶(aldehyde dehydro- genase,ALDH),降低腫瘤復發風險。Liu等[52]將DSF/Cu2+負載的MXene納米片涂覆在PD-1過度表達的T細胞膜上,生成CuX-P系統,該系統能識別表達PD-L1的腫瘤細胞并黏附,從而促進腫瘤細胞對CuX-P和PD-L1的內吞。DSF/Cu2+內化并在細胞質中釋放后,PD-L1的表達就會上調。由于腫瘤微環境中存在CuX-P,腫瘤表面補充的PD-L1又會再次與CuX-P結合進行內化。這種反饋循環不斷阻斷和消耗腫瘤表面的PD-L1,促進腫瘤中CuX-P的富集,誘導銅死亡。在TNBC小鼠模型中,給予激光照射CuX-P治療后,激發了強烈的抗腫瘤免疫反應[52]。因此,該研究開發了一種腫瘤靶向生物仿生系統,可對小鼠誘導銅死亡的同時進行光熱療法和免疫療法[52]。
5 銅死亡聯合治療
鹽酸小檗堿在多種類型的癌細胞中具備化療療效,與銅死亡的結合可能會提高抗癌潛力[53-54]。
P53可以抑制糖酵解途徑和促進線粒體呼吸,導致細胞從糖酵解到氧化磷酸化的轉變,提供更多的能量,協調鐵硫簇、銅螯合劑谷胱甘肽(glutathione,GSH)合成的水平,進一步通過提高代謝水平來增加對銅死亡的敏感性,與此同時GSH的氧化還原作用促進了細胞內銅的釋放[55]。
Shen等[56]發現,PTEN敲除后SLC31A1的表達上調,而TFAM敲除后ATP7A水平升高,ATF2敲低后LIPT1被抑制;這表明銅死亡和鐵死亡之間存在較強的相關性,因此推測在癌癥中,銅死亡和鐵死亡調節因子之間存在著相互作用和生物學調控。
6 小結與展望
乳腺癌是一種常見的惡性腫瘤,發病率在女性中居高不下。盡管目前已經了解到很多與乳腺癌發生有關的因素,它仍然是一種具有挑戰性的疾病。隨著醫學技術和研究的不斷進展,我們對于乳腺癌的認識和治療手段也在不斷地提高和完善,對患者生存質量愈加重視并提供個體化干預措施[57]。隨著銅死亡概念的引入,以及銅通過靶向蛋白脂酰化修飾來影響細胞命運的機制的不斷闡明,為開發新的抗腫瘤藥物提供了新思路。銅可能成為具有潛力的抑制癌癥發生的靶點,且既往研究為探索銅死亡和腫瘤的關系提供了充分的依據。銅金屬結合化合物在治療癌癥方面具有巨大的潛力,能夠選擇性靶向癌細胞的新型銅結合化合物備受關注。銅離子載體和銅螯合劑都被認為是抗癌劑,在多種腫瘤中已進行臨床前及臨床研究。銅死亡在乳腺癌治療中的作用也有所突破。盡管銅離子載體目前尚未在臨床中廣泛應用,但銅螯合劑TM、AmphinexTM(ATN-224)在乳腺癌領域已經進入Ⅱ期臨床試驗。
大部分理論研究表明銅離子載體利用氧化應激引起癌細胞的易感性,因此靶向銅死亡可以治療乳腺癌,下一代選擇性銅離子載體應該利用僅能被特定受體識別的靶向單元。然而這些受體僅存在于特定類型的癌細胞中,應該預先評估可能受益的患者群體,比如篩選具有較高線粒體代謝、腫瘤干細胞特性及某些藥物耐藥的癌癥患者,拓展乳腺癌精準治療。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:任黎蕾查閱文獻、設計選題及撰寫文章,趙小波和高硯春對論文寫作進行指導,侯令密對文章及選題設計進行指導。