引用本文: 叢赟, 李國煜, 王丹妮, 邵英梅, 吐爾干艾力·阿吉, 狄濤. 肝細胞癌行根治性肝切除術后早期復發的危險因素分析及其預測模型的建立. 中國普外基礎與臨床雜志, 2024, 31(4): 433-438. doi: 10.7507/1007-9424.202312030 復制
版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
肝細胞癌(hepatocellular carcinoma,HCC)占世界癌癥發病率的第6位和癌癥死亡率的第3位[1]且呈上升趨勢[2]。目前,根治性肝切除仍是HCC最常用且最有效的治療方法。然而HCC病程隱匿,多數患者就診時錯過了根治性手術治療時機。《原發性肝癌診療指南(2022年版)》[3]將外科手術切除治療HCC的適應證擴大至Ⅲa期,這樣可能會間接導致術后復發概率增加。因此,探究HCC術后預測早期復發的危險因素具有一定的臨床價值。既往相關研究通常使用logistic回歸模型來探討HCC術后早期復發的影響因素,相比之下,近年來興起的列線圖具有預測連續數值直觀、解釋更明確、計算簡單、表現穩定且具有較好的擬合效果等優勢,可將影響因素量化并以圖形方式直觀計算結局事件概率。本研究結合HCC手術治療患者的一般臨床資料、腫瘤信息和圍術期資料,探討了HCC術后早期復發的影響因素并構建了風險預測列線圖模型,以幫助預測術后復發風險。
1 資料與方法
1.1 患者納入和排除標準
回顧性收集2017年8月至2021年8月期間在新疆醫科大學第一附屬醫院收治的HCC患者的臨床病理資料。納入標準:① 符合《原發性肝癌診療規范(2019年版)》[4]診斷標準且術后標本經組織病理學檢查確診為HCC;② 行根治性肝切除且經組織病理學檢查證實切緣陰性(R0切除);③ 臨床病理資料及隨訪資料完整者;④ 術后2年內復發患者。排除標準:① 術后因出現嚴重心、肺、腦、腎等臟器并發癥或感染出血原因導致圍術期死亡患者;② 巴塞羅那臨床肝癌(Barcelona Clinic Liver Cancer,BCLC)分期D期患者;③ Child-Pugh分級C級患者;④ 伴有其他惡性腫瘤病史;⑤ 伴有自身免疫性疾病、血液系統疾病等;⑥ 非腫瘤復發及轉移原因死亡患者。本研究中全部患者均知情同意并獲得醫院倫理委員會批準通過。
1.2 資料收集
1.2.1 患者術前一般臨床資料
① 人口學數據:年齡、性別、體質量指數(body mass index,BMI);② 病因:乙型肝炎病毒(hepatitis B virus,HBV)病史、脂肪肝病史等。③ 實驗室參數:中性粒細胞(neutrophils,Neut)計數、血小板(platelet,PLT)計數、淋巴細胞(lymphocyte,Lym)計數、乳酸脫氫酶(lactate dehydrogenase,LDH)、血紅蛋白(hemoglobin,Hb)、國際標準化比率(international normalized ratio,INR),同時計算中性粒細胞與淋巴細胞比率(neutrophil to lymphocyte ratio,NLR)和血小板與淋巴細胞比率(platelet to lymphocyte ratio,PLR),其計算方法分別是:NLR=Neut絕對計數/Lym絕對計數×100%、PLR=PLT絕對計數/Lym絕對計數×100%。④ 肝功能相關指標:Child-Pugh分級和肝硬化病史、丙氨酸轉氨酶(aspartate aminotransferase,ALT)、天冬氨酸轉氨酶(alanine aminotransferase,AST)、總膽紅素(total bilirubin,TB)、白蛋白(albumin,Alb)、γ-谷氨酰轉移酶(γ-glutamyl transferase,GGT)、堿性磷酸酶(alkaline phosphatase,ALP),同時計算血小板-白蛋白-膽紅素指數(platelet-albumin-bilirubin index,PALBI)[5],其計算公式:PALBI=(2.02×log10TB)+[–0.37×(log10TB)2]+(–0.04×Alb)+(–3.48×log10PLT)+[1.01×(log10PLT)2],其結果分為1級(≤–2.53)、2級(–2.53,–2.09)和3級(>–2.09)[6] 3個等級。
1.2.2 腫瘤信息和圍術期相關臨床資料
① 腫瘤信息:數量、大小(指直徑)、甲胎蛋白(alpha-fetoprotein,AFP)、微血管侵犯(microvascular invasion,MVI)、腫瘤分化程度、衛星結節、BCLC分期等;② 手術資料:手術方式、手術時間、術中失血量及肝血流阻斷時間。
1.3 早期復發的定義
本研究根據HCC是否在術后2年內復發來區分早期復發和晚期復發標準(雖然有對早期復發定義為在1年內甚至6個月內復發者[7])。
1.4 統計學方法
采用SPSS 25.0和Rstudio 4.3.1統計學軟件。正態分布的計量資料以均數±標準差( ±s)描述且2組間比較采用獨立樣本比較的t檢驗;非正態分布的計量資料根據中位數轉化為計數資料,以“例(%)”描述且采用χ2檢驗。采用單因素和多因素logistic回歸模型分析影響HCC患者行根治手術后復發的風險因素,將單因素分析結果中P<0.05的指標以及結合臨床有意義的指標納入進行多因素logistic 回歸分析,將多因素分析篩選出P<0.05的指標用于構建HCC行根治手術后早期復發的列線圖預測模型,并采用校準曲線Hosmer-Lemeshow擬合優度檢驗評估列線圖預測模型的準確性,預測模型對應曲線與校準圖中 45°對角線貼合度越好提示模型預測結果與實際情況一致性越好;并利用受試者操作特征(receiver operating characteristics,ROC)曲線評估列線圖預測模型的區分能力;通過決策曲線分析(decision curve analysis,DCA)評價其臨床實用性。檢驗水準α=0.05。
±s)描述且2組間比較采用獨立樣本比較的t檢驗;非正態分布的計量資料根據中位數轉化為計數資料,以“例(%)”描述且采用χ2檢驗。采用單因素和多因素logistic回歸模型分析影響HCC患者行根治手術后復發的風險因素,將單因素分析結果中P<0.05的指標以及結合臨床有意義的指標納入進行多因素logistic 回歸分析,將多因素分析篩選出P<0.05的指標用于構建HCC行根治手術后早期復發的列線圖預測模型,并采用校準曲線Hosmer-Lemeshow擬合優度檢驗評估列線圖預測模型的準確性,預測模型對應曲線與校準圖中 45°對角線貼合度越好提示模型預測結果與實際情況一致性越好;并利用受試者操作特征(receiver operating characteristics,ROC)曲線評估列線圖預測模型的區分能力;通過決策曲線分析(decision curve analysis,DCA)評價其臨床實用性。檢驗水準α=0.05。
2 結果
2.1 納入患者的基本情況
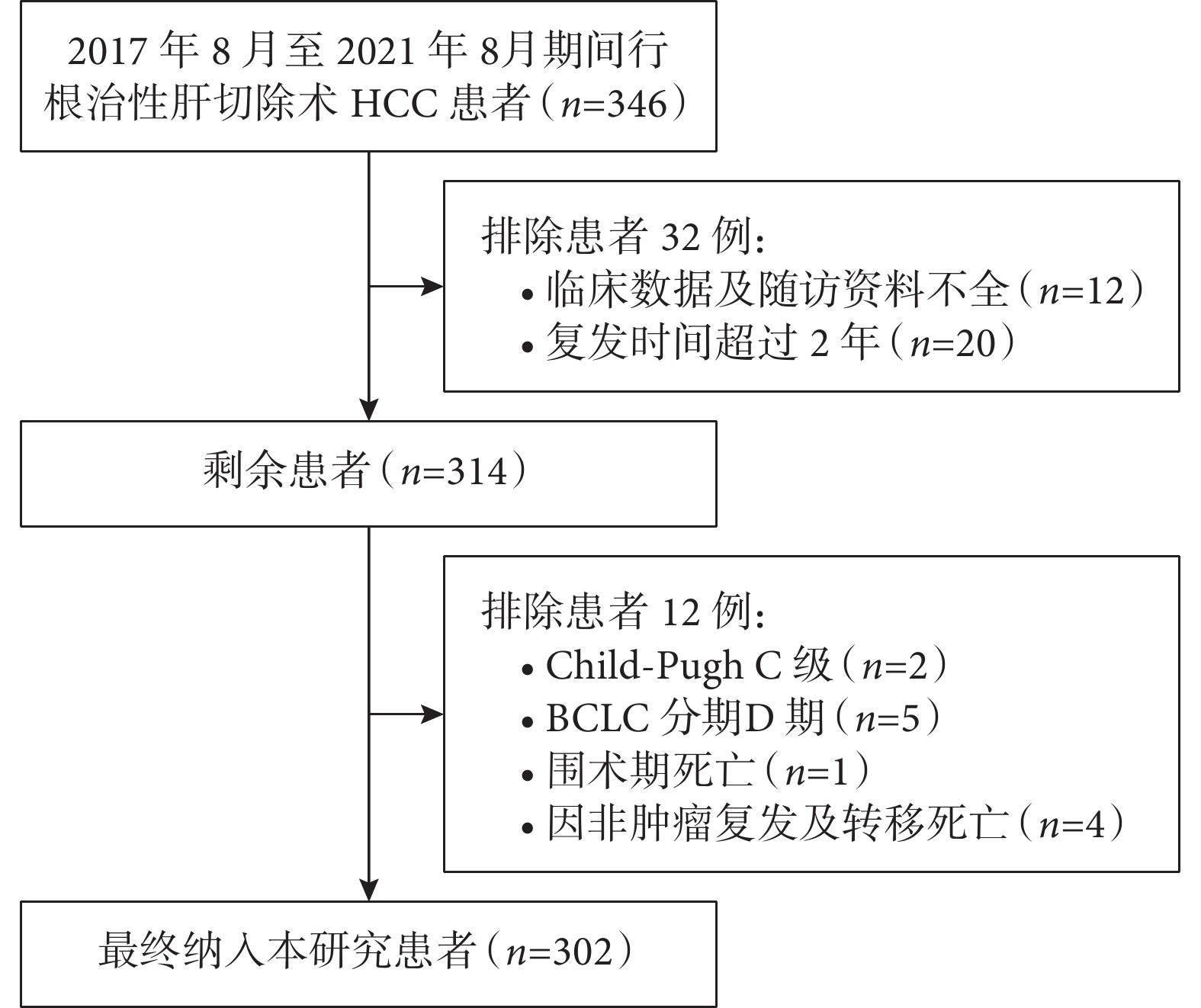
本研究納入患者的篩選流程及結果見圖1。最終納入302例HCC行根治性肝切除術患者,其中術后早期復發145例(48.01%)。
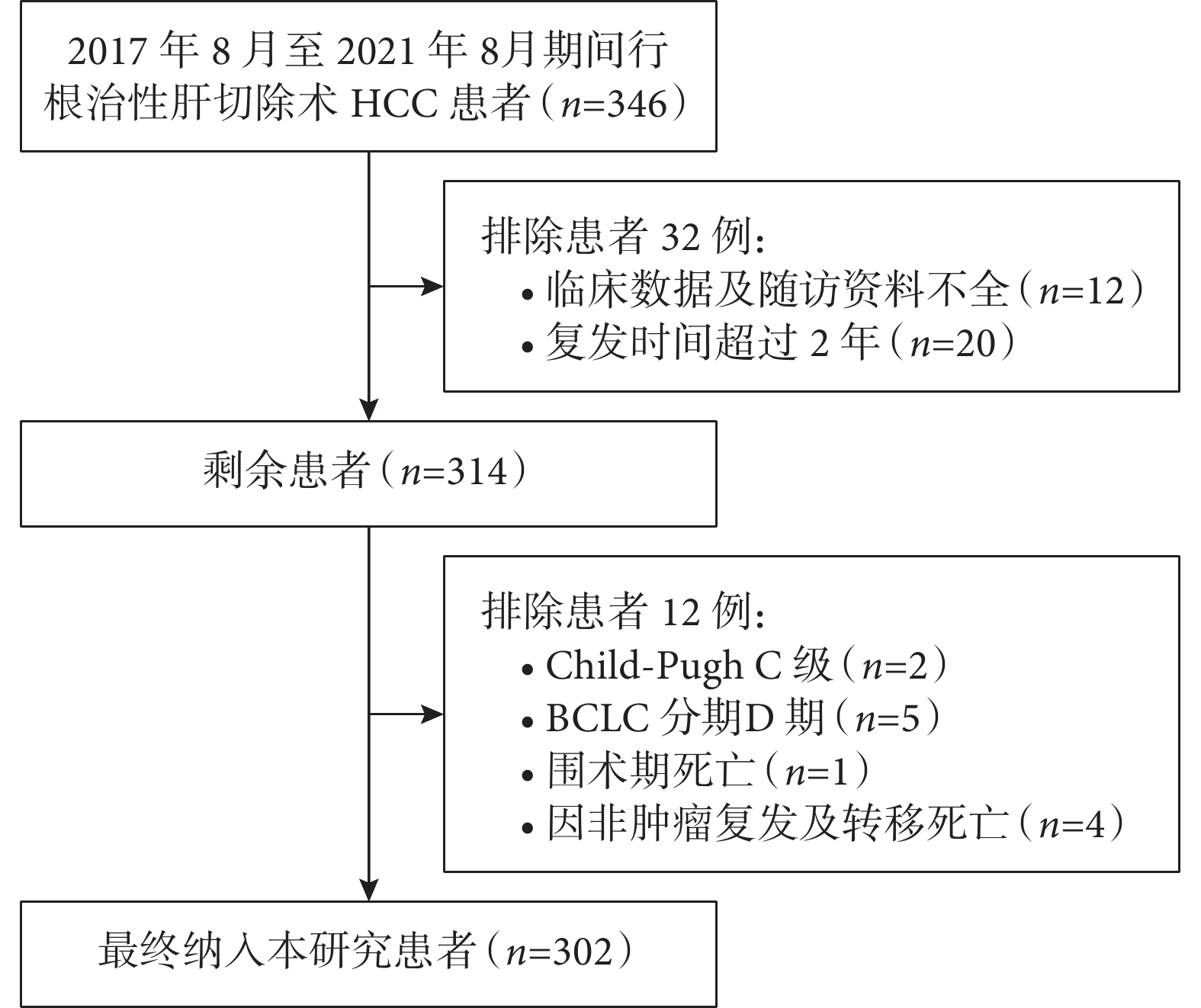 圖1
示本研究納入患者的篩選流程及結果
圖1
示本研究納入患者的篩選流程及結果
2.2 HCC行根治性肝切除術后早期復發的影響因素分析結果
影響HCC行根治性肝切除術后早期復發的單因素分析結果見表1。從表1可見,患者的BMI、Neut、PLT、NLR、PLR、ALT、AST、GGT、ALP、AFP、腫瘤大小、MVI、BCLC分期、手術方式及術中失血量與HCC行根治性肝切除術后早期復發有關(均P<0.05),而未發現其他因素與此有關(P>0.05)。以術后是否復發(是=1,否=0)為應變量,將單因素分析中P<0.05的因素及結合臨床有意義的變量作為自變量進行多因素logistic回歸分析,結果顯示,術前NLR、PLR、GGT、AFP、腫瘤大小、MVI是HCC患者根治性肝切除術后早期復發的影響因素(均P<0.05,表2)。
2.3 列結果線圖預測模型構建及驗證結果
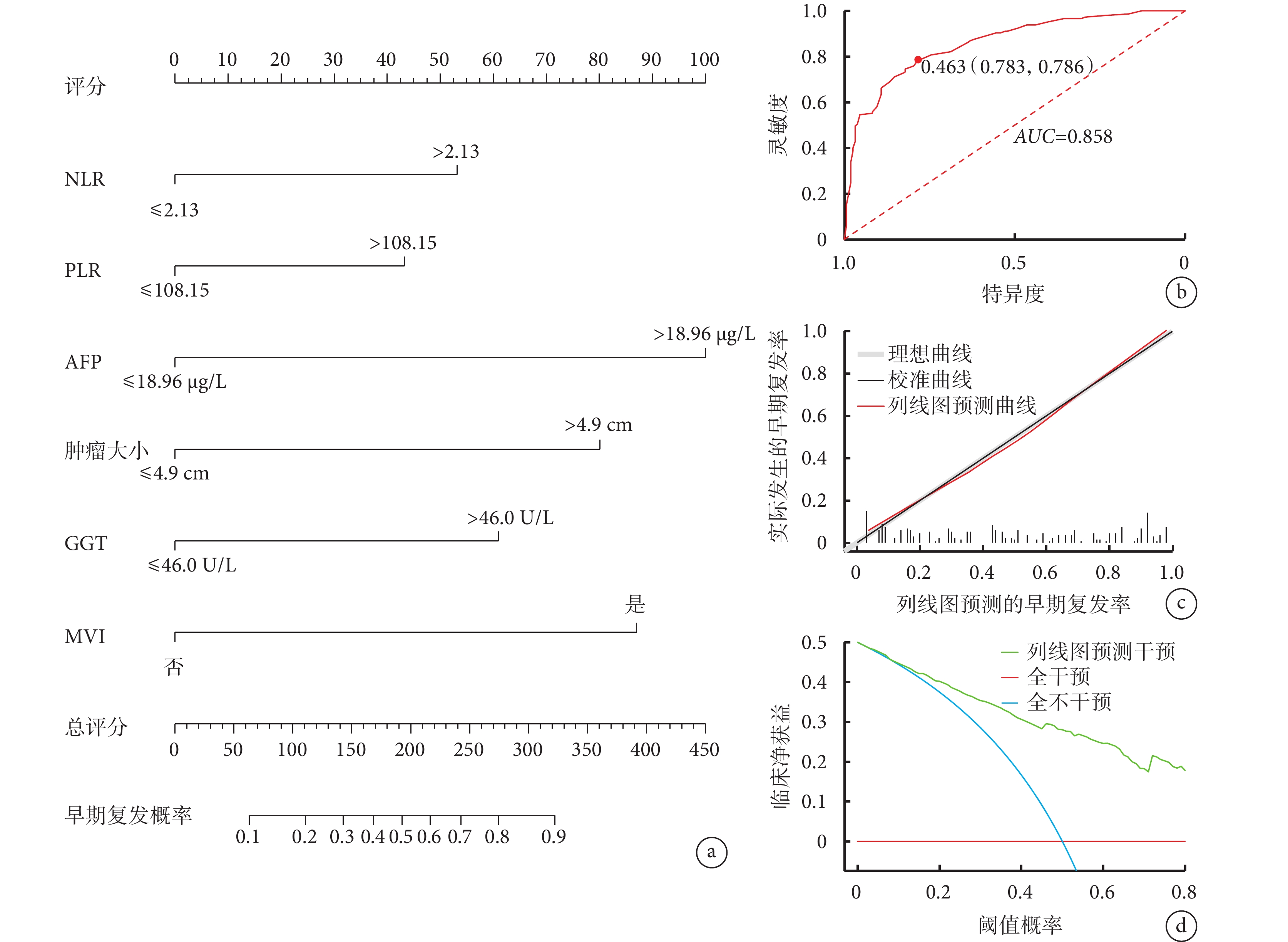
根據多因素logistic回歸分析篩選出的影響因素構建HCC患者行根治性肝切除術后早期復發的列線圖預測模型(圖2a),每例患者根據影響因素計算得到一個總分,總分越高者對應的HCC患者術后早期復發發生概率越高,可以根據得分實現對行根治性肝切除術后早期復發HCC患者的初步預測。列線圖預測模型區分術后早期復發的ROC曲線(圖2b)下面積為0.858 [95%CI(0.816,0.899)],其最佳截斷值為0.463,靈敏度和特異度分別為0.783和0.786,約登指數為0.569。校準曲線評價列線圖預測模型的Brier指數為0.152,列線圖預測模型的預測情況與實際發生情況之間較接近(Hosmer–Lemeshow檢驗,P=0.913),見圖2c。DCA(圖2d)結果顯示,閾值概率在0.1~0.8的范圍內,根據模型預測的概率進行干預的臨床凈收益高于對所有HCC患者不進行干預或對所有患者進行干預。
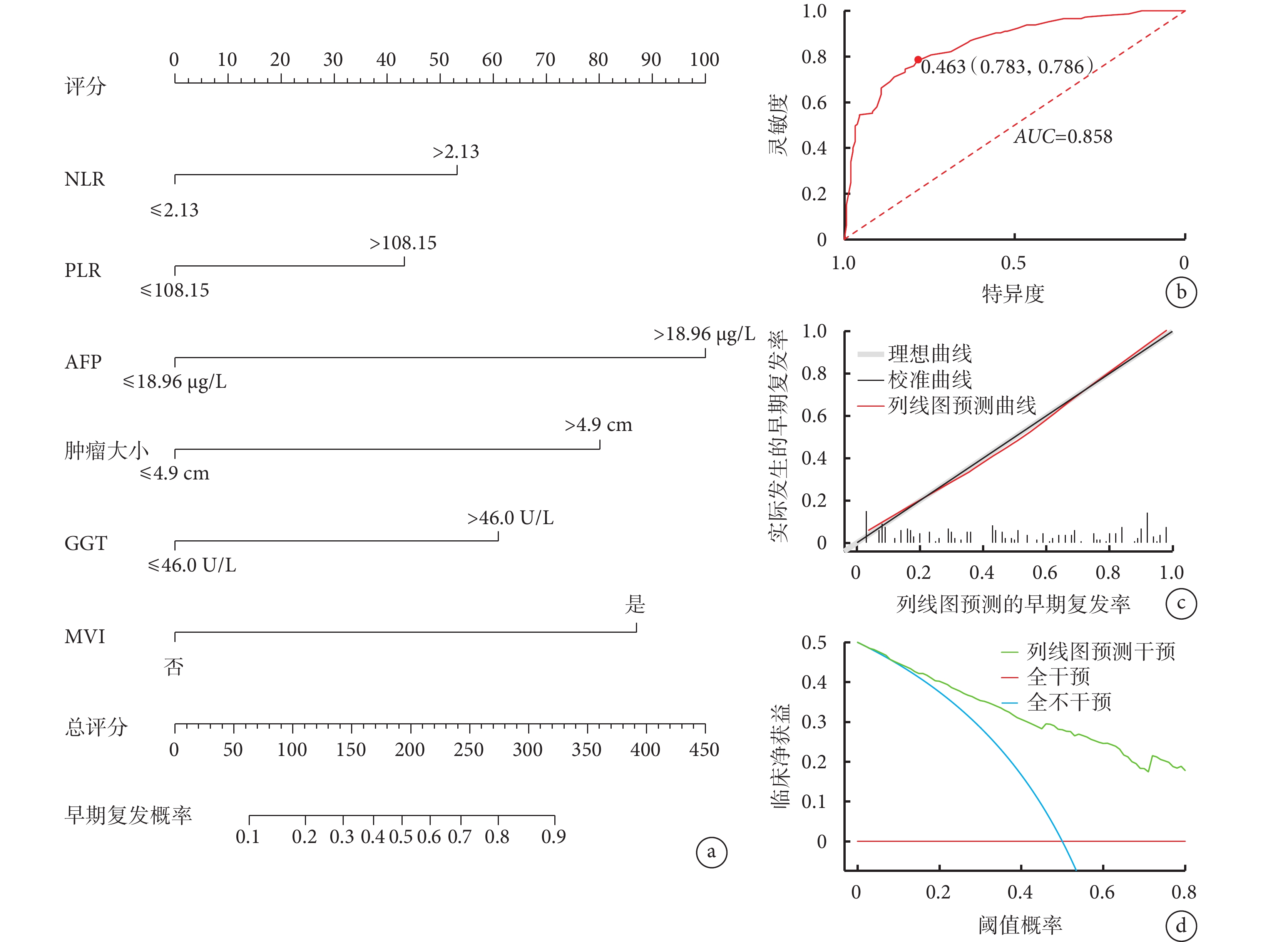 圖2
示構建的列線圖預測模型及驗證曲線
圖2
示構建的列線圖預測模型及驗證曲線
a:列線圖;b:ROC曲線;c:校準曲線;d:DCA曲線
3 討論
由于HCC行根治性肝切除術后仍易早期復發,本研究探討了HCC行根治性肝切除術后早期復發的危險因素并構建了列線圖預測模型,首先通過單因素和多因素logistic回歸分析篩選出了術前NLR、PLR、GGT、AFP、腫瘤大小及MVI是HCC行根治性切除術后早期復發的影響因素(P<0.05),對這些因素結合文獻進行分析。
有研究[8-18]表明,術前高NLR和PLR值可能與較多惡性腫瘤患者術后不良預后相關。在HCC的研究[9]中發現,較高的NLR和PLR值可能表示HCC患者的炎癥反應更嚴重,免疫功能受損,這與HCC的惡性程度、腫瘤的侵襲性以及預后密切相關。但目前研究中NLR和PLR值的最佳截斷值沒有統一,比如,NLR的最佳截斷值有研究中為2.4[13]和2.63[14],PLR的最佳截斷值有研究中為128.1[19]和100.25[20]等,在本研究中NLR和PLR值的最佳截斷值分別為2.13和108.15,這些現象對各研究結論的判讀可能有一定影響,因此這需要進一步規范。但這兩個指標是一種方便、易獲得、低成本且可靠的生物標志物,以此來對初步判斷行根治性切除后的HCC患者術后復發具有一定的參考價值。
有多項研究[21-23]證實,GGT水平升高與多種腫瘤(如腎細胞癌、尿路上皮癌和食管鱗狀細胞癌)的發生、發展和預后密切相關。在關于HCC患者術后早期復發的研究[24]中也發現,GGT>50 U/L的患者復發時間明顯更短、復發率更高(51.2%比26.4%);在本研究中也發現,GGT水平>46.0 U/L的HCC患者行根治性切除術后早期復發的風險較GGT水平≤46.0 U/L更高 [OR(95%CI)=2.36(1.25,4.47)]。分析其原因,HCC患者GGT的升高與膽汁淤積有關,膽汁淤積導致肝內膽汁酸積累,增加肝臟氧化應激的程度,進而促進GGT的產生;此外,HCC細胞本身也能產生GGT,會進一步提高血漿中的GGT水平。高水平的GGT可能提示腫瘤負擔重、惡性程度高以及較差的預后[25]。然而,目前尚需進一步研究來探索GGT在HCC發展和進展中的具體作用機制以及確定其最佳截斷值。
有文獻[26]報道,腫瘤大小>5 cm、術前AFP水平升高增加HCC肝切除術后早期復發的風險。有研究者[27]報道,在腫瘤直徑≥5 cm的患者中,腫瘤的局部增殖活性較高,這可能導致手術時程加長,進而削弱患者的免疫反應,并提升了手術后復發的可能性。另有研究者[28]報道,AFP的最佳臨界值為26 μg/L時預測丙型肝炎病毒感染HCC患者活體供體肝移植后復發有一定的價值;Magro等[29]也報道AFP的最佳臨界值為25.5 μg/L時預測HCC肝移植術后復發有一定價值。在本研究中,腫瘤大小和AFP的最佳臨界值分別是4.9 cm和18.96 μg/L時預測HCC患者行根治性切除術后早期復發有一定的價值,腫瘤大小的最佳臨界值與文獻報道比較接近,然而AFP的最佳臨界值相差較大,這些需要進一步分析。
關于MVI,它的存在意味著腫瘤細胞侵入血管[30],對HCC患者術后的總生存期有影響,而且是術后早期復發的危險因素[31-32],在本研究的發現基本與此結論一致。
以上6個風險因素在文獻報道中均對HCC患者根治性切除術后的早期復發有一定影響,本研究根據這6個因素建立了HCC行根治性切除術后早期復發的列線圖預測模型,它對區分術后早期復發有一定的臨床價值(ROC曲線下面積為0.858),而且校正曲線結果驗證了該列線圖預測模型預測的發生概率與實際發生的概率具有良好的一致性,DCA分析結果也提示它臨床獲益的閾值概率范圍較寬(10%~80%)。
盡管HCC行根治性切除術后早期復發與多種因素有關,但本研究根據篩選出的風險因素建立的列線圖預測模型仍具有良好的預測價值。只是需要注意的是,本研究只收集了患者住院期間的相關數據,未對遠期并發癥和病死亡率進行長期隨訪與追蹤;同時,由于本研究數據來源單一且樣本較小,可能會影響該模型的穩定性和準確性。因此,仍需收集更多的外部數據來優化預測模型,并通過DCA來評價該模型在臨床實用性方面的表現。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:叢赟負責課題設計、統計分析及撰寫論文,李國煜負責數據收集,王丹妮負責數據核對,邵英梅負責對文章指導、修改和審核,吐爾干艾力·阿吉負責技術指導,狄濤負責患者隨訪。
倫理聲明:本研究通過了新疆醫科大學第一附屬醫院倫理委員會審批(批文編號:K202312-43)。
肝細胞癌(hepatocellular carcinoma,HCC)占世界癌癥發病率的第6位和癌癥死亡率的第3位[1]且呈上升趨勢[2]。目前,根治性肝切除仍是HCC最常用且最有效的治療方法。然而HCC病程隱匿,多數患者就診時錯過了根治性手術治療時機。《原發性肝癌診療指南(2022年版)》[3]將外科手術切除治療HCC的適應證擴大至Ⅲa期,這樣可能會間接導致術后復發概率增加。因此,探究HCC術后預測早期復發的危險因素具有一定的臨床價值。既往相關研究通常使用logistic回歸模型來探討HCC術后早期復發的影響因素,相比之下,近年來興起的列線圖具有預測連續數值直觀、解釋更明確、計算簡單、表現穩定且具有較好的擬合效果等優勢,可將影響因素量化并以圖形方式直觀計算結局事件概率。本研究結合HCC手術治療患者的一般臨床資料、腫瘤信息和圍術期資料,探討了HCC術后早期復發的影響因素并構建了風險預測列線圖模型,以幫助預測術后復發風險。
1 資料與方法
1.1 患者納入和排除標準
回顧性收集2017年8月至2021年8月期間在新疆醫科大學第一附屬醫院收治的HCC患者的臨床病理資料。納入標準:① 符合《原發性肝癌診療規范(2019年版)》[4]診斷標準且術后標本經組織病理學檢查確診為HCC;② 行根治性肝切除且經組織病理學檢查證實切緣陰性(R0切除);③ 臨床病理資料及隨訪資料完整者;④ 術后2年內復發患者。排除標準:① 術后因出現嚴重心、肺、腦、腎等臟器并發癥或感染出血原因導致圍術期死亡患者;② 巴塞羅那臨床肝癌(Barcelona Clinic Liver Cancer,BCLC)分期D期患者;③ Child-Pugh分級C級患者;④ 伴有其他惡性腫瘤病史;⑤ 伴有自身免疫性疾病、血液系統疾病等;⑥ 非腫瘤復發及轉移原因死亡患者。本研究中全部患者均知情同意并獲得醫院倫理委員會批準通過。
1.2 資料收集
1.2.1 患者術前一般臨床資料
① 人口學數據:年齡、性別、體質量指數(body mass index,BMI);② 病因:乙型肝炎病毒(hepatitis B virus,HBV)病史、脂肪肝病史等。③ 實驗室參數:中性粒細胞(neutrophils,Neut)計數、血小板(platelet,PLT)計數、淋巴細胞(lymphocyte,Lym)計數、乳酸脫氫酶(lactate dehydrogenase,LDH)、血紅蛋白(hemoglobin,Hb)、國際標準化比率(international normalized ratio,INR),同時計算中性粒細胞與淋巴細胞比率(neutrophil to lymphocyte ratio,NLR)和血小板與淋巴細胞比率(platelet to lymphocyte ratio,PLR),其計算方法分別是:NLR=Neut絕對計數/Lym絕對計數×100%、PLR=PLT絕對計數/Lym絕對計數×100%。④ 肝功能相關指標:Child-Pugh分級和肝硬化病史、丙氨酸轉氨酶(aspartate aminotransferase,ALT)、天冬氨酸轉氨酶(alanine aminotransferase,AST)、總膽紅素(total bilirubin,TB)、白蛋白(albumin,Alb)、γ-谷氨酰轉移酶(γ-glutamyl transferase,GGT)、堿性磷酸酶(alkaline phosphatase,ALP),同時計算血小板-白蛋白-膽紅素指數(platelet-albumin-bilirubin index,PALBI)[5],其計算公式:PALBI=(2.02×log10TB)+[–0.37×(log10TB)2]+(–0.04×Alb)+(–3.48×log10PLT)+[1.01×(log10PLT)2],其結果分為1級(≤–2.53)、2級(–2.53,–2.09)和3級(>–2.09)[6] 3個等級。
1.2.2 腫瘤信息和圍術期相關臨床資料
① 腫瘤信息:數量、大小(指直徑)、甲胎蛋白(alpha-fetoprotein,AFP)、微血管侵犯(microvascular invasion,MVI)、腫瘤分化程度、衛星結節、BCLC分期等;② 手術資料:手術方式、手術時間、術中失血量及肝血流阻斷時間。
1.3 早期復發的定義
本研究根據HCC是否在術后2年內復發來區分早期復發和晚期復發標準(雖然有對早期復發定義為在1年內甚至6個月內復發者[7])。
1.4 統計學方法
采用SPSS 25.0和Rstudio 4.3.1統計學軟件。正態分布的計量資料以均數±標準差( ±s)描述且2組間比較采用獨立樣本比較的t檢驗;非正態分布的計量資料根據中位數轉化為計數資料,以“例(%)”描述且采用χ2檢驗。采用單因素和多因素logistic回歸模型分析影響HCC患者行根治手術后復發的風險因素,將單因素分析結果中P<0.05的指標以及結合臨床有意義的指標納入進行多因素logistic 回歸分析,將多因素分析篩選出P<0.05的指標用于構建HCC行根治手術后早期復發的列線圖預測模型,并采用校準曲線Hosmer-Lemeshow擬合優度檢驗評估列線圖預測模型的準確性,預測模型對應曲線與校準圖中 45°對角線貼合度越好提示模型預測結果與實際情況一致性越好;并利用受試者操作特征(receiver operating characteristics,ROC)曲線評估列線圖預測模型的區分能力;通過決策曲線分析(decision curve analysis,DCA)評價其臨床實用性。檢驗水準α=0.05。
±s)描述且2組間比較采用獨立樣本比較的t檢驗;非正態分布的計量資料根據中位數轉化為計數資料,以“例(%)”描述且采用χ2檢驗。采用單因素和多因素logistic回歸模型分析影響HCC患者行根治手術后復發的風險因素,將單因素分析結果中P<0.05的指標以及結合臨床有意義的指標納入進行多因素logistic 回歸分析,將多因素分析篩選出P<0.05的指標用于構建HCC行根治手術后早期復發的列線圖預測模型,并采用校準曲線Hosmer-Lemeshow擬合優度檢驗評估列線圖預測模型的準確性,預測模型對應曲線與校準圖中 45°對角線貼合度越好提示模型預測結果與實際情況一致性越好;并利用受試者操作特征(receiver operating characteristics,ROC)曲線評估列線圖預測模型的區分能力;通過決策曲線分析(decision curve analysis,DCA)評價其臨床實用性。檢驗水準α=0.05。
2 結果
2.1 納入患者的基本情況
本研究納入患者的篩選流程及結果見圖1。最終納入302例HCC行根治性肝切除術患者,其中術后早期復發145例(48.01%)。
 圖1
示本研究納入患者的篩選流程及結果
圖1
示本研究納入患者的篩選流程及結果
2.2 HCC行根治性肝切除術后早期復發的影響因素分析結果
影響HCC行根治性肝切除術后早期復發的單因素分析結果見表1。從表1可見,患者的BMI、Neut、PLT、NLR、PLR、ALT、AST、GGT、ALP、AFP、腫瘤大小、MVI、BCLC分期、手術方式及術中失血量與HCC行根治性肝切除術后早期復發有關(均P<0.05),而未發現其他因素與此有關(P>0.05)。以術后是否復發(是=1,否=0)為應變量,將單因素分析中P<0.05的因素及結合臨床有意義的變量作為自變量進行多因素logistic回歸分析,結果顯示,術前NLR、PLR、GGT、AFP、腫瘤大小、MVI是HCC患者根治性肝切除術后早期復發的影響因素(均P<0.05,表2)。
2.3 列結果線圖預測模型構建及驗證結果
根據多因素logistic回歸分析篩選出的影響因素構建HCC患者行根治性肝切除術后早期復發的列線圖預測模型(圖2a),每例患者根據影響因素計算得到一個總分,總分越高者對應的HCC患者術后早期復發發生概率越高,可以根據得分實現對行根治性肝切除術后早期復發HCC患者的初步預測。列線圖預測模型區分術后早期復發的ROC曲線(圖2b)下面積為0.858 [95%CI(0.816,0.899)],其最佳截斷值為0.463,靈敏度和特異度分別為0.783和0.786,約登指數為0.569。校準曲線評價列線圖預測模型的Brier指數為0.152,列線圖預測模型的預測情況與實際發生情況之間較接近(Hosmer–Lemeshow檢驗,P=0.913),見圖2c。DCA(圖2d)結果顯示,閾值概率在0.1~0.8的范圍內,根據模型預測的概率進行干預的臨床凈收益高于對所有HCC患者不進行干預或對所有患者進行干預。
 圖2
示構建的列線圖預測模型及驗證曲線
圖2
示構建的列線圖預測模型及驗證曲線
a:列線圖;b:ROC曲線;c:校準曲線;d:DCA曲線
3 討論
由于HCC行根治性肝切除術后仍易早期復發,本研究探討了HCC行根治性肝切除術后早期復發的危險因素并構建了列線圖預測模型,首先通過單因素和多因素logistic回歸分析篩選出了術前NLR、PLR、GGT、AFP、腫瘤大小及MVI是HCC行根治性切除術后早期復發的影響因素(P<0.05),對這些因素結合文獻進行分析。
有研究[8-18]表明,術前高NLR和PLR值可能與較多惡性腫瘤患者術后不良預后相關。在HCC的研究[9]中發現,較高的NLR和PLR值可能表示HCC患者的炎癥反應更嚴重,免疫功能受損,這與HCC的惡性程度、腫瘤的侵襲性以及預后密切相關。但目前研究中NLR和PLR值的最佳截斷值沒有統一,比如,NLR的最佳截斷值有研究中為2.4[13]和2.63[14],PLR的最佳截斷值有研究中為128.1[19]和100.25[20]等,在本研究中NLR和PLR值的最佳截斷值分別為2.13和108.15,這些現象對各研究結論的判讀可能有一定影響,因此這需要進一步規范。但這兩個指標是一種方便、易獲得、低成本且可靠的生物標志物,以此來對初步判斷行根治性切除后的HCC患者術后復發具有一定的參考價值。
有多項研究[21-23]證實,GGT水平升高與多種腫瘤(如腎細胞癌、尿路上皮癌和食管鱗狀細胞癌)的發生、發展和預后密切相關。在關于HCC患者術后早期復發的研究[24]中也發現,GGT>50 U/L的患者復發時間明顯更短、復發率更高(51.2%比26.4%);在本研究中也發現,GGT水平>46.0 U/L的HCC患者行根治性切除術后早期復發的風險較GGT水平≤46.0 U/L更高 [OR(95%CI)=2.36(1.25,4.47)]。分析其原因,HCC患者GGT的升高與膽汁淤積有關,膽汁淤積導致肝內膽汁酸積累,增加肝臟氧化應激的程度,進而促進GGT的產生;此外,HCC細胞本身也能產生GGT,會進一步提高血漿中的GGT水平。高水平的GGT可能提示腫瘤負擔重、惡性程度高以及較差的預后[25]。然而,目前尚需進一步研究來探索GGT在HCC發展和進展中的具體作用機制以及確定其最佳截斷值。
有文獻[26]報道,腫瘤大小>5 cm、術前AFP水平升高增加HCC肝切除術后早期復發的風險。有研究者[27]報道,在腫瘤直徑≥5 cm的患者中,腫瘤的局部增殖活性較高,這可能導致手術時程加長,進而削弱患者的免疫反應,并提升了手術后復發的可能性。另有研究者[28]報道,AFP的最佳臨界值為26 μg/L時預測丙型肝炎病毒感染HCC患者活體供體肝移植后復發有一定的價值;Magro等[29]也報道AFP的最佳臨界值為25.5 μg/L時預測HCC肝移植術后復發有一定價值。在本研究中,腫瘤大小和AFP的最佳臨界值分別是4.9 cm和18.96 μg/L時預測HCC患者行根治性切除術后早期復發有一定的價值,腫瘤大小的最佳臨界值與文獻報道比較接近,然而AFP的最佳臨界值相差較大,這些需要進一步分析。
關于MVI,它的存在意味著腫瘤細胞侵入血管[30],對HCC患者術后的總生存期有影響,而且是術后早期復發的危險因素[31-32],在本研究的發現基本與此結論一致。
以上6個風險因素在文獻報道中均對HCC患者根治性切除術后的早期復發有一定影響,本研究根據這6個因素建立了HCC行根治性切除術后早期復發的列線圖預測模型,它對區分術后早期復發有一定的臨床價值(ROC曲線下面積為0.858),而且校正曲線結果驗證了該列線圖預測模型預測的發生概率與實際發生的概率具有良好的一致性,DCA分析結果也提示它臨床獲益的閾值概率范圍較寬(10%~80%)。
盡管HCC行根治性切除術后早期復發與多種因素有關,但本研究根據篩選出的風險因素建立的列線圖預測模型仍具有良好的預測價值。只是需要注意的是,本研究只收集了患者住院期間的相關數據,未對遠期并發癥和病死亡率進行長期隨訪與追蹤;同時,由于本研究數據來源單一且樣本較小,可能會影響該模型的穩定性和準確性。因此,仍需收集更多的外部數據來優化預測模型,并通過DCA來評價該模型在臨床實用性方面的表現。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:叢赟負責課題設計、統計分析及撰寫論文,李國煜負責數據收集,王丹妮負責數據核對,邵英梅負責對文章指導、修改和審核,吐爾干艾力·阿吉負責技術指導,狄濤負責患者隨訪。
倫理聲明:本研究通過了新疆醫科大學第一附屬醫院倫理委員會審批(批文編號:K202312-43)。