引用本文: 王雯, 郭越, 李潔瑩, 王斐然. 度普利尤單抗治療中重度哮喘的療效及安全性分析:一項真實世界研究. 中國呼吸與危重監護雜志, 2023, 22(10): 685-691. doi: 10.7507/1671-6205.202305069 復制
版權信息: ?四川大學華西醫院華西期刊社《中國呼吸與危重監護雜志》版權所有,未經授權不得轉載、改編
支氣管哮喘(簡稱哮喘)是一種常見的呼吸系統疾病,以氣道慢性炎癥為特征,臨床表現為反復發作的喘息、氣急,伴或不伴咳嗽或胸悶等癥狀,同時伴有氣道高反應性和可逆性氣流受限,隨著病程的遷延和炎癥的進展可導致氣道重塑[1]。我國20歲及以上人群哮喘患病率為4.2%,患者人數推算約為4570萬[2]。哮喘具有不同臨床類型,同時有生物學表型異質性。根據2型炎癥(type 2 inflammation,T2)水平的高低,分為低T2和高T2哮喘兩種類型[3]。高T2哮喘中常見兒童期早發過敏性哮喘以及成人期晚發重度嗜酸性粒細胞性哮喘,以嗜酸性氣道炎癥為特征,表現為嗜酸性粒細胞計數增多和(或)呼出氣一氧化氮(fractional exhaled nitric oxide,FeNO)升高[4-5]。臨床上根據達到哮喘控制所采用的治療級別對哮喘嚴重程度進行分級[1],常聯用中高劑量的吸入性糖皮質激素(inhaled corticosteroids,ICS)和長效β2受體激動劑(long acting beta-agonist,LABA)對中重度哮喘進行治療[1]。
T2疾病 哮喘的關鍵細胞因子包括白細胞介素(interleukin,IL)-5、IL-4和IL-13等,針對關鍵細胞因子的生物靶向治療是哮喘新藥開發的熱點之一。度普利尤單抗(dupilumab)是一種全人源IL-4受體α亞基(IL-4Rα)的單克隆抗體,通過與IL-4和IL-13共享的IL-4Rα結合抑制其信號傳導[6],從而阻斷IgE類別轉換、嗜酸性粒細胞趨化性和氣道高反應性相關的重疊效應以及抑制JAK/TYK信號通路的激活[6-7],最終抑制T2疾病 介導的炎癥反應。臨床研究表明,度普利尤單抗可顯著減少哮喘的急性加重、改善哮喘控制情況,并增加支氣管舒張劑前后的第1秒用力呼氣容積(forced expiratory volume in 1 second,FEV1)[8-10]。此外,度普利尤單抗治療特應性皮炎和慢性鼻竇炎伴鼻息肉等哮喘共存疾病也具有顯著療效[11-12]。歐美和日本等國和地區已批準度普利尤單抗用于治療不同年齡人群中的特定哮喘、中重度特應性皮炎或特定慢性鼻竇炎伴鼻息肉。本研究首次對不耐受ICS+LABA長期治療或療效不佳的中重度哮喘患者經過臨床評估后換用度普利尤單抗進行治療,觀察并評價其療效及安全性,旨在為我國中重度哮喘的臨床應用提供參考。
1 資料與方法
1.1 臨床資料
經首都醫科大學附屬北京朝陽醫院及醫院倫理審查委員會批準,對接受1年及以上中高劑量ICS+LABA的規范治療后哮喘仍未控制、急診就診的嗜酸性粒細胞增高的中重度哮喘患者使用度普尤利單抗進行本實驗性臨床醫療研究。本研究為回顧性研究,收集2021年5月—2022年4月在本院呼吸科門診就診的中重度哮喘患者。納入標準:① 符合2021版全球哮喘防治創議中重度哮喘的診斷標準[13];② 氣道炎癥類型表現為嗜酸型,外周血嗜酸性粒細胞計數≥500個/μL或FeNO≥30 ppb;③ 接受1年及以上中高劑量ICS+LABA的規范治療;④ 患者本人或其監護人完全理解并同意本實驗性臨床醫療研究的目的和實施,能配合醫師完成問卷調查。排除標準:① 正在接受其他單克隆抗體治療者;② 對度普利尤單抗活性成分或任何輔料過敏者;③ 妊娠或哺乳期患者;④ 接受免疫抑制劑或長期類固醇激素治療的惡性腫瘤、慢性自身免疫性疾病患者;⑤ 心肝腦腎等重要臟器嚴重受損者;⑥ 嚴重精神疾病患者。參與本研究的患者均簽署知情同意書。
1.2 方法
1.2.1 治療方法
納入研究組(度普尤利單抗治療組)的患者均接受度普利尤單抗治療,首次600 mg皮下注射,之后每2周300 mg皮下注射,單個療程為16周。納入對照組(ICS+LABA治療組)的患者,布地奈德福莫特羅160/4.5 μg 2~3吸2次/d或沙美特羅替卡松250~500 μg 1吸2次/d,和(或)聯合孟魯司特及口服糖皮質激素(oral corticosteroids,OCS)。所有患者每2周~4周隨訪1次,根據患者癥狀及檢查指標對OCS劑量使用進行調整。
1.2.2 數據采集
收集信息包括性別、年齡、身高、體重、體重指數、吸煙狀況、 哮喘病程、癥狀及嚴重程度、急性加重次數、基線治療(包括生物制劑)、T2疾病共存疾病及其他并發癥。收集基線、治療第1、3、6、12個月外周血嗜酸性粒細胞計數、嗜堿性粒細胞計數、血清總IgE、FeNO、哮喘控制測試(Asthma Control Test,ACT)評分、用力肺活量(forced vital capacity,FVC)、FEV1、FEV1/FVC、FEV1占預計值百分比(FEV1%pred)、呼氣峰值流量(peak expiratory flow,PEF)、肺活量75%、50%、25%時的最大呼氣流量(MEF75、MEF50和MEF25)和最大用力呼氣中段流量(MMEF或FEF25%-75%),以及每日維持劑量的潑尼松。ACT評分:<19分表示哮喘未控制,20~25分表示控制良好,分數越高表示哮喘控制越好。
1.3 統計學方法
采用SPSS 26.0軟件,分類變量使用例(n)和百分數(%)表示;連續變量呈正態及近似正態分布時使用均數±標準差( ±s)表示,采用配對t檢驗(組內)或獨立樣本t檢驗(組間)進行比較;連續變量呈非正態分布時使用中位數和四分位間距1、3 [M(Q1,Q3)]表示,采用曼–惠特尼U檢驗進行比較。P<0.05為差異有統計學意義。
±s)表示,采用配對t檢驗(組內)或獨立樣本t檢驗(組間)進行比較;連續變量呈非正態分布時使用中位數和四分位間距1、3 [M(Q1,Q3)]表示,采用曼–惠特尼U檢驗進行比較。P<0.05為差異有統計學意義。
2 結果
2.1 人口學特征及基線特征
納入研究組的中重度哮喘患者共17例,男8例,女9例,平均年齡(51.94±14.30)歲。其中,15例接受高劑量ICS+LABA治療,2例為中劑量但患有其他未控制的T2疾病 。7例需加用OCS,平均日劑量為(9.71±14.52)mg。4例既往接受抗IgE奧馬珠單抗(Omalizumab)治療,由于哮喘控制不佳,血嗜酸性粒細胞反復增高,經臨床評估后換用度普利尤單抗。13例存在哮喘共存疾病。7例慢性鼻竇炎伴鼻息肉患者中,3例曾行鼻內鏡息肉切除術。
納入對照組的中重度哮喘患者共30例,男14例,女16例,平均年齡(52.57±16.42)歲。其中,26例接受高劑量ICS+LABA治療,4例為中劑量但患有其他未控制的T2疾病 。14例需加用OCS,平均日劑量為(8.67±15.46)mg。22例存在哮喘共存疾病。13例慢性鼻竇炎伴鼻息肉患者中,8例曾行鼻內鏡息肉切除術。
研究組和對照組的患者基本情況見表1。兩組間患者情況基本均衡。
2.2 治療前后ACT及各項指標的變化
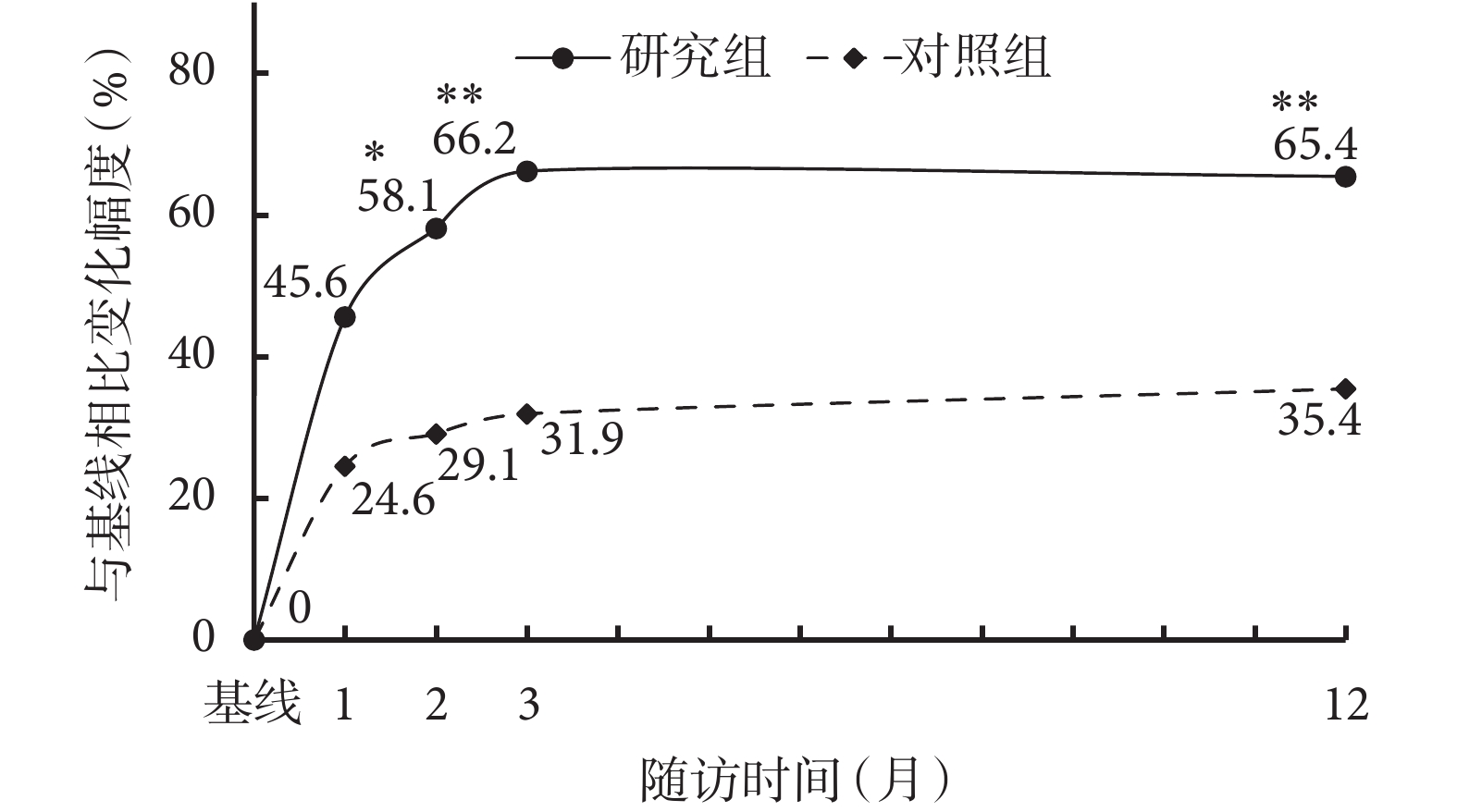
患者接受治療前后ACT評分及各項指標見表2。治療后第1、2、3和12個月時研究組和對照組患者的ACT均較基線顯著增加(P<0.001);治療后第2、3和12個月時,研究組患者ACT較對照組顯著增加(第2個月:P=0.002; 第3和12個月:P<0.001)。治療12個月后,研究組ACT相較基線增加65.4%,顯著高于對照組相較基線的增幅35.4%(P<0.001)(圖1)。
 )/M (Q1,Q3)]
)/M (Q1,Q3)]
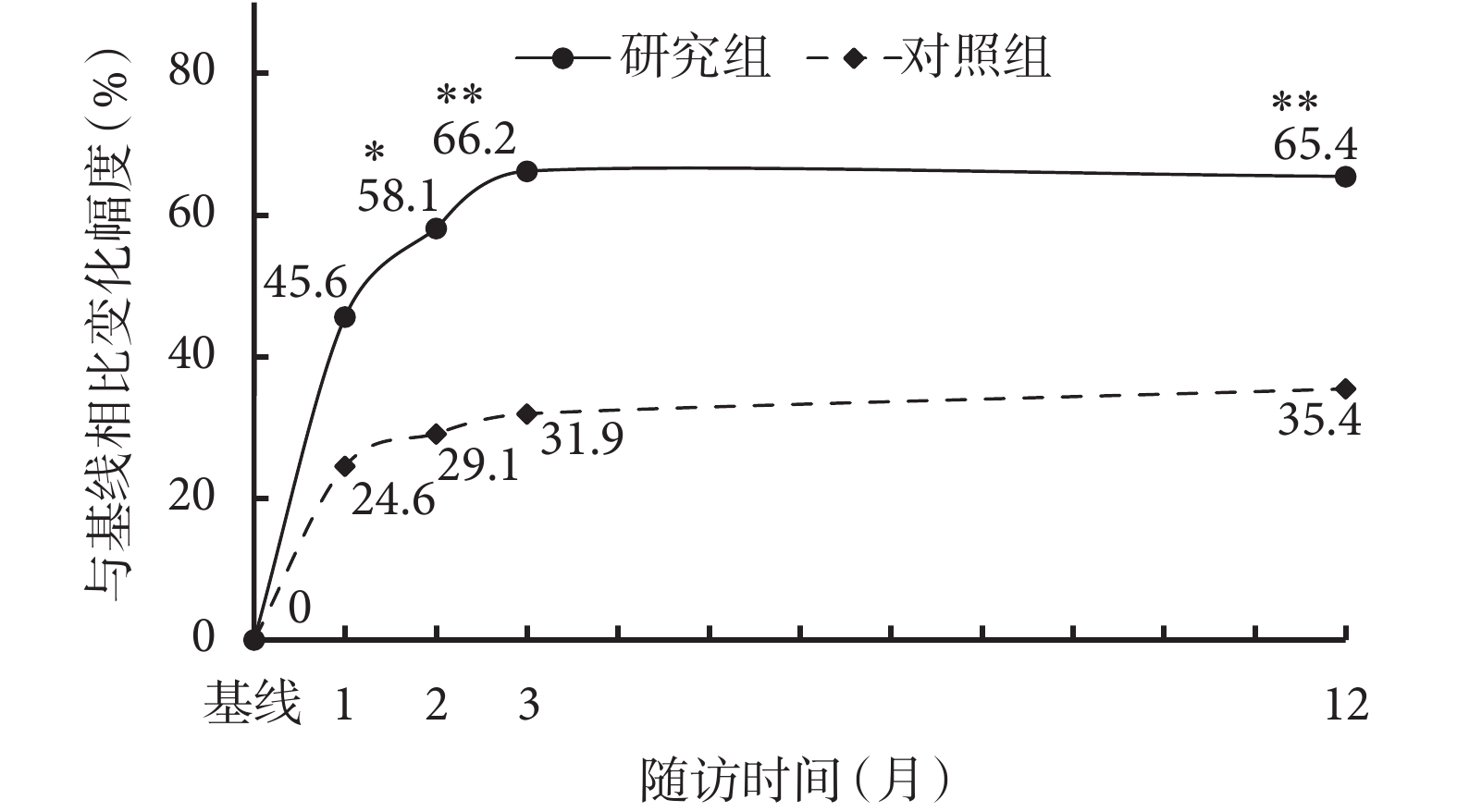 圖1
治療后相較基線ACT隨時間的變化趨勢圖
圖1
治療后相較基線ACT隨時間的變化趨勢圖
*
治療后第12個月,研究組和對照組的年急性加重次數差異無統計學意義(P=0.204),但相對基線均顯著下降(P=0.007)。
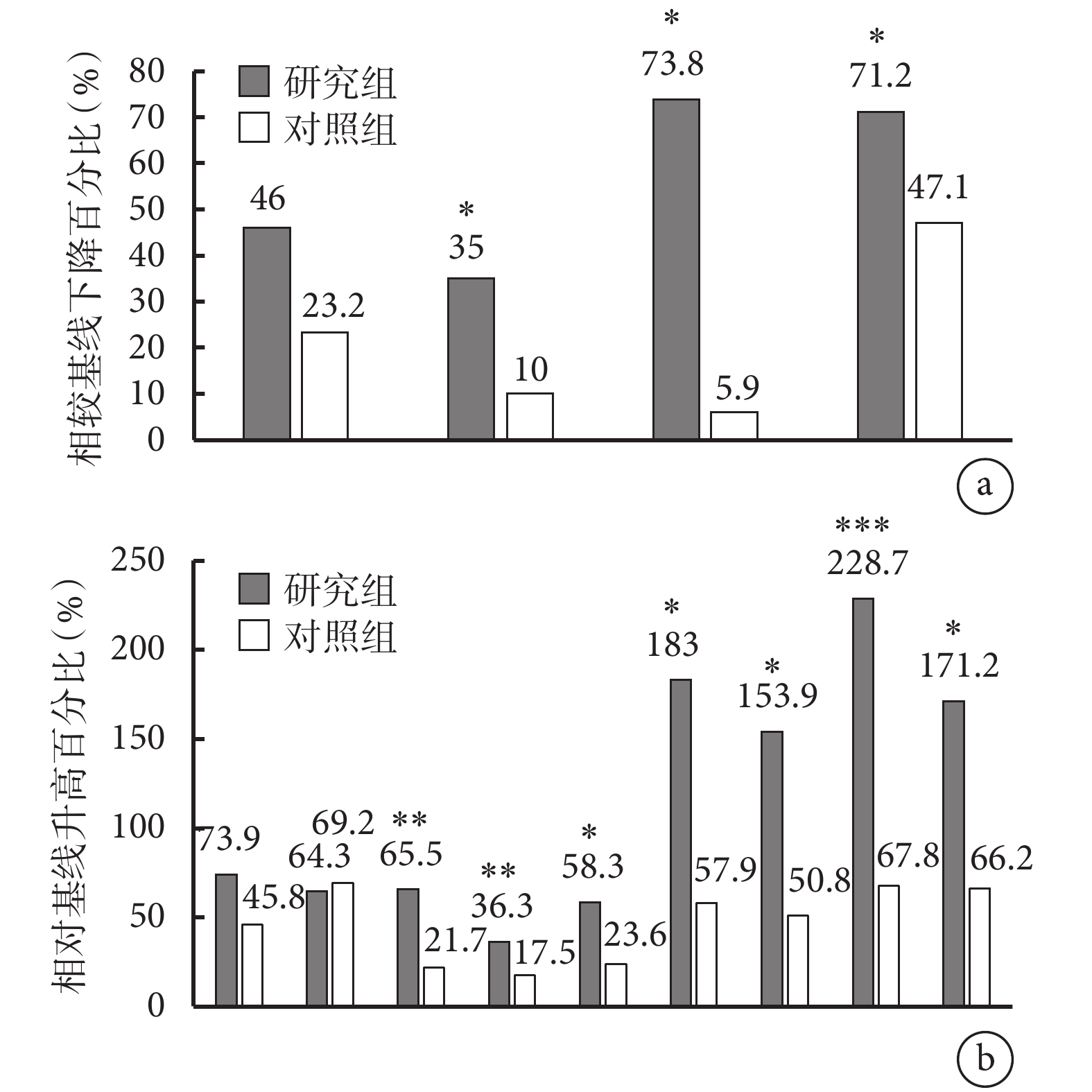
兩組血清總IgE、外周血嗜酸性粒細胞計數、外周血嗜堿性粒細胞計數及FeNO水平治療后相較基線均呈下降趨勢;治療后第12個月,研究組的血清總IgE 、外周血嗜酸性粒細胞計數、外周血嗜堿性粒細胞計數及FeNO 均較基線顯著下降(P值分別為0.048、0.015、0.0012和0.006),而對照組僅FeNO 相較基線顯著下降(P=0.037);治療后第12個月,研究組相較對照組外周血嗜堿性粒細胞計數、總IgE及FeNO的降幅顯著增大(圖2a)。
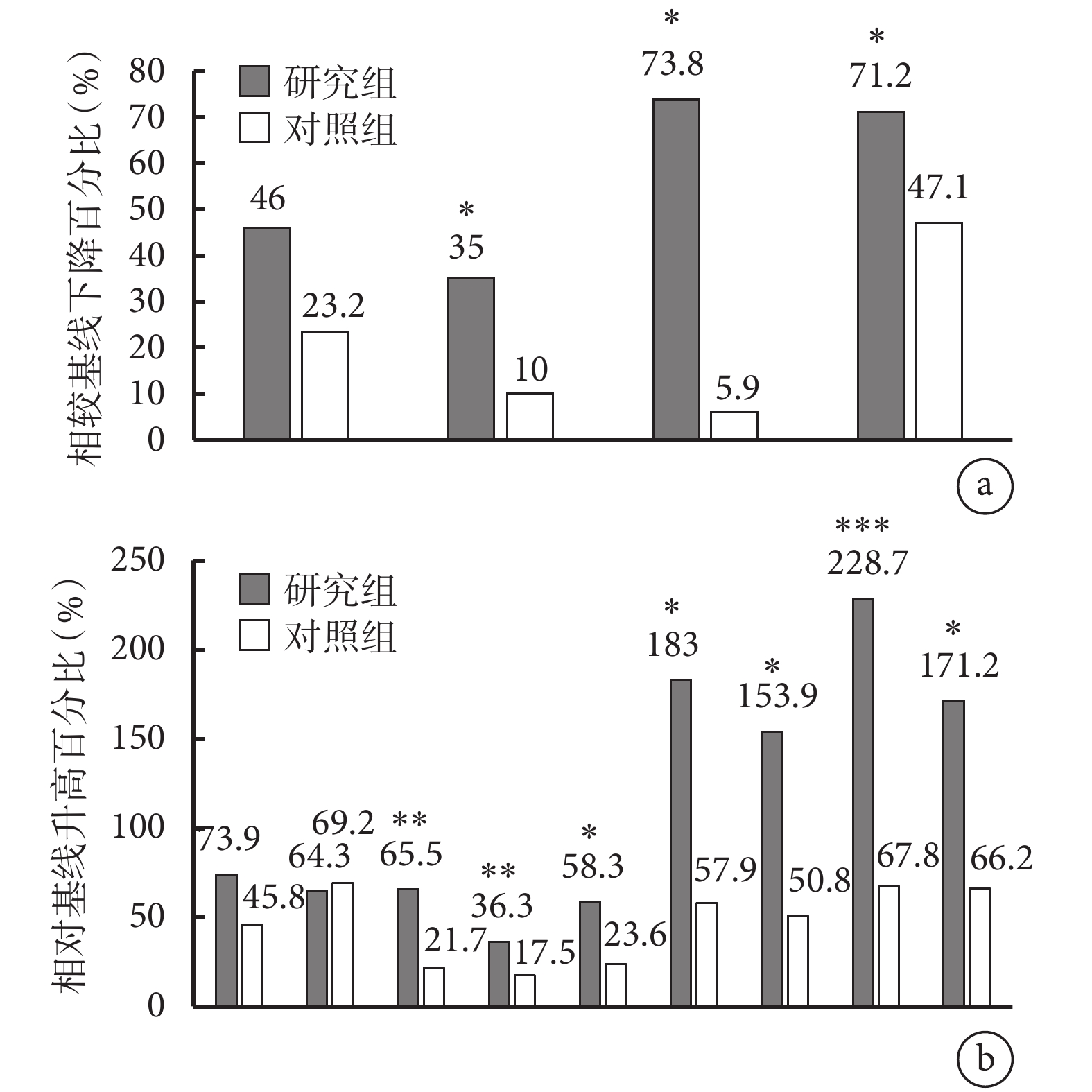 圖2
治療12個月后兩組血清游離總IgE、外周血嗜酸性粒細胞計數、外周血嗜堿性粒細胞計數以及肺功能各項指標的比較
圖2
治療12個月后兩組血清游離總IgE、外周血嗜酸性粒細胞計數、外周血嗜堿性粒細胞計數以及肺功能各項指標的比較
a. 兩組血清游離總IgE、外周血嗜酸性粒細胞計數、外周血嗜堿性粒細胞計數及FeNO較基線降低百分比(*
肺功能各項指標(包括FVC、FEV1、FEV1%pred、FEV1/FVC、PEF、MEF25、MEF50、MEF75及MMEF)均在度普利尤單抗治療12個月后相較基線顯著升高(P<0.05),對照組除FEV1%pred與基線差異無統計學顯著性外,其余肺功能指標(包括FVC、FEV1、FEV1/FVC、PEF、MEF25、MEF50、MEF75及MMEF)相較基線也均顯著升高。度普尤利單抗治療12個月后對FEV1%pred、FEV1/FVC、PEF、MEF25、MEF50、MEF75及MMEF的改善顯著優于對照組(P<0.05)(圖2b)。
研究組中,7例基線時加用OCS的患者經度普利尤單抗治療后,OCS劑量均逐步減少至停用;4例既往使用奧馬珠單抗、后換用度普利尤單抗的患者,臨床癥狀較前緩解,急性加重次數減少;所有患者初次注射度普利尤單抗后1周內癥狀得到明顯緩解,最短癥狀緩解時間為4 h;合并慢性鼻竇炎伴鼻息肉及特應性皮炎的患者,相關癥狀較前改善;合并支氣管擴張、ABPA、塵肺的患者未見哮喘癥狀加重引起原發結構性疾病進行性加重的情況。
對照組中,83.3%(25/30)的患者在長期規范治療后癥狀減輕。14例吸入高劑量ICS/LABA的患者經過長期規范化治療后OCS減少50%及以上,其中6例患者OCS實現減停。16例患者仍需高劑量ICS/LABA維持癥狀的穩定。在慢性鼻竇炎伴鼻息肉的患者中,標準治療并未明顯減輕患者鼻部癥狀,2例患者在12個月隨訪期間行鼻息肉切除手術。
2.3 不良反應
治療期間,研究組患者出現注射部位腫痛4例、皮膚瘙癢2例、紅斑1例、乏力1例,均為輕度且自行緩解。1例患者首次注射600 mg半個月后出現帶狀皰疹,經靜脈激素及抗病毒治療后痊愈,未影響繼續度普利尤單抗治療。對照組不良反應主要為長期高劑量吸入糖皮質激素所致聲音嘶啞(1例)、口腔真菌感染(4例)、血糖(2例)和血壓(3例)控制欠佳以及重度骨質疏松(1例)。
3 討論
本研究回顧性分析并比較了度普利尤單抗和ICS+LABA常規治療中重度哮喘過程中ACT評分和各項血液學及肺功能指標的變化,是首篇評估度普利尤單抗治療中重度哮喘中國患者療效和安全性的真實世界研究。結果顯示,度普利尤單抗治療12個月后,年急性加重次數較基線下降62.5%,略高于Numata等[14]在日本真實世界研究中報道的53%。本研究7例患者基線加用的OCS劑量經度普利尤單抗治療后均逐步較少至停用,與日本患者OCS維持劑量減少54%的觀察相似[14]。此外,日本患者治療后6個月后的ACT、FeNO及總IgE較基線均顯著降低[14],與本研究結果相同。此外,本研究觀察到中國患者肺功能各項指標在治療12個月后較基線均顯著改善,而日本患者治療6個月后相較基線無顯著性差異,可能與本研究納入患者的基線肺功能本身較差或(和)日本研究隨訪時間較短有關。
本研究度普利尤單抗治療期間出現1例帶狀皰疹,經治療后痊愈。目前尚無研究表明度普利尤單抗會增加病毒感染的風險,其余不良反應均為輕度且自行緩解。Castro等[8]研究顯示4.1%的患者治療期間可出現嗜酸性粒細胞增多癥、治療后16~20周增幅最大、平均增幅約10%。Dupin等[15]研究結果顯示,25%的患者隨訪期間出現至少1次嗜酸粒細胞增多≥1500個/μL、14%的患者治療后6個月仍持續存在嗜酸粒細胞增多、嗜酸性粒細胞計數通常在持續治療28~52周時降至基線水平。本研究中,研究組觀察到約13%的患者出現嗜酸性粒細胞增多,但治療期間嗜酸性粒細胞總體呈下降趨勢,度普利尤單抗治療后12個月嗜酸性粒細胞較基線顯著下降46.0%(P=0.015)。Dupin等[15]認為一過性嗜酸性粒細胞增多具有自限性,不改變疾病的病程和臨床反應。度普利尤單抗導致嗜酸性粒細胞增多的機制尚不清楚。阻斷IL-4和IL-13對可能引起嗜酸性粒細胞促進介質(如IL-5)的影響報道不一,有研究認為IL-5可短暫性升高[16],然而哮喘小鼠模型顯示IL-5的表達下降[17];IL-4和IL-13可募集并促進嗜酸性粒細胞的組織遷移,雙重阻斷IL-4和IL-13可導致嗜酸性粒細胞在外周血中的積聚[18];此外,ICS可顯著影響血嗜酸性粒細胞水平[19],因此,應結合ICS的當前劑量解釋外周血嗜酸性粒細胞的變化,而度普利尤單抗的療效與患者基線使用的ICS劑量無關。
IL-4和IL-13可通過誘導B細胞分化和免疫球蛋白的類別轉換使IgE水平增加[20],體外實驗也顯示度普利尤單抗可抑制IL-4誘導B細胞產生的IgE[21]。Zhou等[22]系統綜述和薈萃分析了特應性皮炎血清總IgE水平的變化,顯示度普利尤單抗可顯著降低患者的總IgE水平,對高IgE水平的患者,增加劑量可獲得更好的療效。本研究結果顯示度普利尤單抗也可顯著降低中重度哮喘患者的血清總IgE。
ABPA是哮喘的一種并發癥,可大大增加哮喘管理的難度,常需OCS治療[23]。ABPA發病機制尚不完全清楚,研究顯示ABPA主要激活T輔助細胞2(Th2)CD4+ T細胞應答,不能清除真菌,釋放的IL-4、IL-5、IL-13、CCL-17和IL-9等炎癥細胞因子可導致患者氣道出現持續的免疫反應而誘發炎癥反應[24-26],表現為血清IgE水平的升高、肥大細胞脫顆粒的增加、嗜酸性粒細胞和中性粒細胞的活化增強,最終導致黏液性阻塞、嗜酸性粒細胞性肺炎或支氣管擴張。Nishimura等[27]報道了1例ABPA患者經度普利尤單抗治療后完全停用糖皮質激素,van der Veer等[28]對8例ABPA患者的病例系列報道結果顯示度普利尤單抗可顯著減少急性加重次數和潑尼松的維持劑量。本研究度普利尤單抗治療的1例ABPA患者實現OCS減量71.4%進行維持治療,未出現急性加重。
綜上所述,度普利尤單抗可緩解中重度哮喘患者哮喘及共存疾病的癥狀、改善肺功能、減少急性加重次數以及減停OCS。治療期間無嚴重不良反應,具有良好的安全性,與RCT及迄今為止發表的少數真實世界研究結果相一致。本研究尚存在患者例數偏少、隨訪時間較短的局限性。另外,本研究為實驗性臨床醫療,經臨床評估后使用度普利尤單抗對適宜患者進行治療,療效判定依據為患者治療前后的自身對照,未同期匹配標準對照組。今后將增加納入患者樣本量并延長隨訪時間以觀察長期療效和安全性,并探索超級應答者的預測因子。
利益沖突:本研究不涉及任何利益沖突。
支氣管哮喘(簡稱哮喘)是一種常見的呼吸系統疾病,以氣道慢性炎癥為特征,臨床表現為反復發作的喘息、氣急,伴或不伴咳嗽或胸悶等癥狀,同時伴有氣道高反應性和可逆性氣流受限,隨著病程的遷延和炎癥的進展可導致氣道重塑[1]。我國20歲及以上人群哮喘患病率為4.2%,患者人數推算約為4570萬[2]。哮喘具有不同臨床類型,同時有生物學表型異質性。根據2型炎癥(type 2 inflammation,T2)水平的高低,分為低T2和高T2哮喘兩種類型[3]。高T2哮喘中常見兒童期早發過敏性哮喘以及成人期晚發重度嗜酸性粒細胞性哮喘,以嗜酸性氣道炎癥為特征,表現為嗜酸性粒細胞計數增多和(或)呼出氣一氧化氮(fractional exhaled nitric oxide,FeNO)升高[4-5]。臨床上根據達到哮喘控制所采用的治療級別對哮喘嚴重程度進行分級[1],常聯用中高劑量的吸入性糖皮質激素(inhaled corticosteroids,ICS)和長效β2受體激動劑(long acting beta-agonist,LABA)對中重度哮喘進行治療[1]。
T2疾病 哮喘的關鍵細胞因子包括白細胞介素(interleukin,IL)-5、IL-4和IL-13等,針對關鍵細胞因子的生物靶向治療是哮喘新藥開發的熱點之一。度普利尤單抗(dupilumab)是一種全人源IL-4受體α亞基(IL-4Rα)的單克隆抗體,通過與IL-4和IL-13共享的IL-4Rα結合抑制其信號傳導[6],從而阻斷IgE類別轉換、嗜酸性粒細胞趨化性和氣道高反應性相關的重疊效應以及抑制JAK/TYK信號通路的激活[6-7],最終抑制T2疾病 介導的炎癥反應。臨床研究表明,度普利尤單抗可顯著減少哮喘的急性加重、改善哮喘控制情況,并增加支氣管舒張劑前后的第1秒用力呼氣容積(forced expiratory volume in 1 second,FEV1)[8-10]。此外,度普利尤單抗治療特應性皮炎和慢性鼻竇炎伴鼻息肉等哮喘共存疾病也具有顯著療效[11-12]。歐美和日本等國和地區已批準度普利尤單抗用于治療不同年齡人群中的特定哮喘、中重度特應性皮炎或特定慢性鼻竇炎伴鼻息肉。本研究首次對不耐受ICS+LABA長期治療或療效不佳的中重度哮喘患者經過臨床評估后換用度普利尤單抗進行治療,觀察并評價其療效及安全性,旨在為我國中重度哮喘的臨床應用提供參考。
1 資料與方法
1.1 臨床資料
經首都醫科大學附屬北京朝陽醫院及醫院倫理審查委員會批準,對接受1年及以上中高劑量ICS+LABA的規范治療后哮喘仍未控制、急診就診的嗜酸性粒細胞增高的中重度哮喘患者使用度普尤利單抗進行本實驗性臨床醫療研究。本研究為回顧性研究,收集2021年5月—2022年4月在本院呼吸科門診就診的中重度哮喘患者。納入標準:① 符合2021版全球哮喘防治創議中重度哮喘的診斷標準[13];② 氣道炎癥類型表現為嗜酸型,外周血嗜酸性粒細胞計數≥500個/μL或FeNO≥30 ppb;③ 接受1年及以上中高劑量ICS+LABA的規范治療;④ 患者本人或其監護人完全理解并同意本實驗性臨床醫療研究的目的和實施,能配合醫師完成問卷調查。排除標準:① 正在接受其他單克隆抗體治療者;② 對度普利尤單抗活性成分或任何輔料過敏者;③ 妊娠或哺乳期患者;④ 接受免疫抑制劑或長期類固醇激素治療的惡性腫瘤、慢性自身免疫性疾病患者;⑤ 心肝腦腎等重要臟器嚴重受損者;⑥ 嚴重精神疾病患者。參與本研究的患者均簽署知情同意書。
1.2 方法
1.2.1 治療方法
納入研究組(度普尤利單抗治療組)的患者均接受度普利尤單抗治療,首次600 mg皮下注射,之后每2周300 mg皮下注射,單個療程為16周。納入對照組(ICS+LABA治療組)的患者,布地奈德福莫特羅160/4.5 μg 2~3吸2次/d或沙美特羅替卡松250~500 μg 1吸2次/d,和(或)聯合孟魯司特及口服糖皮質激素(oral corticosteroids,OCS)。所有患者每2周~4周隨訪1次,根據患者癥狀及檢查指標對OCS劑量使用進行調整。
1.2.2 數據采集
收集信息包括性別、年齡、身高、體重、體重指數、吸煙狀況、 哮喘病程、癥狀及嚴重程度、急性加重次數、基線治療(包括生物制劑)、T2疾病共存疾病及其他并發癥。收集基線、治療第1、3、6、12個月外周血嗜酸性粒細胞計數、嗜堿性粒細胞計數、血清總IgE、FeNO、哮喘控制測試(Asthma Control Test,ACT)評分、用力肺活量(forced vital capacity,FVC)、FEV1、FEV1/FVC、FEV1占預計值百分比(FEV1%pred)、呼氣峰值流量(peak expiratory flow,PEF)、肺活量75%、50%、25%時的最大呼氣流量(MEF75、MEF50和MEF25)和最大用力呼氣中段流量(MMEF或FEF25%-75%),以及每日維持劑量的潑尼松。ACT評分:<19分表示哮喘未控制,20~25分表示控制良好,分數越高表示哮喘控制越好。
1.3 統計學方法
采用SPSS 26.0軟件,分類變量使用例(n)和百分數(%)表示;連續變量呈正態及近似正態分布時使用均數±標準差( ±s)表示,采用配對t檢驗(組內)或獨立樣本t檢驗(組間)進行比較;連續變量呈非正態分布時使用中位數和四分位間距1、3 [M(Q1,Q3)]表示,采用曼–惠特尼U檢驗進行比較。P<0.05為差異有統計學意義。
±s)表示,采用配對t檢驗(組內)或獨立樣本t檢驗(組間)進行比較;連續變量呈非正態分布時使用中位數和四分位間距1、3 [M(Q1,Q3)]表示,采用曼–惠特尼U檢驗進行比較。P<0.05為差異有統計學意義。
2 結果
2.1 人口學特征及基線特征
納入研究組的中重度哮喘患者共17例,男8例,女9例,平均年齡(51.94±14.30)歲。其中,15例接受高劑量ICS+LABA治療,2例為中劑量但患有其他未控制的T2疾病 。7例需加用OCS,平均日劑量為(9.71±14.52)mg。4例既往接受抗IgE奧馬珠單抗(Omalizumab)治療,由于哮喘控制不佳,血嗜酸性粒細胞反復增高,經臨床評估后換用度普利尤單抗。13例存在哮喘共存疾病。7例慢性鼻竇炎伴鼻息肉患者中,3例曾行鼻內鏡息肉切除術。
納入對照組的中重度哮喘患者共30例,男14例,女16例,平均年齡(52.57±16.42)歲。其中,26例接受高劑量ICS+LABA治療,4例為中劑量但患有其他未控制的T2疾病 。14例需加用OCS,平均日劑量為(8.67±15.46)mg。22例存在哮喘共存疾病。13例慢性鼻竇炎伴鼻息肉患者中,8例曾行鼻內鏡息肉切除術。
研究組和對照組的患者基本情況見表1。兩組間患者情況基本均衡。
2.2 治療前后ACT及各項指標的變化
患者接受治療前后ACT評分及各項指標見表2。治療后第1、2、3和12個月時研究組和對照組患者的ACT均較基線顯著增加(P<0.001);治療后第2、3和12個月時,研究組患者ACT較對照組顯著增加(第2個月:P=0.002; 第3和12個月:P<0.001)。治療12個月后,研究組ACT相較基線增加65.4%,顯著高于對照組相較基線的增幅35.4%(P<0.001)(圖1)。
 )/M (Q1,Q3)]
)/M (Q1,Q3)]
 圖1
治療后相較基線ACT隨時間的變化趨勢圖
圖1
治療后相較基線ACT隨時間的變化趨勢圖
*
治療后第12個月,研究組和對照組的年急性加重次數差異無統計學意義(P=0.204),但相對基線均顯著下降(P=0.007)。
兩組血清總IgE、外周血嗜酸性粒細胞計數、外周血嗜堿性粒細胞計數及FeNO水平治療后相較基線均呈下降趨勢;治療后第12個月,研究組的血清總IgE 、外周血嗜酸性粒細胞計數、外周血嗜堿性粒細胞計數及FeNO 均較基線顯著下降(P值分別為0.048、0.015、0.0012和0.006),而對照組僅FeNO 相較基線顯著下降(P=0.037);治療后第12個月,研究組相較對照組外周血嗜堿性粒細胞計數、總IgE及FeNO的降幅顯著增大(圖2a)。
 圖2
治療12個月后兩組血清游離總IgE、外周血嗜酸性粒細胞計數、外周血嗜堿性粒細胞計數以及肺功能各項指標的比較
圖2
治療12個月后兩組血清游離總IgE、外周血嗜酸性粒細胞計數、外周血嗜堿性粒細胞計數以及肺功能各項指標的比較
a. 兩組血清游離總IgE、外周血嗜酸性粒細胞計數、外周血嗜堿性粒細胞計數及FeNO較基線降低百分比(*
肺功能各項指標(包括FVC、FEV1、FEV1%pred、FEV1/FVC、PEF、MEF25、MEF50、MEF75及MMEF)均在度普利尤單抗治療12個月后相較基線顯著升高(P<0.05),對照組除FEV1%pred與基線差異無統計學顯著性外,其余肺功能指標(包括FVC、FEV1、FEV1/FVC、PEF、MEF25、MEF50、MEF75及MMEF)相較基線也均顯著升高。度普尤利單抗治療12個月后對FEV1%pred、FEV1/FVC、PEF、MEF25、MEF50、MEF75及MMEF的改善顯著優于對照組(P<0.05)(圖2b)。
研究組中,7例基線時加用OCS的患者經度普利尤單抗治療后,OCS劑量均逐步減少至停用;4例既往使用奧馬珠單抗、后換用度普利尤單抗的患者,臨床癥狀較前緩解,急性加重次數減少;所有患者初次注射度普利尤單抗后1周內癥狀得到明顯緩解,最短癥狀緩解時間為4 h;合并慢性鼻竇炎伴鼻息肉及特應性皮炎的患者,相關癥狀較前改善;合并支氣管擴張、ABPA、塵肺的患者未見哮喘癥狀加重引起原發結構性疾病進行性加重的情況。
對照組中,83.3%(25/30)的患者在長期規范治療后癥狀減輕。14例吸入高劑量ICS/LABA的患者經過長期規范化治療后OCS減少50%及以上,其中6例患者OCS實現減停。16例患者仍需高劑量ICS/LABA維持癥狀的穩定。在慢性鼻竇炎伴鼻息肉的患者中,標準治療并未明顯減輕患者鼻部癥狀,2例患者在12個月隨訪期間行鼻息肉切除手術。
2.3 不良反應
治療期間,研究組患者出現注射部位腫痛4例、皮膚瘙癢2例、紅斑1例、乏力1例,均為輕度且自行緩解。1例患者首次注射600 mg半個月后出現帶狀皰疹,經靜脈激素及抗病毒治療后痊愈,未影響繼續度普利尤單抗治療。對照組不良反應主要為長期高劑量吸入糖皮質激素所致聲音嘶啞(1例)、口腔真菌感染(4例)、血糖(2例)和血壓(3例)控制欠佳以及重度骨質疏松(1例)。
3 討論
本研究回顧性分析并比較了度普利尤單抗和ICS+LABA常規治療中重度哮喘過程中ACT評分和各項血液學及肺功能指標的變化,是首篇評估度普利尤單抗治療中重度哮喘中國患者療效和安全性的真實世界研究。結果顯示,度普利尤單抗治療12個月后,年急性加重次數較基線下降62.5%,略高于Numata等[14]在日本真實世界研究中報道的53%。本研究7例患者基線加用的OCS劑量經度普利尤單抗治療后均逐步較少至停用,與日本患者OCS維持劑量減少54%的觀察相似[14]。此外,日本患者治療后6個月后的ACT、FeNO及總IgE較基線均顯著降低[14],與本研究結果相同。此外,本研究觀察到中國患者肺功能各項指標在治療12個月后較基線均顯著改善,而日本患者治療6個月后相較基線無顯著性差異,可能與本研究納入患者的基線肺功能本身較差或(和)日本研究隨訪時間較短有關。
本研究度普利尤單抗治療期間出現1例帶狀皰疹,經治療后痊愈。目前尚無研究表明度普利尤單抗會增加病毒感染的風險,其余不良反應均為輕度且自行緩解。Castro等[8]研究顯示4.1%的患者治療期間可出現嗜酸性粒細胞增多癥、治療后16~20周增幅最大、平均增幅約10%。Dupin等[15]研究結果顯示,25%的患者隨訪期間出現至少1次嗜酸粒細胞增多≥1500個/μL、14%的患者治療后6個月仍持續存在嗜酸粒細胞增多、嗜酸性粒細胞計數通常在持續治療28~52周時降至基線水平。本研究中,研究組觀察到約13%的患者出現嗜酸性粒細胞增多,但治療期間嗜酸性粒細胞總體呈下降趨勢,度普利尤單抗治療后12個月嗜酸性粒細胞較基線顯著下降46.0%(P=0.015)。Dupin等[15]認為一過性嗜酸性粒細胞增多具有自限性,不改變疾病的病程和臨床反應。度普利尤單抗導致嗜酸性粒細胞增多的機制尚不清楚。阻斷IL-4和IL-13對可能引起嗜酸性粒細胞促進介質(如IL-5)的影響報道不一,有研究認為IL-5可短暫性升高[16],然而哮喘小鼠模型顯示IL-5的表達下降[17];IL-4和IL-13可募集并促進嗜酸性粒細胞的組織遷移,雙重阻斷IL-4和IL-13可導致嗜酸性粒細胞在外周血中的積聚[18];此外,ICS可顯著影響血嗜酸性粒細胞水平[19],因此,應結合ICS的當前劑量解釋外周血嗜酸性粒細胞的變化,而度普利尤單抗的療效與患者基線使用的ICS劑量無關。
IL-4和IL-13可通過誘導B細胞分化和免疫球蛋白的類別轉換使IgE水平增加[20],體外實驗也顯示度普利尤單抗可抑制IL-4誘導B細胞產生的IgE[21]。Zhou等[22]系統綜述和薈萃分析了特應性皮炎血清總IgE水平的變化,顯示度普利尤單抗可顯著降低患者的總IgE水平,對高IgE水平的患者,增加劑量可獲得更好的療效。本研究結果顯示度普利尤單抗也可顯著降低中重度哮喘患者的血清總IgE。
ABPA是哮喘的一種并發癥,可大大增加哮喘管理的難度,常需OCS治療[23]。ABPA發病機制尚不完全清楚,研究顯示ABPA主要激活T輔助細胞2(Th2)CD4+ T細胞應答,不能清除真菌,釋放的IL-4、IL-5、IL-13、CCL-17和IL-9等炎癥細胞因子可導致患者氣道出現持續的免疫反應而誘發炎癥反應[24-26],表現為血清IgE水平的升高、肥大細胞脫顆粒的增加、嗜酸性粒細胞和中性粒細胞的活化增強,最終導致黏液性阻塞、嗜酸性粒細胞性肺炎或支氣管擴張。Nishimura等[27]報道了1例ABPA患者經度普利尤單抗治療后完全停用糖皮質激素,van der Veer等[28]對8例ABPA患者的病例系列報道結果顯示度普利尤單抗可顯著減少急性加重次數和潑尼松的維持劑量。本研究度普利尤單抗治療的1例ABPA患者實現OCS減量71.4%進行維持治療,未出現急性加重。
綜上所述,度普利尤單抗可緩解中重度哮喘患者哮喘及共存疾病的癥狀、改善肺功能、減少急性加重次數以及減停OCS。治療期間無嚴重不良反應,具有良好的安全性,與RCT及迄今為止發表的少數真實世界研究結果相一致。本研究尚存在患者例數偏少、隨訪時間較短的局限性。另外,本研究為實驗性臨床醫療,經臨床評估后使用度普利尤單抗對適宜患者進行治療,療效判定依據為患者治療前后的自身對照,未同期匹配標準對照組。今后將增加納入患者樣本量并延長隨訪時間以觀察長期療效和安全性,并探索超級應答者的預測因子。
利益沖突:本研究不涉及任何利益沖突。