引用本文: 張連芳, 謝榕城, 林雪烽, 馬杰飛. 重癥監護室內重癥肺炎患者新發血栓事件和病死率的研究分析. 中國呼吸與危重監護雜志, 2024, 23(1): 7-14. doi: 10.7507/1671-6205.202310019 復制
版權信息: ?四川大學華西醫院華西期刊社《中國呼吸與危重監護雜志》版權所有,未經授權不得轉載、改編
據文獻統計報道,肺部感染在全球具有很高的病死率,且在感染性疾病中是致死的首要原因[1],對患者預后有較大影響,嚴重威脅人民身體健康。與此同時,這個常見疾病給患者、國家帶來了巨大的經濟負擔[2]。而入住重癥監護室(intensive care unit,ICU)的肺炎患者,其病死率可高達30%~50%[3],且各項醫療成本和費用明顯增加。尤其2019年新型冠狀病毒感染(coronavirus disease 2019,COVID-19)暴發流行至今,不少報道感染新型冠狀病毒后,重型和危重型患者常常合并下肢深靜脈血栓、肺栓塞、或微循環血栓等血栓性事件,極大地增加了患者的病死率。因此重癥肺炎患者的血栓事件發生率,值得重點關注。關于重癥肺炎患者血栓形成的原因,目前研究認為重癥感染或膿毒血癥所導致的急性炎癥因子可以通過多種途徑影響凝血和纖溶功能,包括循環蛋白C和抗凝血酶-Ⅲ水平下降,纖溶酶原激活物抑制劑-1水平的上調等因素,最終導致凝血級聯反應的活化和纖溶過程的抑制,從而進一步促進血栓形成;同時還與長期臥床、機械通氣和靜脈置管等因素密切相關。目前,國內關于重癥肺炎的血栓發生事件的報道較少,本研究旨在對ICU內不同類型重癥肺炎[包括社區獲得性肺炎(community acquired pneumonia,CAP)和COVID-19]患者的新發血栓事件發生率進行分組研究,并進一步探討預測重癥肺炎患者血栓發生及死亡的高危因素,以期早期干預,降低發生率和病死率。
1 資料與方法
1.1 臨床資料
本研究為回顧性研究分析,經篩查后共收集2018年1月—2023年2月期間復旦大學附屬中山醫院廈門醫院重癥醫學科收治重癥肺炎患者161例。該研究已通過復旦大學附屬中山醫院廈門醫院倫理委員會的批準(倫理號B2023-059),并遵守1975年赫爾辛基宣言的倫理準則。
1.2 方法
1.2.1 病例納入、排除標準
納入標準:(1)符合重癥肺炎的臨床及影像學診斷標準[4];(2)COVID-19患者感染的重型和危重型患者;(3)下肢深靜脈彩色多普勒超聲檢查;(4)年齡≥18歲。排除標準:(1)未行相關血栓事件篩查患者;(2)既往血栓事件不計入本次研究結果;(3)數據缺失:缺少入ICU首次的腎功能、血常規、血清炎癥指標、CURB-65評分與急性生理學和慢性健康狀況評價Ⅱ(acute physiology and chronic health evaluation Ⅱ,APACHEⅡ)評分數據;(4)孕婦及哺乳婦女。研究期間多次住院的重復患者,選擇最后一次住院數據為基線指標。
1.2.2 分組與數據收集
根據本次入住ICU肺炎類型分為COVID-19組與CAP組。另外根據是否合并血栓事件的發生,分為血栓組和非血栓組。收集患者的人口統計學資料,記錄納入患者的靜脈血栓栓塞癥(venous thromboembolism,VTE)評分(采用Padua評分表,總分≥4分,高危;<4分,低危),血栓發生事件,疾病嚴重程度評分(CURB-65評分及APACHEⅡ評分),機械通氣情況,合并癥[糖尿病、循環系統疾病(高血壓、冠心病、心功能不全等)、電解質紊亂、腎功能不全、慢性肝臟疾病、甲狀腺功能減退等],實驗室指標[如血小板計數(platelet count,PLT)、乳酸、白蛋白、肌酐、尿素氮、尿素氮與肌酐比值(urea nitrogen to creatinine ratio,UCR)、降鈣素原(procalcitonin,PCT)、活化部分凝血活酶時間(activated partial thromboplastin time,APTT)、纖維蛋白原(fibrinogen,Fib)、D-二聚體等],臨床治療結局(好轉出院或死亡)。
所有患者轉入ICU當天或次日常規行下肢深靜脈彩色多普勒超聲檢查,在ICU住院期間結合患者癥狀按需完善肺動脈CT血管造影(CT angiography,CTA)、心電圖、頭顱CT或灌注CT,或頭顱磁共振成像等篩查血栓相關事件的輔助檢查。我們記錄的血栓事件均為ICU住院期間新發現的血栓事件,包括肌間靜脈血栓或深靜脈血栓形成(deep vein thrombosis,DVT)(多普勒超聲檢測),肺栓塞(肺動脈CTA),急性心肌梗死(血清心肌壞死標志物升高、心電圖確診),急性缺血性腦梗死(通過觀察新的局灶性神經體征和癥狀并通過磁共振成像或CT成像確診)。
1.2.3 觀察指標
(1)比較COVID-19組和CAP組的一般資料、實驗室指標的水平差異,以及兩組的血栓事件發生率、臨床結局病死率;(2)分析兩組的一般資料、并發癥、疾病嚴重程度評分、實驗室指標與血栓事件發生的相關性;(3)評估及分析各項指標對病死率的影響。
1.3 統計學方法
使用SPSS19.0軟件進行統計學分析。分類變量報告為計數和百分比;連續變量若為正態分布以均數±標準差(x±s)表示;若非正態分布,以中位數和四分位間距[M(P25,P75)]表示。分類變量的差異性通過χ2檢驗或Fisher精確檢驗進行評估。所有連續變量均用Shapiro-Wilk檢驗進行正態性檢驗。對于正態分布的連續變量,采用t檢驗,非正態分布變量采用非參數檢驗(Mann-Whitney 和 Wilcoxon秩和相關檢驗)。通過Logistics模型評估不同因素對血栓事件的影響,并計算Wald置信區間(confidential interval,CI)和優勢比(odds ratio,OR)。將Logistics模型中的連續變量納入受試者操作特征曲線(receiver operator characteristic curve,ROC曲線)分析不同因素的敏感性及特異性;而分類變量以Kappa值評價其一致性。P<0.05為差異有統計學意義。
2 結果
2.1 COVID-19組與CAP組的臨床特征
本研究最終納入重癥肺炎患者161例,其中男119例,女42例。根據肺炎類型分為COVID-19組88例(男68例、女20例)和CAP組73例(男51例、女22例),兩組的性別及年齡差異無統計學意義(P>0.05)。兩組的臨床與實驗室資料見表1。
CAP組入住ICU時心血管系統疾病患病率更高(28.4%比52.1%,P<0.05);兩組轉入ICU前的住院天數、合并癥(高血壓、惡性腫瘤、肝腎功能不全等)均無顯著差異(P>0.05)。兩組的ICU住院天數差異有統計學意義(P<0.05),COVID-19組的ICU住院時間更長,但總住院天數差異無統計學意義(P>0.05)。COVID-19組轉入ICU時APACHEⅡ評分(22.0分比18.0分,P<0.05)和CURB-65評分(4分比3分,P<0.05)更高;氧合指數更低(94.5 mm Hg比164.0 mm Hg,P<0.05;1 mm Hg=0.133 kPa)、無創通氣使用率更低(26.1%比41.1%,P<0.05)。上述指標提示COVID-19組的患者入ICU時病情更危重(表1)。
相比于CAP組,COVID-19組的白蛋白水平更低(30.80 g/L比33.59 g/L,P<0.05),肌酐(106 .00 μmol/L比83.00 μmol/L,P<0.05)、尿素氮(14.45 mmol/L比8.50 mmol/L,P<0.05)、UCR(32.18比24.75,P<0.05)更高,提示合并COVID-19感染可能蛋白消耗、能量代謝比普通CAP更加劇烈。COVID-19組中APTT延長(34.0 s比30.3 s,P<0.05)、PLT降低(148.50×109/L比213.00×109/L,P<0.05),但Fib、D-二聚體未見顯著差異,同時兩組的血栓發生率無顯著差異(表1)。
2.2 COVID-19組與CAP組的血栓臨床特征
CAP組中出現24例(32.9%)血栓,均為靜脈血栓,無動脈血栓形成;COVID-19組出現32例(36.4%)血栓,其中31例為靜脈血栓(2例合并新發腦梗死),1例為新發心肌梗死。兩組血栓發生率無明顯差異(P>0.05)。結果見表2。
COVID-19組中,血栓與非血栓組間APTT呈現差異,即血栓組中APTT明顯縮短(32.1 s比35.4 s,P<0.05),其余因素差異無統計學意義。而CAP組中,性別(女,50%比20.4%,P<0.05)、年齡(79.5歲比68.0歲,P<0.05)、VTE評分(7.58分比6.26分,P<0.05)、PCT(0.19 ng/mL比0.99 ng/mL,P<0.05)、APTT(28.8 s比30.8 s,P<0.05)及Fib(420.08 mg/dL比530.02 mg/dL,P<0.05)差異均有統計學意義。結果見表3。
2.3 血栓的相關因素分析
對所有重肺患者的血栓因素進行分析,血栓組與非血栓組間的性別、年齡、VTE評分、APTT及PCT差異有統計學意義(P<0.05);同時,是否合并COVID-19并未增加血栓事件的發生(表4)。女性、高齡、高VTE評分、APTT縮短及低PCT可能和血栓的發生密切相關。在Logistics模型中,血栓事件的發生與性別、年齡及APTT呈相關性;其中,性別(女性:OR=2.47,95%CI 1.13~5.39,P<0.05)與年齡(OR=1.04,95%CI 1.01~1.07,P<0.05)與血栓事件的發生呈正相關。結果見表5。
2.4 結局分析
88例合并COVID-19感染的重肺患者中出現39例死亡(占44.3%),73例CAP組感染的重肺患者中有31例死亡(占42.5%),兩組間死亡發生率無明顯差異(表1)。同時,COVID-19組與CAP組內分析是否發生血栓事件未增加患者病死率,分別為(46.9%比42.9%,P>0.05)、(33.3%比46.9%,P>0.05)(表3)。且血栓事件相關多因素分析后證實重癥患者的血栓發生與死亡并無顯著相關性(表4)。
分析死亡事件的相關因素發現,性別、腎臟疾病、有創通氣、無創通氣、轉入ICU前住院天數、CURB-65評分、尿素氮、APACHEⅡ評分、乳酸、Fib、肌酐、PCT、D-二聚體、VTE評分及氧合指數均差異有統計學意義(P<0.05)。
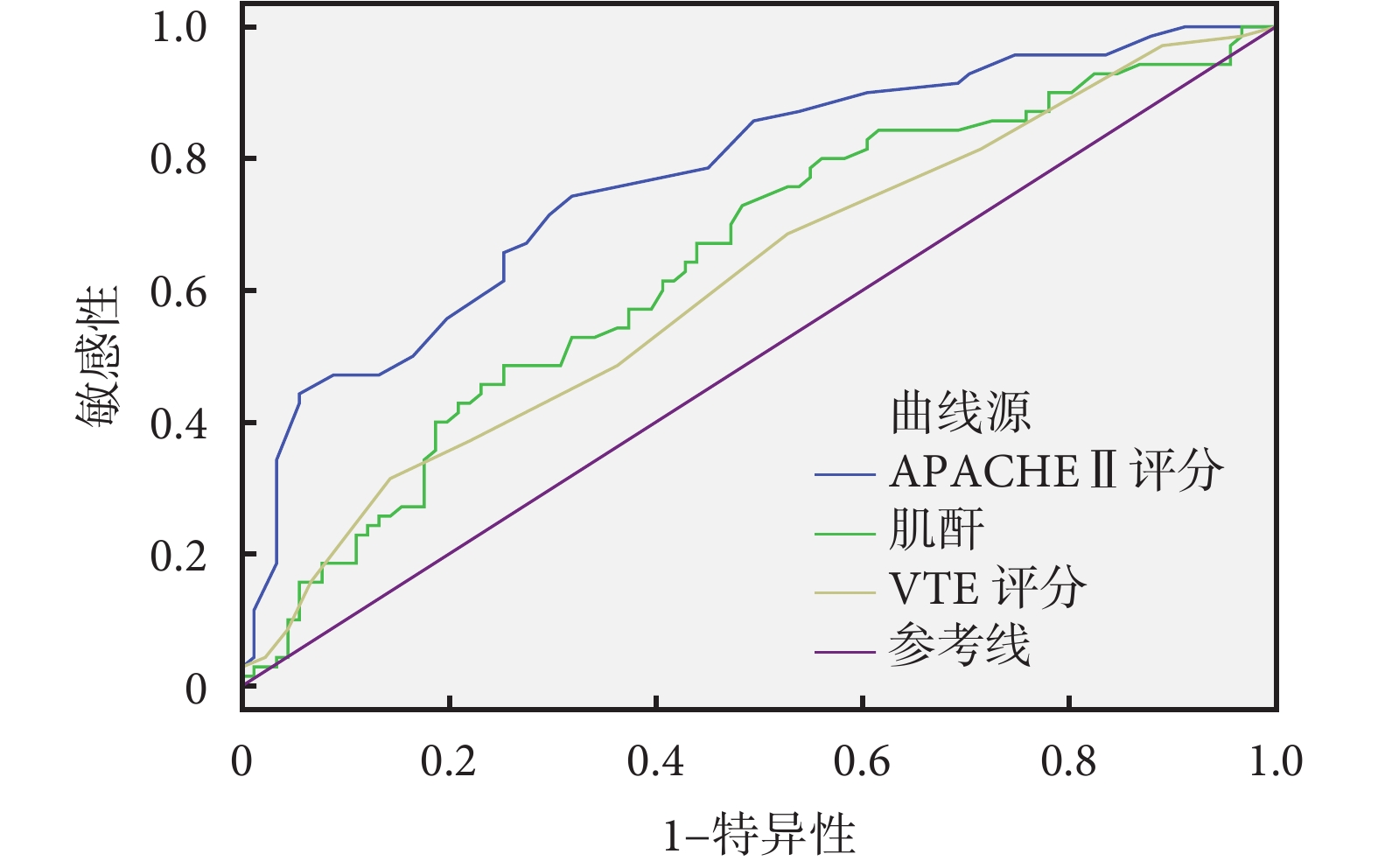
將上述因素納入納入Logistics模型中,逐步剔除相關變量,最終腎臟疾病、肌酐、APACHEⅡ評分及VTE評分納入模型(表6)。其中腎臟疾病的OR值最高。將Logistics模型中因素納入ROC曲線(圖1),APACHEⅡ評分的ROC曲線下面積(area under ROC curve,AUC)為0.77(95%CI 0.70~0.84,敏感性74.3%,特異性68.1%),VTE評分的AUC為0.61(95%CI 0.53~0.70,敏感性31.4%,特異性81.7%),肌酐的AUC為0.64(95%CI 0.56~0.73,敏感性72.9%,特異性51.2%)。而腎臟疾病的Kappa值為0.409(P<0.05),呈現中度一致性。
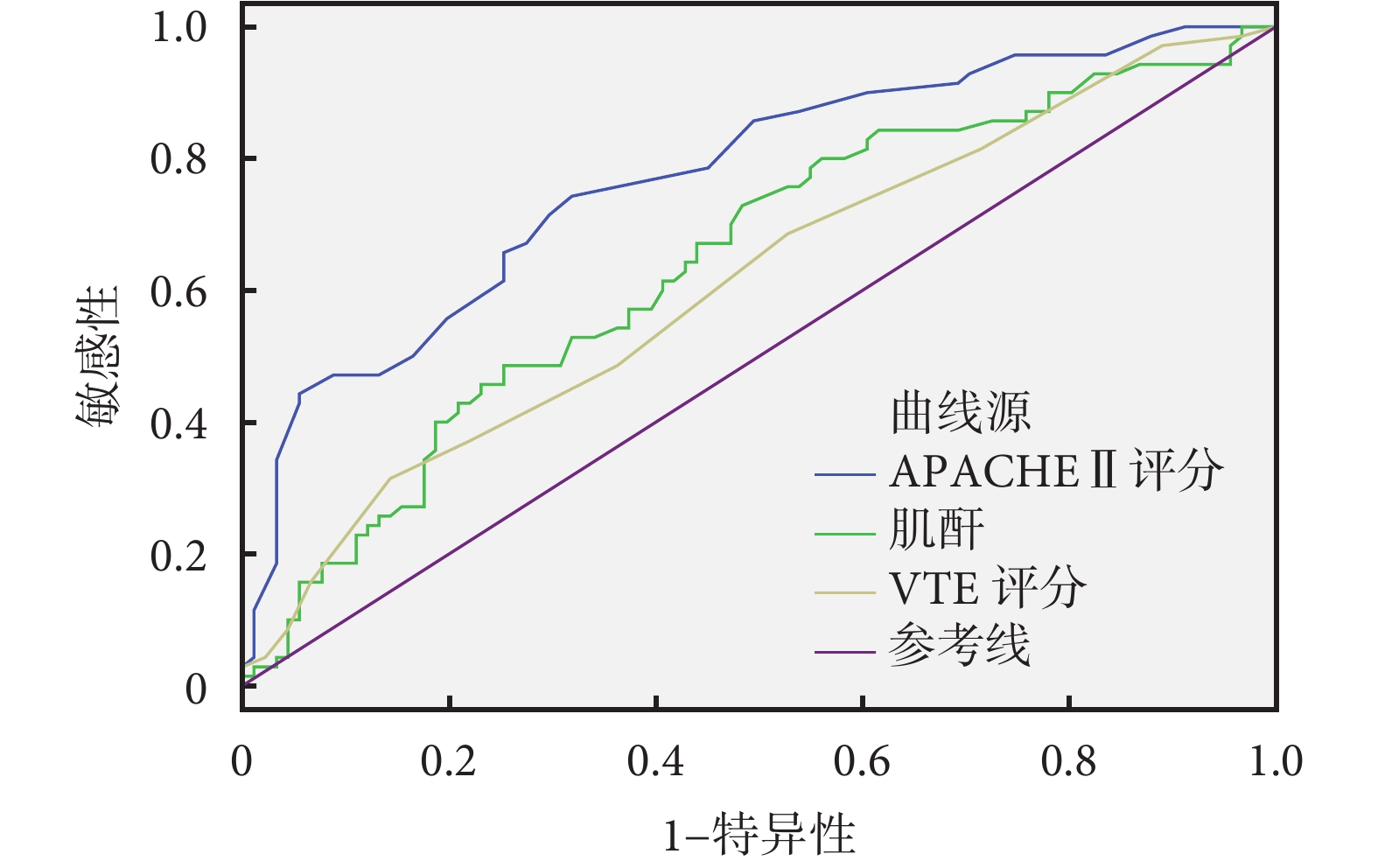 圖1
各指標預測重癥肺炎患者預后的ROC曲線
圖1
各指標預測重癥肺炎患者預后的ROC曲線
3 討論
本研究結果顯示不同類型重癥肺炎患者出現了循環障礙,產生頑固性缺氧與休克時,COVID-19所致的重癥肺炎的嚴重程度高于CAP感染有引起的重癥肺炎。經抗生素、氧療等綜合治療,兩組患者的血栓事件的發生率、病死率差異無統計學意義,但均明顯升高。進一步研究分析發現,ICU內重癥肺炎患者的新發血栓發生與性別、年齡及APTT呈相關性;APACHEⅡ評分、VTE評分、肌酐值為預測重癥肺炎死亡的獨立危險因素。
本研究中COVID-19組患者的有創機械通氣使用率、APACHEⅡ評分、CURB-65評分、肌酐、尿素氮、UCR較CAP分組更高;氧合指數、白蛋白水平更低;ICU住院時間更長。上述指標可能提示COVID-19感染所致的重癥肺炎患者氧耗量高、能量代謝更劇烈、蛋白消耗高、嚴重程度可能更高。1985年Knaus推出APACHEⅡ評分系統包括急性生理評分(包括了氧合指數、肌酐等)、年齡、慢性健康評分構成,目前已成為世界范圍內ICU普遍使用的評分系統,評分越高、疾病越嚴重。CURB-65評分包括年齡、意識障礙、尿素氮、呼吸頻率、血壓5個方面[5],是臨床上廣泛用來評估社區獲得性肺炎的輕重程度的標準,但其對住院患者的死亡預測效能不佳[6]。相關研究指出原因可能為該評分系統以年齡及生命體征作為評價標準,未結合更多的輔助檢查項目進行綜合評估,因而導致預測效能有一定局限性[7]。本研究對死亡的因素篩查中CURB-65評分未被納入作為預測因子。符翔等[8]的報道尿素氮、UCR值越高,則表示機體分解代謝狀態越嚴重,考慮是生物能量失效、蛋白穩態改變與肌肉持續消耗等綜合因素作用的結果,導致極為嚴重的炎癥“瀑布效應”,嚴重損害機體免疫功能與營養狀態,表明重癥肺炎患者處于高分解代謝狀態。這表明肺炎早期疾病嚴重程度的評分越高,但其血栓發生率或死亡率不一定越高。
在ICU日常臨床工作中,隨著無創靜脈超聲檢查逐步普及,VTE檢測率較既往大大提高,將其結合臨床表現和預測VTE的生物標志物,用于指導VTE的早期預防及治療干預[9]。2020年COVID-19流行初期,我國學者關于新冠的臨床特征報道中提及由于炎癥過度反應、缺氧和彌漫性血管內凝血,COVID-19可能更易導致靜脈和動脈血栓栓塞性疾病[10]。但是,目前關于重癥肺炎患者(尤其是CAP所致)的血栓發生率的相關報道較少。本研究基于此,進一步劃分為COVID-19組和CAP組,研究兩組間血栓發生率的差異及危險因素。結果CAP組出現24例(32.9%)血栓,COVID-19組出現32例(36.4%)血栓。這一發現與相關報道結果一致。2021年德國的一項薈萃分析報告了COVID-19患者的靜脈血栓栓塞發生率約為13%[11]。意大利學者報道入住ICU的COVID-19患者血栓事件發生率為41.3%,與此同時非ICU患者COVID-19患者為11.6%[12]。在本研究中,兩組之間血栓發生率差異無統計學意義(COVID-19組36.4%比CAP組32.9%,P=0.644),這表明合并COVID-19感染的重型患者與CAP所致的重型患者之間血栓事件發生率無顯著差異。但是,相比于普通肺炎感染者,不同感染來源的重癥肺炎患者的血栓事件的發生率均顯著升高。
本研究對重癥肺炎患者血栓事件的危險因素進行分析,結果顯示女性、高齡、高VTE評分、APTT縮短及低PLT可能提示血栓的發生;在Logistics模型中,血栓發生與性別、年齡及APTT呈相關性,其中性別(女性OR=2.47,95%CI 1.13~5.39,P<0.05)與年齡(OR=1.04,95%CI 1.01~1.07,P<0.05)與血栓發生呈正相關。國外流行病學調查結果顯示,女性人群VTE年發病率為11/10 000~12.3/10 000,育齡婦女VTE年發病率為0.7/10 000~13.5/1 000[13]。雌激素對于心血管系統有一定的保護作用,隨著年齡增長,雌激素水平降,女性的VTE患病風險增加。Nahum等[14]研究報道凝血功能障礙和年齡是血栓并發癥的獨立預測因素,與本研究結果相一致。隨著年齡遞增,人體機能逐漸下降,可發生一些凝血因子異常激活或血小板功能失調,進一步導致血栓形成[15]。凝血功能障礙在重癥感染中非常常見,其中APTT是臨床上最常用的反映內源性凝血系統凝血活性的敏感篩選試驗,它縮短表示血液處于高凝狀態,多見于血栓性疾病和血栓前狀態。雖然D-二聚體升高是血栓的敏感指標,但在本研究中敏感性卻較差,考慮研究中收集的相關實驗指標均為轉入ICU當天的數據結果,未動態對后續指標數據進行進一步分析,可能造成了一定偏倚。因此,動態隨訪治療過程中的各項血凝指標的變化可能會有不同的臨床意義[16]。
肺炎是一個的值得重視的健康問題,與高發病率、短期和長期病死率有關,也是全世界各年齡段人群死亡的主要傳染病病因[17]。本研究中CAP組和COVID-19組重癥肺炎患者的病死率均較高,分別高達44.3%和42.5%。再進一步對所有患者進行相關因素的Logistics模型ROC曲線分析得出,預測重癥肺炎患者死亡風險的預后指標為APACHEⅡ評分(AUC=0.77,95%CI 0.70~0.84)、VTE評分(AUC=0.61,95%CI 0.53~0.70)、肌酐(AUC=0.64,95%CI 0.56~0.73),而腎臟疾病的Kappa值為0.409(P<0.05),呈現中度一致性。APACHEⅡ評分自其問世以來,便以其簡便和可靠的特點備受醫學界的認可,其預測病死率的正確率達86%,在臨床上使用廣泛。國內學者黃澤波等[18]關于連續性腎臟替代治療治療重癥肺部感染相關膿毒癥患者預后路線圖模型的建立中,預測因素為高APACHEⅡ評分、內毒素水平以及低白蛋白水平等,與本研究結果相符合。本研究中重癥肺炎患者的VTE評分評估采用2018版《肺血栓栓塞癥診治與預防指南》[19]推薦的Padua評分。武漢新冠疫情流行期間,研究顯示Padua評分較高者的預后可能較差[16],可能作為新冠肺炎患者疾病嚴重程度和預后的相關指標之一;本研究結果與之相符合。重癥肺炎患者出現低氧、組織灌注不足,容易導致多器官功能障礙,往往早期出現急性腎功能不全,表現為尿少、肌酐升高、電解質紊亂等。張煒宗等[20]關于新冠患者院內死亡危險因素的分析指出,在合并癥中,發現腎臟疾病、腦卒中等是COVID-19 患者院內死亡的危險因素。在本研究中,兩個分組間病死率差異無統計學意義,考慮可能與部分COVID-19組患者早期使用特效藥物(包括Paxlovid、Molnupiravir等)可降低總體病死率有一定影響。在香港奧密克戎暴發期,Wong等[21]報告早期使用Molnupiravir或Paxlovid治療與死亡風險降低和住院后疾病進展風險降低顯著相關,Paxlovid治療還與住院風險降低顯著相關。Arbel等[22]研究顯示Paxlovid能夠顯著降低65歲及以上的老年人的住院風險或死亡風險。
本研究存在一定的局限性:研究對象為回顧性研究,部分數據存在丟失,資料收集難度大,影響結果偏倚;病例數量有限,樣本量不足夠大;因特殊時期普通病房未全面開展COVID-19感染患者對血栓事件的篩查,導致部分數據缺失,因而本研究未收集普通社區獲得性肺炎及非ICU住院COVID-19感染患者的相關資料進行分析,需進一步設計分組研究。
利益沖突:本研究不涉及任何利益沖突。
據文獻統計報道,肺部感染在全球具有很高的病死率,且在感染性疾病中是致死的首要原因[1],對患者預后有較大影響,嚴重威脅人民身體健康。與此同時,這個常見疾病給患者、國家帶來了巨大的經濟負擔[2]。而入住重癥監護室(intensive care unit,ICU)的肺炎患者,其病死率可高達30%~50%[3],且各項醫療成本和費用明顯增加。尤其2019年新型冠狀病毒感染(coronavirus disease 2019,COVID-19)暴發流行至今,不少報道感染新型冠狀病毒后,重型和危重型患者常常合并下肢深靜脈血栓、肺栓塞、或微循環血栓等血栓性事件,極大地增加了患者的病死率。因此重癥肺炎患者的血栓事件發生率,值得重點關注。關于重癥肺炎患者血栓形成的原因,目前研究認為重癥感染或膿毒血癥所導致的急性炎癥因子可以通過多種途徑影響凝血和纖溶功能,包括循環蛋白C和抗凝血酶-Ⅲ水平下降,纖溶酶原激活物抑制劑-1水平的上調等因素,最終導致凝血級聯反應的活化和纖溶過程的抑制,從而進一步促進血栓形成;同時還與長期臥床、機械通氣和靜脈置管等因素密切相關。目前,國內關于重癥肺炎的血栓發生事件的報道較少,本研究旨在對ICU內不同類型重癥肺炎[包括社區獲得性肺炎(community acquired pneumonia,CAP)和COVID-19]患者的新發血栓事件發生率進行分組研究,并進一步探討預測重癥肺炎患者血栓發生及死亡的高危因素,以期早期干預,降低發生率和病死率。
1 資料與方法
1.1 臨床資料
本研究為回顧性研究分析,經篩查后共收集2018年1月—2023年2月期間復旦大學附屬中山醫院廈門醫院重癥醫學科收治重癥肺炎患者161例。該研究已通過復旦大學附屬中山醫院廈門醫院倫理委員會的批準(倫理號B2023-059),并遵守1975年赫爾辛基宣言的倫理準則。
1.2 方法
1.2.1 病例納入、排除標準
納入標準:(1)符合重癥肺炎的臨床及影像學診斷標準[4];(2)COVID-19患者感染的重型和危重型患者;(3)下肢深靜脈彩色多普勒超聲檢查;(4)年齡≥18歲。排除標準:(1)未行相關血栓事件篩查患者;(2)既往血栓事件不計入本次研究結果;(3)數據缺失:缺少入ICU首次的腎功能、血常規、血清炎癥指標、CURB-65評分與急性生理學和慢性健康狀況評價Ⅱ(acute physiology and chronic health evaluation Ⅱ,APACHEⅡ)評分數據;(4)孕婦及哺乳婦女。研究期間多次住院的重復患者,選擇最后一次住院數據為基線指標。
1.2.2 分組與數據收集
根據本次入住ICU肺炎類型分為COVID-19組與CAP組。另外根據是否合并血栓事件的發生,分為血栓組和非血栓組。收集患者的人口統計學資料,記錄納入患者的靜脈血栓栓塞癥(venous thromboembolism,VTE)評分(采用Padua評分表,總分≥4分,高危;<4分,低危),血栓發生事件,疾病嚴重程度評分(CURB-65評分及APACHEⅡ評分),機械通氣情況,合并癥[糖尿病、循環系統疾病(高血壓、冠心病、心功能不全等)、電解質紊亂、腎功能不全、慢性肝臟疾病、甲狀腺功能減退等],實驗室指標[如血小板計數(platelet count,PLT)、乳酸、白蛋白、肌酐、尿素氮、尿素氮與肌酐比值(urea nitrogen to creatinine ratio,UCR)、降鈣素原(procalcitonin,PCT)、活化部分凝血活酶時間(activated partial thromboplastin time,APTT)、纖維蛋白原(fibrinogen,Fib)、D-二聚體等],臨床治療結局(好轉出院或死亡)。
所有患者轉入ICU當天或次日常規行下肢深靜脈彩色多普勒超聲檢查,在ICU住院期間結合患者癥狀按需完善肺動脈CT血管造影(CT angiography,CTA)、心電圖、頭顱CT或灌注CT,或頭顱磁共振成像等篩查血栓相關事件的輔助檢查。我們記錄的血栓事件均為ICU住院期間新發現的血栓事件,包括肌間靜脈血栓或深靜脈血栓形成(deep vein thrombosis,DVT)(多普勒超聲檢測),肺栓塞(肺動脈CTA),急性心肌梗死(血清心肌壞死標志物升高、心電圖確診),急性缺血性腦梗死(通過觀察新的局灶性神經體征和癥狀并通過磁共振成像或CT成像確診)。
1.2.3 觀察指標
(1)比較COVID-19組和CAP組的一般資料、實驗室指標的水平差異,以及兩組的血栓事件發生率、臨床結局病死率;(2)分析兩組的一般資料、并發癥、疾病嚴重程度評分、實驗室指標與血栓事件發生的相關性;(3)評估及分析各項指標對病死率的影響。
1.3 統計學方法
使用SPSS19.0軟件進行統計學分析。分類變量報告為計數和百分比;連續變量若為正態分布以均數±標準差(x±s)表示;若非正態分布,以中位數和四分位間距[M(P25,P75)]表示。分類變量的差異性通過χ2檢驗或Fisher精確檢驗進行評估。所有連續變量均用Shapiro-Wilk檢驗進行正態性檢驗。對于正態分布的連續變量,采用t檢驗,非正態分布變量采用非參數檢驗(Mann-Whitney 和 Wilcoxon秩和相關檢驗)。通過Logistics模型評估不同因素對血栓事件的影響,并計算Wald置信區間(confidential interval,CI)和優勢比(odds ratio,OR)。將Logistics模型中的連續變量納入受試者操作特征曲線(receiver operator characteristic curve,ROC曲線)分析不同因素的敏感性及特異性;而分類變量以Kappa值評價其一致性。P<0.05為差異有統計學意義。
2 結果
2.1 COVID-19組與CAP組的臨床特征
本研究最終納入重癥肺炎患者161例,其中男119例,女42例。根據肺炎類型分為COVID-19組88例(男68例、女20例)和CAP組73例(男51例、女22例),兩組的性別及年齡差異無統計學意義(P>0.05)。兩組的臨床與實驗室資料見表1。
CAP組入住ICU時心血管系統疾病患病率更高(28.4%比52.1%,P<0.05);兩組轉入ICU前的住院天數、合并癥(高血壓、惡性腫瘤、肝腎功能不全等)均無顯著差異(P>0.05)。兩組的ICU住院天數差異有統計學意義(P<0.05),COVID-19組的ICU住院時間更長,但總住院天數差異無統計學意義(P>0.05)。COVID-19組轉入ICU時APACHEⅡ評分(22.0分比18.0分,P<0.05)和CURB-65評分(4分比3分,P<0.05)更高;氧合指數更低(94.5 mm Hg比164.0 mm Hg,P<0.05;1 mm Hg=0.133 kPa)、無創通氣使用率更低(26.1%比41.1%,P<0.05)。上述指標提示COVID-19組的患者入ICU時病情更危重(表1)。
相比于CAP組,COVID-19組的白蛋白水平更低(30.80 g/L比33.59 g/L,P<0.05),肌酐(106 .00 μmol/L比83.00 μmol/L,P<0.05)、尿素氮(14.45 mmol/L比8.50 mmol/L,P<0.05)、UCR(32.18比24.75,P<0.05)更高,提示合并COVID-19感染可能蛋白消耗、能量代謝比普通CAP更加劇烈。COVID-19組中APTT延長(34.0 s比30.3 s,P<0.05)、PLT降低(148.50×109/L比213.00×109/L,P<0.05),但Fib、D-二聚體未見顯著差異,同時兩組的血栓發生率無顯著差異(表1)。
2.2 COVID-19組與CAP組的血栓臨床特征
CAP組中出現24例(32.9%)血栓,均為靜脈血栓,無動脈血栓形成;COVID-19組出現32例(36.4%)血栓,其中31例為靜脈血栓(2例合并新發腦梗死),1例為新發心肌梗死。兩組血栓發生率無明顯差異(P>0.05)。結果見表2。
COVID-19組中,血栓與非血栓組間APTT呈現差異,即血栓組中APTT明顯縮短(32.1 s比35.4 s,P<0.05),其余因素差異無統計學意義。而CAP組中,性別(女,50%比20.4%,P<0.05)、年齡(79.5歲比68.0歲,P<0.05)、VTE評分(7.58分比6.26分,P<0.05)、PCT(0.19 ng/mL比0.99 ng/mL,P<0.05)、APTT(28.8 s比30.8 s,P<0.05)及Fib(420.08 mg/dL比530.02 mg/dL,P<0.05)差異均有統計學意義。結果見表3。
2.3 血栓的相關因素分析
對所有重肺患者的血栓因素進行分析,血栓組與非血栓組間的性別、年齡、VTE評分、APTT及PCT差異有統計學意義(P<0.05);同時,是否合并COVID-19并未增加血栓事件的發生(表4)。女性、高齡、高VTE評分、APTT縮短及低PCT可能和血栓的發生密切相關。在Logistics模型中,血栓事件的發生與性別、年齡及APTT呈相關性;其中,性別(女性:OR=2.47,95%CI 1.13~5.39,P<0.05)與年齡(OR=1.04,95%CI 1.01~1.07,P<0.05)與血栓事件的發生呈正相關。結果見表5。
2.4 結局分析
88例合并COVID-19感染的重肺患者中出現39例死亡(占44.3%),73例CAP組感染的重肺患者中有31例死亡(占42.5%),兩組間死亡發生率無明顯差異(表1)。同時,COVID-19組與CAP組內分析是否發生血栓事件未增加患者病死率,分別為(46.9%比42.9%,P>0.05)、(33.3%比46.9%,P>0.05)(表3)。且血栓事件相關多因素分析后證實重癥患者的血栓發生與死亡并無顯著相關性(表4)。
分析死亡事件的相關因素發現,性別、腎臟疾病、有創通氣、無創通氣、轉入ICU前住院天數、CURB-65評分、尿素氮、APACHEⅡ評分、乳酸、Fib、肌酐、PCT、D-二聚體、VTE評分及氧合指數均差異有統計學意義(P<0.05)。
將上述因素納入納入Logistics模型中,逐步剔除相關變量,最終腎臟疾病、肌酐、APACHEⅡ評分及VTE評分納入模型(表6)。其中腎臟疾病的OR值最高。將Logistics模型中因素納入ROC曲線(圖1),APACHEⅡ評分的ROC曲線下面積(area under ROC curve,AUC)為0.77(95%CI 0.70~0.84,敏感性74.3%,特異性68.1%),VTE評分的AUC為0.61(95%CI 0.53~0.70,敏感性31.4%,特異性81.7%),肌酐的AUC為0.64(95%CI 0.56~0.73,敏感性72.9%,特異性51.2%)。而腎臟疾病的Kappa值為0.409(P<0.05),呈現中度一致性。
 圖1
各指標預測重癥肺炎患者預后的ROC曲線
圖1
各指標預測重癥肺炎患者預后的ROC曲線
3 討論
本研究結果顯示不同類型重癥肺炎患者出現了循環障礙,產生頑固性缺氧與休克時,COVID-19所致的重癥肺炎的嚴重程度高于CAP感染有引起的重癥肺炎。經抗生素、氧療等綜合治療,兩組患者的血栓事件的發生率、病死率差異無統計學意義,但均明顯升高。進一步研究分析發現,ICU內重癥肺炎患者的新發血栓發生與性別、年齡及APTT呈相關性;APACHEⅡ評分、VTE評分、肌酐值為預測重癥肺炎死亡的獨立危險因素。
本研究中COVID-19組患者的有創機械通氣使用率、APACHEⅡ評分、CURB-65評分、肌酐、尿素氮、UCR較CAP分組更高;氧合指數、白蛋白水平更低;ICU住院時間更長。上述指標可能提示COVID-19感染所致的重癥肺炎患者氧耗量高、能量代謝更劇烈、蛋白消耗高、嚴重程度可能更高。1985年Knaus推出APACHEⅡ評分系統包括急性生理評分(包括了氧合指數、肌酐等)、年齡、慢性健康評分構成,目前已成為世界范圍內ICU普遍使用的評分系統,評分越高、疾病越嚴重。CURB-65評分包括年齡、意識障礙、尿素氮、呼吸頻率、血壓5個方面[5],是臨床上廣泛用來評估社區獲得性肺炎的輕重程度的標準,但其對住院患者的死亡預測效能不佳[6]。相關研究指出原因可能為該評分系統以年齡及生命體征作為評價標準,未結合更多的輔助檢查項目進行綜合評估,因而導致預測效能有一定局限性[7]。本研究對死亡的因素篩查中CURB-65評分未被納入作為預測因子。符翔等[8]的報道尿素氮、UCR值越高,則表示機體分解代謝狀態越嚴重,考慮是生物能量失效、蛋白穩態改變與肌肉持續消耗等綜合因素作用的結果,導致極為嚴重的炎癥“瀑布效應”,嚴重損害機體免疫功能與營養狀態,表明重癥肺炎患者處于高分解代謝狀態。這表明肺炎早期疾病嚴重程度的評分越高,但其血栓發生率或死亡率不一定越高。
在ICU日常臨床工作中,隨著無創靜脈超聲檢查逐步普及,VTE檢測率較既往大大提高,將其結合臨床表現和預測VTE的生物標志物,用于指導VTE的早期預防及治療干預[9]。2020年COVID-19流行初期,我國學者關于新冠的臨床特征報道中提及由于炎癥過度反應、缺氧和彌漫性血管內凝血,COVID-19可能更易導致靜脈和動脈血栓栓塞性疾病[10]。但是,目前關于重癥肺炎患者(尤其是CAP所致)的血栓發生率的相關報道較少。本研究基于此,進一步劃分為COVID-19組和CAP組,研究兩組間血栓發生率的差異及危險因素。結果CAP組出現24例(32.9%)血栓,COVID-19組出現32例(36.4%)血栓。這一發現與相關報道結果一致。2021年德國的一項薈萃分析報告了COVID-19患者的靜脈血栓栓塞發生率約為13%[11]。意大利學者報道入住ICU的COVID-19患者血栓事件發生率為41.3%,與此同時非ICU患者COVID-19患者為11.6%[12]。在本研究中,兩組之間血栓發生率差異無統計學意義(COVID-19組36.4%比CAP組32.9%,P=0.644),這表明合并COVID-19感染的重型患者與CAP所致的重型患者之間血栓事件發生率無顯著差異。但是,相比于普通肺炎感染者,不同感染來源的重癥肺炎患者的血栓事件的發生率均顯著升高。
本研究對重癥肺炎患者血栓事件的危險因素進行分析,結果顯示女性、高齡、高VTE評分、APTT縮短及低PLT可能提示血栓的發生;在Logistics模型中,血栓發生與性別、年齡及APTT呈相關性,其中性別(女性OR=2.47,95%CI 1.13~5.39,P<0.05)與年齡(OR=1.04,95%CI 1.01~1.07,P<0.05)與血栓發生呈正相關。國外流行病學調查結果顯示,女性人群VTE年發病率為11/10 000~12.3/10 000,育齡婦女VTE年發病率為0.7/10 000~13.5/1 000[13]。雌激素對于心血管系統有一定的保護作用,隨著年齡增長,雌激素水平降,女性的VTE患病風險增加。Nahum等[14]研究報道凝血功能障礙和年齡是血栓并發癥的獨立預測因素,與本研究結果相一致。隨著年齡遞增,人體機能逐漸下降,可發生一些凝血因子異常激活或血小板功能失調,進一步導致血栓形成[15]。凝血功能障礙在重癥感染中非常常見,其中APTT是臨床上最常用的反映內源性凝血系統凝血活性的敏感篩選試驗,它縮短表示血液處于高凝狀態,多見于血栓性疾病和血栓前狀態。雖然D-二聚體升高是血栓的敏感指標,但在本研究中敏感性卻較差,考慮研究中收集的相關實驗指標均為轉入ICU當天的數據結果,未動態對后續指標數據進行進一步分析,可能造成了一定偏倚。因此,動態隨訪治療過程中的各項血凝指標的變化可能會有不同的臨床意義[16]。
肺炎是一個的值得重視的健康問題,與高發病率、短期和長期病死率有關,也是全世界各年齡段人群死亡的主要傳染病病因[17]。本研究中CAP組和COVID-19組重癥肺炎患者的病死率均較高,分別高達44.3%和42.5%。再進一步對所有患者進行相關因素的Logistics模型ROC曲線分析得出,預測重癥肺炎患者死亡風險的預后指標為APACHEⅡ評分(AUC=0.77,95%CI 0.70~0.84)、VTE評分(AUC=0.61,95%CI 0.53~0.70)、肌酐(AUC=0.64,95%CI 0.56~0.73),而腎臟疾病的Kappa值為0.409(P<0.05),呈現中度一致性。APACHEⅡ評分自其問世以來,便以其簡便和可靠的特點備受醫學界的認可,其預測病死率的正確率達86%,在臨床上使用廣泛。國內學者黃澤波等[18]關于連續性腎臟替代治療治療重癥肺部感染相關膿毒癥患者預后路線圖模型的建立中,預測因素為高APACHEⅡ評分、內毒素水平以及低白蛋白水平等,與本研究結果相符合。本研究中重癥肺炎患者的VTE評分評估采用2018版《肺血栓栓塞癥診治與預防指南》[19]推薦的Padua評分。武漢新冠疫情流行期間,研究顯示Padua評分較高者的預后可能較差[16],可能作為新冠肺炎患者疾病嚴重程度和預后的相關指標之一;本研究結果與之相符合。重癥肺炎患者出現低氧、組織灌注不足,容易導致多器官功能障礙,往往早期出現急性腎功能不全,表現為尿少、肌酐升高、電解質紊亂等。張煒宗等[20]關于新冠患者院內死亡危險因素的分析指出,在合并癥中,發現腎臟疾病、腦卒中等是COVID-19 患者院內死亡的危險因素。在本研究中,兩個分組間病死率差異無統計學意義,考慮可能與部分COVID-19組患者早期使用特效藥物(包括Paxlovid、Molnupiravir等)可降低總體病死率有一定影響。在香港奧密克戎暴發期,Wong等[21]報告早期使用Molnupiravir或Paxlovid治療與死亡風險降低和住院后疾病進展風險降低顯著相關,Paxlovid治療還與住院風險降低顯著相關。Arbel等[22]研究顯示Paxlovid能夠顯著降低65歲及以上的老年人的住院風險或死亡風險。
本研究存在一定的局限性:研究對象為回顧性研究,部分數據存在丟失,資料收集難度大,影響結果偏倚;病例數量有限,樣本量不足夠大;因特殊時期普通病房未全面開展COVID-19感染患者對血栓事件的篩查,導致部分數據缺失,因而本研究未收集普通社區獲得性肺炎及非ICU住院COVID-19感染患者的相關資料進行分析,需進一步設計分組研究。
利益沖突:本研究不涉及任何利益沖突。