引用本文: 郭闖, 儲蘊, 張鳳香, 崔向飛. 重癥急性胰腺炎合并急性呼吸窘迫綜合征患者膀胱內壓與膈肌移動度的相關性及其對撤機結局的預測價值. 中國呼吸與危重監護雜志, 2024, 23(8): 563-568. doi: 10.7507/1671-6205.202402018 復制
版權信息: ?四川大學華西醫院華西期刊社《中國呼吸與危重監護雜志》版權所有,未經授權不得轉載、改編
重癥急性胰腺炎(severe acute pancreatitis,SAP)是一種非常嚴重的疾病,會對患者的生命構成威脅。它可以引發全身炎癥反應和多器官功能障礙,甚至導致器官衰竭,增加患者死亡風險。其中,肺部是全身炎癥反應的主要受影響器官之一[1]。由于炎癥因子的介導,肺部的微循環會受到障礙,同時線粒體和溶酶體膜的損傷也可能引發急性呼吸窘迫綜合征(acute respiratory distress syndrome,ARDS)。這些并發癥在重癥急性胰腺炎的早期階段最為嚴重和常見[2]。機械通氣可以顯著降低SAP合并ARDS患者的病死率,但使用過程中很容易導致呼吸機相關性肺炎和呼吸肌疲勞等問題。這些并發癥可能會導致患者難以順利脫離呼吸機。膈肌作為主要的呼吸肌肉,其運動的減少可能會影響患者的撤機結局。另外,膀胱內壓(intravesical pressure,IP)的增加和呼吸功能受限被認為是導致SAP患者撤機困難的重要因素之一。因此,了解IP與膈肌移動度(diaphragm excursion,DE)的相關性,并評估其對撤機結局的預測價值對于優化臨床管理和改善SAP合并ARDS患者的預后具有重要意義。
1 資料與方法
1.1 研究對象
回顧性分析2020年1月至2023年12月錦州醫科大學附屬第一醫院重癥醫學科收治的SAP合并ARDS患者的臨床資料。
1.1.1 納入標準
① 氣管插管;② 年齡>18歲;③ 機械通氣時間>24 h。
1.1.2 排除標準
① 神經肌肉疾病;② 脊髓損傷;③ 腹部術后;④ 胸部術后;⑤中途轉為氣管切開。
1.2 方法
1.2.1 IP測量
通過一次性膀胱壓力傳感器經導尿管測得IP。測量時患者需保持平臥位,還需要留意患者是否有呼吸窘迫情況,并記錄測量結果。
1.2.2 DE測量
通過床旁超聲測量每位患者的DE。在患者呼吸期間,通過超聲圖像觀察膈肌的收縮和舒張情況,并測量其運動范圍,記錄結果。
1.2.3 撤機結局
所有患者在撤機拔管前必須完成自主呼吸試驗、氣囊漏氣試驗等各項評估,并在撤機前測出IP與DE,并記錄結果。患者拔管撤機時間大于48 h視為成功,相反患者在48 h內重新插管上機視為失敗。根據撤機結果將患者分為成功組與失敗組,比較兩組患者的一般資料:性別、年齡、急性生理學與慢性健康狀況評分Ⅱ(acute physiological and chronic health evaluation Ⅱ,APACHEⅡ),以及撤機前測量IP與DE評分。
1.3 統計學處理
1.3.1 樣本量計算
預期的相關系數(r)為 0.6,設定顯著性水平(α)為 0.05,檢驗效能(1-β)為 0.8。使用相關性研究的樣本量計算公式: 。代入數值計算:需要至少約 102 個樣本。
。代入數值計算:需要至少約 102 個樣本。
1.3.2 采用SPSS25.0軟件對數據進行分析與處理
計量資料以均數±標準差(x±s)表示,采用獨立樣本t檢驗。使用二元Logistic回歸分析IP與DE是否為影響SAP患者撤機的危險因素,采用受試者工作特征曲線 (receiver?operator?characteristic?curve,ROC)分析IP和DE對SAP合并ARDS患者撤機結果的預測價值,采用Pearson相關分析IP和DE之間的相關性。P< 0.05為差異有統計學意義。
2 結果
2.1 一般資料
共納入144例SAP合并ARDS患者,其中撤機成功108例,失敗36例。兩組患者的性別、年齡、APACHEⅡ評分差異無統計學意義(P>0.05)。結果見表1。
2.2 兩組患者入ICU時及撤機前的氧合指數比較
兩組患者入ICU時的氧合指數異無統計學意義(P>0.05),失敗組患者撤機前氧合指數明顯低于成功組(P<0.05)。結果見表2。
2.3 兩組患者撤機前的IP和DE比較
失敗組患者IP明顯高于成功組,DE明顯低于成功組(均 P<0.05)。結果見表3。
2.4 影響SAP合并ARDS患者撤機的二元Logistic回歸分析
二元Logistic回歸分析顯示,IP和DE均為影響SAP合并ARDS患者撤機的獨立危險因素(均 P<0.05)。結果見表4。
2.5 IP和DE對SAP合并ARDS患者撤機結果的預測價值
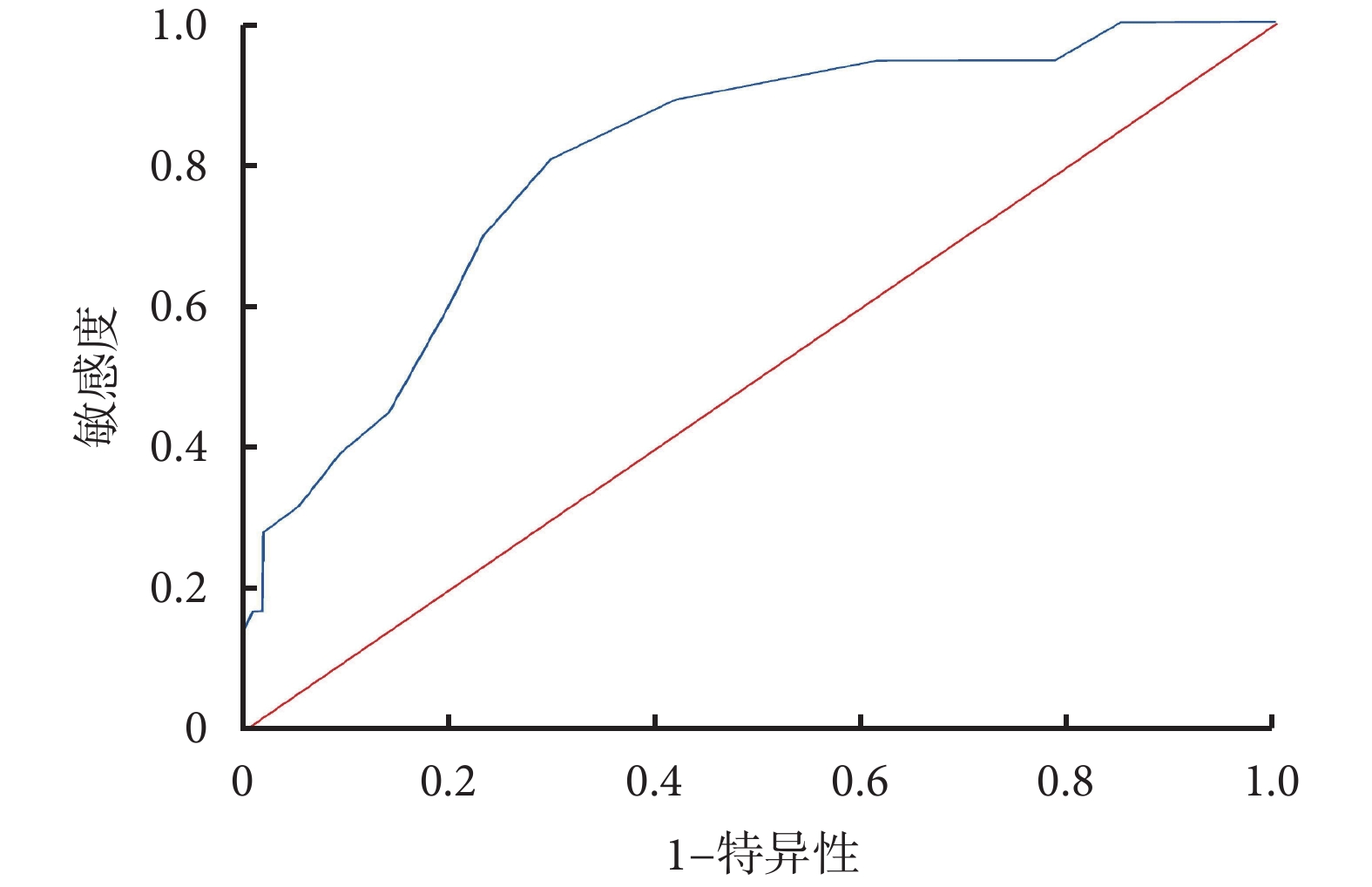
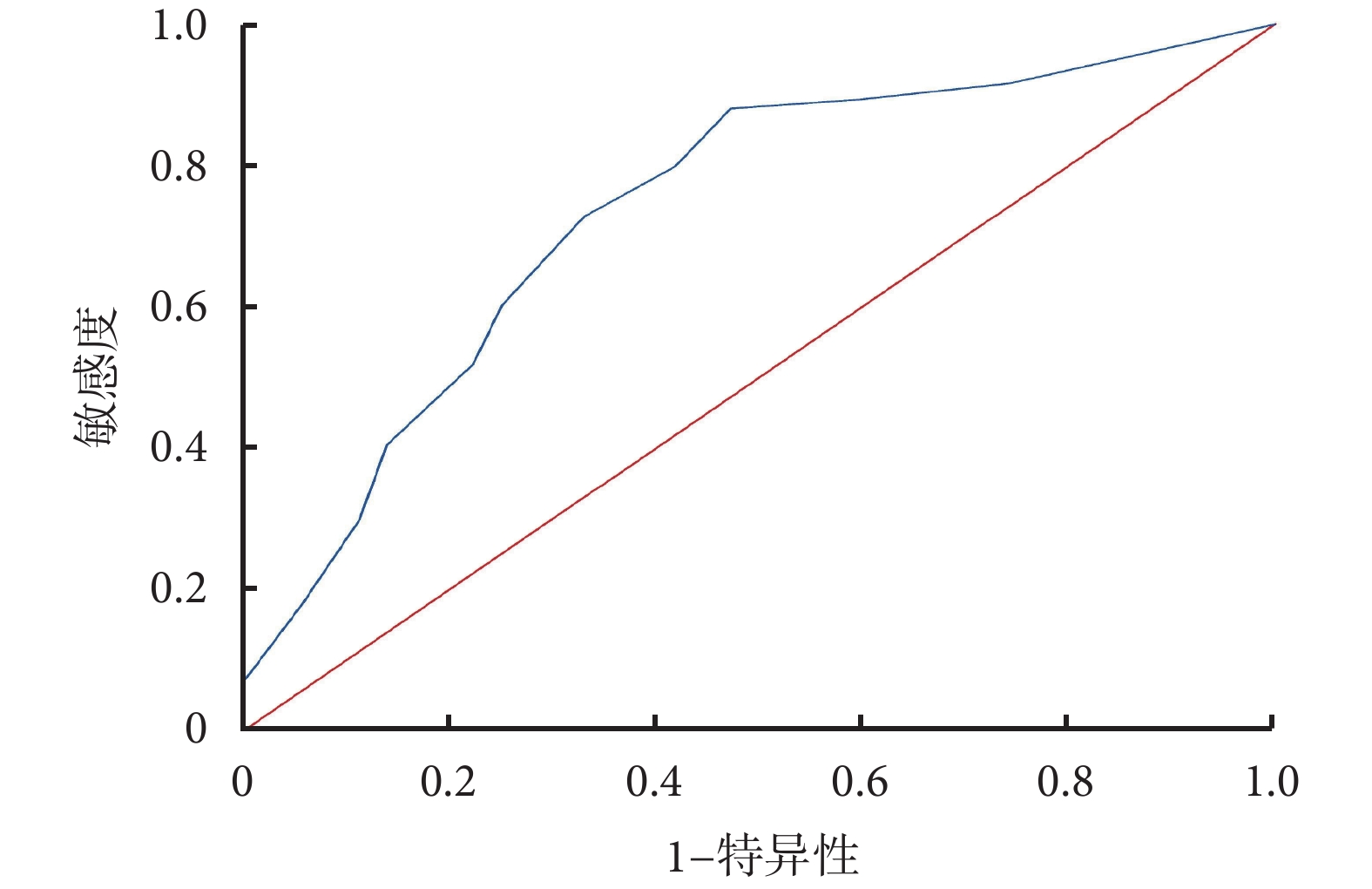
IP預測SAP合并ARDS患者撤機失敗的AUC>0.7,當截斷值為19.5 mmHg時敏感度為91.57%,特異度為47.54%;DE預測SAP合并ARDS患者撤機成功的AUC>0.7,當截斷值為11.5分時敏感度為84.82%,特異度為59.38%。結果見圖1、圖2、表5。
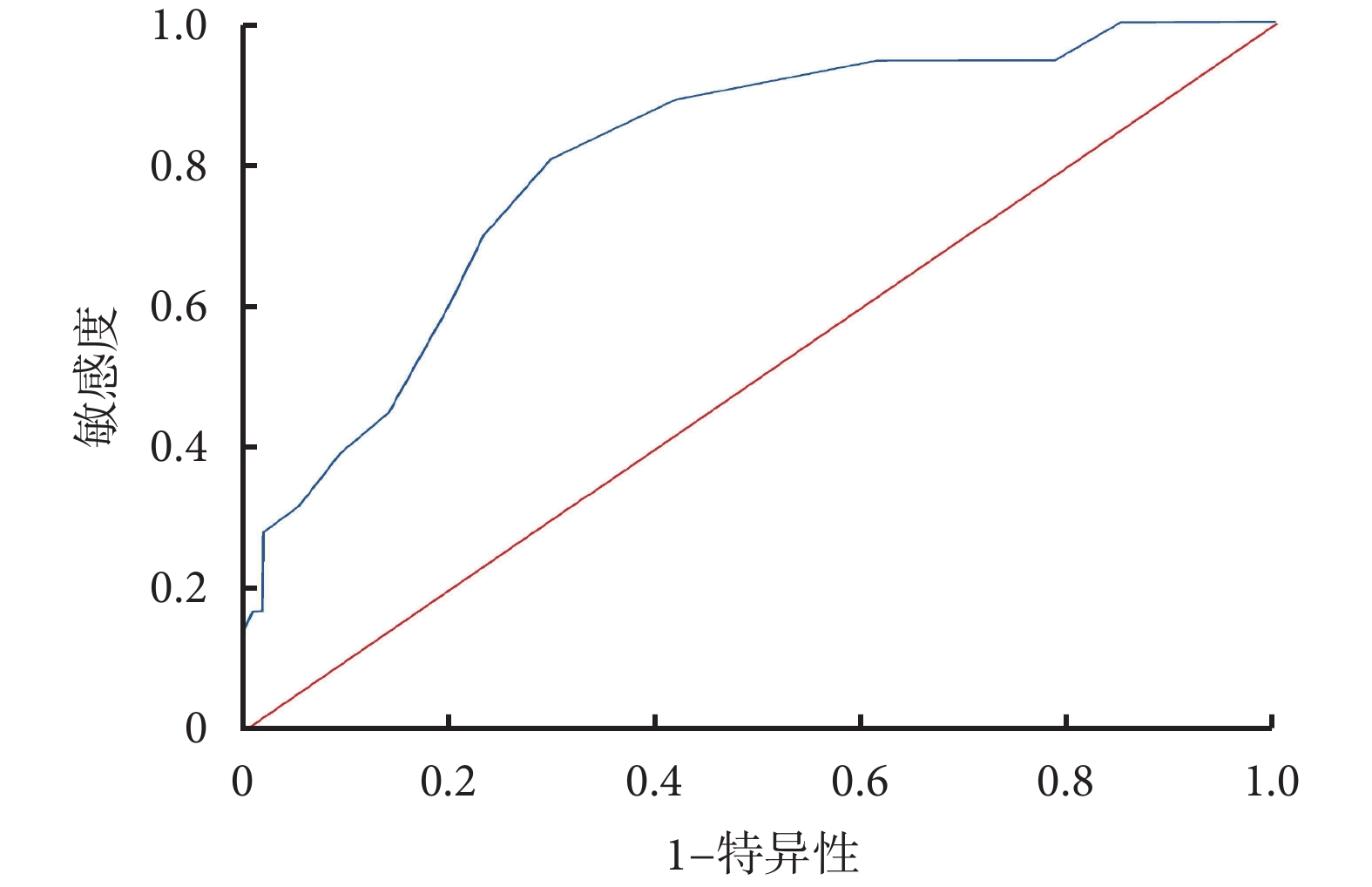 圖1
IP預測SAP合并ARDS患者撤機結果的ROC曲線
圖1
IP預測SAP合并ARDS患者撤機結果的ROC曲線
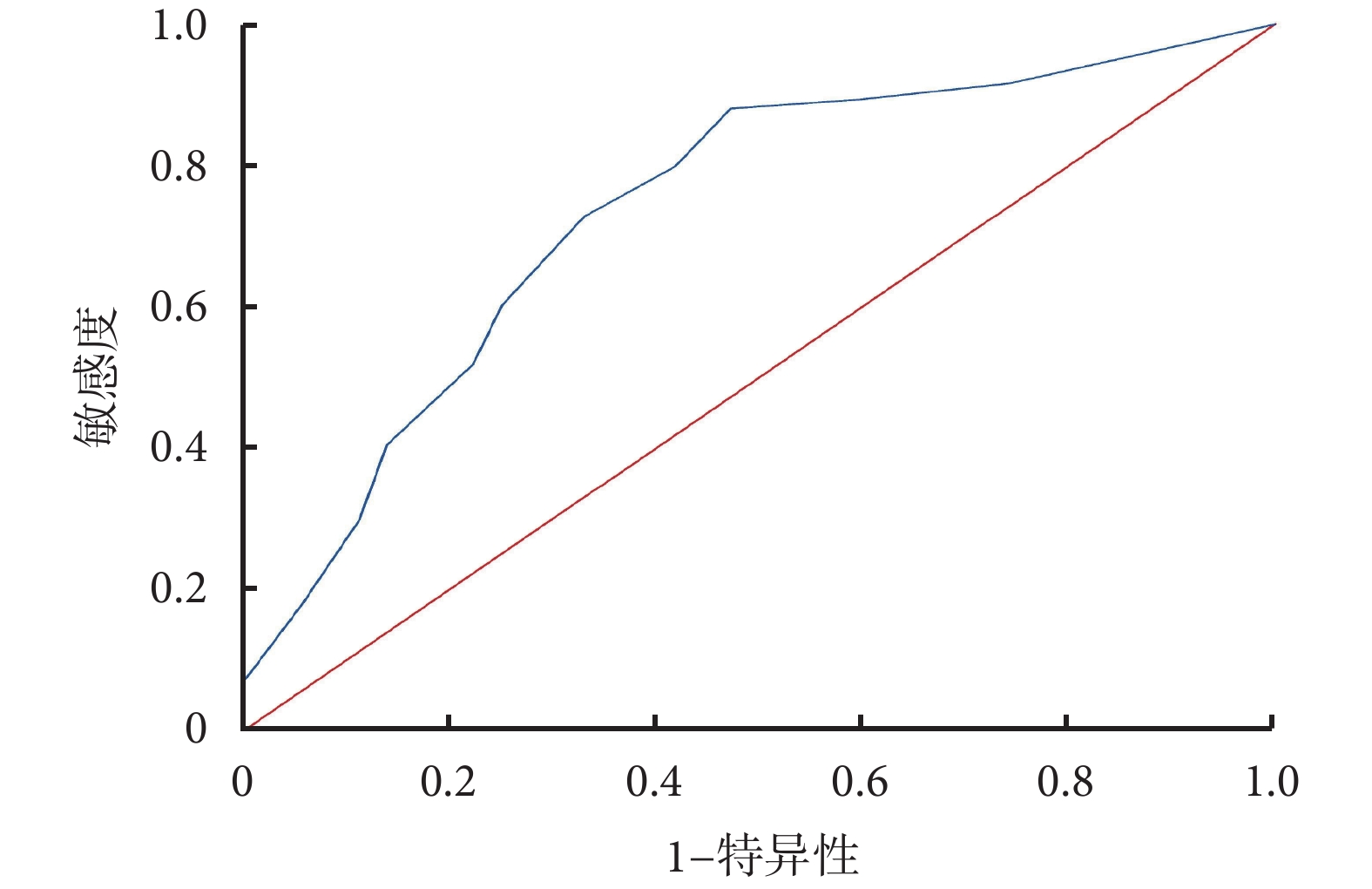 圖2
DE預測SAP合并ARDS患者撤機結果的ROC曲線
圖2
DE預測SAP合并ARDS患者撤機結果的ROC曲線
2.6 SAP合并ARDS患者撤機前IP和DE的相關性分析
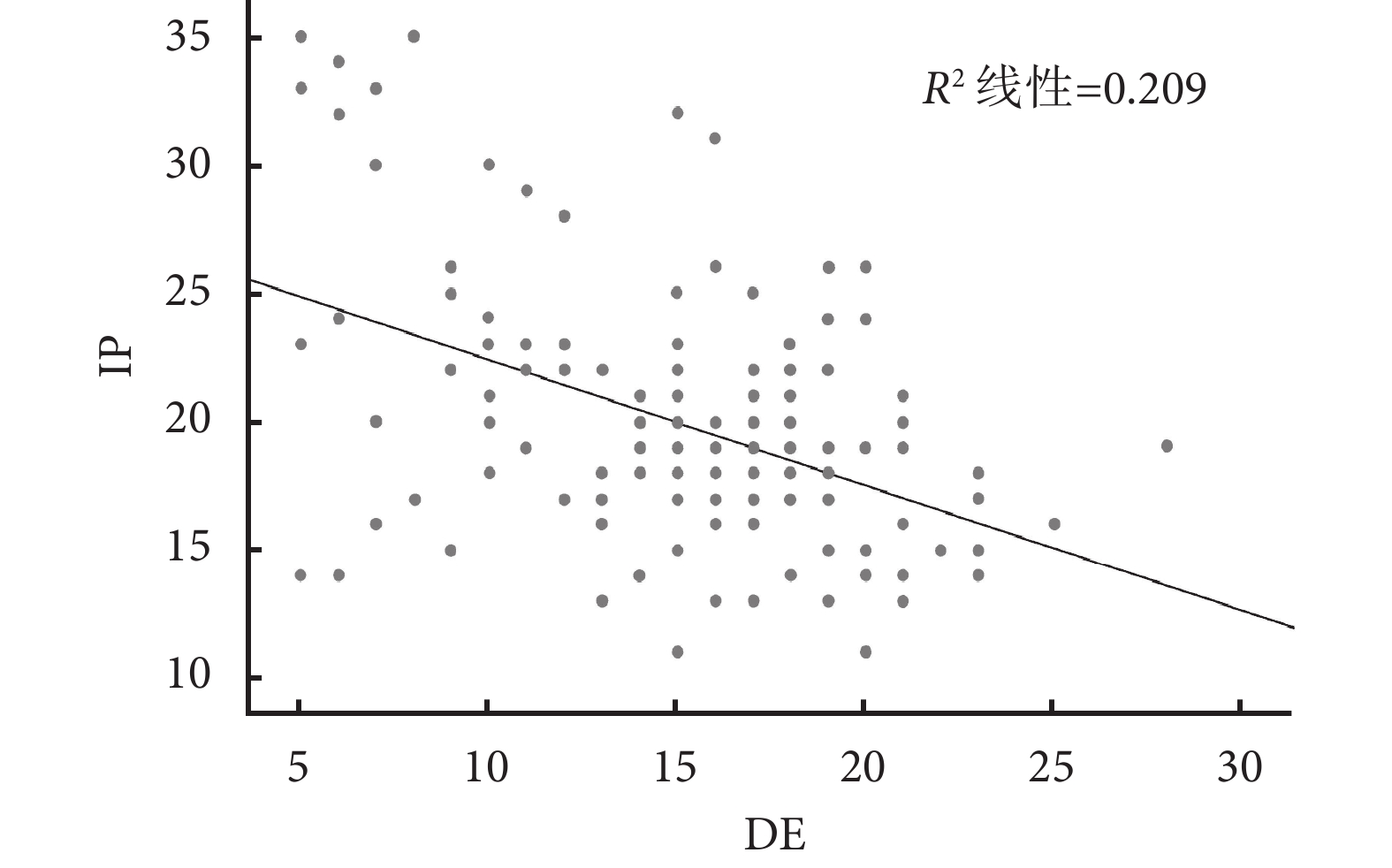
SAP合并ARDS患者撤機前IP和DE呈明顯負相關(r=–0.457,P<0.001)。結果見圖3。
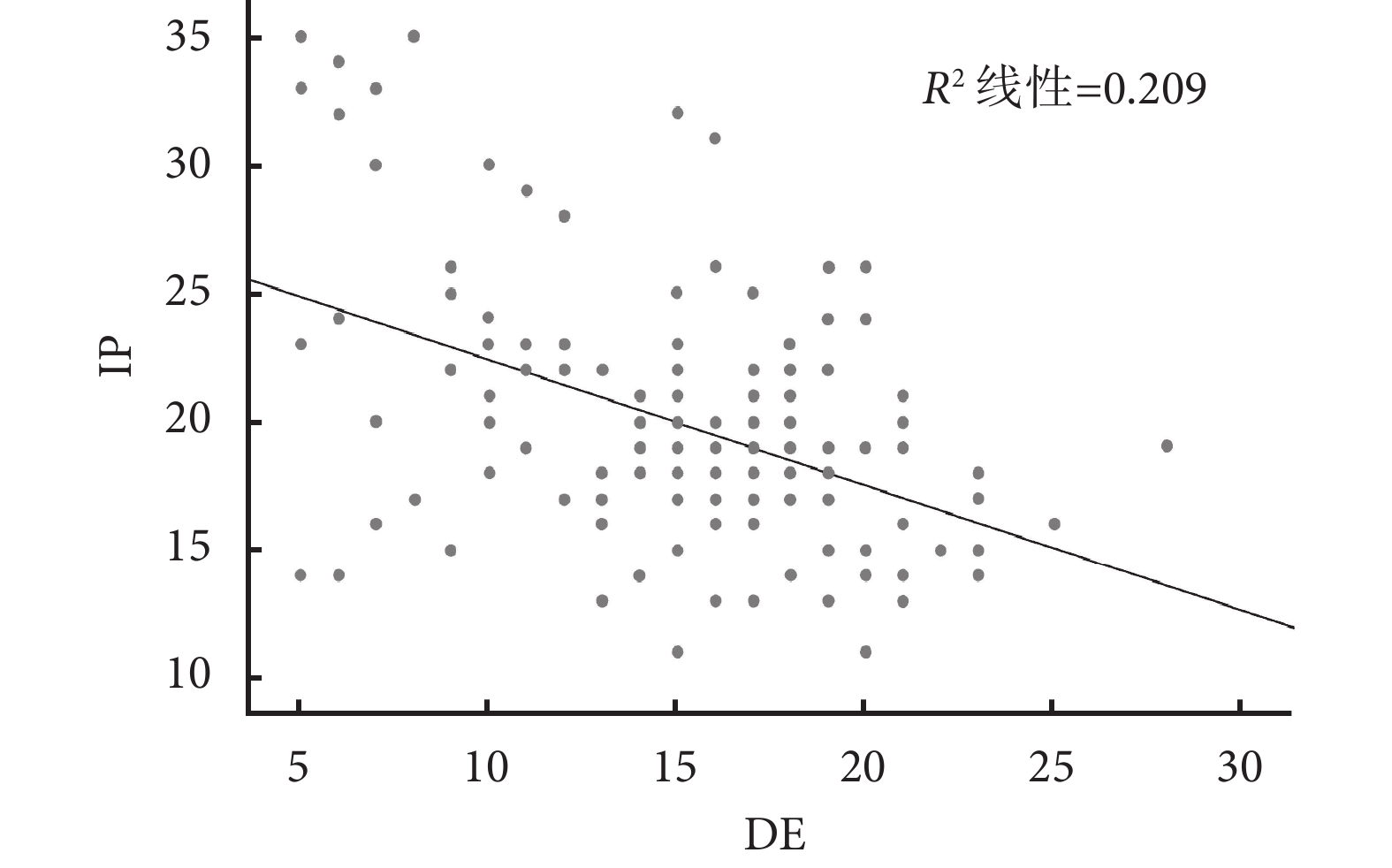 圖3
SAP合并ARDS患者撤機前IP和DE的相關性分析
圖3
SAP合并ARDS患者撤機前IP和DE的相關性分析
3 討論
ARDS 是 SAP 常見并發癥,是 SAP 患者死亡的重要原因之一。早期使用機械通氣治療可明顯降低ARDS患者的呼吸功,及時緩解呼吸窘迫狀態,可以有效糾正全身器官組織的嚴重缺氧,從而避免肺外重要器官受到嚴重損害。呼吸機能夠提供足夠的氧氣和維持適當的通氣,以確保全身組織得到充足的氧供,這有助于維持器官的正常功能,并降低因缺氧而引起的損傷。但機械通氣治療過程中會出現很多并發癥(如呼吸機相關性肺炎等),如不有效的預防和控制,會導致病死率增加。因此,當前的臨床實踐中主張在確保有效機械通氣治療的前提下,應盡量縮短機械通氣時間。長時間使用呼吸機可能導致膈肌的退化和功能受損。有研究指出[3],評估膈肌功能可以對撤機時機的選擇提供依據。膈肌是最主要也是最重要的呼吸肌之一,它負責控制呼吸運動。機械通氣的時間越長,患者對呼吸機也越依賴[4]。長時間依賴機械通氣可能導致膈肌的功能受損,使得膈肌的收縮能力出現障礙。這可能是由于膈肌長期處于不主動工作的狀態,逐漸失去了正常的張力和力量。因此,對于長時間通氣的患者,恢復和維護膈肌的功能至關重要,以確保他們能夠自主地進行呼吸。有研究表明[5],如果機械通氣時間超過 12 h,就會引起膈肌的退化和功能障礙,時間越長癥狀越重。膈肌在自主呼吸中不可或缺,因此在撤機的過程中,呼吸負荷過重和膈肌疲勞的情況經常出現[6]。所以,對于機械通氣患者來說監測膈肌功能尤為重要。通過觀察DE的減少,可以直觀地指示患者是否出現了膈肌疲勞或功能障礙[7]。膈肌功能障礙可出現在危重癥疾病早期,且其與撤機失敗及住院時間延長有關[8]。以往診斷膈肌功能障礙較困難,近年來,床旁超聲在重癥醫學領域應用十分廣泛,它在監測膈肌功能方面的應用也日益廣泛。通過超聲技術,醫生可以實時觀察和評估患者膈肌的收縮情況和運動模式,以便及時發現和監測膈肌的功能障礙。超聲技術在膈肌監測中的應用,可以提供非侵入性、可重復性和實時性的信息,有助于準確評估膈肌的收縮能力和運動情況。通過監測DE,如膈肌運動幅度和運動速度,醫生可以判斷膈肌功能是否正常,是否存在疲勞或障礙。這種基于超聲技術的膈肌監測方法,為醫生提供了更加可靠和直觀的指導,可以幫助他們更好地評估和管理機械通氣患者的膈肌功能,優化撤機過程,降低膈肌疲勞的風險,提高患者的呼吸能力和康復效果。超聲也被證實在預測術后并發癥、評估膈肌功能、指導撤機等方面均有重要價值[9]。超聲檢查可在床旁實時成像、無電離輻射、具有較好的可重復性[10],能夠方便、快速地為臨床醫師提供定量數據。Elshazly等[11]研究發現 DE 與 APACHE Ⅱ具有良好的相關性,表明隨著患者病情加重,DE 降低,因此可以根據 DE 動態評估患者病情。基于此,本研究探討了SAP合并ARDS患者DE 預測撤機風險的臨床價值。DE 為呼吸周期中膈肌的位移,反映了膈肌收縮的幅度,DE 越低提示膈肌收縮力越差,即膈肌功能障礙越嚴重;DE 的降低導致肺通氣不足,加重了患者呼吸衰竭程度。感染導致機體釋放大量促炎因子,進而增加了毛細血管的通透性,加重微循環障礙,損傷膈肌細胞,影響肌肉收縮功能,馬金蘭等[12]研究發現膿毒癥及感染性休克患者 DE 與超敏 C 反蛋白和白細胞介素-6 均呈負相關,表明炎癥反應強度與膈肌功能障礙程度相關;另一方面,促炎因子激活蛋白水解途徑,引起收縮蛋白減少,導致膈肌無力[13]。
SAP的病情進展快,并發癥多,患者可能出現嚴重的腹膜后水腫、腹水、痙攣性腸梗阻或胃腸道出血,這些情況有可能導致腹內壓升高,甚至發展為腹腔間室綜合征(abdominal compartment syndrome ,ACS)。腹內壓(intra-abdominal pressure,IAP)在SAP患者的臨床監測中具有重要意義。高IAP可能加重腸道黏膜屏障功能障礙,導致腸道黏膜組織受損,且受損的程度與高IAP呈正相關。高IAP還可能直接或間接導致其他器官功能障礙。IAP與呼吸功能之間存在雙向影響,高IAP受氣道壓力、呼氣末正壓、呼吸機模式等因素影響,同時也會影響氣道峰壓、吸入氧濃度、呼氣末肺容積等指標,但氣道壓力對高IAP的影響很小[14]。高IAP可能暫時導致膈肌上抬,胸腔壓力增加,肺容積減少,肺的順應性下降,最終可能導致呼吸功能衰竭[15]。SAP是一種病情險惡、并發癥多、病死率高的急腹癥,屬急性胰腺炎特殊類型,亦是導致IAP增高,引發ACS的主要原因之一。ACS由于其發病具有隱匿性,容易被人們所忽視而不能及時給予治療,從而增加患者病死率。 由于IAP 與IP具有良好相關性,因此持續監測IP對早期發現 ACS具有重要意義。當持續IAP>20 mmHg伴(或不伴)<60 mmHg的腹腔灌注壓,且當新的器官功能不全或衰竭出現時,被定義為ACS。SAP并發ACS的情況下,病情發展速度快,若未及時處理,病死率約在50%至75%之間[16]。因此,針對SAP的科學有效的臨床護理和IAP監測變得越來越重要。研究顯示[17],IAP與IP有著良好的相關性,IP成為一種實用而簡單的測量IAP的可靠方法。持續監測IP是早期發現ACS的“金標準”。研究還表明[18],IAP逐步下降提示病情和預后有所改善,而持續維持較高水平甚至不斷上升則提示病情惡化。目前研究認為[19],IAP的變化直接影響SAP的治療和預后,SAP的嚴重程度與IAP、ACS的發生呈正相關。IP監測有助于及時發現IAP升高,醫生可以根據IAP升高的情況盡早進行干預。IP測定是一種可靠的監測IAP的方法,在臨床應用較為廣泛,IAP與IP之間存在良好的相關性[20],可提早發現ACS,改善對SAP患者的治療效果。因此,本研究探討了SAP合并ARDS患者IP預測撤機風險的臨床價值,并發現IP可以很好的預測SAP合并ARDS患者的撤機結果,同時本研究結果表明,IP與DE之間存在顯著負相關性。這意味著當IP增加時,膈肌的運動范圍減少,這可能是由于IP增加導致膈肌受限,影響了患者的呼吸功能,患者的撤機成功率較低。這種負相關性的發現提醒臨床醫生在治療SAP時需要重視IP的監測,并留意患者膈肌運動的情況。因此,通過監測IP與DE,可以幫助臨床醫生更好地了解患者的情況,提供決策支持和指導,以便更具信心地決定是否進行撤機,并更好地管理和優化患者的呼吸機治療過程。
綜上所述,IP監測和DE評估是評估SAP合并ARDS患者撤機能力的可行方法,且IP與DE之間存在顯著負相關性。通過監測和評估這些指標,臨床醫生可以更好地預測撤機成功率,并作出相應的處理措施,調整治療方案,以提高撤機成功率。然而,進一步的研究仍需要彌補當前研究的一些限制。首先,由于本研究采用了回顧性設計,存在信息偏倚和回顧性誤差的可能性。后續的前瞻性研究應該考慮更大的樣本量,以增加結果的可靠性和泛化能力。其次,IP和DE只是影響撤機的多個因素之一,如肺部狀況和患者整體肺功能等因素也需要考慮進來。進一步的研究可以探索如何綜合考慮這些因素,從而提高撤機預測的準確性和指導治療決策的精確度。此外,相關研究還應探索IP和DE與撤機結局之間的因果關系。雖然我們的研究發現了這兩個指標的相關性,但我們無法確定哪個是因,哪個是果。進一步的實驗研究可以通過干預IP和DE,如通過IP控制和膈肌訓練等方式,來驗證這種關系。這將有助于更好地理解IP和DE對撤機結局的影響機制,并為臨床提供更加優化的干預策略。因而,進一步的研究仍然是必要的,進一步的研究應該努力彌補當前研究的限制,并探索更精確、可靠的指標和方法,以指導臨床決策并提高撤機的成功率和患者預后,以驗證這些結果并確定最佳的治療策略。
利益沖突:本研究不涉及任何利益沖突
重癥急性胰腺炎(severe acute pancreatitis,SAP)是一種非常嚴重的疾病,會對患者的生命構成威脅。它可以引發全身炎癥反應和多器官功能障礙,甚至導致器官衰竭,增加患者死亡風險。其中,肺部是全身炎癥反應的主要受影響器官之一[1]。由于炎癥因子的介導,肺部的微循環會受到障礙,同時線粒體和溶酶體膜的損傷也可能引發急性呼吸窘迫綜合征(acute respiratory distress syndrome,ARDS)。這些并發癥在重癥急性胰腺炎的早期階段最為嚴重和常見[2]。機械通氣可以顯著降低SAP合并ARDS患者的病死率,但使用過程中很容易導致呼吸機相關性肺炎和呼吸肌疲勞等問題。這些并發癥可能會導致患者難以順利脫離呼吸機。膈肌作為主要的呼吸肌肉,其運動的減少可能會影響患者的撤機結局。另外,膀胱內壓(intravesical pressure,IP)的增加和呼吸功能受限被認為是導致SAP患者撤機困難的重要因素之一。因此,了解IP與膈肌移動度(diaphragm excursion,DE)的相關性,并評估其對撤機結局的預測價值對于優化臨床管理和改善SAP合并ARDS患者的預后具有重要意義。
1 資料與方法
1.1 研究對象
回顧性分析2020年1月至2023年12月錦州醫科大學附屬第一醫院重癥醫學科收治的SAP合并ARDS患者的臨床資料。
1.1.1 納入標準
① 氣管插管;② 年齡>18歲;③ 機械通氣時間>24 h。
1.1.2 排除標準
① 神經肌肉疾病;② 脊髓損傷;③ 腹部術后;④ 胸部術后;⑤中途轉為氣管切開。
1.2 方法
1.2.1 IP測量
通過一次性膀胱壓力傳感器經導尿管測得IP。測量時患者需保持平臥位,還需要留意患者是否有呼吸窘迫情況,并記錄測量結果。
1.2.2 DE測量
通過床旁超聲測量每位患者的DE。在患者呼吸期間,通過超聲圖像觀察膈肌的收縮和舒張情況,并測量其運動范圍,記錄結果。
1.2.3 撤機結局
所有患者在撤機拔管前必須完成自主呼吸試驗、氣囊漏氣試驗等各項評估,并在撤機前測出IP與DE,并記錄結果。患者拔管撤機時間大于48 h視為成功,相反患者在48 h內重新插管上機視為失敗。根據撤機結果將患者分為成功組與失敗組,比較兩組患者的一般資料:性別、年齡、急性生理學與慢性健康狀況評分Ⅱ(acute physiological and chronic health evaluation Ⅱ,APACHEⅡ),以及撤機前測量IP與DE評分。
1.3 統計學處理
1.3.1 樣本量計算
預期的相關系數(r)為 0.6,設定顯著性水平(α)為 0.05,檢驗效能(1-β)為 0.8。使用相關性研究的樣本量計算公式: 。代入數值計算:需要至少約 102 個樣本。
。代入數值計算:需要至少約 102 個樣本。
1.3.2 采用SPSS25.0軟件對數據進行分析與處理
計量資料以均數±標準差(x±s)表示,采用獨立樣本t檢驗。使用二元Logistic回歸分析IP與DE是否為影響SAP患者撤機的危險因素,采用受試者工作特征曲線 (receiver?operator?characteristic?curve,ROC)分析IP和DE對SAP合并ARDS患者撤機結果的預測價值,采用Pearson相關分析IP和DE之間的相關性。P< 0.05為差異有統計學意義。
2 結果
2.1 一般資料
共納入144例SAP合并ARDS患者,其中撤機成功108例,失敗36例。兩組患者的性別、年齡、APACHEⅡ評分差異無統計學意義(P>0.05)。結果見表1。
2.2 兩組患者入ICU時及撤機前的氧合指數比較
兩組患者入ICU時的氧合指數異無統計學意義(P>0.05),失敗組患者撤機前氧合指數明顯低于成功組(P<0.05)。結果見表2。
2.3 兩組患者撤機前的IP和DE比較
失敗組患者IP明顯高于成功組,DE明顯低于成功組(均 P<0.05)。結果見表3。
2.4 影響SAP合并ARDS患者撤機的二元Logistic回歸分析
二元Logistic回歸分析顯示,IP和DE均為影響SAP合并ARDS患者撤機的獨立危險因素(均 P<0.05)。結果見表4。
2.5 IP和DE對SAP合并ARDS患者撤機結果的預測價值
IP預測SAP合并ARDS患者撤機失敗的AUC>0.7,當截斷值為19.5 mmHg時敏感度為91.57%,特異度為47.54%;DE預測SAP合并ARDS患者撤機成功的AUC>0.7,當截斷值為11.5分時敏感度為84.82%,特異度為59.38%。結果見圖1、圖2、表5。
 圖1
IP預測SAP合并ARDS患者撤機結果的ROC曲線
圖1
IP預測SAP合并ARDS患者撤機結果的ROC曲線
 圖2
DE預測SAP合并ARDS患者撤機結果的ROC曲線
圖2
DE預測SAP合并ARDS患者撤機結果的ROC曲線
2.6 SAP合并ARDS患者撤機前IP和DE的相關性分析
SAP合并ARDS患者撤機前IP和DE呈明顯負相關(r=–0.457,P<0.001)。結果見圖3。
 圖3
SAP合并ARDS患者撤機前IP和DE的相關性分析
圖3
SAP合并ARDS患者撤機前IP和DE的相關性分析
3 討論
ARDS 是 SAP 常見并發癥,是 SAP 患者死亡的重要原因之一。早期使用機械通氣治療可明顯降低ARDS患者的呼吸功,及時緩解呼吸窘迫狀態,可以有效糾正全身器官組織的嚴重缺氧,從而避免肺外重要器官受到嚴重損害。呼吸機能夠提供足夠的氧氣和維持適當的通氣,以確保全身組織得到充足的氧供,這有助于維持器官的正常功能,并降低因缺氧而引起的損傷。但機械通氣治療過程中會出現很多并發癥(如呼吸機相關性肺炎等),如不有效的預防和控制,會導致病死率增加。因此,當前的臨床實踐中主張在確保有效機械通氣治療的前提下,應盡量縮短機械通氣時間。長時間使用呼吸機可能導致膈肌的退化和功能受損。有研究指出[3],評估膈肌功能可以對撤機時機的選擇提供依據。膈肌是最主要也是最重要的呼吸肌之一,它負責控制呼吸運動。機械通氣的時間越長,患者對呼吸機也越依賴[4]。長時間依賴機械通氣可能導致膈肌的功能受損,使得膈肌的收縮能力出現障礙。這可能是由于膈肌長期處于不主動工作的狀態,逐漸失去了正常的張力和力量。因此,對于長時間通氣的患者,恢復和維護膈肌的功能至關重要,以確保他們能夠自主地進行呼吸。有研究表明[5],如果機械通氣時間超過 12 h,就會引起膈肌的退化和功能障礙,時間越長癥狀越重。膈肌在自主呼吸中不可或缺,因此在撤機的過程中,呼吸負荷過重和膈肌疲勞的情況經常出現[6]。所以,對于機械通氣患者來說監測膈肌功能尤為重要。通過觀察DE的減少,可以直觀地指示患者是否出現了膈肌疲勞或功能障礙[7]。膈肌功能障礙可出現在危重癥疾病早期,且其與撤機失敗及住院時間延長有關[8]。以往診斷膈肌功能障礙較困難,近年來,床旁超聲在重癥醫學領域應用十分廣泛,它在監測膈肌功能方面的應用也日益廣泛。通過超聲技術,醫生可以實時觀察和評估患者膈肌的收縮情況和運動模式,以便及時發現和監測膈肌的功能障礙。超聲技術在膈肌監測中的應用,可以提供非侵入性、可重復性和實時性的信息,有助于準確評估膈肌的收縮能力和運動情況。通過監測DE,如膈肌運動幅度和運動速度,醫生可以判斷膈肌功能是否正常,是否存在疲勞或障礙。這種基于超聲技術的膈肌監測方法,為醫生提供了更加可靠和直觀的指導,可以幫助他們更好地評估和管理機械通氣患者的膈肌功能,優化撤機過程,降低膈肌疲勞的風險,提高患者的呼吸能力和康復效果。超聲也被證實在預測術后并發癥、評估膈肌功能、指導撤機等方面均有重要價值[9]。超聲檢查可在床旁實時成像、無電離輻射、具有較好的可重復性[10],能夠方便、快速地為臨床醫師提供定量數據。Elshazly等[11]研究發現 DE 與 APACHE Ⅱ具有良好的相關性,表明隨著患者病情加重,DE 降低,因此可以根據 DE 動態評估患者病情。基于此,本研究探討了SAP合并ARDS患者DE 預測撤機風險的臨床價值。DE 為呼吸周期中膈肌的位移,反映了膈肌收縮的幅度,DE 越低提示膈肌收縮力越差,即膈肌功能障礙越嚴重;DE 的降低導致肺通氣不足,加重了患者呼吸衰竭程度。感染導致機體釋放大量促炎因子,進而增加了毛細血管的通透性,加重微循環障礙,損傷膈肌細胞,影響肌肉收縮功能,馬金蘭等[12]研究發現膿毒癥及感染性休克患者 DE 與超敏 C 反蛋白和白細胞介素-6 均呈負相關,表明炎癥反應強度與膈肌功能障礙程度相關;另一方面,促炎因子激活蛋白水解途徑,引起收縮蛋白減少,導致膈肌無力[13]。
SAP的病情進展快,并發癥多,患者可能出現嚴重的腹膜后水腫、腹水、痙攣性腸梗阻或胃腸道出血,這些情況有可能導致腹內壓升高,甚至發展為腹腔間室綜合征(abdominal compartment syndrome ,ACS)。腹內壓(intra-abdominal pressure,IAP)在SAP患者的臨床監測中具有重要意義。高IAP可能加重腸道黏膜屏障功能障礙,導致腸道黏膜組織受損,且受損的程度與高IAP呈正相關。高IAP還可能直接或間接導致其他器官功能障礙。IAP與呼吸功能之間存在雙向影響,高IAP受氣道壓力、呼氣末正壓、呼吸機模式等因素影響,同時也會影響氣道峰壓、吸入氧濃度、呼氣末肺容積等指標,但氣道壓力對高IAP的影響很小[14]。高IAP可能暫時導致膈肌上抬,胸腔壓力增加,肺容積減少,肺的順應性下降,最終可能導致呼吸功能衰竭[15]。SAP是一種病情險惡、并發癥多、病死率高的急腹癥,屬急性胰腺炎特殊類型,亦是導致IAP增高,引發ACS的主要原因之一。ACS由于其發病具有隱匿性,容易被人們所忽視而不能及時給予治療,從而增加患者病死率。 由于IAP 與IP具有良好相關性,因此持續監測IP對早期發現 ACS具有重要意義。當持續IAP>20 mmHg伴(或不伴)<60 mmHg的腹腔灌注壓,且當新的器官功能不全或衰竭出現時,被定義為ACS。SAP并發ACS的情況下,病情發展速度快,若未及時處理,病死率約在50%至75%之間[16]。因此,針對SAP的科學有效的臨床護理和IAP監測變得越來越重要。研究顯示[17],IAP與IP有著良好的相關性,IP成為一種實用而簡單的測量IAP的可靠方法。持續監測IP是早期發現ACS的“金標準”。研究還表明[18],IAP逐步下降提示病情和預后有所改善,而持續維持較高水平甚至不斷上升則提示病情惡化。目前研究認為[19],IAP的變化直接影響SAP的治療和預后,SAP的嚴重程度與IAP、ACS的發生呈正相關。IP監測有助于及時發現IAP升高,醫生可以根據IAP升高的情況盡早進行干預。IP測定是一種可靠的監測IAP的方法,在臨床應用較為廣泛,IAP與IP之間存在良好的相關性[20],可提早發現ACS,改善對SAP患者的治療效果。因此,本研究探討了SAP合并ARDS患者IP預測撤機風險的臨床價值,并發現IP可以很好的預測SAP合并ARDS患者的撤機結果,同時本研究結果表明,IP與DE之間存在顯著負相關性。這意味著當IP增加時,膈肌的運動范圍減少,這可能是由于IP增加導致膈肌受限,影響了患者的呼吸功能,患者的撤機成功率較低。這種負相關性的發現提醒臨床醫生在治療SAP時需要重視IP的監測,并留意患者膈肌運動的情況。因此,通過監測IP與DE,可以幫助臨床醫生更好地了解患者的情況,提供決策支持和指導,以便更具信心地決定是否進行撤機,并更好地管理和優化患者的呼吸機治療過程。
綜上所述,IP監測和DE評估是評估SAP合并ARDS患者撤機能力的可行方法,且IP與DE之間存在顯著負相關性。通過監測和評估這些指標,臨床醫生可以更好地預測撤機成功率,并作出相應的處理措施,調整治療方案,以提高撤機成功率。然而,進一步的研究仍需要彌補當前研究的一些限制。首先,由于本研究采用了回顧性設計,存在信息偏倚和回顧性誤差的可能性。后續的前瞻性研究應該考慮更大的樣本量,以增加結果的可靠性和泛化能力。其次,IP和DE只是影響撤機的多個因素之一,如肺部狀況和患者整體肺功能等因素也需要考慮進來。進一步的研究可以探索如何綜合考慮這些因素,從而提高撤機預測的準確性和指導治療決策的精確度。此外,相關研究還應探索IP和DE與撤機結局之間的因果關系。雖然我們的研究發現了這兩個指標的相關性,但我們無法確定哪個是因,哪個是果。進一步的實驗研究可以通過干預IP和DE,如通過IP控制和膈肌訓練等方式,來驗證這種關系。這將有助于更好地理解IP和DE對撤機結局的影響機制,并為臨床提供更加優化的干預策略。因而,進一步的研究仍然是必要的,進一步的研究應該努力彌補當前研究的限制,并探索更精確、可靠的指標和方法,以指導臨床決策并提高撤機的成功率和患者預后,以驗證這些結果并確定最佳的治療策略。
利益沖突:本研究不涉及任何利益沖突