引用本文: 何權瀛. 對于慢性支氣管炎、肺氣腫和支氣管哮喘三環圖的一些困惑. 中國呼吸與危重監護雜志, 2024, 23(8): 533-536. doi: 10.7507/1671-6205.202407129 復制
版權信息: ?四川大學華西醫院華西期刊社《中國呼吸與危重監護雜志》版權所有,未經授權不得轉載、改編
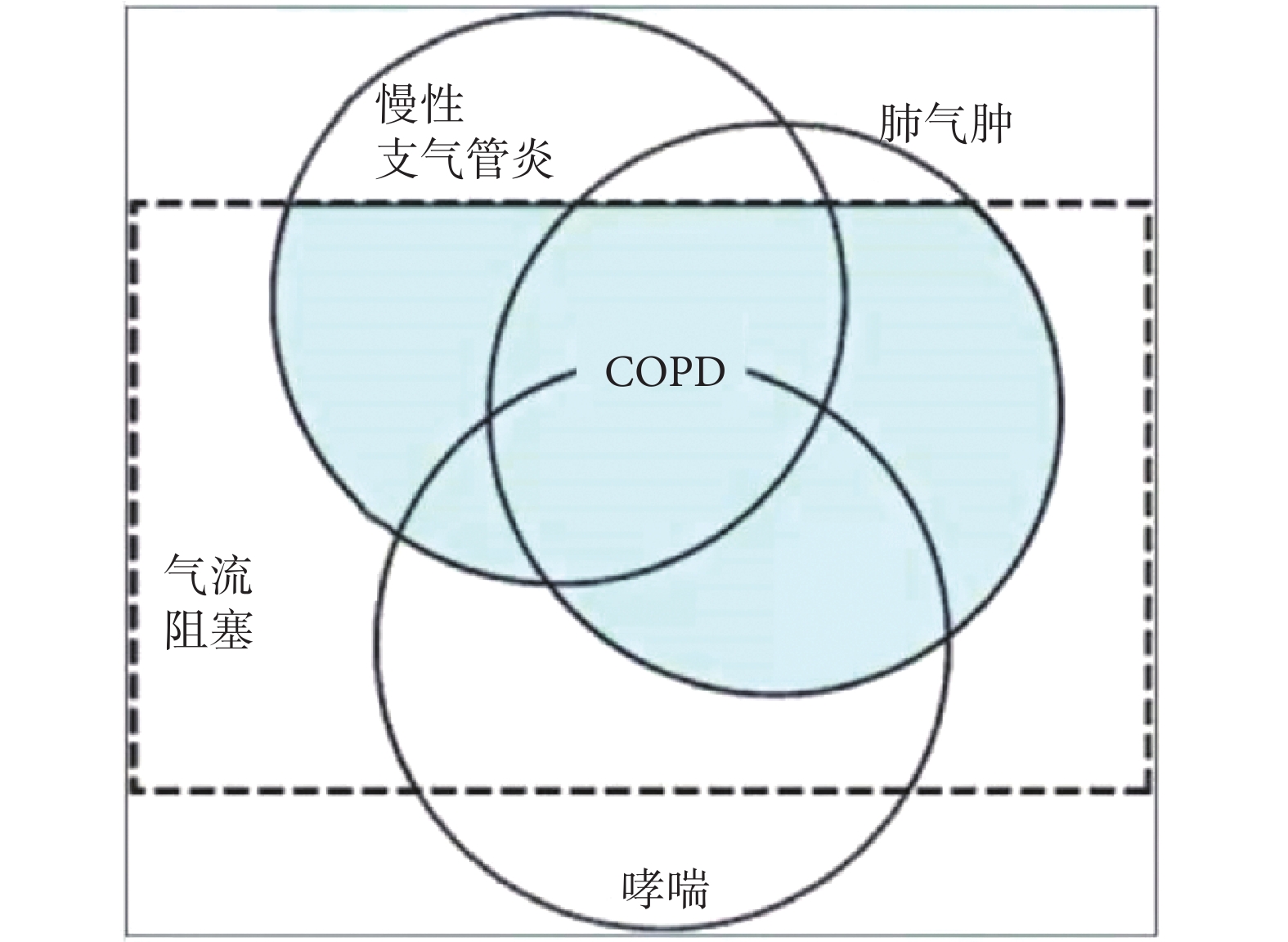
長期以來(1995年起)人們一直習慣用三環圖(圖1)來表示慢性支氣管炎、肺氣腫與支氣管哮喘以及慢阻肺的關系[1],對此很少有人提出異議。然而近幾年筆者發現這個圖形有很多令人質疑之處,故不揣冒昧,對此提出以下問題,希望與大家一起討論。
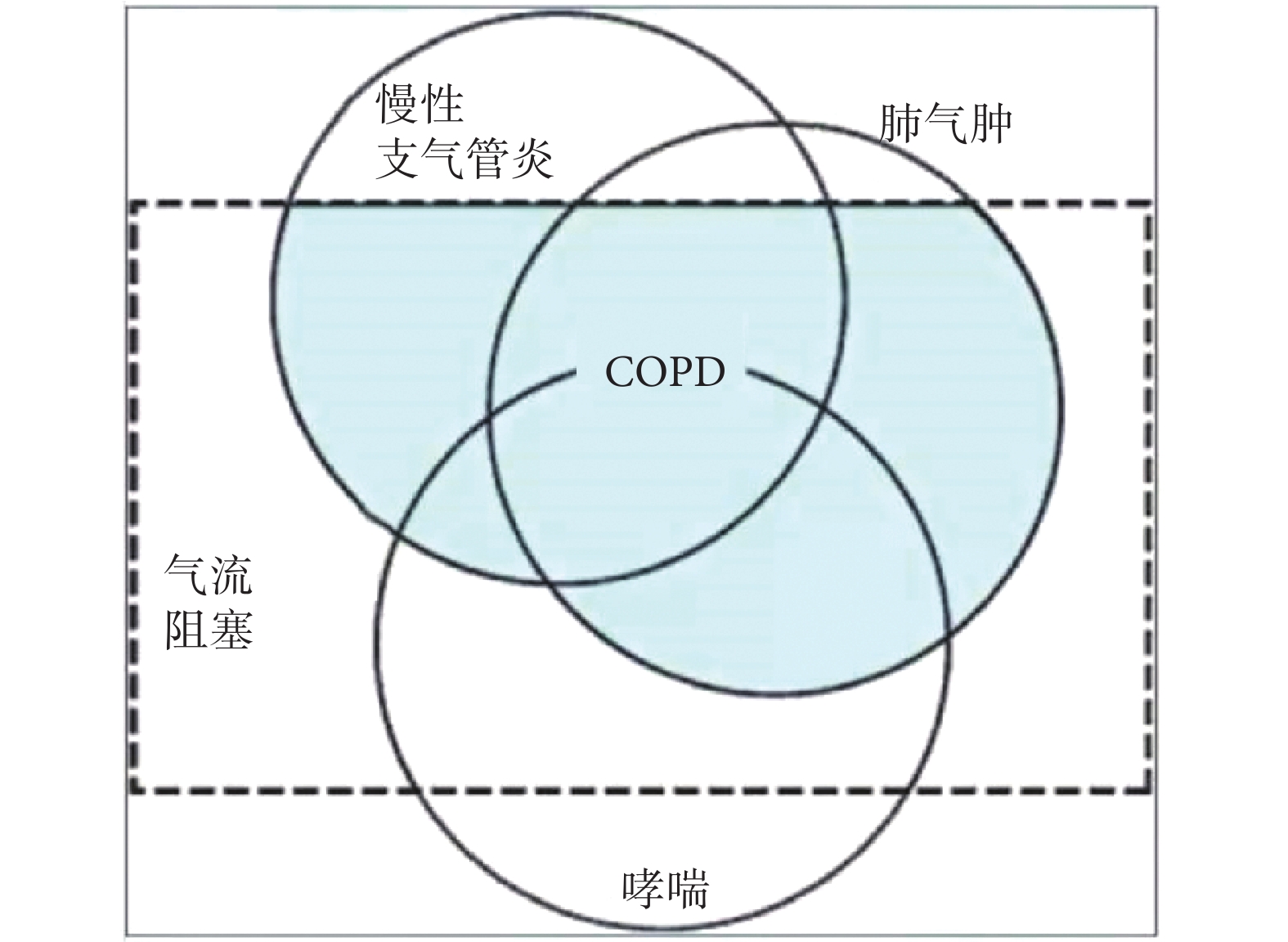 圖1
慢性支氣管炎、肺氣腫、支氣管哮喘、慢阻肺的關系(Am J Respir Crit Care Med. 1995 Nov;152(5 Pt 2):S77-121)
圖1
慢性支氣管炎、肺氣腫、支氣管哮喘、慢阻肺的關系(Am J Respir Crit Care Med. 1995 Nov;152(5 Pt 2):S77-121)
1 支氣管哮喘進入氣流受限不可逆階段還是哮喘嗎?
通常認為氣流受限具有可逆性是哮喘有別于慢阻肺的重要特征。眾所周知,支氣管哮喘的三種主要病理改變分別為氣道炎癥、平滑肌功能障礙和氣道重塑。所謂氣道重塑主要為氣道上皮纖維化、平滑肌增生、血管新生、黏液腺肥大、黏液高分泌和氣道水腫。其中黏液高分泌、氣道水腫尚屬可逆成分,然而上皮纖維化、平滑肌增生、血管新生以及黏液腺肥大則屬于不可逆成分,即一旦發生氣道重塑,其氣流受限就會變為不可逆[2]。那么哮喘患者一旦其氣流受限由可逆轉變為不可逆階段,那它還屬于支氣管哮喘嗎?有學者認為哮喘患者即使由于氣道重塑,氣流受限由可逆變為不可逆,仍舊屬于哮喘,只是進入了哮喘的后期。但是也有學者認為既然其氣流受限進入不可逆階段,那便應當屬于慢阻肺。因為慢阻肺的定義和診斷標準之一就是氣流受限為不可逆。既然由于氣道重塑,哮喘患者的氣流受限已進入不可逆階段,那它與慢阻肺就沒有什么不同了。近年來GOLD一直認為哮喘本身也是慢阻肺的發病危險因素之一[3],所以,哮喘患者一旦出現氣流受限不可逆,就應該按照慢阻肺進行治療,不知你怎么看待這個問題?
2 支氣管哮喘與肺氣腫不可能發生重疊
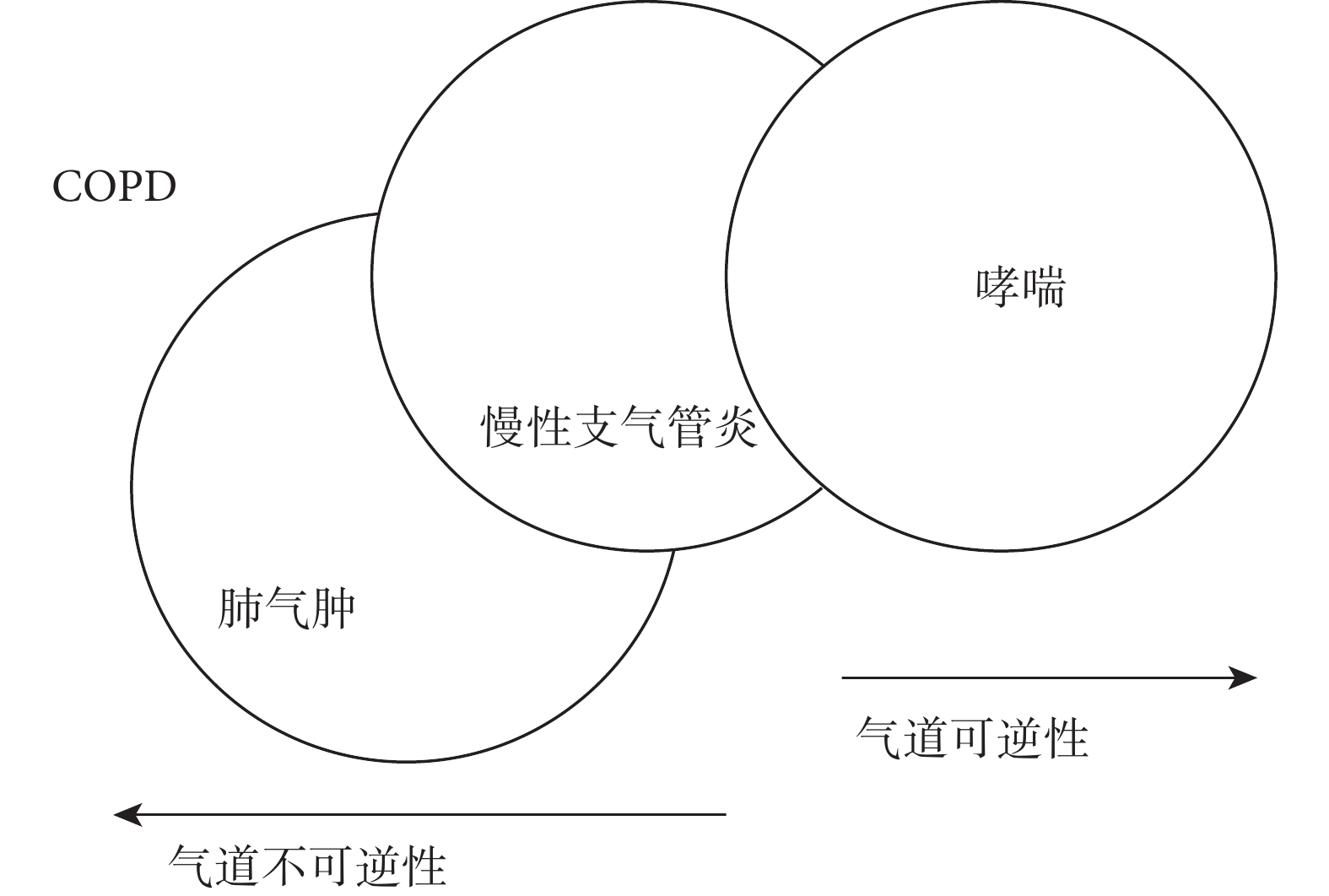
從上面那個三環圖中可以清楚的看到支氣管哮喘與肺氣腫可能會發生一定程度的交叉和重疊。多年來,從來無人對此提出疑問。然而我對于這個問題一直持有異議,認為這兩者不能發生重疊。理由很簡單,盡管引發哮喘的病因多種多樣,包括接觸多種過敏原、感染病毒,甚至真菌,其發病機理十分復雜,涉及多種炎癥細胞和細胞因子,但是有一點是十分肯定和明確的,那就是其病變只局限于各級氣道粘膜,后期發生氣道重塑會累及氣道平滑肌和黏液腺,但是不會累及肺泡。然而肺氣腫就不同了,長期大量吸煙,接觸生物燃料燃燒后產生的有害顆粒或氣體以及大氣污染,引發肺氣腫的病理改變,主要是上述有害致病因子引起彈性蛋白酶增加,而抗蛋白酶水平下降,即蛋白酶/抗蛋白酶系統失衡,從而造成大量肺泡破裂,融合,進而引發肺氣腫和肺大泡。由于大量肺泡破裂,肺泡對于依附于其上的氣道牽引力下降,從而使小氣道阻塞,氣流受限,然而病變只局限于肺泡,而不會引起氣道組織破壞。多年來許多學者強調支氣管炎型(BB型)氣腫型(PP型)患者具有截然不同的特點。當然,臨床上也會出現一定數量的患者既有氣道炎癥又有肺泡破壞,甚至最后發展為慢阻肺,然而,這只能說明在這部分慢阻肺患者身上,慢性氣道炎癥同時合并了肺氣腫,而不能說是肺氣腫合并支氣管哮喘。最近從文獻上看到一幅圖(圖2)[4],倒是比較合理地描述了這三者的關系。不知你如何認識這個問題?
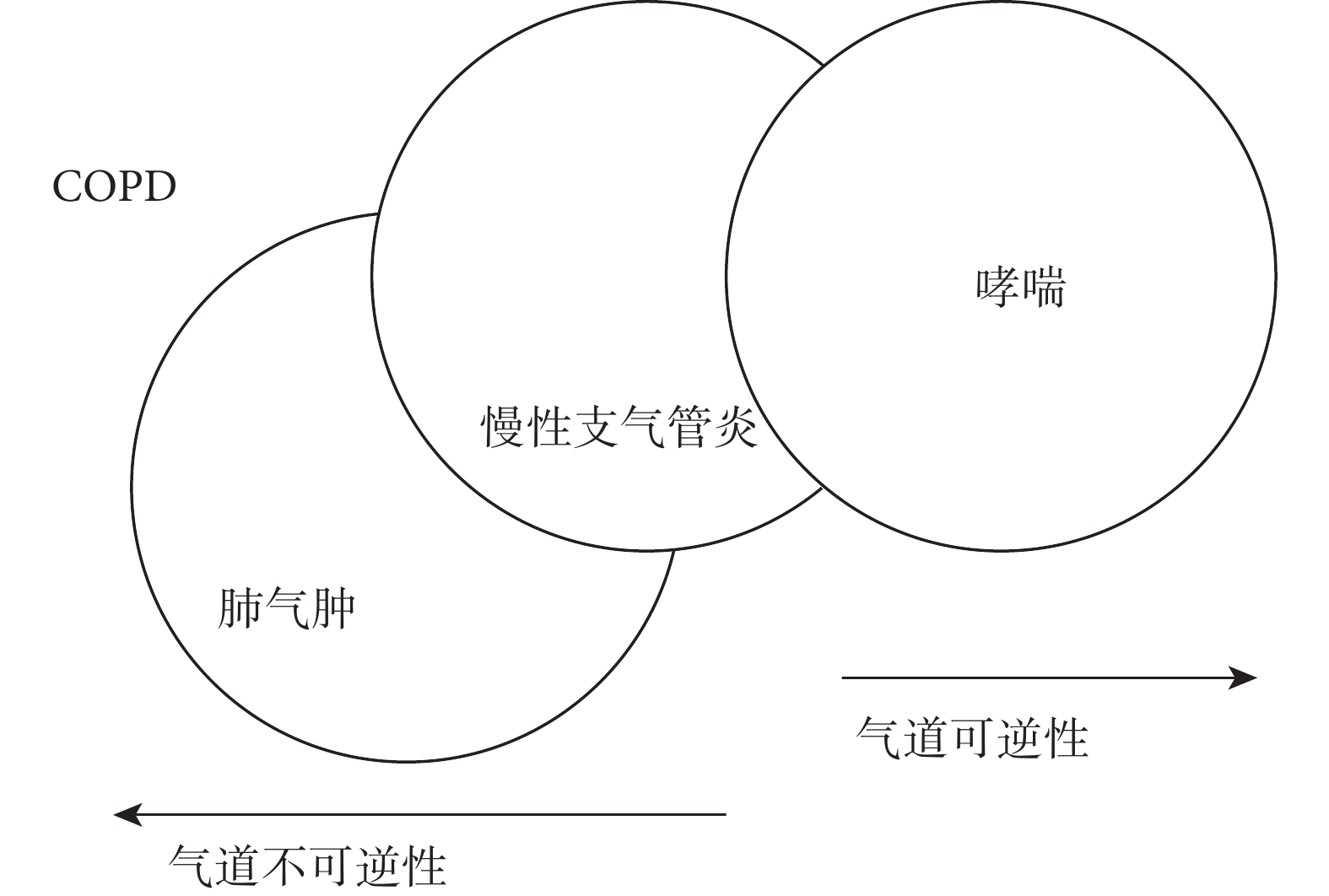 圖2
慢性支氣管炎、哮喘和肺氣腫的關系
圖2
慢性支氣管炎、哮喘和肺氣腫的關系
3 氣道炎癥細胞類型問題
長期以來人們一直認為慢阻肺與支氣管哮喘不同之處在于哮喘是一種以嗜酸性粒細胞升高為主要特征的慢性氣道疾病,而慢阻肺則是以淋巴細胞和中性粒細胞增多為主的氣道炎癥,反映到臨床科研工作中,長期以來人們復制哮喘動物模型時絕大多數研究者均把實驗動物氣道管壁中出現嗜酸性粒細胞增多作為復制模型成功的標志,很少有作者去計算嗜酸性粒細胞與炎癥細胞的百分比。后來部分研究者的研究會計算實驗動物BALF中嗜酸性粒細胞/炎癥細胞總數 的百分比,似乎哮喘和嗜酸性粒細胞炎癥成為同義語。對此筆者曾撰文加以討論[5]。事實上我們很難把這兩種疾病的不同之處簡單的歸結為氣道炎癥細胞成分的差異。
近年來在研究哮喘臨床表型,尤其是炎癥細胞表型時,Simpson等[6]澳大利亞學者明確提出按照氣道炎癥細胞種類劃分,哮喘的炎癥表型可分為以下4種:① 嗜酸性粒細胞性哮喘(嗜酸性粒細胞>1.01%);② 中性粒細胞性哮喘(中性粒細胞>61%);③ 少細胞性哮喘(嗜酸性粒細胞<1.01%,中性粒細胞<61%),④ 混合性粒細胞性哮喘(嗜酸性粒細胞>1.01%,中性粒細胞>61%)。表明糖皮質激素治療僅對 ① 型和 ④ 型哮喘有效,對 ② 型(中性粒細胞性哮喘)無效。Barnes[7]早在2013年就曾經說明,40%以上的哮喘患者是以中性粒細胞浸潤為主,10%~15%的嚴重哮喘患者對吸入ICS不敏感,甚至產生激素抵抗。Simpson等研究顯示,嗜酸性粒胞性哮喘約占40%,中性粒細胞性哮喘約占20%。Chung等[8]研究發現中性粒細胞性哮喘竟然會占到哮喘總數的50%,這些哮喘患者往往病情控制不佳、對激素反應差。國內也有類似的研究,張永明等[9]的研究結果顯示哮喘患者氣道炎癥分布特點是嗜酸性粒細胞性哮喘占46.6%,中性粒細胞性哮喘占21.5%,少細胞性哮喘占4.4%,混合性粒細胞性哮喘占27.5%。盡管上述作者報道的數據不完全一致,但有一點是可以肯定且一致的,即哮喘患者的氣道炎癥類型絕不全都是嗜酸性粒細胞性哮喘。這表明嗜酸性粒細胞性氣道炎癥并不能代表全部哮喘,另一方面大量研究資料顯示慢阻肺患者中氣道炎癥細胞中也有相當比例為嗜酸性粒細胞[10],因此近年來人們開始重視吸入糖皮質激素或全身糖皮質激素對于慢阻肺治療的適應證和臨床意義。所以,上述資料顯示氣道炎癥中的嗜酸性粒細胞增高并不是區分哮喘和慢阻肺的重要證據,或者說不能將嗜酸性粒細胞是否升高作為鑒別上述兩種疾病的證據,對此你有什么看法?
4 慢阻肺和哮喘氣道炎癥的定位問題
近年來有一種說法認為慢阻肺病變主要是在小氣道,而哮喘屬于大氣道疾病。為了進一步討論這個問題,首先應當明確一下大、小氣道的概念或定義。早在上個世紀70—80年代就明確規定吸氣狀態下,內徑<2 mm的氣道屬于小氣道,從解剖學來看應當包括少部分支氣管、全部細支氣管和呼吸性細支氣管,而內徑>2 mm的氣道,包括氣管、各級支氣管則屬于大氣道。所以,從解剖學上劃分,兩者的界限很明確,不會混淆。臨床上也可以通過胸部CT進行測量,做到這一點并不難。但是至今很少有人去分別檢測哮喘和慢阻肺患者氣道內徑的改變。倒是有不少人研究這兩種疾病患者的肺功能參數。先前人們曾認為常規肺功能參數包括FEV1、FVC、FEV1/FVC異常,則認為大氣道功能異常。如果這些指標正常,只有下述指標降低,包括用力呼氣中期、后期流速[MMEF、 和
和 ],△N2/L,以及用力依賴性肺順應性改變等,則屬于小氣道功能異常。然而這種劃分有很大的局限性,因為呼氣末期流速測定的準確性與患者用力呼氣的程度有很大關系,即屬于用力依賴性指標。另外更重要的一點是盡管慢阻肺和哮喘病因有很大不同,但是仍有不少共同之處,如吸煙、接觸空氣污染、病毒感染,上述各種病因作用于人體的氣道怎么會出現那么明確的定位、劃分結果呢?其機制又是什么呢?則很少有人去研究,對此不知你有什么看法?
],△N2/L,以及用力依賴性肺順應性改變等,則屬于小氣道功能異常。然而這種劃分有很大的局限性,因為呼氣末期流速測定的準確性與患者用力呼氣的程度有很大關系,即屬于用力依賴性指標。另外更重要的一點是盡管慢阻肺和哮喘病因有很大不同,但是仍有不少共同之處,如吸煙、接觸空氣污染、病毒感染,上述各種病因作用于人體的氣道怎么會出現那么明確的定位、劃分結果呢?其機制又是什么呢?則很少有人去研究,對此不知你有什么看法?
5 慢性支氣管炎與肺氣腫的區別
根據慢阻肺的定義可知慢阻肺大體主要可分為慢性支氣管炎和肺氣腫型以及兩型兼具者。盡管兩者在某些方面有共同之處,但是兩者在病因、發病機制、病理改變、臨床癥狀、胸部影像學、治療對策均有很多不同之處(表1)。
盡管肺氣腫患者由于肺泡大量破壞、融合形成肺大泡,與肺泡附著的氣道彈性回縮力下降,從而使氣道阻力增加,氣流受限,然而這兩種疾病之間的差別是顯而易見的,為什么一定要將兩者合為一種疾病——慢阻肺?依我看來,對于這兩種疾病應當區別對待,尤其是治療原則應當有所區別,對此你有什么看法?
6 同為慢性氣流受限性疾病,為什么判斷氣流受限及其可逆性指標及標準不同呢?
2013年我國制定的慢阻肺診治指南中規定,吸入支氣管舒張劑之后FEV1/FVC<70%,確定為持續存在氣流受限,將存在不完全可逆的氣流受限作為診斷慢阻肺的必要條件,即認為肺功能檢查是診斷慢阻肺的金標準,同時根據吸入支氣管舒張劑之后的FEV1占正常預計值百分比,將慢阻肺的嚴重程度評估為1-4級[11]。2022年版指南基本上維持原來的診斷和評估標準 [12] 。而診斷支氣管哮喘時也需要進行支氣管舒張試驗或激發試驗,以及PEF波動率測定,但是規定如果試驗前FEV1/預計值<80%,則需要進行支氣管舒張試驗。1993年制定的支氣管哮喘診治指南中規定應用支氣管舒張劑后FEV1改善率≥15%,同時FEV1增加絕對值>200 ml,則認為舒張試驗陽性[13]。2008年新修訂的支氣管哮喘診治指南中提出只要FEV1增加≥12%,同時FEV1增加的絕對值≥200ml,即可判定為支氣管舒張試驗陽性[14]。同樣是慢性氣道疾病為什么用以判斷氣流受限可逆性的指標和標準不同呢?我們曾經提出假如一患者吸入支氣管舒張劑后后FEV1/FVC<70%,而FEV1改善率≥12%,同時FEV1增加的絕對值≥200 ml,能夠同時診斷為慢阻肺加哮喘嗎[15]?目前文獻中沒有明確規定。2014年GINA[16]和GOLD[17]曾先后提出ACOS或ACO,2019年又被廢除[18]。那么現在到底應該如何處理這個問題,對此你有何看法?
長期以來(1995年起)人們一直習慣用三環圖(圖1)來表示慢性支氣管炎、肺氣腫與支氣管哮喘以及慢阻肺的關系[1],對此很少有人提出異議。然而近幾年筆者發現這個圖形有很多令人質疑之處,故不揣冒昧,對此提出以下問題,希望與大家一起討論。
 圖1
慢性支氣管炎、肺氣腫、支氣管哮喘、慢阻肺的關系(Am J Respir Crit Care Med. 1995 Nov;152(5 Pt 2):S77-121)
圖1
慢性支氣管炎、肺氣腫、支氣管哮喘、慢阻肺的關系(Am J Respir Crit Care Med. 1995 Nov;152(5 Pt 2):S77-121)
1 支氣管哮喘進入氣流受限不可逆階段還是哮喘嗎?
通常認為氣流受限具有可逆性是哮喘有別于慢阻肺的重要特征。眾所周知,支氣管哮喘的三種主要病理改變分別為氣道炎癥、平滑肌功能障礙和氣道重塑。所謂氣道重塑主要為氣道上皮纖維化、平滑肌增生、血管新生、黏液腺肥大、黏液高分泌和氣道水腫。其中黏液高分泌、氣道水腫尚屬可逆成分,然而上皮纖維化、平滑肌增生、血管新生以及黏液腺肥大則屬于不可逆成分,即一旦發生氣道重塑,其氣流受限就會變為不可逆[2]。那么哮喘患者一旦其氣流受限由可逆轉變為不可逆階段,那它還屬于支氣管哮喘嗎?有學者認為哮喘患者即使由于氣道重塑,氣流受限由可逆變為不可逆,仍舊屬于哮喘,只是進入了哮喘的后期。但是也有學者認為既然其氣流受限進入不可逆階段,那便應當屬于慢阻肺。因為慢阻肺的定義和診斷標準之一就是氣流受限為不可逆。既然由于氣道重塑,哮喘患者的氣流受限已進入不可逆階段,那它與慢阻肺就沒有什么不同了。近年來GOLD一直認為哮喘本身也是慢阻肺的發病危險因素之一[3],所以,哮喘患者一旦出現氣流受限不可逆,就應該按照慢阻肺進行治療,不知你怎么看待這個問題?
2 支氣管哮喘與肺氣腫不可能發生重疊
從上面那個三環圖中可以清楚的看到支氣管哮喘與肺氣腫可能會發生一定程度的交叉和重疊。多年來,從來無人對此提出疑問。然而我對于這個問題一直持有異議,認為這兩者不能發生重疊。理由很簡單,盡管引發哮喘的病因多種多樣,包括接觸多種過敏原、感染病毒,甚至真菌,其發病機理十分復雜,涉及多種炎癥細胞和細胞因子,但是有一點是十分肯定和明確的,那就是其病變只局限于各級氣道粘膜,后期發生氣道重塑會累及氣道平滑肌和黏液腺,但是不會累及肺泡。然而肺氣腫就不同了,長期大量吸煙,接觸生物燃料燃燒后產生的有害顆粒或氣體以及大氣污染,引發肺氣腫的病理改變,主要是上述有害致病因子引起彈性蛋白酶增加,而抗蛋白酶水平下降,即蛋白酶/抗蛋白酶系統失衡,從而造成大量肺泡破裂,融合,進而引發肺氣腫和肺大泡。由于大量肺泡破裂,肺泡對于依附于其上的氣道牽引力下降,從而使小氣道阻塞,氣流受限,然而病變只局限于肺泡,而不會引起氣道組織破壞。多年來許多學者強調支氣管炎型(BB型)氣腫型(PP型)患者具有截然不同的特點。當然,臨床上也會出現一定數量的患者既有氣道炎癥又有肺泡破壞,甚至最后發展為慢阻肺,然而,這只能說明在這部分慢阻肺患者身上,慢性氣道炎癥同時合并了肺氣腫,而不能說是肺氣腫合并支氣管哮喘。最近從文獻上看到一幅圖(圖2)[4],倒是比較合理地描述了這三者的關系。不知你如何認識這個問題?
 圖2
慢性支氣管炎、哮喘和肺氣腫的關系
圖2
慢性支氣管炎、哮喘和肺氣腫的關系
3 氣道炎癥細胞類型問題
長期以來人們一直認為慢阻肺與支氣管哮喘不同之處在于哮喘是一種以嗜酸性粒細胞升高為主要特征的慢性氣道疾病,而慢阻肺則是以淋巴細胞和中性粒細胞增多為主的氣道炎癥,反映到臨床科研工作中,長期以來人們復制哮喘動物模型時絕大多數研究者均把實驗動物氣道管壁中出現嗜酸性粒細胞增多作為復制模型成功的標志,很少有作者去計算嗜酸性粒細胞與炎癥細胞的百分比。后來部分研究者的研究會計算實驗動物BALF中嗜酸性粒細胞/炎癥細胞總數 的百分比,似乎哮喘和嗜酸性粒細胞炎癥成為同義語。對此筆者曾撰文加以討論[5]。事實上我們很難把這兩種疾病的不同之處簡單的歸結為氣道炎癥細胞成分的差異。
近年來在研究哮喘臨床表型,尤其是炎癥細胞表型時,Simpson等[6]澳大利亞學者明確提出按照氣道炎癥細胞種類劃分,哮喘的炎癥表型可分為以下4種:① 嗜酸性粒細胞性哮喘(嗜酸性粒細胞>1.01%);② 中性粒細胞性哮喘(中性粒細胞>61%);③ 少細胞性哮喘(嗜酸性粒細胞<1.01%,中性粒細胞<61%),④ 混合性粒細胞性哮喘(嗜酸性粒細胞>1.01%,中性粒細胞>61%)。表明糖皮質激素治療僅對 ① 型和 ④ 型哮喘有效,對 ② 型(中性粒細胞性哮喘)無效。Barnes[7]早在2013年就曾經說明,40%以上的哮喘患者是以中性粒細胞浸潤為主,10%~15%的嚴重哮喘患者對吸入ICS不敏感,甚至產生激素抵抗。Simpson等研究顯示,嗜酸性粒胞性哮喘約占40%,中性粒細胞性哮喘約占20%。Chung等[8]研究發現中性粒細胞性哮喘竟然會占到哮喘總數的50%,這些哮喘患者往往病情控制不佳、對激素反應差。國內也有類似的研究,張永明等[9]的研究結果顯示哮喘患者氣道炎癥分布特點是嗜酸性粒細胞性哮喘占46.6%,中性粒細胞性哮喘占21.5%,少細胞性哮喘占4.4%,混合性粒細胞性哮喘占27.5%。盡管上述作者報道的數據不完全一致,但有一點是可以肯定且一致的,即哮喘患者的氣道炎癥類型絕不全都是嗜酸性粒細胞性哮喘。這表明嗜酸性粒細胞性氣道炎癥并不能代表全部哮喘,另一方面大量研究資料顯示慢阻肺患者中氣道炎癥細胞中也有相當比例為嗜酸性粒細胞[10],因此近年來人們開始重視吸入糖皮質激素或全身糖皮質激素對于慢阻肺治療的適應證和臨床意義。所以,上述資料顯示氣道炎癥中的嗜酸性粒細胞增高并不是區分哮喘和慢阻肺的重要證據,或者說不能將嗜酸性粒細胞是否升高作為鑒別上述兩種疾病的證據,對此你有什么看法?
4 慢阻肺和哮喘氣道炎癥的定位問題
近年來有一種說法認為慢阻肺病變主要是在小氣道,而哮喘屬于大氣道疾病。為了進一步討論這個問題,首先應當明確一下大、小氣道的概念或定義。早在上個世紀70—80年代就明確規定吸氣狀態下,內徑<2 mm的氣道屬于小氣道,從解剖學來看應當包括少部分支氣管、全部細支氣管和呼吸性細支氣管,而內徑>2 mm的氣道,包括氣管、各級支氣管則屬于大氣道。所以,從解剖學上劃分,兩者的界限很明確,不會混淆。臨床上也可以通過胸部CT進行測量,做到這一點并不難。但是至今很少有人去分別檢測哮喘和慢阻肺患者氣道內徑的改變。倒是有不少人研究這兩種疾病患者的肺功能參數。先前人們曾認為常規肺功能參數包括FEV1、FVC、FEV1/FVC異常,則認為大氣道功能異常。如果這些指標正常,只有下述指標降低,包括用力呼氣中期、后期流速[MMEF、 和
和 ],△N2/L,以及用力依賴性肺順應性改變等,則屬于小氣道功能異常。然而這種劃分有很大的局限性,因為呼氣末期流速測定的準確性與患者用力呼氣的程度有很大關系,即屬于用力依賴性指標。另外更重要的一點是盡管慢阻肺和哮喘病因有很大不同,但是仍有不少共同之處,如吸煙、接觸空氣污染、病毒感染,上述各種病因作用于人體的氣道怎么會出現那么明確的定位、劃分結果呢?其機制又是什么呢?則很少有人去研究,對此不知你有什么看法?
],△N2/L,以及用力依賴性肺順應性改變等,則屬于小氣道功能異常。然而這種劃分有很大的局限性,因為呼氣末期流速測定的準確性與患者用力呼氣的程度有很大關系,即屬于用力依賴性指標。另外更重要的一點是盡管慢阻肺和哮喘病因有很大不同,但是仍有不少共同之處,如吸煙、接觸空氣污染、病毒感染,上述各種病因作用于人體的氣道怎么會出現那么明確的定位、劃分結果呢?其機制又是什么呢?則很少有人去研究,對此不知你有什么看法?
5 慢性支氣管炎與肺氣腫的區別
根據慢阻肺的定義可知慢阻肺大體主要可分為慢性支氣管炎和肺氣腫型以及兩型兼具者。盡管兩者在某些方面有共同之處,但是兩者在病因、發病機制、病理改變、臨床癥狀、胸部影像學、治療對策均有很多不同之處(表1)。
盡管肺氣腫患者由于肺泡大量破壞、融合形成肺大泡,與肺泡附著的氣道彈性回縮力下降,從而使氣道阻力增加,氣流受限,然而這兩種疾病之間的差別是顯而易見的,為什么一定要將兩者合為一種疾病——慢阻肺?依我看來,對于這兩種疾病應當區別對待,尤其是治療原則應當有所區別,對此你有什么看法?
6 同為慢性氣流受限性疾病,為什么判斷氣流受限及其可逆性指標及標準不同呢?
2013年我國制定的慢阻肺診治指南中規定,吸入支氣管舒張劑之后FEV1/FVC<70%,確定為持續存在氣流受限,將存在不完全可逆的氣流受限作為診斷慢阻肺的必要條件,即認為肺功能檢查是診斷慢阻肺的金標準,同時根據吸入支氣管舒張劑之后的FEV1占正常預計值百分比,將慢阻肺的嚴重程度評估為1-4級[11]。2022年版指南基本上維持原來的診斷和評估標準 [12] 。而診斷支氣管哮喘時也需要進行支氣管舒張試驗或激發試驗,以及PEF波動率測定,但是規定如果試驗前FEV1/預計值<80%,則需要進行支氣管舒張試驗。1993年制定的支氣管哮喘診治指南中規定應用支氣管舒張劑后FEV1改善率≥15%,同時FEV1增加絕對值>200 ml,則認為舒張試驗陽性[13]。2008年新修訂的支氣管哮喘診治指南中提出只要FEV1增加≥12%,同時FEV1增加的絕對值≥200ml,即可判定為支氣管舒張試驗陽性[14]。同樣是慢性氣道疾病為什么用以判斷氣流受限可逆性的指標和標準不同呢?我們曾經提出假如一患者吸入支氣管舒張劑后后FEV1/FVC<70%,而FEV1改善率≥12%,同時FEV1增加的絕對值≥200 ml,能夠同時診斷為慢阻肺加哮喘嗎[15]?目前文獻中沒有明確規定。2014年GINA[16]和GOLD[17]曾先后提出ACOS或ACO,2019年又被廢除[18]。那么現在到底應該如何處理這個問題,對此你有何看法?