引用本文: 焦欣, 邵阿雪, 何清清, 吳文玉, 劉建博, 王凱. 胃食管反流病與阻塞性睡眠呼吸暫停之間的關系:孟德爾隨機化研究. 中國循證醫學雜志, 2024, 24(9): 1004-1010. doi: 10.7507/1672-2531.202312062 復制
版權信息: ?四川大學華西醫院華西期刊社《中國循證醫學雜志》版權所有,未經授權不得轉載、改編
胃食管反流病(gastroesophageal reflux disease,GERD)是一種常見的胃腸道疾病,其特點是胃、十二指腸酸性內容物異常反流至食管,引起食管黏膜損傷和反流癥狀[1]。據統計,目前13%的全球人口和20%的成年人患有GERD,胃食管反流與反流性食管炎、食管狹窄、巴雷特食管和食管腺癌的風險增加有關[2,3]。近年來,GERD被認為是阻塞性睡眠呼吸暫停(obstructive sleep apnea,OSA)的一個重要誘因[4,5]。OSA是指睡眠期間反復發生上呼吸道塌陷,導致反復發作的呼吸暫停或低通氣[6],具體可表現為夜間反復覺醒、打鼾、白天嗜睡、慢性疲勞、晨起頭痛、注意力和記憶力減退、情緒低落等[7]。研究表明,OSA可直接引起間歇性缺氧和高碳酸血癥,繼而誘發交感神經激活、氧化應激和全身炎癥等反應,長此以往可增加心腦血管疾病、高血壓和糖尿病等的發病風險[8]。全球大約有10億30至69歲的成年人患有OSA,其中有40%至60%的OSA患者同時合并有GERD[9-11]。肥胖、吸煙和飲酒等OSA發展因素同時也被確定為GERD的危險因素[12,13],觀察性研究也發現GERD與OSA存在相關性[14,15]。盡管GERD與OSA的臨床相關性在觀察性研究中已被多次強調,然而他們之間是否存在因果關系尚不明確。
眾所周知,觀察性研究容易受到混雜偏倚因素的影響。孟德爾隨機化(Mendelian randomization,MR)是近年來新起的利用基因型來推斷表型與疾病之間關聯的研究方法,主要是將單核苷酸多態性(single nucleotide polymorphism,SNP)作為遺傳變異工具變量(instrumental variable,IV),借此評估暴露因素與結果事件之間關聯的因果效應[16]。由于這些遺傳基因變異源于母代并且在受孕時隨機分配,因此它滿足時間順序的合理性又更不容易受到反向因果關系和混淆因素的影響[17],是目前除了隨機對照試驗(randomized controlled trial,RCT)以外證據質量較高的臨床科研方法。因此,本研究通過一項多變量雙樣本孟德爾隨機化(two-sample Mendelian randomization,TSMR)方法進一步探究GERD與OSA及其典型癥狀之間的因果關系。
1 資料與方法
1.1 研究設計
本研究全程參照STROBE-MR條目清單進行設計與實施,以確保MR分析的規范性與準確性[18]。根據Bownden等[19]的說法,TSMR分析需滿足以下三個假設:① 關聯性假設:從數據集中選擇的遺傳IV與暴露因素強相關;② 獨立性假設:遺傳IV與任何潛在混雜因素無關;③ 排他性假設:遺傳IV只能通過暴露因素影響結局因素。本研究以GRED作為暴露因素,OSA及其典型癥狀(打鼾、白天嗜睡)作為結局因素,采用MR方法評估GERD與OSA之間的因果關系,MR分析研究流程圖見附件圖1。本研究所選擇暴露和結果隊列研究都僅限于歐洲血統的受試者,以減少人群分層的偏倚[20]。本研究中使用的所有數據均來自相關受試者同意和倫理認可的研究。
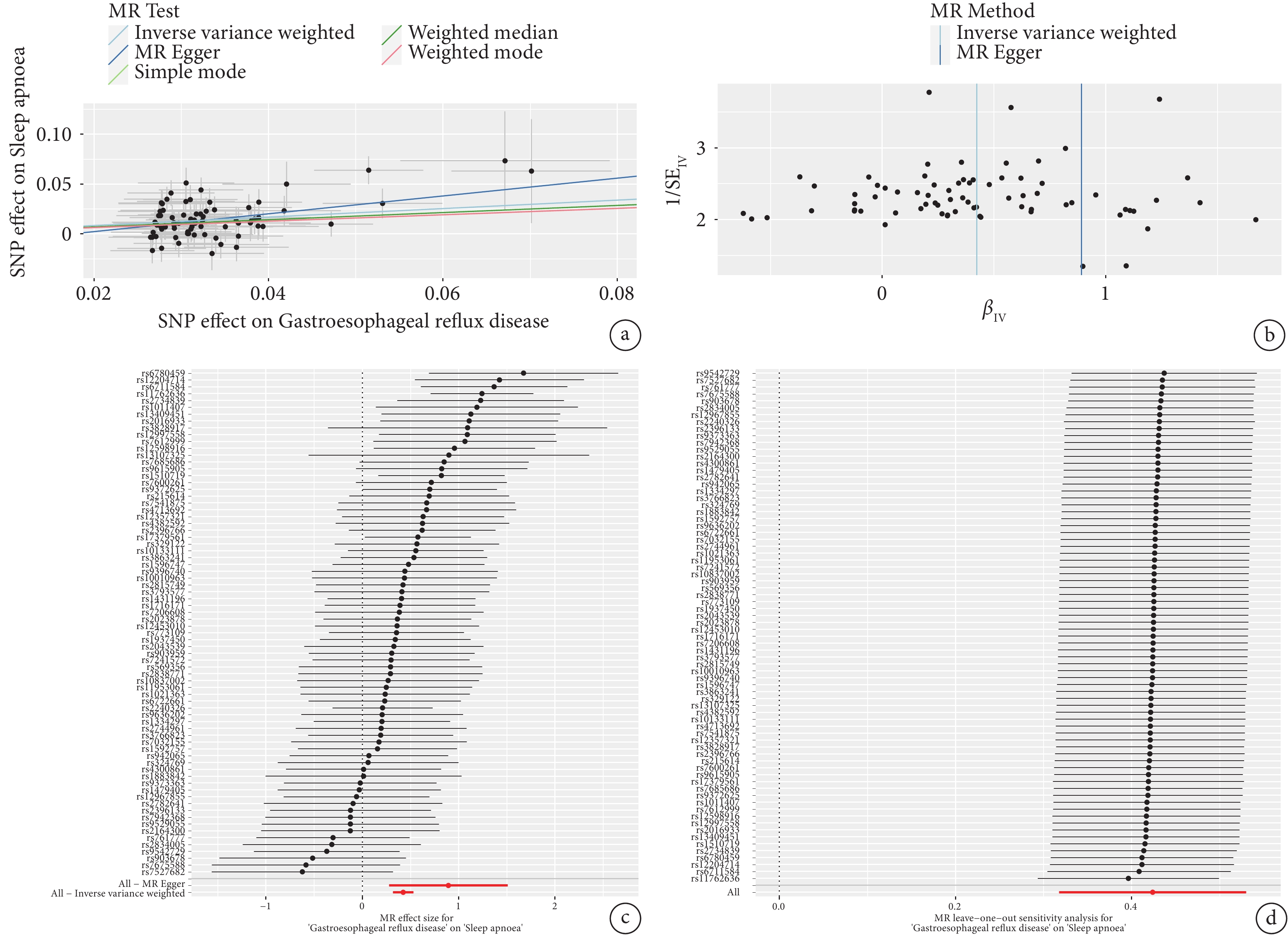 圖1
GERD與OSA關系的孟德爾分析
圖1
GERD與OSA關系的孟德爾分析
a:散點圖;b:漏斗圖;c:森林圖;d:留一法敏感性分析圖。
1.2 數據來源
從IEU open GWAS數據庫中選擇最大最新的GERD數據[21]。GERD病例診斷通過自我報告的GERD癥狀、國際疾病分類診斷和使用抗GERD相關藥物綜合評估[21]。OSA的數據來自FinnGen最近發表的全基因組關聯研究[22]。OSA根據國際疾病統計分類(ICD)代碼(ICD-10:G47.3,ICD-9:3472A)診斷,該代碼基于主觀癥狀、臨床檢查和呼吸暫停低通氣指數(apnea hypopnea index,AHI)≥5進行綜合評估。打鼾與白天嗜睡的數據均來源于英國生物樣本庫(UK Biobank,UKBB)GWAS數據庫[23]。所有數據來源特征信息見表1。
1.3 IV篩選
首先,從GERD的GWAS中選擇符合全基因組顯著性標準(P<5×10?8)的SNPs,并使用Clump函數去除連鎖不平衡(r2<0.001,kb=10 000)[24]。其次,為了避免弱IV導致偏倚,計算每個SNP的F統計量,F統計量>10被認為足以抵消弱工具偏差[25],F值<10的SNP被剔除,計算公式如下[26]:F=β2exposure/SE2exposure,β為暴露的等位基因效應值,SE為暴露的標準誤。最后,還進行了MR多效殘差和離群值檢驗(Mendelian randomization pleiotropy residual sum and outlier,MR-PRESSO),若檢測出異常值則將其剔除,對剩余SNPs進行MR分析。IV篩選流程見附件圖1。
1.4 統計分析
本研究主要采用逆方差加權法(inverse variance-weighted,IVW)、MR-Egger、加權中位數法(weighted median,WM)、加權模型(weighted mode)和簡單模型(simple mode)等進行MR分析[16]。由于IVW法比其他方法檢驗效能更高,可以在存在異質性的條件下獲得更穩健的結果,因此以IVW法分析結果作為主效應分析結果[27]。使用Cochran’s Q統計量評估異質性,P<0.05提示存在異質性。采用留一法進行敏感性分析,評估是否存在由于單個SNP對MR結果產生獨立影響結果而存在偏倚情況[27]。通過MR-Egger回歸法觀察截距項評估基因多效性,當P<0.05時表示存在多效性[28]。同時進行MR-PRESSO異常值檢驗,識別和去除異常值對水平多效性進行校正[29]。所有數據分析均使用R 4.1.2軟件的Two Sample MR 0.5.6包和MR-PRESSO 1.0包進行[30]。
2 結果
2.1 GERD與OSA的MR分析結果
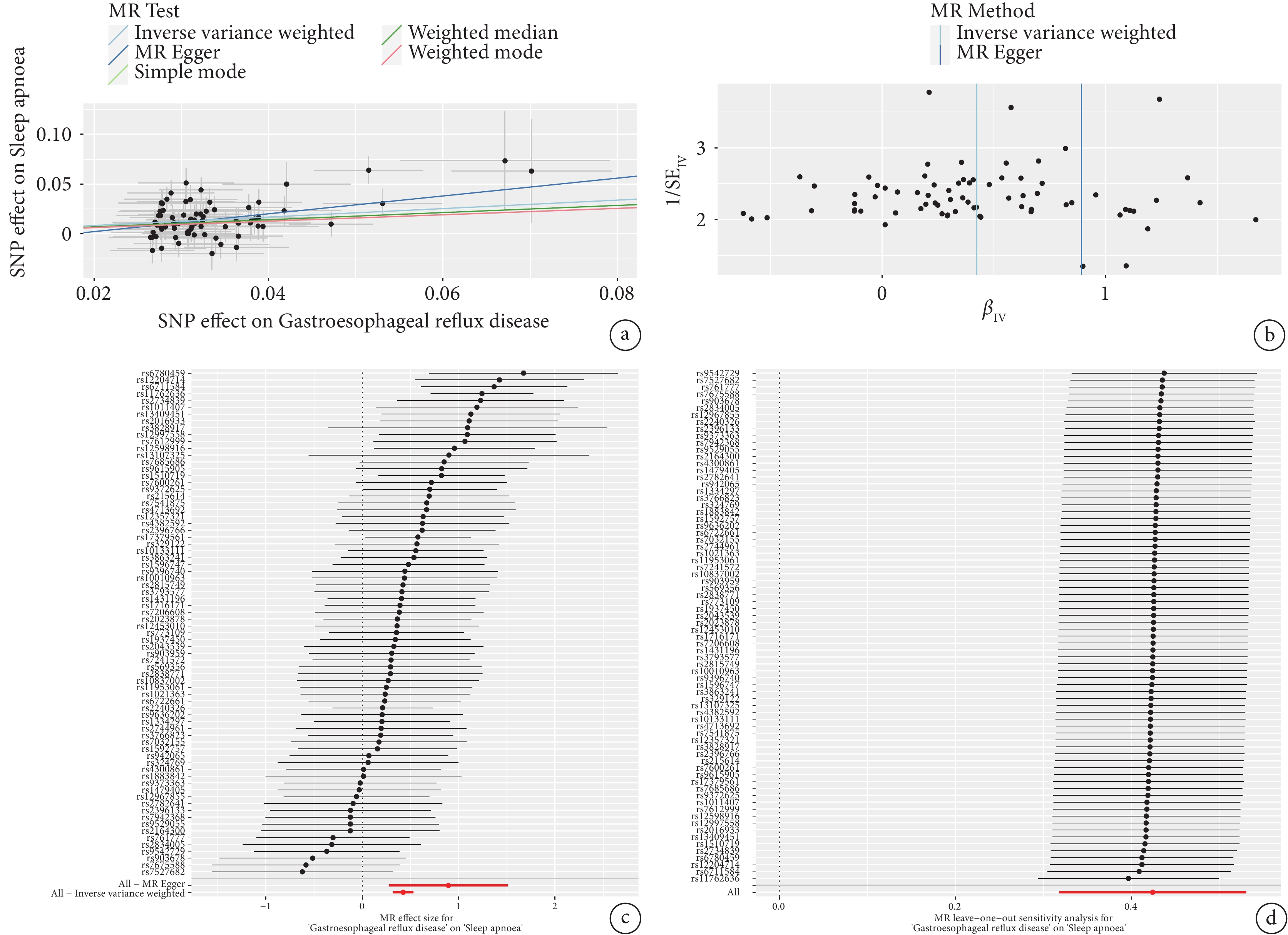
MR結果顯示GERD與OSA之間存在正相關的因果關系[IVW:OR=1.528,95%CI(1.374,1.699),P=5.315E?15],5種方法分析結果一致(表2)。異質性檢驗顯示不存在異質性(P=0.099),敏感性試驗未發現多效性(P=0.133)(表3)。漏斗圖中IVW線左右兩邊的散點基本對稱,說明結果不存在潛在偏倚,留一法分析未發現單個對因果關聯影響較大的SNP,確保了因果效應估計的可靠性。GERD對OSA的MR分析的散點圖、漏斗圖、森林圖、留一法分析圖如圖1所示。
2.2 GERD與打鼾、白天嗜睡的MR分析結果
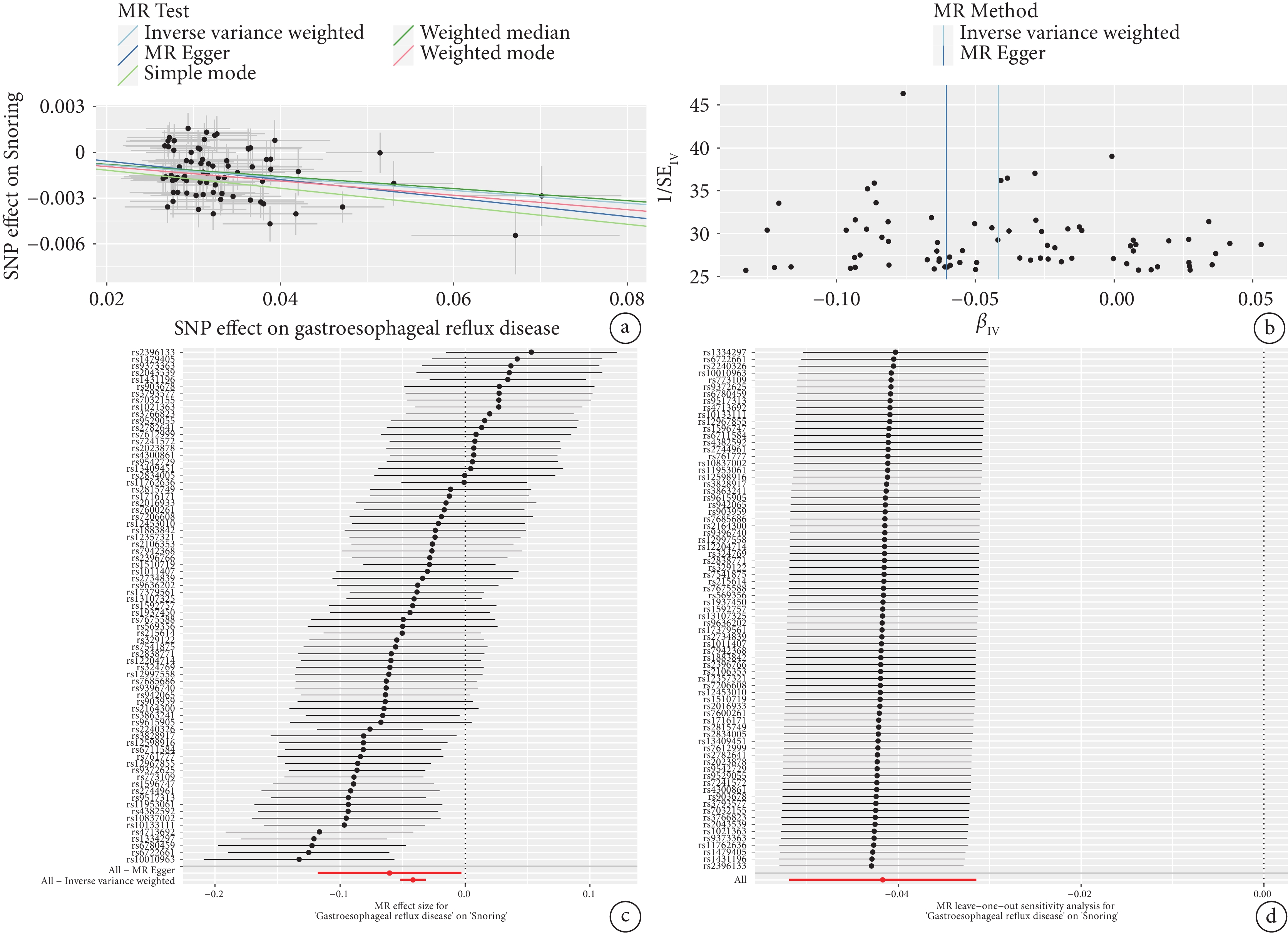
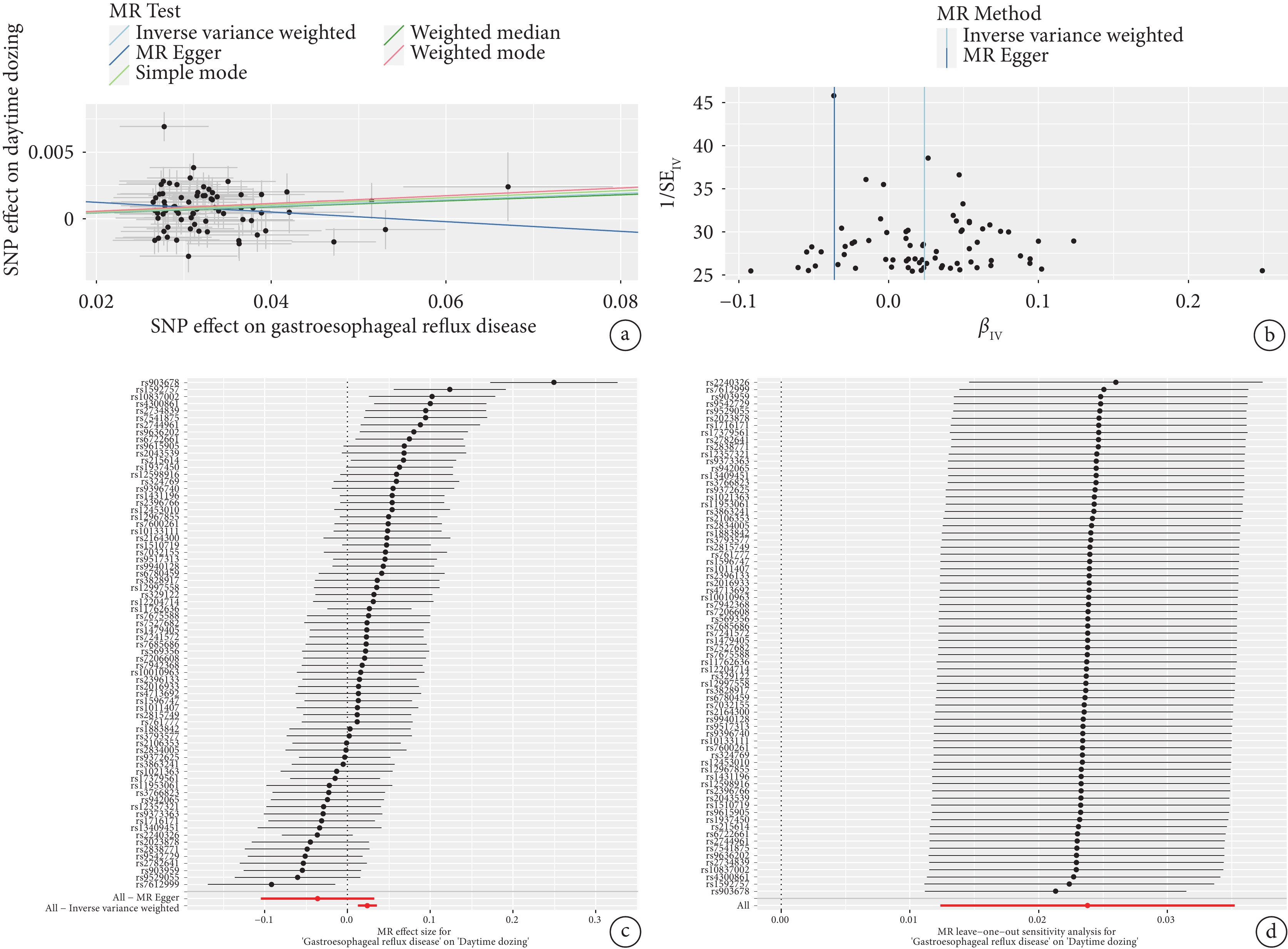
Cochran’s Q檢驗結果顯示,GERD與打鼾、白天嗜睡的MR分析存在異質性(P<0.05)(表3),故采用隨機效應IVW法進行MR分析。結果顯示GERD是打鼾[IVW:OR=0.959,95%CI(0.949,0.969),P=1.507E?15]、白天嗜睡[IVW:OR=1.024,95%CI(1.021,1.036),P=4.580E?5]的強相關因素(表2),敏感性分析結果未發現多效性(表3),說明SNPs并不通過GERD以外的途徑顯著影響打鼾與白天嗜睡。留一法檢驗提示結果穩定,沒有單個SNP對MR結果造成顯著影響。漏斗圖中IVW線的左右兩邊的點大致對稱,提示本研究結果穩定。GERD對打鼾、白天嗜睡的MR分析的漏斗圖、散點圖、森林圖、留一法分析圖分別如圖2、圖3所示。
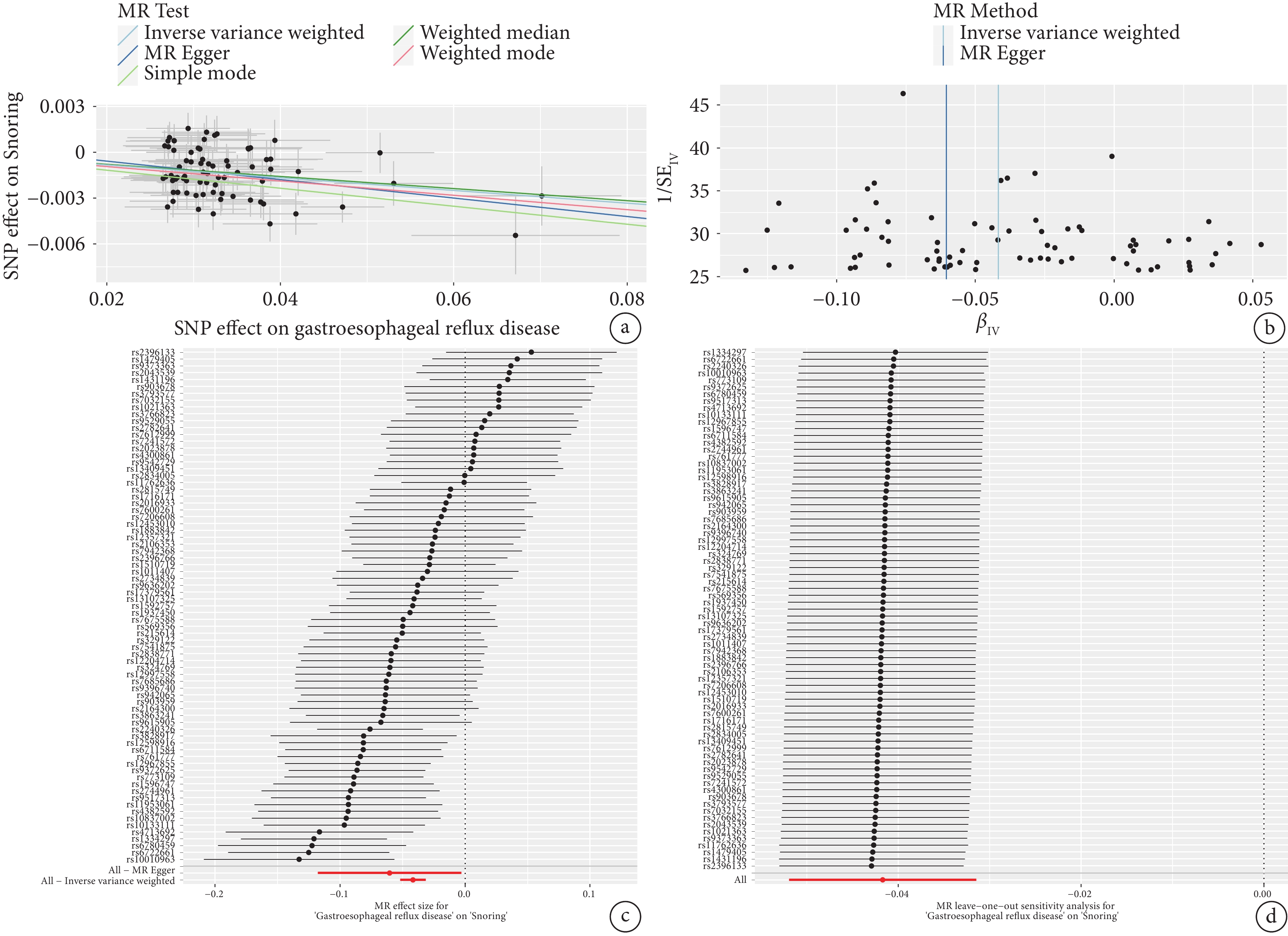 圖2
GERD與打鼾關系的孟德爾分析
圖2
GERD與打鼾關系的孟德爾分析
a:散點圖;b:漏斗圖;c:森林圖;d:留一法敏感性分析圖。
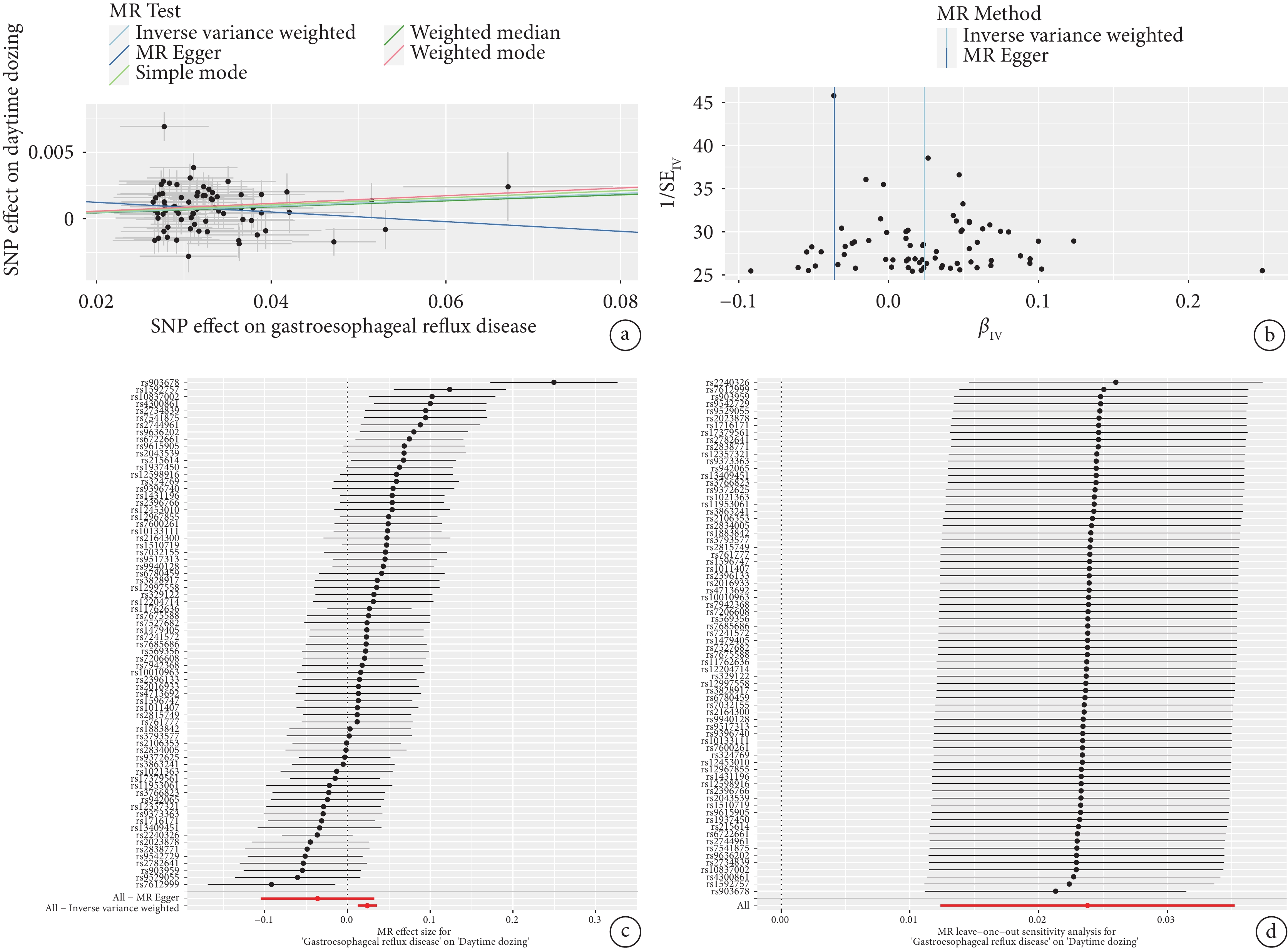 圖3
GERD與白天嗜睡關系的孟德爾分析
圖3
GERD與白天嗜睡關系的孟德爾分析
a:散點圖;b:漏斗圖;c:森林圖;d:留一法敏感性分析圖。
3 討論
GERD是否是OSA的危險因素一直存在爭議,一項來自韓國的隊列研究[14]表明經內窺鏡證實的GERD與更嚴重的OSA相關,GERD更常見于OSA患者中[14,31]。然而也有研究表明OSA與非OSA患者的GERD患病率沒有差異[32],GERD和OSA具有相似的危險因素,他們之間的關聯可能僅僅是共同風險因素的反映[33]。本研究旨在通過兩樣本MR分析探討GERD與OSA及其典型癥狀之間的因果關系,這是第一個通過對大規模GWAS數據進行MR分析來探討GERD與OSA之間的因果關系的研究,豐富了以往相關研究的結果。
本研究發現GERD和OSA之間存在因果關系,基因水平上的GERD與OSA風險呈正相關,與觀察性研究的結果一致[34]。有調查發現,在診斷為GERD的22 677 620例患者中,同時診斷為OSA的患者占比12.21%,未診斷為GERD的患者OSA患病率為4.79%[34],GERD患者的OSA患病率明顯高于非GERD患者。Gilani等[35]的研究也發現,在匹配了年齡、性別、種族、肥胖、鼻竇和喉部疾病、哮喘及其它肺部疾病等可能的混雜因素后,GERD仍與OSA獨立相關。GERD夜間反流癥狀可導致睡眠覺醒次數增加、睡眠剝奪和喉頭水腫,從而加重上呼吸道阻塞,引起或加重OSA[10,11]。研究發現AHI與弱胃酸反流有關[36],夜間胃反流激活自主神經系統,增加迷走神經刺激,引起支氣管收縮,進而導致AHI值增加,引起睡眠障礙[4]。也有研究觀察到治療GERD可以改善睡眠障礙[4],質子泵抑制劑的使用改善了與睡眠障礙相關的生活質量并可改善OSA患者的呼吸暫停指數[37,38]。奧美拉唑治療GERD已被證明可減少呼吸暫停發作[39]。然而,一項旨在評估質子泵抑制劑治療GERD與改善OSA的Meta分析,發現這種方式可能改善夜間睡眠質量,但對AHI沒有影響[40],GERD和OSA關聯的確切機制仍有待進一步研究。
打鼾是一種非常普遍的睡眠狀況,是OSA的主要癥狀之一,但大多數打鼾者并不符合OSA的診斷標準,打鼾應該被視為一個獨立的實體疾病,而不僅僅是OSA的癥狀。據統計,高達78%成年男性和59%成年女性伴有打鼾[41]。白天嗜睡是指白天無法控制的打盹和困倦,容易造成個體注意力不集中、焦慮抑郁等,白天嗜睡在人群中的發生率約為12%~16%[42]。一項大型前瞻性隊列研究發現胃食管反流癥狀與打鼾、白天嗜睡之間有很強的相關性[43]。Emilsson等[44]研究發現在GERD受試者中觀察到的自我報告的打鼾比沒有GERD的受試者更多,并且在調整BMI后,音頻測量的打鼾(>65dB)仍與GERD顯著相關。瑞典一項研究[45]也發現,有持續性夜間胃食管返流癥狀的女性白天嗜睡的患病率明顯高于無夜間胃食管返流癥狀的女性。夜間發生胃食管反流可加重OSA患者白天嗜睡。也有研究發現,在排除OSA導致的白天嗜睡外,白天嗜睡相關的2個參數(斯坦福嗜睡量表、Epworth嗜睡量表)也與GERD相關[46]。本研究也證實了GERD與打鼾、白天嗜睡之間存在因果關系。
本研究的局限性:① 所有納入的參與者都是歐洲人,這減少了人口分層偏差,但種族似乎會影響OSA患者的顱面解剖特征和肥胖傾向,這大約占OSA風險的40%[47,48],因此本研究結果對其他人群的推廣可能有限。② 在GERD與打鼾、白天瞌睡的分析中存在異質性,這可能與原始研究樣本量和研究人群有關,故采用隨機效應IVW法進行分析,未來應通過擴大樣本量、增加分層數據等方法減少異質性。③ 不能完全排除本研究結果受到弱IV偏差影響的可能性,盡管計算的F統計量均>10,并未表明弱IV。
綜上所述,本研究發現GERD與OSA風險及其典型癥狀(打鼾、白天嗜睡)之間存在因果關系,進一步證實了GERD是OSA的獨立危險因素。這些發現對GERD與OSA患者的臨床管理具有重要的指導意義。
胃食管反流病(gastroesophageal reflux disease,GERD)是一種常見的胃腸道疾病,其特點是胃、十二指腸酸性內容物異常反流至食管,引起食管黏膜損傷和反流癥狀[1]。據統計,目前13%的全球人口和20%的成年人患有GERD,胃食管反流與反流性食管炎、食管狹窄、巴雷特食管和食管腺癌的風險增加有關[2,3]。近年來,GERD被認為是阻塞性睡眠呼吸暫停(obstructive sleep apnea,OSA)的一個重要誘因[4,5]。OSA是指睡眠期間反復發生上呼吸道塌陷,導致反復發作的呼吸暫停或低通氣[6],具體可表現為夜間反復覺醒、打鼾、白天嗜睡、慢性疲勞、晨起頭痛、注意力和記憶力減退、情緒低落等[7]。研究表明,OSA可直接引起間歇性缺氧和高碳酸血癥,繼而誘發交感神經激活、氧化應激和全身炎癥等反應,長此以往可增加心腦血管疾病、高血壓和糖尿病等的發病風險[8]。全球大約有10億30至69歲的成年人患有OSA,其中有40%至60%的OSA患者同時合并有GERD[9-11]。肥胖、吸煙和飲酒等OSA發展因素同時也被確定為GERD的危險因素[12,13],觀察性研究也發現GERD與OSA存在相關性[14,15]。盡管GERD與OSA的臨床相關性在觀察性研究中已被多次強調,然而他們之間是否存在因果關系尚不明確。
眾所周知,觀察性研究容易受到混雜偏倚因素的影響。孟德爾隨機化(Mendelian randomization,MR)是近年來新起的利用基因型來推斷表型與疾病之間關聯的研究方法,主要是將單核苷酸多態性(single nucleotide polymorphism,SNP)作為遺傳變異工具變量(instrumental variable,IV),借此評估暴露因素與結果事件之間關聯的因果效應[16]。由于這些遺傳基因變異源于母代并且在受孕時隨機分配,因此它滿足時間順序的合理性又更不容易受到反向因果關系和混淆因素的影響[17],是目前除了隨機對照試驗(randomized controlled trial,RCT)以外證據質量較高的臨床科研方法。因此,本研究通過一項多變量雙樣本孟德爾隨機化(two-sample Mendelian randomization,TSMR)方法進一步探究GERD與OSA及其典型癥狀之間的因果關系。
1 資料與方法
1.1 研究設計
本研究全程參照STROBE-MR條目清單進行設計與實施,以確保MR分析的規范性與準確性[18]。根據Bownden等[19]的說法,TSMR分析需滿足以下三個假設:① 關聯性假設:從數據集中選擇的遺傳IV與暴露因素強相關;② 獨立性假設:遺傳IV與任何潛在混雜因素無關;③ 排他性假設:遺傳IV只能通過暴露因素影響結局因素。本研究以GRED作為暴露因素,OSA及其典型癥狀(打鼾、白天嗜睡)作為結局因素,采用MR方法評估GERD與OSA之間的因果關系,MR分析研究流程圖見附件圖1。本研究所選擇暴露和結果隊列研究都僅限于歐洲血統的受試者,以減少人群分層的偏倚[20]。本研究中使用的所有數據均來自相關受試者同意和倫理認可的研究。
 圖1
GERD與OSA關系的孟德爾分析
圖1
GERD與OSA關系的孟德爾分析
a:散點圖;b:漏斗圖;c:森林圖;d:留一法敏感性分析圖。
1.2 數據來源
從IEU open GWAS數據庫中選擇最大最新的GERD數據[21]。GERD病例診斷通過自我報告的GERD癥狀、國際疾病分類診斷和使用抗GERD相關藥物綜合評估[21]。OSA的數據來自FinnGen最近發表的全基因組關聯研究[22]。OSA根據國際疾病統計分類(ICD)代碼(ICD-10:G47.3,ICD-9:3472A)診斷,該代碼基于主觀癥狀、臨床檢查和呼吸暫停低通氣指數(apnea hypopnea index,AHI)≥5進行綜合評估。打鼾與白天嗜睡的數據均來源于英國生物樣本庫(UK Biobank,UKBB)GWAS數據庫[23]。所有數據來源特征信息見表1。
1.3 IV篩選
首先,從GERD的GWAS中選擇符合全基因組顯著性標準(P<5×10?8)的SNPs,并使用Clump函數去除連鎖不平衡(r2<0.001,kb=10 000)[24]。其次,為了避免弱IV導致偏倚,計算每個SNP的F統計量,F統計量>10被認為足以抵消弱工具偏差[25],F值<10的SNP被剔除,計算公式如下[26]:F=β2exposure/SE2exposure,β為暴露的等位基因效應值,SE為暴露的標準誤。最后,還進行了MR多效殘差和離群值檢驗(Mendelian randomization pleiotropy residual sum and outlier,MR-PRESSO),若檢測出異常值則將其剔除,對剩余SNPs進行MR分析。IV篩選流程見附件圖1。
1.4 統計分析
本研究主要采用逆方差加權法(inverse variance-weighted,IVW)、MR-Egger、加權中位數法(weighted median,WM)、加權模型(weighted mode)和簡單模型(simple mode)等進行MR分析[16]。由于IVW法比其他方法檢驗效能更高,可以在存在異質性的條件下獲得更穩健的結果,因此以IVW法分析結果作為主效應分析結果[27]。使用Cochran’s Q統計量評估異質性,P<0.05提示存在異質性。采用留一法進行敏感性分析,評估是否存在由于單個SNP對MR結果產生獨立影響結果而存在偏倚情況[27]。通過MR-Egger回歸法觀察截距項評估基因多效性,當P<0.05時表示存在多效性[28]。同時進行MR-PRESSO異常值檢驗,識別和去除異常值對水平多效性進行校正[29]。所有數據分析均使用R 4.1.2軟件的Two Sample MR 0.5.6包和MR-PRESSO 1.0包進行[30]。
2 結果
2.1 GERD與OSA的MR分析結果
MR結果顯示GERD與OSA之間存在正相關的因果關系[IVW:OR=1.528,95%CI(1.374,1.699),P=5.315E?15],5種方法分析結果一致(表2)。異質性檢驗顯示不存在異質性(P=0.099),敏感性試驗未發現多效性(P=0.133)(表3)。漏斗圖中IVW線左右兩邊的散點基本對稱,說明結果不存在潛在偏倚,留一法分析未發現單個對因果關聯影響較大的SNP,確保了因果效應估計的可靠性。GERD對OSA的MR分析的散點圖、漏斗圖、森林圖、留一法分析圖如圖1所示。
2.2 GERD與打鼾、白天嗜睡的MR分析結果
Cochran’s Q檢驗結果顯示,GERD與打鼾、白天嗜睡的MR分析存在異質性(P<0.05)(表3),故采用隨機效應IVW法進行MR分析。結果顯示GERD是打鼾[IVW:OR=0.959,95%CI(0.949,0.969),P=1.507E?15]、白天嗜睡[IVW:OR=1.024,95%CI(1.021,1.036),P=4.580E?5]的強相關因素(表2),敏感性分析結果未發現多效性(表3),說明SNPs并不通過GERD以外的途徑顯著影響打鼾與白天嗜睡。留一法檢驗提示結果穩定,沒有單個SNP對MR結果造成顯著影響。漏斗圖中IVW線的左右兩邊的點大致對稱,提示本研究結果穩定。GERD對打鼾、白天嗜睡的MR分析的漏斗圖、散點圖、森林圖、留一法分析圖分別如圖2、圖3所示。
 圖2
GERD與打鼾關系的孟德爾分析
圖2
GERD與打鼾關系的孟德爾分析
a:散點圖;b:漏斗圖;c:森林圖;d:留一法敏感性分析圖。
 圖3
GERD與白天嗜睡關系的孟德爾分析
圖3
GERD與白天嗜睡關系的孟德爾分析
a:散點圖;b:漏斗圖;c:森林圖;d:留一法敏感性分析圖。
3 討論
GERD是否是OSA的危險因素一直存在爭議,一項來自韓國的隊列研究[14]表明經內窺鏡證實的GERD與更嚴重的OSA相關,GERD更常見于OSA患者中[14,31]。然而也有研究表明OSA與非OSA患者的GERD患病率沒有差異[32],GERD和OSA具有相似的危險因素,他們之間的關聯可能僅僅是共同風險因素的反映[33]。本研究旨在通過兩樣本MR分析探討GERD與OSA及其典型癥狀之間的因果關系,這是第一個通過對大規模GWAS數據進行MR分析來探討GERD與OSA之間的因果關系的研究,豐富了以往相關研究的結果。
本研究發現GERD和OSA之間存在因果關系,基因水平上的GERD與OSA風險呈正相關,與觀察性研究的結果一致[34]。有調查發現,在診斷為GERD的22 677 620例患者中,同時診斷為OSA的患者占比12.21%,未診斷為GERD的患者OSA患病率為4.79%[34],GERD患者的OSA患病率明顯高于非GERD患者。Gilani等[35]的研究也發現,在匹配了年齡、性別、種族、肥胖、鼻竇和喉部疾病、哮喘及其它肺部疾病等可能的混雜因素后,GERD仍與OSA獨立相關。GERD夜間反流癥狀可導致睡眠覺醒次數增加、睡眠剝奪和喉頭水腫,從而加重上呼吸道阻塞,引起或加重OSA[10,11]。研究發現AHI與弱胃酸反流有關[36],夜間胃反流激活自主神經系統,增加迷走神經刺激,引起支氣管收縮,進而導致AHI值增加,引起睡眠障礙[4]。也有研究觀察到治療GERD可以改善睡眠障礙[4],質子泵抑制劑的使用改善了與睡眠障礙相關的生活質量并可改善OSA患者的呼吸暫停指數[37,38]。奧美拉唑治療GERD已被證明可減少呼吸暫停發作[39]。然而,一項旨在評估質子泵抑制劑治療GERD與改善OSA的Meta分析,發現這種方式可能改善夜間睡眠質量,但對AHI沒有影響[40],GERD和OSA關聯的確切機制仍有待進一步研究。
打鼾是一種非常普遍的睡眠狀況,是OSA的主要癥狀之一,但大多數打鼾者并不符合OSA的診斷標準,打鼾應該被視為一個獨立的實體疾病,而不僅僅是OSA的癥狀。據統計,高達78%成年男性和59%成年女性伴有打鼾[41]。白天嗜睡是指白天無法控制的打盹和困倦,容易造成個體注意力不集中、焦慮抑郁等,白天嗜睡在人群中的發生率約為12%~16%[42]。一項大型前瞻性隊列研究發現胃食管反流癥狀與打鼾、白天嗜睡之間有很強的相關性[43]。Emilsson等[44]研究發現在GERD受試者中觀察到的自我報告的打鼾比沒有GERD的受試者更多,并且在調整BMI后,音頻測量的打鼾(>65dB)仍與GERD顯著相關。瑞典一項研究[45]也發現,有持續性夜間胃食管返流癥狀的女性白天嗜睡的患病率明顯高于無夜間胃食管返流癥狀的女性。夜間發生胃食管反流可加重OSA患者白天嗜睡。也有研究發現,在排除OSA導致的白天嗜睡外,白天嗜睡相關的2個參數(斯坦福嗜睡量表、Epworth嗜睡量表)也與GERD相關[46]。本研究也證實了GERD與打鼾、白天嗜睡之間存在因果關系。
本研究的局限性:① 所有納入的參與者都是歐洲人,這減少了人口分層偏差,但種族似乎會影響OSA患者的顱面解剖特征和肥胖傾向,這大約占OSA風險的40%[47,48],因此本研究結果對其他人群的推廣可能有限。② 在GERD與打鼾、白天瞌睡的分析中存在異質性,這可能與原始研究樣本量和研究人群有關,故采用隨機效應IVW法進行分析,未來應通過擴大樣本量、增加分層數據等方法減少異質性。③ 不能完全排除本研究結果受到弱IV偏差影響的可能性,盡管計算的F統計量均>10,并未表明弱IV。
綜上所述,本研究發現GERD與OSA風險及其典型癥狀(打鼾、白天嗜睡)之間存在因果關系,進一步證實了GERD是OSA的獨立危險因素。這些發現對GERD與OSA患者的臨床管理具有重要的指導意義。