基因治療是指將遺傳物質引入患者細胞,通過增強、抑制、編輯或引入目標基因以產生治療或預防的效果。基因治療為遺傳性及獲得性視網膜疾病的治療帶來了積極的影響和巨大的潛力。在不斷優化基因載體的同時,各種遞送方式的探索也為視網膜疾病的基因治療帶來了不同的治療效果。目前主要采用的遞送方式為視網膜下注射、玻璃體腔注射和脈絡膜上腔注射;考慮到轉染效率和遞送方式的安全性,新興的內界膜下注射和無創基因傳遞正在研究中。基因遞送方式的選擇對視網膜疾病基因治療的安全性及有效性至關重要,其不僅與器械、技術發展有關,更重要的是與腺相關病毒的改造、啟動子的選擇以及目的基因轉染的視網膜特定細胞有關。因此,應當綜合考慮上述因素,根據最終基因治療藥物和特定轉染細胞進行綜合考慮,選擇最為合適的基因遞送方式。
引用本文: 梁莉聰, 佘凱芩, 陸方. 視網膜疾病基因治療遞送方式的研究現狀與進展. 中華眼底病雜志, 2024, 40(1): 67-75. doi: 10.3760/cma.j.cn511434-20220803-00435 復制
版權信息: ?四川大學華西醫院華西期刊社《中華眼底病雜志》版權所有,未經授權不得轉載、改編
基因治療是指將遺傳物質引入患者細胞,通過增強、抑制、編輯或引入目標基因以產生理想的效果[1]。眼睛是基因治療的理想器官,基因載體能夠直接遞送到眼睛;其解剖結構的特殊性能很好地限制載體的全身暴露;同時視網膜的相對免疫豁免可以限制治療相關的炎癥反應[2]。遺傳性視網膜疾病(IRD)是一組由至少277個核基因或線粒體基因突變引起的復雜且異質的視力障礙表型,是一種影響不同的視網膜結構和功能的疾病[3]。目前基因治療的臨床試驗已廣泛應用于Leber先天性黑矇(LCA)、視網膜色素變性、色盲、X-連鎖視網膜劈裂癥(XLRS)和新生血管性年齡相關性黃斑變性(nAMD)等視網膜病變[4-8]。主要采用的遞送方式為視網膜下注射(SRI)、玻璃體腔注射(IVI)和脈絡膜上腔注射(SCI)(圖1)[9]。考慮到轉染效率和遞送方式的安全性,新興的內界膜(ILM)下注射和無創基因傳遞(圖1)也在研究當中。不同的傳遞方式各有其優缺點,可針對其特性選擇合適的方式治療不同的視網膜疾病。現就視網膜疾病基因治療的不同基因遞送方式作一綜述。
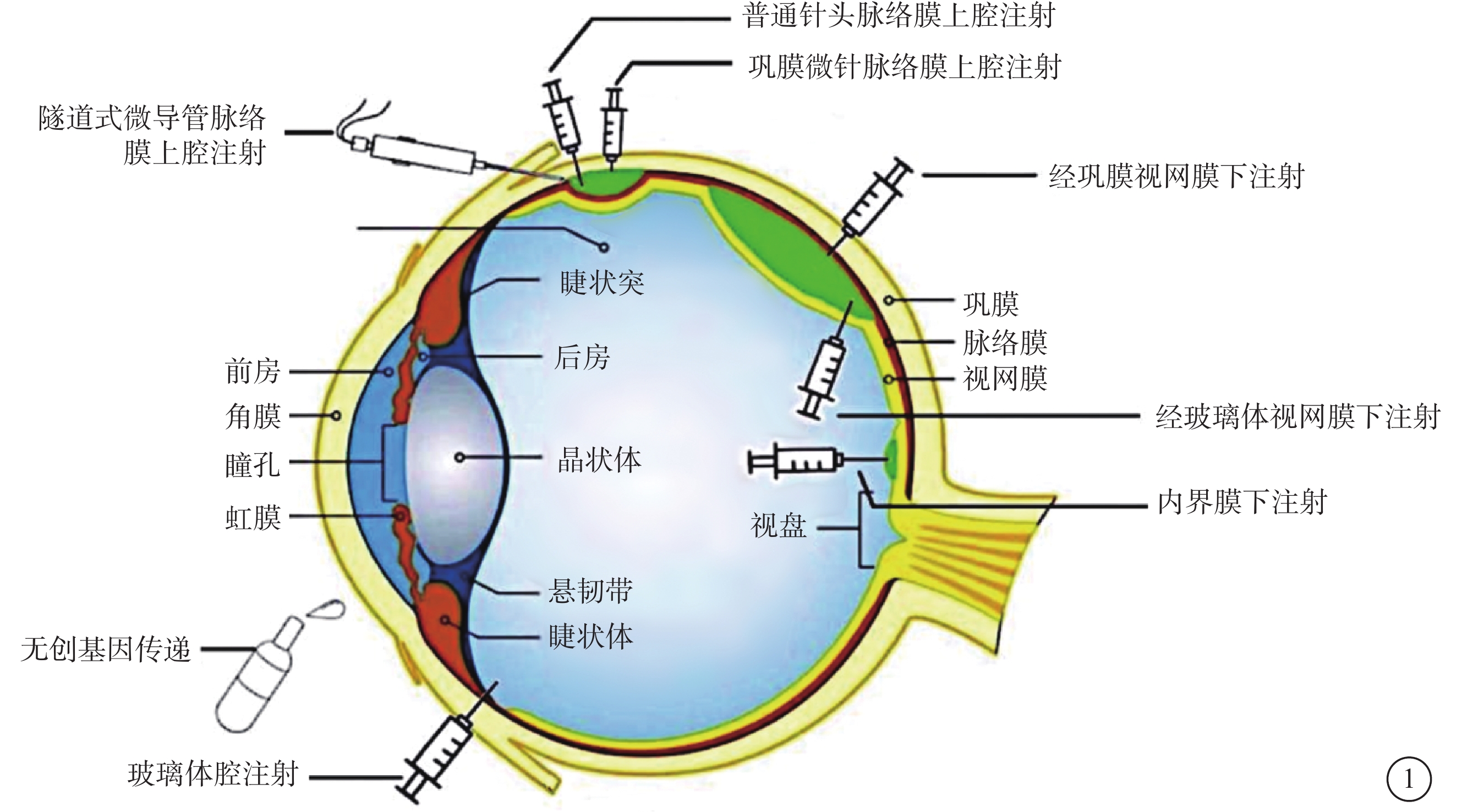
 圖1
視網膜疾病基因治療的載體遞送方式示意圖
圖1
視網膜疾病基因治療的載體遞送方式示意圖
1 SRI
大多數IRD是由光感受器細胞或視網膜色素上皮(RPE)細胞特異性基因的突變引起的。通過SRI遞送,基因治療藥物更接近靶細胞(光感受器細胞和RPE細胞),實現靶細胞的高轉染效率,同時視網膜下腔具有一定的免疫豁免性,引起的免疫反應相對較少,所以SRI被廣泛應用于視網膜疾病的基因治療。然而,SRI卻是一項具有挑戰性的技術。經典的SRI需在注射前行玻璃體切割手術(PPV)和完全的玻璃體后脫離[10]。使用38~41G針頭將病毒載體單點或多點注入視網膜神經上皮層和RPE層之間,病毒載體逐漸擴散至鄰近區域。其操作復雜,治療成本較高,可能出現一系列手術相關的并發癥,包括針尖穿透過深導致視網膜出血或針頭阻塞、意外將載體輸送到脈絡膜上腔或造成永久性的RPE損傷;若針頭過淺,未探及視網膜下,在注射過程中,可形成或加重視網膜結構的破壞;同時PPV本身可能會加重視網膜病變,還可能引發白內障、視網膜脫離、眼內炎和醫源性黃斑裂孔等與PPV相關的并發癥[11]。另外,病毒溶液還可能通過視網膜注射孔返流到玻璃體腔,可刺激炎癥產生且降低轉染率[11]。同時,SRI只能轉染注射泡局部區域的細胞,若要實現大面積的轉染,有時需要進行多點注射來覆蓋所需治療區域[12]。隨著經鞏膜微量注射針頭的出現,使免PPV的SRI成為可能。如此一來,SRI的侵入性小,不僅保留了轉染率高、眼內炎癥反應小的優勢,同時還能夠降低醫源性視網膜撕裂、視網膜脫離或其他玻璃體視網膜手術潛在并發癥的發生率[13]。但目前經鞏膜微針SRI尚未在視網膜疾病基因治療的臨床試驗中使用。
為了提高SRI的安全性,研究者們設計了幾種輔助技術:(1)在給予藥劑之前,首先使用平衡鹽溶液制作預置泡抬高視網膜,以此最大限度地減少藥物的浪費[14]。(2)使用氣動注射器來控制注射速度和壓力[15],避免較高的注射壓力導致的RPE和光感受器受損[16-17],如視網膜過度拉伸、變薄或繼發性黃斑裂孔,同時避免藥劑返流。研究表明,注射壓力與年齡相關,年輕患者往往需要更高壓力來注藥[17]。(3)使用手術中光相干斷層掃描(OCT)檢查輔助確認注射位置[15],避免藥劑注射到脈絡膜上腔或視網膜內層,同時還可估算注射泡體積。
改善SRI的有效性可以通過重復注射來實現,Weed等[18]評估了非人類靈長類動物(NHP)同一只眼睛的相同部位和不同部位進行SRI,其免疫學和結構上都有良好的耐受性。另外,可以通過合理設計和定向進化等方式增加載體的有效性。研究表明,使用合理設計的方法研究出腺相關病毒(AAV)2和AAV5新變體:新型硫酸乙酰肝素結合敲除AAV2變體AAV2-HBKO在視網膜外層向小鼠或NHP傳遞載體時表現出高水平的轉導和轉基因表達,AAV5變體AAV5S194G-增強綠色熒光蛋白(eGFP)變體在光感受器細胞中的eGFP表達顯著增加[19]。
大量的臨床試驗表明,對于LCA、MERTK相關視網膜色素變性(RP)、REP1相關無脈絡膜癥、新生血管性AMD等視網膜疾病,SRI遞送載體具有良好的安全性和有效性(表1)[20-28]。而對于Usher綜合癥、CNGA3和CNGB3相關全色盲、RLBP1相關RP,RPGR相關的RP等疾病的SRI遞送基因治療尚處于動物實驗階段,但實驗結果也證實該方法安全有效,除了眼內炎癥(該眼內炎癥隨著時間推移而改善)和劑量依賴性視網膜變薄外,無其他不良反應發生[29-33]。Min等[34]將載體通過SRI治療XLRS模型小鼠,其發現小鼠的視網膜結構及功能均顯著改善。
2 IVI
通過IVI,基因治療藥物最容易轉染神經節細胞層。Leber遺傳性視神經病變(LHON)的病變部位主要位于神經纖維層,通過IVI的載體距離神經纖維層最近,且IVI能夠有效轉染該層[43],這使LHON成為通過IVI治療的理想視網膜疾病。通過IVI治療LHON的臨床試驗顯示了良好的安全性及耐受性,且能提高患者視力(表2)[35-42]。
在基因治療之前,該技術已經廣泛用于注射抗血管內皮生長因子(VEGF)藥物以治療nAMD和糖尿病黃斑水腫(DME),其操作簡單,在門診即可完成,易于在臨床開展。注射通常使用30G或更小的針頭進行,可安全耐受約0.1 ml的液體,伴有短暫的眼內壓升高。液體返流通常很少,可以用棉簽按壓注射部位[44]。另外,IVI具有全視網膜轉導的潛力,與SRI只能轉染注射泡局部區域的細胞相比,具有一定優勢。同時,由于大多數IRD存在光感受器細胞丟失,視網膜結構逐漸變得脆弱,SRI引起的機械損傷可能會導致反應性神經膠質增生和細胞功能喪失,進一步損害視網膜的功能[45]。并且,IVI侵襲性小,可以避免視網膜受到玻璃體手術帶來的機械損害[46]。以上優勢使得IVI成為遞送IRD基因治療藥物的一種理想的方式。
采用IVI治療IRD,受到ILM和內層視網膜的阻礙,載體不能很好地轉導至外層視網膜。ILM在黃斑中心凹、血管周圍和外周區域較薄,導致載體僅在這些部位進行有效的轉導,不幸的是,人類及NHP的ILM比嚙齒類動物更厚[47]。另外,IVI遞送的基因治療藥物可能受到玻璃體的稀釋或中和,降低病毒的轉染效率。研究表明,IVI的稀釋效應對長期藥物分布影響并不大[48]。
與視網膜下腔的相對免疫豁免不同,宿主玻璃體中可能已有抗AAV中和抗體,中和病毒、降低載體完整性和產量,并誘發炎癥反應[49]。動物實驗表明,在小鼠和NHP中,首次注射可以引起抗AAV體液反應,導致轉導量降低[50];同時由于AAV血清型之間表面抗原的交叉反應性,可能對相同基因產物或類似載體的再注射產生影響[51]。載體在眼外其他組織的分布也是評價基因治療不良反應的重要參數之一。研究表明,相比于SRI,IVI遞送的載體在血液和引流淋巴組織中的分布更高,持續時間更長(長達13周),其脫靶蓄積增加可能導致轉染效率降低[52]。
為了提高外層視網膜轉染效率,需要一種能夠從玻璃體中“穿透”ILM的AAV衣殼。通過定向進化和合理設計策略優化病毒衣殼設計,提高載體跨ILM滲透性和靶細胞特異性。定向進化是利用初始的大型衣殼庫,迭代選擇所需的衣殼使其具備更好的光感受器和RPE趨向性、ILM穿過能力或對中和抗體的抵抗力。定向進化出的AAV變體NHP#9及NHP#26,能夠更好轉染NHP外層視網膜細胞[53]。Pavlou等[54]采用了小鼠體內篩選的方式得到了新的AAV衣殼變體AAV2.GL和AAV2.NN,在小鼠、狗和NHP中通過IVI能介導廣泛和高水平的視網膜轉導,AAV2.GL可以實現Cnga3蛋白在視錐細胞中的廣泛表達。此外,重組AAV經過合理設計后形成自我互補的載體序列,可選擇性地將酪氨酸表面殘基誘變成其他氨基酸,從而提高其生存能力和轉染效率[55]。合理設計策略包括通過第二代工程化衣殼設計,將攜帶編碼阿柏西普轉基因的AAV2.7m8經IVI導入實現有效地轉導視網膜[8]。還有研究提出其他提高玻璃體內遞送效率的方法,手術剝除ILM和蛋白酶消化ILM[56-57]。為了改善載體的中和作用,目前正在研究能夠“逃脫”中和作用的AAV衣殼[58]。Pavlou等[54]發現,AAV中環4的幾何形狀被誘導變化后,形成的AAV變體對中和作用敏感性降低。Mével等[59]表明,AAV衣殼的化學修飾也會影響宿主的免疫反應,將N-乙酰半乳糖胺轉移到AAV2衣殼表面的賴氨酸殘基上后轉染效率提高。
基于IVI的基因治療已針對XLRS、LHON和nAMD等疾病開展了相關實驗室研究和臨床試驗[35-42]。IVI基因治療載體用于XLRS之初,大量的臨床前試驗包括小鼠、兔、NHP中都顯示出良好的安全性。即便有輕度的短期眼內炎癥,也都是自限和劑量依賴性的[60-62],載體在眼外組織中雖有分布,但未發現相關損害[61]。目前,有兩項XLRS的基因治療試驗正在進行中,其主要目的是評估安全性以及劑量的優化,均采用IVI進行AAV遞送[35-42]。然而,試驗6個月中期試驗(NCT號:02416622)臨床數據表明該試驗沒有產生臨床療效的跡象。因此該試驗終止后,重新開始探究SRI治療XLRS的可能性[63]。
3 SCI
SCI是一種相對較新的眼部AAV遞送模式,可以避免玻璃體視網膜手術實現載體的有效遞送和視網膜轉導。脈絡膜上腔是脈絡膜和鞏膜壁之間的一個潛在腔隙[2],目前脈絡膜上腔給藥的最佳研究應用是皮質類固醇注射治療繼發的非感染性葡萄膜炎和視網膜靜脈阻塞的黃斑水腫[64]。
注射方式包括直接注射、經鞏膜微針注射和基于微導管的注射。直接注射是使用標準注射針頭直接注射病毒載體,針頭穿過鞏膜在角膜緣附近切向前進,當推注阻力減小時,液體緩慢注入,使得脈絡膜上腔擴張。注入的液體可能會在脈絡膜上腔內向四周流動,從而實現病毒的廣泛轉導。然而,徒手注射難以控制精準度,同時存在脈絡膜或視網膜穿孔的風險[65]。經鞏膜微針技術是使用長度為700~1 100 μm的針頭進行SCI,可以在局部麻醉下于門診注射室進行。該注射方式的安全性已在臨床試驗中得到驗證[64]。該注射方式已經體現出有效的視網膜轉染[13]。進一步改進微針通路和優化病毒載體特異性有望實現在門診進行SCI基因治療。此外,脈絡膜上腔隧道式微導管(導管內含有照明光纖)還可將藥物輸送到眼后極部[66]。
SCI遞送藥物具有獨特的優勢,它距離受影響的脈絡膜視網膜組織近,且給藥后能夠廣泛擴散,并且避免損傷眼內結構。另外,脈絡膜上腔僅作為容納藥物的儲存空間,不會稀釋藥液[48]。臨床前研究表明,SCI是遞送基因治療藥物的潛在有效途徑[67]。多項動物研究證明,AAV和非病毒載體經SCI后能夠表達目的基因和蛋白[68-69],且SCI較SRI可以實現更多更廣泛的外核層轉導[68]。
盡管SCI基因治療引起的全身炎癥反應和全身分布較IVI少,但有研究表明,SCIAAV8注射比SRI或IVI引起的炎癥細胞局部浸潤更明顯,可能是由于脈絡膜上腔在血視網膜屏障之外,使其缺乏免疫豁免,易與脈絡膜和鞏膜中的巨噬細胞接觸[49]。另外,由于脈絡膜毛細血管的快速清除,脈絡膜上腔給藥后視網膜的有效轉導可能會受到阻礙[70]。此外,各種抗血管生成蛋白,如貝伐單抗和雷珠單抗等大分子,受到脈絡膜和視網膜之間通透性限制,不能從脈絡膜進入視網膜,SCI的有效性也受到限制[48]。研究者提出通過離子電滲療法、使用膠原酶擴大脈絡膜上腔,增加注射量或多次注射來優化脈絡膜上腔給藥[71]。受解剖和組織學特征影響,經脈絡膜上腔注入的液體更傾向于向外周分布而不是向黃斑彌散[72]。所以SCI基因治療更適于外周視網膜、RPE疾病,或新生血管性視網膜疾病,而不是黃斑疾病或光感受器疾病[2]。
nAMD的臨床試驗AAVIATE(NCT號:04514653)中,經SCI遞送RGX-314,6個月中期數據報告了與對照組相似的輕度眼內炎癥,使用皮質類固醇可恢復,具有良好的耐受性。視功能和視網膜結構穩定,并顯著降低抗VEGF藥物的治療負擔[73]。現正在招募在不使用皮質類固醇的前提下接受更高劑量基因治療的患者[73]。評估SCI-RGX-314治療DME的安全性、耐受性和有效性的臨床試驗ALTITUDE(NCT號:04567550),其3個月的中期數據僅報道受試者視力的好轉,尚未報道安全性及其他有效性指標[74]。
4 ILM下注射
ILM下注射是一項新的注射方式。與IVI不同,ILM下注射可以同時避免載體稀釋、中和以及ILM限制轉染等因素。注射方式為在玻璃體切除后,通過ILM下注射黏彈劑,類似SRI的預置泡,沖洗出黏彈劑后注射載體[75],或在驗證黏彈劑與載體混合注射不會影響載體的轉導后,將載體和黏彈劑1∶1混合注射至ILM[76]。
ILM下注射的安全性良好,目前尚未觀察到免疫反應和結構變化,且實現了視網膜神經節細胞均勻、廣泛的轉導。同時Müller細胞、雙極細胞、光感受器細胞、外側膝狀體核、上丘和前頂蓋中都觀察到病毒轉導[75]。
雖然ILM下注射可以規避IVI中ILM的阻礙,但是該操作的容錯率同樣很小,針頭過深可能進入視網膜層間或者進入視網膜下,試驗中需要通過手術后立即的OCT檢測確保載體注射至ILM下而不是視網膜下[76]。注射過淺或者載體通過注射位點滲漏至玻璃體腔,導致實際載體劑量少于理想的載體劑量,甚至誘導玻璃體腔的局部炎癥反應[75]。目前尚無ILM下注射基因治療的臨床研究。
5 無創基因遞送
以上所述的基因傳遞方法均為有創遞送方式,近年有研究探索了通過眼表滴劑實現眼后節的無創基因遞送的可能性。無創基因傳遞可能會增加患者治療的依從性,同時減少手術相關的并發癥。
滴眼液因為富含大量負電荷,且分子量較大,難以轉運至眼后節。而細胞穿透肽,帶正電荷且通常少于30個氨基酸殘基,能夠通過受體非依賴性途徑輕松內化到細胞中[77]。細胞穿透肽中的一種滲透素具有出色的眼滲透性,可以通過局部滴注將共價結合的熒光團轉運到眼底[78]。此外,由多臂聚乙二醇核心和幾個延伸滲透素觸手組成的“章魚狀”柔性多價滲透素,部分滲透素觸須通過靜電相互作用自發結合,凝聚基因,同時與陰離子核酸組裝;而其他觸須則伸出以實現核酸的眼部滲透和眼內遞送[79]。另外,聚酰胺胺樹枝狀大分子(PAMAM)是一種非病毒基因載體,具有很強的基因縮合和保護能力,可以濃縮質粒使其變得更緊密,以增加轉運[80]。目標基因與上述物質結合可制備基因藥物滴眼液。
盡管此類復合物易于制備,對眼部細胞的滲透性和轉染能力強、細胞毒性低。但是,核酸的固有性質,即攜帶負電荷和分子量大;以及淚液分泌帶來的稀釋、角膜不滲透性和鼻淚管引流等都導致其生物利用度不佳[81]。此外,不可生物降解的PAMAM可能有細胞毒性,滲透素和陽離子聚合物與陰離子核酸之間的競爭性結合也可能會損害滲透素的內眼滲透性[77]。
研究發現,制劑滴入大鼠結膜囊后,復合物迅速從眼表滲入眼底,并在視網膜中停留8 h以上,導致紅色熒光蛋白在眼后節有效表達[82]。Tai等[83]研究發現,滲透素/透明質酸/PAMAM/反寡義核苷(ASO)復合體在眼后節分布更多,ASO在視網膜中的停留時間延長8 h。Jiang等[79]研究發現,局部滴注載有小干擾RNA的復合物主要通過非角膜途徑吸收到眼睛中,并且可有效抑制眼內視網膜母細胞瘤模型中的蛋白質表達。更重要的是,該復合物中的8價滲透素在安全性和效率上均優于市售轉染試劑。目前尚無相關無創基因治療運用到眼后節疾病的治療及臨床試驗。
6 小結與展望
確保眼部基因治療的成功實施,關鍵在于采取既安全又有效的基因遞送方式非常重要。大量動物實驗及臨床試驗證實,SRI和IVI仍是目前視網膜疾病治療的主要途徑。SRI已經廣泛用于視網膜疾病的治療,為了更好規避手術相關并發癥的發生,還未應用于臨床的經鞏膜微針的SRI不失為今后視網膜疾病基因治療的理想選擇。IVI較其他幾種方式來說,障礙主要在于全身及局部炎癥反應更重,通過病毒的改造和糖皮質激素的應用可以適當克服。載體通過玻璃體腔注藥主要接觸內層視網膜,故主要使用于神經纖維層受損的疾病如LHON,或視網膜結構較為脆弱的疾病如XLRS。兩項XLRS效果欠佳的臨床試驗提示,SRI可能成為替代IVI的另一種選擇。近年來SCI的研究也正在興起,各種動物實驗及nAMD、DME的臨床試驗,為其他IRD的治療提供了借鑒。雖然有關ILM下注射和無創基因傳遞的相關研究很少,但這為視網膜疾病的治療提供了新的思路和方法,需要更多的臨床前試驗來提供證據支持。基因治療的不同遞送方式選擇不僅與器械、技術的發展有關,AAV的改造、特異性啟動子以及目的基因轉染的視網膜特定細胞也同樣重要。因此,應當綜合考慮上述因素,根據最終基因治療藥物和特定轉染細胞進行綜合考慮,選擇最為合適的基因遞送方式。
基因治療是指將遺傳物質引入患者細胞,通過增強、抑制、編輯或引入目標基因以產生理想的效果[1]。眼睛是基因治療的理想器官,基因載體能夠直接遞送到眼睛;其解剖結構的特殊性能很好地限制載體的全身暴露;同時視網膜的相對免疫豁免可以限制治療相關的炎癥反應[2]。遺傳性視網膜疾病(IRD)是一組由至少277個核基因或線粒體基因突變引起的復雜且異質的視力障礙表型,是一種影響不同的視網膜結構和功能的疾病[3]。目前基因治療的臨床試驗已廣泛應用于Leber先天性黑矇(LCA)、視網膜色素變性、色盲、X-連鎖視網膜劈裂癥(XLRS)和新生血管性年齡相關性黃斑變性(nAMD)等視網膜病變[4-8]。主要采用的遞送方式為視網膜下注射(SRI)、玻璃體腔注射(IVI)和脈絡膜上腔注射(SCI)(圖1)[9]。考慮到轉染效率和遞送方式的安全性,新興的內界膜(ILM)下注射和無創基因傳遞(圖1)也在研究當中。不同的傳遞方式各有其優缺點,可針對其特性選擇合適的方式治療不同的視網膜疾病。現就視網膜疾病基因治療的不同基因遞送方式作一綜述。
 圖1
視網膜疾病基因治療的載體遞送方式示意圖
圖1
視網膜疾病基因治療的載體遞送方式示意圖
1 SRI
大多數IRD是由光感受器細胞或視網膜色素上皮(RPE)細胞特異性基因的突變引起的。通過SRI遞送,基因治療藥物更接近靶細胞(光感受器細胞和RPE細胞),實現靶細胞的高轉染效率,同時視網膜下腔具有一定的免疫豁免性,引起的免疫反應相對較少,所以SRI被廣泛應用于視網膜疾病的基因治療。然而,SRI卻是一項具有挑戰性的技術。經典的SRI需在注射前行玻璃體切割手術(PPV)和完全的玻璃體后脫離[10]。使用38~41G針頭將病毒載體單點或多點注入視網膜神經上皮層和RPE層之間,病毒載體逐漸擴散至鄰近區域。其操作復雜,治療成本較高,可能出現一系列手術相關的并發癥,包括針尖穿透過深導致視網膜出血或針頭阻塞、意外將載體輸送到脈絡膜上腔或造成永久性的RPE損傷;若針頭過淺,未探及視網膜下,在注射過程中,可形成或加重視網膜結構的破壞;同時PPV本身可能會加重視網膜病變,還可能引發白內障、視網膜脫離、眼內炎和醫源性黃斑裂孔等與PPV相關的并發癥[11]。另外,病毒溶液還可能通過視網膜注射孔返流到玻璃體腔,可刺激炎癥產生且降低轉染率[11]。同時,SRI只能轉染注射泡局部區域的細胞,若要實現大面積的轉染,有時需要進行多點注射來覆蓋所需治療區域[12]。隨著經鞏膜微量注射針頭的出現,使免PPV的SRI成為可能。如此一來,SRI的侵入性小,不僅保留了轉染率高、眼內炎癥反應小的優勢,同時還能夠降低醫源性視網膜撕裂、視網膜脫離或其他玻璃體視網膜手術潛在并發癥的發生率[13]。但目前經鞏膜微針SRI尚未在視網膜疾病基因治療的臨床試驗中使用。
為了提高SRI的安全性,研究者們設計了幾種輔助技術:(1)在給予藥劑之前,首先使用平衡鹽溶液制作預置泡抬高視網膜,以此最大限度地減少藥物的浪費[14]。(2)使用氣動注射器來控制注射速度和壓力[15],避免較高的注射壓力導致的RPE和光感受器受損[16-17],如視網膜過度拉伸、變薄或繼發性黃斑裂孔,同時避免藥劑返流。研究表明,注射壓力與年齡相關,年輕患者往往需要更高壓力來注藥[17]。(3)使用手術中光相干斷層掃描(OCT)檢查輔助確認注射位置[15],避免藥劑注射到脈絡膜上腔或視網膜內層,同時還可估算注射泡體積。
改善SRI的有效性可以通過重復注射來實現,Weed等[18]評估了非人類靈長類動物(NHP)同一只眼睛的相同部位和不同部位進行SRI,其免疫學和結構上都有良好的耐受性。另外,可以通過合理設計和定向進化等方式增加載體的有效性。研究表明,使用合理設計的方法研究出腺相關病毒(AAV)2和AAV5新變體:新型硫酸乙酰肝素結合敲除AAV2變體AAV2-HBKO在視網膜外層向小鼠或NHP傳遞載體時表現出高水平的轉導和轉基因表達,AAV5變體AAV5S194G-增強綠色熒光蛋白(eGFP)變體在光感受器細胞中的eGFP表達顯著增加[19]。
大量的臨床試驗表明,對于LCA、MERTK相關視網膜色素變性(RP)、REP1相關無脈絡膜癥、新生血管性AMD等視網膜疾病,SRI遞送載體具有良好的安全性和有效性(表1)[20-28]。而對于Usher綜合癥、CNGA3和CNGB3相關全色盲、RLBP1相關RP,RPGR相關的RP等疾病的SRI遞送基因治療尚處于動物實驗階段,但實驗結果也證實該方法安全有效,除了眼內炎癥(該眼內炎癥隨著時間推移而改善)和劑量依賴性視網膜變薄外,無其他不良反應發生[29-33]。Min等[34]將載體通過SRI治療XLRS模型小鼠,其發現小鼠的視網膜結構及功能均顯著改善。
2 IVI
通過IVI,基因治療藥物最容易轉染神經節細胞層。Leber遺傳性視神經病變(LHON)的病變部位主要位于神經纖維層,通過IVI的載體距離神經纖維層最近,且IVI能夠有效轉染該層[43],這使LHON成為通過IVI治療的理想視網膜疾病。通過IVI治療LHON的臨床試驗顯示了良好的安全性及耐受性,且能提高患者視力(表2)[35-42]。
在基因治療之前,該技術已經廣泛用于注射抗血管內皮生長因子(VEGF)藥物以治療nAMD和糖尿病黃斑水腫(DME),其操作簡單,在門診即可完成,易于在臨床開展。注射通常使用30G或更小的針頭進行,可安全耐受約0.1 ml的液體,伴有短暫的眼內壓升高。液體返流通常很少,可以用棉簽按壓注射部位[44]。另外,IVI具有全視網膜轉導的潛力,與SRI只能轉染注射泡局部區域的細胞相比,具有一定優勢。同時,由于大多數IRD存在光感受器細胞丟失,視網膜結構逐漸變得脆弱,SRI引起的機械損傷可能會導致反應性神經膠質增生和細胞功能喪失,進一步損害視網膜的功能[45]。并且,IVI侵襲性小,可以避免視網膜受到玻璃體手術帶來的機械損害[46]。以上優勢使得IVI成為遞送IRD基因治療藥物的一種理想的方式。
采用IVI治療IRD,受到ILM和內層視網膜的阻礙,載體不能很好地轉導至外層視網膜。ILM在黃斑中心凹、血管周圍和外周區域較薄,導致載體僅在這些部位進行有效的轉導,不幸的是,人類及NHP的ILM比嚙齒類動物更厚[47]。另外,IVI遞送的基因治療藥物可能受到玻璃體的稀釋或中和,降低病毒的轉染效率。研究表明,IVI的稀釋效應對長期藥物分布影響并不大[48]。
與視網膜下腔的相對免疫豁免不同,宿主玻璃體中可能已有抗AAV中和抗體,中和病毒、降低載體完整性和產量,并誘發炎癥反應[49]。動物實驗表明,在小鼠和NHP中,首次注射可以引起抗AAV體液反應,導致轉導量降低[50];同時由于AAV血清型之間表面抗原的交叉反應性,可能對相同基因產物或類似載體的再注射產生影響[51]。載體在眼外其他組織的分布也是評價基因治療不良反應的重要參數之一。研究表明,相比于SRI,IVI遞送的載體在血液和引流淋巴組織中的分布更高,持續時間更長(長達13周),其脫靶蓄積增加可能導致轉染效率降低[52]。
為了提高外層視網膜轉染效率,需要一種能夠從玻璃體中“穿透”ILM的AAV衣殼。通過定向進化和合理設計策略優化病毒衣殼設計,提高載體跨ILM滲透性和靶細胞特異性。定向進化是利用初始的大型衣殼庫,迭代選擇所需的衣殼使其具備更好的光感受器和RPE趨向性、ILM穿過能力或對中和抗體的抵抗力。定向進化出的AAV變體NHP#9及NHP#26,能夠更好轉染NHP外層視網膜細胞[53]。Pavlou等[54]采用了小鼠體內篩選的方式得到了新的AAV衣殼變體AAV2.GL和AAV2.NN,在小鼠、狗和NHP中通過IVI能介導廣泛和高水平的視網膜轉導,AAV2.GL可以實現Cnga3蛋白在視錐細胞中的廣泛表達。此外,重組AAV經過合理設計后形成自我互補的載體序列,可選擇性地將酪氨酸表面殘基誘變成其他氨基酸,從而提高其生存能力和轉染效率[55]。合理設計策略包括通過第二代工程化衣殼設計,將攜帶編碼阿柏西普轉基因的AAV2.7m8經IVI導入實現有效地轉導視網膜[8]。還有研究提出其他提高玻璃體內遞送效率的方法,手術剝除ILM和蛋白酶消化ILM[56-57]。為了改善載體的中和作用,目前正在研究能夠“逃脫”中和作用的AAV衣殼[58]。Pavlou等[54]發現,AAV中環4的幾何形狀被誘導變化后,形成的AAV變體對中和作用敏感性降低。Mével等[59]表明,AAV衣殼的化學修飾也會影響宿主的免疫反應,將N-乙酰半乳糖胺轉移到AAV2衣殼表面的賴氨酸殘基上后轉染效率提高。
基于IVI的基因治療已針對XLRS、LHON和nAMD等疾病開展了相關實驗室研究和臨床試驗[35-42]。IVI基因治療載體用于XLRS之初,大量的臨床前試驗包括小鼠、兔、NHP中都顯示出良好的安全性。即便有輕度的短期眼內炎癥,也都是自限和劑量依賴性的[60-62],載體在眼外組織中雖有分布,但未發現相關損害[61]。目前,有兩項XLRS的基因治療試驗正在進行中,其主要目的是評估安全性以及劑量的優化,均采用IVI進行AAV遞送[35-42]。然而,試驗6個月中期試驗(NCT號:02416622)臨床數據表明該試驗沒有產生臨床療效的跡象。因此該試驗終止后,重新開始探究SRI治療XLRS的可能性[63]。
3 SCI
SCI是一種相對較新的眼部AAV遞送模式,可以避免玻璃體視網膜手術實現載體的有效遞送和視網膜轉導。脈絡膜上腔是脈絡膜和鞏膜壁之間的一個潛在腔隙[2],目前脈絡膜上腔給藥的最佳研究應用是皮質類固醇注射治療繼發的非感染性葡萄膜炎和視網膜靜脈阻塞的黃斑水腫[64]。
注射方式包括直接注射、經鞏膜微針注射和基于微導管的注射。直接注射是使用標準注射針頭直接注射病毒載體,針頭穿過鞏膜在角膜緣附近切向前進,當推注阻力減小時,液體緩慢注入,使得脈絡膜上腔擴張。注入的液體可能會在脈絡膜上腔內向四周流動,從而實現病毒的廣泛轉導。然而,徒手注射難以控制精準度,同時存在脈絡膜或視網膜穿孔的風險[65]。經鞏膜微針技術是使用長度為700~1 100 μm的針頭進行SCI,可以在局部麻醉下于門診注射室進行。該注射方式的安全性已在臨床試驗中得到驗證[64]。該注射方式已經體現出有效的視網膜轉染[13]。進一步改進微針通路和優化病毒載體特異性有望實現在門診進行SCI基因治療。此外,脈絡膜上腔隧道式微導管(導管內含有照明光纖)還可將藥物輸送到眼后極部[66]。
SCI遞送藥物具有獨特的優勢,它距離受影響的脈絡膜視網膜組織近,且給藥后能夠廣泛擴散,并且避免損傷眼內結構。另外,脈絡膜上腔僅作為容納藥物的儲存空間,不會稀釋藥液[48]。臨床前研究表明,SCI是遞送基因治療藥物的潛在有效途徑[67]。多項動物研究證明,AAV和非病毒載體經SCI后能夠表達目的基因和蛋白[68-69],且SCI較SRI可以實現更多更廣泛的外核層轉導[68]。
盡管SCI基因治療引起的全身炎癥反應和全身分布較IVI少,但有研究表明,SCIAAV8注射比SRI或IVI引起的炎癥細胞局部浸潤更明顯,可能是由于脈絡膜上腔在血視網膜屏障之外,使其缺乏免疫豁免,易與脈絡膜和鞏膜中的巨噬細胞接觸[49]。另外,由于脈絡膜毛細血管的快速清除,脈絡膜上腔給藥后視網膜的有效轉導可能會受到阻礙[70]。此外,各種抗血管生成蛋白,如貝伐單抗和雷珠單抗等大分子,受到脈絡膜和視網膜之間通透性限制,不能從脈絡膜進入視網膜,SCI的有效性也受到限制[48]。研究者提出通過離子電滲療法、使用膠原酶擴大脈絡膜上腔,增加注射量或多次注射來優化脈絡膜上腔給藥[71]。受解剖和組織學特征影響,經脈絡膜上腔注入的液體更傾向于向外周分布而不是向黃斑彌散[72]。所以SCI基因治療更適于外周視網膜、RPE疾病,或新生血管性視網膜疾病,而不是黃斑疾病或光感受器疾病[2]。
nAMD的臨床試驗AAVIATE(NCT號:04514653)中,經SCI遞送RGX-314,6個月中期數據報告了與對照組相似的輕度眼內炎癥,使用皮質類固醇可恢復,具有良好的耐受性。視功能和視網膜結構穩定,并顯著降低抗VEGF藥物的治療負擔[73]。現正在招募在不使用皮質類固醇的前提下接受更高劑量基因治療的患者[73]。評估SCI-RGX-314治療DME的安全性、耐受性和有效性的臨床試驗ALTITUDE(NCT號:04567550),其3個月的中期數據僅報道受試者視力的好轉,尚未報道安全性及其他有效性指標[74]。
4 ILM下注射
ILM下注射是一項新的注射方式。與IVI不同,ILM下注射可以同時避免載體稀釋、中和以及ILM限制轉染等因素。注射方式為在玻璃體切除后,通過ILM下注射黏彈劑,類似SRI的預置泡,沖洗出黏彈劑后注射載體[75],或在驗證黏彈劑與載體混合注射不會影響載體的轉導后,將載體和黏彈劑1∶1混合注射至ILM[76]。
ILM下注射的安全性良好,目前尚未觀察到免疫反應和結構變化,且實現了視網膜神經節細胞均勻、廣泛的轉導。同時Müller細胞、雙極細胞、光感受器細胞、外側膝狀體核、上丘和前頂蓋中都觀察到病毒轉導[75]。
雖然ILM下注射可以規避IVI中ILM的阻礙,但是該操作的容錯率同樣很小,針頭過深可能進入視網膜層間或者進入視網膜下,試驗中需要通過手術后立即的OCT檢測確保載體注射至ILM下而不是視網膜下[76]。注射過淺或者載體通過注射位點滲漏至玻璃體腔,導致實際載體劑量少于理想的載體劑量,甚至誘導玻璃體腔的局部炎癥反應[75]。目前尚無ILM下注射基因治療的臨床研究。
5 無創基因遞送
以上所述的基因傳遞方法均為有創遞送方式,近年有研究探索了通過眼表滴劑實現眼后節的無創基因遞送的可能性。無創基因傳遞可能會增加患者治療的依從性,同時減少手術相關的并發癥。
滴眼液因為富含大量負電荷,且分子量較大,難以轉運至眼后節。而細胞穿透肽,帶正電荷且通常少于30個氨基酸殘基,能夠通過受體非依賴性途徑輕松內化到細胞中[77]。細胞穿透肽中的一種滲透素具有出色的眼滲透性,可以通過局部滴注將共價結合的熒光團轉運到眼底[78]。此外,由多臂聚乙二醇核心和幾個延伸滲透素觸手組成的“章魚狀”柔性多價滲透素,部分滲透素觸須通過靜電相互作用自發結合,凝聚基因,同時與陰離子核酸組裝;而其他觸須則伸出以實現核酸的眼部滲透和眼內遞送[79]。另外,聚酰胺胺樹枝狀大分子(PAMAM)是一種非病毒基因載體,具有很強的基因縮合和保護能力,可以濃縮質粒使其變得更緊密,以增加轉運[80]。目標基因與上述物質結合可制備基因藥物滴眼液。
盡管此類復合物易于制備,對眼部細胞的滲透性和轉染能力強、細胞毒性低。但是,核酸的固有性質,即攜帶負電荷和分子量大;以及淚液分泌帶來的稀釋、角膜不滲透性和鼻淚管引流等都導致其生物利用度不佳[81]。此外,不可生物降解的PAMAM可能有細胞毒性,滲透素和陽離子聚合物與陰離子核酸之間的競爭性結合也可能會損害滲透素的內眼滲透性[77]。
研究發現,制劑滴入大鼠結膜囊后,復合物迅速從眼表滲入眼底,并在視網膜中停留8 h以上,導致紅色熒光蛋白在眼后節有效表達[82]。Tai等[83]研究發現,滲透素/透明質酸/PAMAM/反寡義核苷(ASO)復合體在眼后節分布更多,ASO在視網膜中的停留時間延長8 h。Jiang等[79]研究發現,局部滴注載有小干擾RNA的復合物主要通過非角膜途徑吸收到眼睛中,并且可有效抑制眼內視網膜母細胞瘤模型中的蛋白質表達。更重要的是,該復合物中的8價滲透素在安全性和效率上均優于市售轉染試劑。目前尚無相關無創基因治療運用到眼后節疾病的治療及臨床試驗。
6 小結與展望
確保眼部基因治療的成功實施,關鍵在于采取既安全又有效的基因遞送方式非常重要。大量動物實驗及臨床試驗證實,SRI和IVI仍是目前視網膜疾病治療的主要途徑。SRI已經廣泛用于視網膜疾病的治療,為了更好規避手術相關并發癥的發生,還未應用于臨床的經鞏膜微針的SRI不失為今后視網膜疾病基因治療的理想選擇。IVI較其他幾種方式來說,障礙主要在于全身及局部炎癥反應更重,通過病毒的改造和糖皮質激素的應用可以適當克服。載體通過玻璃體腔注藥主要接觸內層視網膜,故主要使用于神經纖維層受損的疾病如LHON,或視網膜結構較為脆弱的疾病如XLRS。兩項XLRS效果欠佳的臨床試驗提示,SRI可能成為替代IVI的另一種選擇。近年來SCI的研究也正在興起,各種動物實驗及nAMD、DME的臨床試驗,為其他IRD的治療提供了借鑒。雖然有關ILM下注射和無創基因傳遞的相關研究很少,但這為視網膜疾病的治療提供了新的思路和方法,需要更多的臨床前試驗來提供證據支持。基因治療的不同遞送方式選擇不僅與器械、技術的發展有關,AAV的改造、特異性啟動子以及目的基因轉染的視網膜特定細胞也同樣重要。因此,應當綜合考慮上述因素,根據最終基因治療藥物和特定轉染細胞進行綜合考慮,選擇最為合適的基因遞送方式。