引用本文: 郭文駿, 李陽, 任朝臣, 甄文瑞, 劉洪濤. 系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞1例. 中華眼底病雜志, 2024, 40(7): 550-551. doi: 10.3760/cma.j.cn511434-20230609-00260 復制
版權信息: ?四川大學華西醫院華西期刊社《中華眼底病雜志》版權所有,未經授權不得轉載、改編
患者女,26歲。因突發右眼視物不清1 d,于2023年4月13日到遵義醫科大學第二附屬醫院眼科就診。患者半個月前因右側腘靜脈血栓栓塞行下腔靜脈濾器置入手術及尿激酶溶栓、那屈肝素鈉抗凝治療。否認其他全身病史。眼科檢查:右眼、左眼最佳矯正視力分別為數指/10 cm、1.0。右眼、左眼眼壓分別為14、11 mm Hg(1 mm Hg=0.133 kPa)。右眼直接對光反射消失。眼底檢查,右眼視盤水腫,盤緣小片狀出血,視網膜靜脈紆曲擴張,“串珠樣”改變,靜脈旁多發散在視網膜前出血,對應靜脈處可見白色栓子樣梗塞,動脈變細,反光增強(圖1A)。紅外眼底掃描激光檢查,右眼僅見上方及顳側渦靜脈輪廓(圖1B)。光相干斷層掃描(OCT)檢查,右眼黃斑區鼻側視網膜水腫增厚,視網膜層間結構模糊,脈絡膜厚度不均(圖1C)。左眼眼前節及眼底檢查均未見明顯異常。右下肢靜脈CT血管成像檢查,右側股靜脈下段-腘靜脈栓塞,周圍軟組織腫脹(圖2A)。右下肢靜脈3D-CT血管造影檢查,右側脛前、脛后及腓靜脈顯影變淡,右側腘動脈局限性輕度狹窄(圖2B)。實驗室檢查,活化部分凝血活酶時間109.4 s(正常值范圍31~43 s)。給予患者靜脈注射800 ml冰凍血漿補充凝血因子、維生素K40 mg/d促進凝血因子合成。治療2 d后患者自覺右眼視力降至無光感。眼底檢查,右眼視網膜大量散在Roth斑樣出血,視網膜靜脈系統“串珠樣”改變伴多發散在節段性栓子栓塞,黃斑區內界膜隆起伴內界膜下出血(圖3A)。OCT檢查,右眼后極部視網膜重度水腫,層間結構紊亂、內界膜脫離(圖3B)。熒光素眼底血管造影(FFA)檢查,右眼全周視網膜大范圍遮蔽熒光,隱約可見動脈前峰充盈,遮蔽區域見脈絡膜背景熒光彌漫增強;造影晚期仍未見視網膜靜脈熒光充盈(圖3C)。實驗室檢查:抗核抗體(+)、抗雙鏈DNA抗體(+)、抗史密斯抗體(抗SM抗體)(+),抗磷脂抗體、狼瘡抗凝物(+);其余血常規、生物化學檢測結果無明顯異常。血栓彈力檢查,凝血因子及纖維蛋白原活性減弱。診斷:(1)右眼視網膜中央動脈阻塞(CRAO)并視網膜中央靜脈阻塞;(2)系統性紅斑狼瘡(SLE)合并抗磷脂綜合征(APS);(3)狼瘡抗凝物-低凝血酶原綜合征。給予患者眼球按摩、高通量氧氣間斷吸氧、靜脈注射甲潑尼龍琥珀酸鈉免疫抑制、維生素促進凝血因子合成、達肝素鈉抗凝、球后注射硫酸阿托品擴血管、噻嗎洛爾滴眼液點眼降眼壓、血栓通活血化瘀治療。但患者視力無明顯改善。
 圖1
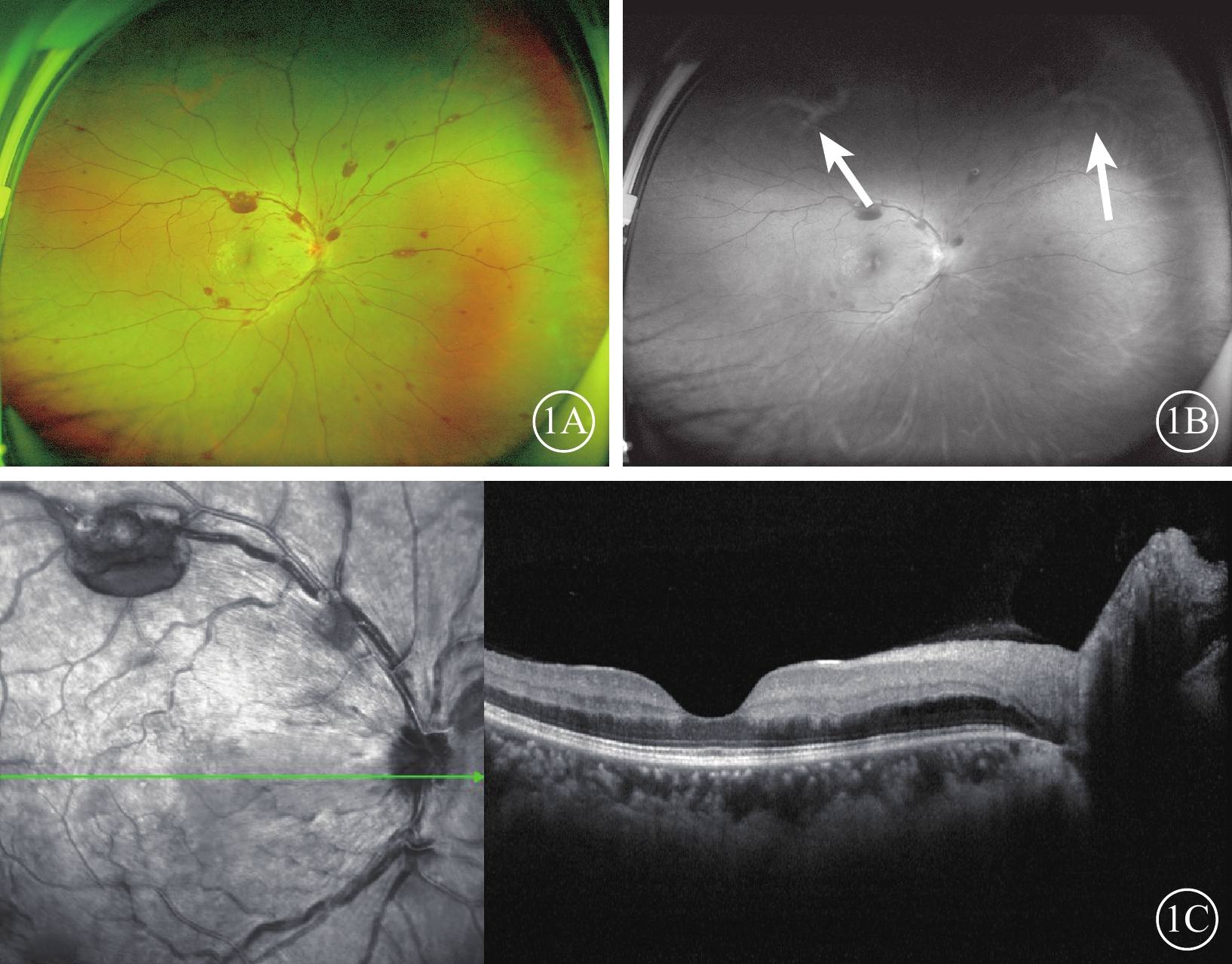
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者初診右眼眼部檢查像
圖1
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者初診右眼眼部檢查像
1A示彩色眼底像,視盤水腫,盤緣小片狀出血,視網膜靜脈紆曲擴張,“串珠樣”改變,靜脈旁多發散在視網膜前出血,對應靜脈處可見白色栓子樣梗塞,動脈變細,反光增強。1B示紅外眼底掃描激光像,脈絡膜大血管形態及背景結構消失,僅見上分及鼻上方渦靜脈輪廓(白箭)。1C示光相干斷層掃描像,左圖為掃描方向和部位,右圖為檢查結果。黃斑區鼻側視網膜水腫增厚,視網膜層間結構模糊,脈絡膜厚度不均
 圖2
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者右下肢靜脈CT像
圖2
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者右下肢靜脈CT像
2A示右下肢靜脈CT血管成像,右側股靜脈下段-腘靜脈栓塞,周圍軟組織腫脹(白箭)。2B示3D-CT血管造影檢查像,右側脛前、脛后及腓靜脈顯影變淡
 圖3
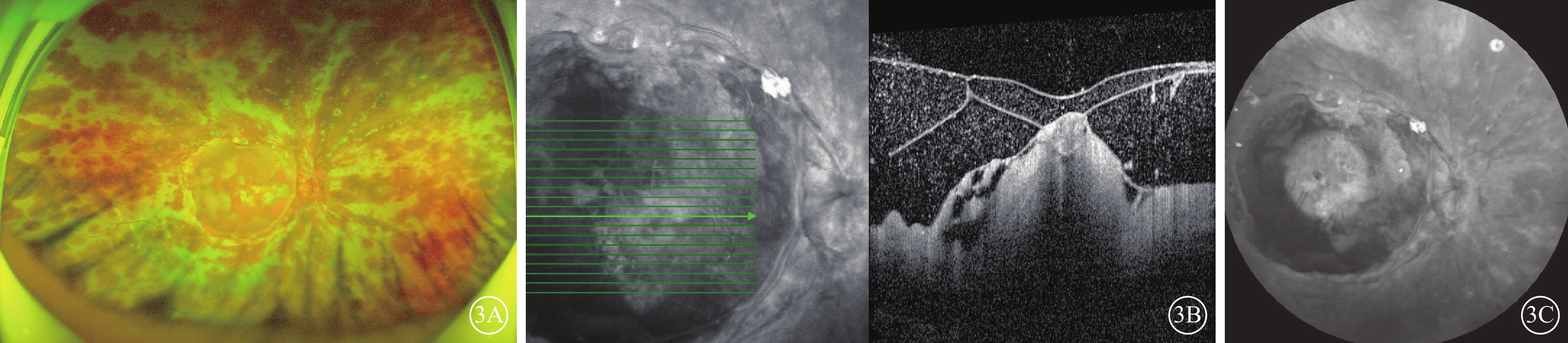
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者治療2 d后右眼眼部檢查像
圖3
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者治療2 d后右眼眼部檢查像
3A示彩色眼底像,視網膜大量散在Roth斑樣出血,視網膜靜脈系統“串珠樣”改變伴多發散在節段性栓子栓塞,黃斑區內界膜隆起伴內界膜下出血。3B示光相干斷層掃描像,左圖為掃描方向和部位,右圖為檢查結果。后極部視網膜重度水腫,層間結構紊亂、內界膜脫離。3C示熒光素眼底血管造影像,全周視網膜大范圍遮蔽熒光,隱約見動脈前峰充盈,遮蔽區域見脈絡膜背景熒光彌漫增強,造影晚期仍未見視網膜靜脈熒光充盈
討論 SLE是一種自身免疫性多系統疾病,其特征是免疫系統失調、免疫復合物形成和補體系統激活。其病變主要累及肌肉骨骼、皮膚、腎臟和眼部[1]。SLE患者伴發視網膜病變的發生率為3.3%~28.1%[2],通常認為是免疫復合物介導的血管炎和以纖維蛋白為主的血栓形成所致,可表現為嚴重的血管閉塞性視網膜病變,其中APS與血栓風險相關。20%的SLE患者可繼發APS。APS以反復動脈或者靜脈血栓、習慣性流產和抗磷脂抗體持續陽性為特征[3]。本例患者以右下肢深靜脈血栓就診,視網膜多發靜脈栓塞且進展迅速。臨床上需與巨細胞動脈炎、眼缺血綜合征、鐮狀細胞貧血視網膜病變等鑒別。既往報道APS患者多因病情進展較快,而很少見到疾病眼底病變的初期表現[4-5]。本例患者疾病早期,可見視網膜大血管處血栓形成并伴周邊視網膜局灶性出血類似Roth斑,這可能是病情惡化的信號。由于自身免疫導致反復血栓形成,初期血栓若無相關干預,后期血液瘀滯,血小板持續活化聚集,血栓節段性形成的惡性循環,導致預后極差。本例患者初診時未見典型CRAO“櫻桃紅斑”改變,考慮可能合并脈絡膜血管栓塞致脈絡膜循環障礙,同時視網膜循環受阻,表現類似眼缺血綜合征。
SLE伴APS所致視網膜血管阻塞患者視力預后不佳,治療較為棘手。本例患者經常規抗凝、溶栓、糖皮質激素沖擊及免疫調節治療效果不佳。
SLE疾病初期常伴隨一些典型的眼底改變,棉絨斑、微動脈瘤、硬性滲出、Purtscher樣視網膜病變等[6]。但本例患者無典型的眼底改變,其視網膜水腫、視網膜動靜脈、脈絡膜循環障礙,反映了全身血管病變的嚴重性。
臨床對于年輕患者單眼的視網膜動靜脈阻塞并多發血栓形成,應注意尋找全身危險因素,結合免疫學檢查做出正確診斷。同時對癥狀不典型的視網膜血管阻塞性疾病需仔細評估局部及全身檢查,及早的干預治療可能避免發生后期嚴重的預后不良。這提示即使是單眼視網膜散在出血合并血管栓塞,臨床上應注意尋找全身危險因素,結合免疫學檢查做出正確診斷。
患者女,26歲。因突發右眼視物不清1 d,于2023年4月13日到遵義醫科大學第二附屬醫院眼科就診。患者半個月前因右側腘靜脈血栓栓塞行下腔靜脈濾器置入手術及尿激酶溶栓、那屈肝素鈉抗凝治療。否認其他全身病史。眼科檢查:右眼、左眼最佳矯正視力分別為數指/10 cm、1.0。右眼、左眼眼壓分別為14、11 mm Hg(1 mm Hg=0.133 kPa)。右眼直接對光反射消失。眼底檢查,右眼視盤水腫,盤緣小片狀出血,視網膜靜脈紆曲擴張,“串珠樣”改變,靜脈旁多發散在視網膜前出血,對應靜脈處可見白色栓子樣梗塞,動脈變細,反光增強(圖1A)。紅外眼底掃描激光檢查,右眼僅見上方及顳側渦靜脈輪廓(圖1B)。光相干斷層掃描(OCT)檢查,右眼黃斑區鼻側視網膜水腫增厚,視網膜層間結構模糊,脈絡膜厚度不均(圖1C)。左眼眼前節及眼底檢查均未見明顯異常。右下肢靜脈CT血管成像檢查,右側股靜脈下段-腘靜脈栓塞,周圍軟組織腫脹(圖2A)。右下肢靜脈3D-CT血管造影檢查,右側脛前、脛后及腓靜脈顯影變淡,右側腘動脈局限性輕度狹窄(圖2B)。實驗室檢查,活化部分凝血活酶時間109.4 s(正常值范圍31~43 s)。給予患者靜脈注射800 ml冰凍血漿補充凝血因子、維生素K40 mg/d促進凝血因子合成。治療2 d后患者自覺右眼視力降至無光感。眼底檢查,右眼視網膜大量散在Roth斑樣出血,視網膜靜脈系統“串珠樣”改變伴多發散在節段性栓子栓塞,黃斑區內界膜隆起伴內界膜下出血(圖3A)。OCT檢查,右眼后極部視網膜重度水腫,層間結構紊亂、內界膜脫離(圖3B)。熒光素眼底血管造影(FFA)檢查,右眼全周視網膜大范圍遮蔽熒光,隱約可見動脈前峰充盈,遮蔽區域見脈絡膜背景熒光彌漫增強;造影晚期仍未見視網膜靜脈熒光充盈(圖3C)。實驗室檢查:抗核抗體(+)、抗雙鏈DNA抗體(+)、抗史密斯抗體(抗SM抗體)(+),抗磷脂抗體、狼瘡抗凝物(+);其余血常規、生物化學檢測結果無明顯異常。血栓彈力檢查,凝血因子及纖維蛋白原活性減弱。診斷:(1)右眼視網膜中央動脈阻塞(CRAO)并視網膜中央靜脈阻塞;(2)系統性紅斑狼瘡(SLE)合并抗磷脂綜合征(APS);(3)狼瘡抗凝物-低凝血酶原綜合征。給予患者眼球按摩、高通量氧氣間斷吸氧、靜脈注射甲潑尼龍琥珀酸鈉免疫抑制、維生素促進凝血因子合成、達肝素鈉抗凝、球后注射硫酸阿托品擴血管、噻嗎洛爾滴眼液點眼降眼壓、血栓通活血化瘀治療。但患者視力無明顯改善。
 圖1
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者初診右眼眼部檢查像
圖1
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者初診右眼眼部檢查像
1A示彩色眼底像,視盤水腫,盤緣小片狀出血,視網膜靜脈紆曲擴張,“串珠樣”改變,靜脈旁多發散在視網膜前出血,對應靜脈處可見白色栓子樣梗塞,動脈變細,反光增強。1B示紅外眼底掃描激光像,脈絡膜大血管形態及背景結構消失,僅見上分及鼻上方渦靜脈輪廓(白箭)。1C示光相干斷層掃描像,左圖為掃描方向和部位,右圖為檢查結果。黃斑區鼻側視網膜水腫增厚,視網膜層間結構模糊,脈絡膜厚度不均
 圖2
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者右下肢靜脈CT像
圖2
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者右下肢靜脈CT像
2A示右下肢靜脈CT血管成像,右側股靜脈下段-腘靜脈栓塞,周圍軟組織腫脹(白箭)。2B示3D-CT血管造影檢查像,右側脛前、脛后及腓靜脈顯影變淡
 圖3
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者治療2 d后右眼眼部檢查像
圖3
系統性紅斑狼瘡并抗磷脂綜合征致視網膜中央動靜脈阻塞患者治療2 d后右眼眼部檢查像
3A示彩色眼底像,視網膜大量散在Roth斑樣出血,視網膜靜脈系統“串珠樣”改變伴多發散在節段性栓子栓塞,黃斑區內界膜隆起伴內界膜下出血。3B示光相干斷層掃描像,左圖為掃描方向和部位,右圖為檢查結果。后極部視網膜重度水腫,層間結構紊亂、內界膜脫離。3C示熒光素眼底血管造影像,全周視網膜大范圍遮蔽熒光,隱約見動脈前峰充盈,遮蔽區域見脈絡膜背景熒光彌漫增強,造影晚期仍未見視網膜靜脈熒光充盈
討論 SLE是一種自身免疫性多系統疾病,其特征是免疫系統失調、免疫復合物形成和補體系統激活。其病變主要累及肌肉骨骼、皮膚、腎臟和眼部[1]。SLE患者伴發視網膜病變的發生率為3.3%~28.1%[2],通常認為是免疫復合物介導的血管炎和以纖維蛋白為主的血栓形成所致,可表現為嚴重的血管閉塞性視網膜病變,其中APS與血栓風險相關。20%的SLE患者可繼發APS。APS以反復動脈或者靜脈血栓、習慣性流產和抗磷脂抗體持續陽性為特征[3]。本例患者以右下肢深靜脈血栓就診,視網膜多發靜脈栓塞且進展迅速。臨床上需與巨細胞動脈炎、眼缺血綜合征、鐮狀細胞貧血視網膜病變等鑒別。既往報道APS患者多因病情進展較快,而很少見到疾病眼底病變的初期表現[4-5]。本例患者疾病早期,可見視網膜大血管處血栓形成并伴周邊視網膜局灶性出血類似Roth斑,這可能是病情惡化的信號。由于自身免疫導致反復血栓形成,初期血栓若無相關干預,后期血液瘀滯,血小板持續活化聚集,血栓節段性形成的惡性循環,導致預后極差。本例患者初診時未見典型CRAO“櫻桃紅斑”改變,考慮可能合并脈絡膜血管栓塞致脈絡膜循環障礙,同時視網膜循環受阻,表現類似眼缺血綜合征。
SLE伴APS所致視網膜血管阻塞患者視力預后不佳,治療較為棘手。本例患者經常規抗凝、溶栓、糖皮質激素沖擊及免疫調節治療效果不佳。
SLE疾病初期常伴隨一些典型的眼底改變,棉絨斑、微動脈瘤、硬性滲出、Purtscher樣視網膜病變等[6]。但本例患者無典型的眼底改變,其視網膜水腫、視網膜動靜脈、脈絡膜循環障礙,反映了全身血管病變的嚴重性。
臨床對于年輕患者單眼的視網膜動靜脈阻塞并多發血栓形成,應注意尋找全身危險因素,結合免疫學檢查做出正確診斷。同時對癥狀不典型的視網膜血管阻塞性疾病需仔細評估局部及全身檢查,及早的干預治療可能避免發生后期嚴重的預后不良。這提示即使是單眼視網膜散在出血合并血管栓塞,臨床上應注意尋找全身危險因素,結合免疫學檢查做出正確診斷。