引用本文: 鄭志坤, 康文偉, 楊怡, 李娟娟. 慢性中心性漿液性脈絡膜視網膜病變所致黃斑囊樣變性的臨床觀察. 中華眼底病雜志, 2024, 40(3): 196-201. doi: 10.3760/cma.j.cn511434-20231023-00427 復制
版權信息: ?四川大學華西醫院華西期刊社《中華眼底病雜志》版權所有,未經授權不得轉載、改編
慢性中心性漿液性脈絡膜視網膜病變(cCSC)中持續或反復的黃斑區視網膜神經上皮層下漿液存留可導致視網膜神經上皮層結構發生變性樣改變,此種改變在光相干斷層掃描(OCT)上可見囊樣間隙,臨床將其定義為黃斑囊樣變性(CMD)[1-2]。CMD形態類似于黃斑囊樣水腫(CME),部分臨床醫生對兩者的認知鑒別不足,從而導致治療策略不當。基于此,本研究回顧性分析了一組cCSC繼發CMD患者的臨床資料,觀察其臨床特點、影像學特征及部分患者光動力療法(PDT)治療后的疾病轉歸。現將結果報道如下。
1 對象和方法
回顧性臨床研究。本研究經云南大學附屬醫院倫理委員會審批(批準號:20180106)。
2018年2月至2023年6月于云南大學附屬醫院眼科檢查確診的cCSC繼發CMD患者9例15只眼納入本研究。患者均為男性;年齡(53.67±3.83)(42~64)歲。雙眼6例12只眼;單眼3例3只眼。患眼視力0.02~0.1,均不能矯正。均主述視力下降、眼前陰影遮擋感持續時間>1年。行半劑量PDT治療8只眼。納入標準:(1)患有中心性漿液性脈絡膜視網膜病變(CSC)且病程>1年;(2)OCT檢查黃斑區可見囊腔樣間隙,熒光素眼底血管造影(FFA)顯示囊腔樣間隙處無明顯熒光素滲漏;(3)伴有至少一種中心凹處結構損傷性改變,如橢圓體帶(EZ)結構損傷、外核層(ONL)變薄、視網膜色素上皮(RPE)萎縮、視網膜內強反光點(病灶)、脈絡膜毛細血管層變薄等。需同時滿足以上3條。排除標準:糖尿病視網膜病變(DR)、高血壓視網膜病變、年齡相關性黃斑變性(AMD)及全身其他疾病史;眼外傷、手術、激光光凝引發的黃斑病變;既往接受過激光治療,無法確定激光引發RPE損傷或病程本身REP萎縮者除外。15只眼CMD病變程度隨病程有所不同,其中病程1~3年的3只眼CMD病變較輕:視網膜內囊腔較小、RPE及視網膜外層萎縮較輕;病程3~10年的12只眼CMD病變較重,視網膜內囊腔大且融合、RPE及視網膜外層萎縮明顯。
所有患眼均行最佳矯正視力(BCVA)、裂隙燈顯微鏡、眼底彩色照相、眼底紅外照相(IR)、眼底自發熒光(AF)、FFA、OCT、OCT血管成像(OCTA)、多波長炫彩成像(MC)檢查。采用日本Nidek公司AFC-330眼底照相機行散瞳后眼底彩色照相檢查;采用德國Herdelberg公司共焦激光掃描眼底血管造影儀行眼底AF、FFA檢查。眼底AF檢查:488 nm激光波長掃描,調節敏感度旋鈕,連續采集3~5張圖像,使用Herdelberg Eye Explore軟件處理,得到眼底AF影像;FFA檢查:患者靜脈注射10%熒光素鈉2 ml,8~10 s后加濾光片進行各象限拍攝,起初為連續拍攝,后改為間歇拍攝,獲取FFA像。采用德國Herdelberg公司Spectralis HRA OCT儀行OCT、MC檢查。OCT:以病變部位為中心進行水平掃描,掃描深度2 mm,選擇質量與位置較佳的圖像進行標記保存;MC:炫彩成像模式下,采用波長532 nm紅外激光、518 nm綠色激光、486 nm藍色激光同時掃描并疊加至100幀獲得清晰MC圖像。選擇圖像質量與位置較佳的像進行標記保存。采用視微影像(河南)科技有限公司如意全眼OCTA行OCTA檢查。采用設備自帶軟件(版本3.0.230)測量黃斑區6 mm×6 mm范圍內視網膜淺層毛細血管叢的血流密度;行半劑量PDT治療的8只眼測量其脈絡膜厚度。
行半劑量PDT治療的8只眼,均為雙眼患者。根據患者體重和體表面積,靜脈推注3 mg/m2維替泊芬,15 min后采用波長689 nm、能量50 J/cm2激光照射預先選定的治療區83 s。治療后患者避光48 h。隨訪觀察至治療后3個月。未行PDT治療的7只眼隨訪觀察至首診后2年。
2 結果
2.1 多模式眼底影像特征
眼底彩色照相檢查,所有患眼視盤、周邊視網膜及視網膜血管未見明顯異常;未見單純視網膜神經上皮脫離。后極部黃斑區反光減弱或消失(圖1A),其中可見黃斑區異常色素沉著、邊界清晰的萎縮灶形成分別為12、3只眼。IR檢查,所有患眼均可見黃斑區彌漫性斑片樣弱熒光,周邊散在點狀強熒光(圖1B)。眼底AF檢查,黃斑區盤狀弱AF,中間及邊緣可見散在少量強AF,其中可見黃斑區向下分布的RPE萎縮軌跡7只眼,呈強AF(圖1C)。
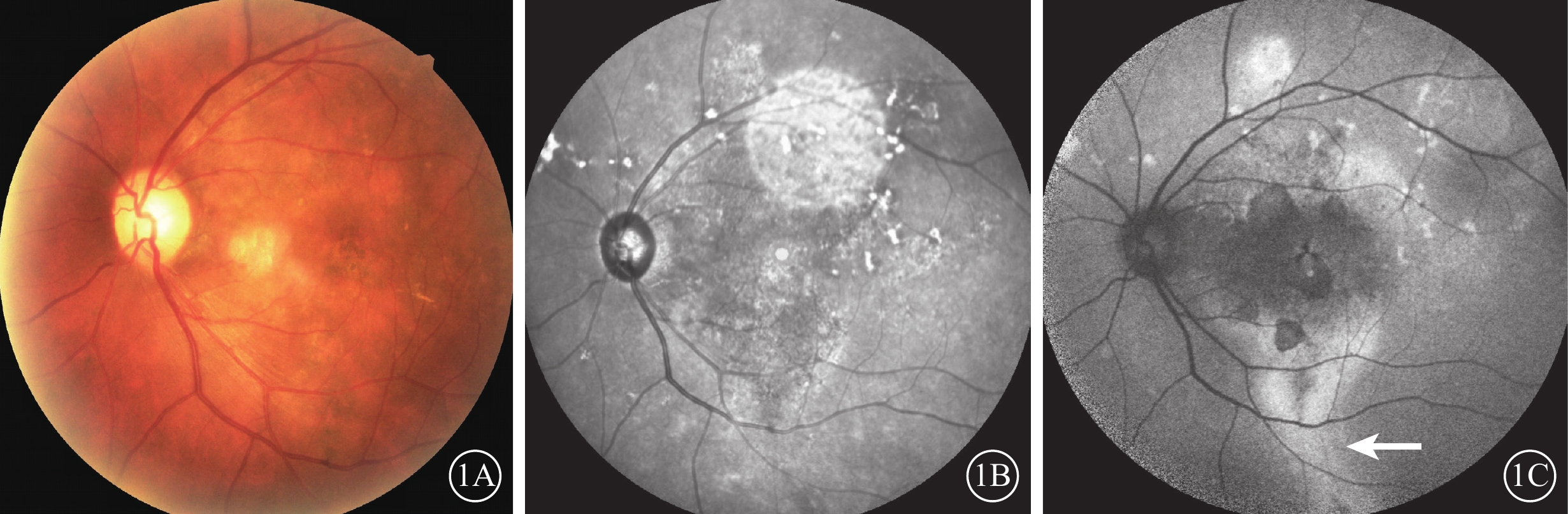 圖1
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼多模式影像
圖1
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼多模式影像
1A示彩色眼底像,黃斑區反光減弱或消失、異常色素沉著,未見單純性視網膜神經上皮脫離;1B示眼底紅外像,黃斑區彌漫性斑片樣弱熒光,周邊散在點狀強熒光;1C示眼底AF像,黃斑區盤狀弱AF,中間及邊緣散在少量強AF,可見呈強AF的視網膜色素上皮萎縮軌跡(白箭) AF:自發熒光
眼底MC檢查,所有患眼后極部黃斑區綠色信號不均勻呈斑駁樣改變,部分區域點狀紅色信號增強(圖2A);紅光通道呈不均勻病變,點狀強熒光改變(圖2B);綠光通道及藍光通道未見明顯異常影像(圖2C,2D)。
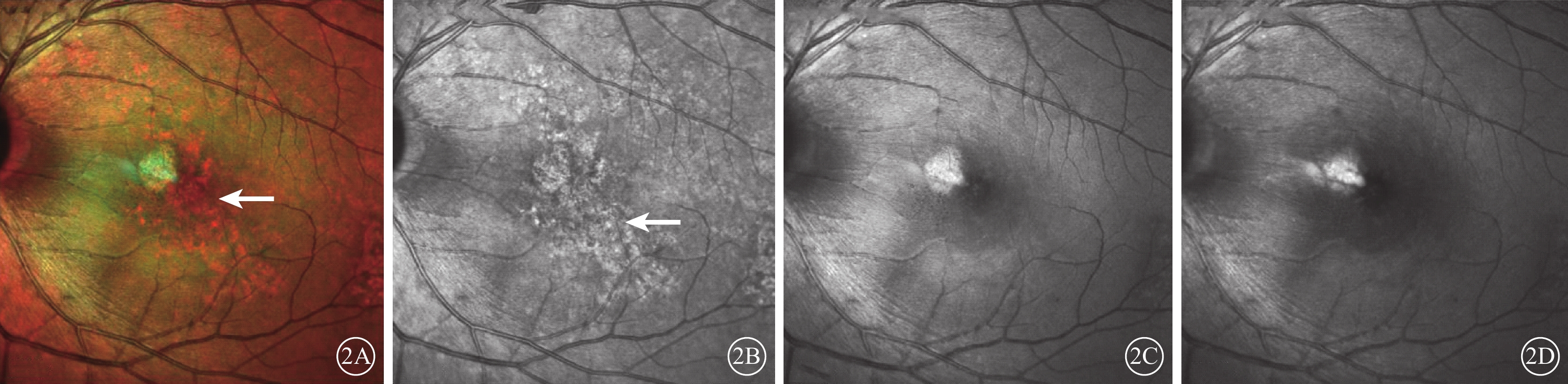 圖2
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼MC圖
圖2
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼MC圖
2A示標準MC像,黃斑區綠色信號不均勻呈斑駁樣改變(白箭);2B示紅外通道像,黃斑區不均勻點狀強弱熒光(白箭);2C、2D分別示綠光、藍光通道像,均未見明顯異常 MC:眼底炫彩成像
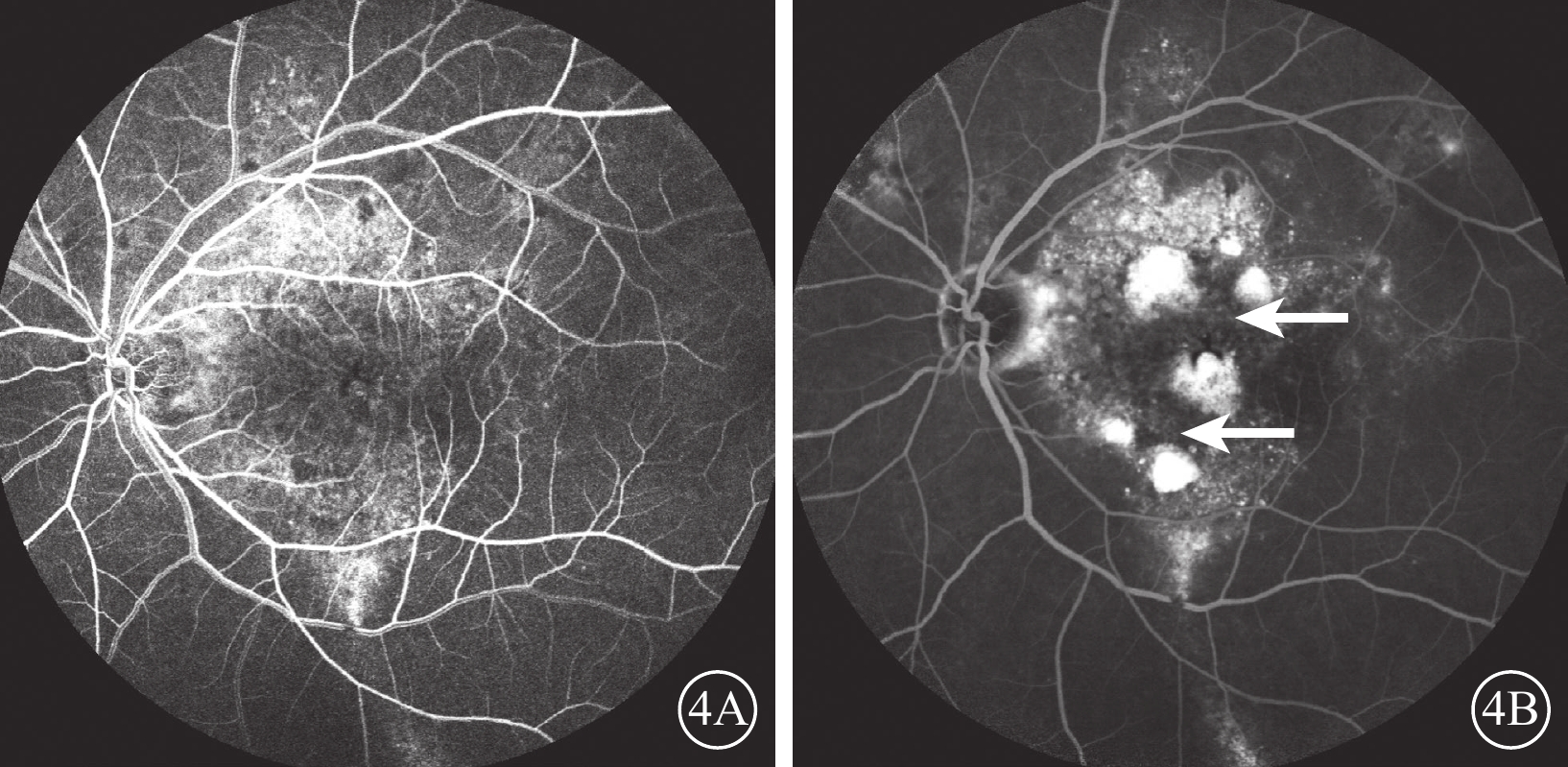
FFA檢查,15只眼中,未見明顯異常熒光素滲漏8只眼,表現為彌漫透見熒光所致的強熒光,晚期未見熒光范圍擴大(圖3)。彌漫透見強熒光內可見少量活動性熒光素滲漏7只眼,早期呈點狀強熒光,晚期呈邊界擴大的強熒光團塊(圖4)。
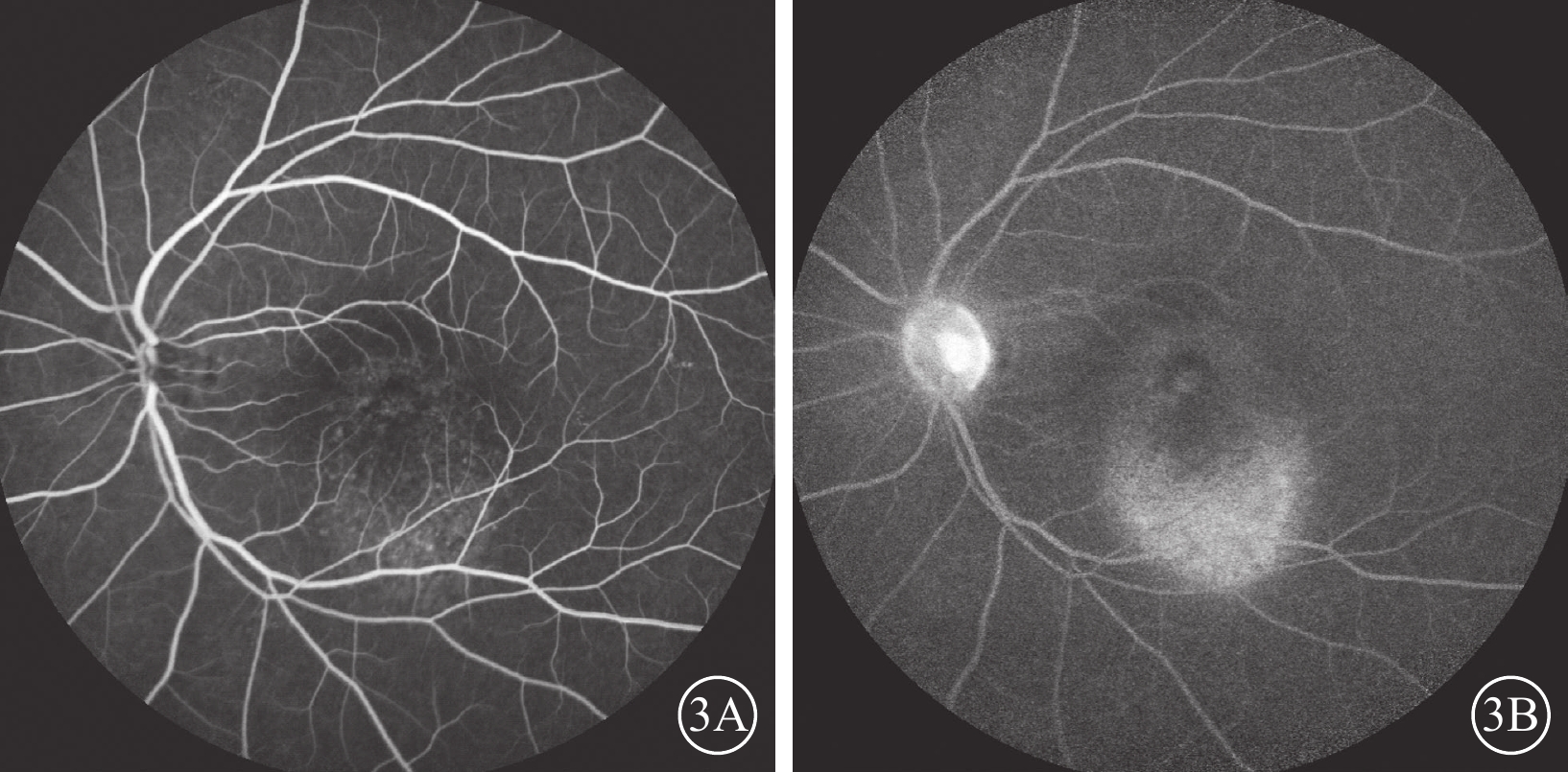 圖3
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼熒光素眼底血管造影像
圖3
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼熒光素眼底血管造影像
3A示0′36″,后極部點狀強熒光;3B示32′48″,點狀強熒光增強,但未見異常滲漏點及熒光素積存
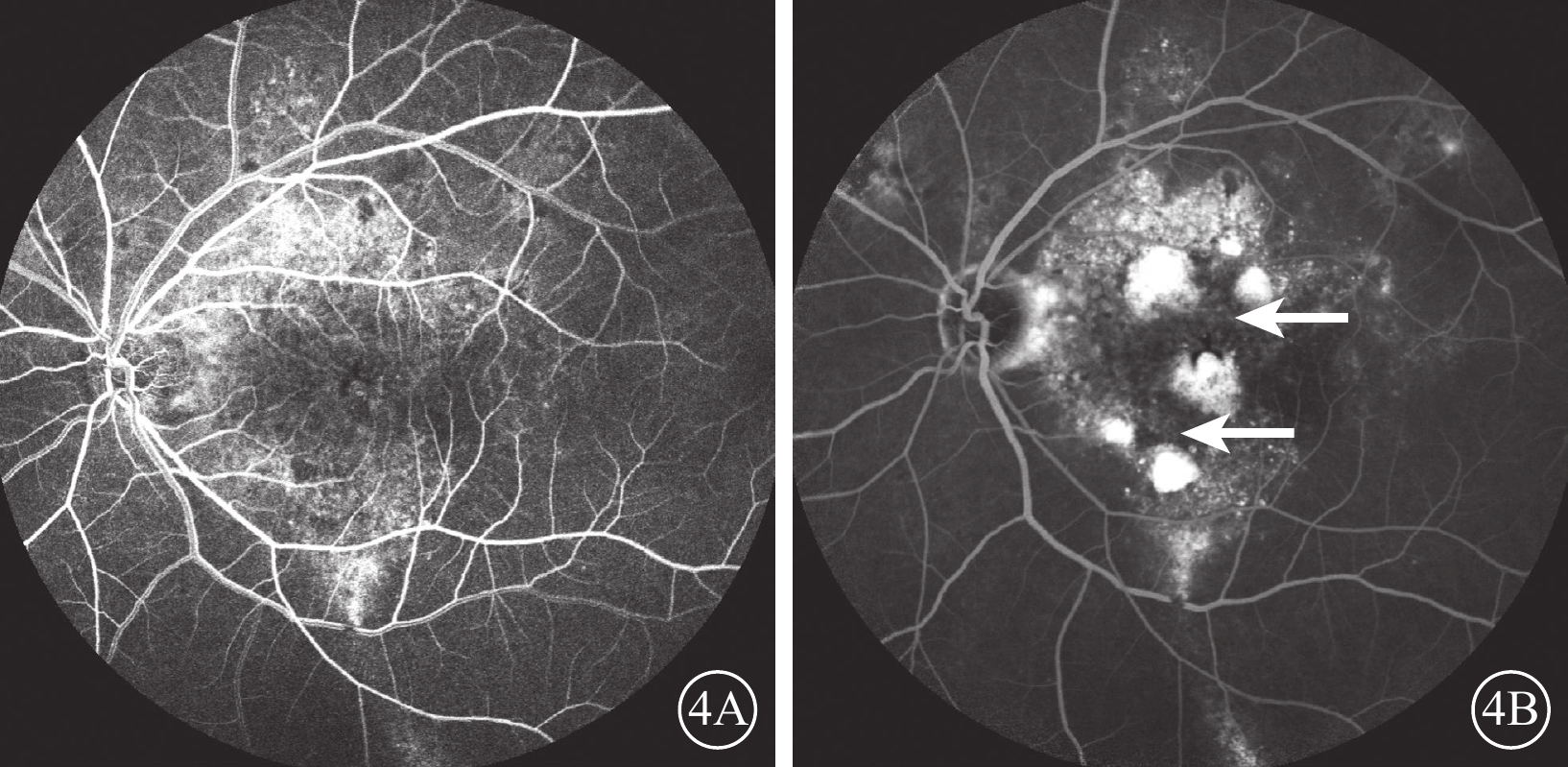 圖4
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性與活動性病灶并存患眼熒光素眼底血管造影像
圖4
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性與活動性病灶并存患眼熒光素眼底血管造影像
4A示0′30″,后極部點狀強熒光,其內有斑片狀弱熒光區;4B示9′04″,黃斑區中間數個熒光素滲漏病灶明顯擴大(白箭)
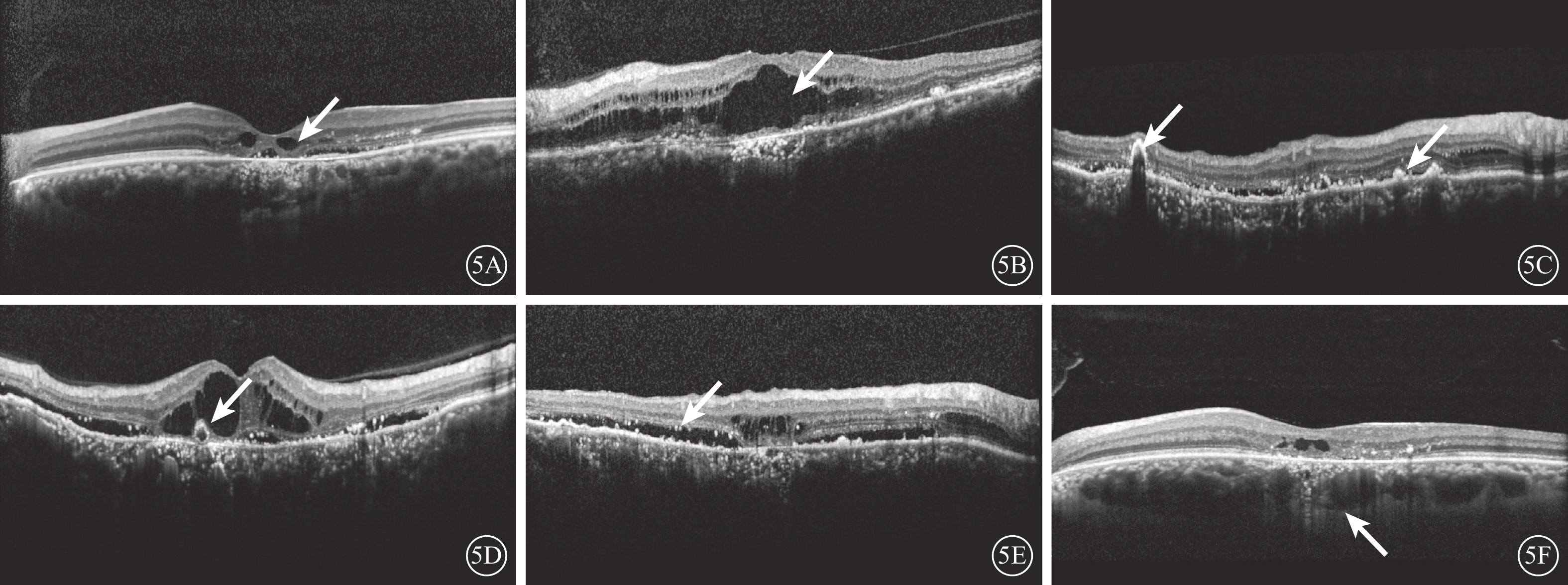
OCT檢查,相對病程<3年的CMD 3只眼,中心凹神經上皮層下可見1個或者多個小囊腔(圖5A);病程>3年的12只眼,囊腔之間連接斷裂消失,融合成大囊腔(圖5B)。所有患眼黃斑區RPE不同程度萎縮。其中,RPE層隆起病灶(圖5C)6只眼,可見明顯視網膜外層結構中強反射點及視網膜外層管狀結構(ORT)(圖5D)。CMD與活動性熒光素滲漏并存的7只眼,可見神經上皮層下積液征(圖5E)。所有患眼均可見脈絡膜肥厚,大血管層擴張明顯,擠壓中血管層及毛細血管層,其中毛細血管層明顯萎縮變薄(圖5F)9只眼。
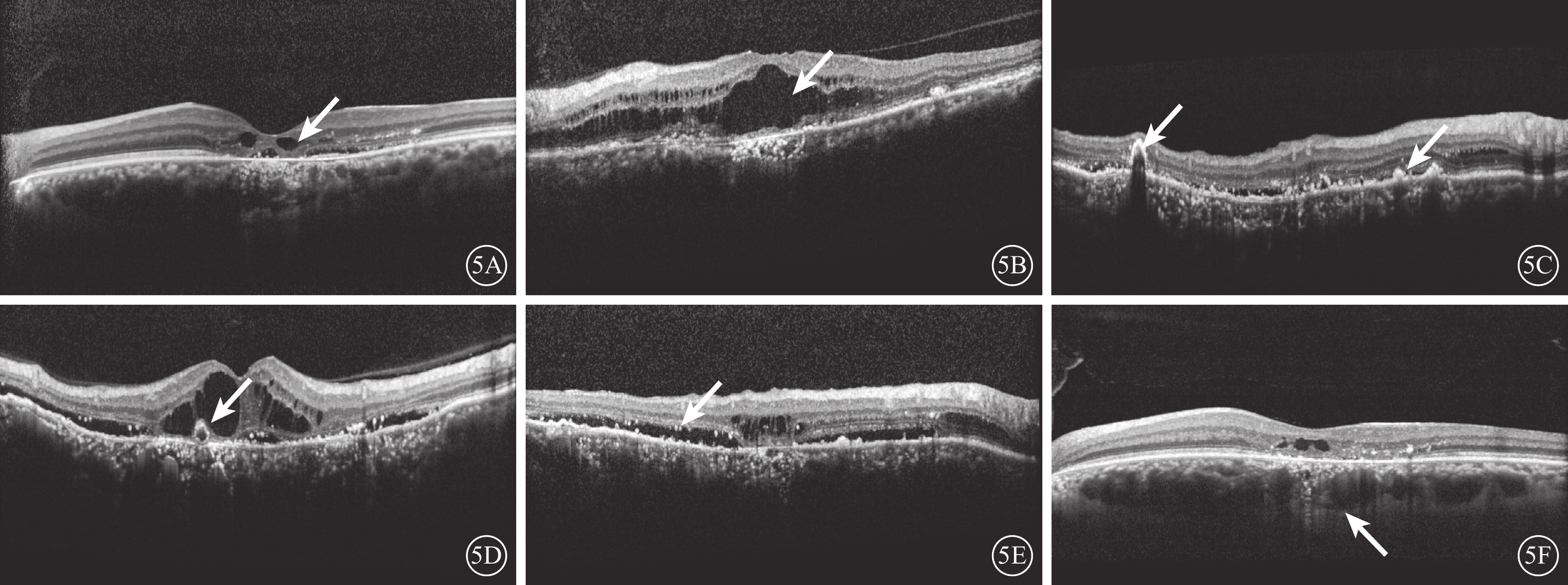 圖5
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼光相干斷層掃描像
圖5
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼光相干斷層掃描像
5A示中心凹處神經上皮層下多個小囊腔(白箭);5B示囊腔之間連接斷裂消失,融合成大囊腔(白箭);5C示視網膜色素上皮萎縮,代償增生形成隆起病灶(白箭);5D示視網膜外層管狀結構(白箭);5E示視網膜下活動病灶與黃斑囊樣變性共存(白箭);5F示病灶處脈絡膜肥厚、大血管擴張(白箭),毛細血管層被壓縮(白箭)
OCTA檢查,因病程及CMD程度不同,可見不同程度脈絡膜毛細血管丟失。其中,CMD較輕3只眼,可見小片后極部脈絡膜毛細血管血流密度稍低;CMD較重12只眼,可見較大片狀的脈絡膜毛細血管丟失,脈絡膜大血管裸露。所有患眼視網膜淺層毛細血管網未見明顯異常(圖6)。
 圖6
慢性中心性漿液性脈絡膜視網膜病變繼發CMD患眼光相干斷層掃描血管成像圖
圖6
慢性中心性漿液性脈絡膜視網膜病變繼發CMD患眼光相干斷層掃描血管成像圖
6A示CMD較輕患眼,小片后極部脈絡膜毛細血管血流密度稍低(黑箭),視網膜淺層毛細血管網未見異常;6B示CMD較重患眼,較大片狀脈絡膜毛細血管丟失,脈絡膜大血管裸露(黑箭) CMD:黃斑囊樣變性
2.2 PDT治療結果
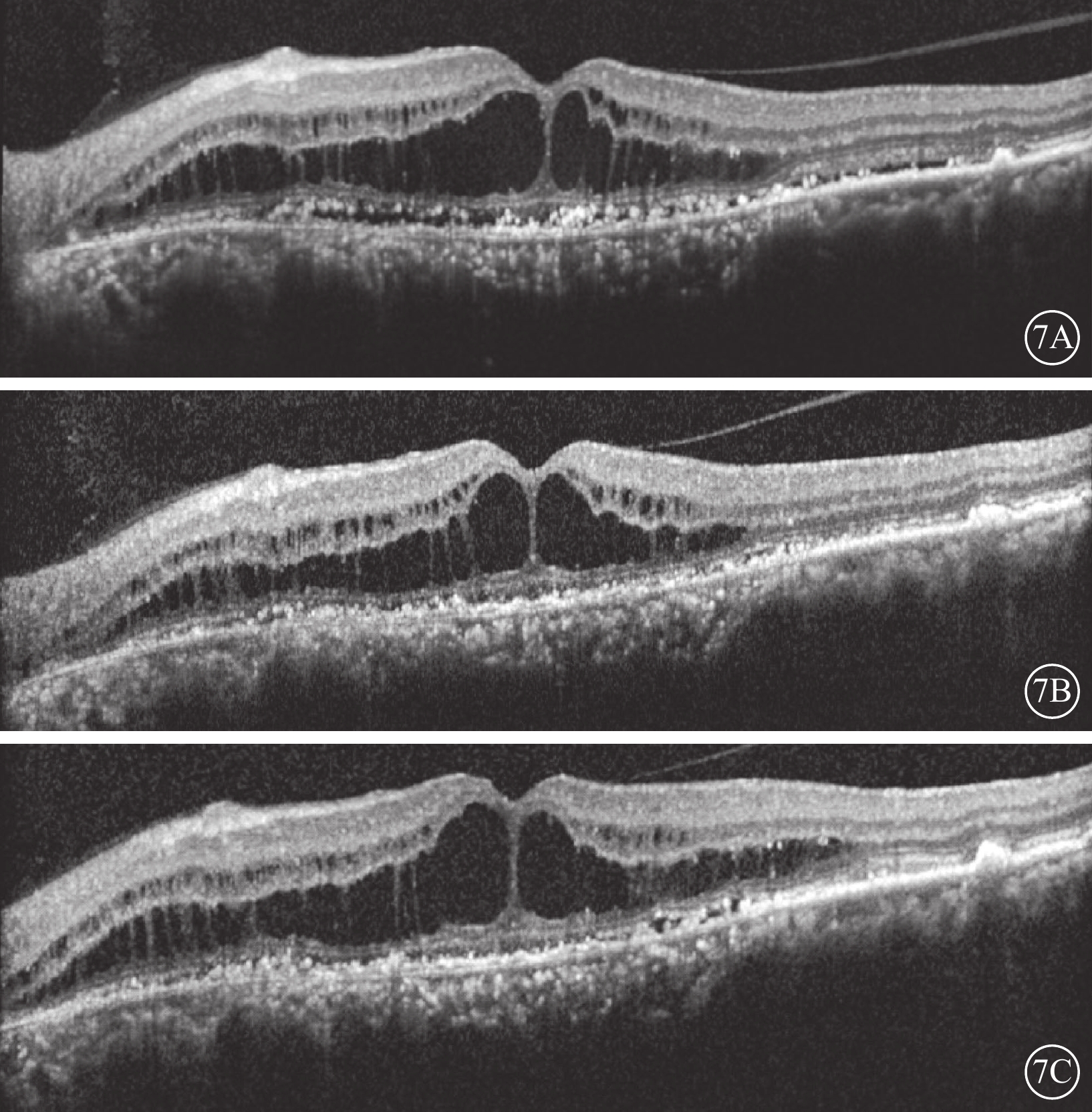
行PDT治療的8只眼中,治療無效6只眼,治療后3個月,眼底檢查可見視盤及中周部視網膜未見明顯異常;后極部黃斑區反光消失,色素紊亂,仍呈微隆起狀。OCT檢查,治療后1、3個月,黃斑區囊腔樣空間較治療前無明顯縮小,內外核層之間拉絲樣改變減少不明顯,中心凹形態同治療前(圖7)。治療前后BCVA范圍均為0.02~0.1。治療有效2只眼,治療后1~3個月,視網膜神經上皮層下積液逐漸吸收。黃斑區囊樣空腔較治療前明顯縮小甚至消失,中心凹形態有所恢復,神經上皮層和RPE貼合良好,但外層EZ結構破壞無明顯恢復(圖8)。2只眼視力較治療前有所提高,分別從0.08提高至0.2、0.05提高至0.1。
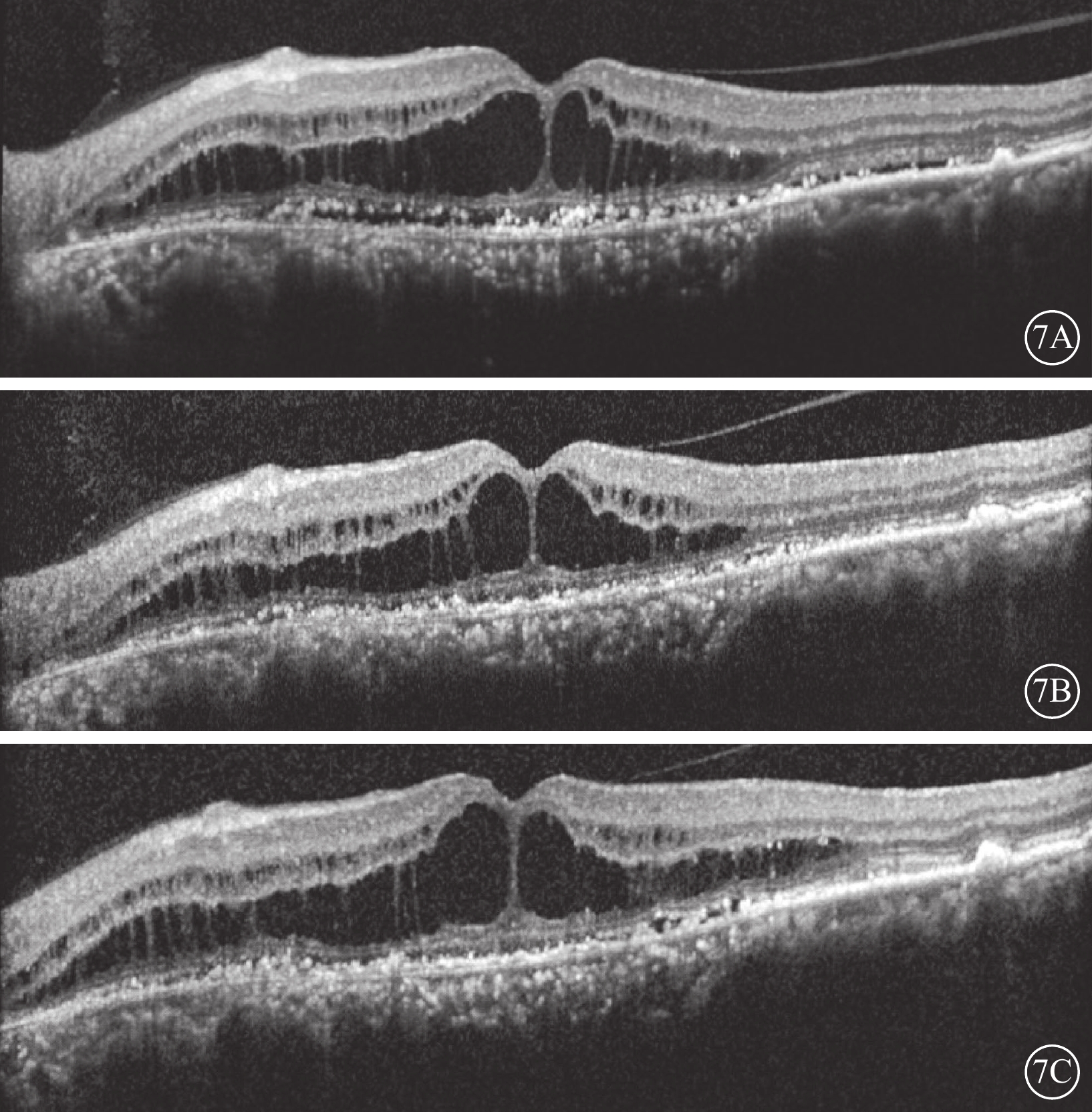 圖7
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患者左眼PDT治療前后光相干斷層掃描像
圖7
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患者左眼PDT治療前后光相干斷層掃描像
7A示治療前,黃斑區視網膜層間不同大小囊腔樣結構,其間可見“橋樣”強反射,RPE不同程度萎縮且表面可見不同程度顆粒樣強反射物質堆積,對應RPE萎縮程度下方脈絡膜反射呈不同程度增強;7B示PDT治療后1個月,視網膜層間囊腔未見明顯改變;7C示治療后3個月,視網膜層間囊腔未見明顯改變 PDT:光動力療法;RPE:視網膜色素上皮
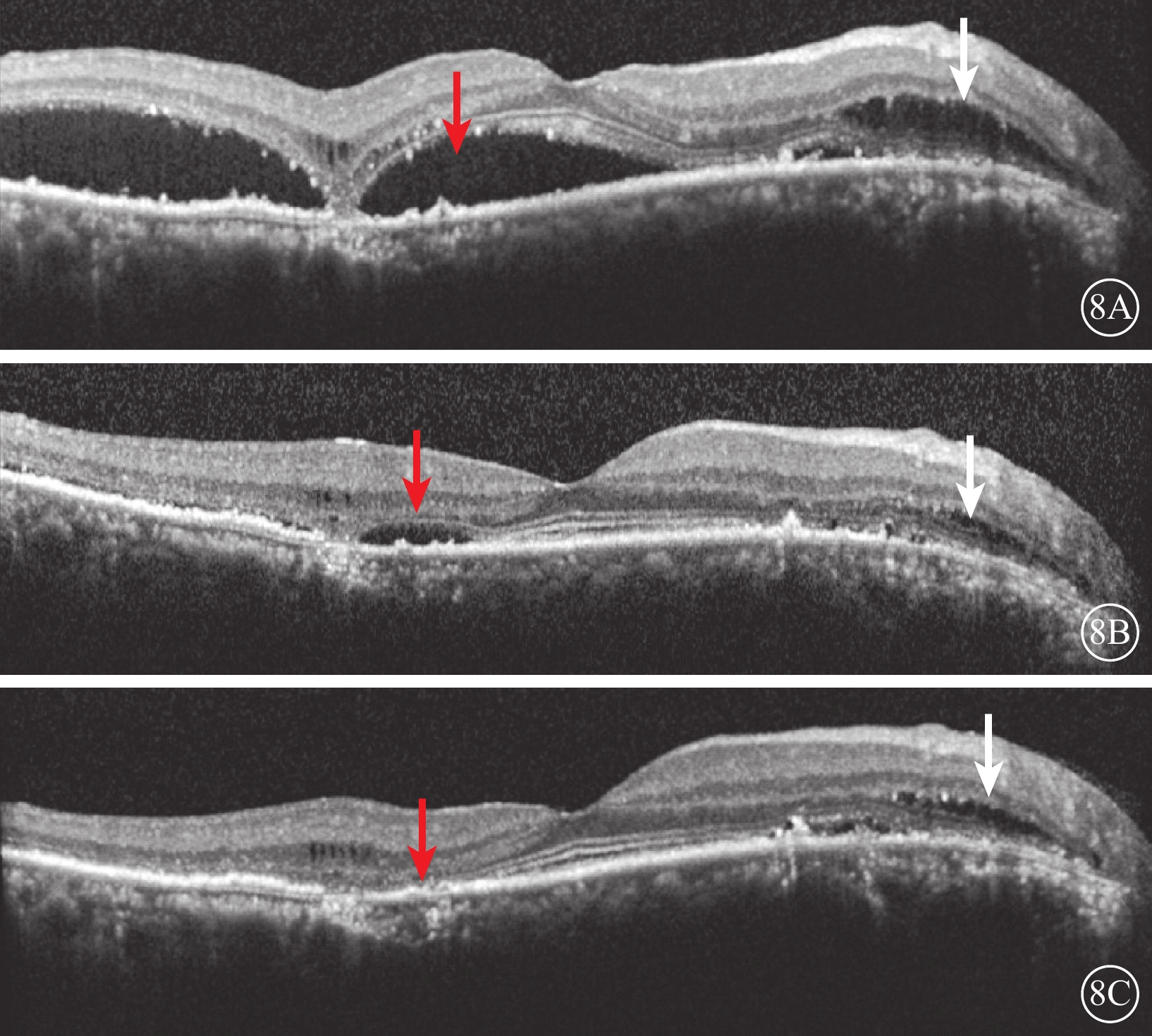
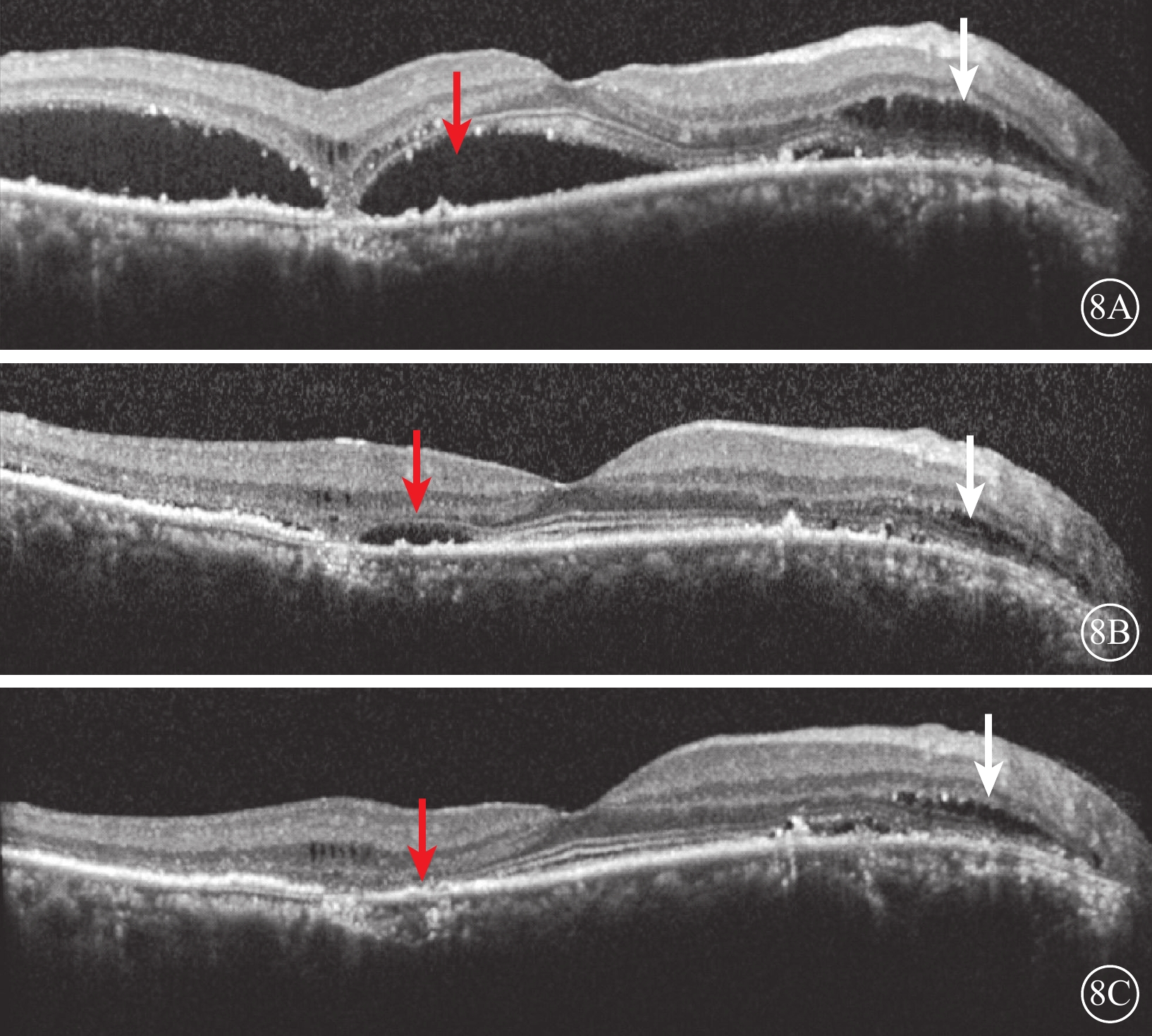 圖8
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患者右眼PDT治療前后光相干斷層掃描像
圖8
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患者右眼PDT治療前后光相干斷層掃描像
8A示治療前,黃斑區神經上皮層下積液(紅箭)及視盤旁囊樣變性(白箭);8B示PDT治療后1個月,神經上皮層下積液明顯吸收,僅少許殘留(紅箭),視盤旁囊樣變性區內囊腔縮小明顯(白箭);8C示治療后3個月,黃斑區神經上皮層下積液完全吸收(紅箭),神經上皮層和RPE貼合良好,但囊樣變性區較治療后1個月時變化不大,積液未完全吸收(白箭),橢圓體帶結構破壞及RPE增生明顯 PDT:光動力療法;RPE:視網膜色素上皮
8只眼中,治療前未見明顯脈絡膜血管擴張、脈絡膜肥厚3只眼;脈絡膜肥厚、脈絡膜厚度無明顯改變3只眼,均為治療無效者;脈絡膜厚度降低2只眼。
未行PDT治療的7只眼,隨訪2年時,CMD結構無明顯改善;隨病程延長,BCVA呈現繼續下降趨勢,平均視力由治療前0.06降低為0.02。
3 討論
CMD并非新術語,既往被簡單用于描述其導致視網膜囊性空腔樣改變,2003年Iida等[2]首次對CSC中CMD進行了描述。CMD臨床特征及其病理損傷包括:(1)視網膜外屏障功能障礙導致更多液體進入視網膜或視網膜下間隙而形成的囊樣空腔[3],當長期病變未得到控制時,最終Müller細胞因胞漿內水腫死亡后留下囊狀空隙,并融合形成大小不等的囊樣空腔[4]。(2)EZ結構損傷和ONL變薄:黃斑區長期漿液性視網膜脫離,視細胞外節與RPE細胞絨毛突正常定向性生理嵌合被破壞,內外核層之間連接受損斷裂,加之囊樣空腔的縱向壓力,加重了EZ和ONL的缺血缺氧,最終使得EZ結構損傷、連續性變差和ONL變薄[5]。(3)RPE和脈絡膜萎縮:cCSC病程較長,RPE和脈絡膜在滲漏部位發生慢性萎縮,由此進一步加重滲漏,形成病變的惡性循環。此外,當脈絡膜毛細血管處于明顯高通透性時,視網膜下滲出物中的纖維蛋白原更易形成cCSC的視網膜下纖維化膜,故部分患者可在CMD下見瘢痕形成,造成視網膜血屏障的永久性破壞[6]。而CMD并非是cCSC唯一表現,多種慢性眼底疾病如糖尿病黃斑水腫、視網膜靜脈阻塞黃斑水腫以及AMD等晚期階段均有可能表現為CMD,對于原發疾病的診斷同為重要。多模式影像為臨床提供了原發疾病的診斷依據,cCSC眼底彩色照相可見廣泛后極部色素紊亂,眼底AF可見斑駁樣強弱AF,FFA中無明顯血管病變均是相應特征性診斷依據。而DR、視網膜靜脈阻塞則有相應血管改變影像,AMD患者則有典型脈絡膜新生血管影像特征。
CMD與CME具有類似OCT表現,導致對兩者區別認識不足。兩者病理機制有本質不同[7]:CME多繼發于眼部炎癥性疾病、視網膜血管疾病、視網膜色素變性、眼前節手術和脈絡膜病變等造成血視網膜屏障功能下降、細胞毒性機制、氧化應激等[8]。而CMD則是長時間慢性病變導致Müller細胞壞死形成的囊樣空腔[9]。兩者其他眼底影像表現也有明顯差異,FFA:CME常表現為典型熒光素滲漏和積存;而CMD無明顯熒光素滲漏,多為熒光染色。OCT:兩者除相似的囊樣空腔外,CMD可有EZ結構損傷、ONL變薄、RPE萎縮、脈絡膜衰減變薄、視網膜下纖維化形成等[10];CME外層損傷則相對輕微。對于CME,玻璃體腔注射抗血管內皮生長因子(VEGF)藥物或糖皮質激素可通過降低VEGF和其他促炎介質改善CME [11]。對于CMD,因其視網膜脈絡膜結構損傷較重且不可逆,目前尚無有效治療手段 [12]。目前有學者認為CME可能是CMD的前期過程,CMD發生時CME仍可能與其并存。
目前對于CMD的治療尚無明確療效的治療方法[13]。本組8只眼嘗試給予半劑量PDT治療,結果顯示,僅2只眼治療有效,CMD囊腔好轉;6只眼治療無效,BCVA無提高,CMD改善不明顯,其原因可能是cCSC病程較長,Müller細胞廣泛死亡,內外核層之間難于重新建立緊密連接,RPE、脈絡膜均衰減變薄所致[14-15]。
雖然目前對于CMD的病因仍知之甚少,但是識別其作為cCSC發展轉歸的特征性表現能擴大對cCSC的認知。對于病程較長的cCSC患眼,在早期或急性期積極給予相應治療手段,最大可能避免CMD的發生。此外,CMD并非cCSC特有表現,應與各類病因的CME進行鑒別,避免不合理的治療策略。
慢性中心性漿液性脈絡膜視網膜病變(cCSC)中持續或反復的黃斑區視網膜神經上皮層下漿液存留可導致視網膜神經上皮層結構發生變性樣改變,此種改變在光相干斷層掃描(OCT)上可見囊樣間隙,臨床將其定義為黃斑囊樣變性(CMD)[1-2]。CMD形態類似于黃斑囊樣水腫(CME),部分臨床醫生對兩者的認知鑒別不足,從而導致治療策略不當。基于此,本研究回顧性分析了一組cCSC繼發CMD患者的臨床資料,觀察其臨床特點、影像學特征及部分患者光動力療法(PDT)治療后的疾病轉歸。現將結果報道如下。
1 對象和方法
回顧性臨床研究。本研究經云南大學附屬醫院倫理委員會審批(批準號:20180106)。
2018年2月至2023年6月于云南大學附屬醫院眼科檢查確診的cCSC繼發CMD患者9例15只眼納入本研究。患者均為男性;年齡(53.67±3.83)(42~64)歲。雙眼6例12只眼;單眼3例3只眼。患眼視力0.02~0.1,均不能矯正。均主述視力下降、眼前陰影遮擋感持續時間>1年。行半劑量PDT治療8只眼。納入標準:(1)患有中心性漿液性脈絡膜視網膜病變(CSC)且病程>1年;(2)OCT檢查黃斑區可見囊腔樣間隙,熒光素眼底血管造影(FFA)顯示囊腔樣間隙處無明顯熒光素滲漏;(3)伴有至少一種中心凹處結構損傷性改變,如橢圓體帶(EZ)結構損傷、外核層(ONL)變薄、視網膜色素上皮(RPE)萎縮、視網膜內強反光點(病灶)、脈絡膜毛細血管層變薄等。需同時滿足以上3條。排除標準:糖尿病視網膜病變(DR)、高血壓視網膜病變、年齡相關性黃斑變性(AMD)及全身其他疾病史;眼外傷、手術、激光光凝引發的黃斑病變;既往接受過激光治療,無法確定激光引發RPE損傷或病程本身REP萎縮者除外。15只眼CMD病變程度隨病程有所不同,其中病程1~3年的3只眼CMD病變較輕:視網膜內囊腔較小、RPE及視網膜外層萎縮較輕;病程3~10年的12只眼CMD病變較重,視網膜內囊腔大且融合、RPE及視網膜外層萎縮明顯。
所有患眼均行最佳矯正視力(BCVA)、裂隙燈顯微鏡、眼底彩色照相、眼底紅外照相(IR)、眼底自發熒光(AF)、FFA、OCT、OCT血管成像(OCTA)、多波長炫彩成像(MC)檢查。采用日本Nidek公司AFC-330眼底照相機行散瞳后眼底彩色照相檢查;采用德國Herdelberg公司共焦激光掃描眼底血管造影儀行眼底AF、FFA檢查。眼底AF檢查:488 nm激光波長掃描,調節敏感度旋鈕,連續采集3~5張圖像,使用Herdelberg Eye Explore軟件處理,得到眼底AF影像;FFA檢查:患者靜脈注射10%熒光素鈉2 ml,8~10 s后加濾光片進行各象限拍攝,起初為連續拍攝,后改為間歇拍攝,獲取FFA像。采用德國Herdelberg公司Spectralis HRA OCT儀行OCT、MC檢查。OCT:以病變部位為中心進行水平掃描,掃描深度2 mm,選擇質量與位置較佳的圖像進行標記保存;MC:炫彩成像模式下,采用波長532 nm紅外激光、518 nm綠色激光、486 nm藍色激光同時掃描并疊加至100幀獲得清晰MC圖像。選擇圖像質量與位置較佳的像進行標記保存。采用視微影像(河南)科技有限公司如意全眼OCTA行OCTA檢查。采用設備自帶軟件(版本3.0.230)測量黃斑區6 mm×6 mm范圍內視網膜淺層毛細血管叢的血流密度;行半劑量PDT治療的8只眼測量其脈絡膜厚度。
行半劑量PDT治療的8只眼,均為雙眼患者。根據患者體重和體表面積,靜脈推注3 mg/m2維替泊芬,15 min后采用波長689 nm、能量50 J/cm2激光照射預先選定的治療區83 s。治療后患者避光48 h。隨訪觀察至治療后3個月。未行PDT治療的7只眼隨訪觀察至首診后2年。
2 結果
2.1 多模式眼底影像特征
眼底彩色照相檢查,所有患眼視盤、周邊視網膜及視網膜血管未見明顯異常;未見單純視網膜神經上皮脫離。后極部黃斑區反光減弱或消失(圖1A),其中可見黃斑區異常色素沉著、邊界清晰的萎縮灶形成分別為12、3只眼。IR檢查,所有患眼均可見黃斑區彌漫性斑片樣弱熒光,周邊散在點狀強熒光(圖1B)。眼底AF檢查,黃斑區盤狀弱AF,中間及邊緣可見散在少量強AF,其中可見黃斑區向下分布的RPE萎縮軌跡7只眼,呈強AF(圖1C)。
 圖1
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼多模式影像
圖1
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼多模式影像
1A示彩色眼底像,黃斑區反光減弱或消失、異常色素沉著,未見單純性視網膜神經上皮脫離;1B示眼底紅外像,黃斑區彌漫性斑片樣弱熒光,周邊散在點狀強熒光;1C示眼底AF像,黃斑區盤狀弱AF,中間及邊緣散在少量強AF,可見呈強AF的視網膜色素上皮萎縮軌跡(白箭) AF:自發熒光
眼底MC檢查,所有患眼后極部黃斑區綠色信號不均勻呈斑駁樣改變,部分區域點狀紅色信號增強(圖2A);紅光通道呈不均勻病變,點狀強熒光改變(圖2B);綠光通道及藍光通道未見明顯異常影像(圖2C,2D)。
 圖2
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼MC圖
圖2
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼MC圖
2A示標準MC像,黃斑區綠色信號不均勻呈斑駁樣改變(白箭);2B示紅外通道像,黃斑區不均勻點狀強弱熒光(白箭);2C、2D分別示綠光、藍光通道像,均未見明顯異常 MC:眼底炫彩成像
FFA檢查,15只眼中,未見明顯異常熒光素滲漏8只眼,表現為彌漫透見熒光所致的強熒光,晚期未見熒光范圍擴大(圖3)。彌漫透見強熒光內可見少量活動性熒光素滲漏7只眼,早期呈點狀強熒光,晚期呈邊界擴大的強熒光團塊(圖4)。
 圖3
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼熒光素眼底血管造影像
圖3
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼熒光素眼底血管造影像
3A示0′36″,后極部點狀強熒光;3B示32′48″,點狀強熒光增強,但未見異常滲漏點及熒光素積存
 圖4
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性與活動性病灶并存患眼熒光素眼底血管造影像
圖4
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性與活動性病灶并存患眼熒光素眼底血管造影像
4A示0′30″,后極部點狀強熒光,其內有斑片狀弱熒光區;4B示9′04″,黃斑區中間數個熒光素滲漏病灶明顯擴大(白箭)
OCT檢查,相對病程<3年的CMD 3只眼,中心凹神經上皮層下可見1個或者多個小囊腔(圖5A);病程>3年的12只眼,囊腔之間連接斷裂消失,融合成大囊腔(圖5B)。所有患眼黃斑區RPE不同程度萎縮。其中,RPE層隆起病灶(圖5C)6只眼,可見明顯視網膜外層結構中強反射點及視網膜外層管狀結構(ORT)(圖5D)。CMD與活動性熒光素滲漏并存的7只眼,可見神經上皮層下積液征(圖5E)。所有患眼均可見脈絡膜肥厚,大血管層擴張明顯,擠壓中血管層及毛細血管層,其中毛細血管層明顯萎縮變薄(圖5F)9只眼。
 圖5
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼光相干斷層掃描像
圖5
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患眼光相干斷層掃描像
5A示中心凹處神經上皮層下多個小囊腔(白箭);5B示囊腔之間連接斷裂消失,融合成大囊腔(白箭);5C示視網膜色素上皮萎縮,代償增生形成隆起病灶(白箭);5D示視網膜外層管狀結構(白箭);5E示視網膜下活動病灶與黃斑囊樣變性共存(白箭);5F示病灶處脈絡膜肥厚、大血管擴張(白箭),毛細血管層被壓縮(白箭)
OCTA檢查,因病程及CMD程度不同,可見不同程度脈絡膜毛細血管丟失。其中,CMD較輕3只眼,可見小片后極部脈絡膜毛細血管血流密度稍低;CMD較重12只眼,可見較大片狀的脈絡膜毛細血管丟失,脈絡膜大血管裸露。所有患眼視網膜淺層毛細血管網未見明顯異常(圖6)。
 圖6
慢性中心性漿液性脈絡膜視網膜病變繼發CMD患眼光相干斷層掃描血管成像圖
圖6
慢性中心性漿液性脈絡膜視網膜病變繼發CMD患眼光相干斷層掃描血管成像圖
6A示CMD較輕患眼,小片后極部脈絡膜毛細血管血流密度稍低(黑箭),視網膜淺層毛細血管網未見異常;6B示CMD較重患眼,較大片狀脈絡膜毛細血管丟失,脈絡膜大血管裸露(黑箭) CMD:黃斑囊樣變性
2.2 PDT治療結果
行PDT治療的8只眼中,治療無效6只眼,治療后3個月,眼底檢查可見視盤及中周部視網膜未見明顯異常;后極部黃斑區反光消失,色素紊亂,仍呈微隆起狀。OCT檢查,治療后1、3個月,黃斑區囊腔樣空間較治療前無明顯縮小,內外核層之間拉絲樣改變減少不明顯,中心凹形態同治療前(圖7)。治療前后BCVA范圍均為0.02~0.1。治療有效2只眼,治療后1~3個月,視網膜神經上皮層下積液逐漸吸收。黃斑區囊樣空腔較治療前明顯縮小甚至消失,中心凹形態有所恢復,神經上皮層和RPE貼合良好,但外層EZ結構破壞無明顯恢復(圖8)。2只眼視力較治療前有所提高,分別從0.08提高至0.2、0.05提高至0.1。
 圖7
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患者左眼PDT治療前后光相干斷層掃描像
圖7
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患者左眼PDT治療前后光相干斷層掃描像
7A示治療前,黃斑區視網膜層間不同大小囊腔樣結構,其間可見“橋樣”強反射,RPE不同程度萎縮且表面可見不同程度顆粒樣強反射物質堆積,對應RPE萎縮程度下方脈絡膜反射呈不同程度增強;7B示PDT治療后1個月,視網膜層間囊腔未見明顯改變;7C示治療后3個月,視網膜層間囊腔未見明顯改變 PDT:光動力療法;RPE:視網膜色素上皮
 圖8
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患者右眼PDT治療前后光相干斷層掃描像
圖8
慢性中心性漿液性脈絡膜視網膜病變繼發黃斑囊樣變性患者右眼PDT治療前后光相干斷層掃描像
8A示治療前,黃斑區神經上皮層下積液(紅箭)及視盤旁囊樣變性(白箭);8B示PDT治療后1個月,神經上皮層下積液明顯吸收,僅少許殘留(紅箭),視盤旁囊樣變性區內囊腔縮小明顯(白箭);8C示治療后3個月,黃斑區神經上皮層下積液完全吸收(紅箭),神經上皮層和RPE貼合良好,但囊樣變性區較治療后1個月時變化不大,積液未完全吸收(白箭),橢圓體帶結構破壞及RPE增生明顯 PDT:光動力療法;RPE:視網膜色素上皮
8只眼中,治療前未見明顯脈絡膜血管擴張、脈絡膜肥厚3只眼;脈絡膜肥厚、脈絡膜厚度無明顯改變3只眼,均為治療無效者;脈絡膜厚度降低2只眼。
未行PDT治療的7只眼,隨訪2年時,CMD結構無明顯改善;隨病程延長,BCVA呈現繼續下降趨勢,平均視力由治療前0.06降低為0.02。
3 討論
CMD并非新術語,既往被簡單用于描述其導致視網膜囊性空腔樣改變,2003年Iida等[2]首次對CSC中CMD進行了描述。CMD臨床特征及其病理損傷包括:(1)視網膜外屏障功能障礙導致更多液體進入視網膜或視網膜下間隙而形成的囊樣空腔[3],當長期病變未得到控制時,最終Müller細胞因胞漿內水腫死亡后留下囊狀空隙,并融合形成大小不等的囊樣空腔[4]。(2)EZ結構損傷和ONL變薄:黃斑區長期漿液性視網膜脫離,視細胞外節與RPE細胞絨毛突正常定向性生理嵌合被破壞,內外核層之間連接受損斷裂,加之囊樣空腔的縱向壓力,加重了EZ和ONL的缺血缺氧,最終使得EZ結構損傷、連續性變差和ONL變薄[5]。(3)RPE和脈絡膜萎縮:cCSC病程較長,RPE和脈絡膜在滲漏部位發生慢性萎縮,由此進一步加重滲漏,形成病變的惡性循環。此外,當脈絡膜毛細血管處于明顯高通透性時,視網膜下滲出物中的纖維蛋白原更易形成cCSC的視網膜下纖維化膜,故部分患者可在CMD下見瘢痕形成,造成視網膜血屏障的永久性破壞[6]。而CMD并非是cCSC唯一表現,多種慢性眼底疾病如糖尿病黃斑水腫、視網膜靜脈阻塞黃斑水腫以及AMD等晚期階段均有可能表現為CMD,對于原發疾病的診斷同為重要。多模式影像為臨床提供了原發疾病的診斷依據,cCSC眼底彩色照相可見廣泛后極部色素紊亂,眼底AF可見斑駁樣強弱AF,FFA中無明顯血管病變均是相應特征性診斷依據。而DR、視網膜靜脈阻塞則有相應血管改變影像,AMD患者則有典型脈絡膜新生血管影像特征。
CMD與CME具有類似OCT表現,導致對兩者區別認識不足。兩者病理機制有本質不同[7]:CME多繼發于眼部炎癥性疾病、視網膜血管疾病、視網膜色素變性、眼前節手術和脈絡膜病變等造成血視網膜屏障功能下降、細胞毒性機制、氧化應激等[8]。而CMD則是長時間慢性病變導致Müller細胞壞死形成的囊樣空腔[9]。兩者其他眼底影像表現也有明顯差異,FFA:CME常表現為典型熒光素滲漏和積存;而CMD無明顯熒光素滲漏,多為熒光染色。OCT:兩者除相似的囊樣空腔外,CMD可有EZ結構損傷、ONL變薄、RPE萎縮、脈絡膜衰減變薄、視網膜下纖維化形成等[10];CME外層損傷則相對輕微。對于CME,玻璃體腔注射抗血管內皮生長因子(VEGF)藥物或糖皮質激素可通過降低VEGF和其他促炎介質改善CME [11]。對于CMD,因其視網膜脈絡膜結構損傷較重且不可逆,目前尚無有效治療手段 [12]。目前有學者認為CME可能是CMD的前期過程,CMD發生時CME仍可能與其并存。
目前對于CMD的治療尚無明確療效的治療方法[13]。本組8只眼嘗試給予半劑量PDT治療,結果顯示,僅2只眼治療有效,CMD囊腔好轉;6只眼治療無效,BCVA無提高,CMD改善不明顯,其原因可能是cCSC病程較長,Müller細胞廣泛死亡,內外核層之間難于重新建立緊密連接,RPE、脈絡膜均衰減變薄所致[14-15]。
雖然目前對于CMD的病因仍知之甚少,但是識別其作為cCSC發展轉歸的特征性表現能擴大對cCSC的認知。對于病程較長的cCSC患眼,在早期或急性期積極給予相應治療手段,最大可能避免CMD的發生。此外,CMD并非cCSC特有表現,應與各類病因的CME進行鑒別,避免不合理的治療策略。