引用本文: 林加藤, 姜華靜, 司山成. 血清胱抑素C對威脅視力的糖尿病視網膜病變的預測價值. 中華眼底病雜志, 2024, 40(8): 608-613. doi: 10.3760/cma.j.cn511434-20231207-00475 復制
版權信息: ?四川大學華西醫院華西期刊社《中華眼底病雜志》版權所有,未經授權不得轉載、改編
通過簡單高效的方法及時篩查轉診威脅視力的糖尿病視網膜病變(DR)患者對于預防不可逆盲、減輕疾病醫療負擔具有重大意義。臨床對DR發生或進展風險評估多采用眼底彩色照相、光相干斷層掃描(OCT)、熒光素眼底血管造影或最新的視網膜病變自動檢測和分類人工智能等[1-3]。然而,目前尚無有效的可以預測威脅視力的DR(STDR)發生的血清生物標志物。血清胱抑素C(Cys-C)是一種低分子量蛋白,是內源性半胱氨酸蛋白酶抑制劑,不受炎癥、肌肉含量、性別、年齡等因素影響,因此有潛力成為一種良好的血清生物標志物[4]。文獻報道,血清Cys-C除了能較為敏感地評價早期腎功能損害[5],還與DR相關[6-7]。一項針對英國、印度糖尿病患者的研究顯示,血清Cys-C升高可能預示糖尿病黃斑水腫(DME)、增生型DR(PDR)的發生[7]。然而,STDR的發生與血清Cys-C以及年齡、種族、糖尿病病程、糖化血紅蛋白(HbA1c)等多種因素均相關,因此血清Cys-C在不同群體中的預測價值可能有所不同,需進一步驗證[7]。因此,我們檢測了一組漢族2型糖尿病(T2DM)患者的血清Cys-C,初步探討血清Cys-C對STDR發生的預測價值。現將結果報道如下。
1 對象和方法
非隨機對照的橫斷面臨床研究。本研究經清華大學附屬北京清華長庚醫院倫理委員會審核(批準號:24341-6-01);遵循《赫爾辛基宣言》原則;由于本研究未對患者進行額外的檢查與治療,倫理委員會免除了患者知情同意的書面要求。
2022年1~10月于清華大學附屬北京清華長庚醫院眼科就診的T2DM患者92例納入本研究。納入標準:(1)符合T2DM診斷標準[8];(2)年齡≥18歲;(3)眼軸長度≤26.5 mm。 排除標準:(1)1型糖尿病或其他類型糖尿病;(2)慢性腎臟病分期3期及以上或腎小球濾過率(GFR)<60 ml/(min·1.73 m2);(3)腎臟穿刺病理證實為高血壓腎病;(4)病理性近視;(5)圖像信號強度≤6。
所有患者均行最佳矯正視力、裂隙燈顯微鏡、間接檢眼鏡、眼底彩色照相、OCT以及HbA1c、血脂、腎功能、血壓檢查。眼底彩色照相采用日本Topcon公司TRC-50DX或佳能公司CR-2免散瞳數碼照相機進行;OCT檢查采用德國Heidelberg公司Spectralis HRA+OCT儀進行。彩色眼底像和(或)OCT圖像閱片由同兩名高年資眼底病專家(本文第一、第三作者)分別獨立完成,對不確定診斷者則由兩位醫師共同作出診斷并分級。以2003年美國眼科學會發布的DR臨床指南和國際臨床DR嚴重程度分級標準[9]為診斷和分期依據。STDR定義為重度非增生型DR(SNPDR)、PDR、DME;非STDR定義為輕度至中度非PDR、無DR。根據世界衛生組織高血壓分級標準[10]:高血壓1級定義為收縮壓140~159 mm Hg(1 mm Hg=0.133 kPa),舒張壓90~99 mm Hg;高血壓2級定義為收縮壓160~179 mm Hg,舒張壓100~109 mm Hg;高血壓3級定義為收縮壓≥180 mm Hg,舒張壓≥110 mm Hg。根據1999年美國腎臟病基金會腎臟病預后質量倡議工作組慢性腎臟病分期標準[11]:慢性腎臟病分為5期,1期定義為已有腎病,GFR正常,≥90 ml/(min·1.73 m2);2期定義為GFR降低至60~89 ml/(min·1.73 m2);3期定義為GFR降低至30~59 ml/(min·1.73 m2);4期定義為GFR降低至15~29 ml/(min·1.73 m2);5期定義為終末期腎病(腎衰竭),GFR降低至<15 ml/(min·1.73 m2)。
患者中,男性50例,女性42例;年齡(58.24±12.49)(22~79)歲。人工晶狀體(IOL)13例。全視網膜激光光凝(PRP)24例。眼肌麻痹2例;代謝性白內障5例。無DR 26例。糖尿病病程(13.18±8.35)(1~36)年,其中病程≥10年者38例。高血壓29例,其中高血壓3級17例;高血壓病程(10.76±9.77)(1~30)年,其中病程≥10年者16例。慢性腎臟病2期17例。應用降血脂藥物治療23例。HbA1c(8.05±1.82)%(5.5%~14.2%)。總膽固醇(TC)、三酰甘油(TG)、低密度脂蛋白膽固醇(LDL-C)、高密度脂蛋白膽固醇(HDL-C)分別為(4.57±1.14)、(1.73±1.44)、(2.79±1.01)、(1.19±0.27)mmol/L。血清肌酐(Scr)(70.13±22.12)μmol/L;血清Cys-C(1.07±0.39)mg/L;尿微量白蛋白/肌酐比值(ACR)(26.27±96.67)mg/mmol。根據DR分期,將患者分為STDR組、非STDR組,分別為44、48例。
采用SPSS25.0軟件行統計學分析。符合正態分布的連續變量以均數±標準差(x±s)表示;不符合正態分布的連續變量以中位數(四分位數間距)[M(P25,P75)]表示。符合正態分布的連續變量,組間比較采用獨立樣本t檢驗;不符合正態分布的連續變量,組間比較采用Mann-Whitney U檢驗。分類變量以百分比(n,%)表示,組間比較采用χ2檢驗或Fisher's確切概率法。采用logistic回歸分析估算各候選變量的比值比(OR)。單因素分析中,P<0.1的變量納入多因素回歸分析。應用受試者工作特征(ROC)曲線分析計算Cys-C、ACR預測T2DM患者發生STDR的ROC曲線下面積(AUC),以約登指數(靈敏度+特異性–1)最大為標準確定預測T2DM患者發生STDR的臨界值及對應的靈敏度、特異性。AUC<0.5為預測價值較低、0.5~0.7為預測價值一般,AUC>0.7~0.9為預測價值良好。P<0.05為差異有統計學意義。
2 結果
與非STDR組比較,STDR組患者血清Cys-C、ACR更高,接受PRP治療者更多,差異有統計學意義(P<0.05)(表1,2)。兩組患者年齡、性別構成比、IOL例數、代謝性白內障、眼肌麻痹、糖尿病/高血壓病程、糖尿病/高血壓病程>10年者、高血壓3級、慢性腎臟病2期、應用降血脂藥物、HbA1c、TC、TG、LDL-C、HDL-C、GFR、Scr比較,差異均無統計學意義(P>0.05)(表2)。
單因素logistic回歸分析結果顯示,血清Cys-C、ACR與STDR發生顯著相關(P<0.05);年齡、糖尿病病程、慢性腎臟病分期、GFR與STDR發生無相關性(P>0.05)。多因素logistic回歸分析結果顯示,血清Cys-C是STDR發生的獨立危險因素(P<0.05),血清Cys-C每增加0.1 mg/L,STDR發生的風險增加33.7%(表3)。
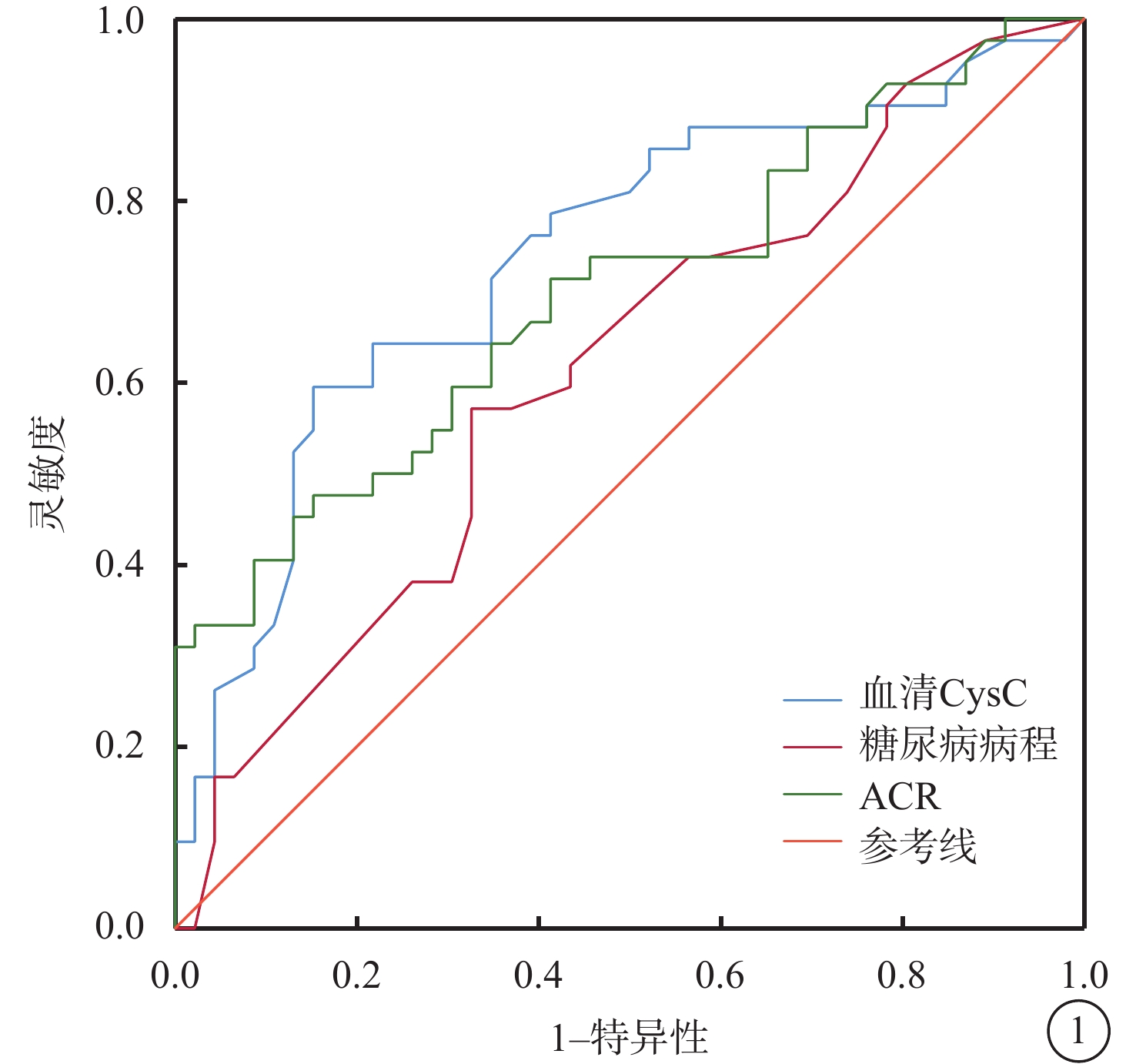
ROC曲線分析結果顯示,血清Cys-C的AUC>0.7,預測的靈敏度較高,預測效能最佳;血清Cys-C>1.065 mg/L聯合ACR>5.84 mg/mmol預測時,AUC為0.661,特異性為95.8%,但靈敏度下降至36.4%(表4,圖1)。
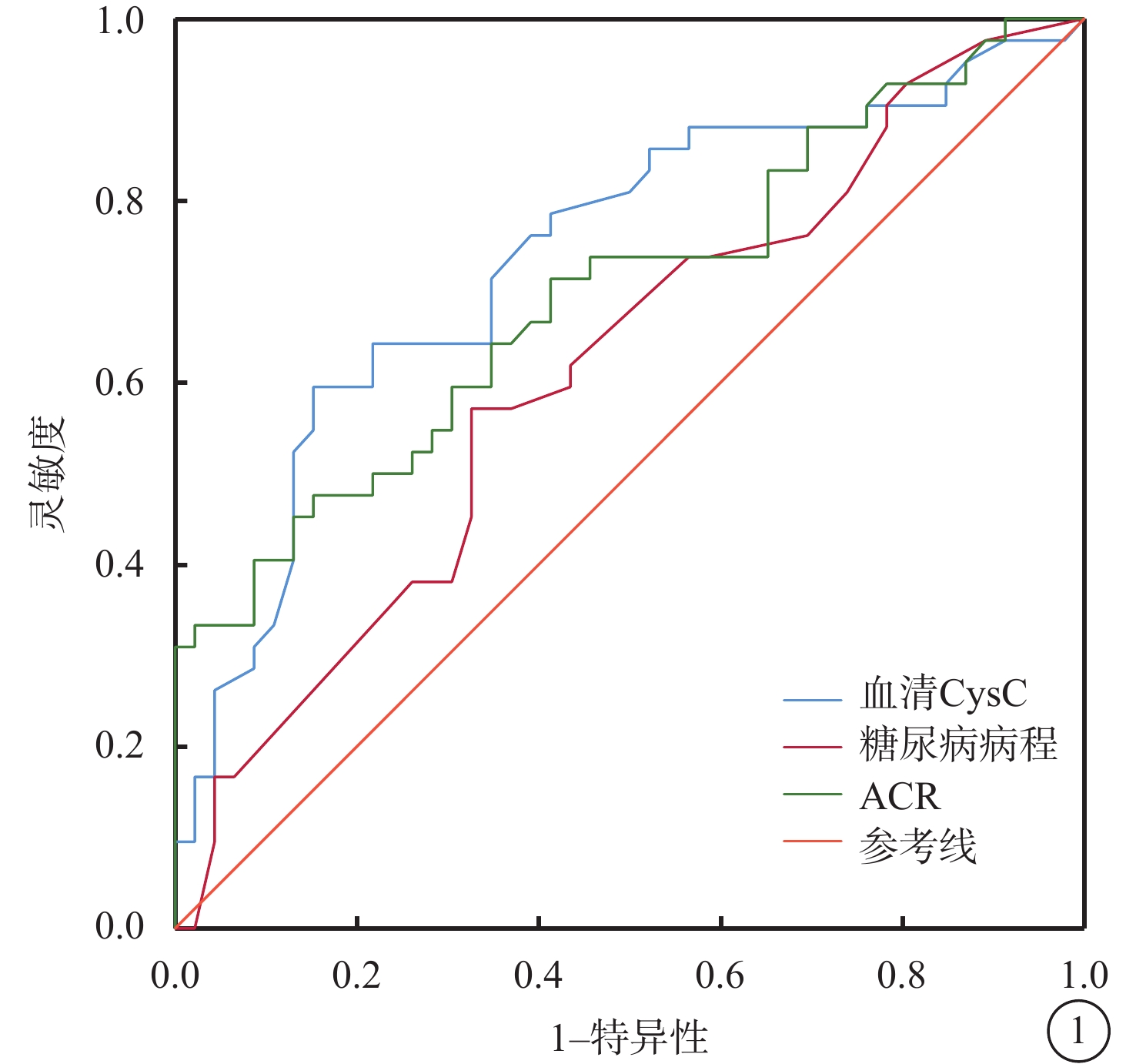 圖1
ROC曲線分析血清Cys-C、ACR、糖尿病病程對T2DM患者發生STDR的預測價值 ROC:受試者工作特征;STDR:威脅視力的糖尿病視網膜病變;T2DM:2型糖尿病;ACR:尿微量白蛋白/肌酐比值
圖1
ROC曲線分析血清Cys-C、ACR、糖尿病病程對T2DM患者發生STDR的預測價值 ROC:受試者工作特征;STDR:威脅視力的糖尿病視網膜病變;T2DM:2型糖尿病;ACR:尿微量白蛋白/肌酐比值
3 討論
近年,血清Cys-C、ACR、Scr、尿微量白蛋白等反映腎功能異常的血清指標對DR以及糖尿病相關脈絡膜薄變、血流灌注下降的預測價值逐漸得到臨床重視[7, 12-14]。Wei等[4]發現,糖尿病患者中,合并腎病與無腎病患者比較,前者血清Cys-C更高(中位數1.11 mg/L)。本研究糖尿病患者合并STDR者血清Cys-C(平均1.21 mg/L)較未合并者更高,與Wei等[4]發現一致。這提示,血清Cys-C水平的升高不僅反映腎功能的損害,同樣反映視網膜病變等的發生。Choi和Kim[12]發現,PDR患者中,與厚脈絡膜組(1.20 mg/L)比較,薄脈絡膜組血清Cys-C(2.20 mg/L)水平更高。Huang等[15]發現,與血清Cys-C水平正常組比較,血清Cys-C水平更高的患者其視盤周圍血流密度及血流灌注均明顯下降;血清Cys-C>1.25 mg/L的患者中,發生嚴重DR的風險增加11倍。上述結果提示,隨著血清Cys-C水平的升高,不僅視網膜循環容易受損,脈絡膜循環同樣容易受損。
本研究中STDR組患者年齡為(58.52±12.30)歲,ACR為4.29 mg/mmol,均較非STDR組患者高,與文獻報道基本一致[13]。另外,兩組間TC、TG、LDL-C、HDL-C差異無統計學意義,與既往研究結果[13-14]一致。多因素回歸分析發現,血清Cys-C是STDR發生的獨立危險因素,血清Cys-C每增加0.1 mg/L,STDR發生的風險增加33.7%。Gurudas等[7]研究發現,英國、印度糖尿病患者血清Cys-C預測STDR發生的OR值分別為1.12、1.38,前者略低于本研究,后者則非常接近本研究數據1.337。這提示在亞洲人群中,血清Cys-C水平預測STDR的發生可能具有更高的價值。
本研究ROC曲線分析結果顯示,血清Cys-C的AUC為0.736(最佳臨界值1.065 mg/L),ACR的特異性最大(85.4%)。AUC略低于英國糖尿病患者(0.779),但高于印度糖尿病患者(0.696),未發現ACR對STDR的預測價值。另外,本研究發現,當采用血清Cys-C>1.065 mg/L且ACR>5.84 mg/mmol作為聯合參數預測STDR時,特異性可提升至95.8%,既往文獻中未見報道。血清Cys-C是一種非糖基化半胱氨酸蛋白酶抑制劑,其生產速率和血液濃度穩定,幾乎不受年齡、性別、生理因素甚至種族的影響,視網膜色素上皮細胞是血清Cys-C的主要分泌部位[15-16]。因此,血清Cys-C非常適合作為STDR發生的預測因子,值得臨床更多關注。
血清Cys-C的另一個優勢是可在慢行腎臟疾病的早期即檢測出腎功能異常[5]。本研究結果顯示,在92例納入患者中,86例患者Scr位于正常水平;而這86例Scr正常患者中,又有33例血清Cys-C水平已經升高,因此血清Cys-C水平可以更及時地預測腎臟疾病及STDR。而即使在晚期慢性腎臟病的評估中,血清肌酐與Cys-C結合計算出的GFR也較單純Scr計算的結果更準確[17]。
本研究存在的局限性:(1)盡管樣本量達到92例,但仍不足以計算出不同血清Cys-C水平STDR的發生率,需在后續研究中繼續收集資料。(2)高水平血清Cys-C介導炎癥反應,可能參與病理變化,如動脈壁重塑、血管完整性、新生血管形成、炎癥和神經元退化等[15],但本研究缺乏對視網膜血管的量化評估,未來將引入OCT血管成像進行視網膜血液循環的研究,揭示血清Cys-C更多的預測價值。(3)血清Cys-C對STDR的預測價值可能受原發性高血壓嚴重程度影響,因為未控制的原發性高血壓、高血壓合并冠心病是引起血清Cys-C升高的重要因素[18-22]。然而,由于嚴重高血壓在本研究中占比較高(對照組16.67%,觀察組20.45%),未能進行去除高血壓的進一步分析,可能使結果產生一定偏倚。
通過簡單高效的方法及時篩查轉診威脅視力的糖尿病視網膜病變(DR)患者對于預防不可逆盲、減輕疾病醫療負擔具有重大意義。臨床對DR發生或進展風險評估多采用眼底彩色照相、光相干斷層掃描(OCT)、熒光素眼底血管造影或最新的視網膜病變自動檢測和分類人工智能等[1-3]。然而,目前尚無有效的可以預測威脅視力的DR(STDR)發生的血清生物標志物。血清胱抑素C(Cys-C)是一種低分子量蛋白,是內源性半胱氨酸蛋白酶抑制劑,不受炎癥、肌肉含量、性別、年齡等因素影響,因此有潛力成為一種良好的血清生物標志物[4]。文獻報道,血清Cys-C除了能較為敏感地評價早期腎功能損害[5],還與DR相關[6-7]。一項針對英國、印度糖尿病患者的研究顯示,血清Cys-C升高可能預示糖尿病黃斑水腫(DME)、增生型DR(PDR)的發生[7]。然而,STDR的發生與血清Cys-C以及年齡、種族、糖尿病病程、糖化血紅蛋白(HbA1c)等多種因素均相關,因此血清Cys-C在不同群體中的預測價值可能有所不同,需進一步驗證[7]。因此,我們檢測了一組漢族2型糖尿病(T2DM)患者的血清Cys-C,初步探討血清Cys-C對STDR發生的預測價值。現將結果報道如下。
1 對象和方法
非隨機對照的橫斷面臨床研究。本研究經清華大學附屬北京清華長庚醫院倫理委員會審核(批準號:24341-6-01);遵循《赫爾辛基宣言》原則;由于本研究未對患者進行額外的檢查與治療,倫理委員會免除了患者知情同意的書面要求。
2022年1~10月于清華大學附屬北京清華長庚醫院眼科就診的T2DM患者92例納入本研究。納入標準:(1)符合T2DM診斷標準[8];(2)年齡≥18歲;(3)眼軸長度≤26.5 mm。 排除標準:(1)1型糖尿病或其他類型糖尿病;(2)慢性腎臟病分期3期及以上或腎小球濾過率(GFR)<60 ml/(min·1.73 m2);(3)腎臟穿刺病理證實為高血壓腎病;(4)病理性近視;(5)圖像信號強度≤6。
所有患者均行最佳矯正視力、裂隙燈顯微鏡、間接檢眼鏡、眼底彩色照相、OCT以及HbA1c、血脂、腎功能、血壓檢查。眼底彩色照相采用日本Topcon公司TRC-50DX或佳能公司CR-2免散瞳數碼照相機進行;OCT檢查采用德國Heidelberg公司Spectralis HRA+OCT儀進行。彩色眼底像和(或)OCT圖像閱片由同兩名高年資眼底病專家(本文第一、第三作者)分別獨立完成,對不確定診斷者則由兩位醫師共同作出診斷并分級。以2003年美國眼科學會發布的DR臨床指南和國際臨床DR嚴重程度分級標準[9]為診斷和分期依據。STDR定義為重度非增生型DR(SNPDR)、PDR、DME;非STDR定義為輕度至中度非PDR、無DR。根據世界衛生組織高血壓分級標準[10]:高血壓1級定義為收縮壓140~159 mm Hg(1 mm Hg=0.133 kPa),舒張壓90~99 mm Hg;高血壓2級定義為收縮壓160~179 mm Hg,舒張壓100~109 mm Hg;高血壓3級定義為收縮壓≥180 mm Hg,舒張壓≥110 mm Hg。根據1999年美國腎臟病基金會腎臟病預后質量倡議工作組慢性腎臟病分期標準[11]:慢性腎臟病分為5期,1期定義為已有腎病,GFR正常,≥90 ml/(min·1.73 m2);2期定義為GFR降低至60~89 ml/(min·1.73 m2);3期定義為GFR降低至30~59 ml/(min·1.73 m2);4期定義為GFR降低至15~29 ml/(min·1.73 m2);5期定義為終末期腎病(腎衰竭),GFR降低至<15 ml/(min·1.73 m2)。
患者中,男性50例,女性42例;年齡(58.24±12.49)(22~79)歲。人工晶狀體(IOL)13例。全視網膜激光光凝(PRP)24例。眼肌麻痹2例;代謝性白內障5例。無DR 26例。糖尿病病程(13.18±8.35)(1~36)年,其中病程≥10年者38例。高血壓29例,其中高血壓3級17例;高血壓病程(10.76±9.77)(1~30)年,其中病程≥10年者16例。慢性腎臟病2期17例。應用降血脂藥物治療23例。HbA1c(8.05±1.82)%(5.5%~14.2%)。總膽固醇(TC)、三酰甘油(TG)、低密度脂蛋白膽固醇(LDL-C)、高密度脂蛋白膽固醇(HDL-C)分別為(4.57±1.14)、(1.73±1.44)、(2.79±1.01)、(1.19±0.27)mmol/L。血清肌酐(Scr)(70.13±22.12)μmol/L;血清Cys-C(1.07±0.39)mg/L;尿微量白蛋白/肌酐比值(ACR)(26.27±96.67)mg/mmol。根據DR分期,將患者分為STDR組、非STDR組,分別為44、48例。
采用SPSS25.0軟件行統計學分析。符合正態分布的連續變量以均數±標準差(x±s)表示;不符合正態分布的連續變量以中位數(四分位數間距)[M(P25,P75)]表示。符合正態分布的連續變量,組間比較采用獨立樣本t檢驗;不符合正態分布的連續變量,組間比較采用Mann-Whitney U檢驗。分類變量以百分比(n,%)表示,組間比較采用χ2檢驗或Fisher's確切概率法。采用logistic回歸分析估算各候選變量的比值比(OR)。單因素分析中,P<0.1的變量納入多因素回歸分析。應用受試者工作特征(ROC)曲線分析計算Cys-C、ACR預測T2DM患者發生STDR的ROC曲線下面積(AUC),以約登指數(靈敏度+特異性–1)最大為標準確定預測T2DM患者發生STDR的臨界值及對應的靈敏度、特異性。AUC<0.5為預測價值較低、0.5~0.7為預測價值一般,AUC>0.7~0.9為預測價值良好。P<0.05為差異有統計學意義。
2 結果
與非STDR組比較,STDR組患者血清Cys-C、ACR更高,接受PRP治療者更多,差異有統計學意義(P<0.05)(表1,2)。兩組患者年齡、性別構成比、IOL例數、代謝性白內障、眼肌麻痹、糖尿病/高血壓病程、糖尿病/高血壓病程>10年者、高血壓3級、慢性腎臟病2期、應用降血脂藥物、HbA1c、TC、TG、LDL-C、HDL-C、GFR、Scr比較,差異均無統計學意義(P>0.05)(表2)。
單因素logistic回歸分析結果顯示,血清Cys-C、ACR與STDR發生顯著相關(P<0.05);年齡、糖尿病病程、慢性腎臟病分期、GFR與STDR發生無相關性(P>0.05)。多因素logistic回歸分析結果顯示,血清Cys-C是STDR發生的獨立危險因素(P<0.05),血清Cys-C每增加0.1 mg/L,STDR發生的風險增加33.7%(表3)。
ROC曲線分析結果顯示,血清Cys-C的AUC>0.7,預測的靈敏度較高,預測效能最佳;血清Cys-C>1.065 mg/L聯合ACR>5.84 mg/mmol預測時,AUC為0.661,特異性為95.8%,但靈敏度下降至36.4%(表4,圖1)。
 圖1
ROC曲線分析血清Cys-C、ACR、糖尿病病程對T2DM患者發生STDR的預測價值 ROC:受試者工作特征;STDR:威脅視力的糖尿病視網膜病變;T2DM:2型糖尿病;ACR:尿微量白蛋白/肌酐比值
圖1
ROC曲線分析血清Cys-C、ACR、糖尿病病程對T2DM患者發生STDR的預測價值 ROC:受試者工作特征;STDR:威脅視力的糖尿病視網膜病變;T2DM:2型糖尿病;ACR:尿微量白蛋白/肌酐比值
3 討論
近年,血清Cys-C、ACR、Scr、尿微量白蛋白等反映腎功能異常的血清指標對DR以及糖尿病相關脈絡膜薄變、血流灌注下降的預測價值逐漸得到臨床重視[7, 12-14]。Wei等[4]發現,糖尿病患者中,合并腎病與無腎病患者比較,前者血清Cys-C更高(中位數1.11 mg/L)。本研究糖尿病患者合并STDR者血清Cys-C(平均1.21 mg/L)較未合并者更高,與Wei等[4]發現一致。這提示,血清Cys-C水平的升高不僅反映腎功能的損害,同樣反映視網膜病變等的發生。Choi和Kim[12]發現,PDR患者中,與厚脈絡膜組(1.20 mg/L)比較,薄脈絡膜組血清Cys-C(2.20 mg/L)水平更高。Huang等[15]發現,與血清Cys-C水平正常組比較,血清Cys-C水平更高的患者其視盤周圍血流密度及血流灌注均明顯下降;血清Cys-C>1.25 mg/L的患者中,發生嚴重DR的風險增加11倍。上述結果提示,隨著血清Cys-C水平的升高,不僅視網膜循環容易受損,脈絡膜循環同樣容易受損。
本研究中STDR組患者年齡為(58.52±12.30)歲,ACR為4.29 mg/mmol,均較非STDR組患者高,與文獻報道基本一致[13]。另外,兩組間TC、TG、LDL-C、HDL-C差異無統計學意義,與既往研究結果[13-14]一致。多因素回歸分析發現,血清Cys-C是STDR發生的獨立危險因素,血清Cys-C每增加0.1 mg/L,STDR發生的風險增加33.7%。Gurudas等[7]研究發現,英國、印度糖尿病患者血清Cys-C預測STDR發生的OR值分別為1.12、1.38,前者略低于本研究,后者則非常接近本研究數據1.337。這提示在亞洲人群中,血清Cys-C水平預測STDR的發生可能具有更高的價值。
本研究ROC曲線分析結果顯示,血清Cys-C的AUC為0.736(最佳臨界值1.065 mg/L),ACR的特異性最大(85.4%)。AUC略低于英國糖尿病患者(0.779),但高于印度糖尿病患者(0.696),未發現ACR對STDR的預測價值。另外,本研究發現,當采用血清Cys-C>1.065 mg/L且ACR>5.84 mg/mmol作為聯合參數預測STDR時,特異性可提升至95.8%,既往文獻中未見報道。血清Cys-C是一種非糖基化半胱氨酸蛋白酶抑制劑,其生產速率和血液濃度穩定,幾乎不受年齡、性別、生理因素甚至種族的影響,視網膜色素上皮細胞是血清Cys-C的主要分泌部位[15-16]。因此,血清Cys-C非常適合作為STDR發生的預測因子,值得臨床更多關注。
血清Cys-C的另一個優勢是可在慢行腎臟疾病的早期即檢測出腎功能異常[5]。本研究結果顯示,在92例納入患者中,86例患者Scr位于正常水平;而這86例Scr正常患者中,又有33例血清Cys-C水平已經升高,因此血清Cys-C水平可以更及時地預測腎臟疾病及STDR。而即使在晚期慢性腎臟病的評估中,血清肌酐與Cys-C結合計算出的GFR也較單純Scr計算的結果更準確[17]。
本研究存在的局限性:(1)盡管樣本量達到92例,但仍不足以計算出不同血清Cys-C水平STDR的發生率,需在后續研究中繼續收集資料。(2)高水平血清Cys-C介導炎癥反應,可能參與病理變化,如動脈壁重塑、血管完整性、新生血管形成、炎癥和神經元退化等[15],但本研究缺乏對視網膜血管的量化評估,未來將引入OCT血管成像進行視網膜血液循環的研究,揭示血清Cys-C更多的預測價值。(3)血清Cys-C對STDR的預測價值可能受原發性高血壓嚴重程度影響,因為未控制的原發性高血壓、高血壓合并冠心病是引起血清Cys-C升高的重要因素[18-22]。然而,由于嚴重高血壓在本研究中占比較高(對照組16.67%,觀察組20.45%),未能進行去除高血壓的進一步分析,可能使結果產生一定偏倚。