引用本文: 包鄭伊琳, 康文偉, 楊怡, 李娟娟. 光相干斷層掃描血管成像對視網膜靜脈阻塞中側支循環的觀察. 中華眼底病雜志, 2024, 40(7): 500-505. doi: 10.3760/cma.j.cn511434-20240110-00016 復制
版權信息: ?四川大學華西醫院華西期刊社《中華眼底病雜志》版權所有,未經授權不得轉載、改編
視網膜靜脈阻塞(RVO)后建立的側支循環是一類較為常見的代償反應[1]。既往對于側支循環的觀察主要依靠眼底彩色照相及熒光素眼底血管造影(FFA)檢查,但受檢查技術的限制,主要集中于后極部側支循環形態的觀察,而周邊部側支循環情況不明;側支循環建立時間受FFA可重復性差的影響也認識有限。此外,傳統影像檢查僅能對視網膜淺層血管的側支循環進行觀察,深層血管側支循環知之甚少[2]。廣角光相干斷層掃描(OCT)血管成像(OCTA)是觀察眼底血管形態的非侵入性技術,分辨率高,可清晰顯示視網膜淺層、深層血管形態,是觀察RVO側支循環的新技術手段。為此,我們對一組不同類型RVO患者進行了掃頻源OCTA(SS-OCTA)檢查,觀察其側支循環發生率、部位、形態特點、形成時間以及抗血管內皮生長因子(VEGF)藥物治療對側支循環形成的影響。現將結果報道如下。
1 對象和方法
回顧性臨床研究。本研究遵循《赫爾辛基宣言》原則,并經云南大學附屬醫院倫理委員會審核批準(2024073)。
2021年12月至2023年12月于云南大學附屬醫院眼科檢查確診的RVO患者360例360只眼納入本研究。其中,男性157例157只眼,女性203例203只眼;均為單眼發病。年齡(61.0±5.9)(45~82)歲。缺血型232只眼;非缺血型128只眼。合并黃斑水腫210只眼。出現癥狀至就診時病程為3 d~6個月。所有患者均符合RVO臨床診斷標準[3]:無痛性視力下降;阻塞區域視網膜靜脈擴張,沿阻塞血管分布的“火焰狀”出血,可合并棉絨斑及滲出。排除標準:視網膜大動脈瘤、視網膜血管炎、糖尿病視網膜病變等其他類型的眼底血管病變;既往有激光光凝、抗VEGF藥物治療史;圖像信號強度<6。
患眼均行最佳矯正視力、裂隙燈顯微鏡、間接檢眼鏡、眼底彩色照相、OCT、OCTA檢查。采用視微影像(河南)科技有限公司VG200D SS-OCT儀行黃斑區OCTA檢查。掃描區域分別為中心凹、顳上、顳下、鼻上、鼻下;掃描范圍12 mm×12 mm。設備自帶軟件自動將采集的圖像進行拼接。連接阻塞區域與非阻塞區域的血管定義為側支循環,且連結區域視網膜無出血[4]。排除阻塞區域紆曲擴張的血管及缺血區域的新生血管。
參照文獻[5]的方法,根據阻塞部位將RVO分為黃斑分支靜脈阻塞(MBRVO)、視網膜分支靜脈阻塞(BRVO)、視網膜中央靜脈阻塞(CRVO),分別為67、187、106只眼。MBRVO者67只眼中,缺血型、非缺血型分別為50、17只眼;合并黃斑水腫60只眼。BRVO者187只眼中,缺血型、非缺血型分別為116、71只眼;半側BRVO 32只眼;合并黃斑水腫119只眼。CRVO者106只眼中,缺血型、非缺血型分別為75、31只眼;合并黃斑水腫21只眼。
明確診斷后,合并黃斑水腫的210只眼均給予玻璃體腔注射抗VEGF藥物治療。每一個月1次,連續3~5個月的負荷治療后,經評估按需治療。其中,MBRVO、BRVO者注藥次數為3~8次,平均5.2次;CRVO者注藥次數為3~28次,平均9.8次。
隨訪時間(4.0±1.9)(0.3~6.0)個月。隨訪時采用初診時相同設備和方法行相關檢查。從視盤發出呈血管袢樣血管在視盤走形一段后回到視盤的短路循環定義為視盤睫狀血管短路型側支循環。觀察不同類型RVO側支循環的發生率、發生部位、形態特點、形成時間以及抗VEGF藥物治療對側支循環形成的影響。
采用SPSS25.0軟件行統計學分析。不同類型RVO側支循環建立率的比較采用χ2檢驗。P<0.05為差異有統計學意義。
2 結果
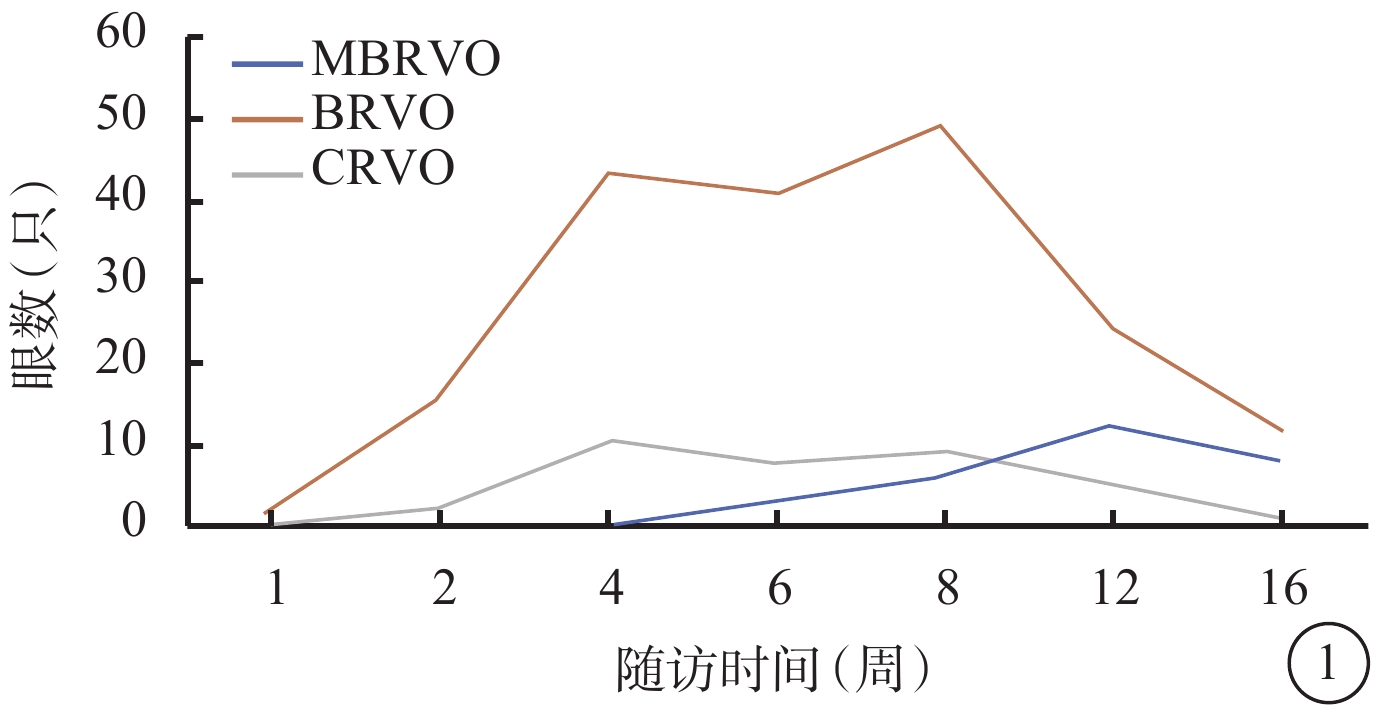
出現癥狀至就診時病程1周時,MBRVO、BRVO患眼部分側支循環已建立;1~2個月時,已建立較為豐富而穩定的側支循環。病程1個月時,CRVO患眼視盤短路支未見形成;病程2~3個月時,多數患眼視盤短路支形成(圖1,2)。
 圖1
不同類型視網膜靜脈阻塞側支循環建立時間 MBRVO:黃斑分支靜脈阻塞;BRVO:視網膜分支靜脈阻塞;CRVO:視網膜中央靜脈阻塞
圖1
不同類型視網膜靜脈阻塞側支循環建立時間 MBRVO:黃斑分支靜脈阻塞;BRVO:視網膜分支靜脈阻塞;CRVO:視網膜中央靜脈阻塞
 圖2
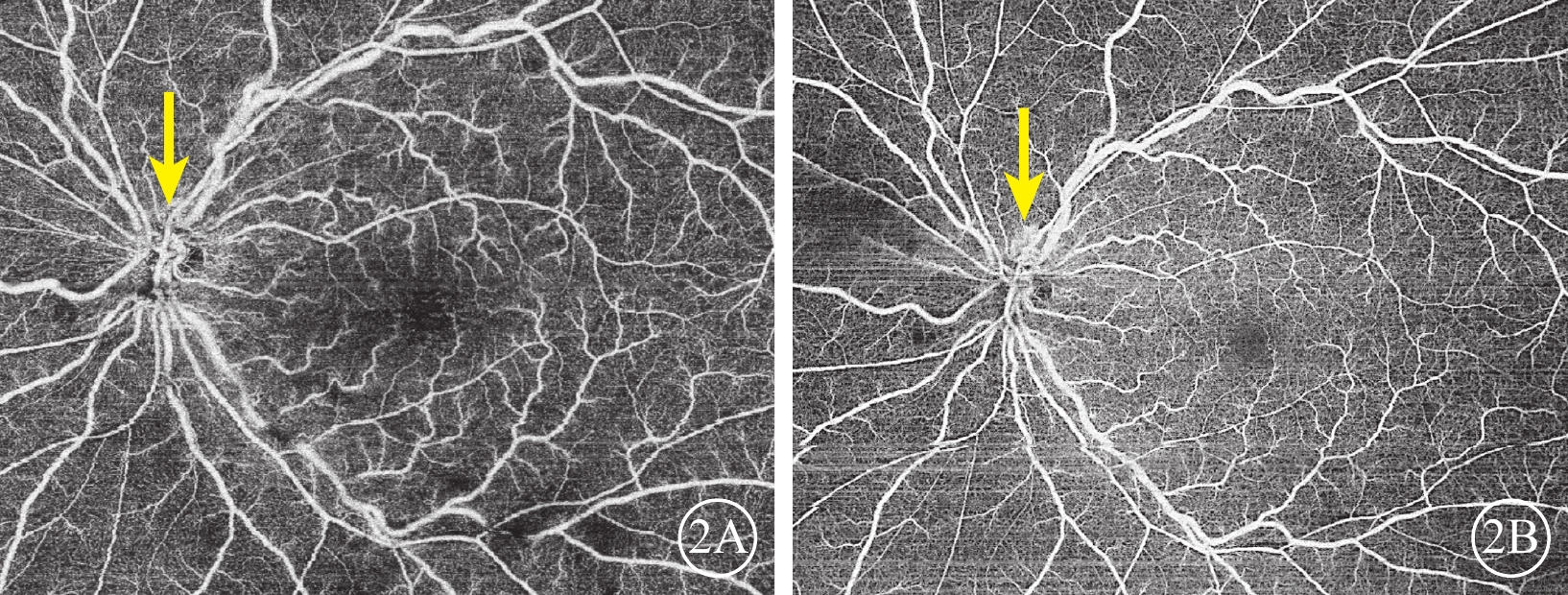
CRVO側支循環OCTA像 2A示初診時,未見視盤側支循環(黃箭);2B示出現癥狀至就診時病程3個月時,視盤側支循環建立(黃箭) CRVO:視網膜中央靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖2
CRVO側支循環OCTA像 2A示初診時,未見視盤側支循環(黃箭);2B示出現癥狀至就診時病程3個月時,視盤側支循環建立(黃箭) CRVO:視網膜中央靜脈阻塞;OCTA:光相干斷層掃描血管成像
出現癥狀至就診時病程6個月時,360只眼中,側支循環建立252只眼(70.0%,252/360)。MBRVO者67只眼中,側支循環建立36只眼(53.7%,36/67),其中缺血型、非缺血型分別為24、12只眼。BRVO者187只眼均建立側支循環(100.0%,187/187),其中缺血型、非缺血型分別為116、71只眼。CRVO者106只眼中,視盤側支循環建立29只眼(18.1%,29/106),其中缺血型、非缺血型分別為20、9只眼;未觀察到視網膜血管之間的側支循環。MBRVO、BRVO、CRVO患眼側支循環建立率比較,差異有統計學意義(χ2=0.024,P<0.05)。
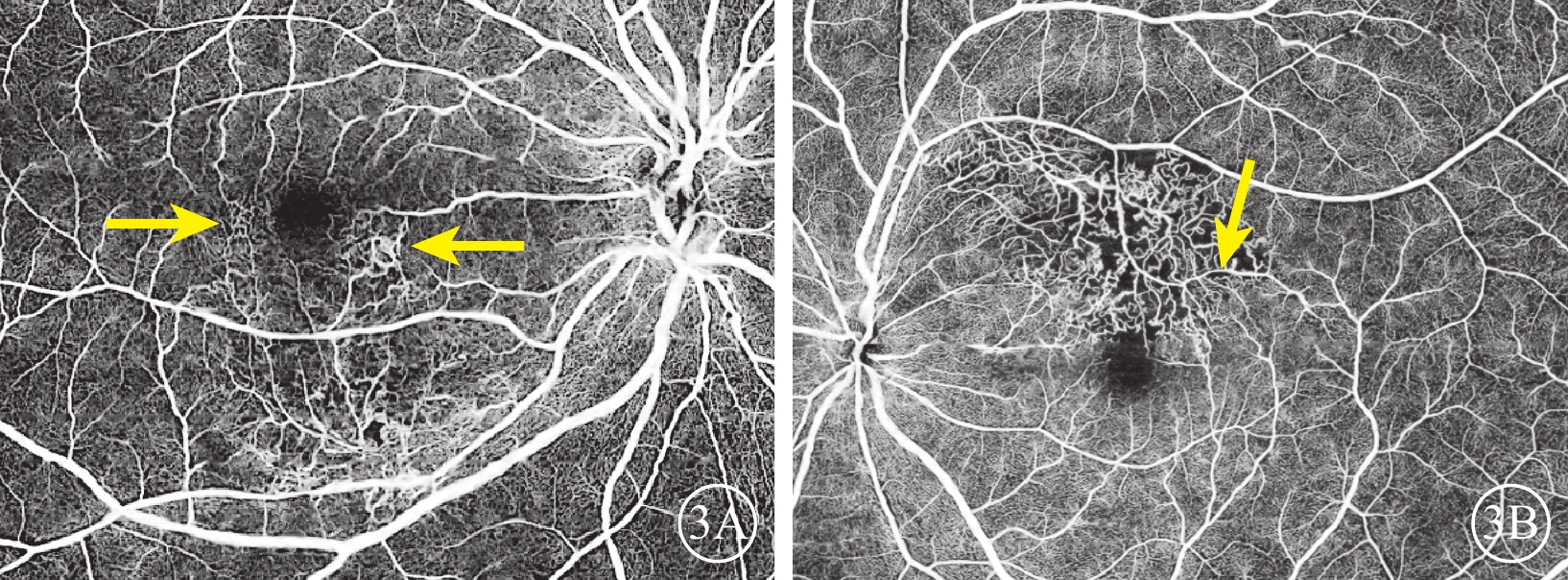
MBRVO者中建立側支循環的36只眼,其側支循環均建立于阻塞區域和非阻塞區域之間的垂直水平縫處,可見于黃斑中心凹鼻側及顳側(圖3A),也可見于距中心凹稍遠處(圖3B),數量為1~4支;其管徑較CRVO的側支血管小。
 圖3
MBRVO側支循環OCTA像 3A、3B示跨越水平縫建立的側支循環(黃箭),緊鄰中心凹(3A)或中心凹較遠處(3B) MBRVO:黃斑分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖3
MBRVO側支循環OCTA像 3A、3B示跨越水平縫建立的側支循環(黃箭),緊鄰中心凹(3A)或中心凹較遠處(3B) MBRVO:黃斑分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
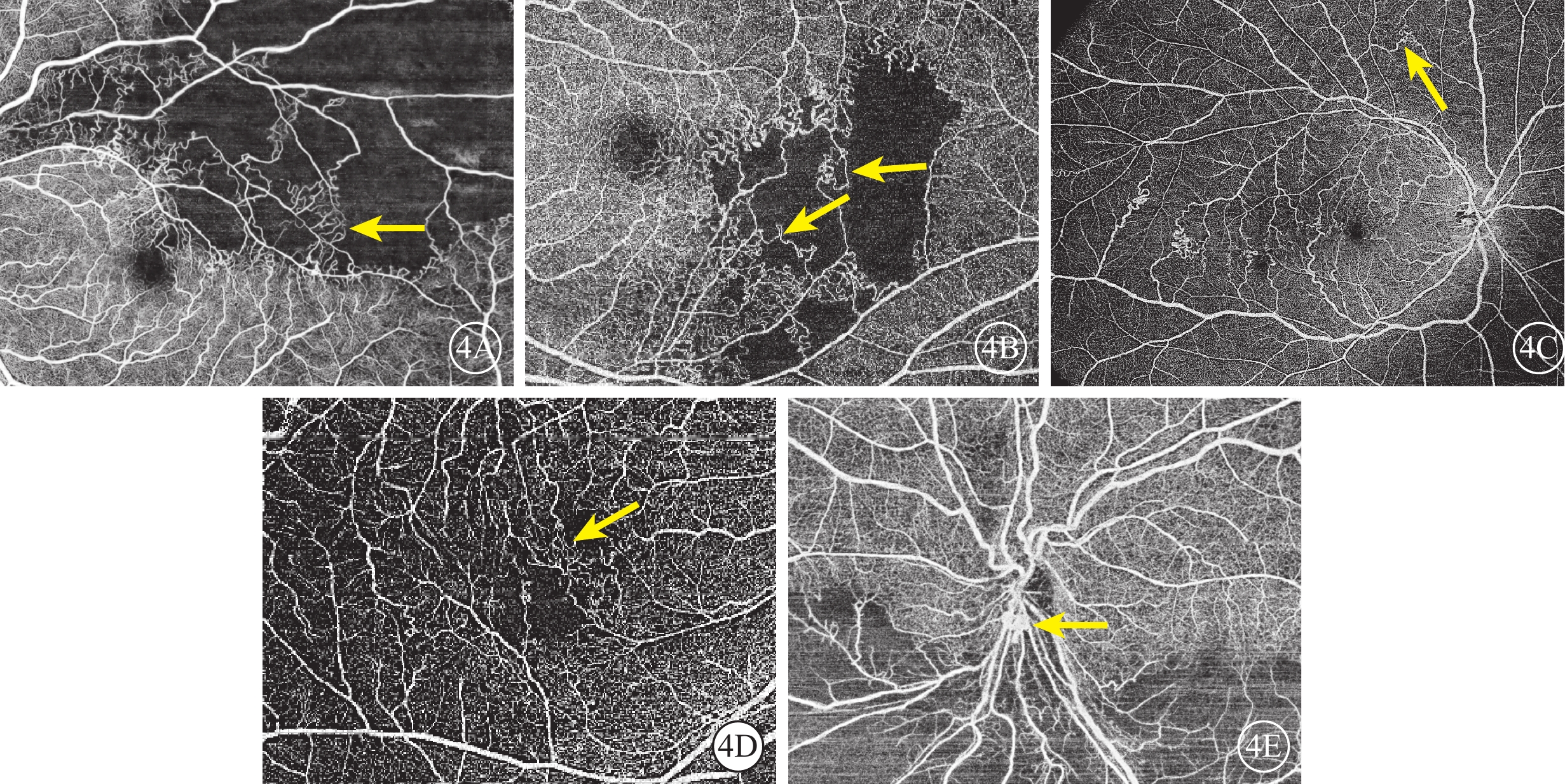
BRVO者187只眼中,側支循環建立于阻塞區域和非阻塞區域之間的垂直水平縫處(圖4A)102只眼;阻塞最中央逐級搭橋至正常血管上的側支循環(圖4B)54只眼;通過鼻側與顳側建立側支循環(圖4C)19只眼;通過中心凹建立的側支循環(圖4D)12只眼。除常規區域的側支循環外,18只眼同時建立了視盤睫狀血管短路型側支循環(圖4E),均為半側BRVO者。建立的側支循環其形態表現為平直(圖5A)、螺旋狀紆曲(圖5B)和花簇狀(圖5C)。此外,除視網膜淺層毛細血管叢可見豐富的側支循環外(圖6A),側支循環也可建立于深層毛細血管叢之間(圖6B)。
 圖4
BRVO側支循環建立部位OCTA像 4A示垂直于水平縫建立的阻塞與非阻塞區域之間的側支循環(黃箭);4B示阻塞最中央逐級搭橋至正常血管上的側支循環(黃箭);4C示鼻側與顳側間建立的側支循環(黃箭);4D示通過中心凹建立的側支循環(黃箭) ;4E示視盤睫狀血管短路型側支循環(黃箭) BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖4
BRVO側支循環建立部位OCTA像 4A示垂直于水平縫建立的阻塞與非阻塞區域之間的側支循環(黃箭);4B示阻塞最中央逐級搭橋至正常血管上的側支循環(黃箭);4C示鼻側與顳側間建立的側支循環(黃箭);4D示通過中心凹建立的側支循環(黃箭) ;4E示視盤睫狀血管短路型側支循環(黃箭) BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
 圖5
BRVO側支循環血管形態OCTA像 5A~5C分別示平直、螺旋狀紆曲、花簇狀側支循環(黃箭) BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖5
BRVO側支循環血管形態OCTA像 5A~5C分別示平直、螺旋狀紆曲、花簇狀側支循環(黃箭) BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
 圖6
BRVO側支循環分層情況OCTA像 6A示淺層視網膜毛細血管叢可見豐富的側支循環;6B示深層視網膜毛細血管叢之間建立的側支循環 BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖6
BRVO側支循環分層情況OCTA像 6A示淺層視網膜毛細血管叢可見豐富的側支循環;6B示深層視網膜毛細血管叢之間建立的側支循環 BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
CRVO建立側支循環的29只眼,均為視盤睫狀血管短路型側支循環(圖7)。
 圖7
CRVO側支循環OCTA像 視盤睫狀血管短路型側支循環(黃箭) CRVO:視網膜中央靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖7
CRVO側支循環OCTA像 視盤睫狀血管短路型側支循環(黃箭) CRVO:視網膜中央靜脈阻塞;OCTA:光相干斷層掃描血管成像
隨訪6個月,行抗VEGF藥物治療的210只眼中,側支循環建立160只眼(76.19%,160/210)。其中,MBRVO 32只眼(50.7%,32/63);BRVO 119只眼(100.0%,119/119)(圖8);CRVO 9只眼(32.1%,9/28)。
 圖8
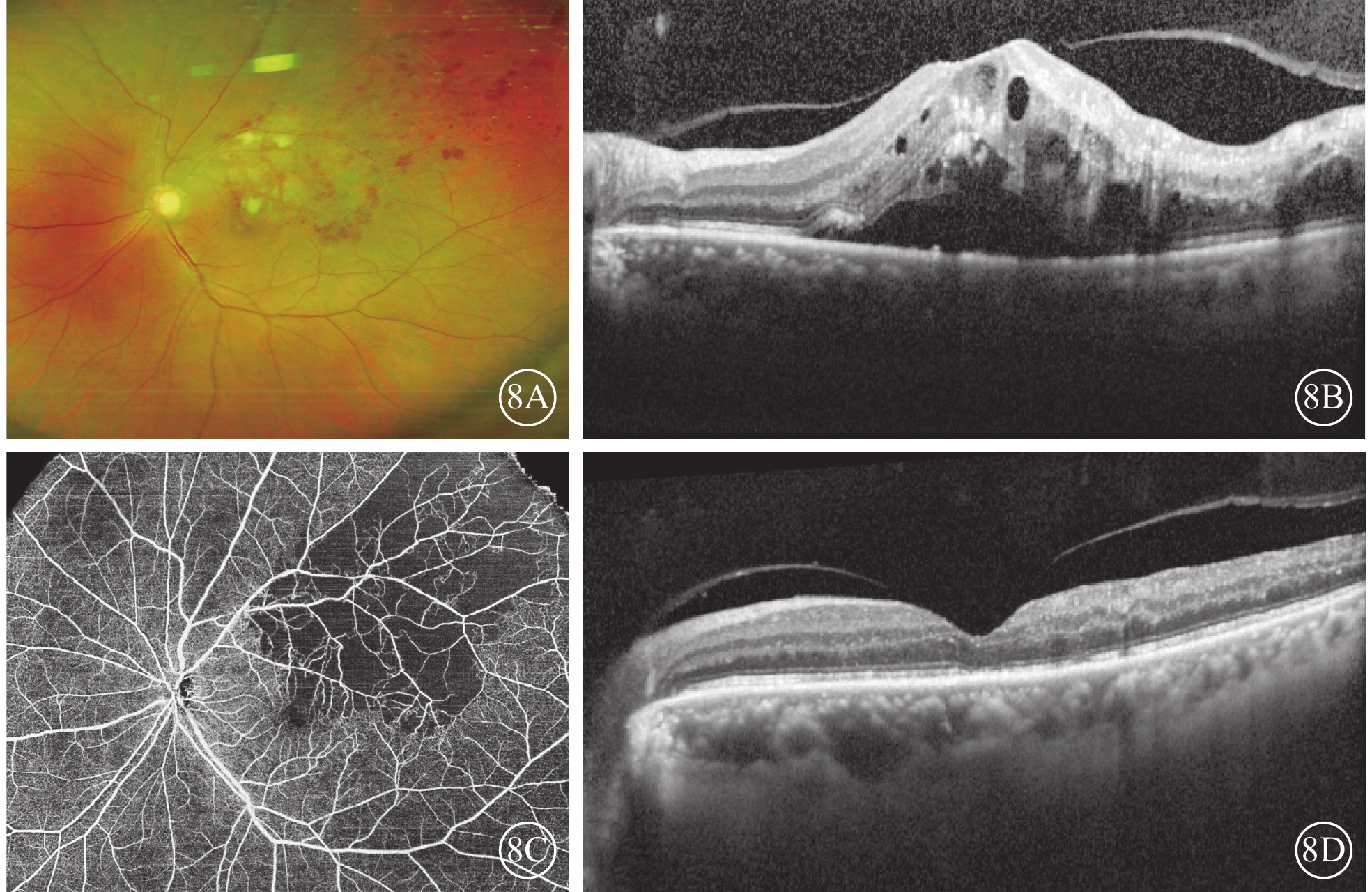
BRVO合并黃斑水腫患眼抗VEGF藥物治療后側支循環OCTA像 8A、8B分別示首診時彩色眼底、OCT像,顳上靜脈阻塞、視網膜出血、黃斑水腫;8C、8D分別示抗VEGF藥物治療1個月時OCTA、OCT像,側支循環建立(8C)、黃斑水腫消退(8D) BRVO:視網膜分支靜脈阻塞;VEGF:血管內皮生長因子;OCT:光相干斷層掃描;OCTA:OCT血管成像
圖8
BRVO合并黃斑水腫患眼抗VEGF藥物治療后側支循環OCTA像 8A、8B分別示首診時彩色眼底、OCT像,顳上靜脈阻塞、視網膜出血、黃斑水腫;8C、8D分別示抗VEGF藥物治療1個月時OCTA、OCT像,側支循環建立(8C)、黃斑水腫消退(8D) BRVO:視網膜分支靜脈阻塞;VEGF:血管內皮生長因子;OCT:光相干斷層掃描;OCTA:OCT血管成像
3 討論
廣角OCTA為臨床提供了無創、可重復性好、血管形態不受造影劑滲漏影響的影像手段,與既往傳統檢查比較,對RVO側支循環有了更多角度的觀察結果[6]。
對于不同類型RVO建立側支循環的概率,OCTA相對于FFA可進行更精準的觀察。在所有類型的RVO中BRVO的側支循環建立最為豐富。Suzuki等[7]對18例BRVO患者(28只眼)進行OCTA觀察,所有患者均觀察到側支循環建立。既往認為MBRVO阻塞程度較輕,代償機制不旺盛,而這部分血管較小,分辨率較差,所以認為MBRVO較少形成側支循環。隨著OCTA技術的發展,更多側支循環在MBRVO中被發現。Suzuki等[7]對18例BRVO患者(28只眼)行OCTA檢查,隨訪6個月時,MBRVO 10只眼中5只眼發現側支循環。本組患眼觀察結果也相似,53.7%的MBRVO患眼觀察到側支循環的建立。而對于CRVO,由于阻塞旁路空間最少,側支循環建立也最困難,本組CRVO 106只眼中,僅18.1%的患眼觀察到側支循環的建立。
不同類型側支循環建立部位和特點也存在差異。BRVO由于阻塞的是大支分支靜脈,周邊血管代償能力強,旁路空間多,所以側支循環最為豐富。Weinberg等[8]使用OCTA對一組BRVO患眼進行檢查,初診后12 個月,其側支循環主要在水平縫區域,連接阻塞區域和非阻塞區域。本組患眼除典型通過水平縫阻塞區域與非阻塞區域之間側支循環建立,還觀察到鼻側與顳側之間也可建立側支循環,阻塞中心區域通過逐級搭橋的形式與正常靜脈建立側支循環。而MBRVO常見的側支循環主要形式是通過黃斑區末梢血管之間的水平縫建立。而對于阻塞面積較大的CRVO和半側BRVO,視盤短路是觀察到最典型而獨特的側支循環方式。對其病理機制,Fuller等[9]認為CRVO阻塞部位一般位于或靠近篩板,導致視網膜中央靜脈的所有分支回流受到影響,導致視網膜循環內沒有壓力梯度驅動視網膜內側支循環的形成,但在視神經邊緣存在從視網膜到脈絡膜循環的視盤睫狀短路引流。因此,呈環狀的繼發性視盤血管袢是CRVO側支循環的主要形式。既往對于側支循環的部位觀察主要依靠眼底彩色照相和FFA,但均存在不能分層的局限性,因此對于側支循環的觀察一直停留在淺層視網膜血管,隨著OCTA的應用,發現側支循環也可發生在深層血管網中[10]。Freund等[11]觀察23例BRVO患者的110支側支血管,發現側支循環主要位于深層毛細血管叢,且未觀察到僅存在于淺層毛細血管叢的側支循環。
對于側支循環建立的時間,目前文獻報道的數據存在較大差異。Christoffersen和Larsen[12]對250例BRVO患者的臨床資料進行回顧性分析,發現側支循環的建立發生在BRVO發病后6~24個月。但也有學者認為側支循環作為RVO的一種代償機制,啟動應該更早。Takahashi等[13]應用激光誘導建立小鼠RVO模型,通過OCTA檢查觀察發現,建模后3 d,閉塞血管周圍的血管粗大,出現側支循環;5~7 d,側支循環更加清晰可見;14 d時,在遠離閉塞血管的區域均觀察到側支循環的建立。根據動物實驗,有證據懷疑側支循環出現的時間可能早于6~24個月。本組患眼阻塞發生后10 d即觀察到側支血管向阻塞區域延伸,多數患眼1個月左右可觀察到不同程度的側支循環。因此,我們認為側支循環建立的時間應比傳統認知更早發生。
對于抗VEGF藥物治療是否影響側支循環的建立,一直為臨床關注。抗VEGF藥物治療目前已成為治療RVO合并黃斑水腫的一線治療方案[14]。理論上,降低眼內VEGF水平的同時也抑制側支循環的建立,阻斷機體自身啟動的代償機制也存在可能性[15]。本研究雖然因治療方案未能設置對照組進行前瞻性對比觀察,但各種類型的RVO抗VEGF藥物治療后側支循環建立的比率未受到大幅度影響,我們認為抗VEGF藥物治療并不抑制側支循環的建立。該結論與目前文獻結論相似。Montero-Moreno和Ruiz-Moreno[16]觀察了一組經歷2年抗VEGF藥物治療的BRVO及CRVO患者,其中BRVO組21只眼中17只眼建立側支循環,CRVO組7只眼出現視盤分流。其機制我們認為是,新生血管的建立依賴VEGF水平的增高,但側支循環更多為正常血管的延伸,而非新生血管,故其并不依賴VEGF,因此抗VEGF藥物治療并不影響側支循環的建立。
本研究存在的局限性:(1)一次性掃描面積有限,不能進行大面積掃描成像;(2)OCTA無需注射造影劑,在觀察血管滲漏方面存在缺陷,對于新生血管與側支血管在特定時間存在鑒別難點;(3)觀察深層視網膜毛細血管叢時,可以看到來自淺層血管網的影像和投射軌跡,造成偽影。隨著OCTA技術和算法的不斷發展,在包括側支循環等多個領域將會出現更多研究成果。
視網膜靜脈阻塞(RVO)后建立的側支循環是一類較為常見的代償反應[1]。既往對于側支循環的觀察主要依靠眼底彩色照相及熒光素眼底血管造影(FFA)檢查,但受檢查技術的限制,主要集中于后極部側支循環形態的觀察,而周邊部側支循環情況不明;側支循環建立時間受FFA可重復性差的影響也認識有限。此外,傳統影像檢查僅能對視網膜淺層血管的側支循環進行觀察,深層血管側支循環知之甚少[2]。廣角光相干斷層掃描(OCT)血管成像(OCTA)是觀察眼底血管形態的非侵入性技術,分辨率高,可清晰顯示視網膜淺層、深層血管形態,是觀察RVO側支循環的新技術手段。為此,我們對一組不同類型RVO患者進行了掃頻源OCTA(SS-OCTA)檢查,觀察其側支循環發生率、部位、形態特點、形成時間以及抗血管內皮生長因子(VEGF)藥物治療對側支循環形成的影響。現將結果報道如下。
1 對象和方法
回顧性臨床研究。本研究遵循《赫爾辛基宣言》原則,并經云南大學附屬醫院倫理委員會審核批準(2024073)。
2021年12月至2023年12月于云南大學附屬醫院眼科檢查確診的RVO患者360例360只眼納入本研究。其中,男性157例157只眼,女性203例203只眼;均為單眼發病。年齡(61.0±5.9)(45~82)歲。缺血型232只眼;非缺血型128只眼。合并黃斑水腫210只眼。出現癥狀至就診時病程為3 d~6個月。所有患者均符合RVO臨床診斷標準[3]:無痛性視力下降;阻塞區域視網膜靜脈擴張,沿阻塞血管分布的“火焰狀”出血,可合并棉絨斑及滲出。排除標準:視網膜大動脈瘤、視網膜血管炎、糖尿病視網膜病變等其他類型的眼底血管病變;既往有激光光凝、抗VEGF藥物治療史;圖像信號強度<6。
患眼均行最佳矯正視力、裂隙燈顯微鏡、間接檢眼鏡、眼底彩色照相、OCT、OCTA檢查。采用視微影像(河南)科技有限公司VG200D SS-OCT儀行黃斑區OCTA檢查。掃描區域分別為中心凹、顳上、顳下、鼻上、鼻下;掃描范圍12 mm×12 mm。設備自帶軟件自動將采集的圖像進行拼接。連接阻塞區域與非阻塞區域的血管定義為側支循環,且連結區域視網膜無出血[4]。排除阻塞區域紆曲擴張的血管及缺血區域的新生血管。
參照文獻[5]的方法,根據阻塞部位將RVO分為黃斑分支靜脈阻塞(MBRVO)、視網膜分支靜脈阻塞(BRVO)、視網膜中央靜脈阻塞(CRVO),分別為67、187、106只眼。MBRVO者67只眼中,缺血型、非缺血型分別為50、17只眼;合并黃斑水腫60只眼。BRVO者187只眼中,缺血型、非缺血型分別為116、71只眼;半側BRVO 32只眼;合并黃斑水腫119只眼。CRVO者106只眼中,缺血型、非缺血型分別為75、31只眼;合并黃斑水腫21只眼。
明確診斷后,合并黃斑水腫的210只眼均給予玻璃體腔注射抗VEGF藥物治療。每一個月1次,連續3~5個月的負荷治療后,經評估按需治療。其中,MBRVO、BRVO者注藥次數為3~8次,平均5.2次;CRVO者注藥次數為3~28次,平均9.8次。
隨訪時間(4.0±1.9)(0.3~6.0)個月。隨訪時采用初診時相同設備和方法行相關檢查。從視盤發出呈血管袢樣血管在視盤走形一段后回到視盤的短路循環定義為視盤睫狀血管短路型側支循環。觀察不同類型RVO側支循環的發生率、發生部位、形態特點、形成時間以及抗VEGF藥物治療對側支循環形成的影響。
采用SPSS25.0軟件行統計學分析。不同類型RVO側支循環建立率的比較采用χ2檢驗。P<0.05為差異有統計學意義。
2 結果
出現癥狀至就診時病程1周時,MBRVO、BRVO患眼部分側支循環已建立;1~2個月時,已建立較為豐富而穩定的側支循環。病程1個月時,CRVO患眼視盤短路支未見形成;病程2~3個月時,多數患眼視盤短路支形成(圖1,2)。
 圖1
不同類型視網膜靜脈阻塞側支循環建立時間 MBRVO:黃斑分支靜脈阻塞;BRVO:視網膜分支靜脈阻塞;CRVO:視網膜中央靜脈阻塞
圖1
不同類型視網膜靜脈阻塞側支循環建立時間 MBRVO:黃斑分支靜脈阻塞;BRVO:視網膜分支靜脈阻塞;CRVO:視網膜中央靜脈阻塞
 圖2
CRVO側支循環OCTA像 2A示初診時,未見視盤側支循環(黃箭);2B示出現癥狀至就診時病程3個月時,視盤側支循環建立(黃箭) CRVO:視網膜中央靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖2
CRVO側支循環OCTA像 2A示初診時,未見視盤側支循環(黃箭);2B示出現癥狀至就診時病程3個月時,視盤側支循環建立(黃箭) CRVO:視網膜中央靜脈阻塞;OCTA:光相干斷層掃描血管成像
出現癥狀至就診時病程6個月時,360只眼中,側支循環建立252只眼(70.0%,252/360)。MBRVO者67只眼中,側支循環建立36只眼(53.7%,36/67),其中缺血型、非缺血型分別為24、12只眼。BRVO者187只眼均建立側支循環(100.0%,187/187),其中缺血型、非缺血型分別為116、71只眼。CRVO者106只眼中,視盤側支循環建立29只眼(18.1%,29/106),其中缺血型、非缺血型分別為20、9只眼;未觀察到視網膜血管之間的側支循環。MBRVO、BRVO、CRVO患眼側支循環建立率比較,差異有統計學意義(χ2=0.024,P<0.05)。
MBRVO者中建立側支循環的36只眼,其側支循環均建立于阻塞區域和非阻塞區域之間的垂直水平縫處,可見于黃斑中心凹鼻側及顳側(圖3A),也可見于距中心凹稍遠處(圖3B),數量為1~4支;其管徑較CRVO的側支血管小。
 圖3
MBRVO側支循環OCTA像 3A、3B示跨越水平縫建立的側支循環(黃箭),緊鄰中心凹(3A)或中心凹較遠處(3B) MBRVO:黃斑分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖3
MBRVO側支循環OCTA像 3A、3B示跨越水平縫建立的側支循環(黃箭),緊鄰中心凹(3A)或中心凹較遠處(3B) MBRVO:黃斑分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
BRVO者187只眼中,側支循環建立于阻塞區域和非阻塞區域之間的垂直水平縫處(圖4A)102只眼;阻塞最中央逐級搭橋至正常血管上的側支循環(圖4B)54只眼;通過鼻側與顳側建立側支循環(圖4C)19只眼;通過中心凹建立的側支循環(圖4D)12只眼。除常規區域的側支循環外,18只眼同時建立了視盤睫狀血管短路型側支循環(圖4E),均為半側BRVO者。建立的側支循環其形態表現為平直(圖5A)、螺旋狀紆曲(圖5B)和花簇狀(圖5C)。此外,除視網膜淺層毛細血管叢可見豐富的側支循環外(圖6A),側支循環也可建立于深層毛細血管叢之間(圖6B)。
 圖4
BRVO側支循環建立部位OCTA像 4A示垂直于水平縫建立的阻塞與非阻塞區域之間的側支循環(黃箭);4B示阻塞最中央逐級搭橋至正常血管上的側支循環(黃箭);4C示鼻側與顳側間建立的側支循環(黃箭);4D示通過中心凹建立的側支循環(黃箭) ;4E示視盤睫狀血管短路型側支循環(黃箭) BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖4
BRVO側支循環建立部位OCTA像 4A示垂直于水平縫建立的阻塞與非阻塞區域之間的側支循環(黃箭);4B示阻塞最中央逐級搭橋至正常血管上的側支循環(黃箭);4C示鼻側與顳側間建立的側支循環(黃箭);4D示通過中心凹建立的側支循環(黃箭) ;4E示視盤睫狀血管短路型側支循環(黃箭) BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
 圖5
BRVO側支循環血管形態OCTA像 5A~5C分別示平直、螺旋狀紆曲、花簇狀側支循環(黃箭) BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖5
BRVO側支循環血管形態OCTA像 5A~5C分別示平直、螺旋狀紆曲、花簇狀側支循環(黃箭) BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
 圖6
BRVO側支循環分層情況OCTA像 6A示淺層視網膜毛細血管叢可見豐富的側支循環;6B示深層視網膜毛細血管叢之間建立的側支循環 BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖6
BRVO側支循環分層情況OCTA像 6A示淺層視網膜毛細血管叢可見豐富的側支循環;6B示深層視網膜毛細血管叢之間建立的側支循環 BRVO:視網膜分支靜脈阻塞;OCTA:光相干斷層掃描血管成像
CRVO建立側支循環的29只眼,均為視盤睫狀血管短路型側支循環(圖7)。
 圖7
CRVO側支循環OCTA像 視盤睫狀血管短路型側支循環(黃箭) CRVO:視網膜中央靜脈阻塞;OCTA:光相干斷層掃描血管成像
圖7
CRVO側支循環OCTA像 視盤睫狀血管短路型側支循環(黃箭) CRVO:視網膜中央靜脈阻塞;OCTA:光相干斷層掃描血管成像
隨訪6個月,行抗VEGF藥物治療的210只眼中,側支循環建立160只眼(76.19%,160/210)。其中,MBRVO 32只眼(50.7%,32/63);BRVO 119只眼(100.0%,119/119)(圖8);CRVO 9只眼(32.1%,9/28)。
 圖8
BRVO合并黃斑水腫患眼抗VEGF藥物治療后側支循環OCTA像 8A、8B分別示首診時彩色眼底、OCT像,顳上靜脈阻塞、視網膜出血、黃斑水腫;8C、8D分別示抗VEGF藥物治療1個月時OCTA、OCT像,側支循環建立(8C)、黃斑水腫消退(8D) BRVO:視網膜分支靜脈阻塞;VEGF:血管內皮生長因子;OCT:光相干斷層掃描;OCTA:OCT血管成像
圖8
BRVO合并黃斑水腫患眼抗VEGF藥物治療后側支循環OCTA像 8A、8B分別示首診時彩色眼底、OCT像,顳上靜脈阻塞、視網膜出血、黃斑水腫;8C、8D分別示抗VEGF藥物治療1個月時OCTA、OCT像,側支循環建立(8C)、黃斑水腫消退(8D) BRVO:視網膜分支靜脈阻塞;VEGF:血管內皮生長因子;OCT:光相干斷層掃描;OCTA:OCT血管成像
3 討論
廣角OCTA為臨床提供了無創、可重復性好、血管形態不受造影劑滲漏影響的影像手段,與既往傳統檢查比較,對RVO側支循環有了更多角度的觀察結果[6]。
對于不同類型RVO建立側支循環的概率,OCTA相對于FFA可進行更精準的觀察。在所有類型的RVO中BRVO的側支循環建立最為豐富。Suzuki等[7]對18例BRVO患者(28只眼)進行OCTA觀察,所有患者均觀察到側支循環建立。既往認為MBRVO阻塞程度較輕,代償機制不旺盛,而這部分血管較小,分辨率較差,所以認為MBRVO較少形成側支循環。隨著OCTA技術的發展,更多側支循環在MBRVO中被發現。Suzuki等[7]對18例BRVO患者(28只眼)行OCTA檢查,隨訪6個月時,MBRVO 10只眼中5只眼發現側支循環。本組患眼觀察結果也相似,53.7%的MBRVO患眼觀察到側支循環的建立。而對于CRVO,由于阻塞旁路空間最少,側支循環建立也最困難,本組CRVO 106只眼中,僅18.1%的患眼觀察到側支循環的建立。
不同類型側支循環建立部位和特點也存在差異。BRVO由于阻塞的是大支分支靜脈,周邊血管代償能力強,旁路空間多,所以側支循環最為豐富。Weinberg等[8]使用OCTA對一組BRVO患眼進行檢查,初診后12 個月,其側支循環主要在水平縫區域,連接阻塞區域和非阻塞區域。本組患眼除典型通過水平縫阻塞區域與非阻塞區域之間側支循環建立,還觀察到鼻側與顳側之間也可建立側支循環,阻塞中心區域通過逐級搭橋的形式與正常靜脈建立側支循環。而MBRVO常見的側支循環主要形式是通過黃斑區末梢血管之間的水平縫建立。而對于阻塞面積較大的CRVO和半側BRVO,視盤短路是觀察到最典型而獨特的側支循環方式。對其病理機制,Fuller等[9]認為CRVO阻塞部位一般位于或靠近篩板,導致視網膜中央靜脈的所有分支回流受到影響,導致視網膜循環內沒有壓力梯度驅動視網膜內側支循環的形成,但在視神經邊緣存在從視網膜到脈絡膜循環的視盤睫狀短路引流。因此,呈環狀的繼發性視盤血管袢是CRVO側支循環的主要形式。既往對于側支循環的部位觀察主要依靠眼底彩色照相和FFA,但均存在不能分層的局限性,因此對于側支循環的觀察一直停留在淺層視網膜血管,隨著OCTA的應用,發現側支循環也可發生在深層血管網中[10]。Freund等[11]觀察23例BRVO患者的110支側支血管,發現側支循環主要位于深層毛細血管叢,且未觀察到僅存在于淺層毛細血管叢的側支循環。
對于側支循環建立的時間,目前文獻報道的數據存在較大差異。Christoffersen和Larsen[12]對250例BRVO患者的臨床資料進行回顧性分析,發現側支循環的建立發生在BRVO發病后6~24個月。但也有學者認為側支循環作為RVO的一種代償機制,啟動應該更早。Takahashi等[13]應用激光誘導建立小鼠RVO模型,通過OCTA檢查觀察發現,建模后3 d,閉塞血管周圍的血管粗大,出現側支循環;5~7 d,側支循環更加清晰可見;14 d時,在遠離閉塞血管的區域均觀察到側支循環的建立。根據動物實驗,有證據懷疑側支循環出現的時間可能早于6~24個月。本組患眼阻塞發生后10 d即觀察到側支血管向阻塞區域延伸,多數患眼1個月左右可觀察到不同程度的側支循環。因此,我們認為側支循環建立的時間應比傳統認知更早發生。
對于抗VEGF藥物治療是否影響側支循環的建立,一直為臨床關注。抗VEGF藥物治療目前已成為治療RVO合并黃斑水腫的一線治療方案[14]。理論上,降低眼內VEGF水平的同時也抑制側支循環的建立,阻斷機體自身啟動的代償機制也存在可能性[15]。本研究雖然因治療方案未能設置對照組進行前瞻性對比觀察,但各種類型的RVO抗VEGF藥物治療后側支循環建立的比率未受到大幅度影響,我們認為抗VEGF藥物治療并不抑制側支循環的建立。該結論與目前文獻結論相似。Montero-Moreno和Ruiz-Moreno[16]觀察了一組經歷2年抗VEGF藥物治療的BRVO及CRVO患者,其中BRVO組21只眼中17只眼建立側支循環,CRVO組7只眼出現視盤分流。其機制我們認為是,新生血管的建立依賴VEGF水平的增高,但側支循環更多為正常血管的延伸,而非新生血管,故其并不依賴VEGF,因此抗VEGF藥物治療并不影響側支循環的建立。
本研究存在的局限性:(1)一次性掃描面積有限,不能進行大面積掃描成像;(2)OCTA無需注射造影劑,在觀察血管滲漏方面存在缺陷,對于新生血管與側支血管在特定時間存在鑒別難點;(3)觀察深層視網膜毛細血管叢時,可以看到來自淺層血管網的影像和投射軌跡,造成偽影。隨著OCTA技術和算法的不斷發展,在包括側支循環等多個領域將會出現更多研究成果。