引用本文: 朱海燕, 劉培, 安廣琪, 路晨雨, 李姝, 杜利平, 金學民. 中心性漿液性脈絡膜視網膜病變患者厚玻璃膜疣的臨床特征和危險因素. 中華眼底病雜志, 2024, 40(12): 930-935. doi: 10.3760/cma.j.cn511434-20240704-00250 復制
版權信息: ?四川大學華西醫院華西期刊社《中華眼底病雜志》版權所有,未經授權不得轉載、改編
中心性漿液性脈絡膜視網膜病變(CSC)被歸類于厚脈絡膜疾病譜。其特征是脈絡膜局灶性或彌漫性增厚和脈絡膜通透性增加[1-3]。玻璃膜疣是介于視網膜色素上皮(RPE)和Bruch膜之間的黃白色沉積物,由補體蛋白、酯化和非酯化膽固醇、載脂蛋白、碳水化合物和微量元素組成[4-5]。有研究發現,在厚脈絡膜疾病中存在特征性玻璃膜疣[6]。Spaide[7]首次將該玻璃膜疣命名為厚玻璃膜疣,并描述其為邊界清晰、形態不規則、直徑超過125 μm,呈獨立或散在分布的單團或簇狀玻璃膜疣。文獻報道的發生率差異較大,為6.82%~60.0%[8-9]。Kim等[10]比較了CSC和息肉樣脈絡膜血管病變(PCV)厚玻璃膜疣的特點,發現PCV的厚玻璃膜疣與脈絡膜厚度密切相關,而CSC的厚玻璃膜疣與年齡密切相關。Baek等[11]發現,厚玻璃膜疣下脈絡膜Haller層厚度增加,脈絡膜毛細血管層血流衰減。Matsumoto等[12]觀察到CSC患眼厚玻璃膜疣常與脈絡膜毛細血管層充盈延遲區和擴張的大脈絡膜血管共定位。厚玻璃膜疣在疾病進展中的作用及其對疾病的影響仍有爭議。本研究初步探討了厚玻璃膜疣的特征并分析其對疾病的影響。現將結果報道如下。
1 對象和方法
回顧性臨床研究。本研究經鄭州大學第一附屬醫院倫理委員會審核(批準號:2022-KY-0547-002);遵循《赫爾辛基宣言》原則;所有患者均知情并簽署書面知情同意書。
2021年7月至2024年6月于鄭州大學第一附屬醫院眼科檢查確診且未接受治療的CSC患者144例158只眼納入本研究。其中,男性98例(68.06%,98/144),女性46例(31.94%,46/144);年齡20~71(45.53±9.33)歲。納入標準:(1)主述單眼或雙眼視力下降、視物模糊、視物變形、變小或有中心暗點;(2)眼底彩色照相顯示黃斑區顏色變暗,中心凹可見橢圓形光暈;(3)掃頻源光相干斷層掃描(SS-OCT)檢查顯示黃斑區漿液性神經視網膜脫離,伴或不伴漿液性RPE脫離(PED);(4)熒光素眼底血管造影(FFA)檢查顯示漿液性視網膜脫離區域內有特征性熒光素滲漏。排除標準:(1)存在其他可導致視網膜下積液的視網膜或脈絡膜疾病;(2)既往有激光光凝治療史或其他眼部手術史;(3)圖像質量差,影響準確分析;(4)高度近視,等效球鏡度(SE)>-6 D。CSC病程≤3個月、>3個月分別定義為急性CSC(aCSC)、慢性CSC(cCSC)[13]。
患眼均行最佳矯正視力(BCVA)、裂隙燈顯微鏡聯合前置鏡、驗光、眼底彩色照相、FFA、SS-OCT、SS-OCT血管成像(SS-OCTA)檢查。行吲哚青綠血管造影(ICGA)檢查58只眼。采用英國Optos公司Daytona P200T激光掃描檢眼鏡行眼底彩色照相檢查;采用德國Heidelberg公司Spectralis HRA+OCT儀行FFA、ICGA檢查。FFA熒光素滲漏分為“墨漬樣”、“炊煙樣”、彌漫性點狀滲漏,同時記錄滲漏點數量。采用國際標準視力表行BCVA檢查,統計時換算為最小分辨角對數(logMAR)視力。屈光度數以SE表示,SE=球鏡+1/2柱鏡。
采用賽煒(河南)科技有限公司VG200D行黃斑區SS-OCTA檢查。波長1 050 nm,掃頻速率200 000 A掃描/s,軸向分辨率為1.8 μm,掃描深度6 mm,掃描模式Angio 512×512 R4和Star 18Line R16。采用系統默認結構分層。脈絡膜定義為RPE-Bruch膜復合物基底邊界至脈絡膜鞏膜交界處。應用系統內人工智能識別與量化分析軟件計算中心凹下脈絡膜厚度(SFCT)。厚玻璃膜疣定義為位于RPE下孤立或分散的黃白色沉積物,具有卵圓形或其他復雜形狀且未覆蓋的色素[14]。將其位置分為距中心凹<3 mm、3~6 mm、>6 mm。扁平不規則PED(FIPED)定義為RPE至Bruch膜不規則的PED。SFCT定義黃斑中心1 mm范圍內RPE層外界至鞏膜內界之間的垂直距離。所有患眼圖像采集和分析由2名眼底病醫師分別獨立完成,判斷厚玻璃膜疣位置;ICGA像,厚玻璃膜疣與強熒光點和脈絡膜血管高通透性區域的共定位;橫斷面(en-face)OCT像、OCTA像,厚玻璃膜疣與脈絡膜血管擴張、脈絡膜毛細血管層衰減區的共定位。FFA像,熒光素滲漏形式和強熒光點數。若結果存在差異,則由第3名資深眼底病專家對其進行判斷,最終得出準確結果。
患眼SE-3.75~14.00(0.45±1.54)D;logMAR BCVA 0~1.70(0.359±0.323);SFCT 249.00~1 002.00(533.51±139.98)μm。脈絡膜新生血管(CNV)、FIPED分別為16、68只眼。aCSC、cCSC分別為77(48.73%,77/158)、81(51.27%,81/158)只眼。根據是否合并厚玻璃膜疣將患者分為CSC合并厚玻璃膜疣組(A組)、CSC未合并厚玻璃膜疣組(B組)。
采用SPSS25.0軟件進行統計分析。計量資料以均數±標準差(x±s)表示。兩組間定量資料比較行獨立樣本t檢驗或Mann-Whitney U檢驗;定性資料比較行χ2檢驗。與厚玻璃膜疣存在的相關因素分析采用logistic回歸分析。檢驗水準α=0.05,雙側檢驗。P<0.05為差異有統計學意義。
2 結果
158只眼中,合并厚玻璃膜疣72只眼(45.6%,72/158),其中cCSC、aCSC分別為51(62.96%,51/81)、21(27.27%,21/77)只眼;未合并厚玻璃膜疣86只眼(54.4%,86/158)。位于距中心凹<3 mm、3~6 mm、>6 mm處分別為35(68.61%,35/72)、27(37.50%,27/72)、10(13.89%,10/72)只眼。眼底彩色照相檢查, 可見黃白色厚玻璃膜疣(圖1A)。SS-OCT檢查,B掃描像,厚玻璃膜疣孤立存在(圖1B);en-face OCT檢查,厚玻璃膜疣與擴張的脈絡膜外層血管共定位(圖1C)59只眼(81.94%,59/72);OCTA像,與脈絡膜毛細血管層血流衰減區共定位(圖1D)61只眼(84.72%,61/72)。FFA檢查,熒光素“墨漬樣”、“炊煙樣”、彌漫性點狀滲漏分別為77、44、37只眼(圖1E)。行ICGA檢查的58只眼中,厚玻璃膜疣與點狀強熒光相對應(圖1F)46只眼(79.31%,46/58);位于脈絡膜高通透性區域43只眼(74.14%,43/58)。
 圖1
中心性漿液性脈絡膜視網膜病變合并厚玻璃膜疣患眼多模式影像 1A示彩色眼底像,黃白色厚玻璃膜疣(白箭)。1B示掃頻源OCT像,左圖示掃描方向和部位,右圖為B掃描像。可見厚玻璃膜疣孤立存在。1C示橫斷面OCT像,厚玻璃膜疣相對應于擴張的脈絡膜血管(白箭)。1D示OCT血管成像,厚玻璃膜疣與脈絡膜毛細血管血流衰減區相對應(白箭)。1E示熒光素眼底血管造影像,多發性熒光素滲漏(白箭)。1F示吲哚青綠血管造影像,厚玻璃膜疣存在于脈絡膜血管高通透性區域,且與點狀強熒光斑點相對應(白箭) OCT:光相干斷層掃描
圖1
中心性漿液性脈絡膜視網膜病變合并厚玻璃膜疣患眼多模式影像 1A示彩色眼底像,黃白色厚玻璃膜疣(白箭)。1B示掃頻源OCT像,左圖示掃描方向和部位,右圖為B掃描像。可見厚玻璃膜疣孤立存在。1C示橫斷面OCT像,厚玻璃膜疣相對應于擴張的脈絡膜血管(白箭)。1D示OCT血管成像,厚玻璃膜疣與脈絡膜毛細血管血流衰減區相對應(白箭)。1E示熒光素眼底血管造影像,多發性熒光素滲漏(白箭)。1F示吲哚青綠血管造影像,厚玻璃膜疣存在于脈絡膜血管高通透性區域,且與點狀強熒光斑點相對應(白箭) OCT:光相干斷層掃描
A組、B組患者性別構成比、SE、SFCT以及FFA熒光素“墨漬樣”、“炊煙樣”滲漏眼數比較,差異均無統計學意義(P>0.05);年齡、logMAR BCVA、cCSC、CNV、FIPED、FFA熒光素彌漫性點狀滲漏、滲漏點(>3個)比較,差異均有統計學意義(P<0.05)(表1)。
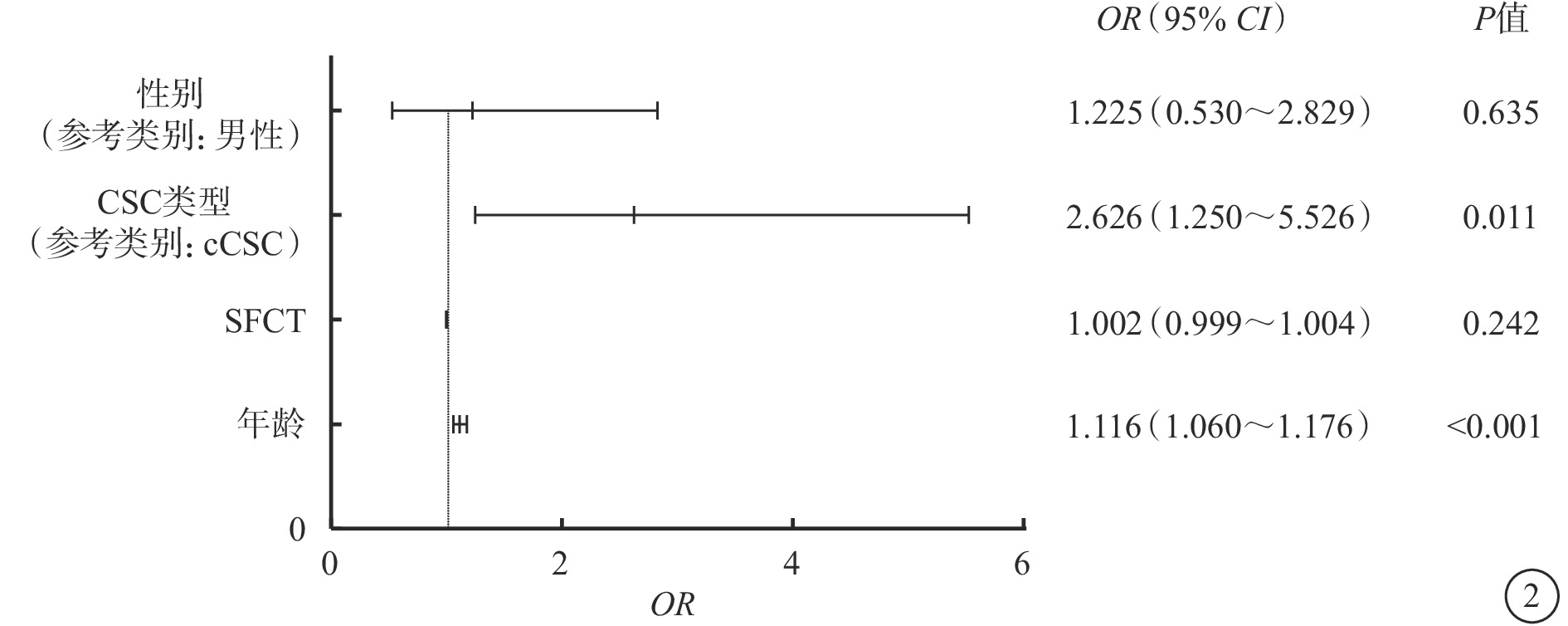
logistic回歸分析結果顯示,年齡[比值比(OR)=1.116,95%可信區間(CI)1.060~1.176,P<0.001]、cCSC(OR=2.628,95%CI 1.250~5.526,P=0.011)是厚玻璃膜疣發生的獨立危險因素;SFCT與厚玻璃膜疣發生無相關性(OR=1.002,95%CI 0.999~1.004,P=0.242)(圖2)。
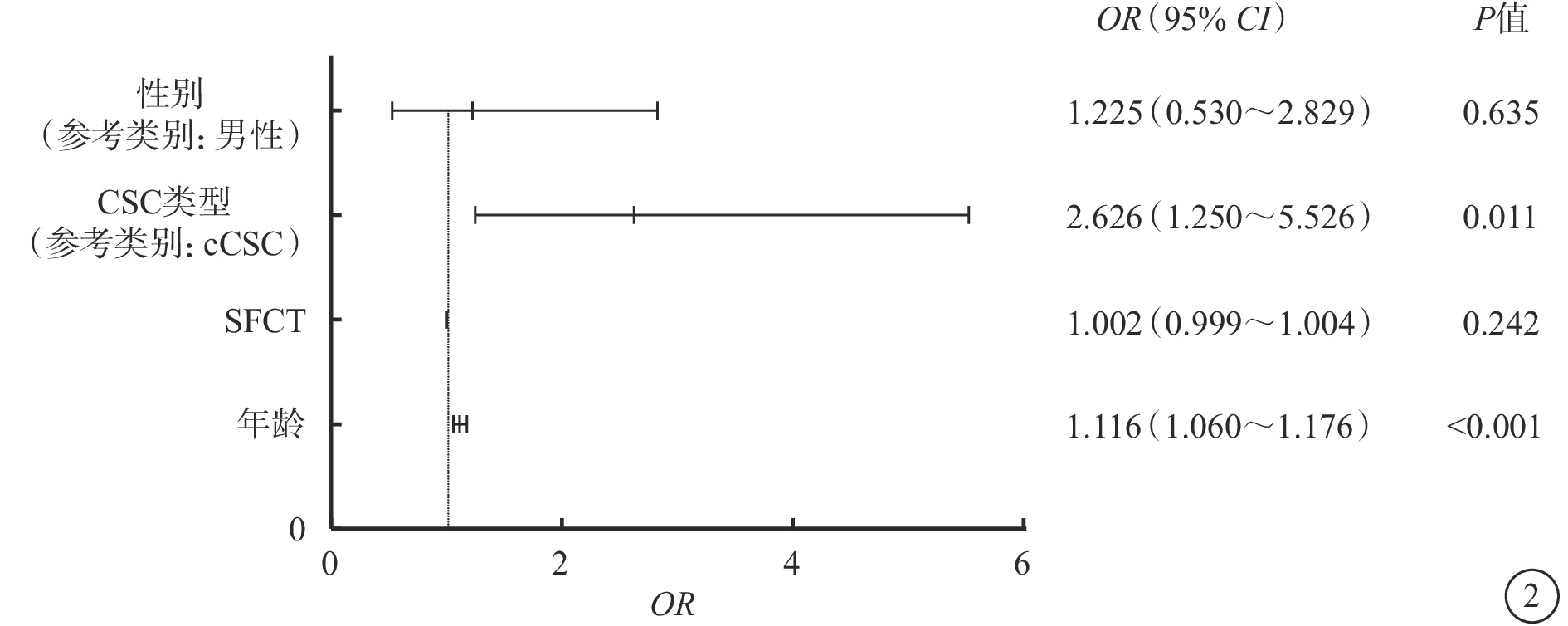 圖2
logistic回歸分析結果 CSC:中心性漿液性脈絡膜視網膜病變;cCSC:慢性CSC;SFCT:中心凹下脈絡膜厚度;OR:比值比;CI:可信區間
圖2
logistic回歸分析結果 CSC:中心性漿液性脈絡膜視網膜病變;cCSC:慢性CSC;SFCT:中心凹下脈絡膜厚度;OR:比值比;CI:可信區間
3 討論
厚玻璃膜疣需要與軟玻璃膜疣以及視網膜下的玻璃膜疣樣沉積物區分開來。軟玻璃膜疣在RPE下方表現為均勻的黃白色沉積物,形狀通常是圓形或卵圓形,邊界模糊,有時會密集堆積甚至相互融合,并可能伴有色素沉著。另一方面,視網膜下的玻璃膜疣樣沉積物則分布在黃斑中心凹及其周圍區域,呈現為位于RPE與橢圓體帶之間的黃白色點狀病灶。當這些沉積物體積增加時,它們有可能穿透外界膜并向外核層延伸[4, 14]。
本組患者厚玻璃膜疣發生率為45.50%(72/158),較既往文獻報道的發生率高[9, 15]。其原因除種族差異外,cCSC患者占比較高(51.27%,51/81)可能也是一個重要因素。此外,我們還觀察到cCSC者合并厚玻璃膜疣較aCSC者更高(62.96% vs. 27.27%)。Cheung等[16]認為,SFCT與不同玻璃膜疣亞型獨立相關,較厚的脈絡膜與厚玻璃膜疣有關,較薄的脈絡膜與假性玻璃膜疣有關。然而,Kim等[10]發現,厚玻璃膜疣發生與CSC患者年齡密切相關,而與SFCT無關。本研究結果支持上述結論。此外,相關性分析發現,cCSC與厚玻璃膜疣的發生呈顯著相關。Baek等[11]觀察了厚玻璃膜疣下脈絡膜特征,發現厚玻璃膜疣下Haller層厚度增加,而脈絡膜毛細血管層厚度減低。同樣,Matsumoto等[12]發現,CSC患者的厚玻璃膜疣通常位于脈絡膜毛細血管充盈延遲區域,與擴張的脈絡膜血管位置對應。我們推測,脈絡膜外層血管擴張引起的脈絡膜內循環中斷影響RPE功能,導致細胞外物質沉積增加,促進厚玻璃膜疣形成。cCSC患者病程較長,上述因素影響持續時間較長,從而增加了厚玻璃膜疣形成的可能性。
CSC合并厚玻璃膜疣患者FIPED和CNV的發生率明顯增高。FIPED與CNV密切相關。一項回顧性研究發現,伴有CNV的CSC患者均存在FIPED[17]。Su等[18]利用多模式成像技術觀察CSC患者FIPED與CNV的關系。結果顯示,FIPED與1型CNV密切相關,在長期隨訪期間可能導致更差的視力結果。此外,作者還提出RPE功能損傷可能在患者血管化FIPED的發展中起重要作用。本研究結果顯示,CSC合并厚玻璃膜疣患者FFA熒光素彌漫性點狀滲漏和多灶性滲漏的發生率明顯更高,表明RPE損害更為嚴重和廣泛。Lai等[15]發現,合并厚玻璃膜疣患者,其眼底自發熒光表現出更為廣泛的異常。因此,我們認為,厚玻璃膜疣可能是RPE功能嚴重受損的一個指標。
目前缺乏流行病學證據直接將厚玻璃膜疣與疾病進展聯系起來。然而,Kang等[19]采用ICGA對一組CSC患者進行檢查,發現厚玻璃膜疣與脈絡膜高通透性和點狀強熒光區相對應。本研究結果顯示,厚玻璃膜疣與擴張的脈絡膜血管和脈絡膜毛細血流空洞共存。這些特征已被證實與RPE層滲漏點相對應[13, 20-21]。這提示在厚玻璃膜疣的部位,RPE嚴重受累。此外,RPE和外視網膜的血液供應依賴于脈絡膜毛細血管。RPE下方玻璃膜疣的積累增加了RPE與脈絡膜毛細血管層之間的距離,可能影響RPE與光感受器的血液灌注,這可能導致其結構和功能損傷,以及血管內皮生長因子分泌增加[22]。因此,厚玻璃膜疣可能是CSC活動或發展的潛在風險因素,包括新滲漏部位或CNV形成。此外,本組患眼黃斑和黃斑旁區的脈絡膜血管和RPE異常與厚玻璃膜疣相關的比例高于周圍區域。然而,這些發現的長期進展仍需要進一步觀察。
本研究存在的局限性:(1)納入對象均為中國漢族患者,可能限制了研究結果在其他國家或民族的推廣。(2)由于未能獲取患者的眼底自發熒光圖像以直接評估RPE的異常情況,因此我們采用了FFA中的熒光素滲漏模式及滲漏點來進行間接評估,但這并不能完全替代直接觀察RPE代謝活性的能力。(3)接受ICGA檢查的患者占比較小,需要更多ICGA的影像學資料進一步驗證本研究結果。(4)因回顧性研究的局限性,只能根據影像學特征推測厚玻璃膜疣的長期發展,確定厚玻璃膜疣是否在疾病進展中起直接作用或僅僅是厚脈絡膜的附帶現象需要長期觀察。(5)由于位于周邊的厚玻璃膜疣較少,不同部位的厚玻璃膜疣亞群分析結果可能容易出現誤差,這需要進一步擴大樣本量加以驗證。
中心性漿液性脈絡膜視網膜病變(CSC)被歸類于厚脈絡膜疾病譜。其特征是脈絡膜局灶性或彌漫性增厚和脈絡膜通透性增加[1-3]。玻璃膜疣是介于視網膜色素上皮(RPE)和Bruch膜之間的黃白色沉積物,由補體蛋白、酯化和非酯化膽固醇、載脂蛋白、碳水化合物和微量元素組成[4-5]。有研究發現,在厚脈絡膜疾病中存在特征性玻璃膜疣[6]。Spaide[7]首次將該玻璃膜疣命名為厚玻璃膜疣,并描述其為邊界清晰、形態不規則、直徑超過125 μm,呈獨立或散在分布的單團或簇狀玻璃膜疣。文獻報道的發生率差異較大,為6.82%~60.0%[8-9]。Kim等[10]比較了CSC和息肉樣脈絡膜血管病變(PCV)厚玻璃膜疣的特點,發現PCV的厚玻璃膜疣與脈絡膜厚度密切相關,而CSC的厚玻璃膜疣與年齡密切相關。Baek等[11]發現,厚玻璃膜疣下脈絡膜Haller層厚度增加,脈絡膜毛細血管層血流衰減。Matsumoto等[12]觀察到CSC患眼厚玻璃膜疣常與脈絡膜毛細血管層充盈延遲區和擴張的大脈絡膜血管共定位。厚玻璃膜疣在疾病進展中的作用及其對疾病的影響仍有爭議。本研究初步探討了厚玻璃膜疣的特征并分析其對疾病的影響。現將結果報道如下。
1 對象和方法
回顧性臨床研究。本研究經鄭州大學第一附屬醫院倫理委員會審核(批準號:2022-KY-0547-002);遵循《赫爾辛基宣言》原則;所有患者均知情并簽署書面知情同意書。
2021年7月至2024年6月于鄭州大學第一附屬醫院眼科檢查確診且未接受治療的CSC患者144例158只眼納入本研究。其中,男性98例(68.06%,98/144),女性46例(31.94%,46/144);年齡20~71(45.53±9.33)歲。納入標準:(1)主述單眼或雙眼視力下降、視物模糊、視物變形、變小或有中心暗點;(2)眼底彩色照相顯示黃斑區顏色變暗,中心凹可見橢圓形光暈;(3)掃頻源光相干斷層掃描(SS-OCT)檢查顯示黃斑區漿液性神經視網膜脫離,伴或不伴漿液性RPE脫離(PED);(4)熒光素眼底血管造影(FFA)檢查顯示漿液性視網膜脫離區域內有特征性熒光素滲漏。排除標準:(1)存在其他可導致視網膜下積液的視網膜或脈絡膜疾病;(2)既往有激光光凝治療史或其他眼部手術史;(3)圖像質量差,影響準確分析;(4)高度近視,等效球鏡度(SE)>-6 D。CSC病程≤3個月、>3個月分別定義為急性CSC(aCSC)、慢性CSC(cCSC)[13]。
患眼均行最佳矯正視力(BCVA)、裂隙燈顯微鏡聯合前置鏡、驗光、眼底彩色照相、FFA、SS-OCT、SS-OCT血管成像(SS-OCTA)檢查。行吲哚青綠血管造影(ICGA)檢查58只眼。采用英國Optos公司Daytona P200T激光掃描檢眼鏡行眼底彩色照相檢查;采用德國Heidelberg公司Spectralis HRA+OCT儀行FFA、ICGA檢查。FFA熒光素滲漏分為“墨漬樣”、“炊煙樣”、彌漫性點狀滲漏,同時記錄滲漏點數量。采用國際標準視力表行BCVA檢查,統計時換算為最小分辨角對數(logMAR)視力。屈光度數以SE表示,SE=球鏡+1/2柱鏡。
采用賽煒(河南)科技有限公司VG200D行黃斑區SS-OCTA檢查。波長1 050 nm,掃頻速率200 000 A掃描/s,軸向分辨率為1.8 μm,掃描深度6 mm,掃描模式Angio 512×512 R4和Star 18Line R16。采用系統默認結構分層。脈絡膜定義為RPE-Bruch膜復合物基底邊界至脈絡膜鞏膜交界處。應用系統內人工智能識別與量化分析軟件計算中心凹下脈絡膜厚度(SFCT)。厚玻璃膜疣定義為位于RPE下孤立或分散的黃白色沉積物,具有卵圓形或其他復雜形狀且未覆蓋的色素[14]。將其位置分為距中心凹<3 mm、3~6 mm、>6 mm。扁平不規則PED(FIPED)定義為RPE至Bruch膜不規則的PED。SFCT定義黃斑中心1 mm范圍內RPE層外界至鞏膜內界之間的垂直距離。所有患眼圖像采集和分析由2名眼底病醫師分別獨立完成,判斷厚玻璃膜疣位置;ICGA像,厚玻璃膜疣與強熒光點和脈絡膜血管高通透性區域的共定位;橫斷面(en-face)OCT像、OCTA像,厚玻璃膜疣與脈絡膜血管擴張、脈絡膜毛細血管層衰減區的共定位。FFA像,熒光素滲漏形式和強熒光點數。若結果存在差異,則由第3名資深眼底病專家對其進行判斷,最終得出準確結果。
患眼SE-3.75~14.00(0.45±1.54)D;logMAR BCVA 0~1.70(0.359±0.323);SFCT 249.00~1 002.00(533.51±139.98)μm。脈絡膜新生血管(CNV)、FIPED分別為16、68只眼。aCSC、cCSC分別為77(48.73%,77/158)、81(51.27%,81/158)只眼。根據是否合并厚玻璃膜疣將患者分為CSC合并厚玻璃膜疣組(A組)、CSC未合并厚玻璃膜疣組(B組)。
采用SPSS25.0軟件進行統計分析。計量資料以均數±標準差(x±s)表示。兩組間定量資料比較行獨立樣本t檢驗或Mann-Whitney U檢驗;定性資料比較行χ2檢驗。與厚玻璃膜疣存在的相關因素分析采用logistic回歸分析。檢驗水準α=0.05,雙側檢驗。P<0.05為差異有統計學意義。
2 結果
158只眼中,合并厚玻璃膜疣72只眼(45.6%,72/158),其中cCSC、aCSC分別為51(62.96%,51/81)、21(27.27%,21/77)只眼;未合并厚玻璃膜疣86只眼(54.4%,86/158)。位于距中心凹<3 mm、3~6 mm、>6 mm處分別為35(68.61%,35/72)、27(37.50%,27/72)、10(13.89%,10/72)只眼。眼底彩色照相檢查, 可見黃白色厚玻璃膜疣(圖1A)。SS-OCT檢查,B掃描像,厚玻璃膜疣孤立存在(圖1B);en-face OCT檢查,厚玻璃膜疣與擴張的脈絡膜外層血管共定位(圖1C)59只眼(81.94%,59/72);OCTA像,與脈絡膜毛細血管層血流衰減區共定位(圖1D)61只眼(84.72%,61/72)。FFA檢查,熒光素“墨漬樣”、“炊煙樣”、彌漫性點狀滲漏分別為77、44、37只眼(圖1E)。行ICGA檢查的58只眼中,厚玻璃膜疣與點狀強熒光相對應(圖1F)46只眼(79.31%,46/58);位于脈絡膜高通透性區域43只眼(74.14%,43/58)。
 圖1
中心性漿液性脈絡膜視網膜病變合并厚玻璃膜疣患眼多模式影像 1A示彩色眼底像,黃白色厚玻璃膜疣(白箭)。1B示掃頻源OCT像,左圖示掃描方向和部位,右圖為B掃描像。可見厚玻璃膜疣孤立存在。1C示橫斷面OCT像,厚玻璃膜疣相對應于擴張的脈絡膜血管(白箭)。1D示OCT血管成像,厚玻璃膜疣與脈絡膜毛細血管血流衰減區相對應(白箭)。1E示熒光素眼底血管造影像,多發性熒光素滲漏(白箭)。1F示吲哚青綠血管造影像,厚玻璃膜疣存在于脈絡膜血管高通透性區域,且與點狀強熒光斑點相對應(白箭) OCT:光相干斷層掃描
圖1
中心性漿液性脈絡膜視網膜病變合并厚玻璃膜疣患眼多模式影像 1A示彩色眼底像,黃白色厚玻璃膜疣(白箭)。1B示掃頻源OCT像,左圖示掃描方向和部位,右圖為B掃描像。可見厚玻璃膜疣孤立存在。1C示橫斷面OCT像,厚玻璃膜疣相對應于擴張的脈絡膜血管(白箭)。1D示OCT血管成像,厚玻璃膜疣與脈絡膜毛細血管血流衰減區相對應(白箭)。1E示熒光素眼底血管造影像,多發性熒光素滲漏(白箭)。1F示吲哚青綠血管造影像,厚玻璃膜疣存在于脈絡膜血管高通透性區域,且與點狀強熒光斑點相對應(白箭) OCT:光相干斷層掃描
A組、B組患者性別構成比、SE、SFCT以及FFA熒光素“墨漬樣”、“炊煙樣”滲漏眼數比較,差異均無統計學意義(P>0.05);年齡、logMAR BCVA、cCSC、CNV、FIPED、FFA熒光素彌漫性點狀滲漏、滲漏點(>3個)比較,差異均有統計學意義(P<0.05)(表1)。
logistic回歸分析結果顯示,年齡[比值比(OR)=1.116,95%可信區間(CI)1.060~1.176,P<0.001]、cCSC(OR=2.628,95%CI 1.250~5.526,P=0.011)是厚玻璃膜疣發生的獨立危險因素;SFCT與厚玻璃膜疣發生無相關性(OR=1.002,95%CI 0.999~1.004,P=0.242)(圖2)。
 圖2
logistic回歸分析結果 CSC:中心性漿液性脈絡膜視網膜病變;cCSC:慢性CSC;SFCT:中心凹下脈絡膜厚度;OR:比值比;CI:可信區間
圖2
logistic回歸分析結果 CSC:中心性漿液性脈絡膜視網膜病變;cCSC:慢性CSC;SFCT:中心凹下脈絡膜厚度;OR:比值比;CI:可信區間
3 討論
厚玻璃膜疣需要與軟玻璃膜疣以及視網膜下的玻璃膜疣樣沉積物區分開來。軟玻璃膜疣在RPE下方表現為均勻的黃白色沉積物,形狀通常是圓形或卵圓形,邊界模糊,有時會密集堆積甚至相互融合,并可能伴有色素沉著。另一方面,視網膜下的玻璃膜疣樣沉積物則分布在黃斑中心凹及其周圍區域,呈現為位于RPE與橢圓體帶之間的黃白色點狀病灶。當這些沉積物體積增加時,它們有可能穿透外界膜并向外核層延伸[4, 14]。
本組患者厚玻璃膜疣發生率為45.50%(72/158),較既往文獻報道的發生率高[9, 15]。其原因除種族差異外,cCSC患者占比較高(51.27%,51/81)可能也是一個重要因素。此外,我們還觀察到cCSC者合并厚玻璃膜疣較aCSC者更高(62.96% vs. 27.27%)。Cheung等[16]認為,SFCT與不同玻璃膜疣亞型獨立相關,較厚的脈絡膜與厚玻璃膜疣有關,較薄的脈絡膜與假性玻璃膜疣有關。然而,Kim等[10]發現,厚玻璃膜疣發生與CSC患者年齡密切相關,而與SFCT無關。本研究結果支持上述結論。此外,相關性分析發現,cCSC與厚玻璃膜疣的發生呈顯著相關。Baek等[11]觀察了厚玻璃膜疣下脈絡膜特征,發現厚玻璃膜疣下Haller層厚度增加,而脈絡膜毛細血管層厚度減低。同樣,Matsumoto等[12]發現,CSC患者的厚玻璃膜疣通常位于脈絡膜毛細血管充盈延遲區域,與擴張的脈絡膜血管位置對應。我們推測,脈絡膜外層血管擴張引起的脈絡膜內循環中斷影響RPE功能,導致細胞外物質沉積增加,促進厚玻璃膜疣形成。cCSC患者病程較長,上述因素影響持續時間較長,從而增加了厚玻璃膜疣形成的可能性。
CSC合并厚玻璃膜疣患者FIPED和CNV的發生率明顯增高。FIPED與CNV密切相關。一項回顧性研究發現,伴有CNV的CSC患者均存在FIPED[17]。Su等[18]利用多模式成像技術觀察CSC患者FIPED與CNV的關系。結果顯示,FIPED與1型CNV密切相關,在長期隨訪期間可能導致更差的視力結果。此外,作者還提出RPE功能損傷可能在患者血管化FIPED的發展中起重要作用。本研究結果顯示,CSC合并厚玻璃膜疣患者FFA熒光素彌漫性點狀滲漏和多灶性滲漏的發生率明顯更高,表明RPE損害更為嚴重和廣泛。Lai等[15]發現,合并厚玻璃膜疣患者,其眼底自發熒光表現出更為廣泛的異常。因此,我們認為,厚玻璃膜疣可能是RPE功能嚴重受損的一個指標。
目前缺乏流行病學證據直接將厚玻璃膜疣與疾病進展聯系起來。然而,Kang等[19]采用ICGA對一組CSC患者進行檢查,發現厚玻璃膜疣與脈絡膜高通透性和點狀強熒光區相對應。本研究結果顯示,厚玻璃膜疣與擴張的脈絡膜血管和脈絡膜毛細血流空洞共存。這些特征已被證實與RPE層滲漏點相對應[13, 20-21]。這提示在厚玻璃膜疣的部位,RPE嚴重受累。此外,RPE和外視網膜的血液供應依賴于脈絡膜毛細血管。RPE下方玻璃膜疣的積累增加了RPE與脈絡膜毛細血管層之間的距離,可能影響RPE與光感受器的血液灌注,這可能導致其結構和功能損傷,以及血管內皮生長因子分泌增加[22]。因此,厚玻璃膜疣可能是CSC活動或發展的潛在風險因素,包括新滲漏部位或CNV形成。此外,本組患眼黃斑和黃斑旁區的脈絡膜血管和RPE異常與厚玻璃膜疣相關的比例高于周圍區域。然而,這些發現的長期進展仍需要進一步觀察。
本研究存在的局限性:(1)納入對象均為中國漢族患者,可能限制了研究結果在其他國家或民族的推廣。(2)由于未能獲取患者的眼底自發熒光圖像以直接評估RPE的異常情況,因此我們采用了FFA中的熒光素滲漏模式及滲漏點來進行間接評估,但這并不能完全替代直接觀察RPE代謝活性的能力。(3)接受ICGA檢查的患者占比較小,需要更多ICGA的影像學資料進一步驗證本研究結果。(4)因回顧性研究的局限性,只能根據影像學特征推測厚玻璃膜疣的長期發展,確定厚玻璃膜疣是否在疾病進展中起直接作用或僅僅是厚脈絡膜的附帶現象需要長期觀察。(5)由于位于周邊的厚玻璃膜疣較少,不同部位的厚玻璃膜疣亞群分析結果可能容易出現誤差,這需要進一步擴大樣本量加以驗證。