腫瘤電場治療是一種新的治療惡性實體腫瘤的療法,多采用電場仿真分析不同參數的腫瘤電場治療在瘤體上產生的電場分布。但目前,由于仿真模型構建技術路線較難復現或實現成本較高,因此本研究采用常用的軟件工具建立了易實現的高精度腫瘤電場治療有限元仿真模型,模型精度在1 mm3水平。本研究利用該仿真模型開展了不同組織電學參數、電極配置等因素分析,研究結果顯示,對腫瘤內電場分布存在影響的因素包括:頭皮、頭骨電導率的變化(瘤體治療場最高變化21.0%)、腫瘤電導率的變化(瘤體治療場最高變化157.8%)和不同的電極位置及組合(瘤體治療場最高變化74.2%)。綜上,本文研究結果驗證了所提建模方法的可行性與有效性,或可為今后的腫瘤電場治療仿真分析和臨床應用提供重要參考。
引用本文: 秦麗平, 謝旭, 王敏敏, 馬明偉, 潘赟, 陳光弟, 張韶岷. 腫瘤電場治療的模型仿真研究. 生物醫學工程學雜志, 2024, 41(2): 360-367. doi: 10.7507/1001-5515.202306074 復制
版權信息: ?四川大學華西醫院華西期刊社《生物醫學工程學雜志》版權所有,未經授權不得轉載、改編
0 引言
腫瘤電場治療(tumor-treating fields,TTFields)是一種新型無創治療癌癥的物理療法。離體實驗發現,對腫瘤細胞施加低強度(1~3 V/cm)的中頻交變電場(100~500 kHz),可以達到抑制腫瘤細胞分裂的效果,該效果和施加電場的方向、時長、強度有關,不同腫瘤細胞的最佳治療電場頻率也不同[1]。在針對多形性膠質母細胞瘤(glioblastoma,GBM)的臨床試驗中,腫瘤電場治療顯著延長了患者的中位總生存期[2]。腫瘤電場治療在早期的細胞模型實驗和臨床試驗中已經表現出可以抑制不同類型實體腫瘤細胞的分裂和增殖的效果,包括人和動物的黑色素瘤、胸膜間皮瘤、肺癌和人乳腺癌等不同惡性腫瘤[3-4]。相比傳統的癌癥治療方法,腫瘤電場治療產生的副作用較小,具有較好的安全性[5]。腫瘤電場治療的作用機制尚不確切,通常認為是中頻(100~300 kHz)、低強度(1~3 V/cm)的交變電場會干擾細胞的有絲分裂,影響細胞分裂周期[6-8]。腫瘤電場治療抑制腫瘤細胞分裂的效果和電場強度、頻率有密切關系,所以在動物實驗以及臨床試驗中,確定腫瘤所在位置的電場分布至關重要,而目前主要通過建模仿真方法進行估計。
腫瘤電場治療仿真模型的構建一般包括組織分割、電極放置、網格劃分、有限元計算等步驟,但已有研究的具體建模路線不一致,整體建模流程常使用成本較高的商用軟件,復現難度較大。2014年,Miranda等[9]已開展了相關仿真研究,該研究基于磁共振影像數據進行真實頭模構建,使用腦部圖像處理軟件 BrainSuite(California University,美國)進行組織分割,并用醫學圖像處理軟件Mimics(Materialise Inc.,比利時)進行有限元網格劃分,多物理場建模和仿真軟件COMSOL(Comsol Inc.,瑞典)進行計算仿真和結果可視化,最終發現顱內的電場分布和組織結構密切相關。Korshoej等[10-11]利用非侵入式腦刺激模擬軟件SimNIBS(Technical University of Denmark,丹麥)進行了近似條件的腫瘤電場治療仿真研究,分析了電極陣列對真實頭部模型內電場分布的影響。Bomzon等[12]利用生物電磁場仿真平臺Sim4Life(Zurich MedTech Inc.,瑞士),對人體軀干模型進行了仿真研究。Timmons等[13]和Lok等[14]使用數值計算和仿真軟件MATLAB(Mathworks Inc.,美國)內的工具包,對頭部磁共振影像數據進行組織分割和虛擬電極放置等操作,利用三維圖像處理軟件ScanIP(Simpleware Inc.,英國)進行后處理和有限元網格模型生成,最后使用COMSOL進行計算仿真。Yang等[15]采用COMSOL建立真實頭部腫瘤仿真模型,探索了顱骨修飾、缺損等情形對顱內電場分布的影響,但相關模型精度較差,丟失了較多的解剖結構細節。杜宗倫等[16]使用Mimics軟件建立了高精度的頭部真實仿真模型。總的來看,目前腫瘤電場治療模型構建技術路線不一致,大都選擇成本較高的商用軟件,難以進行橫向復現對比分析,阻礙了腫瘤電場治療模型的推廣應用。此外,腦組織在不同條件下的電導率會發生明顯變化,例如頭部皮膚的干燥程度不同會導致其電導率有明顯差異、顱骨的骨密質和骨松質部分對應的電導率大小也不同;腫瘤生長階段的不同也會造成其電導率變化范圍大等,而采用不同的電極對顱內電場的分布也有著明顯不同的影響。針對上述多種情形,目前尚缺乏系統性的相關仿真研究。基于此,本研究旨在開發易實現的腫瘤電場治療仿真模型構建方法。首先,基于頭部磁共振影像數據進行組織分割和三維重建,添加模擬腫瘤和電極,得到有限元網格模型;而后,基于仿真模型探索不同組織電學特性,包括不同電極位置、數量和大小對仿真結果的影響,以證明本文所提建模方法的可行性與有效性,為未來的腫瘤電場治療的仿真分析和臨床應用提供參考。
1 材料和方法
1.1 腫瘤電場治療頭部仿真模型構建
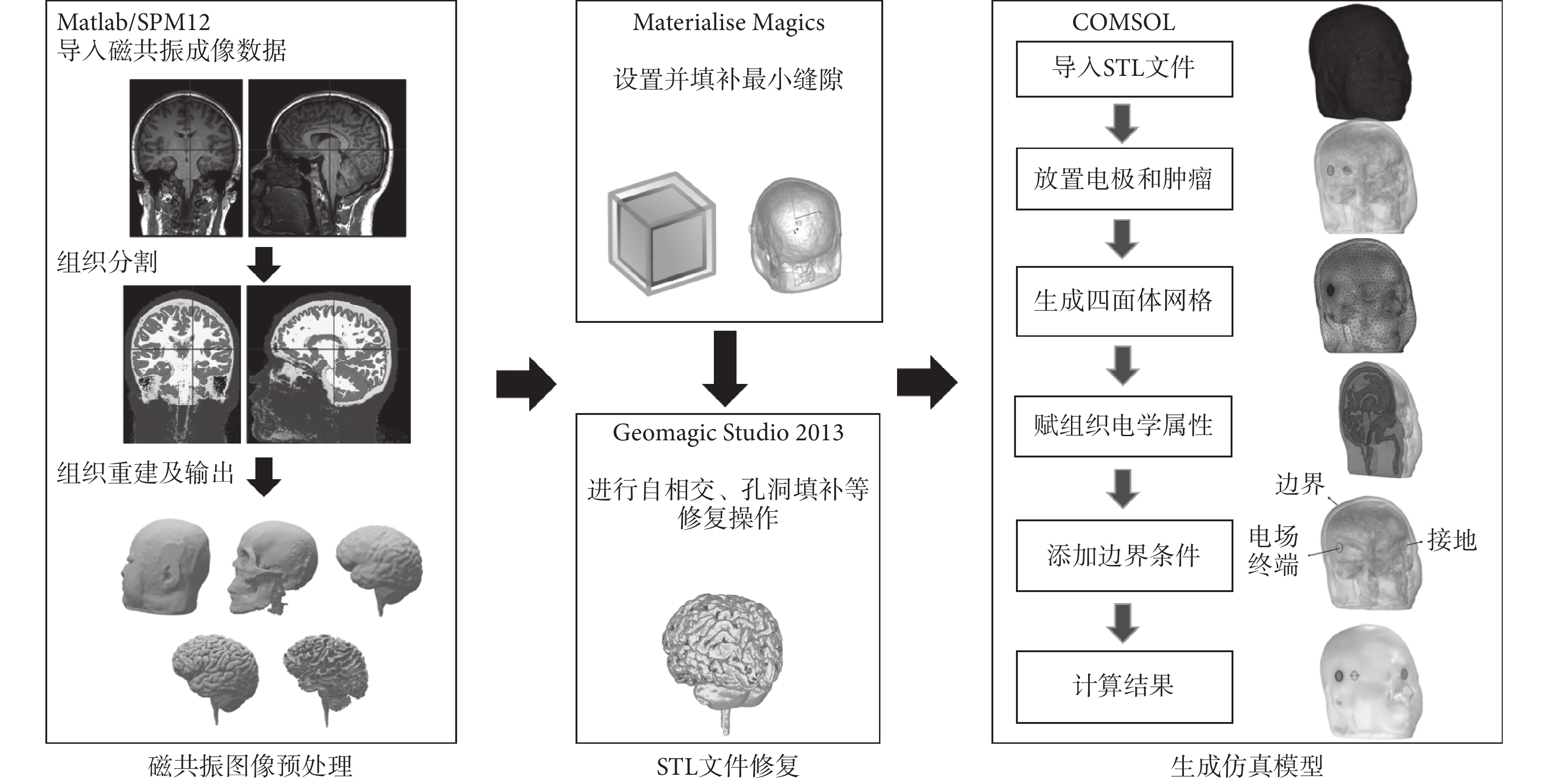
構建腫瘤電場治療的頭部仿真模型的總流程如圖1所示。主要包括三個步驟:磁共振圖像預處理、標準三角面片語言(standard tessellation language,STL)文件修復和生成仿真模型。頭部磁共振圖像來源于目前廣泛使用的公開數據庫——蒙特利爾神經科學研究所152號腦成像國際聯盟數據庫(International Consortium for Brain Mapping 152,ICBM152)。
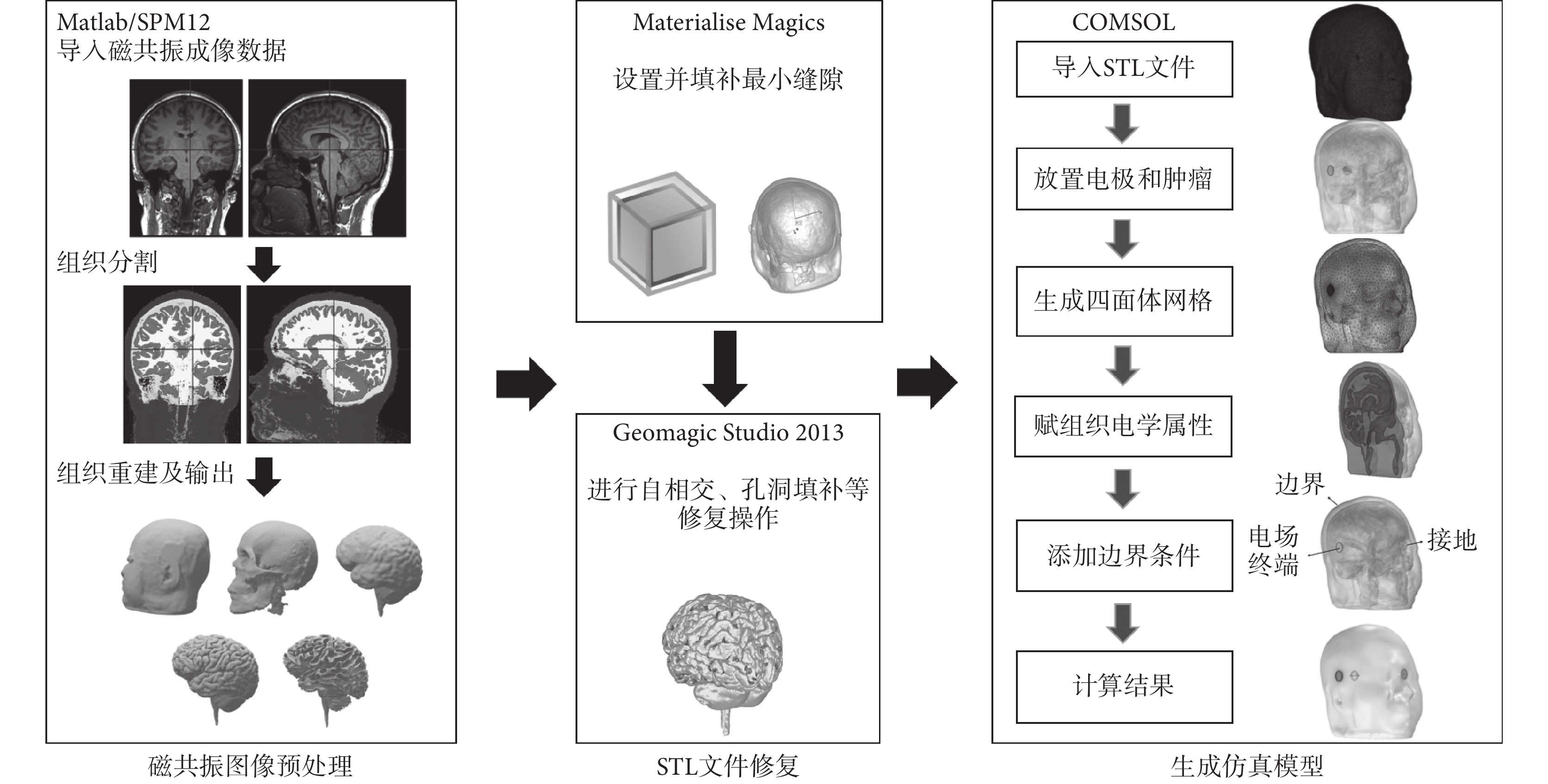 圖1
頭部仿真模型構建流程
Figure1.
The construction process of the head simulation model
圖1
頭部仿真模型構建流程
Figure1.
The construction process of the head simulation model
1.1.1 基于頭部磁共振圖像的組織分割
在本研究中,使用腦結構成像數據分析軟件SPM12(University College London,英國)來實現圖像和組織分割,主要包括原始圖的歸一化、分割、調制和平滑操作四個步驟[17-19]。
1.1.2 組織分割后優化處理
在完成組織分割以后,導出的組織模型常出現表面不封閉、組織邊界自相交等問題,需進一步優化處理。
首先,將不同組織的STL文件導入優化軟件,本研究使用的軟件是數據處理軟件Materialise Magics(Materialise Inc.,比利時)和建模軟件Geomagic Studio 2013(3D System Inc.,美國)。首先用Materialise Magics軟件的零件包裹功能,填充和消除小于特定精度的結構和縫隙;第二步使用Geomagic Studio 2013軟件對分割后不同組織的STL文件進行修復處理,主要包括消除自相交、釘狀物、高度折射邊以及小通道等操作。
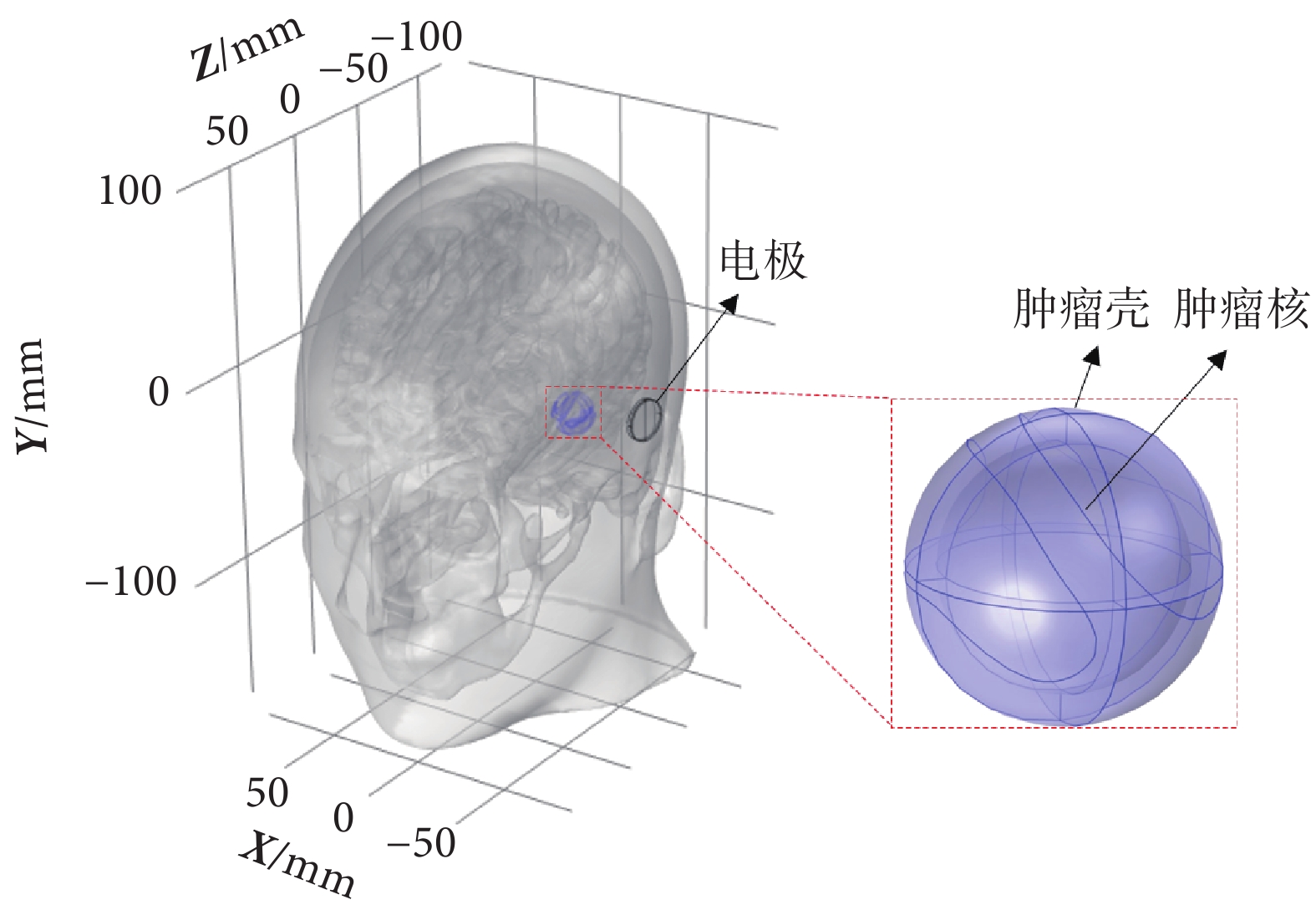
所有組織文件修復結束以后,導入COMSOL生成幾何,利用COMSOL的幾何生成工具放置電極、導電膏以及模擬腫瘤,其中電極尺寸按照美國諾沃庫勒(Novocure)公司的電極大小進行建模。模擬腫瘤為半徑為10 mm的球體,分為兩層:表層3 mm作為腫瘤殼,對應腫瘤侵入正常組織的浸潤區域;內層為腫瘤核[20],對應腫瘤內部的壞死區域。由于腫瘤核和其交界區域的組織結構差異,兩部分組織的電學屬性也明顯不同,仿真時將被賦予不同的電導率和介電常數[21]。在COMSOL中生成的整體幾何結構和電極、腫瘤如圖2所示。
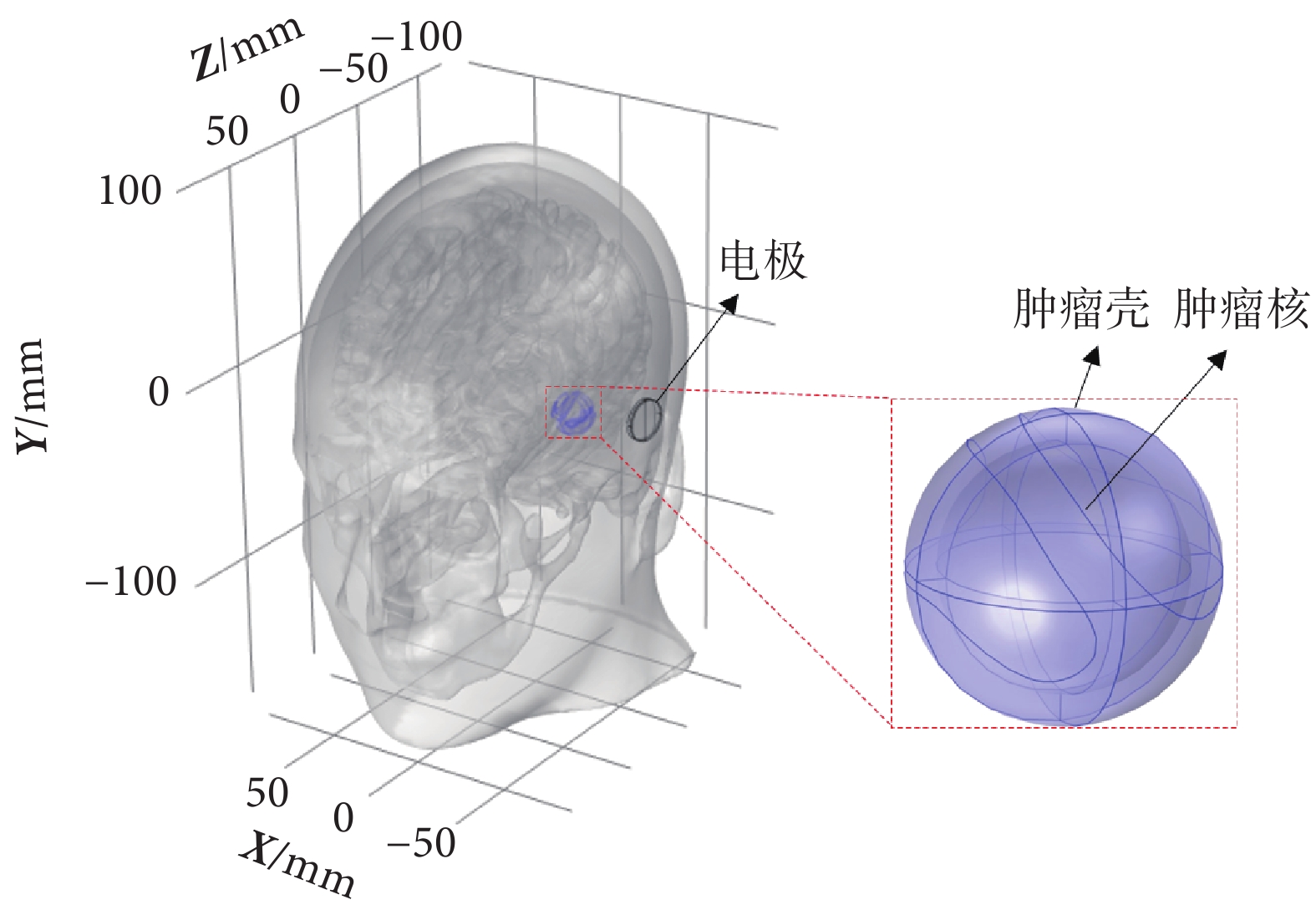 圖2
生成腫瘤結構和新增電極示意圖
Figure2.
Schematic illustration of generating tumor structure and adding electrodes
圖2
生成腫瘤結構和新增電極示意圖
Figure2.
Schematic illustration of generating tumor structure and adding electrodes
1.1.3 基于有限元方法的頭部仿真模型構建
在COMSOL軟件中,對之前處理好的頭部仿真幾何模型進行有限元網格劃分,自動生成自由四面體網格,從而實現頭部仿真模型的構建。
1.2 不同組織介電特性與刺激參數的腫瘤電場治療頭部仿真模型研究
在完成腫瘤電場治療的頭部仿真模型的構建后,即可進行在不同條件下的腫瘤電場治療仿真研究。為體現仿真模型的通用和一般性,本研究采用公開數據庫ICBM152構建腫瘤電場治療的頭部仿真模型[22-23]。
1.2.1 組織介電特性影響顱內電場分布的仿真研究設置
組織的介電特性是影響腫瘤電場治療仿真結果的重要因素。本實驗采用200 kHz下頭部組織常用的電學屬性為參照,在此基礎上通過合理改變不同組織的電導率和介電常數,進行仿真分析顱內及腫瘤附近的電場變化,進而推斷出不同組織電學屬性對腫瘤處的電場分布的影響程度。頭部不同的組織在200 kHz下常用的電學屬性如表1所示[24-25],其值作為標準仿真參照組。
本文重點研究頭皮、頭骨、腫瘤這三種組織的電導率變化產生的影響,根據表1取頭皮的電導率為:0.001、0.010 S/m,另再增加0.100 S/m作更大電導率值的差異性對比[26];顱骨電導率按照骨密質和骨松質的情況,分別取:0.020、0.080 S/m作對比[27];腫瘤殼電導率取上下十倍變化:0.024 S/m和2.400 S/m;腫瘤核電導率取上下十倍變化:10.000 S/m和0.100 S/m[15]。
關于組織的介電常數對顱內及腫瘤電場分布的影響,根據麥克斯韋—安培定律,若腫瘤電場治療的頻段在100~300 kHz,根據人體頭部組織在該頻段的電導率和相對介電常數[25],相關電導率的數值遠大于組織介電常數與角頻率的乘積,因此介電常數對實際的電場分布應該影響很小。為證實此觀點,將所有頭部組織的相對介電常數設置為1,再和正常相對介電常數的仿真結果對比。
1.2.2 電極位置、數量和大小影響顱內電場分布的仿真研究設置
在實際臨床應用和研究中,電極的位置等參數需要根據腫瘤的大小和位置來設計治療方案。對于膠質母細胞瘤來說,該腫瘤好發于額葉、顳葉、頂葉白質內[28-30],所以本實驗在顳葉放置半徑為10 mm的球體腫瘤模型,在X-Y-Z軸上腫瘤的具體坐標位置為(?45,?19,?16)。
確定了腫瘤位置之后,在頭部模型左右和前后位置各放置一對標準電極(電極直徑為9.60 mm),通過對比不同距離的仿真結果,判斷電極位置對顱內及腫瘤電場分布的影響。按照電學理論估計,距離腫瘤距離越近,電流密度越大,產生的電場強度也越大,所以在研究電極數量的影響時,選擇距離腫瘤最近的一對標準電極和相同位置附近的三對標準電極對比。由于電極數量的增加,為保證整體電流相等,每對電極電流大小變為一對標準電極的三分之一,在仿真時,一對標準電極的電流密度設置為150 A/m2,三對標準電極的電流密度為50 A/m2。在研究電極大小對顱內及腫瘤電場分布的影響時,將距離腫瘤最近的一對標準電極的面積增加三倍,為保持電流大小不變,大電極電流密度同樣為標準電極的三分之一,設置為50 A/m2。三對電極和大電極對在面積上相等,電流大小也相等,可進一步作對比分析。綜上,以三種電極在不同位置、數量和大小方面對比分析,三種電極前后放置的示意如圖3所示。
 圖3
模型的三種電極示意圖
Figure3.
Three types of electrodes of the model
圖3
模型的三種電極示意圖
Figure3.
Three types of electrodes of the model
2 結果
2.1 組織介電特性對腫瘤電場治療場分布的影響
在顳葉腫瘤模型上,由于腫瘤位置相對靠中,分析顱內和腫瘤內的電場均采用腫瘤球心坐標所在的X-Y-Z平面。在研究頭皮和頭骨電導率對顱內和腫瘤內電場分布的影響方面,經仿真后計算顱內和腫瘤內的平均電場強度值,如表2所示。區域的平均電場強度在COMSOL軟件中可通過計算該區域所有體素點上的電場強度體積積分平均值來得到,可以反映出組織電特性變化等因素對電場分布的影響程度。通過觀察顱內和腫瘤內不同截面的電場分布以及對比平均電場強度可以看出,隨著頭皮電導率的增大,顱內和腫瘤處的電場強度有小幅度的降低(顱內平均治療場強相對于標準設置下降16.4%,瘤體內平均場強下降21.0%),說明頭皮組織電導率對顱內和腫瘤內電場影響較小。顱骨組織電導率增大,會引起顱內和腫瘤的電場強度小幅度地降低(顱內平均治療場強相對于標準設置下降2.1%,瘤體內平均場強下降2.6%),這和頭皮組織電導率變化引起的電場變化趨勢一致,其原因為顱骨組織電導率增大,會減少顱內和腫瘤的電流密度,進而影響相應的誘發電場強度。
腫瘤組織在不同電導率下的仿真分析具體考慮如下幾個方面:腫瘤殼組織電導率分別在0.024、0.240、2.400 S/m條件下進行仿真分析;腫瘤核組織電導率分別在0.100、1.000、10.000 S/m條件下進行仿真分析。計算顱內、腫瘤殼和腫瘤核內平均電場強度,如表3所示。顱內平均電場強度變化隨腫瘤各組織電導率變化較小(顱內平均治療場強相對于標準設置最高變化1.1%),主要原因為腫瘤的體積相對較小,腫瘤殼和腫瘤核的組織電導率增大導致腫瘤內部的平均電場強度減小。同時腫瘤核組織電導率增大,對于腫瘤殼整體平均電場強度影響較小,而增大腫瘤殼組織電導率會使得腫瘤殼內平均電場強度減小,其原因和電導率改變引起附近電流密度的改變有關。
介電常數對顱內和腫瘤內電場分布的仿真分析應考慮,不同組織在正常介電常數和介電常數全為1的條件下,仿真結果差異較小,計算腫瘤的平均電場強度分別為27.271 V/m和27.274 V/m,顱內平均電場強度分別為:15.219 V/m和15.379 V/m,此結果也進一步驗證先前假設。
2.2 電極位置、數量和大小對腫瘤電場治療場分布的影響
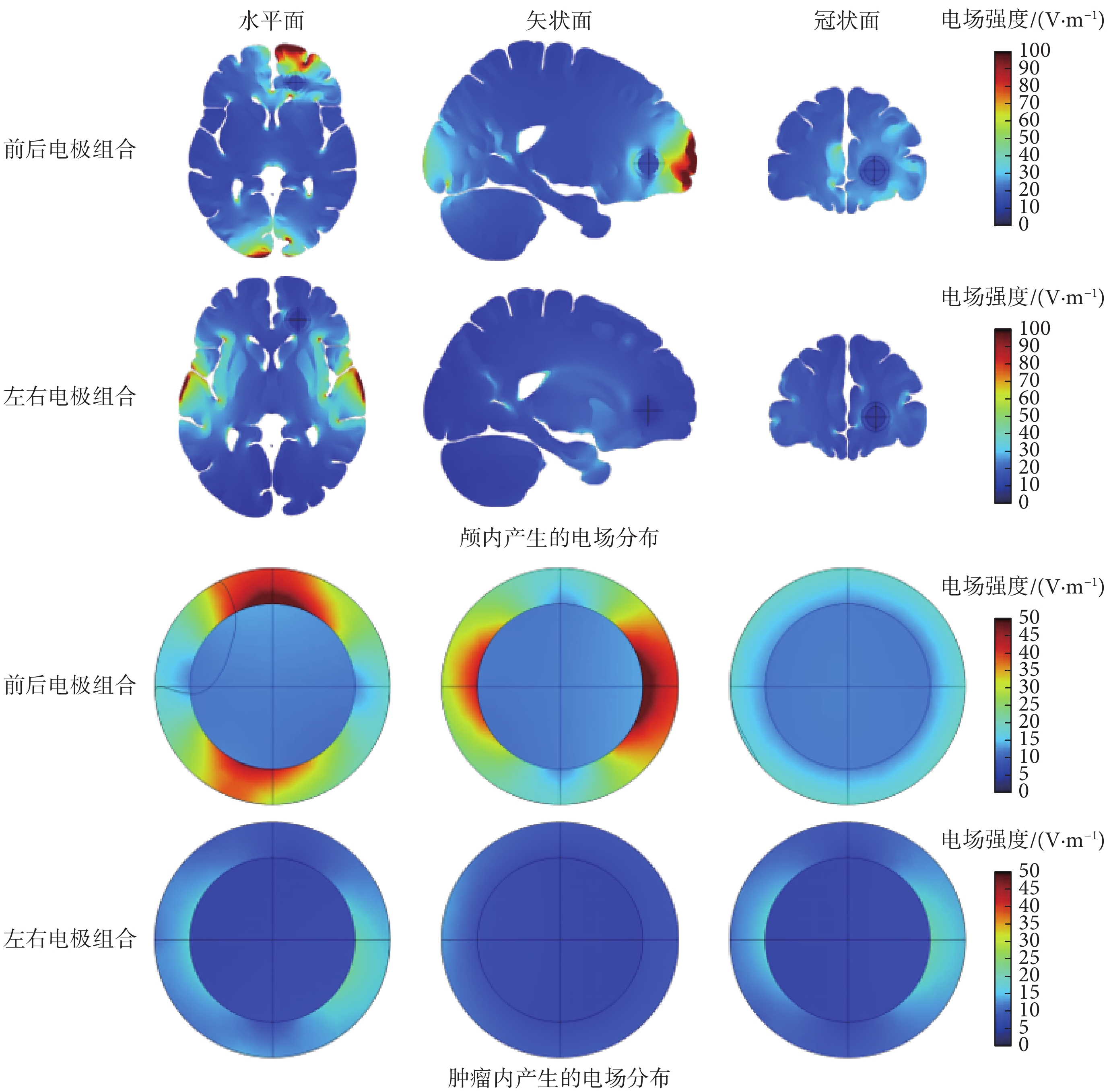
在顳葉腫瘤模型上,分別通過左右和前后位置的電極施加電場,顱內和腫瘤電場分布仿真結果如圖4所示。從電場分布圖可以看出,顱內較大的電場強度集中分布在電極附近;腫瘤內較大電場的方向和電極方向一致;腫瘤距離電極位置越遠,內部電場強度越低。計算顱內、腦脊液和腫瘤的平均電場強度值,如表4所示。顱內平均電場強度在左右電極組合下大于前后電極組合的情況,腦脊液中的電場強度在前后電極下大于左右電極的情況,原因為前后電極距離較遠,更多的電流分布在導電性更好的腦脊液中,導致顱內電場強度降低。由于腫瘤距離左右電極較近,內部電場強度遠大于前后電極產生的電場強度。
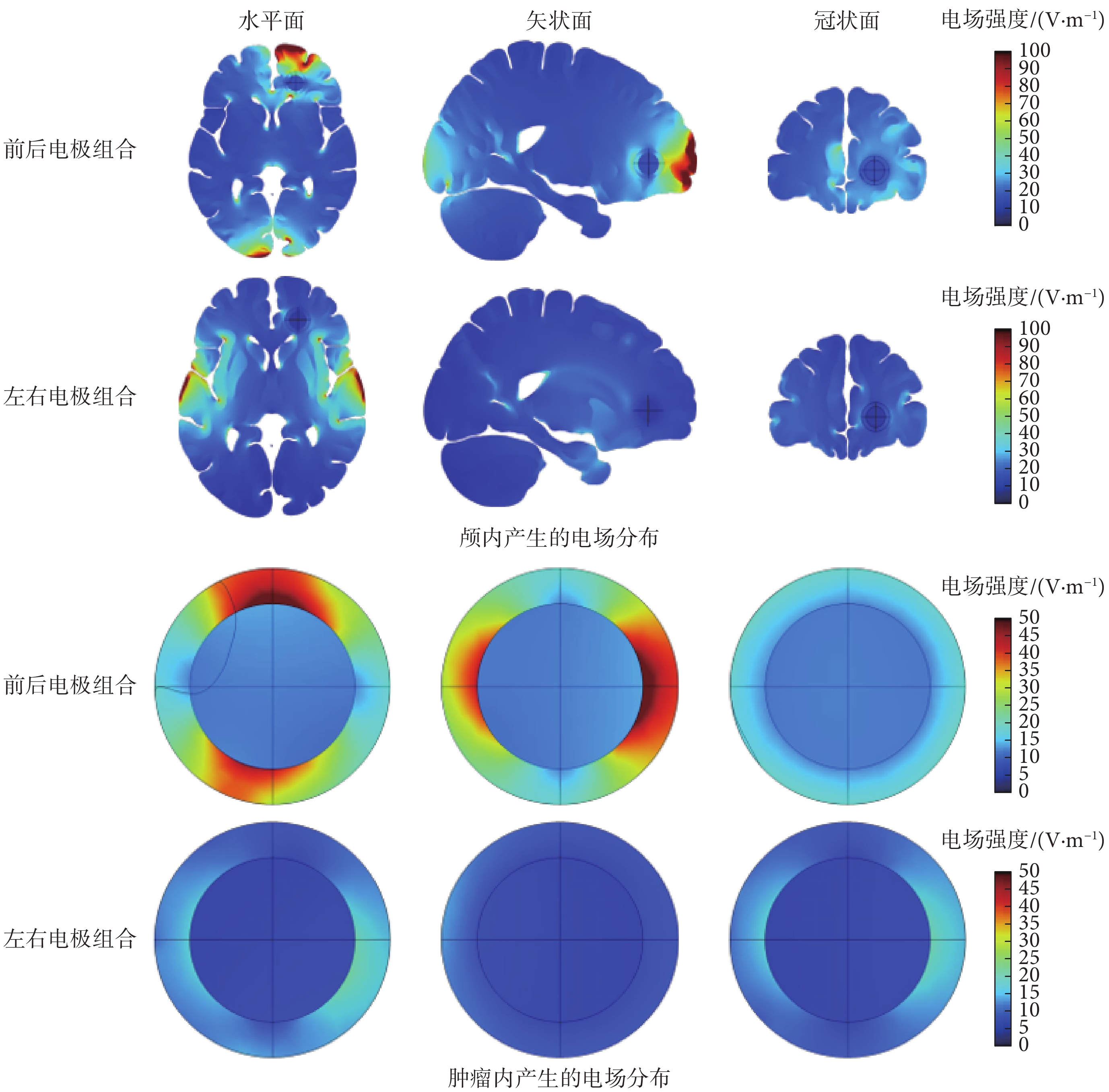 圖4
前后電極組合和左右電極組合在顱內及腫瘤內產生的電場分布
Figure4.
The electric fields distribution generated by the anterior-posterior electrode and the right-left electrode in the intracranial and intratumoral regions
圖4
前后電極組合和左右電極組合在顱內及腫瘤內產生的電場分布
Figure4.
The electric fields distribution generated by the anterior-posterior electrode and the right-left electrode in the intracranial and intratumoral regions
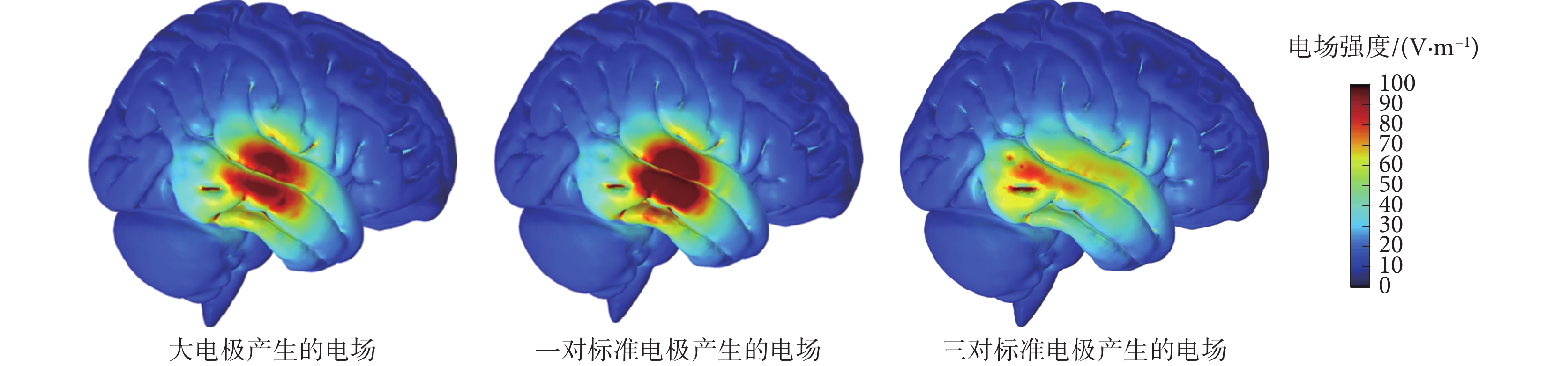
不同電極數量和大小對顱內和腫瘤內電場分布的仿真分析如下:大電極、一對標準電極和三對標準電極在顳葉區域施加電場時,在顱內灰質表面的電場分布如圖5所示。圖5中一對標準電極產生的高場強(對應圖中深紅色區域)的區域面積最大,其次是大電極,三對標準電極產生的高場強區域面積最小。圖5中,較強電場(對應圖5中淡青色區域)的區域以三對標準電極產生的范圍最大。分別計算顱內和腫瘤內的平均電場強度值,如表5所示。顱內和腫瘤內電場都呈現出一對標準電極產生最大的場強、大電極其次、三對標準電極產生的場強最小的結果,也與計算的顱內和腫瘤內平均電場強度值的情況相符。三種電極在顱內和腫瘤內產生的電場有所不同,其原因是電極法向電流密度和頭部接觸面存在差異,電極面積越大,接觸面的曲面角度越大,法向電流在顱內的矢量抵消也就越多,所以大電極和三對標準電極在顱內和腫瘤內產生的電場強度要小于一對標準電極產生的電場強度。如圖6所示,大電極相對于三對標準電極的放置的整體接觸面更加平整,法向電流密度矢量抵消的少,同時距離腫瘤更近,所以在顱內和腫瘤內的電場強度方面,大電極略大于三對標準電極。
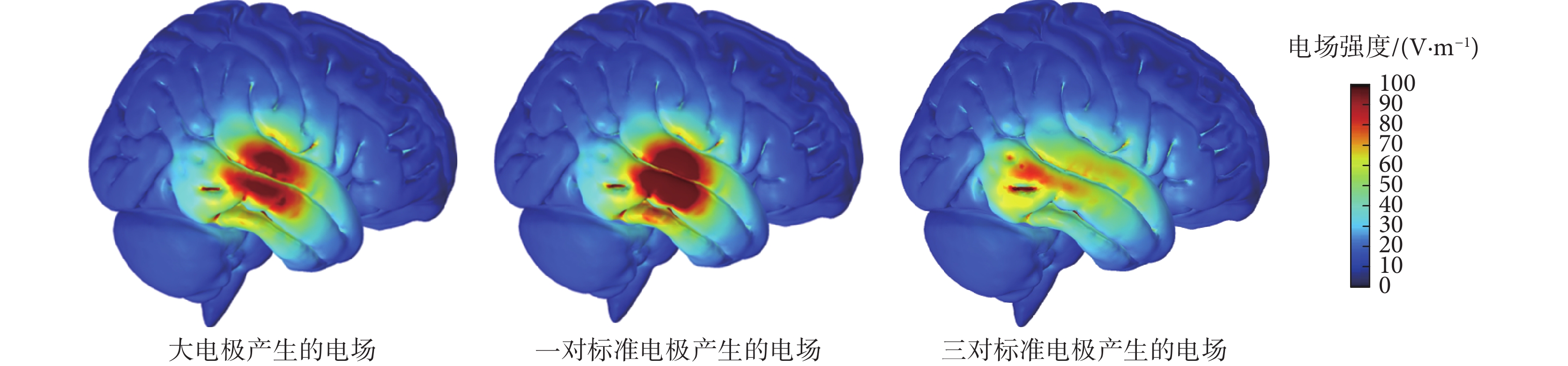 圖5
不同電極組合在顱內產生的電場分布
Figure5.
Electric field distribution generated by different electrode montages
圖5
不同電極組合在顱內產生的電場分布
Figure5.
Electric field distribution generated by different electrode montages
 圖6
大電極和三對標準電極與腫瘤的空間位置
Figure6.
Spatial location of large electrodes and three pairs of standard electrodes in the temporal lobe and tumors
圖6
大電極和三對標準電極與腫瘤的空間位置
Figure6.
Spatial location of large electrodes and three pairs of standard electrodes in the temporal lobe and tumors
3 討論
在腫瘤電場治療的科學研究和臨床應用中,建模仿真的分析方法發揮著重要作用,是不可缺少的環節。然而在針對腫瘤電場治療的建模和仿真的相關研究中,存在著不少問題。在構建仿真模型方面,國外相關研究已構建較高精度的仿真模型,但其所報道的技術路線不能很好地適配不同的用戶場景,如在建模中使用專業的組織分割和處理軟件Mimics對影像學數據直接處理[31],或者在生成有限元網格時直接利用 ScanIP軟件進行操作,相關軟件使用成本較高,對于沒有軟件資源的研究團隊而言,難以開展類似相關工作[32]。因此,本研究基于頭部磁共振影像數據進行組織分割和三維重建,利用常用的軟件資源對模型進行修飾和完善,添加模擬腫瘤和電極,確定計算仿真的電學條件,最終得到能直接計算的有限元網格模型。
此外,已有的腫瘤電場治療仿真研究仍不夠系統,大多基于單一的應用方案,缺少其他類型的仿真分析,因此需要進一步探索不同組織電學特性,包括電極位置、數量和大小等參數對仿真結果的影響。本研究利用前面已建立的仿真方法,對構建的含有顳葉腫瘤的頭部仿真模型進行仿真分析,首先分析了不同組織的電學參數對顱內和腫瘤內電場分布的影響;其次研究了不同電極位置、數量和大小對顱內和腫瘤內電場分布的影響。不同電學參數的對比研究包含頭皮、顱骨和腫瘤三種組織的電導率變化,以及所有頭部組織的介電常數變化。從仿真結果上可以看出,頭皮組織的電導率增加,對顱內和腫瘤內的電場分布影響不大,平均電場強度分別下降了16.4%和21.0%;顱骨的電導率增大對電場分布影響很小,顱內和腫瘤內的平均電場強度分別只下降了2.1%和2.6%;腫瘤組織本身電導率的變化會顯著改變其內部電場強度,所以確定腫瘤電場治療頻段下腫瘤組織的電導率參數對仿真結果的準確程度至關重要。在腫瘤電場治療中,組織的介電常數參數對于顱內和腫瘤內電場分布幾乎沒有影響,在相關的研究和實驗中,可以忽略掉該參數。在對電極位置、數量和大小進行仿真分析的結果表明,電極位置距離腫瘤越近,腫瘤內部電場越強;在相同電流條件下,一對標準電極在顱內和腫瘤內產生的電場較強,大電極和多數量的電極由于接觸面較一對標準電極存在較大曲度,注入頭部的法向電流密度存在矢量抵消,產生的電場會略小。因此在腫瘤治療過程中使用數量較少的小電極可以更容易在顱內腫瘤處產生更大的刺激場強。
在構建高精度頭部仿真模型和仿真研究工作中,仍有一些亟待改善的方面。首先,構建高精度頭部仿真模型時需要使用的軟件較多,各步驟銜接不夠流暢,模型優化操作繁瑣,并且在生成有限元網格時容易出現錯誤,整體過程耗時較長、工作量大,需要更加簡便快捷的構建方法,例如在分割組織后生成可直接用于計算的有限元網格、更加便捷的放置電極操作等。其次,實際情況下不同腫瘤的大小、形狀等性質差異較大,電導率、相對介電常數的分布個體差異也比較明顯,因此需要綜合臨床數據建立一個更加符合實際腫瘤特性的腫瘤仿真模型。在實際應用中,電極發熱控制也是一項重要的設計原則,電極功率高、發熱大,會造成嚴重的皮膚不良反應,但在對頭部腫瘤模型進行仿真研究中,未考慮施加電場的功率和發熱問題。同時,本次仿真研究未和實際應用廠家的電極放置方式作對比,也缺少增加顱內和腫瘤內電場強度的方法仿真研究,如顱骨摘除術等。
4 結論
腫瘤電場治療作為一種前景廣闊的無創腫瘤治療方式,已廣泛應用在科研和臨床中,其中腫瘤電場治療的仿真分析是個體量效評估和方案優化的重要一環。本研究建立了一套易實現的腫瘤電場治療仿真模型構建方法,并基于該仿真模型開展了不同組織電學參數、電極大小和數量差異等因素的理論分析,探究了這些因素對顱內和腫瘤內電場分布的影響,發現腫瘤自身介電特性與電極位置是影響其治療場分布的重要因素,同時驗證了所提出建模方法的可行性和有效性。
重要聲明
利益沖突:本文全體作者均聲明不存在利益沖突。
作者貢獻說明:秦麗平、謝旭、馬明偉負責仿真分析、數據整理與論文撰寫,潘赟、陳光弟、張韶岷指導數據分析及論文撰寫,王敏敏指導課題實施、數據分析及論文撰寫。
0 引言
腫瘤電場治療(tumor-treating fields,TTFields)是一種新型無創治療癌癥的物理療法。離體實驗發現,對腫瘤細胞施加低強度(1~3 V/cm)的中頻交變電場(100~500 kHz),可以達到抑制腫瘤細胞分裂的效果,該效果和施加電場的方向、時長、強度有關,不同腫瘤細胞的最佳治療電場頻率也不同[1]。在針對多形性膠質母細胞瘤(glioblastoma,GBM)的臨床試驗中,腫瘤電場治療顯著延長了患者的中位總生存期[2]。腫瘤電場治療在早期的細胞模型實驗和臨床試驗中已經表現出可以抑制不同類型實體腫瘤細胞的分裂和增殖的效果,包括人和動物的黑色素瘤、胸膜間皮瘤、肺癌和人乳腺癌等不同惡性腫瘤[3-4]。相比傳統的癌癥治療方法,腫瘤電場治療產生的副作用較小,具有較好的安全性[5]。腫瘤電場治療的作用機制尚不確切,通常認為是中頻(100~300 kHz)、低強度(1~3 V/cm)的交變電場會干擾細胞的有絲分裂,影響細胞分裂周期[6-8]。腫瘤電場治療抑制腫瘤細胞分裂的效果和電場強度、頻率有密切關系,所以在動物實驗以及臨床試驗中,確定腫瘤所在位置的電場分布至關重要,而目前主要通過建模仿真方法進行估計。
腫瘤電場治療仿真模型的構建一般包括組織分割、電極放置、網格劃分、有限元計算等步驟,但已有研究的具體建模路線不一致,整體建模流程常使用成本較高的商用軟件,復現難度較大。2014年,Miranda等[9]已開展了相關仿真研究,該研究基于磁共振影像數據進行真實頭模構建,使用腦部圖像處理軟件 BrainSuite(California University,美國)進行組織分割,并用醫學圖像處理軟件Mimics(Materialise Inc.,比利時)進行有限元網格劃分,多物理場建模和仿真軟件COMSOL(Comsol Inc.,瑞典)進行計算仿真和結果可視化,最終發現顱內的電場分布和組織結構密切相關。Korshoej等[10-11]利用非侵入式腦刺激模擬軟件SimNIBS(Technical University of Denmark,丹麥)進行了近似條件的腫瘤電場治療仿真研究,分析了電極陣列對真實頭部模型內電場分布的影響。Bomzon等[12]利用生物電磁場仿真平臺Sim4Life(Zurich MedTech Inc.,瑞士),對人體軀干模型進行了仿真研究。Timmons等[13]和Lok等[14]使用數值計算和仿真軟件MATLAB(Mathworks Inc.,美國)內的工具包,對頭部磁共振影像數據進行組織分割和虛擬電極放置等操作,利用三維圖像處理軟件ScanIP(Simpleware Inc.,英國)進行后處理和有限元網格模型生成,最后使用COMSOL進行計算仿真。Yang等[15]采用COMSOL建立真實頭部腫瘤仿真模型,探索了顱骨修飾、缺損等情形對顱內電場分布的影響,但相關模型精度較差,丟失了較多的解剖結構細節。杜宗倫等[16]使用Mimics軟件建立了高精度的頭部真實仿真模型。總的來看,目前腫瘤電場治療模型構建技術路線不一致,大都選擇成本較高的商用軟件,難以進行橫向復現對比分析,阻礙了腫瘤電場治療模型的推廣應用。此外,腦組織在不同條件下的電導率會發生明顯變化,例如頭部皮膚的干燥程度不同會導致其電導率有明顯差異、顱骨的骨密質和骨松質部分對應的電導率大小也不同;腫瘤生長階段的不同也會造成其電導率變化范圍大等,而采用不同的電極對顱內電場的分布也有著明顯不同的影響。針對上述多種情形,目前尚缺乏系統性的相關仿真研究。基于此,本研究旨在開發易實現的腫瘤電場治療仿真模型構建方法。首先,基于頭部磁共振影像數據進行組織分割和三維重建,添加模擬腫瘤和電極,得到有限元網格模型;而后,基于仿真模型探索不同組織電學特性,包括不同電極位置、數量和大小對仿真結果的影響,以證明本文所提建模方法的可行性與有效性,為未來的腫瘤電場治療的仿真分析和臨床應用提供參考。
1 材料和方法
1.1 腫瘤電場治療頭部仿真模型構建
構建腫瘤電場治療的頭部仿真模型的總流程如圖1所示。主要包括三個步驟:磁共振圖像預處理、標準三角面片語言(standard tessellation language,STL)文件修復和生成仿真模型。頭部磁共振圖像來源于目前廣泛使用的公開數據庫——蒙特利爾神經科學研究所152號腦成像國際聯盟數據庫(International Consortium for Brain Mapping 152,ICBM152)。
 圖1
頭部仿真模型構建流程
Figure1.
The construction process of the head simulation model
圖1
頭部仿真模型構建流程
Figure1.
The construction process of the head simulation model
1.1.1 基于頭部磁共振圖像的組織分割
在本研究中,使用腦結構成像數據分析軟件SPM12(University College London,英國)來實現圖像和組織分割,主要包括原始圖的歸一化、分割、調制和平滑操作四個步驟[17-19]。
1.1.2 組織分割后優化處理
在完成組織分割以后,導出的組織模型常出現表面不封閉、組織邊界自相交等問題,需進一步優化處理。
首先,將不同組織的STL文件導入優化軟件,本研究使用的軟件是數據處理軟件Materialise Magics(Materialise Inc.,比利時)和建模軟件Geomagic Studio 2013(3D System Inc.,美國)。首先用Materialise Magics軟件的零件包裹功能,填充和消除小于特定精度的結構和縫隙;第二步使用Geomagic Studio 2013軟件對分割后不同組織的STL文件進行修復處理,主要包括消除自相交、釘狀物、高度折射邊以及小通道等操作。
所有組織文件修復結束以后,導入COMSOL生成幾何,利用COMSOL的幾何生成工具放置電極、導電膏以及模擬腫瘤,其中電極尺寸按照美國諾沃庫勒(Novocure)公司的電極大小進行建模。模擬腫瘤為半徑為10 mm的球體,分為兩層:表層3 mm作為腫瘤殼,對應腫瘤侵入正常組織的浸潤區域;內層為腫瘤核[20],對應腫瘤內部的壞死區域。由于腫瘤核和其交界區域的組織結構差異,兩部分組織的電學屬性也明顯不同,仿真時將被賦予不同的電導率和介電常數[21]。在COMSOL中生成的整體幾何結構和電極、腫瘤如圖2所示。
 圖2
生成腫瘤結構和新增電極示意圖
Figure2.
Schematic illustration of generating tumor structure and adding electrodes
圖2
生成腫瘤結構和新增電極示意圖
Figure2.
Schematic illustration of generating tumor structure and adding electrodes
1.1.3 基于有限元方法的頭部仿真模型構建
在COMSOL軟件中,對之前處理好的頭部仿真幾何模型進行有限元網格劃分,自動生成自由四面體網格,從而實現頭部仿真模型的構建。
1.2 不同組織介電特性與刺激參數的腫瘤電場治療頭部仿真模型研究
在完成腫瘤電場治療的頭部仿真模型的構建后,即可進行在不同條件下的腫瘤電場治療仿真研究。為體現仿真模型的通用和一般性,本研究采用公開數據庫ICBM152構建腫瘤電場治療的頭部仿真模型[22-23]。
1.2.1 組織介電特性影響顱內電場分布的仿真研究設置
組織的介電特性是影響腫瘤電場治療仿真結果的重要因素。本實驗采用200 kHz下頭部組織常用的電學屬性為參照,在此基礎上通過合理改變不同組織的電導率和介電常數,進行仿真分析顱內及腫瘤附近的電場變化,進而推斷出不同組織電學屬性對腫瘤處的電場分布的影響程度。頭部不同的組織在200 kHz下常用的電學屬性如表1所示[24-25],其值作為標準仿真參照組。
本文重點研究頭皮、頭骨、腫瘤這三種組織的電導率變化產生的影響,根據表1取頭皮的電導率為:0.001、0.010 S/m,另再增加0.100 S/m作更大電導率值的差異性對比[26];顱骨電導率按照骨密質和骨松質的情況,分別取:0.020、0.080 S/m作對比[27];腫瘤殼電導率取上下十倍變化:0.024 S/m和2.400 S/m;腫瘤核電導率取上下十倍變化:10.000 S/m和0.100 S/m[15]。
關于組織的介電常數對顱內及腫瘤電場分布的影響,根據麥克斯韋—安培定律,若腫瘤電場治療的頻段在100~300 kHz,根據人體頭部組織在該頻段的電導率和相對介電常數[25],相關電導率的數值遠大于組織介電常數與角頻率的乘積,因此介電常數對實際的電場分布應該影響很小。為證實此觀點,將所有頭部組織的相對介電常數設置為1,再和正常相對介電常數的仿真結果對比。
1.2.2 電極位置、數量和大小影響顱內電場分布的仿真研究設置
在實際臨床應用和研究中,電極的位置等參數需要根據腫瘤的大小和位置來設計治療方案。對于膠質母細胞瘤來說,該腫瘤好發于額葉、顳葉、頂葉白質內[28-30],所以本實驗在顳葉放置半徑為10 mm的球體腫瘤模型,在X-Y-Z軸上腫瘤的具體坐標位置為(?45,?19,?16)。
確定了腫瘤位置之后,在頭部模型左右和前后位置各放置一對標準電極(電極直徑為9.60 mm),通過對比不同距離的仿真結果,判斷電極位置對顱內及腫瘤電場分布的影響。按照電學理論估計,距離腫瘤距離越近,電流密度越大,產生的電場強度也越大,所以在研究電極數量的影響時,選擇距離腫瘤最近的一對標準電極和相同位置附近的三對標準電極對比。由于電極數量的增加,為保證整體電流相等,每對電極電流大小變為一對標準電極的三分之一,在仿真時,一對標準電極的電流密度設置為150 A/m2,三對標準電極的電流密度為50 A/m2。在研究電極大小對顱內及腫瘤電場分布的影響時,將距離腫瘤最近的一對標準電極的面積增加三倍,為保持電流大小不變,大電極電流密度同樣為標準電極的三分之一,設置為50 A/m2。三對電極和大電極對在面積上相等,電流大小也相等,可進一步作對比分析。綜上,以三種電極在不同位置、數量和大小方面對比分析,三種電極前后放置的示意如圖3所示。
 圖3
模型的三種電極示意圖
Figure3.
Three types of electrodes of the model
圖3
模型的三種電極示意圖
Figure3.
Three types of electrodes of the model
2 結果
2.1 組織介電特性對腫瘤電場治療場分布的影響
在顳葉腫瘤模型上,由于腫瘤位置相對靠中,分析顱內和腫瘤內的電場均采用腫瘤球心坐標所在的X-Y-Z平面。在研究頭皮和頭骨電導率對顱內和腫瘤內電場分布的影響方面,經仿真后計算顱內和腫瘤內的平均電場強度值,如表2所示。區域的平均電場強度在COMSOL軟件中可通過計算該區域所有體素點上的電場強度體積積分平均值來得到,可以反映出組織電特性變化等因素對電場分布的影響程度。通過觀察顱內和腫瘤內不同截面的電場分布以及對比平均電場強度可以看出,隨著頭皮電導率的增大,顱內和腫瘤處的電場強度有小幅度的降低(顱內平均治療場強相對于標準設置下降16.4%,瘤體內平均場強下降21.0%),說明頭皮組織電導率對顱內和腫瘤內電場影響較小。顱骨組織電導率增大,會引起顱內和腫瘤的電場強度小幅度地降低(顱內平均治療場強相對于標準設置下降2.1%,瘤體內平均場強下降2.6%),這和頭皮組織電導率變化引起的電場變化趨勢一致,其原因為顱骨組織電導率增大,會減少顱內和腫瘤的電流密度,進而影響相應的誘發電場強度。
腫瘤組織在不同電導率下的仿真分析具體考慮如下幾個方面:腫瘤殼組織電導率分別在0.024、0.240、2.400 S/m條件下進行仿真分析;腫瘤核組織電導率分別在0.100、1.000、10.000 S/m條件下進行仿真分析。計算顱內、腫瘤殼和腫瘤核內平均電場強度,如表3所示。顱內平均電場強度變化隨腫瘤各組織電導率變化較小(顱內平均治療場強相對于標準設置最高變化1.1%),主要原因為腫瘤的體積相對較小,腫瘤殼和腫瘤核的組織電導率增大導致腫瘤內部的平均電場強度減小。同時腫瘤核組織電導率增大,對于腫瘤殼整體平均電場強度影響較小,而增大腫瘤殼組織電導率會使得腫瘤殼內平均電場強度減小,其原因和電導率改變引起附近電流密度的改變有關。
介電常數對顱內和腫瘤內電場分布的仿真分析應考慮,不同組織在正常介電常數和介電常數全為1的條件下,仿真結果差異較小,計算腫瘤的平均電場強度分別為27.271 V/m和27.274 V/m,顱內平均電場強度分別為:15.219 V/m和15.379 V/m,此結果也進一步驗證先前假設。
2.2 電極位置、數量和大小對腫瘤電場治療場分布的影響
在顳葉腫瘤模型上,分別通過左右和前后位置的電極施加電場,顱內和腫瘤電場分布仿真結果如圖4所示。從電場分布圖可以看出,顱內較大的電場強度集中分布在電極附近;腫瘤內較大電場的方向和電極方向一致;腫瘤距離電極位置越遠,內部電場強度越低。計算顱內、腦脊液和腫瘤的平均電場強度值,如表4所示。顱內平均電場強度在左右電極組合下大于前后電極組合的情況,腦脊液中的電場強度在前后電極下大于左右電極的情況,原因為前后電極距離較遠,更多的電流分布在導電性更好的腦脊液中,導致顱內電場強度降低。由于腫瘤距離左右電極較近,內部電場強度遠大于前后電極產生的電場強度。
 圖4
前后電極組合和左右電極組合在顱內及腫瘤內產生的電場分布
Figure4.
The electric fields distribution generated by the anterior-posterior electrode and the right-left electrode in the intracranial and intratumoral regions
圖4
前后電極組合和左右電極組合在顱內及腫瘤內產生的電場分布
Figure4.
The electric fields distribution generated by the anterior-posterior electrode and the right-left electrode in the intracranial and intratumoral regions
不同電極數量和大小對顱內和腫瘤內電場分布的仿真分析如下:大電極、一對標準電極和三對標準電極在顳葉區域施加電場時,在顱內灰質表面的電場分布如圖5所示。圖5中一對標準電極產生的高場強(對應圖中深紅色區域)的區域面積最大,其次是大電極,三對標準電極產生的高場強區域面積最小。圖5中,較強電場(對應圖5中淡青色區域)的區域以三對標準電極產生的范圍最大。分別計算顱內和腫瘤內的平均電場強度值,如表5所示。顱內和腫瘤內電場都呈現出一對標準電極產生最大的場強、大電極其次、三對標準電極產生的場強最小的結果,也與計算的顱內和腫瘤內平均電場強度值的情況相符。三種電極在顱內和腫瘤內產生的電場有所不同,其原因是電極法向電流密度和頭部接觸面存在差異,電極面積越大,接觸面的曲面角度越大,法向電流在顱內的矢量抵消也就越多,所以大電極和三對標準電極在顱內和腫瘤內產生的電場強度要小于一對標準電極產生的電場強度。如圖6所示,大電極相對于三對標準電極的放置的整體接觸面更加平整,法向電流密度矢量抵消的少,同時距離腫瘤更近,所以在顱內和腫瘤內的電場強度方面,大電極略大于三對標準電極。
 圖5
不同電極組合在顱內產生的電場分布
Figure5.
Electric field distribution generated by different electrode montages
圖5
不同電極組合在顱內產生的電場分布
Figure5.
Electric field distribution generated by different electrode montages
 圖6
大電極和三對標準電極與腫瘤的空間位置
Figure6.
Spatial location of large electrodes and three pairs of standard electrodes in the temporal lobe and tumors
圖6
大電極和三對標準電極與腫瘤的空間位置
Figure6.
Spatial location of large electrodes and three pairs of standard electrodes in the temporal lobe and tumors
3 討論
在腫瘤電場治療的科學研究和臨床應用中,建模仿真的分析方法發揮著重要作用,是不可缺少的環節。然而在針對腫瘤電場治療的建模和仿真的相關研究中,存在著不少問題。在構建仿真模型方面,國外相關研究已構建較高精度的仿真模型,但其所報道的技術路線不能很好地適配不同的用戶場景,如在建模中使用專業的組織分割和處理軟件Mimics對影像學數據直接處理[31],或者在生成有限元網格時直接利用 ScanIP軟件進行操作,相關軟件使用成本較高,對于沒有軟件資源的研究團隊而言,難以開展類似相關工作[32]。因此,本研究基于頭部磁共振影像數據進行組織分割和三維重建,利用常用的軟件資源對模型進行修飾和完善,添加模擬腫瘤和電極,確定計算仿真的電學條件,最終得到能直接計算的有限元網格模型。
此外,已有的腫瘤電場治療仿真研究仍不夠系統,大多基于單一的應用方案,缺少其他類型的仿真分析,因此需要進一步探索不同組織電學特性,包括電極位置、數量和大小等參數對仿真結果的影響。本研究利用前面已建立的仿真方法,對構建的含有顳葉腫瘤的頭部仿真模型進行仿真分析,首先分析了不同組織的電學參數對顱內和腫瘤內電場分布的影響;其次研究了不同電極位置、數量和大小對顱內和腫瘤內電場分布的影響。不同電學參數的對比研究包含頭皮、顱骨和腫瘤三種組織的電導率變化,以及所有頭部組織的介電常數變化。從仿真結果上可以看出,頭皮組織的電導率增加,對顱內和腫瘤內的電場分布影響不大,平均電場強度分別下降了16.4%和21.0%;顱骨的電導率增大對電場分布影響很小,顱內和腫瘤內的平均電場強度分別只下降了2.1%和2.6%;腫瘤組織本身電導率的變化會顯著改變其內部電場強度,所以確定腫瘤電場治療頻段下腫瘤組織的電導率參數對仿真結果的準確程度至關重要。在腫瘤電場治療中,組織的介電常數參數對于顱內和腫瘤內電場分布幾乎沒有影響,在相關的研究和實驗中,可以忽略掉該參數。在對電極位置、數量和大小進行仿真分析的結果表明,電極位置距離腫瘤越近,腫瘤內部電場越強;在相同電流條件下,一對標準電極在顱內和腫瘤內產生的電場較強,大電極和多數量的電極由于接觸面較一對標準電極存在較大曲度,注入頭部的法向電流密度存在矢量抵消,產生的電場會略小。因此在腫瘤治療過程中使用數量較少的小電極可以更容易在顱內腫瘤處產生更大的刺激場強。
在構建高精度頭部仿真模型和仿真研究工作中,仍有一些亟待改善的方面。首先,構建高精度頭部仿真模型時需要使用的軟件較多,各步驟銜接不夠流暢,模型優化操作繁瑣,并且在生成有限元網格時容易出現錯誤,整體過程耗時較長、工作量大,需要更加簡便快捷的構建方法,例如在分割組織后生成可直接用于計算的有限元網格、更加便捷的放置電極操作等。其次,實際情況下不同腫瘤的大小、形狀等性質差異較大,電導率、相對介電常數的分布個體差異也比較明顯,因此需要綜合臨床數據建立一個更加符合實際腫瘤特性的腫瘤仿真模型。在實際應用中,電極發熱控制也是一項重要的設計原則,電極功率高、發熱大,會造成嚴重的皮膚不良反應,但在對頭部腫瘤模型進行仿真研究中,未考慮施加電場的功率和發熱問題。同時,本次仿真研究未和實際應用廠家的電極放置方式作對比,也缺少增加顱內和腫瘤內電場強度的方法仿真研究,如顱骨摘除術等。
4 結論
腫瘤電場治療作為一種前景廣闊的無創腫瘤治療方式,已廣泛應用在科研和臨床中,其中腫瘤電場治療的仿真分析是個體量效評估和方案優化的重要一環。本研究建立了一套易實現的腫瘤電場治療仿真模型構建方法,并基于該仿真模型開展了不同組織電學參數、電極大小和數量差異等因素的理論分析,探究了這些因素對顱內和腫瘤內電場分布的影響,發現腫瘤自身介電特性與電極位置是影響其治療場分布的重要因素,同時驗證了所提出建模方法的可行性和有效性。
重要聲明
利益沖突:本文全體作者均聲明不存在利益沖突。
作者貢獻說明:秦麗平、謝旭、馬明偉負責仿真分析、數據整理與論文撰寫,潘赟、陳光弟、張韶岷指導數據分析及論文撰寫,王敏敏指導課題實施、數據分析及論文撰寫。