引用本文: 楊磊, 牟德武, 楊宏偉, 陳茂山. 初診單純骨轉移乳腺癌局部手術獲益預測模型的構建與驗證:基于 SEER 數據庫的回顧性研究. 華西醫學, 2024, 39(5): 754-762. doi: 10.7507/1002-0179.202309139 復制
版權信息: ?四川大學華西醫院華西期刊社《華西醫學》版權所有,未經授權不得轉載、改編
初診Ⅳ期乳腺癌(de novo metastatic breast cancer, dnMBC)在所有新診乳腺癌中的占比為 6%~10%,是一種不可治愈性疾病,預后差,中位生存期為 18~24 個月,5 年生存率僅為 16%~20%[1-2]。隨著對乳腺癌腫瘤生物學行為的深入研究及現代醫學診療手段的不斷進步,基于個體化的分類治療策略已顯著改善 dnMBC 患者的預后[3-4]。全身治療是 dnMBC 的主要治療方式,原發灶手術能否改善該類患者的遠期生存尚存較大爭議[5]。多項臨床研究探索了乳房原發腫瘤外科手術對 dnMBC 患者預后的價值,但未能給臨床診療提供一致的結論[6-8]。多數學者認為,腫瘤生物學良好、轉移負荷低的 dnMBC 患者是局部手術的潛在獲益人群,其中單純骨轉移乳腺癌(bone-only metastatic breast cancer, bMBC)常被認為可通過局部手術改善預后[5, 9]。然而,部分骨轉移乳腺癌的腫瘤惡性程度高、進展快、預后差,并非所有 bMBC 患者均能從局部手術治療中獲益[10]。因此,對 bMBC 患者進行準確的預后評估,篩選出能從局部手術治療獲益的人群具有重要的臨床意義。美國癌癥監測、流行病學和最終結果(the Surveillance, Epidemiology and End Results, SEER)數據庫登記了涵蓋約 28% 美國人口的癌癥數據,為大樣本的真實世界研究提供可能[11]。本研究使用 SEER 數據庫中 bMBC 病例資料,回顧性分析局部手術對預后的價值,通過分析獨立預后因素并構建預后預測模型,根據預后預測模型將患者進行預后風險分層,分析不同風險患者局部手術的獲益情況。
1 資料與方法
1.1 研究設計
本研究為回顧性隊列研究,遵照《加強流行病學中觀察性研究報告質量(STROBE)指南》[12]進行實施和報告。本研究通過遂寧市中心醫院科研倫理委員會審批(編號:LLSLH20220067),因使用公共免費開放數據庫數據,不涉及患者隱私及利益,經倫理委員會申請豁免了知情同意。
1.2 資料來源
使用 SEER*Stat(8.4.0 版)提取美國 SEER 數據庫中符合本研究納入標準的病例數據。納入標準:① 診斷年份為 2010 年—2019 年;② 病理組織確診為浸潤性乳腺癌;③ 性別女;④ 確診年齡 18~70 歲;⑤ 合并骨轉移;⑥ 隨訪信息完整。排除標準:① 合并腦、肺或肝等其他部位轉移;② 多源性腫瘤;③ 炎性乳腺癌;④ 手術方式信息缺失;⑤ T3 期、T4 期及 T 分期不明確;⑥ 重要信息缺失。
1.3 研究指標
提取所有患者的診斷年份、診斷年齡、種族、手術信息、腫瘤 TNM 分期、組織學分級、病理類型、分子分型、放療、化療、轉移部位、雌激素受體(estrogen receptor, ER)狀態、孕激素受體(progesterone receptor, PR)狀態、人表皮生長因子受體 2(human epidermal growth factor receptor-2, HER2)狀態、生存時間及生存結局等資料。采用美國癌癥聯合會乳腺癌 TNM 分期系統(第 8 版)對患者進行腫瘤分期[13],將患者腋窩淋巴結狀態劃分為淋巴結陰性和陽性 2 種狀態。病理類型劃分為浸潤性導管癌、浸潤性小葉癌和其他類型 3 類。根據患者診斷時年齡劃分為 18~55 歲和 56~70 歲 2 組。
1.4 結局指標
本研究的生存終點為總生存,定義為從確診乳腺癌至因任何原因死亡的時間間隔,失訪病例作為刪失數據。
1.5 統計學方法
根據患者是否接受局部手術劃分為手術組與未手術組,以 7∶3 比例將所有病例隨機分為訓練集與驗證集。基礎特征中的數值變量轉換為分類變量,采用例數和/或百分率進行統計描述,組間對比采用 χ2 檢驗。隨訪時長以中位數(下四分位數,上四分位數)進行統計描述。采用 Kaplan-Meier 法繪制生存曲線,對數秩檢驗比較生存率。采用單因素和多因素 Cox 比例風險模型進行預后因素分析并計算風險比(hazard ratio, HR)及對應的 95% 置信區間(confidence interval, CI),單因素分析 P<0.05 或臨床評估有意義的變量進入多因素模型。采用向后法構建預后預測模型,采用時間依賴的臨床受試者操作特征(receiver operating characteristic, ROC)曲線及曲線下面積(area under the curve, AUC)、校準曲線、決策曲線分析(decision curve analysis, DCA)分別在訓練集和驗證集評價模型的區分度、校準度和臨床適用度。根據預測模型計算患者預后風險得分,采用 X-tile 軟件將患者劃分為低、中、高風險組,使用生存分析在不同風險亞組患者中比較手術和未手術患者的生存差異。所有統計分析及作圖使用 R 4.0.3 軟件完成。雙側檢驗水準 α=0.05。
2 結果
2.1 患者臨床病理學特征
經篩選,共
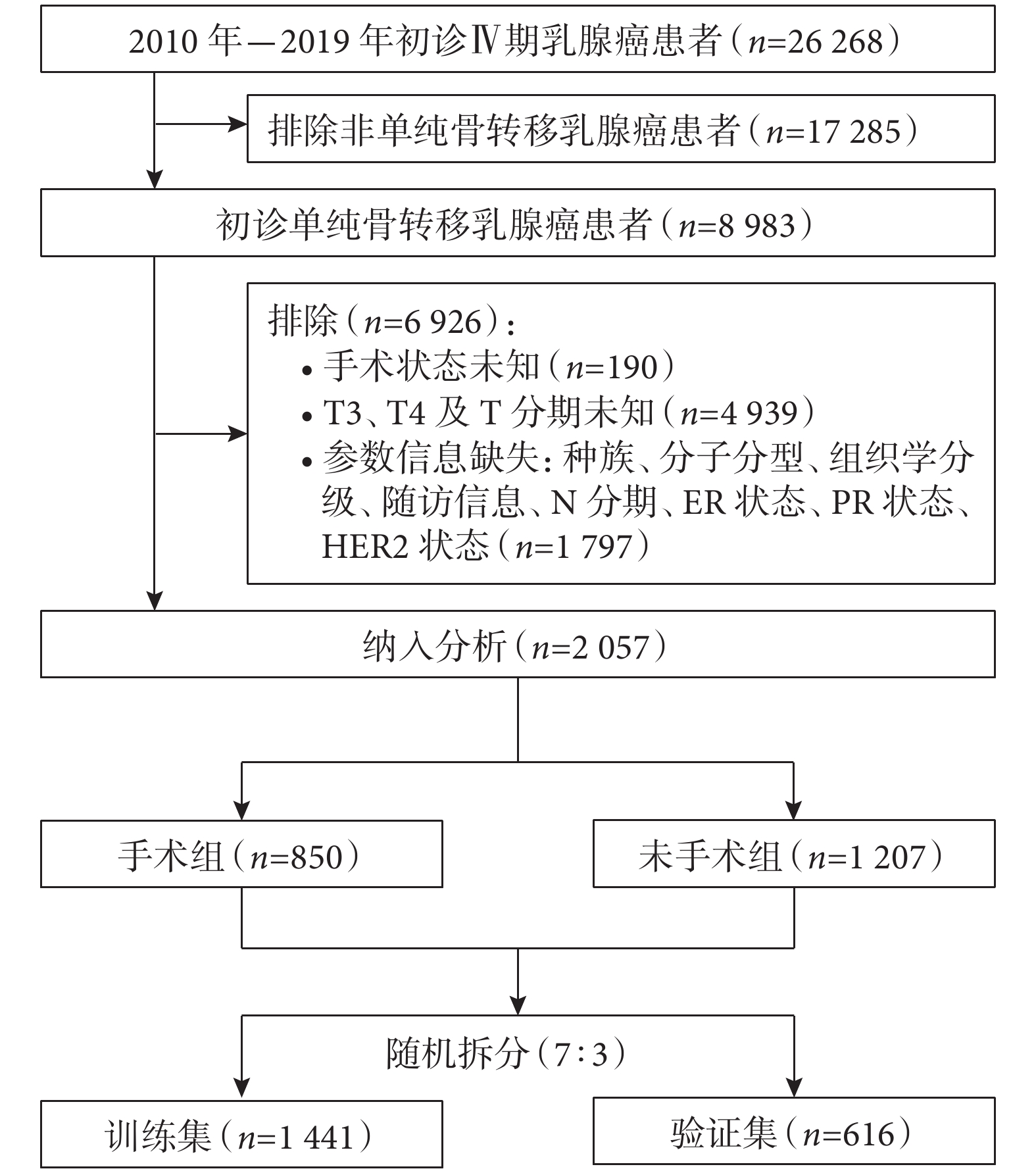
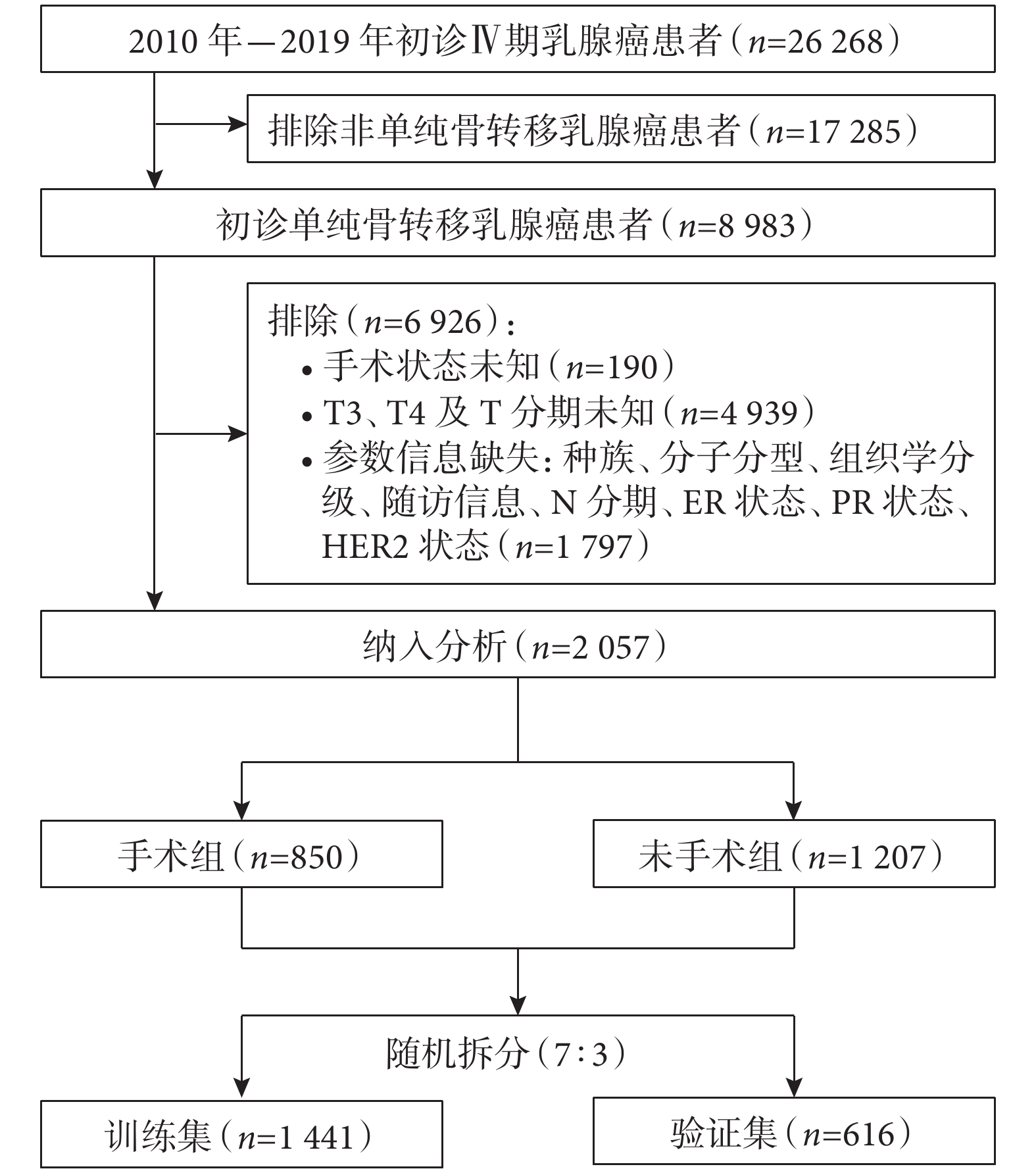 圖1
病例篩選流程圖
圖1
病例篩選流程圖
ER:雌激素受體;PR:孕激素受體;HER2:人表皮生長因子受體 2
2.2 生存分析
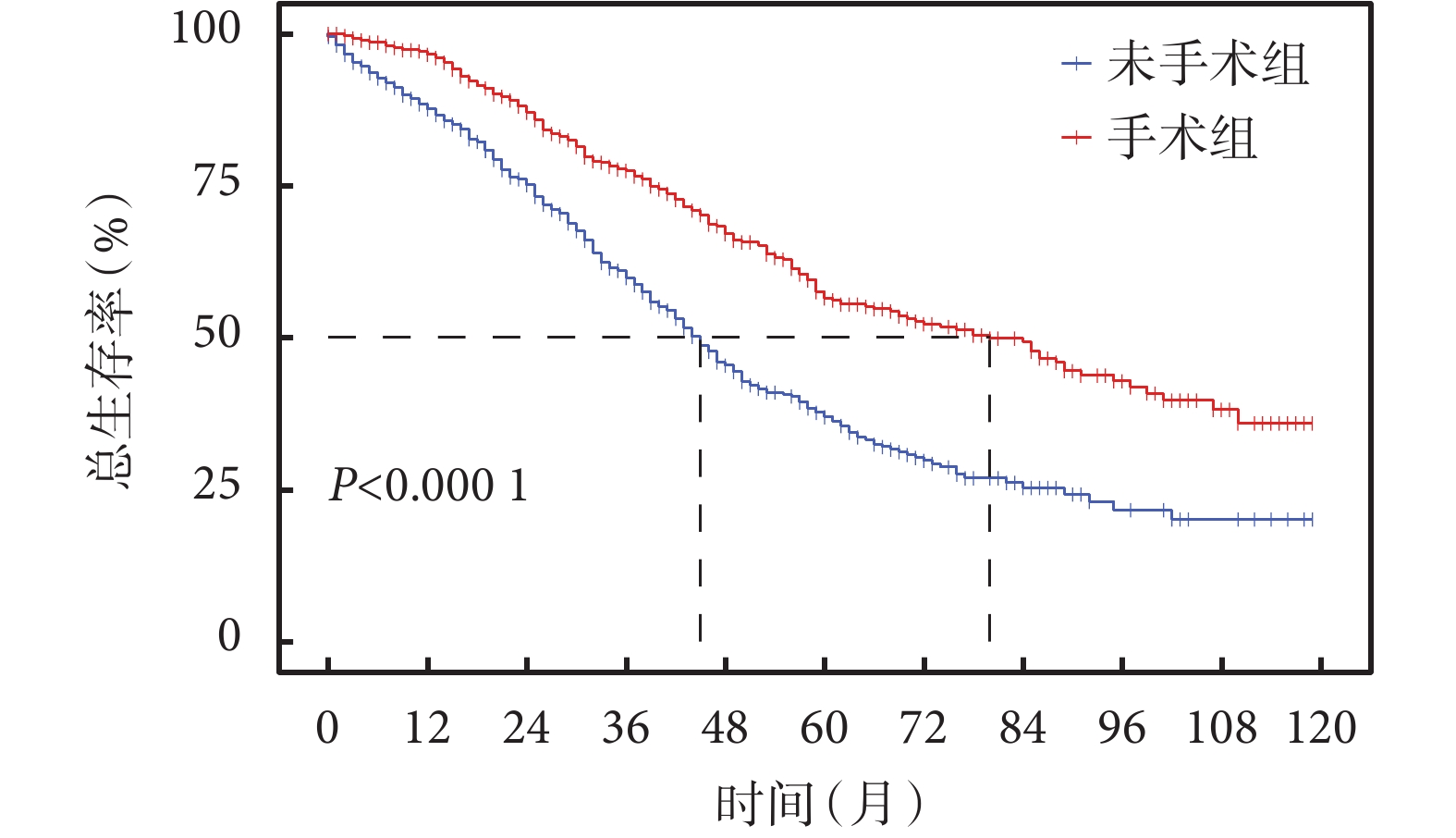
總人群中位隨訪時間 32(16,53)個月,發生死亡 865 例(42.1%),其中手術組 322 例(37.9%),未手術組 543 例(44.9%)。生存分析顯示訓練集手術組患者的總生存優于未手術組患者(P<0.001),見圖2。在訓練集中行單因素 Cox 回歸分析,結果顯示手術、年齡、種族、婚姻狀態、分子分型、組織學分級、ER 狀態、PR 狀態、HER2 狀態及化療與患者總生存相關(P<0.05),T 分期、腋窩淋巴結狀態、病理類型及放療與患者總生存未見相關性(P>0.05),見表2。將單因素分析 P<0.05 相關因素及病理類型納入多因素 Cox 回歸分析(因 ER 狀態、PR 狀態及 HER2 狀態與分子分型變量效應重疊,僅將分子分型納入模型),多因素 Cox 回歸模型分析結果顯示手術可改善 bMBC 患者的總生存[HR=0.51,95%CI(0.43,0.60),P<0.001],此外化療、婚姻狀態、分子分型、年齡、組織學分級及病理類型與總生存獨立相關(P<0.05),種族與總生存未見相關性(P>0.05),見表2。
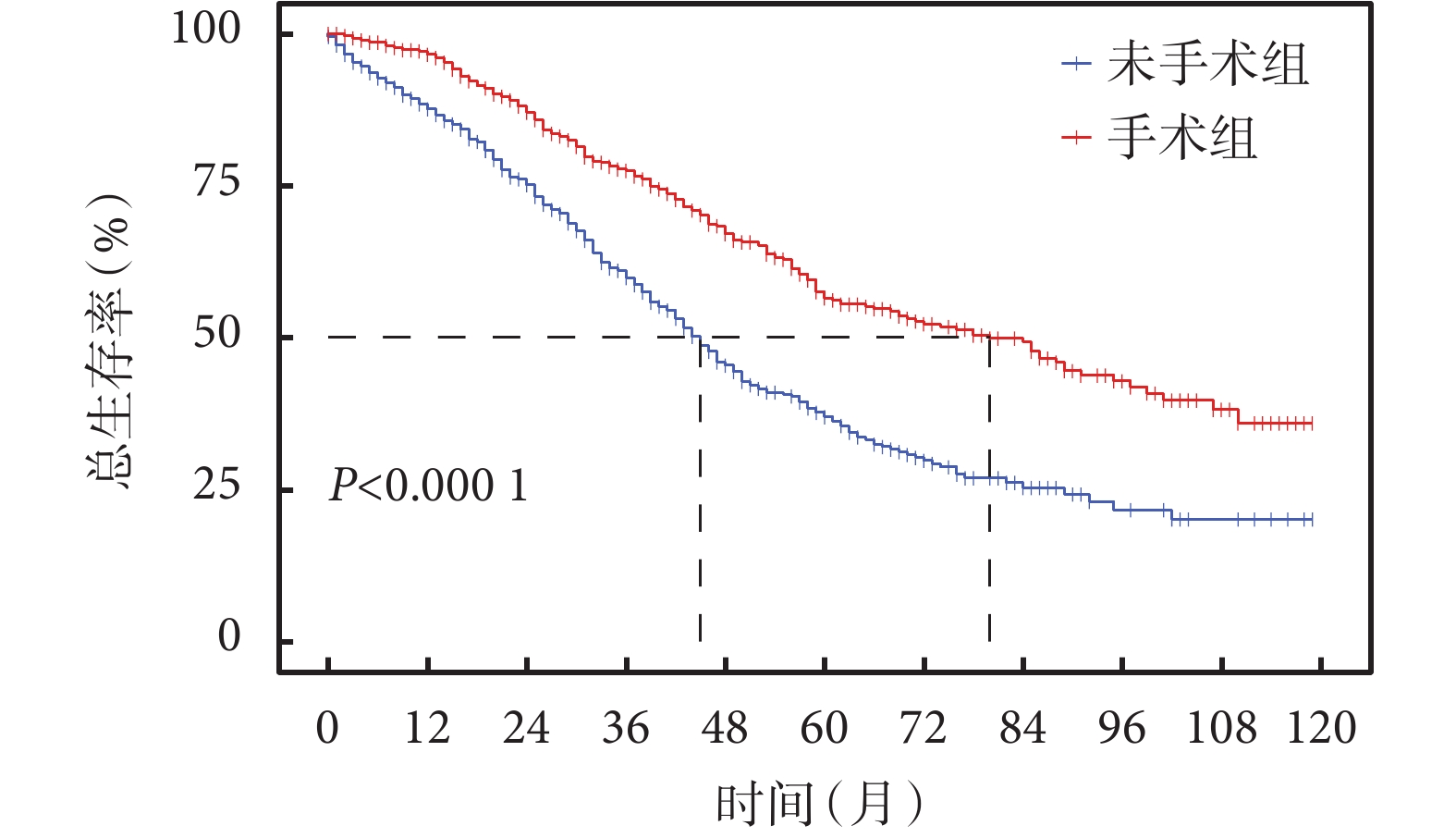 圖2
訓練集手術與未手術患者總生存的生存曲線
圖2
訓練集手術與未手術患者總生存的生存曲線
2.3 預后預測模型構建與驗證
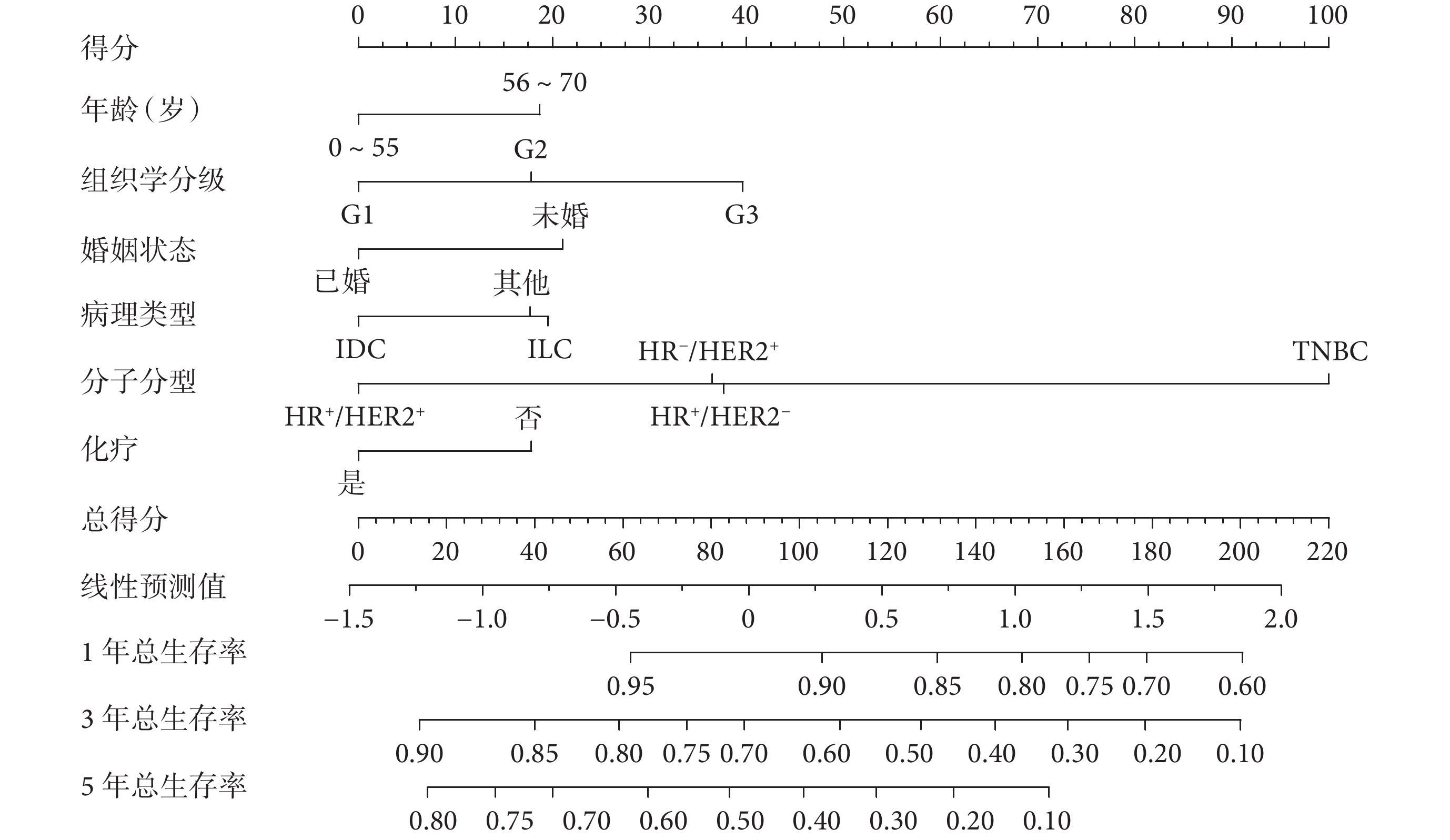
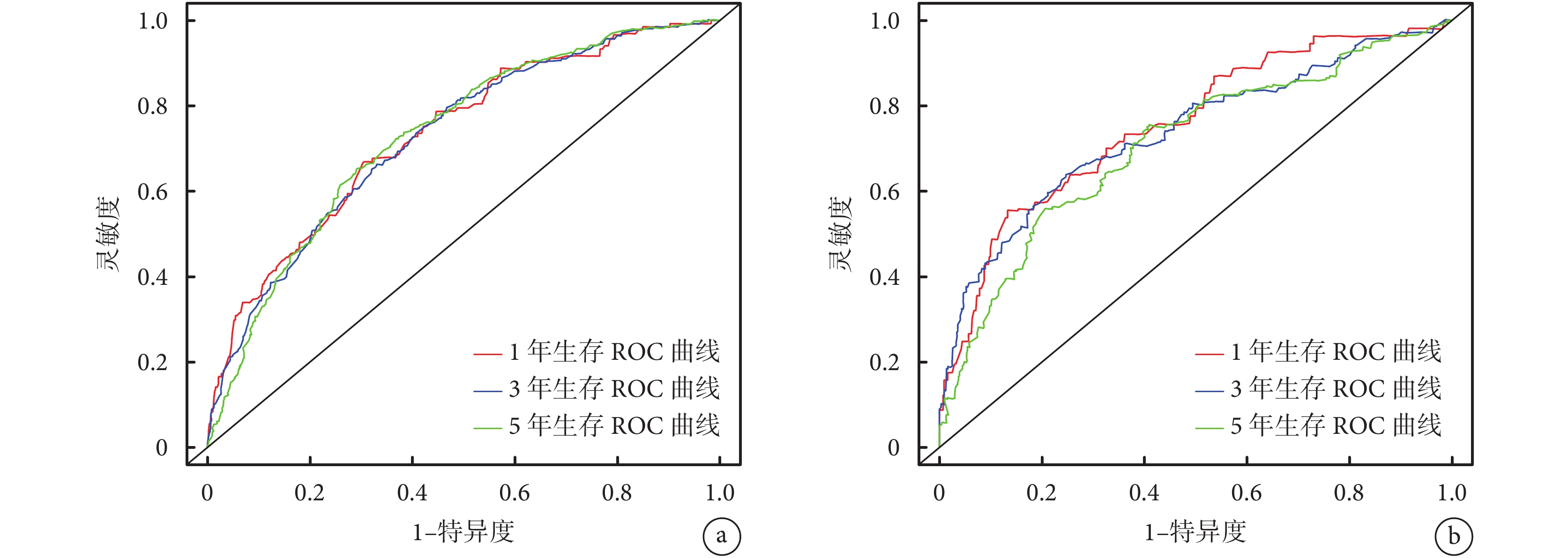
在訓練集中將單因素 Cox 回歸分析 P<0.05 及病理類型(未納入變量“手術”)采用向后法篩選變量并構建預后預測模型,最終化療、婚姻狀態、分子分型、年齡、病理類型及組織學分級 6 個變量被納入預后預測模型。通過該模型計算訓練集中所有患者 1、3、5 年總生存率并構建預后預測模型列線圖,見圖3。訓練集和驗證集的 C-index 分別為 0.702[95%CI(0.677,0.725)]和 0.703[95%CI(0.66,0.73)];訓練集 1、3、5 年 AUC 分別為 0.734、0.727、0.731(圖4a),驗證集 1、3、5 年 AUC 分別為 0.755、0.737、0.708(圖4b),提示模型有較好的區分度。構建訓練集及驗證集 1、3、5 年校準曲線,結果均顯示預測生存率與實際生存率高度吻合(圖5)。DCA 曲線顯示模型具有一定臨床適用性(圖6)。
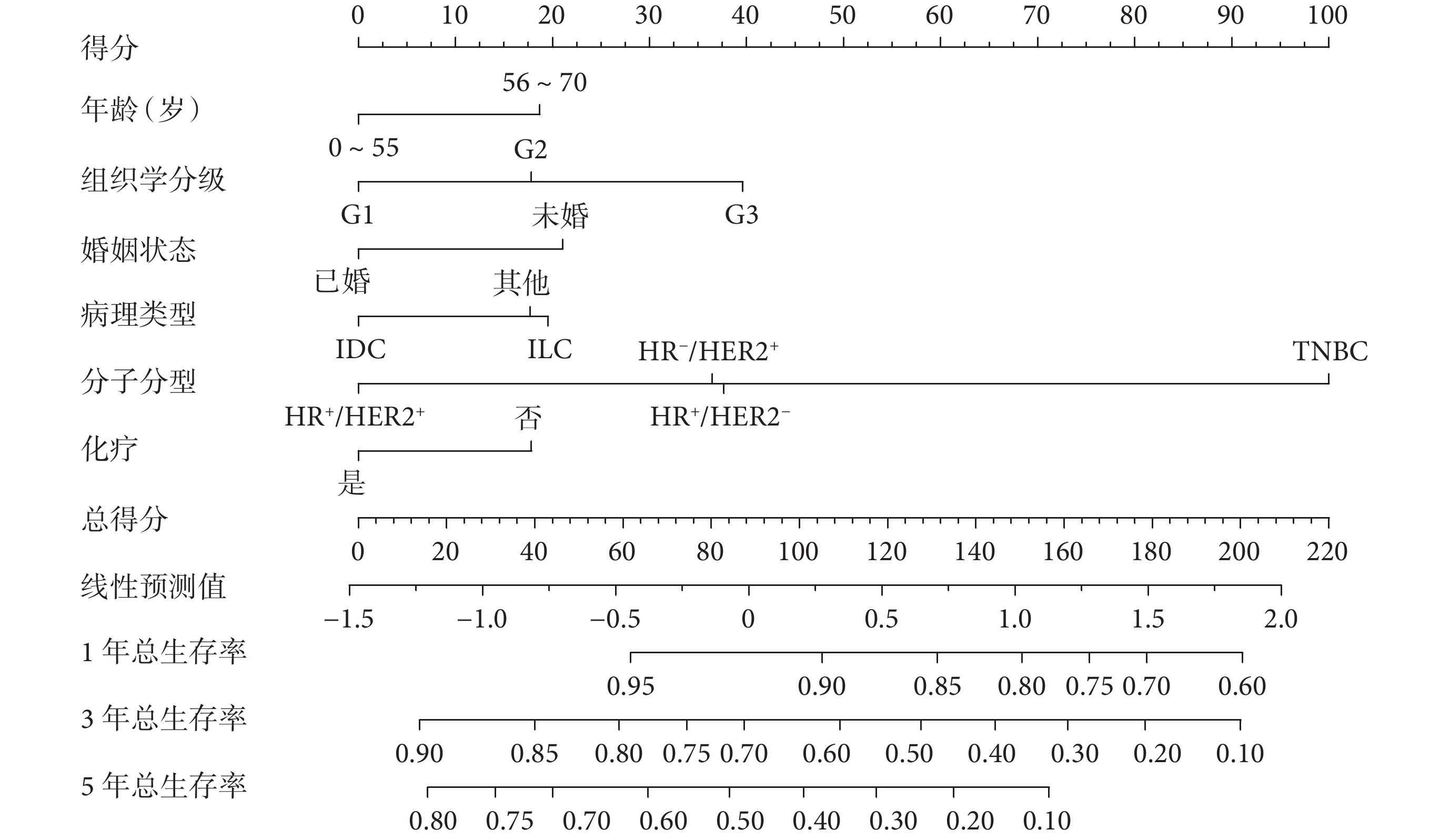 圖3
初診單純骨轉移乳腺癌患者預后列線圖
圖3
初診單純骨轉移乳腺癌患者預后列線圖
IDC:浸潤性導管癌;ILC:浸潤性小葉癌;HR:激素受體;HER2:人表皮生長因子受體 2;TNBC:三陰乳腺癌
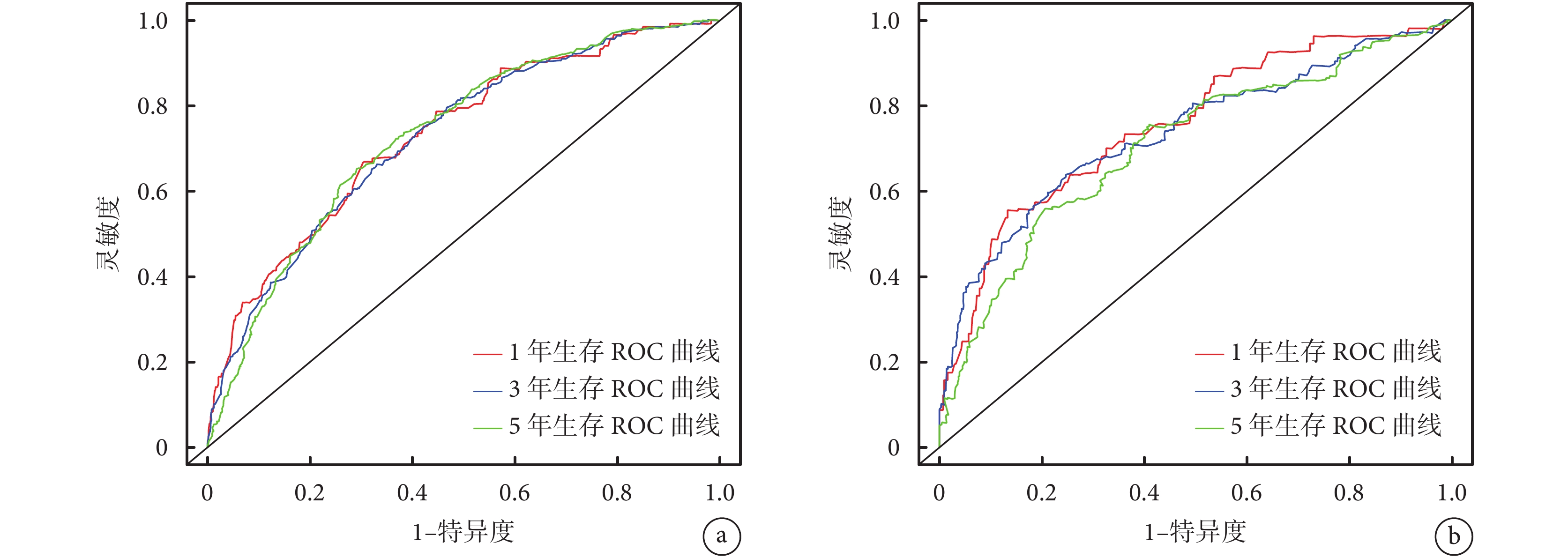 圖4
訓練集與驗證集中預后模型預測 1、3、5 年總生存率的 ROC 曲線
圖4
訓練集與驗證集中預后模型預測 1、3、5 年總生存率的 ROC 曲線
a. 訓練集;b. 驗證集。ROC:受試者操作特征
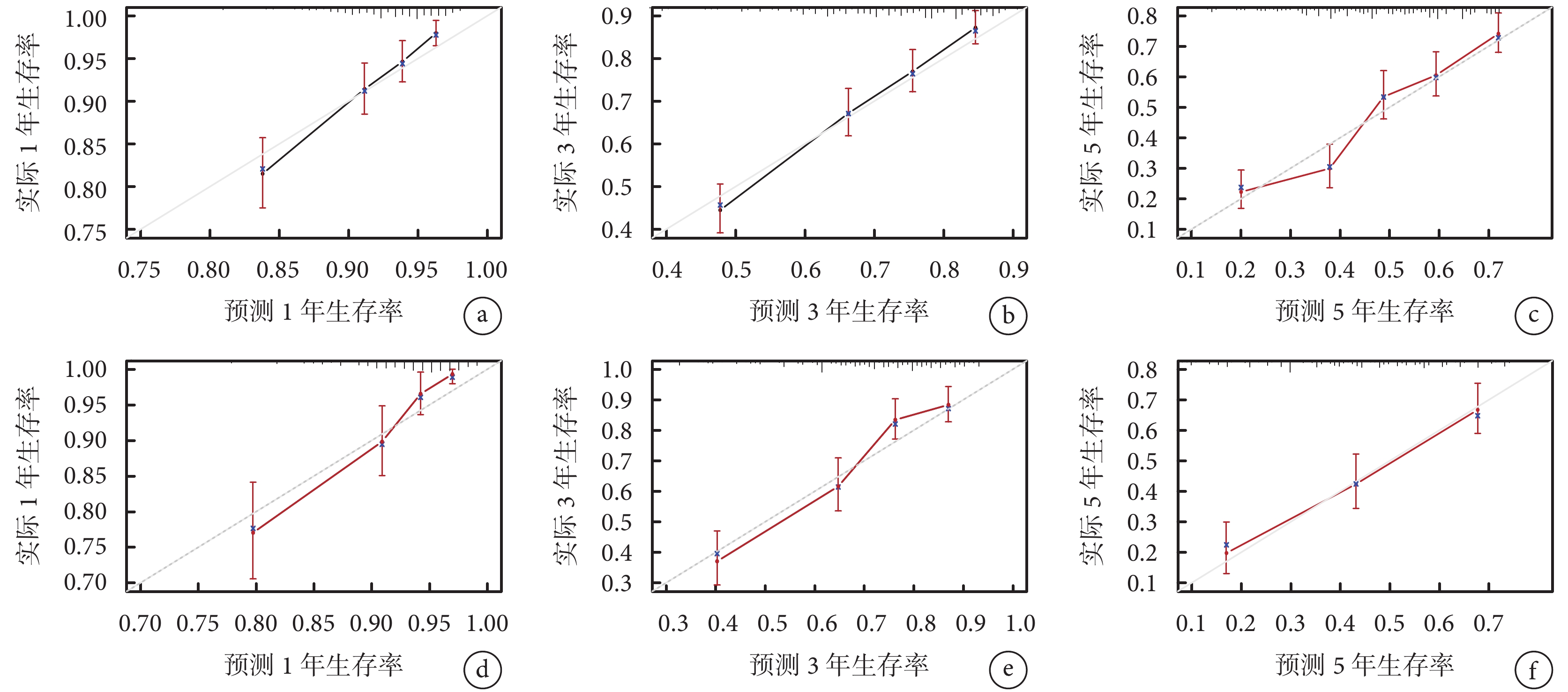 圖5
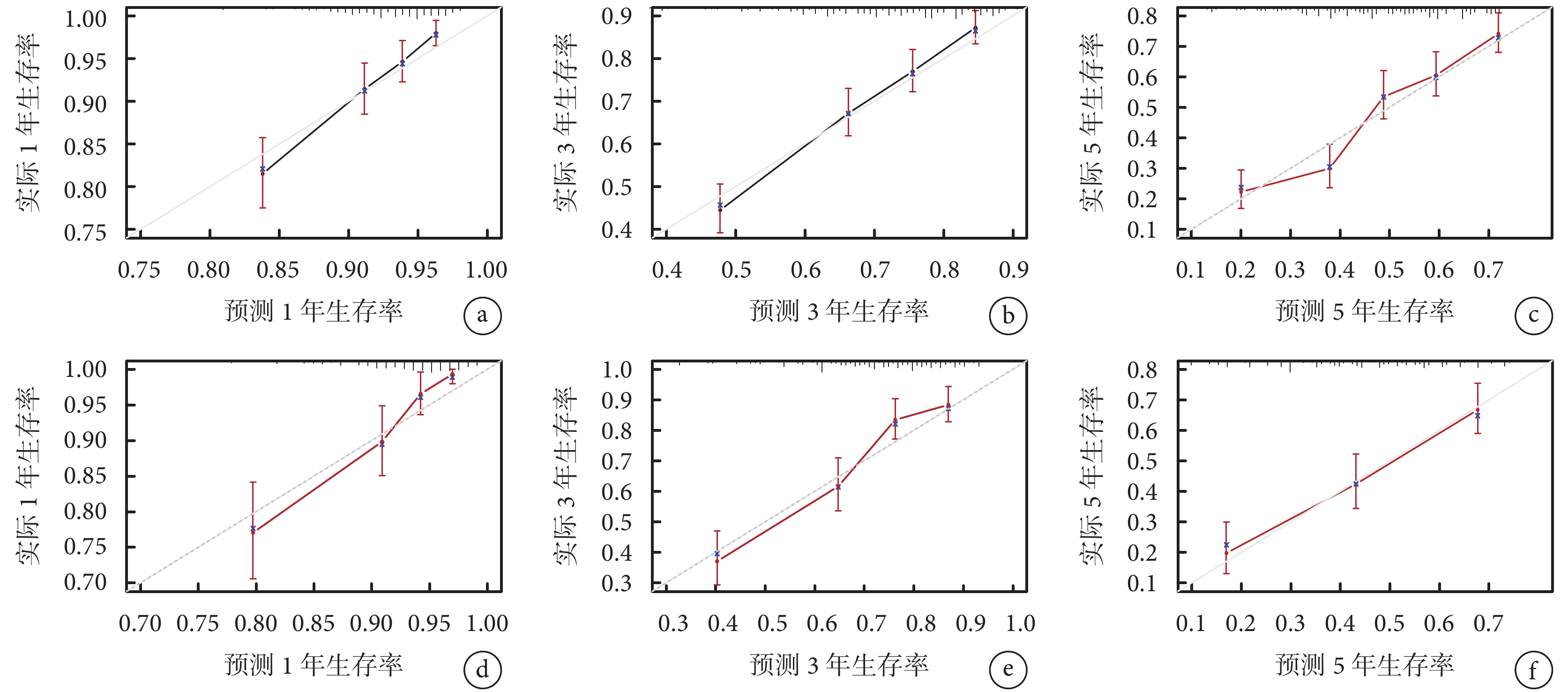
訓練集與驗證集中預后模型預測 1、3、5 年總生存率的校準曲線
圖5
訓練集與驗證集中預后模型預測 1、3、5 年總生存率的校準曲線
a~c. 訓練集 1、3、5 年總生存率的校準曲線;d~f. 驗證集 1、3、5 年總生存率的校準曲線
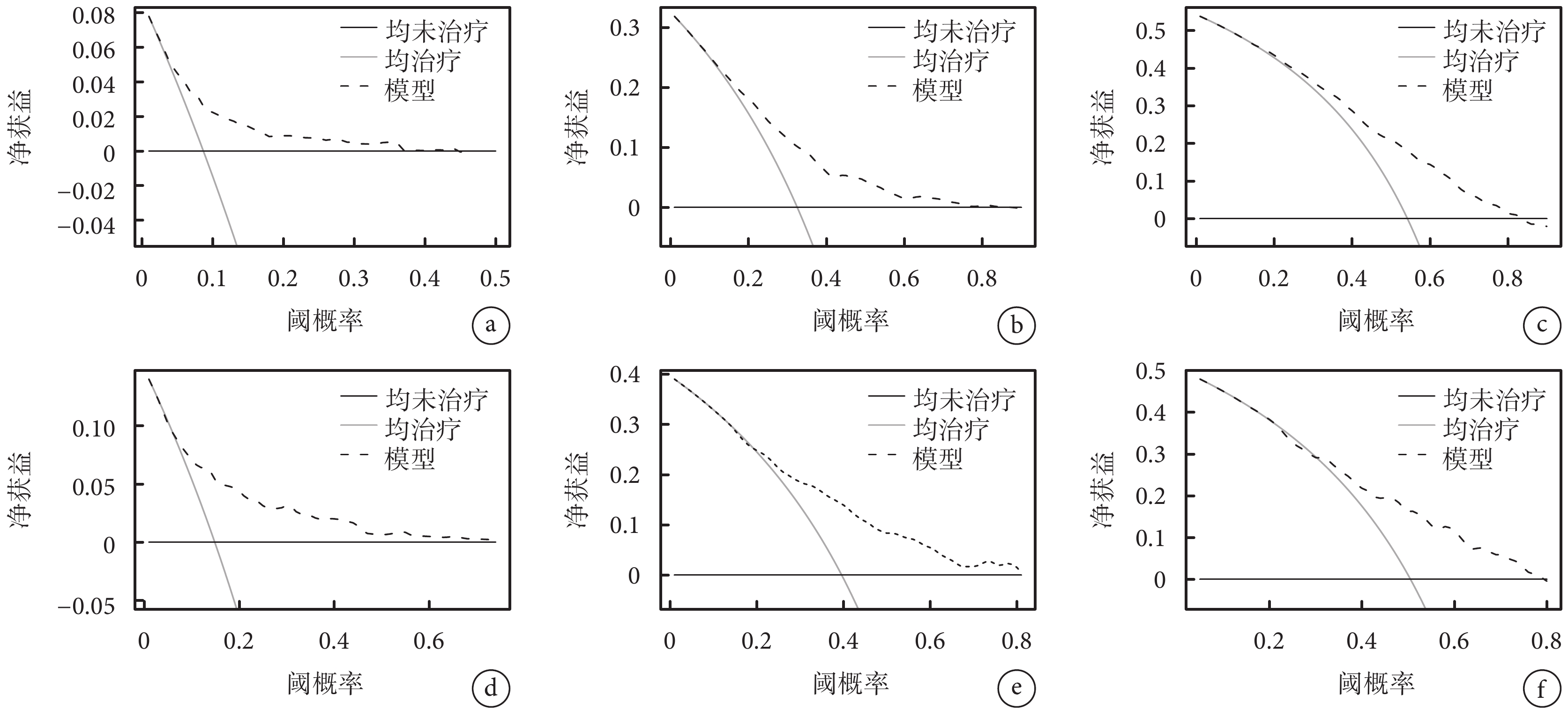 圖6
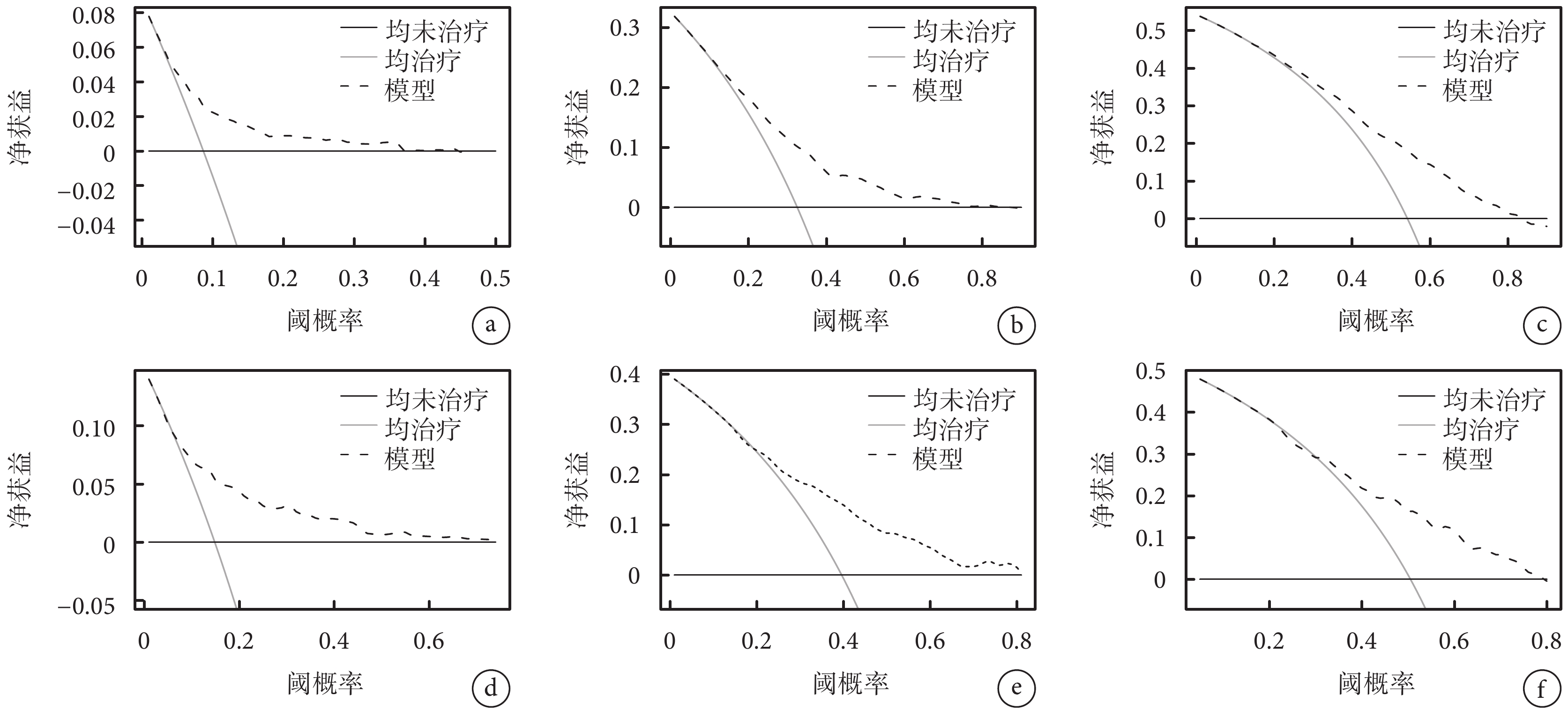
訓練集與驗證集中預后模型 1、3、5 年臨床決策曲線
圖6
訓練集與驗證集中預后模型 1、3、5 年臨床決策曲線
a~c. 訓練集 1、3、5 年臨床決策曲線;d~f. 驗證集 1、3、5 年臨床決策曲線
2.4 風險分層及手術獲益分析
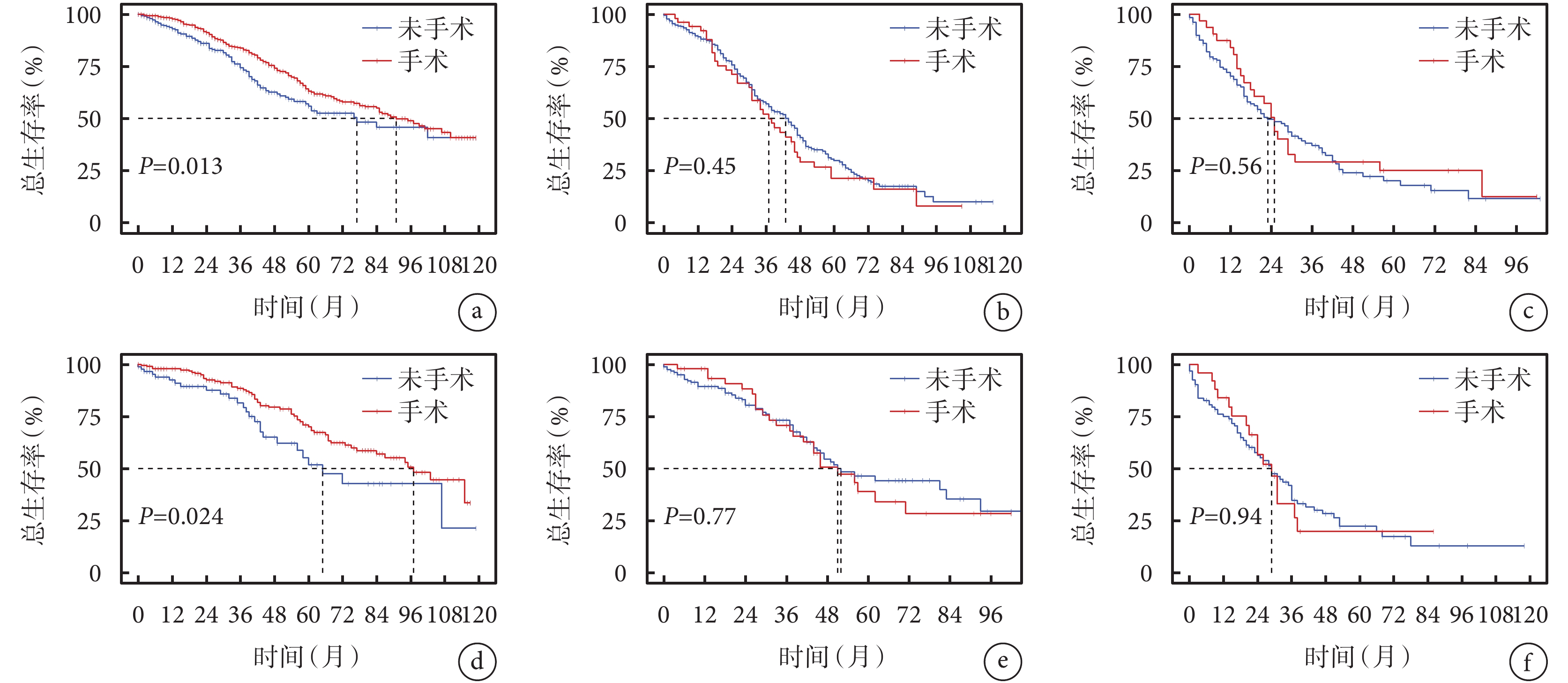
利用預后預測模型計算訓練集與驗證集中每例患者的預后風險預測評分。使用 X-tile 軟件根據訓練集風險預測評分將患者劃分為低風險組(<70 分)、中風險組(70~160 分)和高風險組(>160 分),生存分析對數秩檢驗結果顯示,局部手術改善低風險患者的總生存(訓練集:P=0.013;驗證集:P=0.024),不改善中、高風險患者的總生存(訓練集中風險組:P=0.45;訓練集高風險組:P=0.56;驗證集中風險組:P=0.77;驗證集高風險組:P=0.94)。見圖7。
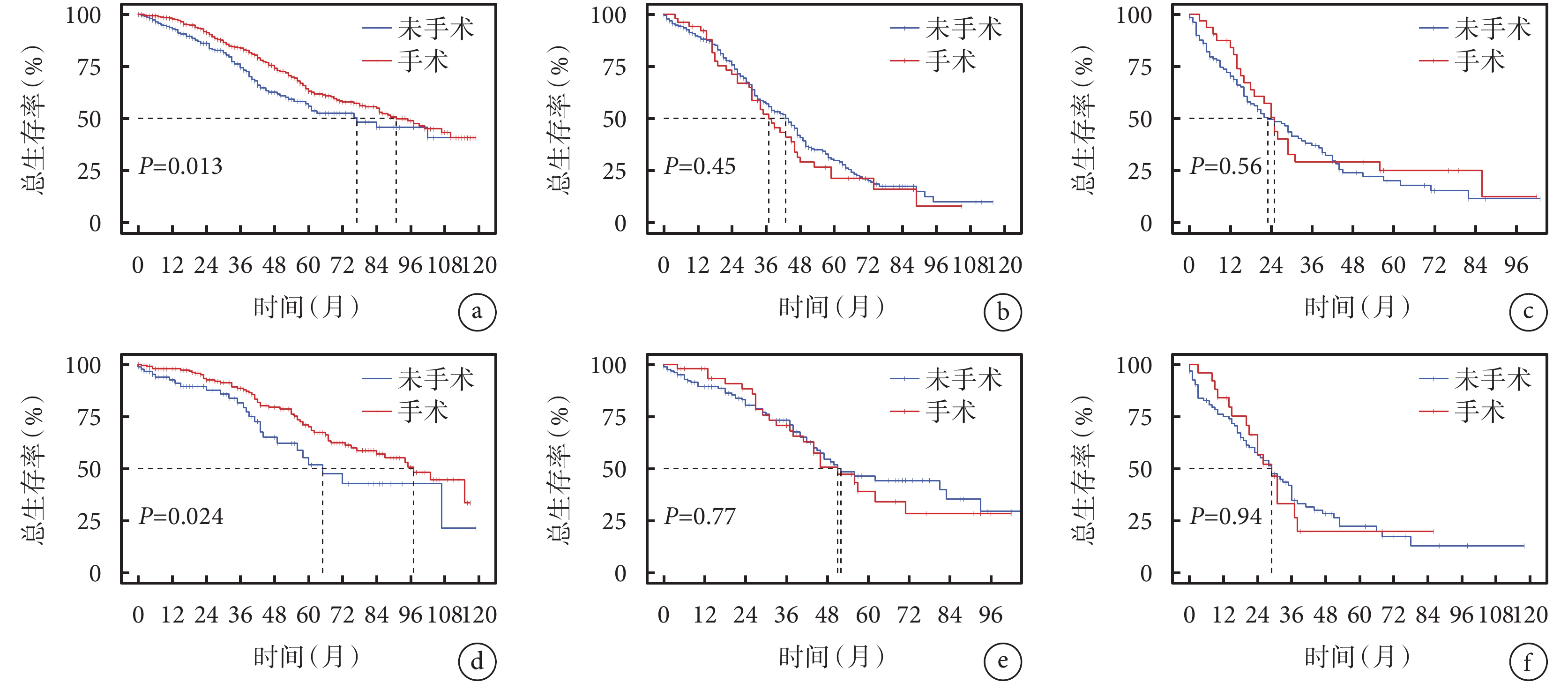 圖7
訓練集和驗證集中手術在低、中、高風險組中的生存獲益
圖7
訓練集和驗證集中手術在低、中、高風險組中的生存獲益
a~c. 訓練集中手術在低、中、高風險組中的生存獲益;d~f. 驗證集中手術在低、中、高風險組中的生存獲益
3 討論
本研究利用 SEER 數據庫病例分析顯示,局部手術可改善初診 bMBC 患者的預后,進一步分析發現手術、化療、婚姻狀態、分子分型、年齡、病理類型及組織學分級與患者的總生存獨立相關。通過構建預后風險預測模型,計算每例患者的預后風險得分并進一步將患者劃分為低、中、高風險組,生存分析顯示局部手術主要改善低風險患者的預后,對中、高風險患者預后的改善作用有限。
局部手術能否改善初診晚期乳腺癌患者預后尚存爭議[6-7, 14-15],Tata 試驗、ABCSG-28 試驗及 ECOG-ACRIN E2108 試驗研究結果均提示手術不能改善 dnMBC 患者預后[6-8]。MF07-01 試驗納入共 274 例 dnMBC 患者,按照 1∶1 隨機分為手術組(n=138)和未手術組(n=136),在中位隨訪 40 個月時發現手術組的死亡風險較未手術組降低了 34%;在其非計劃的亞組分析中發現年輕患者及單純骨轉移患者從局部手術中獲益更大,該研究提示骨轉移患者可能是局部手術的主要獲益人群[16]。另有研究發現部分小腫瘤負荷的乳腺癌患者有從局部手術中獲益的趨勢[17-18],臨床中腫瘤轉移負荷較小的患者也更多被推薦行局部手術治療。骨是乳腺癌最常見的轉移部位[19],bMBC 患者通常較其他轉移部位乳腺癌患者具有更小的腫瘤負荷及更長的預期生存時間,常常被臨床醫師推薦行局部手術[20]。一項納入 187 例初診 bMBC 患者的回顧性研究發現,局部手術患者較未手術患者遠期生存更好[18];另一項針對國內患者的研究同樣發現手術可改善 bMBC 患者預后生存[21]。本研究通過 SEER 數據庫大樣本研究發現手術組較未手術組死亡風險下降了 49%,與 MF07-01 研究結果比較一致。此外,本研究結果提示化療、婚姻狀態、分子分型、年齡、病理類型及組織學分級與總生存具有獨立相關性,這與既往相似研究結果相似[22-24]。在本組數據中,HR+/HER2+亞型患者的預后優于其他亞型,與常規認為 HR+/HER2–患者是預后最好的亞型存在一定差異,這可能與抗 HER2 靶向治療和內分泌治療藥物的不斷發展和應用有著密切關系[25]。曲妥珠單抗是一種抗 HER2 的人源化單克隆抗體,可使 HER2 型晚期乳腺癌患者死亡風險降低約 44%,而在曲妥珠和多西他賽的基礎上加入帕妥珠單抗可進一步降低 HER2 型晚期乳腺癌患者死亡風險[26]。此外,有研究發現抑制 HER2 可以提高內分泌治療的敏感性[27-28]。
初診 bMBC 患者通常較其他轉移部位乳腺癌患者預后更好,目前國內外指南均認為初診 bMBC 患者是局部手術獲益的潛在人群[5, 9],但是否所有 bMBC 患者均可從局部手術中獲益尚存爭議。一項研究亞組分析發現部分預后較差 bMBC 患者并不能從局部手術中改善遠期生存[10],另一項來自國內多中心回顧性研究分析發現分子分型等多種因素與 bMBC 患者預后相關[29],提示初診 bMBC 患者局部手術策略的制定應根據患者臨床病理特征、預期生存時間等進行綜合考慮而進行個體化制定。因此,構建可用于臨床評估患者手術獲益風險模型十分重要。本研究通過對 SEER 數據庫中大樣本數據分析發現手術、化療、婚姻狀態、分子分型、年齡、病理類型及組織學分級與初診 bMBC 患者遠期生存獨立相關,進一步構建手術獲益預測模型并以列線圖進行展示,使用所構建的預測模型預測每例患者的預后風險總得分并將患者劃分為低、中、高風險組,生存分析發現局部手術僅可改善低風險組患者預后,而不改變中、高風險組患者遠期生存,這為臨床醫師手術決策提供了更為準確的信息。
本研究存在以下局限性:① 本研究為真實世界癌癥登記數據庫病例的回顧性研究,不可避免存在一定程度的選擇性偏倚;② 由于數據庫可獲取的數據有限,無法獲得骨轉移灶、內分泌治療及放化療方案的詳細資料,限制了數據更為準確和詳細的分析。盡管存在一定程度的局限性,本研究也可能為部分骨轉移患者臨床決策提供一定的參考,期待更多大樣本前瞻性研究探討局部手術在單純骨轉移患者預后中的價值。
利益沖突:所有作者聲明不存在利益沖突。
初診Ⅳ期乳腺癌(de novo metastatic breast cancer, dnMBC)在所有新診乳腺癌中的占比為 6%~10%,是一種不可治愈性疾病,預后差,中位生存期為 18~24 個月,5 年生存率僅為 16%~20%[1-2]。隨著對乳腺癌腫瘤生物學行為的深入研究及現代醫學診療手段的不斷進步,基于個體化的分類治療策略已顯著改善 dnMBC 患者的預后[3-4]。全身治療是 dnMBC 的主要治療方式,原發灶手術能否改善該類患者的遠期生存尚存較大爭議[5]。多項臨床研究探索了乳房原發腫瘤外科手術對 dnMBC 患者預后的價值,但未能給臨床診療提供一致的結論[6-8]。多數學者認為,腫瘤生物學良好、轉移負荷低的 dnMBC 患者是局部手術的潛在獲益人群,其中單純骨轉移乳腺癌(bone-only metastatic breast cancer, bMBC)常被認為可通過局部手術改善預后[5, 9]。然而,部分骨轉移乳腺癌的腫瘤惡性程度高、進展快、預后差,并非所有 bMBC 患者均能從局部手術治療中獲益[10]。因此,對 bMBC 患者進行準確的預后評估,篩選出能從局部手術治療獲益的人群具有重要的臨床意義。美國癌癥監測、流行病學和最終結果(the Surveillance, Epidemiology and End Results, SEER)數據庫登記了涵蓋約 28% 美國人口的癌癥數據,為大樣本的真實世界研究提供可能[11]。本研究使用 SEER 數據庫中 bMBC 病例資料,回顧性分析局部手術對預后的價值,通過分析獨立預后因素并構建預后預測模型,根據預后預測模型將患者進行預后風險分層,分析不同風險患者局部手術的獲益情況。
1 資料與方法
1.1 研究設計
本研究為回顧性隊列研究,遵照《加強流行病學中觀察性研究報告質量(STROBE)指南》[12]進行實施和報告。本研究通過遂寧市中心醫院科研倫理委員會審批(編號:LLSLH20220067),因使用公共免費開放數據庫數據,不涉及患者隱私及利益,經倫理委員會申請豁免了知情同意。
1.2 資料來源
使用 SEER*Stat(8.4.0 版)提取美國 SEER 數據庫中符合本研究納入標準的病例數據。納入標準:① 診斷年份為 2010 年—2019 年;② 病理組織確診為浸潤性乳腺癌;③ 性別女;④ 確診年齡 18~70 歲;⑤ 合并骨轉移;⑥ 隨訪信息完整。排除標準:① 合并腦、肺或肝等其他部位轉移;② 多源性腫瘤;③ 炎性乳腺癌;④ 手術方式信息缺失;⑤ T3 期、T4 期及 T 分期不明確;⑥ 重要信息缺失。
1.3 研究指標
提取所有患者的診斷年份、診斷年齡、種族、手術信息、腫瘤 TNM 分期、組織學分級、病理類型、分子分型、放療、化療、轉移部位、雌激素受體(estrogen receptor, ER)狀態、孕激素受體(progesterone receptor, PR)狀態、人表皮生長因子受體 2(human epidermal growth factor receptor-2, HER2)狀態、生存時間及生存結局等資料。采用美國癌癥聯合會乳腺癌 TNM 分期系統(第 8 版)對患者進行腫瘤分期[13],將患者腋窩淋巴結狀態劃分為淋巴結陰性和陽性 2 種狀態。病理類型劃分為浸潤性導管癌、浸潤性小葉癌和其他類型 3 類。根據患者診斷時年齡劃分為 18~55 歲和 56~70 歲 2 組。
1.4 結局指標
本研究的生存終點為總生存,定義為從確診乳腺癌至因任何原因死亡的時間間隔,失訪病例作為刪失數據。
1.5 統計學方法
根據患者是否接受局部手術劃分為手術組與未手術組,以 7∶3 比例將所有病例隨機分為訓練集與驗證集。基礎特征中的數值變量轉換為分類變量,采用例數和/或百分率進行統計描述,組間對比采用 χ2 檢驗。隨訪時長以中位數(下四分位數,上四分位數)進行統計描述。采用 Kaplan-Meier 法繪制生存曲線,對數秩檢驗比較生存率。采用單因素和多因素 Cox 比例風險模型進行預后因素分析并計算風險比(hazard ratio, HR)及對應的 95% 置信區間(confidence interval, CI),單因素分析 P<0.05 或臨床評估有意義的變量進入多因素模型。采用向后法構建預后預測模型,采用時間依賴的臨床受試者操作特征(receiver operating characteristic, ROC)曲線及曲線下面積(area under the curve, AUC)、校準曲線、決策曲線分析(decision curve analysis, DCA)分別在訓練集和驗證集評價模型的區分度、校準度和臨床適用度。根據預測模型計算患者預后風險得分,采用 X-tile 軟件將患者劃分為低、中、高風險組,使用生存分析在不同風險亞組患者中比較手術和未手術患者的生存差異。所有統計分析及作圖使用 R 4.0.3 軟件完成。雙側檢驗水準 α=0.05。
2 結果
2.1 患者臨床病理學特征
經篩選,共
 圖1
病例篩選流程圖
圖1
病例篩選流程圖
ER:雌激素受體;PR:孕激素受體;HER2:人表皮生長因子受體 2
2.2 生存分析
總人群中位隨訪時間 32(16,53)個月,發生死亡 865 例(42.1%),其中手術組 322 例(37.9%),未手術組 543 例(44.9%)。生存分析顯示訓練集手術組患者的總生存優于未手術組患者(P<0.001),見圖2。在訓練集中行單因素 Cox 回歸分析,結果顯示手術、年齡、種族、婚姻狀態、分子分型、組織學分級、ER 狀態、PR 狀態、HER2 狀態及化療與患者總生存相關(P<0.05),T 分期、腋窩淋巴結狀態、病理類型及放療與患者總生存未見相關性(P>0.05),見表2。將單因素分析 P<0.05 相關因素及病理類型納入多因素 Cox 回歸分析(因 ER 狀態、PR 狀態及 HER2 狀態與分子分型變量效應重疊,僅將分子分型納入模型),多因素 Cox 回歸模型分析結果顯示手術可改善 bMBC 患者的總生存[HR=0.51,95%CI(0.43,0.60),P<0.001],此外化療、婚姻狀態、分子分型、年齡、組織學分級及病理類型與總生存獨立相關(P<0.05),種族與總生存未見相關性(P>0.05),見表2。
 圖2
訓練集手術與未手術患者總生存的生存曲線
圖2
訓練集手術與未手術患者總生存的生存曲線
2.3 預后預測模型構建與驗證
在訓練集中將單因素 Cox 回歸分析 P<0.05 及病理類型(未納入變量“手術”)采用向后法篩選變量并構建預后預測模型,最終化療、婚姻狀態、分子分型、年齡、病理類型及組織學分級 6 個變量被納入預后預測模型。通過該模型計算訓練集中所有患者 1、3、5 年總生存率并構建預后預測模型列線圖,見圖3。訓練集和驗證集的 C-index 分別為 0.702[95%CI(0.677,0.725)]和 0.703[95%CI(0.66,0.73)];訓練集 1、3、5 年 AUC 分別為 0.734、0.727、0.731(圖4a),驗證集 1、3、5 年 AUC 分別為 0.755、0.737、0.708(圖4b),提示模型有較好的區分度。構建訓練集及驗證集 1、3、5 年校準曲線,結果均顯示預測生存率與實際生存率高度吻合(圖5)。DCA 曲線顯示模型具有一定臨床適用性(圖6)。
 圖3
初診單純骨轉移乳腺癌患者預后列線圖
圖3
初診單純骨轉移乳腺癌患者預后列線圖
IDC:浸潤性導管癌;ILC:浸潤性小葉癌;HR:激素受體;HER2:人表皮生長因子受體 2;TNBC:三陰乳腺癌
 圖4
訓練集與驗證集中預后模型預測 1、3、5 年總生存率的 ROC 曲線
圖4
訓練集與驗證集中預后模型預測 1、3、5 年總生存率的 ROC 曲線
a. 訓練集;b. 驗證集。ROC:受試者操作特征
 圖5
訓練集與驗證集中預后模型預測 1、3、5 年總生存率的校準曲線
圖5
訓練集與驗證集中預后模型預測 1、3、5 年總生存率的校準曲線
a~c. 訓練集 1、3、5 年總生存率的校準曲線;d~f. 驗證集 1、3、5 年總生存率的校準曲線
 圖6
訓練集與驗證集中預后模型 1、3、5 年臨床決策曲線
圖6
訓練集與驗證集中預后模型 1、3、5 年臨床決策曲線
a~c. 訓練集 1、3、5 年臨床決策曲線;d~f. 驗證集 1、3、5 年臨床決策曲線
2.4 風險分層及手術獲益分析
利用預后預測模型計算訓練集與驗證集中每例患者的預后風險預測評分。使用 X-tile 軟件根據訓練集風險預測評分將患者劃分為低風險組(<70 分)、中風險組(70~160 分)和高風險組(>160 分),生存分析對數秩檢驗結果顯示,局部手術改善低風險患者的總生存(訓練集:P=0.013;驗證集:P=0.024),不改善中、高風險患者的總生存(訓練集中風險組:P=0.45;訓練集高風險組:P=0.56;驗證集中風險組:P=0.77;驗證集高風險組:P=0.94)。見圖7。
 圖7
訓練集和驗證集中手術在低、中、高風險組中的生存獲益
圖7
訓練集和驗證集中手術在低、中、高風險組中的生存獲益
a~c. 訓練集中手術在低、中、高風險組中的生存獲益;d~f. 驗證集中手術在低、中、高風險組中的生存獲益
3 討論
本研究利用 SEER 數據庫病例分析顯示,局部手術可改善初診 bMBC 患者的預后,進一步分析發現手術、化療、婚姻狀態、分子分型、年齡、病理類型及組織學分級與患者的總生存獨立相關。通過構建預后風險預測模型,計算每例患者的預后風險得分并進一步將患者劃分為低、中、高風險組,生存分析顯示局部手術主要改善低風險患者的預后,對中、高風險患者預后的改善作用有限。
局部手術能否改善初診晚期乳腺癌患者預后尚存爭議[6-7, 14-15],Tata 試驗、ABCSG-28 試驗及 ECOG-ACRIN E2108 試驗研究結果均提示手術不能改善 dnMBC 患者預后[6-8]。MF07-01 試驗納入共 274 例 dnMBC 患者,按照 1∶1 隨機分為手術組(n=138)和未手術組(n=136),在中位隨訪 40 個月時發現手術組的死亡風險較未手術組降低了 34%;在其非計劃的亞組分析中發現年輕患者及單純骨轉移患者從局部手術中獲益更大,該研究提示骨轉移患者可能是局部手術的主要獲益人群[16]。另有研究發現部分小腫瘤負荷的乳腺癌患者有從局部手術中獲益的趨勢[17-18],臨床中腫瘤轉移負荷較小的患者也更多被推薦行局部手術治療。骨是乳腺癌最常見的轉移部位[19],bMBC 患者通常較其他轉移部位乳腺癌患者具有更小的腫瘤負荷及更長的預期生存時間,常常被臨床醫師推薦行局部手術[20]。一項納入 187 例初診 bMBC 患者的回顧性研究發現,局部手術患者較未手術患者遠期生存更好[18];另一項針對國內患者的研究同樣發現手術可改善 bMBC 患者預后生存[21]。本研究通過 SEER 數據庫大樣本研究發現手術組較未手術組死亡風險下降了 49%,與 MF07-01 研究結果比較一致。此外,本研究結果提示化療、婚姻狀態、分子分型、年齡、病理類型及組織學分級與總生存具有獨立相關性,這與既往相似研究結果相似[22-24]。在本組數據中,HR+/HER2+亞型患者的預后優于其他亞型,與常規認為 HR+/HER2–患者是預后最好的亞型存在一定差異,這可能與抗 HER2 靶向治療和內分泌治療藥物的不斷發展和應用有著密切關系[25]。曲妥珠單抗是一種抗 HER2 的人源化單克隆抗體,可使 HER2 型晚期乳腺癌患者死亡風險降低約 44%,而在曲妥珠和多西他賽的基礎上加入帕妥珠單抗可進一步降低 HER2 型晚期乳腺癌患者死亡風險[26]。此外,有研究發現抑制 HER2 可以提高內分泌治療的敏感性[27-28]。
初診 bMBC 患者通常較其他轉移部位乳腺癌患者預后更好,目前國內外指南均認為初診 bMBC 患者是局部手術獲益的潛在人群[5, 9],但是否所有 bMBC 患者均可從局部手術中獲益尚存爭議。一項研究亞組分析發現部分預后較差 bMBC 患者并不能從局部手術中改善遠期生存[10],另一項來自國內多中心回顧性研究分析發現分子分型等多種因素與 bMBC 患者預后相關[29],提示初診 bMBC 患者局部手術策略的制定應根據患者臨床病理特征、預期生存時間等進行綜合考慮而進行個體化制定。因此,構建可用于臨床評估患者手術獲益風險模型十分重要。本研究通過對 SEER 數據庫中大樣本數據分析發現手術、化療、婚姻狀態、分子分型、年齡、病理類型及組織學分級與初診 bMBC 患者遠期生存獨立相關,進一步構建手術獲益預測模型并以列線圖進行展示,使用所構建的預測模型預測每例患者的預后風險總得分并將患者劃分為低、中、高風險組,生存分析發現局部手術僅可改善低風險組患者預后,而不改變中、高風險組患者遠期生存,這為臨床醫師手術決策提供了更為準確的信息。
本研究存在以下局限性:① 本研究為真實世界癌癥登記數據庫病例的回顧性研究,不可避免存在一定程度的選擇性偏倚;② 由于數據庫可獲取的數據有限,無法獲得骨轉移灶、內分泌治療及放化療方案的詳細資料,限制了數據更為準確和詳細的分析。盡管存在一定程度的局限性,本研究也可能為部分骨轉移患者臨床決策提供一定的參考,期待更多大樣本前瞻性研究探討局部手術在單純骨轉移患者預后中的價值。
利益沖突:所有作者聲明不存在利益沖突。