外科二尖瓣生物瓣置換術后瓣膜多在 10~15 年發生衰敗,需再次進行二尖瓣手術。既往此類患者只能選擇再次進行外科開胸二尖瓣置換,盡管再次心內直視手術的風險更高。近年來,通過“瓣中瓣”植入實現經導管二尖瓣置換的介入治療方式已成為再次外科開胸手術的合理替代方案。該文報道了 1 例二尖瓣生物瓣衰敗的 81 歲女性患者,盡管因雙側巨大心房伴小心室腔等解剖原因介入操作難度高,但基于完善的術前 CT 評估,最終成功地經股靜脈-房間隔途徑實施了經導管二尖瓣置換術。
引用本文: 晏夢云, 馮沅, 陳飛, 朱中凱, 趙振剛, 陳茂. 經導管二尖瓣瓣中瓣置換術治療二尖瓣生物瓣假體衰敗一例. 華西醫學, 2024, 39(9): 1371-1374. doi: 10.7507/1002-0179.202309200 復制
版權信息: ?四川大學華西醫院華西期刊社《華西醫學》版權所有,未經授權不得轉載、改編
病例介紹 患者,女,81 歲,因“勞力性呼吸困難 10+年,加重 3 d”于 2023 年 3 月 27 日入四川大學華西醫院(以下簡稱“我院”)心臟內科。入院前 10+年患者因“勞力性呼吸困難進行性加重”診斷“二尖瓣重度反流”于外院開胸行“二尖瓣置換術”,使用瓣膜為 Hancock Ⅱ生物瓣(美國美敦力公司)。入院前 3 d 患者呼吸困難癥狀再發加重,伴雙下肢對稱性凹陷性水腫,遂于我院就診。患者既往有“反流性食管炎、膽囊結石伴膽囊炎、重度貧血”等病史。專科體格檢查:心界向兩側擴大,心律不齊,第一心音強弱不等,心尖部可聞及 4/6 級收縮期吹風樣雜音,余瓣膜區未聞及明顯雜音,雙下肢凹陷性水腫。輔助檢查:超聲心動圖提示左心室內徑 45 mm,左心房內徑 59 mm,右心室內徑 16 mm,右心房內徑 53 mm,左心室射血分數 77%,二尖瓣生物瓣瓣葉明顯增厚、關閉錯位伴重度反流(圖1a),跨瓣血流速度加快[峰值流速(maximum velocity, Vmax)=1.9 m/s],有效瓣口面積 1.9 cm2,三尖瓣輕-中度反流[Vmax=3.0 m/s,估測肺動脈收縮壓 44 mm Hg(1 mm Hg=0.133 kPa)];心電圖提示快室率心房顫動;氨基末端腦鈉肽前體
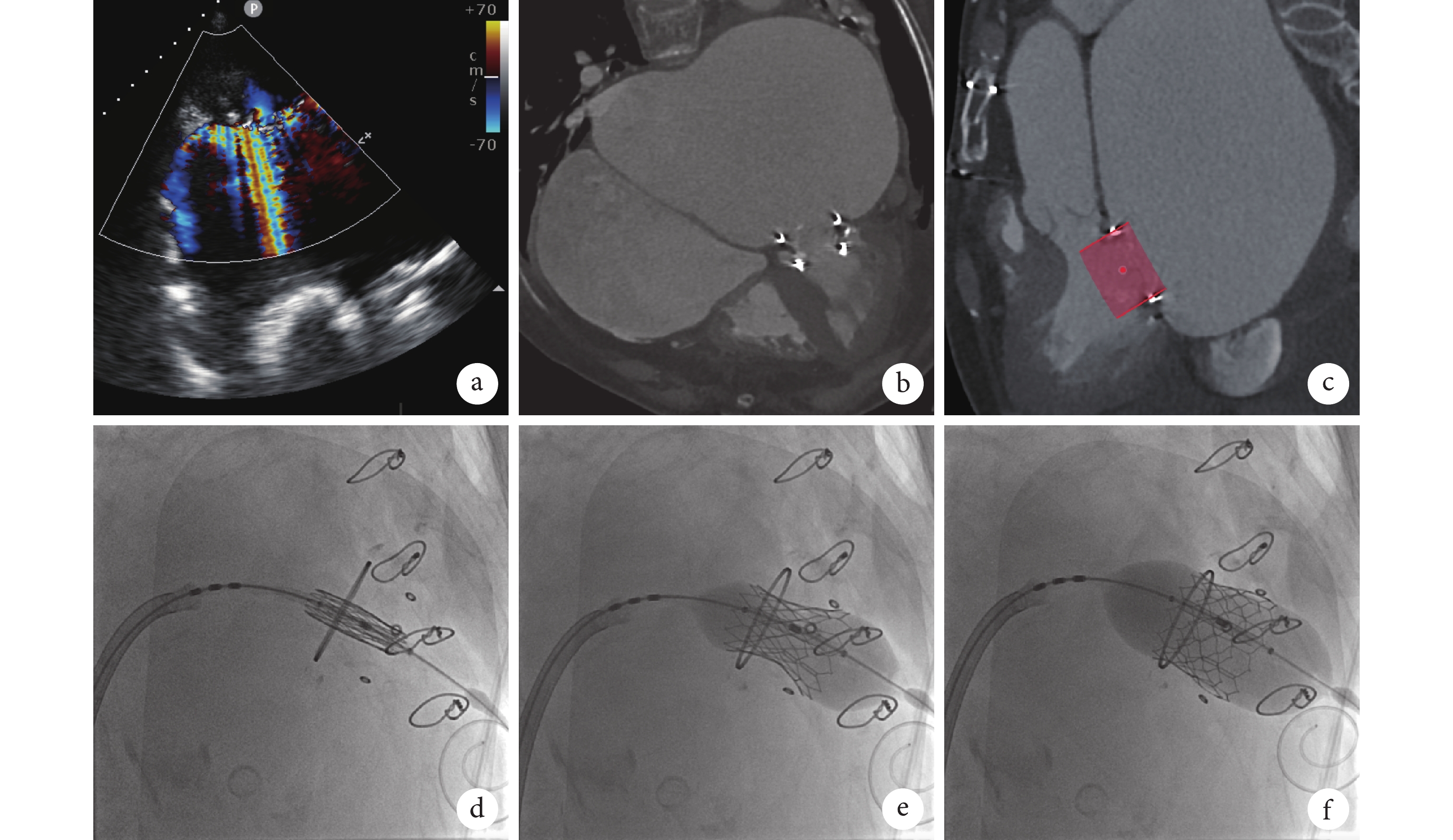 圖1
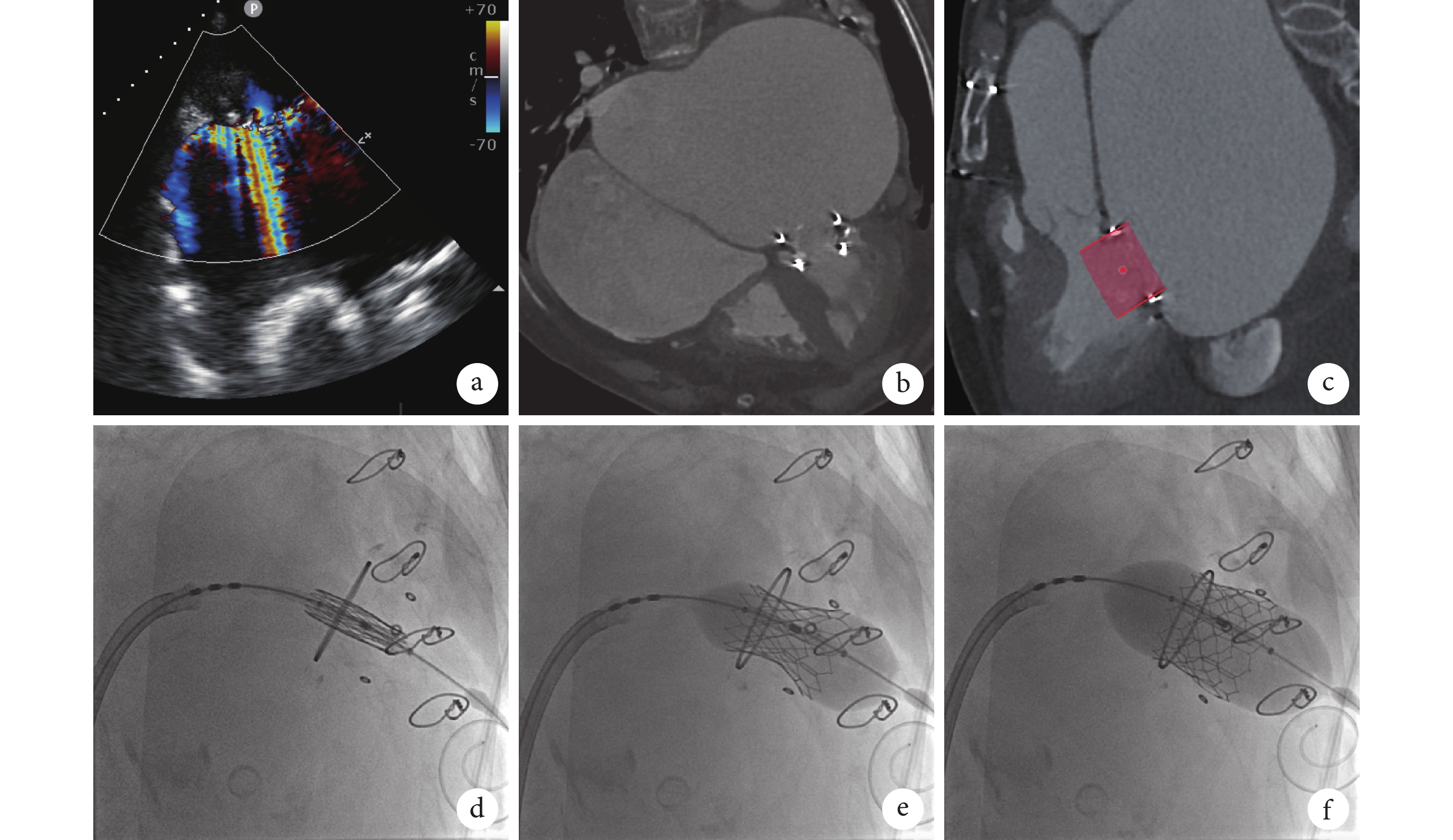
術前影像及經導管二尖瓣置換術過程
圖1
術前影像及經導管二尖瓣置換術過程
a. 術前超聲示二尖瓣生物瓣大量反流;b. 術前 CT 示雙側巨大心房及小心室;c. 基于 CT 模擬 26 mm 球囊擴張式瓣膜置入(紅色部分);d. 基于二尖瓣生物瓣金屬環進行經導管瓣膜定位;e. 充盈球囊釋放經導管瓣膜;f. 球囊后擴張
患者二尖瓣生物瓣衰敗,存在明顯心力衰竭癥狀,有明確干預指征,但患者高齡、既往外科開胸術后、一般情況較差,美國胸外科醫師協會評分為 8.77%。心臟瓣膜多學科團隊評估后,認為患者再次行外科開胸二尖瓣置換手術風險極高,建議評估經導管二尖瓣置換術(transcatheter mitral valve replacement, TMVR),即經導管二尖瓣瓣中瓣植入(valve-in-valve TMVR, ViV-TMVR)。ViV-TMVR 的優點在于創傷小、術后恢復期短,既往研究顯示其治療二尖瓣生物瓣衰敗的效果良好[1]。
術前心臟 CT 提示雙側巨大心房(圖1b),左心房擴大尤為顯著(左心房內徑為 84.2 mm×92.1 mm×112.1 mm,右心房內徑為 64.4 mm×88.8 mm×91.9 mm);雙心室內徑則明顯較小,左心室收縮末期內徑為 25.4 mm,舒張末期內徑為 43.2 mm。巨大雙心房和小心室結構會對經股靜脈-穿房間隔途徑 ViV-TMVR 操作造成巨大挑戰,因輸送軌道扭曲、左心室鋼絲穩定性差等原因,可能造成經導管人工瓣膜難以通過二尖瓣、左心室導絲彈出左心室、左心室穿孔等,導致手術失敗甚至患者死亡。對于此類解剖,選用輸送系統具備可調彎功能的器械有助于減少失敗和嚴重并發癥風險。患者既往行二尖瓣置換時曾行房間隔切開及縫合、CT 提示房間隔增厚及少許鈣化,再加上巨大左心房,房間隔穿刺難度及相關并發癥風險均較高,需經食管超聲引導、使用可調彎穿刺鞘及必要時電刀輔助穿刺。CT 測得二尖瓣生物瓣瓣環真實內徑為 24.2 mm,結合 Valve in Valve App(version 2.0,UBQO Limited,London,UK)推薦,患者適合使用 26 mm SAPIEN 3 瓣膜進行 ViV-TMVR。左心室流出道(left ventricular outflow tract, LVOT)梗阻是 TMVR 術后的嚴重并發癥,通過術前 CT 可預測 LVOT 梗阻風險。對本例患者,基于術前 CT 模擬植入 26 mm SAPIEN 3 瓣膜后,測得新 LVOT(Neo-LVOT)面積為 2.5 cm2,LVOT 梗阻風險較低。綜合上述考慮,心臟瓣膜團隊擬使用 SAPIEN 3 球囊擴張式瓣膜經股靜脈-穿房間隔途徑行 ViV-TMVR。
術中過程見圖1c~1f。患者全身麻醉,氣管插管,穿刺右側股靜脈作為操作主入路,放置鞘管至右心房,行右心房測壓和右心房造影術,術前上腔靜脈 15/10/8 mm Hg,肺動脈 57/31/18 mm Hg,左心房 39/24/17 mm Hg。退出導絲后,在食管超聲引導下使用可調彎房間隔穿刺鞘,根據患者術前心臟 CT 提示的房間隔解剖特點,穿刺部位選取房間隔靠后、靠下的位置。房間隔穿刺成功后全身肝素化,通過房間隔穿刺鞘導入 6F 豬尾巴導管,通過調整房間隔穿刺鞘彎度及方向,操縱豬尾巴導管從二尖瓣生物瓣中心進入左心室,然后通過豬尾巴導管將頭端預塑形的加硬導絲送至左心室心尖部建立軌道。在加硬導絲支撐下將 10 mm 球囊送至房間隔處行房間隔擴張,以利于后續經導管瓣膜通過。將 SAPIEN 3 瓣膜反裝并通過 Commander 輸送系統延加硬導絲送至二尖瓣生物瓣瓣環處,在基于術前 CT 預先選取的二尖瓣生物瓣金屬環切線位下準確定位瓣膜,直接通過已置入左心室心尖部的加硬導絲實施快速起搏,快速起搏至 180 次/min、收縮壓降至 60 mm Hg 以下后充盈球囊置入瓣膜,球囊回縮后停止起搏。初步評估后,為改善瓣膜形態、增加穩定性,使用同一球囊于快速起搏下行球囊后擴張。術后造影及即刻超聲提示人工瓣膜植入效果良好,二尖瓣平均跨瓣壓差為 3 mm Hg,人工瓣瓣口及瓣周未見明顯反流,LVOT 血流通暢、無血流加速,術后心臟測壓:左心房 26/19/15 mm Hg,肺動脈 46/28/16 mm Hg。患者術后恢復順利,無不良事件發生,術后 7 d 超聲心動圖提示二尖瓣位人工瓣,瓣架穩定,人工瓣周及瓣口未見明顯反流,肺動脈瓣前向血流稍加速。出院時癥狀較前明顯改善。術后規律隨訪,隨訪 1 年超聲心動圖提示人工生物瓣功能未見明顯異常,瓣口及瓣周未見明顯反流。
討論 二尖瓣疾病是人群中最常見的心臟瓣膜病類型[2],對于無法修復的器質性二尖瓣病變,外科二尖瓣置換術是主要的治療手段。為避免長期抗凝治療,對于年齡相對較大的患者常選擇生物瓣而非機械瓣[3]。生物瓣有一定的使用年限,通常在 10~15 年后發生衰敗,需要再次進行換瓣手術[4]。既往研究顯示,再次外科開胸手術風險明顯大于初次手術[5-6],尤其是對于常常存在多重合并癥的老年患者,亟需創傷小而療效相當的替代治療手段。迫切的臨床需求推動了經導管二尖瓣介入治療技術的進步[7-10]。2009 年 Cheung 等[7]首次報道了 ViV-TMVR 治療外科二尖瓣生物瓣衰敗的成功經驗,給此類患者的治療帶來一種新的思路。2021 年的前瞻性 MITRAL 研究中 ViV-TMVR 的成功率為 100%,且 1 年隨訪顯示沒有患者發生死亡或其他嚴重不良事件[10]。本例患者高齡、再次行外科開胸手術風險極高,盡管其解剖結構對于 ViV-TMVR 而言也頗具挑戰,但經心臟瓣膜團隊評估認為經導管介入治療仍然是更佳的治療選擇。
國際上報道用于 ViV-TMVR 的器械包括 Lotus 機械擴張式瓣膜(已退市)和 Edwards SAPIEN 系列球囊擴張式瓣膜。其中,SAPIEN 3 瓣膜于 2017 年獲美國食品藥物監督管理局批準用于二尖瓣生物瓣衰敗后的 ViV-TMVR 治療,目前在國外已積累了一定的臨床經驗[11]。在國內,SAPIEN 3 是目前為止唯一一款獲批上市的球囊擴張式瓣膜,但其用于 ViV-TMVR 的經驗相對缺乏。球囊擴張式瓣膜用于 ViV-TMVR 的優勢在于:① 瓣架短,對左心房、左心室結構影響小,LVOT 梗阻風險較低;② 可在定位后快速完成精準釋放;③ 可調彎輸送系統保證了系統通過性和瓣膜釋放時的同軸性。早期文獻報道的 ViV-TMVR 采用的是經心尖入路[12]。為避免與經心尖入路相關的并發癥,ViV-TMVR 的入路選擇逐漸向經股靜脈-房間隔途徑轉變[13-16]。Frerker 等[17]對比了經股靜脈-穿房間隔途徑和經心尖途徑在臨床效果、并發癥及遠期生存率等,結果顯示接受經股靜脈-穿房間隔途徑 ViV-TMVR 的患者遠期生存率更高。
與其他經導管瓣膜置換技術一樣,CT 影像分析是 ViV-TMVR 術前評估中必不可少的環節,是明確技術可行性、預估操作難度及重要并發癥風險、規劃術中策略的主要依據[18]。術前通過 CT 影像分析和模擬植入 TMVR 瓣膜,可以評估人工瓣膜與毗鄰組織貼靠位置及 LVOT 梗阻風險,進一步優化穿刺部位的選擇,從而建立理想的輸送軌道,提高 TMVR 手術的成功率和安全性。ViV-TMVR 房間隔穿刺位置通常選擇卵圓窩靠后、靠下處,并且盡可能保證穿刺高度在 3.5 cm 左右,穿刺高度過低(即穿刺點距離二尖瓣瓣環水平過近)可能導致經導管瓣膜難以與外科生物瓣瓣環同軸[19]。本例患者的術中操作難點主要與雙側巨大心房和相對較小的心室結構相關,此類患者人群多數左心房較大,軌道穩定性不佳,術中可能因軌道鋼絲在右心房-左心房-左心室段的成角大和在左心室腔內的錨定不足造成經導管瓣膜無法送達二尖瓣、軌道鋼絲脫出左心室或穿出左心室等嚴重情況。為應對上述解剖挑戰,除選用具有可調彎功能、通過性良好的瓣膜系統外,術者經驗和操作技巧亦至關重要,要求第一術者恰當控制瓣膜推送節奏并正確使用調彎功能、第二術者穩定控制導絲位置和張力且第一、二術者之間默契配合。此外,TMVR 術前 CT 分析時需仔細評估 LVOT 梗阻這一潛在致命并發癥的風險。本例患者基于術前 CT 行瓣膜模擬置入后 Neo-LVOT 面積為 2.5 cm2,LVOT 梗阻風險較低,適合進行 ViV-TMVR;通常認為術前 CT 預估 Neo-LVOT 面積小于 1.8 cm2 的患者,TMVR 術后發生 LVOT 梗阻的風險較高[20]。對于預估 LVOT 梗阻風險高的患者,應慎重選擇 TMVR。有研究報道了在擬行 TMVR 但 LVOT 梗阻風險高的患者中預防性行酒精室間隔消融術(alcohol septal ablation, ASA)以降低 LVOT 風險的可行性,30 例 Neo-LVOT 梗阻高危患者經消融術后,8 例在 ASA 后得到臨床改善,2 例在 TMVR 之前死亡,20 例成功施行 TMVR,TMVR 術后僅 1 例院內死亡,原因為 ASA 后 LVOT 重塑不足;整個隊列的死亡率為 10%;綜上,預防性 ASA 可能使因 LVOT 梗阻風險過高而排除的患者能夠安全地進行 TMVR[21]。因此,經 CT 預估 LVOT 梗阻風險高的患者,應由心臟瓣膜團隊充分權衡外科開胸手術風險和 TMVR 相關風險后,結合患者意愿決定治療方式。
目前,針對患者自體二尖瓣病變的 TMVR 技術仍在發展階段,針對二尖瓣生物瓣衰敗的 ViV-TMVR 的發展相對成熟,但 ViV-TMVR 仍是一項技術難度較大的治療方式,我國目前積累臨床經驗還十分有限。不過,從國外報道數據和我們初步的臨床應用經驗看,對于解剖條件合適、外科手術風險較高的二尖瓣生物瓣衰敗患者,ViV-TMVR 可以作為再次外科換瓣手術的合理替代方案。
利益沖突:所有作者聲明不存在利益沖突。
病例介紹 患者,女,81 歲,因“勞力性呼吸困難 10+年,加重 3 d”于 2023 年 3 月 27 日入四川大學華西醫院(以下簡稱“我院”)心臟內科。入院前 10+年患者因“勞力性呼吸困難進行性加重”診斷“二尖瓣重度反流”于外院開胸行“二尖瓣置換術”,使用瓣膜為 Hancock Ⅱ生物瓣(美國美敦力公司)。入院前 3 d 患者呼吸困難癥狀再發加重,伴雙下肢對稱性凹陷性水腫,遂于我院就診。患者既往有“反流性食管炎、膽囊結石伴膽囊炎、重度貧血”等病史。專科體格檢查:心界向兩側擴大,心律不齊,第一心音強弱不等,心尖部可聞及 4/6 級收縮期吹風樣雜音,余瓣膜區未聞及明顯雜音,雙下肢凹陷性水腫。輔助檢查:超聲心動圖提示左心室內徑 45 mm,左心房內徑 59 mm,右心室內徑 16 mm,右心房內徑 53 mm,左心室射血分數 77%,二尖瓣生物瓣瓣葉明顯增厚、關閉錯位伴重度反流(圖1a),跨瓣血流速度加快[峰值流速(maximum velocity, Vmax)=1.9 m/s],有效瓣口面積 1.9 cm2,三尖瓣輕-中度反流[Vmax=3.0 m/s,估測肺動脈收縮壓 44 mm Hg(1 mm Hg=0.133 kPa)];心電圖提示快室率心房顫動;氨基末端腦鈉肽前體
 圖1
術前影像及經導管二尖瓣置換術過程
圖1
術前影像及經導管二尖瓣置換術過程
a. 術前超聲示二尖瓣生物瓣大量反流;b. 術前 CT 示雙側巨大心房及小心室;c. 基于 CT 模擬 26 mm 球囊擴張式瓣膜置入(紅色部分);d. 基于二尖瓣生物瓣金屬環進行經導管瓣膜定位;e. 充盈球囊釋放經導管瓣膜;f. 球囊后擴張
患者二尖瓣生物瓣衰敗,存在明顯心力衰竭癥狀,有明確干預指征,但患者高齡、既往外科開胸術后、一般情況較差,美國胸外科醫師協會評分為 8.77%。心臟瓣膜多學科團隊評估后,認為患者再次行外科開胸二尖瓣置換手術風險極高,建議評估經導管二尖瓣置換術(transcatheter mitral valve replacement, TMVR),即經導管二尖瓣瓣中瓣植入(valve-in-valve TMVR, ViV-TMVR)。ViV-TMVR 的優點在于創傷小、術后恢復期短,既往研究顯示其治療二尖瓣生物瓣衰敗的效果良好[1]。
術前心臟 CT 提示雙側巨大心房(圖1b),左心房擴大尤為顯著(左心房內徑為 84.2 mm×92.1 mm×112.1 mm,右心房內徑為 64.4 mm×88.8 mm×91.9 mm);雙心室內徑則明顯較小,左心室收縮末期內徑為 25.4 mm,舒張末期內徑為 43.2 mm。巨大雙心房和小心室結構會對經股靜脈-穿房間隔途徑 ViV-TMVR 操作造成巨大挑戰,因輸送軌道扭曲、左心室鋼絲穩定性差等原因,可能造成經導管人工瓣膜難以通過二尖瓣、左心室導絲彈出左心室、左心室穿孔等,導致手術失敗甚至患者死亡。對于此類解剖,選用輸送系統具備可調彎功能的器械有助于減少失敗和嚴重并發癥風險。患者既往行二尖瓣置換時曾行房間隔切開及縫合、CT 提示房間隔增厚及少許鈣化,再加上巨大左心房,房間隔穿刺難度及相關并發癥風險均較高,需經食管超聲引導、使用可調彎穿刺鞘及必要時電刀輔助穿刺。CT 測得二尖瓣生物瓣瓣環真實內徑為 24.2 mm,結合 Valve in Valve App(version 2.0,UBQO Limited,London,UK)推薦,患者適合使用 26 mm SAPIEN 3 瓣膜進行 ViV-TMVR。左心室流出道(left ventricular outflow tract, LVOT)梗阻是 TMVR 術后的嚴重并發癥,通過術前 CT 可預測 LVOT 梗阻風險。對本例患者,基于術前 CT 模擬植入 26 mm SAPIEN 3 瓣膜后,測得新 LVOT(Neo-LVOT)面積為 2.5 cm2,LVOT 梗阻風險較低。綜合上述考慮,心臟瓣膜團隊擬使用 SAPIEN 3 球囊擴張式瓣膜經股靜脈-穿房間隔途徑行 ViV-TMVR。
術中過程見圖1c~1f。患者全身麻醉,氣管插管,穿刺右側股靜脈作為操作主入路,放置鞘管至右心房,行右心房測壓和右心房造影術,術前上腔靜脈 15/10/8 mm Hg,肺動脈 57/31/18 mm Hg,左心房 39/24/17 mm Hg。退出導絲后,在食管超聲引導下使用可調彎房間隔穿刺鞘,根據患者術前心臟 CT 提示的房間隔解剖特點,穿刺部位選取房間隔靠后、靠下的位置。房間隔穿刺成功后全身肝素化,通過房間隔穿刺鞘導入 6F 豬尾巴導管,通過調整房間隔穿刺鞘彎度及方向,操縱豬尾巴導管從二尖瓣生物瓣中心進入左心室,然后通過豬尾巴導管將頭端預塑形的加硬導絲送至左心室心尖部建立軌道。在加硬導絲支撐下將 10 mm 球囊送至房間隔處行房間隔擴張,以利于后續經導管瓣膜通過。將 SAPIEN 3 瓣膜反裝并通過 Commander 輸送系統延加硬導絲送至二尖瓣生物瓣瓣環處,在基于術前 CT 預先選取的二尖瓣生物瓣金屬環切線位下準確定位瓣膜,直接通過已置入左心室心尖部的加硬導絲實施快速起搏,快速起搏至 180 次/min、收縮壓降至 60 mm Hg 以下后充盈球囊置入瓣膜,球囊回縮后停止起搏。初步評估后,為改善瓣膜形態、增加穩定性,使用同一球囊于快速起搏下行球囊后擴張。術后造影及即刻超聲提示人工瓣膜植入效果良好,二尖瓣平均跨瓣壓差為 3 mm Hg,人工瓣瓣口及瓣周未見明顯反流,LVOT 血流通暢、無血流加速,術后心臟測壓:左心房 26/19/15 mm Hg,肺動脈 46/28/16 mm Hg。患者術后恢復順利,無不良事件發生,術后 7 d 超聲心動圖提示二尖瓣位人工瓣,瓣架穩定,人工瓣周及瓣口未見明顯反流,肺動脈瓣前向血流稍加速。出院時癥狀較前明顯改善。術后規律隨訪,隨訪 1 年超聲心動圖提示人工生物瓣功能未見明顯異常,瓣口及瓣周未見明顯反流。
討論 二尖瓣疾病是人群中最常見的心臟瓣膜病類型[2],對于無法修復的器質性二尖瓣病變,外科二尖瓣置換術是主要的治療手段。為避免長期抗凝治療,對于年齡相對較大的患者常選擇生物瓣而非機械瓣[3]。生物瓣有一定的使用年限,通常在 10~15 年后發生衰敗,需要再次進行換瓣手術[4]。既往研究顯示,再次外科開胸手術風險明顯大于初次手術[5-6],尤其是對于常常存在多重合并癥的老年患者,亟需創傷小而療效相當的替代治療手段。迫切的臨床需求推動了經導管二尖瓣介入治療技術的進步[7-10]。2009 年 Cheung 等[7]首次報道了 ViV-TMVR 治療外科二尖瓣生物瓣衰敗的成功經驗,給此類患者的治療帶來一種新的思路。2021 年的前瞻性 MITRAL 研究中 ViV-TMVR 的成功率為 100%,且 1 年隨訪顯示沒有患者發生死亡或其他嚴重不良事件[10]。本例患者高齡、再次行外科開胸手術風險極高,盡管其解剖結構對于 ViV-TMVR 而言也頗具挑戰,但經心臟瓣膜團隊評估認為經導管介入治療仍然是更佳的治療選擇。
國際上報道用于 ViV-TMVR 的器械包括 Lotus 機械擴張式瓣膜(已退市)和 Edwards SAPIEN 系列球囊擴張式瓣膜。其中,SAPIEN 3 瓣膜于 2017 年獲美國食品藥物監督管理局批準用于二尖瓣生物瓣衰敗后的 ViV-TMVR 治療,目前在國外已積累了一定的臨床經驗[11]。在國內,SAPIEN 3 是目前為止唯一一款獲批上市的球囊擴張式瓣膜,但其用于 ViV-TMVR 的經驗相對缺乏。球囊擴張式瓣膜用于 ViV-TMVR 的優勢在于:① 瓣架短,對左心房、左心室結構影響小,LVOT 梗阻風險較低;② 可在定位后快速完成精準釋放;③ 可調彎輸送系統保證了系統通過性和瓣膜釋放時的同軸性。早期文獻報道的 ViV-TMVR 采用的是經心尖入路[12]。為避免與經心尖入路相關的并發癥,ViV-TMVR 的入路選擇逐漸向經股靜脈-房間隔途徑轉變[13-16]。Frerker 等[17]對比了經股靜脈-穿房間隔途徑和經心尖途徑在臨床效果、并發癥及遠期生存率等,結果顯示接受經股靜脈-穿房間隔途徑 ViV-TMVR 的患者遠期生存率更高。
與其他經導管瓣膜置換技術一樣,CT 影像分析是 ViV-TMVR 術前評估中必不可少的環節,是明確技術可行性、預估操作難度及重要并發癥風險、規劃術中策略的主要依據[18]。術前通過 CT 影像分析和模擬植入 TMVR 瓣膜,可以評估人工瓣膜與毗鄰組織貼靠位置及 LVOT 梗阻風險,進一步優化穿刺部位的選擇,從而建立理想的輸送軌道,提高 TMVR 手術的成功率和安全性。ViV-TMVR 房間隔穿刺位置通常選擇卵圓窩靠后、靠下處,并且盡可能保證穿刺高度在 3.5 cm 左右,穿刺高度過低(即穿刺點距離二尖瓣瓣環水平過近)可能導致經導管瓣膜難以與外科生物瓣瓣環同軸[19]。本例患者的術中操作難點主要與雙側巨大心房和相對較小的心室結構相關,此類患者人群多數左心房較大,軌道穩定性不佳,術中可能因軌道鋼絲在右心房-左心房-左心室段的成角大和在左心室腔內的錨定不足造成經導管瓣膜無法送達二尖瓣、軌道鋼絲脫出左心室或穿出左心室等嚴重情況。為應對上述解剖挑戰,除選用具有可調彎功能、通過性良好的瓣膜系統外,術者經驗和操作技巧亦至關重要,要求第一術者恰當控制瓣膜推送節奏并正確使用調彎功能、第二術者穩定控制導絲位置和張力且第一、二術者之間默契配合。此外,TMVR 術前 CT 分析時需仔細評估 LVOT 梗阻這一潛在致命并發癥的風險。本例患者基于術前 CT 行瓣膜模擬置入后 Neo-LVOT 面積為 2.5 cm2,LVOT 梗阻風險較低,適合進行 ViV-TMVR;通常認為術前 CT 預估 Neo-LVOT 面積小于 1.8 cm2 的患者,TMVR 術后發生 LVOT 梗阻的風險較高[20]。對于預估 LVOT 梗阻風險高的患者,應慎重選擇 TMVR。有研究報道了在擬行 TMVR 但 LVOT 梗阻風險高的患者中預防性行酒精室間隔消融術(alcohol septal ablation, ASA)以降低 LVOT 風險的可行性,30 例 Neo-LVOT 梗阻高危患者經消融術后,8 例在 ASA 后得到臨床改善,2 例在 TMVR 之前死亡,20 例成功施行 TMVR,TMVR 術后僅 1 例院內死亡,原因為 ASA 后 LVOT 重塑不足;整個隊列的死亡率為 10%;綜上,預防性 ASA 可能使因 LVOT 梗阻風險過高而排除的患者能夠安全地進行 TMVR[21]。因此,經 CT 預估 LVOT 梗阻風險高的患者,應由心臟瓣膜團隊充分權衡外科開胸手術風險和 TMVR 相關風險后,結合患者意愿決定治療方式。
目前,針對患者自體二尖瓣病變的 TMVR 技術仍在發展階段,針對二尖瓣生物瓣衰敗的 ViV-TMVR 的發展相對成熟,但 ViV-TMVR 仍是一項技術難度較大的治療方式,我國目前積累臨床經驗還十分有限。不過,從國外報道數據和我們初步的臨床應用經驗看,對于解剖條件合適、外科手術風險較高的二尖瓣生物瓣衰敗患者,ViV-TMVR 可以作為再次外科換瓣手術的合理替代方案。
利益沖突:所有作者聲明不存在利益沖突。