該文報道 1 例經頸靜脈入路行經導管三尖瓣置換術(transcatheter tricuspid valve replacement, TTVR)治療經導管二尖瓣置換術后持續性重度三尖瓣反流的病例。該患者為 80 歲女性,入院前 2 個月于四川大學華西醫院心臟內科行經導管二尖瓣置換術,術后因三尖瓣反流未改善與右心衰竭而病情惡化。患者入院后在全身麻醉下經頸靜脈入路行 TTVR,在心臟超聲及 X 線透視輔助下,順利植入人工瓣膜,三尖瓣反流緩解,患者手術順利,術后 25 d 病情明顯改善,并于術后 34 d 出院。
引用本文: 蒲星州, 趙振剛, 魏薪, 馮沅, 陳飛, 陳茂. 經頸靜脈入路行經導管三尖瓣置換術治療經導管二尖瓣置換術后持續性重度三尖瓣反流一例. 華西醫學, 2024, 39(9): 1375-1378. doi: 10.7507/1002-0179.202407266 復制
版權信息: ?四川大學華西醫院華西期刊社《華西醫學》版權所有,未經授權不得轉載、改編
病例介紹 患者,女性,80 歲,因“勞力性呼吸困難 10+年,加重伴下肢水腫 1 周”于 2022 年 8 月 7 日入四川大學華西醫院(以下簡稱“我院”)心臟內科。入院前 10+年患者漸出現勞力性呼吸困難,活動耐量下降,間斷伴夜間陣發性呼吸困難以及雙下肢水腫,多次于外院予藥物治療(具體不詳),效果欠佳。入院前 2 個月患者病情加重,出現端坐呼吸,于我院行超聲心動圖檢查提示二尖瓣瓣葉嚴重增厚鈣化、重度狹窄伴中度反流,且合并重度三尖瓣反流(tricuspid regurgitation, TR)與中度主動脈瓣狹窄,遂使用球擴式經導管瓣膜系統(PrizValve,上海紐脈醫療科技有限公司)經股靜脈入路行經導管二尖瓣置換術,術后癥狀改善。入院前 1 周患者病情惡化,再次出現勞力性呼吸困難和雙下肢水腫,無夜間陣發性呼吸困難或端坐呼吸,調整利尿藥物后癥狀無明顯改善,遂再次收入我院心臟內科治療。患者既往一般情況稍差,否認肝炎、結核或其他傳染病史,預防接種史不詳,對頭孢類藥物過敏;有肩胛外傷致骨裂微創手術史;糖尿病史 2+年,平時未規律控制血糖;既往有心房顫動病史;無輸血史,無其他特殊病史。
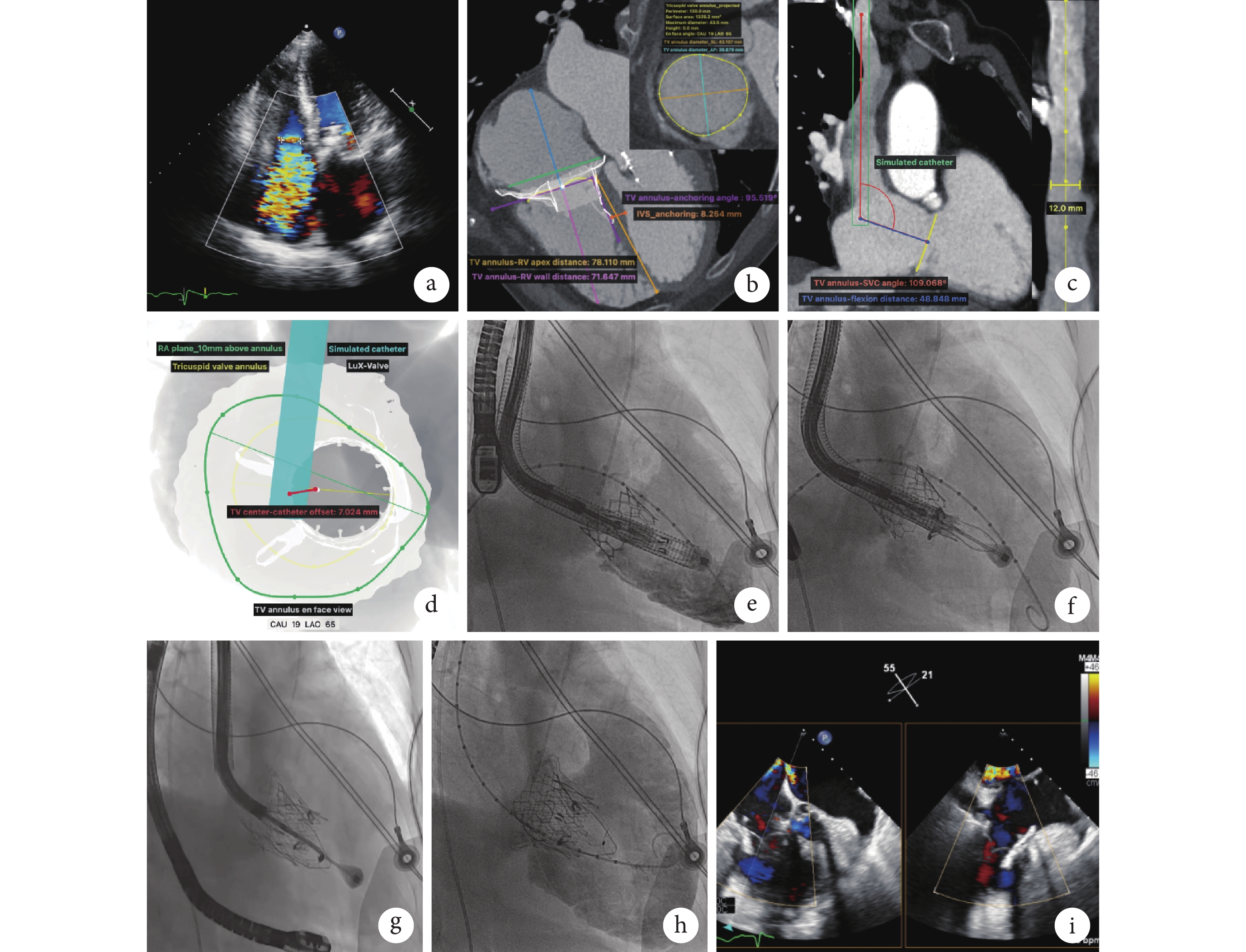
入院體格檢查:體溫 36.5℃,脈搏 68 次/min,呼吸頻率 18 次/min,血壓 110/70 mm Hg(1 mm Hg=0.133 kPa)。2022 年 8 月 11 日經胸超聲心動圖檢查顯示(圖1a):經導管二尖瓣置換術后人工二尖瓣瓣周輕度反流,平均跨瓣壓差 6 mm Hg,三尖瓣重度反流(縮流頸寬度 14 mm,反流峰值速度 3.1 m/s),主動脈瓣中度狹窄(平均跨瓣壓差 22 mm Hg);右心增大(右心室前后徑 29 mm,右心房中部橫徑 48 mm),右心室收縮功能降低(三尖瓣側瓣環收縮期位移 10 mm),估測肺動脈收縮壓 53 mm Hg。8 月 15 日實驗室檢查提示:血紅蛋白 113 g/L,國際標準化比值 1.18,總膽紅素 31.4 μmol/L,血清肌酐 134 μmol/L,估算腎小球濾過率 32.26 mL/(min·1.73 m2),氨基末端腦利尿鈉肽前體
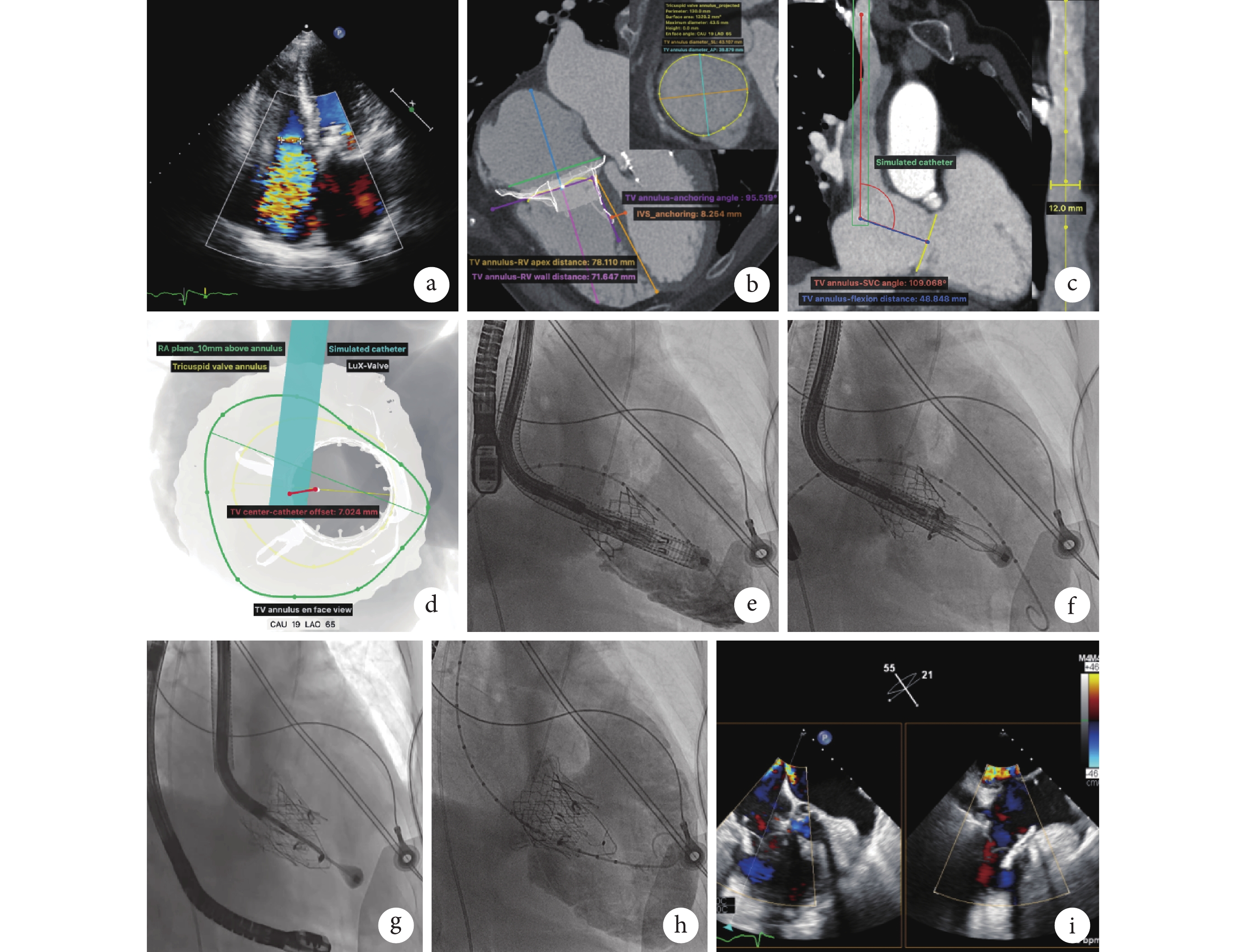 圖1
患者圍手術期圖像
圖1
患者圍手術期圖像
a. 術前超聲心動圖檢查顯示三尖瓣重度反流,縮流頸寬度 14 mm,反流峰值速度 3.1 m/s;b、c. 術前評估瓣膜與右心結構參數;d. 模擬瓣膜植入;e~g. 術中右心室造影;h. 術后右心室造影顯示人工三尖瓣位置穩定;i. 術后即刻超聲心動圖檢查顯示人工三尖瓣平均跨瓣壓 2 mm Hg(1 mm Hg=0.133 kPa),微量瓣周漏,瓣膜功能良好
經心臟團隊討論,患者此次病情惡化原因主要為經導管二尖瓣置換術后 TR 未改善與右心衰竭,有三尖瓣干預指征,但是由于高齡與合并癥情況導致外科開胸三尖瓣手術風險高(美國胸外科醫師協會死亡風險預測評分為 19.4%),因此擬評估患者是否適合經導管三尖瓣置換術(transcatheter tricuspid valve replacement, TTVR)。
8 月 15 日行心電門控心臟增強 CT 與頸部血管增強 CT 血管成像,使用 FluoroCT 軟件(版本 3.0),通過多平面重建、曲面重建、最大密度投影、透視模擬等三維重建技術對右心與靜脈進行三維重建與測量分析(圖1b~1d),結果顯示:三尖瓣環周長 130 mm,瓣環隔側徑 43.1 mm,瓣環前后徑 39.9 mm,瓣環與錨定區室間隔夾角 95.5°,瓣環至右心室心尖距離 78.1 mm,瓣環至右心室游離壁距離 71.6 mm,瓣環軸線與上腔靜脈軸線夾角 109.1°,瓣環中心至模擬輸送系統調彎點距離 48.8 mm,頸靜脈-上腔靜脈入路最小徑線 12 mm,模擬輸送系統偏離瓣環中心距離 7.0 mm。綜合評估患者右心與靜脈結構 CT 影像學特征適宜 LuX-Valve Plus 頸靜脈入路 TTVR 系統(寧波健世科技股份有限公司)。
與患者及其家屬充分溝通并簽署知情同意書后,于 8 月 18 日在全身麻醉下經數字減影血管造影與經食管超聲引導下經頸靜脈入路行 TTVR。具體操作步驟:經皮建立右側頸內靜脈通路,通過導絲引入 LuX-Valve Plus 輸送系統并推進至右心房,將輸送系統調彎并跨三尖瓣瓣環進入右心室,通過將輸送系統調彎、整體回撤或旋轉,使之在前后方向、上下方向垂直于瓣環且經過其中心,實現與瓣環中心軸線的配準(圖1e)。適當調整輸送系統深度后,緩慢回撤外鞘以釋放室間隔錨定裝置與前瓣夾持裝置,隨后系統稍微向左側旋轉,并向右心房回撤,使前葉夾持裝置回鉤住前葉(圖1f)。確認系統位置和軸向后,釋放人工三尖瓣主體部分。調整人工三尖瓣植入深度、軸向與朝向,確保不存在明顯瓣周漏以及錨定裝置與室間隔之間的平行性。隨后將輸送系統向上方旋轉,使錨定裝置貼合室間隔,確認無明顯瓣周漏后,推進錨定針穿過錨定舌并扎入室間隔(圖1g),完全釋放人工三尖瓣,移除輸送系統。右心室造影和超聲心動圖提示人工三尖瓣位置穩定,微量瓣周漏,跨人工三尖瓣平均壓差 2 mm Hg(圖1h、1i)。
術后,患者入住心臟重癥監護室,予利尿、床旁持續性腎臟替代治療、抗凝、抗感染、控制血糖等治療,病情穩定后轉入普通病房繼續治療。患者術后 25 d 病情明顯改善,并于術后 34 d 順利出院。
討論 Framingham 心臟研究報告顯示,中度及以上 TR 患病率為 0.8%,且隨著年齡增長而上升[1]。美國 160 多萬中度或重度 TR 患者中,約一半患者的 TR 繼發于左側瓣膜病,且在二尖瓣疾病中更常見[2]。左側瓣膜介入治療若未處理三尖瓣,即使二尖瓣或主動脈瓣疾病被成功糾正(包括手術或經導管干預),TR 通常仍持續存在甚至進展,并對患者的預后產生不良影響,TR 的嚴重程度越高,患者的臨床癥狀越嚴重,6 個月存活率越低[3]。
二尖瓣狹窄或反流時,會引起左心房壓力升高,當嚴重程度過高時,會引起繼發性肺動脈高壓。長期肺動脈高壓可能促使右心室重塑和功能障礙,導致三尖瓣瓣環擴張、乳頭肌移位和三尖瓣瓣葉的融合,從而出現 TR;TR 本身會引起進一步的右心室重塑和功能障礙,以及更嚴重的瓣環擴張和瓣葉融合,使 TR 惡化。同時,左心房的壓力和大小增加也可能導致心房顫動,進而導致右心房擴張,使三尖瓣環更進一步擴張[4]。既往有研究發現,高齡、女性、心房顫動、術前左心房大小、術后二尖瓣反流≥Ⅱ級和三尖瓣環擴張(≥34 mm)是二尖瓣術后 TR 持續或進展的重要預測因素[5-6]。
二尖瓣手術中是否應同期對三尖瓣進行干預,目前尚無定論。盡管瓣膜病管理指南建議在進行左心瓣膜手術的患者中,若存在輕度或中度繼發性 TR 且伴有三尖瓣環擴張(≥40 mm 或>21 mm/m2)(Ⅱa 級推薦),或者存在重度繼發性 TR(Ⅰ級推薦),應考慮同期對三尖瓣進行外科修復或置換,因為該措施能促進右心室反向重塑,并改善環狀擴張時的功能狀態[7]。但有研究表明,外科三尖瓣成形術后 5 年內再次出現中重度 TR 的患者達 60%[8],10 年內需要再次三尖瓣手術的患者約占 20%[9]。另外,Atluri 等[10]報告在左心手術時外科修復三尖瓣的過程中,額外的手術步驟雖然可以治療右心衰竭,但代價是房室結損傷導致自體心臟傳導喪失。以上研究表明在二尖瓣術中同期行外科矯正 TR 的行為,并不能確保術后穩定的 TR 降低或預后的改善。同時,同期行三尖瓣介入治療的優先級也不高。基于血流動力學,對于二尖瓣病變伴有 TR 的情況,優先處理二尖瓣后,能減輕左心負荷,誘導左心室逆重構,使肺動脈壓力下降,從而右心負荷也隨之減輕,TR 程度也可能隨之降低[11],因此可以在一定程度上避免不必要的三尖瓣介入治療。
而在分期經導管瓣膜介入治療方面,曾有少量研究報道了分期處理二尖瓣和三尖瓣的可行性。Toselli 等[12]報道了一例重度二尖瓣反流伴重度 TR 患者在經導管二尖瓣緣對緣修復術后 2 個月,又接受了經導管三尖瓣緣對緣修復,術后 6 個月隨訪時二尖瓣反流降至中度,TR 降至輕度。Staubach 等[13]報道了一例曾接受經導管二尖瓣緣對緣修復的患者,6 年后因急性心力衰竭入院接受了經導管三尖瓣緣對緣修復術,術后 1 年隨訪時,TR 由術前的重度降至輕微,心力衰竭癥狀緩解。因此,分期進行瓣膜介入手術為無法耐受外科手術高風險的多瓣膜病變患者提供了新的治療選擇。
此外,如前所述,雖然二尖瓣術后 TR 程度可能降低,但 Kavsur 等[6]也報道了三尖瓣環擴張阻礙了經導管二尖瓣緣對緣修復術后的 TR 消退,因此分期介入有助于在二尖瓣術后更準確地評估 TR 的真實情況,從而采取更好的決策,為后續三尖瓣的介入治療創造有利條件。二尖瓣與三尖瓣的分期處理能最大限度地改善患者的預后和結局,減少治療相關的風險和并發癥。
近年來,三尖瓣的經導管介入治療飛速發展,治療方法主要分為修復和置換兩大類。與修復相比,置換對 TR 的小葉形態或病因的依賴程度較低,且大大降低了開胸手術相關并發癥發生率和病死率[14]。目前適用于 TTVR 的瓣膜主要有 Evoque、NaviGate 以及 LuX-Valve[14]。首例使用 LuX-Valve 行 TTVR 的研究結果顯示,手術成功率為 97.8%,82.6%的患者術后 TR 程度下降 2 級,術后半年病死率為 17.4%,臨床癥狀得到顯著改善[15]。
在本病例中,患者入院診斷為重度繼發性 TR、右心衰竭(心功能Ⅳ級)、心房顫動、2 型糖尿病和慢性腎功能不全,高齡且合并癥多。由于 TR 的傳統開胸手術圍手術期病死率高、術中出血量多、術后恢復時間長、預后不佳[16],患者顯然無法承受行外科三尖瓣修復所帶來的開胸手術和體外循環的打擊。即使進行保守治療,對 TR 的藥物治療也主要限于利尿劑,而其通常不能成功緩解癥狀[17]。因此,經導管瓣膜介入治療成為該患者的唯一選擇。
由于三尖瓣結構和部位的特殊性,盡管國際上一直致力于研發 TTVR 技術,但國內開展難度大、例數少,主要的阻力源于三尖瓣復雜的解剖結構:① 三尖瓣具有復雜的瓣下成分,包括多個腱索和乳頭肌,增加了卡住的風險,阻礙了裝置的可操作性;② 瓣環呈 D 形,在心臟周期內是動態的,高度依賴于血管內體積和血流動力學條件;③ 三尖瓣環與房室結和希氏系統之間的密切解剖關系可能導致傳導障礙的新發或惡化,特別是原位置換術中;④ 右冠狀動脈中段和遠段位于房室溝內,靠近三尖瓣環(某些點<3 mm),這增加了環成形術和置換術中急性冠狀動脈壓迫的風險;⑤ 下腔靜脈通往右心房和三尖瓣之間的距離較短,使得輸送系統到達預期的適當同軸定位更具挑戰性,因為需要在相對較小的腔內急劇彎曲[18],這些都使 TTVR 操作非常困難,對術者的技術和經驗都是考驗。
目前經導管多瓣膜手術治療的臨床經驗和結果數據有限,且既往鮮見有報道經導管二尖瓣置換術后行 TTVR 的案例。本病例為臨床上高危多瓣膜患者的治療提供了新思路,當患者高齡或存在其他嚴重合并癥時,可根據患者病情考慮分期經導管介入治療,即優先處理最嚴重或緊要的瓣膜后,再根據術后其他病變瓣膜的情況再行二次處理。
利益沖突:所有作者聲明不存在利益沖突。
病例介紹 患者,女性,80 歲,因“勞力性呼吸困難 10+年,加重伴下肢水腫 1 周”于 2022 年 8 月 7 日入四川大學華西醫院(以下簡稱“我院”)心臟內科。入院前 10+年患者漸出現勞力性呼吸困難,活動耐量下降,間斷伴夜間陣發性呼吸困難以及雙下肢水腫,多次于外院予藥物治療(具體不詳),效果欠佳。入院前 2 個月患者病情加重,出現端坐呼吸,于我院行超聲心動圖檢查提示二尖瓣瓣葉嚴重增厚鈣化、重度狹窄伴中度反流,且合并重度三尖瓣反流(tricuspid regurgitation, TR)與中度主動脈瓣狹窄,遂使用球擴式經導管瓣膜系統(PrizValve,上海紐脈醫療科技有限公司)經股靜脈入路行經導管二尖瓣置換術,術后癥狀改善。入院前 1 周患者病情惡化,再次出現勞力性呼吸困難和雙下肢水腫,無夜間陣發性呼吸困難或端坐呼吸,調整利尿藥物后癥狀無明顯改善,遂再次收入我院心臟內科治療。患者既往一般情況稍差,否認肝炎、結核或其他傳染病史,預防接種史不詳,對頭孢類藥物過敏;有肩胛外傷致骨裂微創手術史;糖尿病史 2+年,平時未規律控制血糖;既往有心房顫動病史;無輸血史,無其他特殊病史。
入院體格檢查:體溫 36.5℃,脈搏 68 次/min,呼吸頻率 18 次/min,血壓 110/70 mm Hg(1 mm Hg=0.133 kPa)。2022 年 8 月 11 日經胸超聲心動圖檢查顯示(圖1a):經導管二尖瓣置換術后人工二尖瓣瓣周輕度反流,平均跨瓣壓差 6 mm Hg,三尖瓣重度反流(縮流頸寬度 14 mm,反流峰值速度 3.1 m/s),主動脈瓣中度狹窄(平均跨瓣壓差 22 mm Hg);右心增大(右心室前后徑 29 mm,右心房中部橫徑 48 mm),右心室收縮功能降低(三尖瓣側瓣環收縮期位移 10 mm),估測肺動脈收縮壓 53 mm Hg。8 月 15 日實驗室檢查提示:血紅蛋白 113 g/L,國際標準化比值 1.18,總膽紅素 31.4 μmol/L,血清肌酐 134 μmol/L,估算腎小球濾過率 32.26 mL/(min·1.73 m2),氨基末端腦利尿鈉肽前體
 圖1
患者圍手術期圖像
圖1
患者圍手術期圖像
a. 術前超聲心動圖檢查顯示三尖瓣重度反流,縮流頸寬度 14 mm,反流峰值速度 3.1 m/s;b、c. 術前評估瓣膜與右心結構參數;d. 模擬瓣膜植入;e~g. 術中右心室造影;h. 術后右心室造影顯示人工三尖瓣位置穩定;i. 術后即刻超聲心動圖檢查顯示人工三尖瓣平均跨瓣壓 2 mm Hg(1 mm Hg=0.133 kPa),微量瓣周漏,瓣膜功能良好
經心臟團隊討論,患者此次病情惡化原因主要為經導管二尖瓣置換術后 TR 未改善與右心衰竭,有三尖瓣干預指征,但是由于高齡與合并癥情況導致外科開胸三尖瓣手術風險高(美國胸外科醫師協會死亡風險預測評分為 19.4%),因此擬評估患者是否適合經導管三尖瓣置換術(transcatheter tricuspid valve replacement, TTVR)。
8 月 15 日行心電門控心臟增強 CT 與頸部血管增強 CT 血管成像,使用 FluoroCT 軟件(版本 3.0),通過多平面重建、曲面重建、最大密度投影、透視模擬等三維重建技術對右心與靜脈進行三維重建與測量分析(圖1b~1d),結果顯示:三尖瓣環周長 130 mm,瓣環隔側徑 43.1 mm,瓣環前后徑 39.9 mm,瓣環與錨定區室間隔夾角 95.5°,瓣環至右心室心尖距離 78.1 mm,瓣環至右心室游離壁距離 71.6 mm,瓣環軸線與上腔靜脈軸線夾角 109.1°,瓣環中心至模擬輸送系統調彎點距離 48.8 mm,頸靜脈-上腔靜脈入路最小徑線 12 mm,模擬輸送系統偏離瓣環中心距離 7.0 mm。綜合評估患者右心與靜脈結構 CT 影像學特征適宜 LuX-Valve Plus 頸靜脈入路 TTVR 系統(寧波健世科技股份有限公司)。
與患者及其家屬充分溝通并簽署知情同意書后,于 8 月 18 日在全身麻醉下經數字減影血管造影與經食管超聲引導下經頸靜脈入路行 TTVR。具體操作步驟:經皮建立右側頸內靜脈通路,通過導絲引入 LuX-Valve Plus 輸送系統并推進至右心房,將輸送系統調彎并跨三尖瓣瓣環進入右心室,通過將輸送系統調彎、整體回撤或旋轉,使之在前后方向、上下方向垂直于瓣環且經過其中心,實現與瓣環中心軸線的配準(圖1e)。適當調整輸送系統深度后,緩慢回撤外鞘以釋放室間隔錨定裝置與前瓣夾持裝置,隨后系統稍微向左側旋轉,并向右心房回撤,使前葉夾持裝置回鉤住前葉(圖1f)。確認系統位置和軸向后,釋放人工三尖瓣主體部分。調整人工三尖瓣植入深度、軸向與朝向,確保不存在明顯瓣周漏以及錨定裝置與室間隔之間的平行性。隨后將輸送系統向上方旋轉,使錨定裝置貼合室間隔,確認無明顯瓣周漏后,推進錨定針穿過錨定舌并扎入室間隔(圖1g),完全釋放人工三尖瓣,移除輸送系統。右心室造影和超聲心動圖提示人工三尖瓣位置穩定,微量瓣周漏,跨人工三尖瓣平均壓差 2 mm Hg(圖1h、1i)。
術后,患者入住心臟重癥監護室,予利尿、床旁持續性腎臟替代治療、抗凝、抗感染、控制血糖等治療,病情穩定后轉入普通病房繼續治療。患者術后 25 d 病情明顯改善,并于術后 34 d 順利出院。
討論 Framingham 心臟研究報告顯示,中度及以上 TR 患病率為 0.8%,且隨著年齡增長而上升[1]。美國 160 多萬中度或重度 TR 患者中,約一半患者的 TR 繼發于左側瓣膜病,且在二尖瓣疾病中更常見[2]。左側瓣膜介入治療若未處理三尖瓣,即使二尖瓣或主動脈瓣疾病被成功糾正(包括手術或經導管干預),TR 通常仍持續存在甚至進展,并對患者的預后產生不良影響,TR 的嚴重程度越高,患者的臨床癥狀越嚴重,6 個月存活率越低[3]。
二尖瓣狹窄或反流時,會引起左心房壓力升高,當嚴重程度過高時,會引起繼發性肺動脈高壓。長期肺動脈高壓可能促使右心室重塑和功能障礙,導致三尖瓣瓣環擴張、乳頭肌移位和三尖瓣瓣葉的融合,從而出現 TR;TR 本身會引起進一步的右心室重塑和功能障礙,以及更嚴重的瓣環擴張和瓣葉融合,使 TR 惡化。同時,左心房的壓力和大小增加也可能導致心房顫動,進而導致右心房擴張,使三尖瓣環更進一步擴張[4]。既往有研究發現,高齡、女性、心房顫動、術前左心房大小、術后二尖瓣反流≥Ⅱ級和三尖瓣環擴張(≥34 mm)是二尖瓣術后 TR 持續或進展的重要預測因素[5-6]。
二尖瓣手術中是否應同期對三尖瓣進行干預,目前尚無定論。盡管瓣膜病管理指南建議在進行左心瓣膜手術的患者中,若存在輕度或中度繼發性 TR 且伴有三尖瓣環擴張(≥40 mm 或>21 mm/m2)(Ⅱa 級推薦),或者存在重度繼發性 TR(Ⅰ級推薦),應考慮同期對三尖瓣進行外科修復或置換,因為該措施能促進右心室反向重塑,并改善環狀擴張時的功能狀態[7]。但有研究表明,外科三尖瓣成形術后 5 年內再次出現中重度 TR 的患者達 60%[8],10 年內需要再次三尖瓣手術的患者約占 20%[9]。另外,Atluri 等[10]報告在左心手術時外科修復三尖瓣的過程中,額外的手術步驟雖然可以治療右心衰竭,但代價是房室結損傷導致自體心臟傳導喪失。以上研究表明在二尖瓣術中同期行外科矯正 TR 的行為,并不能確保術后穩定的 TR 降低或預后的改善。同時,同期行三尖瓣介入治療的優先級也不高。基于血流動力學,對于二尖瓣病變伴有 TR 的情況,優先處理二尖瓣后,能減輕左心負荷,誘導左心室逆重構,使肺動脈壓力下降,從而右心負荷也隨之減輕,TR 程度也可能隨之降低[11],因此可以在一定程度上避免不必要的三尖瓣介入治療。
而在分期經導管瓣膜介入治療方面,曾有少量研究報道了分期處理二尖瓣和三尖瓣的可行性。Toselli 等[12]報道了一例重度二尖瓣反流伴重度 TR 患者在經導管二尖瓣緣對緣修復術后 2 個月,又接受了經導管三尖瓣緣對緣修復,術后 6 個月隨訪時二尖瓣反流降至中度,TR 降至輕度。Staubach 等[13]報道了一例曾接受經導管二尖瓣緣對緣修復的患者,6 年后因急性心力衰竭入院接受了經導管三尖瓣緣對緣修復術,術后 1 年隨訪時,TR 由術前的重度降至輕微,心力衰竭癥狀緩解。因此,分期進行瓣膜介入手術為無法耐受外科手術高風險的多瓣膜病變患者提供了新的治療選擇。
此外,如前所述,雖然二尖瓣術后 TR 程度可能降低,但 Kavsur 等[6]也報道了三尖瓣環擴張阻礙了經導管二尖瓣緣對緣修復術后的 TR 消退,因此分期介入有助于在二尖瓣術后更準確地評估 TR 的真實情況,從而采取更好的決策,為后續三尖瓣的介入治療創造有利條件。二尖瓣與三尖瓣的分期處理能最大限度地改善患者的預后和結局,減少治療相關的風險和并發癥。
近年來,三尖瓣的經導管介入治療飛速發展,治療方法主要分為修復和置換兩大類。與修復相比,置換對 TR 的小葉形態或病因的依賴程度較低,且大大降低了開胸手術相關并發癥發生率和病死率[14]。目前適用于 TTVR 的瓣膜主要有 Evoque、NaviGate 以及 LuX-Valve[14]。首例使用 LuX-Valve 行 TTVR 的研究結果顯示,手術成功率為 97.8%,82.6%的患者術后 TR 程度下降 2 級,術后半年病死率為 17.4%,臨床癥狀得到顯著改善[15]。
在本病例中,患者入院診斷為重度繼發性 TR、右心衰竭(心功能Ⅳ級)、心房顫動、2 型糖尿病和慢性腎功能不全,高齡且合并癥多。由于 TR 的傳統開胸手術圍手術期病死率高、術中出血量多、術后恢復時間長、預后不佳[16],患者顯然無法承受行外科三尖瓣修復所帶來的開胸手術和體外循環的打擊。即使進行保守治療,對 TR 的藥物治療也主要限于利尿劑,而其通常不能成功緩解癥狀[17]。因此,經導管瓣膜介入治療成為該患者的唯一選擇。
由于三尖瓣結構和部位的特殊性,盡管國際上一直致力于研發 TTVR 技術,但國內開展難度大、例數少,主要的阻力源于三尖瓣復雜的解剖結構:① 三尖瓣具有復雜的瓣下成分,包括多個腱索和乳頭肌,增加了卡住的風險,阻礙了裝置的可操作性;② 瓣環呈 D 形,在心臟周期內是動態的,高度依賴于血管內體積和血流動力學條件;③ 三尖瓣環與房室結和希氏系統之間的密切解剖關系可能導致傳導障礙的新發或惡化,特別是原位置換術中;④ 右冠狀動脈中段和遠段位于房室溝內,靠近三尖瓣環(某些點<3 mm),這增加了環成形術和置換術中急性冠狀動脈壓迫的風險;⑤ 下腔靜脈通往右心房和三尖瓣之間的距離較短,使得輸送系統到達預期的適當同軸定位更具挑戰性,因為需要在相對較小的腔內急劇彎曲[18],這些都使 TTVR 操作非常困難,對術者的技術和經驗都是考驗。
目前經導管多瓣膜手術治療的臨床經驗和結果數據有限,且既往鮮見有報道經導管二尖瓣置換術后行 TTVR 的案例。本病例為臨床上高危多瓣膜患者的治療提供了新思路,當患者高齡或存在其他嚴重合并癥時,可根據患者病情考慮分期經導管介入治療,即優先處理最嚴重或緊要的瓣膜后,再根據術后其他病變瓣膜的情況再行二次處理。
利益沖突:所有作者聲明不存在利益沖突。