引用本文: 鄭燚, 王瑤, 代禮, 王芳, 陳志文, 張凌, 王艷艷. 局部枸櫞酸抗凝在膿毒癥合并高乳酸血癥患者連續性腎臟替代治療中的應用. 華西醫學, 2024, 39(7): 1075-1081. doi: 10.7507/1002-0179.202406136 復制
版權信息: ?四川大學華西醫院華西期刊社《華西醫學》版權所有,未經授權不得轉載、改編
連續性腎臟替代治療(continuous renal replacement therapy, CRRT)是急危重癥患者常見的生命支持治療[1],有效的抗凝可以維持體外循環通暢,減少濾器凝血[2-3]。改善全球腎臟病預后組織指南推薦將局部枸櫞酸抗凝(regional citrate anticoagulation, RCA)作為無枸櫞酸抗凝禁忌證患者的首選[4],相較于無肝素抗凝和低分子肝素抗凝,RCA 可顯著延長體外循環壽命且降低出血風險[5-7]。枸櫞酸在線粒體中通過三羧酸循環進行有氧代謝,伴高乳酸血癥患者組織灌注不足,會降低枸櫞酸代謝且增加枸櫞酸蓄積風險,通常被視為 RCA 的相對禁忌證[4]。且膿毒癥會導致線粒體功能顯著下降[8],進一步降低枸櫞酸代謝。近年來,許多研究已經證實高乳酸血癥并非 RCA 的絕對禁忌證[9-13],但膿毒癥伴高乳酸血癥患者 RCA 的相關研究較少,缺少在不同初始乳酸水平患者中應用 RCA 安全性和有效性的深入探索。因此,本研究回顧性納入行 RCA-CRRT 膿毒癥患者的臨床資料,根據乳酸水平對患者進行分組分析,重點關注應用 RCA 后代謝并發癥發生率、濾器凝血事件、體外循環壽命以及住院期間死亡情況,進而評估在膿毒癥伴不同初始乳酸水平患者中應用 RCA 的安全性和有效性。
1 對象與方法
1.1 研究對象
回顧性納入 2021 年 5 月-2023 年 5 月在四川大學華西醫院行 RCA-CRRT 的膿毒癥患者。納入標準:① 年齡≥18 歲;② 明確診斷為膿毒癥;③ 首次 RCA-CRRT 治療持續時間≥24 h。排除標準:① 治療途中更改抗凝方式;② 已納入其他科研項目;③ CRRT 治療期間進行其他類型 RCA 血液凈化治療;④ 臨床資料缺失。本研究已獲得四川大學華西醫院倫理委員會批準,審批號為 2023 年審(1408)號。本研究為回顧性研究,不涉及任何干預措施,倫理委員會批準免除知情同意。
1.2 臨床資料收集
根據 CRRT 開始前初始乳酸水平將患者分為乳酸正常組(≤2.0 mmol/L)和高乳酸血癥組(>2.0 mmol/L)[14],收集患者 CRRT 開始前的臨床資料,包括性別、年齡、體質量指數、合并癥、平均動脈壓、氧合指數、序貫性器官功能衰竭評分(Sequential Organ Failure Assessment)、pH 值、碳酸氫根、血清鉀、血清鈉、血清離子鈣、乳酸水平、白蛋白、總膽紅素、肌酐、活化部分凝血活酶時間、國際標準化比值、降鈣素原、白細胞介素-6。收集患者結局指標,包括枸櫞酸蓄積、代謝性酸中毒、代謝性堿中毒、高鈉血癥、首個體外循環壽命、濾器凝血事件以及住院期間是否死亡。
1.3 RCA-CRRT 方法
CRRT 采用連續性靜-靜脈血液透析濾過后稀釋治療模式,置換液采用含鈣置換液(成都青山利康藥業股份有限公司),含無水葡萄糖 10.6 mmol/L、氯離子 118 mmol/L、鎂離子 0.797 mmol/L、鈣離子 1.6 mmol/L、鈉離子 113 mmol/L 以及 5%的碳酸氫鈉,置換液與透析液比值為 1∶1,治療劑量為 25~30 mL/(kg·h)。初始治療血流量為 150 mL/min,4%枸櫞酸鈉 180 mL/h,依據濾器后離子鈣維持在 0.25~0.35 mmol/L[15]動態調節。所有患者均使用 Prismaflex V8.0 機器(百特醫療用品貿易有限公司)和膜面積 1.5 m2 的 AN69-ST150 血液濾過器(百特醫療用品貿易有限公司)。
1.4 變量定義及分組
膿毒癥診斷標準:由宿主對感染的反應失調所引發的危及生命的器官功能障礙[16]。高乳酸血癥定義為血清乳酸>2.0 mmol/L[17],并將患者劃分為中度高乳酸血癥(2 mmol/L<乳酸水平<4 mmol/L)和重度高乳酸血癥(乳酸水平≥4.0 mmol/L)[14]。枸櫞酸蓄積定義為充足的鈣劑補充后離子鈣仍顯著降低(<1.1 mmol/L),總鈣濃度增加,總鈣/離子鈣≥2.5[12, 18]。代謝性酸中毒定義為 pH 值<7.4,碳酸氫根水平<22 mmol/L[19];代謝性堿中毒定義為 pH 值>7.45,碳酸氫根水平>30 mmol/L[20-21]。高鈉血癥定義為血清鈉>145 mmol/L[22]。首個體外循環壽命定義為首個濾器從治療開始到治療停止間的時間間隔(上限為 72 h)[23]。濾器凝血事件定義為符合以下 3 種情況之一:跨膜壓>300 mm Hg(1 mm Hg=0.133 kPa)、循環管路或濾器中可見血栓、由于血栓阻塞無法啟動血泵[23-24]。
1.5 統計學方法
采用 SPSS 27.0 軟件進行統計分析及傾向評分匹配(propensity score matching, PSM)。服從正態分布的計量資料以均數±標準差表示,組間比較采用獨立樣本 t 檢驗;非正態分布的計量資料以中位數(下四分位數,上四分位數)表示,組間比較采用 Mann-Whitney U 檢驗;計數資料以頻數和百分比表示,組間比較采用χ2 檢驗或 Fisher 確切概率法。采用最近鄰匹配法以 1∶1 分別對正常乳酸組與高乳酸血癥組以及中度與重度高乳酸血癥組進行 PSM,卡鉗值為 0.05。采用 RStudio(v4.3.1)繪制首個體外循環管路的 Kaplan-Meier 曲線,組間比較采用 log-rank 檢驗。雙側檢驗水準 α=0.05。
2 結果
2.1 乳酸正常組與高乳酸血癥組的基線特征比較
共納入 441 例患者,其中男性 318 例,女性 123 例;乳酸正常組 228 例,高乳酸血癥組 213 例。PSM 前,乳酸正常組與高乳酸血癥組的肝衰竭比例、慢性腎臟病比例、平均動脈壓、碳酸氫根、總膽紅素、肌酐、活化部分凝血活酶時間、國際標準化比值、降鈣素原、白細胞介素-6 差異有統計學意義(P<0.05)。PSM 后,乳酸正常組與高乳酸血癥組均為 162 例患者。兩組患者的基線特征差異均無統計學意義(P>0.05),見表1。
2.2 乳酸正常組與高乳酸血癥組的結局指標比較
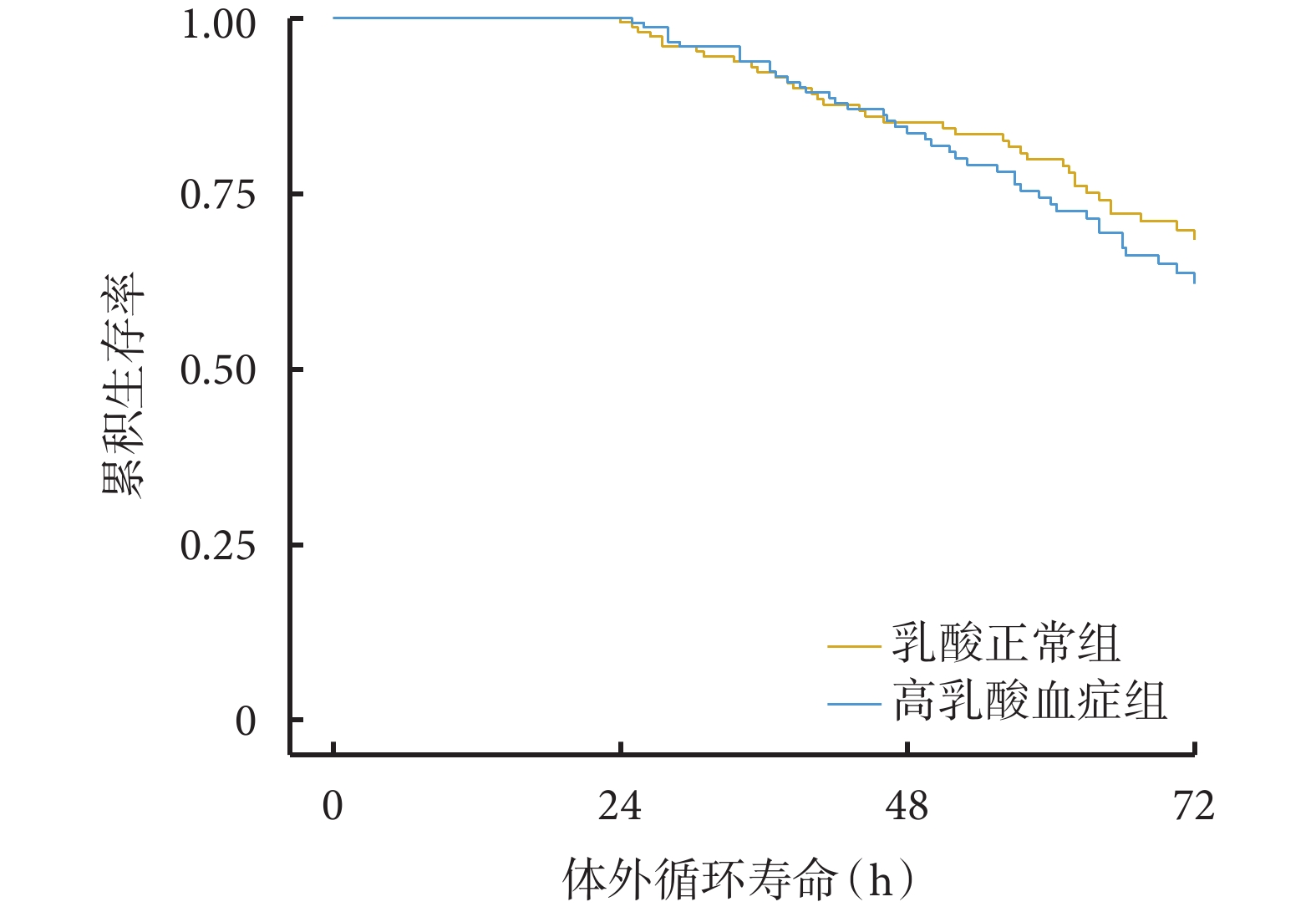
乳酸正常組與高乳酸血癥組的枸櫞酸蓄積發生率分別為 13.0%和 25.9%(P<0.05)。兩組的代謝性酸中毒、代謝性堿中毒、高鈉血癥、濾器凝血事件發生率以及住院期間死亡比例差異均無統計學意義(P>0.05),見表2。乳酸正常組首個體外循環壽命中位時間為 62 h,高乳酸血癥組首個體外循環壽命中位時間為 57.3 h。Kaplan-Meier 生存分析顯示,高乳酸血癥組與正常乳酸組首個體外循環壽命差異無統計學意義,風險比及 95%置信區間為 1.202[(0.774,1.865),P=0.414],見圖1。
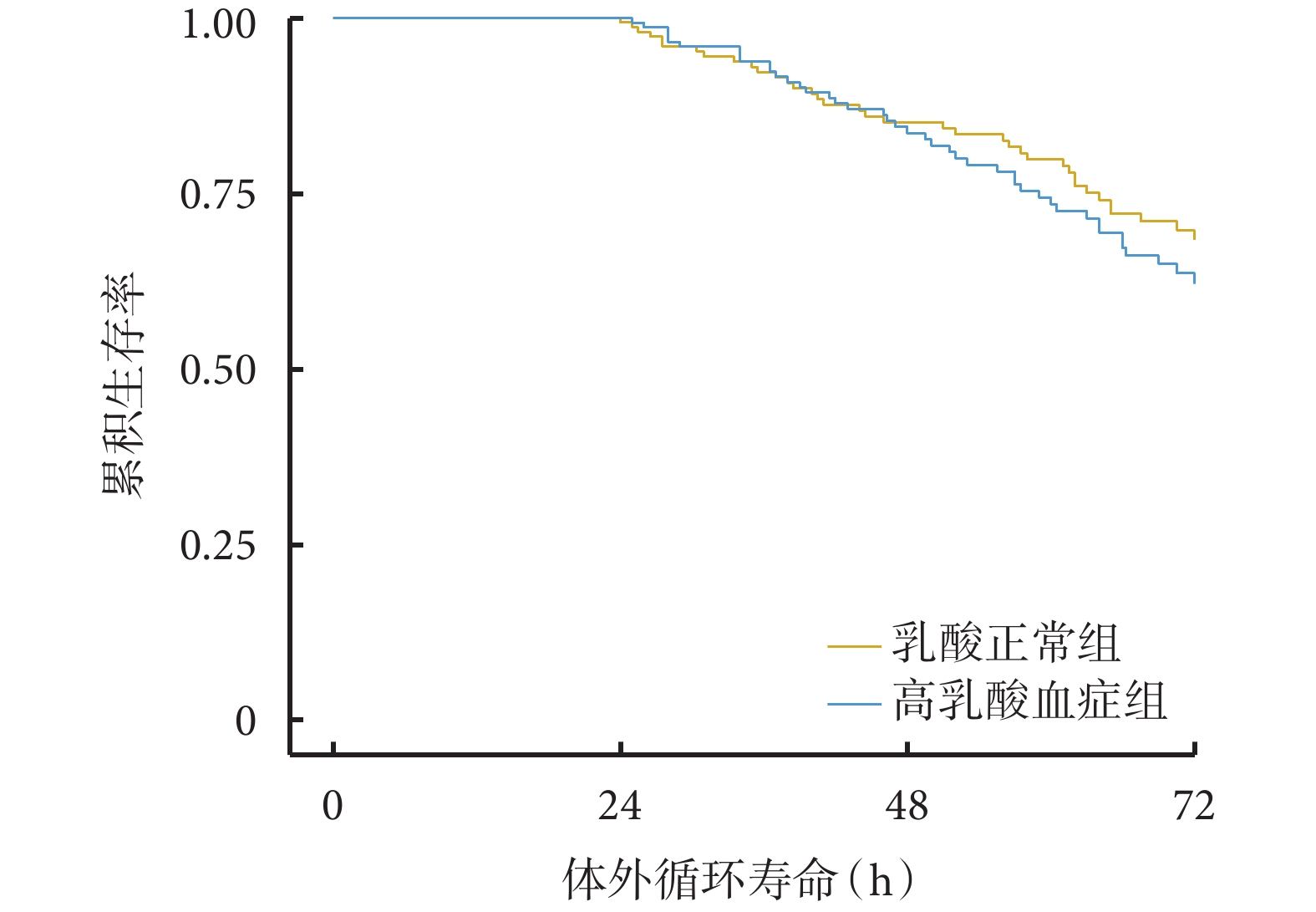 圖1
乳酸正常組與高乳酸血癥組的首個體外循環壽命 Kaplan-Meier 生存曲線
圖1
乳酸正常組與高乳酸血癥組的首個體外循環壽命 Kaplan-Meier 生存曲線
2.3 中度與重度高乳酸血癥組的基線特征比較
共納入 213 例高乳酸血癥患者,其中男性 151 例,女性 62 例;中度高乳酸血癥組 186 例,重度高乳酸血癥組 27 例。PSM 前,中度與重度高乳酸血癥組的男性比例、糖尿病比例、白蛋白水平、國際標準化比值、白細胞介素-6 差異均有統計學意義(P<0.05)。PSM 后,中度與重度高乳酸血癥組均為 22 例患者。兩組患者的基線特征差異均無統計學意義(P>0.05),見表3。
2.4 中度與重度高乳酸血癥組的結局指標比較
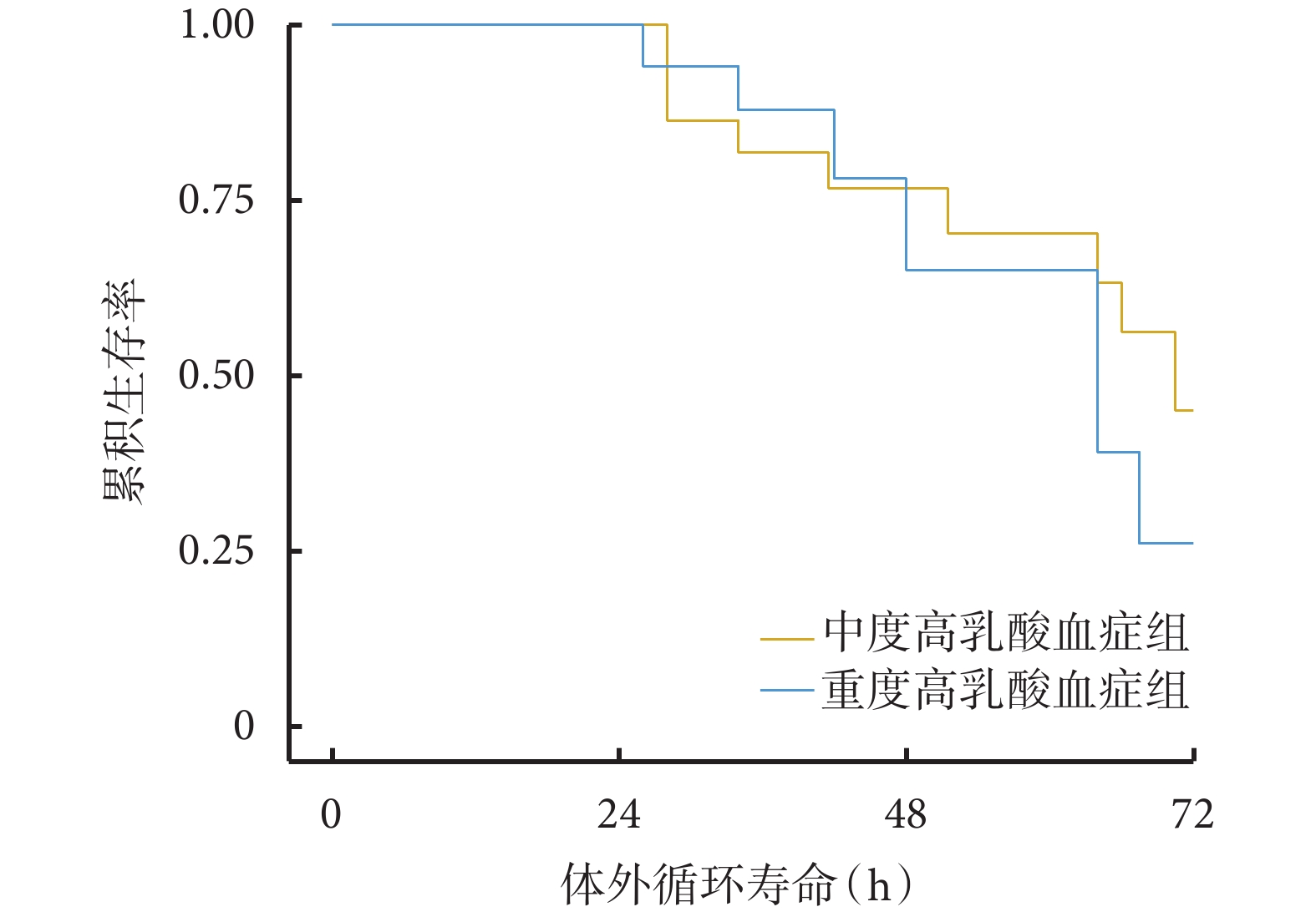
中度高乳酸血癥組與重度高乳酸血癥組的枸櫞酸蓄積發生率分別為 18.2%和 50.0%(P<0.05)。兩組的代謝性酸中毒、代謝性堿中毒、高鈉血癥、濾器凝血事件發生率以及住院期間死亡比例差異均無統計學意義(P>0.05),見表4。中度高乳酸血癥組首個體外循環壽命中位時間為 57.5 h,重度高乳酸血癥組首個體外循環壽命中位時間為 40 h。Kaplan-Meier 生存分析顯示,中度高乳酸血癥組與重度高乳酸血癥組首個體外循環壽命差異無統計學意義,風險比及 95%置信區間為 1.429[(0.527,3.877),P=0.487],見圖2。
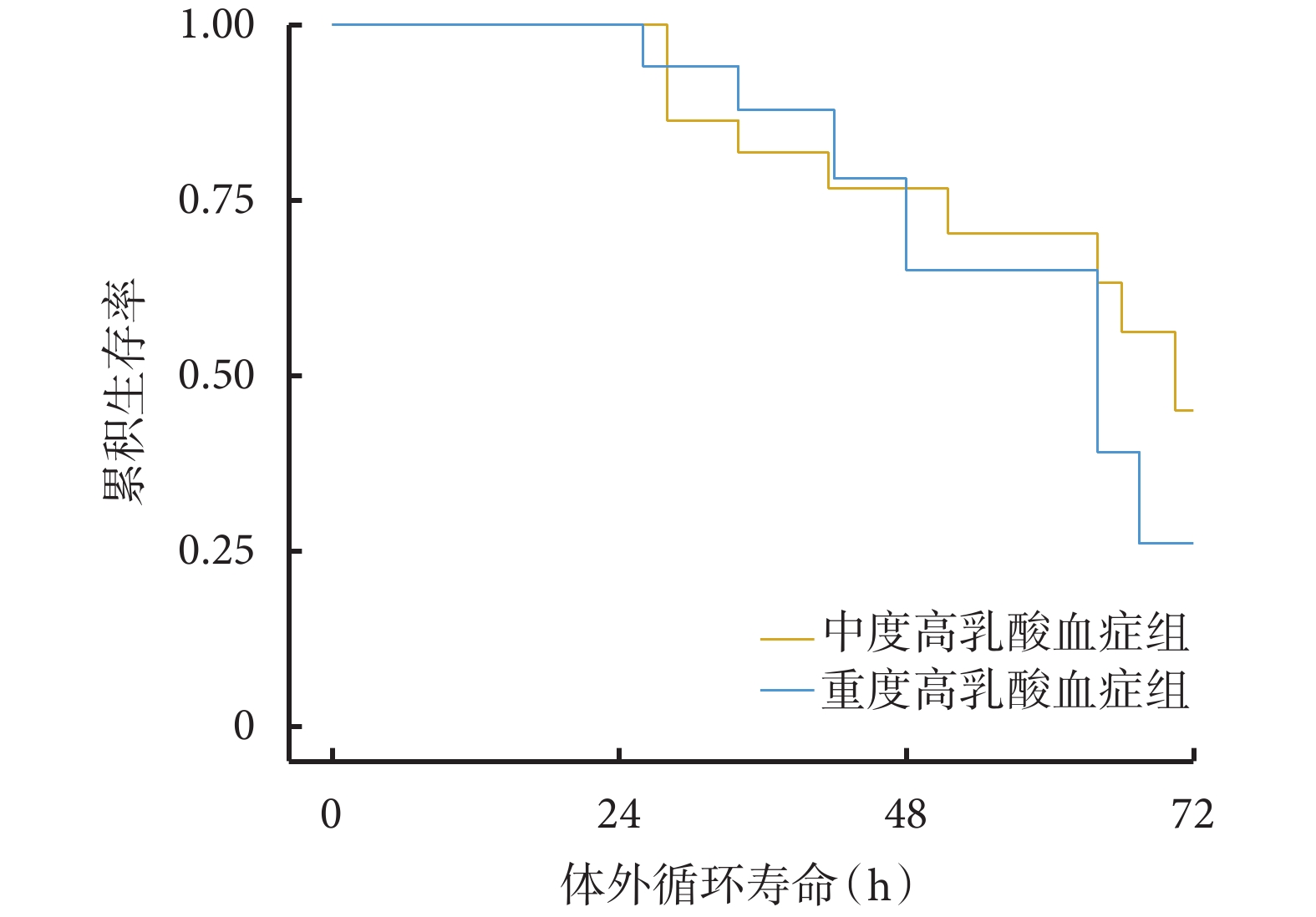 圖2
中度與重度高乳酸血癥組首個體外循環壽命 Kaplan-Meier 生存曲線
圖2
中度與重度高乳酸血癥組首個體外循環壽命 Kaplan-Meier 生存曲線
3 討論
本研究結果顯示,在膿毒癥患者 RCA-CRRT 中,高乳酸血癥組枸櫞酸蓄積發生率較高。既往研究也表明,伴高乳酸血癥患者的枸櫞酸蓄積發生率較高[12, 18],與本研究結果一致,這可能與高乳酸血癥通常提示組織低氧低灌注狀態,枸櫞酸鈉的代謝率降低,更易造成枸櫞酸蓄積相關。且與其他類型(肝硬化、肝衰竭、心臟外科術后)伴高乳酸血癥患者相比[11, 25-27],膿毒癥伴高乳酸血癥患者的枸櫞酸蓄積發生率更高,可能的原因是膿毒癥患者線粒體功能顯著下降。因此,在膿毒癥伴高乳酸血癥患者 CRRT 的 RCA 選擇上更應全面評估。但本研究結果顯示,兩組的住院期間死亡比例差異無統計學意義,表明住院期間死亡可能與 RCA決策無明顯相關。Li 等[5-6]的 2 項回顧性研究顯示,在伴高乳酸血癥患者 CRRT 的抗凝比較中,RCA效果優于低分子肝素和無肝素抗凝,本研究中體外循環壽命不低于 Li 等[5-6]的 2 項研究,說明 RCA 可應用于膿毒癥伴高乳酸血癥的 CRRT 患者。
本研究結果顯示,重度高乳酸組患者枸櫞酸蓄積發生率高于中度高乳酸組,這與先前的 2 項研究結果一致[14, 18]。隨著乳酸水平的升高,可能意味著更嚴重的組織灌注不足和線粒體功能障礙[28],枸櫞酸鈉代謝受損的風險升高,代謝并發癥發生率更高。因此,在重度高乳酸血癥患者 CRRT 中應謹慎選擇 RCA,動態評估患者血清乳酸水平,注意代謝并發癥,可逐步抗感染糾正血流動力學問題后,再嘗試應用 RCA。
綜上所述,本研究結果表明,膿毒癥伴高乳酸血癥患者的枸櫞酸蓄積發生率明顯升高,且重度高乳酸血癥患者的枸櫞酸蓄積發生率高于中度高乳酸血癥患者。因此,RCA 在膿毒癥伴高乳酸血癥患者 CRRT 的應用中應注意嚴密監測。建議在重度高乳酸血癥患者(乳酸≥4 mmol/L)中逐步糾正原發病后再嘗試選擇 RCA。但本研究為回顧性研究,尚需大樣本前瞻性研究來進一步驗證。
利益沖突:所有作者聲明不存在利益沖突。
連續性腎臟替代治療(continuous renal replacement therapy, CRRT)是急危重癥患者常見的生命支持治療[1],有效的抗凝可以維持體外循環通暢,減少濾器凝血[2-3]。改善全球腎臟病預后組織指南推薦將局部枸櫞酸抗凝(regional citrate anticoagulation, RCA)作為無枸櫞酸抗凝禁忌證患者的首選[4],相較于無肝素抗凝和低分子肝素抗凝,RCA 可顯著延長體外循環壽命且降低出血風險[5-7]。枸櫞酸在線粒體中通過三羧酸循環進行有氧代謝,伴高乳酸血癥患者組織灌注不足,會降低枸櫞酸代謝且增加枸櫞酸蓄積風險,通常被視為 RCA 的相對禁忌證[4]。且膿毒癥會導致線粒體功能顯著下降[8],進一步降低枸櫞酸代謝。近年來,許多研究已經證實高乳酸血癥并非 RCA 的絕對禁忌證[9-13],但膿毒癥伴高乳酸血癥患者 RCA 的相關研究較少,缺少在不同初始乳酸水平患者中應用 RCA 安全性和有效性的深入探索。因此,本研究回顧性納入行 RCA-CRRT 膿毒癥患者的臨床資料,根據乳酸水平對患者進行分組分析,重點關注應用 RCA 后代謝并發癥發生率、濾器凝血事件、體外循環壽命以及住院期間死亡情況,進而評估在膿毒癥伴不同初始乳酸水平患者中應用 RCA 的安全性和有效性。
1 對象與方法
1.1 研究對象
回顧性納入 2021 年 5 月-2023 年 5 月在四川大學華西醫院行 RCA-CRRT 的膿毒癥患者。納入標準:① 年齡≥18 歲;② 明確診斷為膿毒癥;③ 首次 RCA-CRRT 治療持續時間≥24 h。排除標準:① 治療途中更改抗凝方式;② 已納入其他科研項目;③ CRRT 治療期間進行其他類型 RCA 血液凈化治療;④ 臨床資料缺失。本研究已獲得四川大學華西醫院倫理委員會批準,審批號為 2023 年審(1408)號。本研究為回顧性研究,不涉及任何干預措施,倫理委員會批準免除知情同意。
1.2 臨床資料收集
根據 CRRT 開始前初始乳酸水平將患者分為乳酸正常組(≤2.0 mmol/L)和高乳酸血癥組(>2.0 mmol/L)[14],收集患者 CRRT 開始前的臨床資料,包括性別、年齡、體質量指數、合并癥、平均動脈壓、氧合指數、序貫性器官功能衰竭評分(Sequential Organ Failure Assessment)、pH 值、碳酸氫根、血清鉀、血清鈉、血清離子鈣、乳酸水平、白蛋白、總膽紅素、肌酐、活化部分凝血活酶時間、國際標準化比值、降鈣素原、白細胞介素-6。收集患者結局指標,包括枸櫞酸蓄積、代謝性酸中毒、代謝性堿中毒、高鈉血癥、首個體外循環壽命、濾器凝血事件以及住院期間是否死亡。
1.3 RCA-CRRT 方法
CRRT 采用連續性靜-靜脈血液透析濾過后稀釋治療模式,置換液采用含鈣置換液(成都青山利康藥業股份有限公司),含無水葡萄糖 10.6 mmol/L、氯離子 118 mmol/L、鎂離子 0.797 mmol/L、鈣離子 1.6 mmol/L、鈉離子 113 mmol/L 以及 5%的碳酸氫鈉,置換液與透析液比值為 1∶1,治療劑量為 25~30 mL/(kg·h)。初始治療血流量為 150 mL/min,4%枸櫞酸鈉 180 mL/h,依據濾器后離子鈣維持在 0.25~0.35 mmol/L[15]動態調節。所有患者均使用 Prismaflex V8.0 機器(百特醫療用品貿易有限公司)和膜面積 1.5 m2 的 AN69-ST150 血液濾過器(百特醫療用品貿易有限公司)。
1.4 變量定義及分組
膿毒癥診斷標準:由宿主對感染的反應失調所引發的危及生命的器官功能障礙[16]。高乳酸血癥定義為血清乳酸>2.0 mmol/L[17],并將患者劃分為中度高乳酸血癥(2 mmol/L<乳酸水平<4 mmol/L)和重度高乳酸血癥(乳酸水平≥4.0 mmol/L)[14]。枸櫞酸蓄積定義為充足的鈣劑補充后離子鈣仍顯著降低(<1.1 mmol/L),總鈣濃度增加,總鈣/離子鈣≥2.5[12, 18]。代謝性酸中毒定義為 pH 值<7.4,碳酸氫根水平<22 mmol/L[19];代謝性堿中毒定義為 pH 值>7.45,碳酸氫根水平>30 mmol/L[20-21]。高鈉血癥定義為血清鈉>145 mmol/L[22]。首個體外循環壽命定義為首個濾器從治療開始到治療停止間的時間間隔(上限為 72 h)[23]。濾器凝血事件定義為符合以下 3 種情況之一:跨膜壓>300 mm Hg(1 mm Hg=0.133 kPa)、循環管路或濾器中可見血栓、由于血栓阻塞無法啟動血泵[23-24]。
1.5 統計學方法
采用 SPSS 27.0 軟件進行統計分析及傾向評分匹配(propensity score matching, PSM)。服從正態分布的計量資料以均數±標準差表示,組間比較采用獨立樣本 t 檢驗;非正態分布的計量資料以中位數(下四分位數,上四分位數)表示,組間比較采用 Mann-Whitney U 檢驗;計數資料以頻數和百分比表示,組間比較采用χ2 檢驗或 Fisher 確切概率法。采用最近鄰匹配法以 1∶1 分別對正常乳酸組與高乳酸血癥組以及中度與重度高乳酸血癥組進行 PSM,卡鉗值為 0.05。采用 RStudio(v4.3.1)繪制首個體外循環管路的 Kaplan-Meier 曲線,組間比較采用 log-rank 檢驗。雙側檢驗水準 α=0.05。
2 結果
2.1 乳酸正常組與高乳酸血癥組的基線特征比較
共納入 441 例患者,其中男性 318 例,女性 123 例;乳酸正常組 228 例,高乳酸血癥組 213 例。PSM 前,乳酸正常組與高乳酸血癥組的肝衰竭比例、慢性腎臟病比例、平均動脈壓、碳酸氫根、總膽紅素、肌酐、活化部分凝血活酶時間、國際標準化比值、降鈣素原、白細胞介素-6 差異有統計學意義(P<0.05)。PSM 后,乳酸正常組與高乳酸血癥組均為 162 例患者。兩組患者的基線特征差異均無統計學意義(P>0.05),見表1。
2.2 乳酸正常組與高乳酸血癥組的結局指標比較
乳酸正常組與高乳酸血癥組的枸櫞酸蓄積發生率分別為 13.0%和 25.9%(P<0.05)。兩組的代謝性酸中毒、代謝性堿中毒、高鈉血癥、濾器凝血事件發生率以及住院期間死亡比例差異均無統計學意義(P>0.05),見表2。乳酸正常組首個體外循環壽命中位時間為 62 h,高乳酸血癥組首個體外循環壽命中位時間為 57.3 h。Kaplan-Meier 生存分析顯示,高乳酸血癥組與正常乳酸組首個體外循環壽命差異無統計學意義,風險比及 95%置信區間為 1.202[(0.774,1.865),P=0.414],見圖1。
 圖1
乳酸正常組與高乳酸血癥組的首個體外循環壽命 Kaplan-Meier 生存曲線
圖1
乳酸正常組與高乳酸血癥組的首個體外循環壽命 Kaplan-Meier 生存曲線
2.3 中度與重度高乳酸血癥組的基線特征比較
共納入 213 例高乳酸血癥患者,其中男性 151 例,女性 62 例;中度高乳酸血癥組 186 例,重度高乳酸血癥組 27 例。PSM 前,中度與重度高乳酸血癥組的男性比例、糖尿病比例、白蛋白水平、國際標準化比值、白細胞介素-6 差異均有統計學意義(P<0.05)。PSM 后,中度與重度高乳酸血癥組均為 22 例患者。兩組患者的基線特征差異均無統計學意義(P>0.05),見表3。
2.4 中度與重度高乳酸血癥組的結局指標比較
中度高乳酸血癥組與重度高乳酸血癥組的枸櫞酸蓄積發生率分別為 18.2%和 50.0%(P<0.05)。兩組的代謝性酸中毒、代謝性堿中毒、高鈉血癥、濾器凝血事件發生率以及住院期間死亡比例差異均無統計學意義(P>0.05),見表4。中度高乳酸血癥組首個體外循環壽命中位時間為 57.5 h,重度高乳酸血癥組首個體外循環壽命中位時間為 40 h。Kaplan-Meier 生存分析顯示,中度高乳酸血癥組與重度高乳酸血癥組首個體外循環壽命差異無統計學意義,風險比及 95%置信區間為 1.429[(0.527,3.877),P=0.487],見圖2。
 圖2
中度與重度高乳酸血癥組首個體外循環壽命 Kaplan-Meier 生存曲線
圖2
中度與重度高乳酸血癥組首個體外循環壽命 Kaplan-Meier 生存曲線
3 討論
本研究結果顯示,在膿毒癥患者 RCA-CRRT 中,高乳酸血癥組枸櫞酸蓄積發生率較高。既往研究也表明,伴高乳酸血癥患者的枸櫞酸蓄積發生率較高[12, 18],與本研究結果一致,這可能與高乳酸血癥通常提示組織低氧低灌注狀態,枸櫞酸鈉的代謝率降低,更易造成枸櫞酸蓄積相關。且與其他類型(肝硬化、肝衰竭、心臟外科術后)伴高乳酸血癥患者相比[11, 25-27],膿毒癥伴高乳酸血癥患者的枸櫞酸蓄積發生率更高,可能的原因是膿毒癥患者線粒體功能顯著下降。因此,在膿毒癥伴高乳酸血癥患者 CRRT 的 RCA 選擇上更應全面評估。但本研究結果顯示,兩組的住院期間死亡比例差異無統計學意義,表明住院期間死亡可能與 RCA決策無明顯相關。Li 等[5-6]的 2 項回顧性研究顯示,在伴高乳酸血癥患者 CRRT 的抗凝比較中,RCA效果優于低分子肝素和無肝素抗凝,本研究中體外循環壽命不低于 Li 等[5-6]的 2 項研究,說明 RCA 可應用于膿毒癥伴高乳酸血癥的 CRRT 患者。
本研究結果顯示,重度高乳酸組患者枸櫞酸蓄積發生率高于中度高乳酸組,這與先前的 2 項研究結果一致[14, 18]。隨著乳酸水平的升高,可能意味著更嚴重的組織灌注不足和線粒體功能障礙[28],枸櫞酸鈉代謝受損的風險升高,代謝并發癥發生率更高。因此,在重度高乳酸血癥患者 CRRT 中應謹慎選擇 RCA,動態評估患者血清乳酸水平,注意代謝并發癥,可逐步抗感染糾正血流動力學問題后,再嘗試應用 RCA。
綜上所述,本研究結果表明,膿毒癥伴高乳酸血癥患者的枸櫞酸蓄積發生率明顯升高,且重度高乳酸血癥患者的枸櫞酸蓄積發生率高于中度高乳酸血癥患者。因此,RCA 在膿毒癥伴高乳酸血癥患者 CRRT 的應用中應注意嚴密監測。建議在重度高乳酸血癥患者(乳酸≥4 mmol/L)中逐步糾正原發病后再嘗試選擇 RCA。但本研究為回顧性研究,尚需大樣本前瞻性研究來進一步驗證。
利益沖突:所有作者聲明不存在利益沖突。