引用本文: 韓龍飛, 林天燁, 何敏聰, 何曉銘, 詹芝瑋, 陸舜, 曾子俊, 林錕, 田佳慶, 侯文淵, 魏騰飛, 魏秋實. 脛骨平臺下低密度區骨量及體積對下肢力線影響的有限元分析. 中國修復重建外科雜志, 2024, 38(6): 734-741. doi: 10.7507/1002-1892.202312026 復制
版權信息: ?四川大學華西醫院華西期刊社《中國修復重建外科雜志》版權所有,未經授權不得轉載、改編
膝關節骨關節炎(knee osteoarthritis,KOA)是一種中老年人群常見的退行性疾病,其特點是關節軟骨破壞,主要表現為膝關節晨僵、疼痛及功能障礙,是該人群關節疼痛和殘疾的主要原因[1]。KOA發病率隨年齡增長而明顯增加。據報道,40歲以上人群KOA發病率為10%~17%,60歲以上人群約為50%,75歲以上人群高達80%,致殘率達53%[2]。骨質疏松癥是由多種原因導致的骨密度和骨質量下降,骨微結構破壞,造成骨脆性增加,從而容易發生骨折的全身性骨病[3]。關于骨質疏松癥與KOA的關系已有許多研究,但尚未達成統一意見[6]。有研究對比KOA與非膝部位關節炎骨密度,發現前者顯著低于后者[4]。目前對于KOA患者膝關節骨密度與疾病進展間的關系研究較多。有研究表明[5],KOA內翻畸形患者膝關節內側骨密度高于外側,并呈內外側不對稱性,這種不對稱性在KOA外翻畸形患者中也存在,即膝關節外側骨密度高于內側,揭示了骨密度值主要與關節間隙和脛股關節間的骨贅形成有關;但該研究骨密度測定僅局限于關節表面附近,不涉及脛骨平臺下。
目前,KOA與骨質疏松癥關系研究中多是將腰椎或股骨近端骨密度[7]作為診斷骨質疏松癥的指標。但KOA患者的軟骨下骨改變并非一成不變,疾病早期軟骨下骨厚度及骨密度降低,骨小梁孔隙率增加,骨小梁情況惡化;而晚期軟骨下骨變厚,伴有微斷裂和骨囊腫形成,提示脛骨平臺下骨小梁重塑過程可能導致低密度區的形成[8]。骨質疏松癥患者骨量及骨強度降低與骨折密切相關,而對于KOA患者,骨贅形成、軟骨骨化等一系列病理因素產生應力遮擋效應,進而導致軟骨下骨骨質流失,造成脛骨平臺下出現一定體積的低密度區改變[9]。但是鮮有研究者關注脛骨平臺下低密度區改變對KOA的影響。
本課題組前期通過觀察KOA患者X線片發現脛骨平臺下多有一定體積骨密度減少區,且隨膝內翻程度加大,脛骨平臺下低密度區范圍逐漸擴大,邊緣逐漸靠近內側[10]。然而KOA與脛骨平臺下骨密度減少之間的具體生物力學機制尚未明確。有限元分析相較于傳統力學分析方法結果更加準確[11],但目前尚無針對脛骨平臺下骨密度減少區的相關有限元研究。本研究采用有限元分析方法,進一步分析脛骨平臺下骨量減少與下肢力線偏移及內翻畸形的關系,為KOA患者內翻畸形的預測并指導早期干預提供生物力學依據。報告如下。
1 資料與方法
1.1 研究對象及研究設備、軟件
健康女性志愿者1名,年齡39歲,身高165 cm,體質量60 kg。排除雙側髖關節、膝關節、下肢及全身系統性疾病病史;骨與關節未見畸形、下肢力線無異常。
Mimics 21.0軟件(Materialise公司,比利時);Geomagic Wrap 2021軟件(Geomagic公司,美國);Solidworks 2023軟件、Abaqus 2022軟件(Dassault Systemes公司,美國)。臺式電腦:操作系統Windows 10 64位(DirectX 12);處理器Inter? CoreTM i7-8700 CPU@3.20GHz;RAM 32.0G;主顯卡:NVIDIA GeForce GTX 1080Ti。64排螺旋CT機(Siemens公司,德國),管電壓120 kV,管電流150 mA,掃描矩陣512×512,層厚1 mm,重建間距1.25 mm。
1.2 影像資料采集
受試者站立位,使雙髂前上棘位于同一水平,雙膝靠攏伸直,雙足并攏成中立位,獲取正位X線片。 受試者仰臥位,雙下肢放松,膝關節自然伸直,不施加任何外部載荷,以64排螺旋CT機對雙側下肢沿橫斷面連續掃描,通過不同分段掃描,獲得全下肢一系列掃描圖像1 734幅,文件以DICOM格式保存,通過光盤拷貝至計算機工作站。
1.3 建立實體模型
1.3.1 正常骨質膝關節有限元模型建立
為了使計算結果更真實,本研究構建了股骨、脛骨、腓骨皮質骨及松質骨,脛骨、股骨軟骨,半月板以及脛骨平臺下低密度區三維模型。具體方法:將DICOM格式CT影像數據導入Mimics 21.0軟件,使用閾值分割功能建立蒙版,使用多層蒙版編輯功能、填充命令進行修補,以符合正常解剖結構,最后生成三維圖像,導出為STL格式。松質骨由皮質骨向內腐蝕2個像素單位得到[12]。由于本院磁共振圖像圖層較少,通過MRI構建的軟組織形態不規則,所以通過在CT圖像上調整灰度值以構建軟骨和半月板,于Solidworks 2023軟件中將各部件通過原點裝配,并與《奈特人體解剖彩色圖譜》(第3版)下肢圖譜進行比較,在外觀上判斷模型可靠。將STL格式的各個部件導入Geomagic Wrap 2021軟件中,生成三維實體模型并保存為STEP格式。將各組件進行裝配,繪制下肢力線草圖,得到下肢力線與股骨解剖軸夾角為6.02°,股骨髁關節面切線與脛骨踝關節面切線水平,符合下肢正常解剖結構[13],外觀上驗證模型準確。見圖1。
 圖1
模型驗證及外觀
圖1
模型驗證及外觀
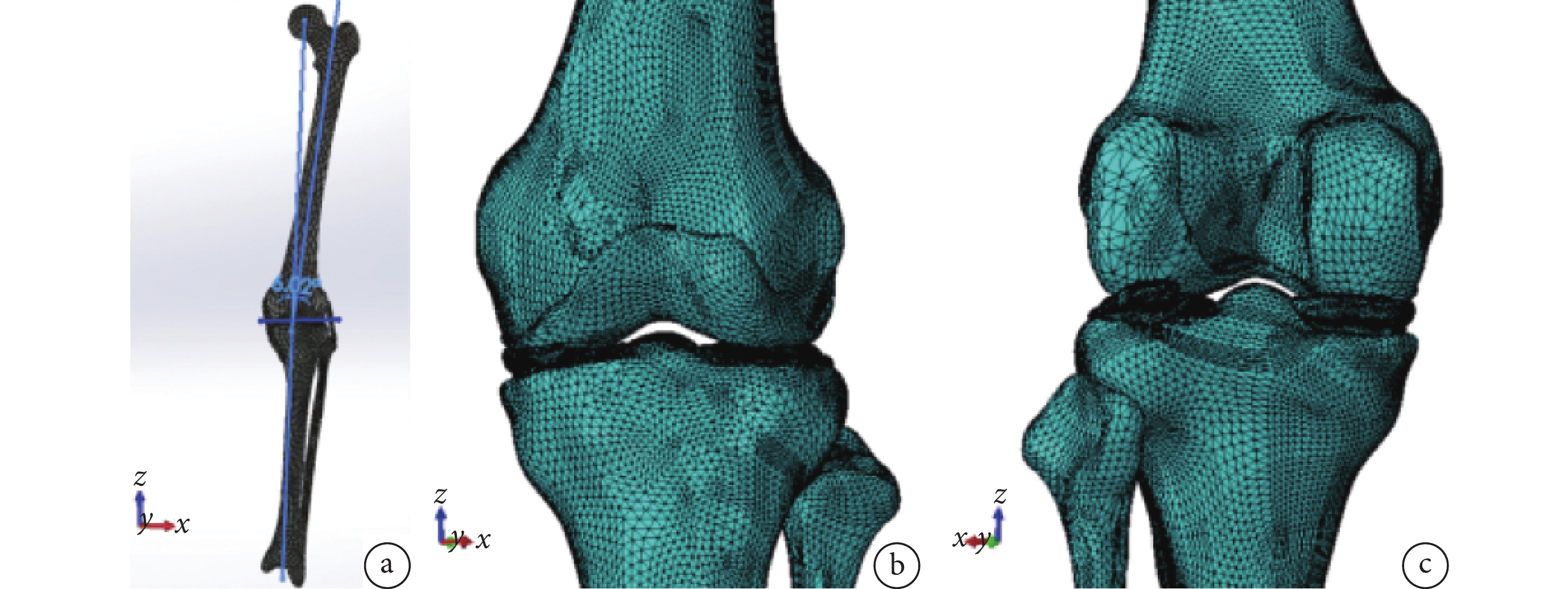
a. 下肢力線與股骨解剖軸夾角為6.02°;b. 膝關節模型前面觀;c. 膝關節模型后面觀
Figure1. Model validation and appearancea. The angle between the alignment and the anatomical axis of the femur was 6.02°; b. Anterior view of the knee joint model; c. Posterior view of the knee joint model
1.3.2 脛骨平臺下低密度區模型建立
基于本團隊前期研究在正位X線片中觀察到的脛骨平臺下低密度區形狀,采用Mimics 21.0軟件在受試者CT圖像中分別畫出3個體積相同 [(26 452±15)mm3]、形狀不同的低密度區模型,保存為STL格式并導入Geomagic Wrap 2021軟件中修飾光滑,生成實體,保存為STEP格式文件并導入Solidworks 2023軟件中,與正常膝關節模型進行配準。見圖2。
 圖2
脛骨平臺下低密度區模型構建
圖2
脛骨平臺下低密度區模型構建
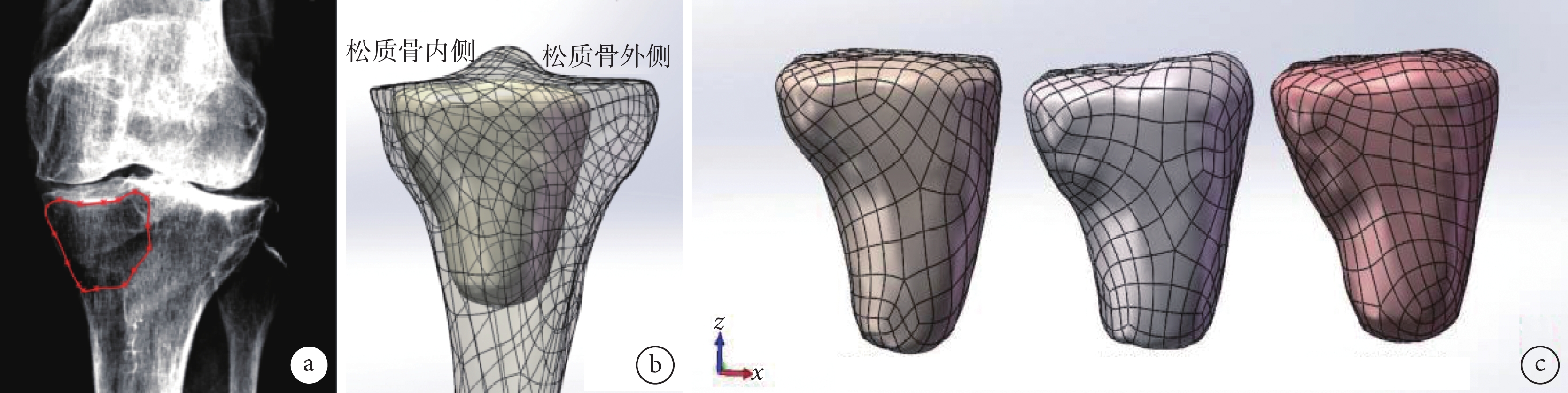
a. X線片上脛骨平臺下低密度區范圍;b. 脛骨平臺下低密度區模型與脛骨松質骨模型配準圖;c. 建立3個體積相同、形狀不同的低密度區模型
Figure2. Construction of the model of the low-density area under the tibial plateaua. Range of low-density area under the tibial plateau on X-ray film; b. Registration map of low-density area under the tibial plateau model and cancellous bone model of tibia; c. Three low-density area models with the same volume and different shapes
1.4 有限元分析
1.4.1 網格劃分、材料屬性
皮質骨和松質骨的網格大小為2.0 mm,軟骨、半月板、低密度區網格大小為1.0 mm。模型包含314 224個四面體單元,531 674個節點,網格類型為C3D10M。定義骨、軟骨、半月板為各向同性、線彈性材料[14]。研究脛骨平臺下低密度區骨量減少程度對膝關節的影響,本研究參考既往文獻(骨量減少和骨質疏松的松質骨彈性模量分別降低33%和66%)[15],設置5種不同骨量丟失程度,將脛骨平臺下低密度區模型彈性模量分別減少22%、33%、44%、55%、66%。各材料屬性賦值見表1。
1.4.2 接觸對設置、載荷及邊界條件
對膝關節不同結構建立接觸對,包括雙間室股骨軟骨與半月板、股骨軟骨與脛骨軟骨、脛骨軟骨與半月板、皮質骨與松質骨、脛骨與腓骨、股骨與股骨軟骨、脛骨與脛骨軟骨、脛骨下低密度區與脛骨松質骨。將骨與軟骨(股骨與股骨軟骨、脛骨與脛骨軟骨)、皮質骨與松質骨、脛骨與腓骨、脛骨軟骨與半月板、脛骨下低密度區與脛骨松質骨設置為綁定。因膝關節腔內含有較多關節液,具有潤滑作用,因此將股骨軟骨與半月板、股骨軟骨與脛骨軟骨之間接觸對設置為無摩擦的有限滑移接觸[18]。根據髖關節“頭臼接觸”理論[19],將載荷加載于股骨頭前外側,受力面積為1 172 mm2,與文獻 [20] 報道接近。
1.4.3 觀測指標
① 模型驗證:參考文獻 [21]方法,于股骨頭上表面沿下肢力線方向施加1 000 N軸向載荷,股骨約束屈伸方向的自由度,而3個平移自由度和旋轉自由度不做約束;脛、腓骨下端完全固定,約束6個方向自由度。進行模型驗證,測量脛骨皮質骨上表面內、外側間室,內、外側脛骨軟骨,內、外側半月板,內、外側股骨軟骨最大應力,并計算內、外側間室應力比。
② 骨量減少不同程度對應力及位移的影響:為模擬人行走過程中膝關節平均最大應力[22],在股骨頭上表面沿下肢力線方向施加1 860 N軸向載荷。脛、腓骨遠端完全固定,限制6個方向自由度,觀測脛骨平臺下低密度區骨量未減少組(1組)、骨量減少22%組(2組)、骨量減少33%組(3組)、骨量減少44%組(4組)、骨量減少55%組(5組)、骨量減少66%組(6組)的脛骨平臺最大應力及脛骨皮質骨、松質骨最大位移。
③ 不同體積低密度區對應力及位移的影響:為研究不同體積低密度區對脛骨內側平臺的影響,需要建立多組模型,通過Solidworks 2023軟件中縮放功能,將脛骨平臺下低密度區彈性模量減少66%的模型分別縮放81%、90%、100%、110%、121%,并分別與脛骨松質骨配準,生成5個不同體積 [分別為(14 064±23)、(19 292±35)、(26 463±53)、(35 223±69)、(46 882±87)mm3]的低密度區模型(分別設為B~F組),并以原始低密度區模型作為對照(A組)。同 ② 中方法施加載荷并檢測各組脛骨平臺最大應力及脛骨皮質骨、松質骨最大位移。
1.5 統計學方法
采用SPSS26.0統計軟件進行分析。計量資料經Shapiro-Wilk正態性檢驗,均符合正態分布,數據以均數±標準差表示,組間比較采用單因素方差分析,兩兩比較采用LSD檢驗;檢驗水準α=0.05。
2 結果
2.1 模型驗證
脛骨皮質骨上表面內、外側間室最大應力分別為(6.74±0.03)、(5.06±0.02)MPa,內、外側半月板最大應力分別為(12.87±0.09)、(7.24±0.06)MPa,內、外側脛骨軟骨最大應力分別為(2.46±0.02)、(5.30±0.05)MPa,內、外側股骨軟骨最大應力分別為(3.76±0.04)、(2.19±0.03)MPa,得出脛骨平臺內、外側間室應力比分別為56.83%±0.27%、43.17%±0.27%,與既往文獻 [18,23-24] 結果一致,驗證構建的模型準確。
2.2 骨量減少程度對應力及位移的影響
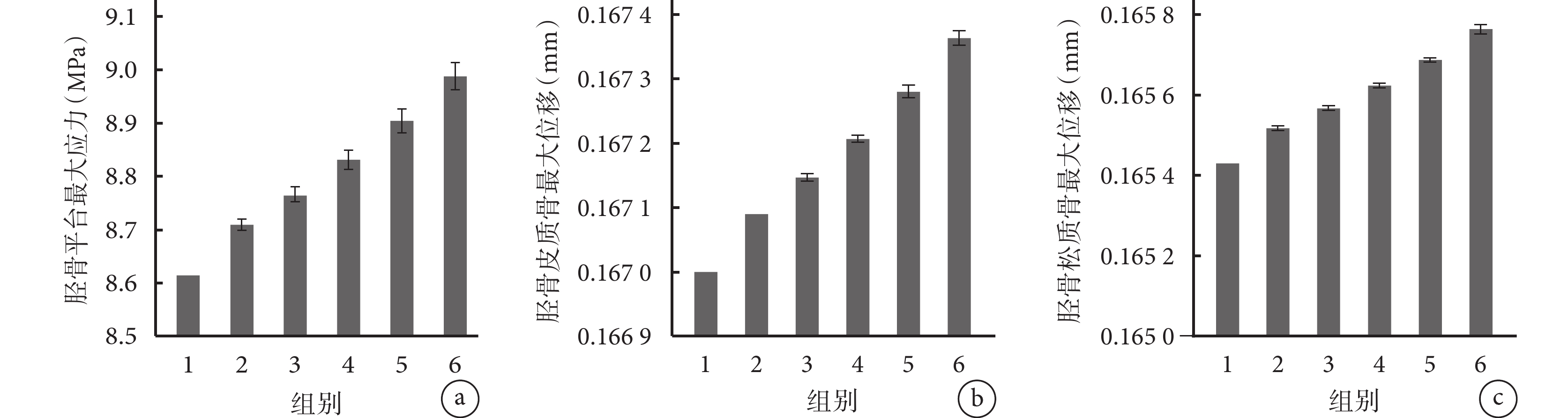
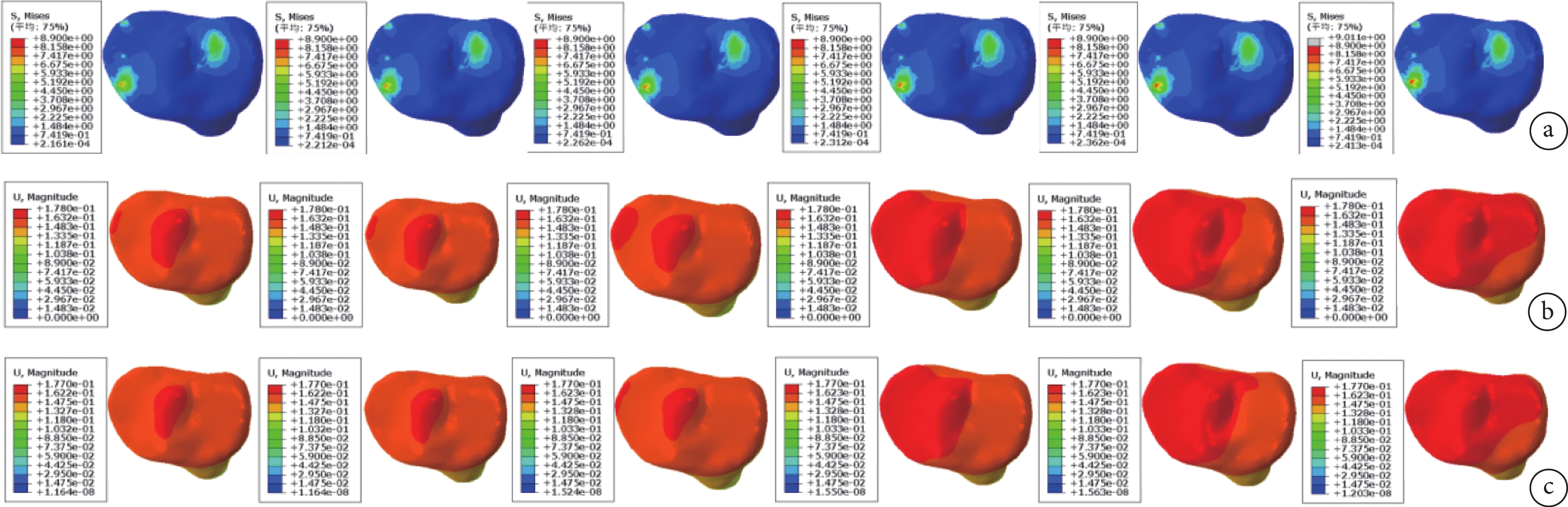
各組脛骨平臺最大應力及脛骨皮質骨、松質骨最大位移主要分布于脛骨平臺內側。隨著脛骨平臺下低密度區骨量逐漸減少,上述指標均隨之增大,各組間差異均有統計學意義(P<0.05)。見圖3、4。
 圖3
脛骨平臺下低密度區骨量丟失程度不同時各指標檢測
圖3
脛骨平臺下低密度區骨量丟失程度不同時各指標檢測
a. 脛骨平臺最大應力;b. 脛骨皮質骨最大位移;c. 脛骨松質骨最大位移
Figure3. Detection of various indicators of bone density loss in low-density areas under the tibial plateau with different degreesa. Maximum stress on tibial plateau; b. Maximum displacement of tibial cortical bone; c. Maximum displacement of tibial cancellous bone
 圖4
脛骨平臺下低密度區骨量丟失不同時應力及位移云圖
圖4
脛骨平臺下低密度區骨量丟失不同時應力及位移云圖
從左至右分別為1~6組 a. 脛骨平臺最大應力云圖;b. 脛骨皮質骨最大位移云圖;c. 脛骨松質骨最大位移云圖
Figure4. Stress and displacement cloud maps of low-density areas under the tibial plateau with varying degrees of bone density lossFrom left to right for groups 1-6 a. Cloud map of maximum stress on tibial plateau; b. Cloud map of maximum displacement of tibial cortical bone; c. Cloud map of maximum displacement of tibial cancellous bone
2.3 低密度區體積對應力及位移的影響
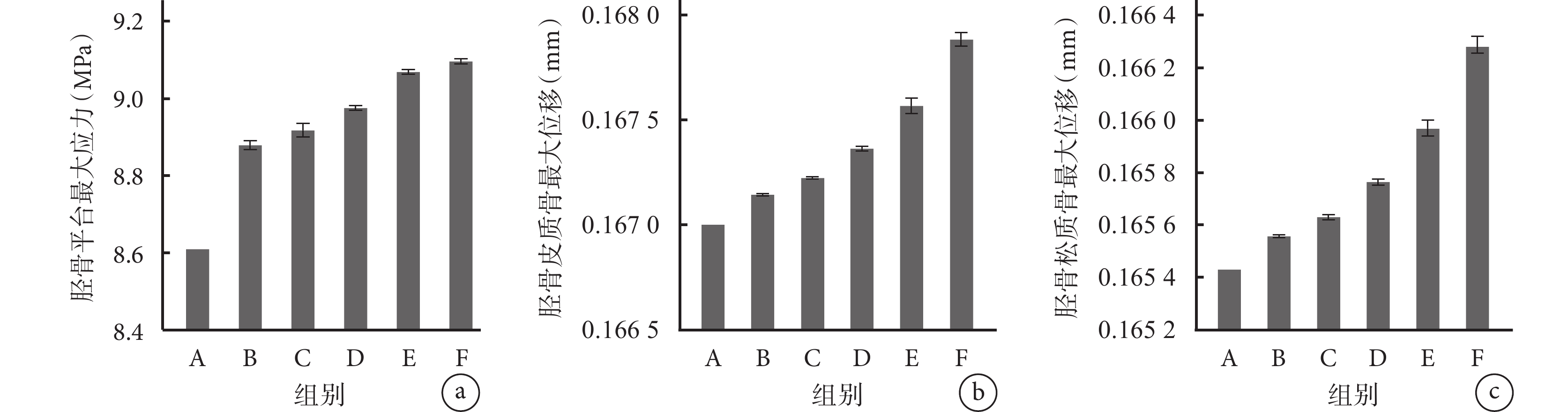
各組脛骨平臺最大應力及脛骨皮質骨、松質骨最大位移主要分布于脛骨平臺內側。隨著脛骨平臺下低密度區體積增大,上述指標均隨之增大,各組間差異均有統計學意義(P<0.05)。見圖5、6。
 圖5
不同體積脛骨平臺下低密度區各指標檢測
圖5
不同體積脛骨平臺下低密度區各指標檢測
a. 脛骨平臺最大應力;b. 脛骨皮質骨最大位移;c. 脛骨松質骨最大位移
Figure5. Detection of various indicators in low-density areas under the tibial plateau with different volumesa. Maximum stress on tibial plateau; b. Maximum displacement of tibial cortical bone; c. Maximum displacement of tibial cancellous bone
 圖6
不同體積脛骨平臺下低密度區應力及位移云圖
圖6
不同體積脛骨平臺下低密度區應力及位移云圖
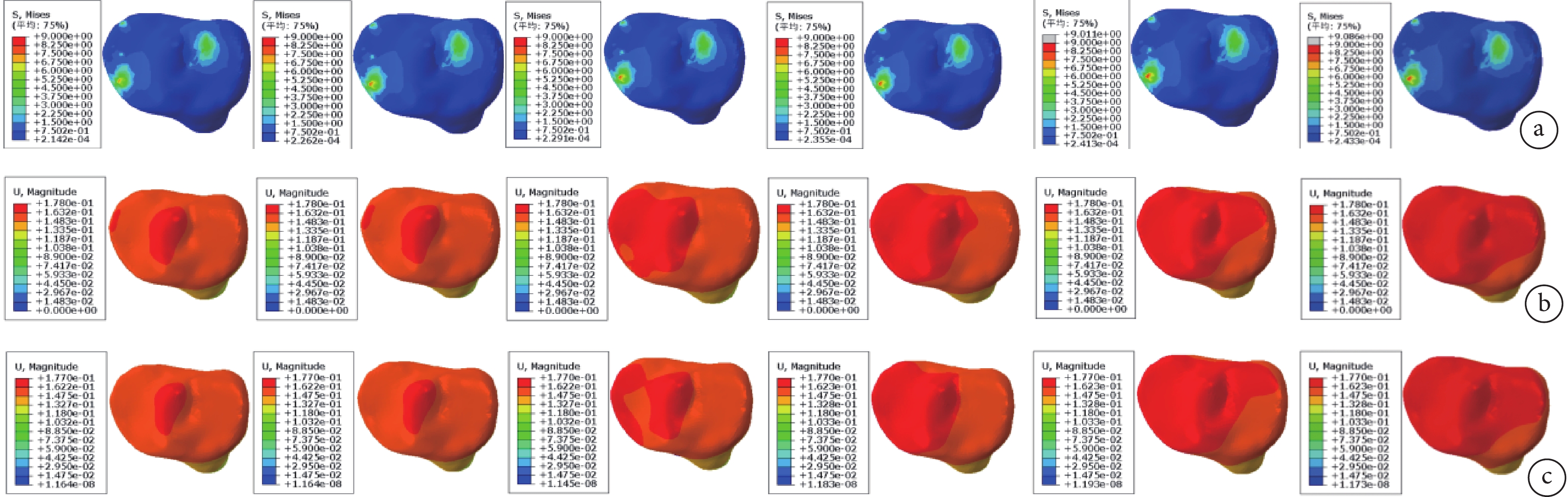
從左至右分別為A~F組 a. 脛骨平臺最大應力云圖;b. 脛骨皮質骨最大位移云圖;c. 脛骨松質骨最大位移云圖
Figure6. Stress and displacement cloud maps of low-density areas under the tibial plateau at different volumesFrom left to right for groups A-F a. Cloud map of maximum stress on tibial plateau; b: Cloud map of maximum displacement of tibial cortical bone; c. Cloud map of maximum displacement of tibial cancellous bone
3 討論
KOA是一種致殘性疾病,病程較長,若不及早治療干預,會加重患者膝關節內翻畸形。KOA診斷首選X線片,可表現為關節間隙狹窄、骨贅形成、軟骨下硬化和骨囊腫形成,最常用分級方法是Kellgren-Lawrence分類系統[25]。在病因方面,KOA可由創傷、應力、炎癥、生化反應及代謝紊亂引起[26],由于關節軟骨缺乏血管及神經支配,膝關節損傷早期階段不會發生疼痛,疼痛多由其他組織如關節囊、滑膜、軟骨下骨、韌帶和關節周圍肌肉引起,由軟骨缺損引起的疼痛則提示關節間隙狹窄。膝關節軟骨磨損是漸進過程,此過程中軟骨完整性受到破壞,軟骨面缺損明顯,粗糙欠平整,邊緣形成骨贅,軟骨下骨形成松質骨硬化灶,同時軟骨細胞減少、形態明顯改變,軟骨層纖維化且軟骨之間有孔隙分布[27]。軟骨基質作為軟骨細胞最重要的營養來源,其厚度減少將加重軟骨磨損和破壞。隨著膝關節內翻畸形進展,膝關節內側肌群神經肌肉活動上調,提示可能加重內側應力及畸形程度[28]。膝關節解剖結構特點也決定著KOA患者較易發展為膝內翻畸形。“不均勻沉降”理論[29]認為,脛骨平臺外側與腓骨之間牢固的支撐作用可防止膝外翻,而當關節軟骨發生退變、軟骨下骨骨髓水腫或脛骨平臺下骨密度降低時,容易引發力學性能較弱的軟骨下骨出現微骨折,從而繼發骨破壞、骨硬化及骨囊性變,進而導致膝關節應力增大及內翻加重。
骨質疏松癥是最常見的慢性代謝性骨病,其特征是骨量減少和骨微結構改變,骨脆性增加易導致軟骨下骨微骨折[30]。而KOA與骨質疏松癥之間關系的探討已有較多文獻報道,但二者相關性仍存在爭議[31-32]。多數研究者認為KOA與骨質疏松癥是負相關關系,骨質疏松癥的基本病理過程是骨量丟失,而KOA在關節附近的病理表現是骨質增生和骨贅形成,但KOA的病理過程也極為復雜。骨質疏松癥是一種全身性骨骼疾病,而KOA的骨質變化主要發生在軟骨下和鄰近的骺端區域。KOA患者關節軟骨病理表現為軟骨成骨及軟骨下骨硬化,體現為緊鄰關節的軟骨下骨增厚及密度增加。本課題組前期通過KOA患者X線片研究得出脛骨下低密度區不涉及脛骨皮質骨,只涉及脛骨平臺下松質骨。當KOA患者內側脛骨平臺所承受的應力較高時,脛骨平臺內側軟骨發生骨重塑,隨之軟骨下骨骨密度增高。而脛骨松質骨存在兩種結局,一是脛骨內側平臺皮質骨發生塌陷使應力傳遞至松質骨,隨之松質骨骨小梁硬化及斷裂,進而導致脛骨內側平臺皮質骨及松質骨骨密度均增高;二是脛骨內側平臺受到較大應力,軟骨及軟骨下皮質骨硬化且尚未塌陷時,由于應力遮擋效應,脛骨內側平臺松質骨骨量流失,進而形成低密度區改變。Li等[6]認為在關節炎早期,軟骨下骨及骨小梁呈骨質疏松樣,而進展到晚期,軟骨骨基質礦化,骨密度增高。研究表明骨質疏松是KOA患者內翻畸形的主要危險因素[33],而保持正常的骨密度值會延緩關節炎的進展[34]。那么骨質疏松癥與脛骨平臺下低密度區是否存在必然聯系呢?對于脛骨平臺下低密度區改變,文獻鮮有報道。本課題組前期研究只著重分析了KOA的不同分級與脛骨平臺下低密度區間的關系,并未涉及到骨質疏松癥與脛骨平臺下低密度區間的關系,故在未來研究中這兩者間的相關性需要重點闡明,有助于更好地理解KOA發病及進展的危險因素。脛骨平臺下低密度區改變實質是脛骨平臺下一定區域骨密度減少,伴或不伴有全身骨質疏松。根據本研究結果,模擬正常力線,從生物力學角度驗證脛骨平臺下骨密度的丟失能夠增大脛骨平臺的應力及位移,最大應力及位移均發生于內側,故膝關節逐漸內翻,隨之下肢力線逐漸內移;隨著力線內移,脛骨平臺應力及位移繼續增大,并形成不可逆轉的惡性循環。因此,脛骨平臺下低密度區的出現對于膝關節內翻畸形的預防具有重要意義。
有限元分析技術在膝關節內翻畸形研究中的應用逐漸普遍[35-38],但大部分研究較多關注具體術式,如膝關節單髁置換術、人工全膝關節置換術、脛骨高位截骨術等,較少有對KOA膝內翻機制過程的生物力學研究。本研究基于臨床觀察發現KOA患者脛骨平臺下低密度區的范圍與疾病進展相關[10],進而通過有限元分析進行驗證。結果顯示脛骨平臺下骨密度丟失越嚴重,相應脛骨平臺應力越大,位移也隨之越大。這可能是由于隨著松質骨密度丟失,對應力的承受能力下降,相應的脛骨皮質骨需要分擔更大應力,進而產生更大位移,進展為膝內翻畸形。而隨著脛骨下低密度區體積增大,脛骨平臺應力和位移也隨之增大。提示脛骨平臺下骨量減少的嚴重程度及范圍是預測膝內翻、力線內移的關鍵因素,對于臨床及早識別、及早干預具有重要意義。在治療上,目前公認的最佳矯正方式為力線經過“Fujisawa”點[39]。通過糾正力線,改變膝關節內、外側間室載荷的分布,從而減緩脛骨軟骨及軟骨下骨的骨重塑進程,延緩KOA的進展。同時,本研究也從生物力學角度驗證了團隊前期臨床觀察結果,表明脛骨平臺下低密度區需要引起足夠重視。
本研究存在一定局限性。首先,僅選取單例受試者構建單個模型,且脛骨平臺下低密度區的3個模型外形與松質骨邊緣不完全貼合,可能會對結果的準確性造成影響。其次,考慮到計算時間的影響,僅設定股骨軟骨與半月板、股骨軟骨與脛骨軟骨之間為無摩擦的有限滑移,而其他接觸關系皆為綁定,未考慮結構間的微動,也未能將膝關節周圍重要肌群及韌帶納入研究,可能會對結果造成影響。另外,本研究只進行靜力分析,未進行下肢動態的受力分析[40],動態分析相較于靜力分析能提供更全面的力學結果,對于理解膝關節受力狀態更具優勢。此外,對于骨質疏松與脛骨平臺下低密度區間的關系尚未見報道,對于理解KOA的發病及進展具有重要意義,有待今后繼續深入探討。
綜上述,本研究從生物力學角度闡釋了脛骨平臺下骨量減少可提示KOA膝內翻發生概率大大增加、力線內移趨勢明顯。因此,在臨床工作中要重視脛骨平臺下低密度區的改變,及早預防,避免膝內翻畸形發生及加重。
利益沖突 在課題研究和文章撰寫過程中不存在利益沖突;項目經費支持沒有影響文章觀點和對研究數據客觀結果的分析及其報道
倫理聲明 研究方案經廣州中醫藥大學第三附屬醫院倫理審查委員會批準(PJ-KY-20221227-018);研究對象知情同意
作者貢獻聲明 魏秋實:研究設計、經費支持;何敏聰、林天燁、何曉銘:研究設計、數據統計分析;詹芝瑋、陸舜、林錕、田佳慶、曾子俊、侯文淵、魏騰飛:負責應力計算,模型修改,數據獲取;韓龍飛:文稿撰寫
膝關節骨關節炎(knee osteoarthritis,KOA)是一種中老年人群常見的退行性疾病,其特點是關節軟骨破壞,主要表現為膝關節晨僵、疼痛及功能障礙,是該人群關節疼痛和殘疾的主要原因[1]。KOA發病率隨年齡增長而明顯增加。據報道,40歲以上人群KOA發病率為10%~17%,60歲以上人群約為50%,75歲以上人群高達80%,致殘率達53%[2]。骨質疏松癥是由多種原因導致的骨密度和骨質量下降,骨微結構破壞,造成骨脆性增加,從而容易發生骨折的全身性骨病[3]。關于骨質疏松癥與KOA的關系已有許多研究,但尚未達成統一意見[6]。有研究對比KOA與非膝部位關節炎骨密度,發現前者顯著低于后者[4]。目前對于KOA患者膝關節骨密度與疾病進展間的關系研究較多。有研究表明[5],KOA內翻畸形患者膝關節內側骨密度高于外側,并呈內外側不對稱性,這種不對稱性在KOA外翻畸形患者中也存在,即膝關節外側骨密度高于內側,揭示了骨密度值主要與關節間隙和脛股關節間的骨贅形成有關;但該研究骨密度測定僅局限于關節表面附近,不涉及脛骨平臺下。
目前,KOA與骨質疏松癥關系研究中多是將腰椎或股骨近端骨密度[7]作為診斷骨質疏松癥的指標。但KOA患者的軟骨下骨改變并非一成不變,疾病早期軟骨下骨厚度及骨密度降低,骨小梁孔隙率增加,骨小梁情況惡化;而晚期軟骨下骨變厚,伴有微斷裂和骨囊腫形成,提示脛骨平臺下骨小梁重塑過程可能導致低密度區的形成[8]。骨質疏松癥患者骨量及骨強度降低與骨折密切相關,而對于KOA患者,骨贅形成、軟骨骨化等一系列病理因素產生應力遮擋效應,進而導致軟骨下骨骨質流失,造成脛骨平臺下出現一定體積的低密度區改變[9]。但是鮮有研究者關注脛骨平臺下低密度區改變對KOA的影響。
本課題組前期通過觀察KOA患者X線片發現脛骨平臺下多有一定體積骨密度減少區,且隨膝內翻程度加大,脛骨平臺下低密度區范圍逐漸擴大,邊緣逐漸靠近內側[10]。然而KOA與脛骨平臺下骨密度減少之間的具體生物力學機制尚未明確。有限元分析相較于傳統力學分析方法結果更加準確[11],但目前尚無針對脛骨平臺下骨密度減少區的相關有限元研究。本研究采用有限元分析方法,進一步分析脛骨平臺下骨量減少與下肢力線偏移及內翻畸形的關系,為KOA患者內翻畸形的預測并指導早期干預提供生物力學依據。報告如下。
1 資料與方法
1.1 研究對象及研究設備、軟件
健康女性志愿者1名,年齡39歲,身高165 cm,體質量60 kg。排除雙側髖關節、膝關節、下肢及全身系統性疾病病史;骨與關節未見畸形、下肢力線無異常。
Mimics 21.0軟件(Materialise公司,比利時);Geomagic Wrap 2021軟件(Geomagic公司,美國);Solidworks 2023軟件、Abaqus 2022軟件(Dassault Systemes公司,美國)。臺式電腦:操作系統Windows 10 64位(DirectX 12);處理器Inter? CoreTM i7-8700 CPU@3.20GHz;RAM 32.0G;主顯卡:NVIDIA GeForce GTX 1080Ti。64排螺旋CT機(Siemens公司,德國),管電壓120 kV,管電流150 mA,掃描矩陣512×512,層厚1 mm,重建間距1.25 mm。
1.2 影像資料采集
受試者站立位,使雙髂前上棘位于同一水平,雙膝靠攏伸直,雙足并攏成中立位,獲取正位X線片。 受試者仰臥位,雙下肢放松,膝關節自然伸直,不施加任何外部載荷,以64排螺旋CT機對雙側下肢沿橫斷面連續掃描,通過不同分段掃描,獲得全下肢一系列掃描圖像1 734幅,文件以DICOM格式保存,通過光盤拷貝至計算機工作站。
1.3 建立實體模型
1.3.1 正常骨質膝關節有限元模型建立
為了使計算結果更真實,本研究構建了股骨、脛骨、腓骨皮質骨及松質骨,脛骨、股骨軟骨,半月板以及脛骨平臺下低密度區三維模型。具體方法:將DICOM格式CT影像數據導入Mimics 21.0軟件,使用閾值分割功能建立蒙版,使用多層蒙版編輯功能、填充命令進行修補,以符合正常解剖結構,最后生成三維圖像,導出為STL格式。松質骨由皮質骨向內腐蝕2個像素單位得到[12]。由于本院磁共振圖像圖層較少,通過MRI構建的軟組織形態不規則,所以通過在CT圖像上調整灰度值以構建軟骨和半月板,于Solidworks 2023軟件中將各部件通過原點裝配,并與《奈特人體解剖彩色圖譜》(第3版)下肢圖譜進行比較,在外觀上判斷模型可靠。將STL格式的各個部件導入Geomagic Wrap 2021軟件中,生成三維實體模型并保存為STEP格式。將各組件進行裝配,繪制下肢力線草圖,得到下肢力線與股骨解剖軸夾角為6.02°,股骨髁關節面切線與脛骨踝關節面切線水平,符合下肢正常解剖結構[13],外觀上驗證模型準確。見圖1。
 圖1
模型驗證及外觀
圖1
模型驗證及外觀
a. 下肢力線與股骨解剖軸夾角為6.02°;b. 膝關節模型前面觀;c. 膝關節模型后面觀
Figure1. Model validation and appearancea. The angle between the alignment and the anatomical axis of the femur was 6.02°; b. Anterior view of the knee joint model; c. Posterior view of the knee joint model
1.3.2 脛骨平臺下低密度區模型建立
基于本團隊前期研究在正位X線片中觀察到的脛骨平臺下低密度區形狀,采用Mimics 21.0軟件在受試者CT圖像中分別畫出3個體積相同 [(26 452±15)mm3]、形狀不同的低密度區模型,保存為STL格式并導入Geomagic Wrap 2021軟件中修飾光滑,生成實體,保存為STEP格式文件并導入Solidworks 2023軟件中,與正常膝關節模型進行配準。見圖2。
 圖2
脛骨平臺下低密度區模型構建
圖2
脛骨平臺下低密度區模型構建
a. X線片上脛骨平臺下低密度區范圍;b. 脛骨平臺下低密度區模型與脛骨松質骨模型配準圖;c. 建立3個體積相同、形狀不同的低密度區模型
Figure2. Construction of the model of the low-density area under the tibial plateaua. Range of low-density area under the tibial plateau on X-ray film; b. Registration map of low-density area under the tibial plateau model and cancellous bone model of tibia; c. Three low-density area models with the same volume and different shapes
1.4 有限元分析
1.4.1 網格劃分、材料屬性
皮質骨和松質骨的網格大小為2.0 mm,軟骨、半月板、低密度區網格大小為1.0 mm。模型包含314 224個四面體單元,531 674個節點,網格類型為C3D10M。定義骨、軟骨、半月板為各向同性、線彈性材料[14]。研究脛骨平臺下低密度區骨量減少程度對膝關節的影響,本研究參考既往文獻(骨量減少和骨質疏松的松質骨彈性模量分別降低33%和66%)[15],設置5種不同骨量丟失程度,將脛骨平臺下低密度區模型彈性模量分別減少22%、33%、44%、55%、66%。各材料屬性賦值見表1。
1.4.2 接觸對設置、載荷及邊界條件
對膝關節不同結構建立接觸對,包括雙間室股骨軟骨與半月板、股骨軟骨與脛骨軟骨、脛骨軟骨與半月板、皮質骨與松質骨、脛骨與腓骨、股骨與股骨軟骨、脛骨與脛骨軟骨、脛骨下低密度區與脛骨松質骨。將骨與軟骨(股骨與股骨軟骨、脛骨與脛骨軟骨)、皮質骨與松質骨、脛骨與腓骨、脛骨軟骨與半月板、脛骨下低密度區與脛骨松質骨設置為綁定。因膝關節腔內含有較多關節液,具有潤滑作用,因此將股骨軟骨與半月板、股骨軟骨與脛骨軟骨之間接觸對設置為無摩擦的有限滑移接觸[18]。根據髖關節“頭臼接觸”理論[19],將載荷加載于股骨頭前外側,受力面積為1 172 mm2,與文獻 [20] 報道接近。
1.4.3 觀測指標
① 模型驗證:參考文獻 [21]方法,于股骨頭上表面沿下肢力線方向施加1 000 N軸向載荷,股骨約束屈伸方向的自由度,而3個平移自由度和旋轉自由度不做約束;脛、腓骨下端完全固定,約束6個方向自由度。進行模型驗證,測量脛骨皮質骨上表面內、外側間室,內、外側脛骨軟骨,內、外側半月板,內、外側股骨軟骨最大應力,并計算內、外側間室應力比。
② 骨量減少不同程度對應力及位移的影響:為模擬人行走過程中膝關節平均最大應力[22],在股骨頭上表面沿下肢力線方向施加1 860 N軸向載荷。脛、腓骨遠端完全固定,限制6個方向自由度,觀測脛骨平臺下低密度區骨量未減少組(1組)、骨量減少22%組(2組)、骨量減少33%組(3組)、骨量減少44%組(4組)、骨量減少55%組(5組)、骨量減少66%組(6組)的脛骨平臺最大應力及脛骨皮質骨、松質骨最大位移。
③ 不同體積低密度區對應力及位移的影響:為研究不同體積低密度區對脛骨內側平臺的影響,需要建立多組模型,通過Solidworks 2023軟件中縮放功能,將脛骨平臺下低密度區彈性模量減少66%的模型分別縮放81%、90%、100%、110%、121%,并分別與脛骨松質骨配準,生成5個不同體積 [分別為(14 064±23)、(19 292±35)、(26 463±53)、(35 223±69)、(46 882±87)mm3]的低密度區模型(分別設為B~F組),并以原始低密度區模型作為對照(A組)。同 ② 中方法施加載荷并檢測各組脛骨平臺最大應力及脛骨皮質骨、松質骨最大位移。
1.5 統計學方法
采用SPSS26.0統計軟件進行分析。計量資料經Shapiro-Wilk正態性檢驗,均符合正態分布,數據以均數±標準差表示,組間比較采用單因素方差分析,兩兩比較采用LSD檢驗;檢驗水準α=0.05。
2 結果
2.1 模型驗證
脛骨皮質骨上表面內、外側間室最大應力分別為(6.74±0.03)、(5.06±0.02)MPa,內、外側半月板最大應力分別為(12.87±0.09)、(7.24±0.06)MPa,內、外側脛骨軟骨最大應力分別為(2.46±0.02)、(5.30±0.05)MPa,內、外側股骨軟骨最大應力分別為(3.76±0.04)、(2.19±0.03)MPa,得出脛骨平臺內、外側間室應力比分別為56.83%±0.27%、43.17%±0.27%,與既往文獻 [18,23-24] 結果一致,驗證構建的模型準確。
2.2 骨量減少程度對應力及位移的影響
各組脛骨平臺最大應力及脛骨皮質骨、松質骨最大位移主要分布于脛骨平臺內側。隨著脛骨平臺下低密度區骨量逐漸減少,上述指標均隨之增大,各組間差異均有統計學意義(P<0.05)。見圖3、4。
 圖3
脛骨平臺下低密度區骨量丟失程度不同時各指標檢測
圖3
脛骨平臺下低密度區骨量丟失程度不同時各指標檢測
a. 脛骨平臺最大應力;b. 脛骨皮質骨最大位移;c. 脛骨松質骨最大位移
Figure3. Detection of various indicators of bone density loss in low-density areas under the tibial plateau with different degreesa. Maximum stress on tibial plateau; b. Maximum displacement of tibial cortical bone; c. Maximum displacement of tibial cancellous bone
 圖4
脛骨平臺下低密度區骨量丟失不同時應力及位移云圖
圖4
脛骨平臺下低密度區骨量丟失不同時應力及位移云圖
從左至右分別為1~6組 a. 脛骨平臺最大應力云圖;b. 脛骨皮質骨最大位移云圖;c. 脛骨松質骨最大位移云圖
Figure4. Stress and displacement cloud maps of low-density areas under the tibial plateau with varying degrees of bone density lossFrom left to right for groups 1-6 a. Cloud map of maximum stress on tibial plateau; b. Cloud map of maximum displacement of tibial cortical bone; c. Cloud map of maximum displacement of tibial cancellous bone
2.3 低密度區體積對應力及位移的影響
各組脛骨平臺最大應力及脛骨皮質骨、松質骨最大位移主要分布于脛骨平臺內側。隨著脛骨平臺下低密度區體積增大,上述指標均隨之增大,各組間差異均有統計學意義(P<0.05)。見圖5、6。
 圖5
不同體積脛骨平臺下低密度區各指標檢測
圖5
不同體積脛骨平臺下低密度區各指標檢測
a. 脛骨平臺最大應力;b. 脛骨皮質骨最大位移;c. 脛骨松質骨最大位移
Figure5. Detection of various indicators in low-density areas under the tibial plateau with different volumesa. Maximum stress on tibial plateau; b. Maximum displacement of tibial cortical bone; c. Maximum displacement of tibial cancellous bone
 圖6
不同體積脛骨平臺下低密度區應力及位移云圖
圖6
不同體積脛骨平臺下低密度區應力及位移云圖
從左至右分別為A~F組 a. 脛骨平臺最大應力云圖;b. 脛骨皮質骨最大位移云圖;c. 脛骨松質骨最大位移云圖
Figure6. Stress and displacement cloud maps of low-density areas under the tibial plateau at different volumesFrom left to right for groups A-F a. Cloud map of maximum stress on tibial plateau; b: Cloud map of maximum displacement of tibial cortical bone; c. Cloud map of maximum displacement of tibial cancellous bone
3 討論
KOA是一種致殘性疾病,病程較長,若不及早治療干預,會加重患者膝關節內翻畸形。KOA診斷首選X線片,可表現為關節間隙狹窄、骨贅形成、軟骨下硬化和骨囊腫形成,最常用分級方法是Kellgren-Lawrence分類系統[25]。在病因方面,KOA可由創傷、應力、炎癥、生化反應及代謝紊亂引起[26],由于關節軟骨缺乏血管及神經支配,膝關節損傷早期階段不會發生疼痛,疼痛多由其他組織如關節囊、滑膜、軟骨下骨、韌帶和關節周圍肌肉引起,由軟骨缺損引起的疼痛則提示關節間隙狹窄。膝關節軟骨磨損是漸進過程,此過程中軟骨完整性受到破壞,軟骨面缺損明顯,粗糙欠平整,邊緣形成骨贅,軟骨下骨形成松質骨硬化灶,同時軟骨細胞減少、形態明顯改變,軟骨層纖維化且軟骨之間有孔隙分布[27]。軟骨基質作為軟骨細胞最重要的營養來源,其厚度減少將加重軟骨磨損和破壞。隨著膝關節內翻畸形進展,膝關節內側肌群神經肌肉活動上調,提示可能加重內側應力及畸形程度[28]。膝關節解剖結構特點也決定著KOA患者較易發展為膝內翻畸形。“不均勻沉降”理論[29]認為,脛骨平臺外側與腓骨之間牢固的支撐作用可防止膝外翻,而當關節軟骨發生退變、軟骨下骨骨髓水腫或脛骨平臺下骨密度降低時,容易引發力學性能較弱的軟骨下骨出現微骨折,從而繼發骨破壞、骨硬化及骨囊性變,進而導致膝關節應力增大及內翻加重。
骨質疏松癥是最常見的慢性代謝性骨病,其特征是骨量減少和骨微結構改變,骨脆性增加易導致軟骨下骨微骨折[30]。而KOA與骨質疏松癥之間關系的探討已有較多文獻報道,但二者相關性仍存在爭議[31-32]。多數研究者認為KOA與骨質疏松癥是負相關關系,骨質疏松癥的基本病理過程是骨量丟失,而KOA在關節附近的病理表現是骨質增生和骨贅形成,但KOA的病理過程也極為復雜。骨質疏松癥是一種全身性骨骼疾病,而KOA的骨質變化主要發生在軟骨下和鄰近的骺端區域。KOA患者關節軟骨病理表現為軟骨成骨及軟骨下骨硬化,體現為緊鄰關節的軟骨下骨增厚及密度增加。本課題組前期通過KOA患者X線片研究得出脛骨下低密度區不涉及脛骨皮質骨,只涉及脛骨平臺下松質骨。當KOA患者內側脛骨平臺所承受的應力較高時,脛骨平臺內側軟骨發生骨重塑,隨之軟骨下骨骨密度增高。而脛骨松質骨存在兩種結局,一是脛骨內側平臺皮質骨發生塌陷使應力傳遞至松質骨,隨之松質骨骨小梁硬化及斷裂,進而導致脛骨內側平臺皮質骨及松質骨骨密度均增高;二是脛骨內側平臺受到較大應力,軟骨及軟骨下皮質骨硬化且尚未塌陷時,由于應力遮擋效應,脛骨內側平臺松質骨骨量流失,進而形成低密度區改變。Li等[6]認為在關節炎早期,軟骨下骨及骨小梁呈骨質疏松樣,而進展到晚期,軟骨骨基質礦化,骨密度增高。研究表明骨質疏松是KOA患者內翻畸形的主要危險因素[33],而保持正常的骨密度值會延緩關節炎的進展[34]。那么骨質疏松癥與脛骨平臺下低密度區是否存在必然聯系呢?對于脛骨平臺下低密度區改變,文獻鮮有報道。本課題組前期研究只著重分析了KOA的不同分級與脛骨平臺下低密度區間的關系,并未涉及到骨質疏松癥與脛骨平臺下低密度區間的關系,故在未來研究中這兩者間的相關性需要重點闡明,有助于更好地理解KOA發病及進展的危險因素。脛骨平臺下低密度區改變實質是脛骨平臺下一定區域骨密度減少,伴或不伴有全身骨質疏松。根據本研究結果,模擬正常力線,從生物力學角度驗證脛骨平臺下骨密度的丟失能夠增大脛骨平臺的應力及位移,最大應力及位移均發生于內側,故膝關節逐漸內翻,隨之下肢力線逐漸內移;隨著力線內移,脛骨平臺應力及位移繼續增大,并形成不可逆轉的惡性循環。因此,脛骨平臺下低密度區的出現對于膝關節內翻畸形的預防具有重要意義。
有限元分析技術在膝關節內翻畸形研究中的應用逐漸普遍[35-38],但大部分研究較多關注具體術式,如膝關節單髁置換術、人工全膝關節置換術、脛骨高位截骨術等,較少有對KOA膝內翻機制過程的生物力學研究。本研究基于臨床觀察發現KOA患者脛骨平臺下低密度區的范圍與疾病進展相關[10],進而通過有限元分析進行驗證。結果顯示脛骨平臺下骨密度丟失越嚴重,相應脛骨平臺應力越大,位移也隨之越大。這可能是由于隨著松質骨密度丟失,對應力的承受能力下降,相應的脛骨皮質骨需要分擔更大應力,進而產生更大位移,進展為膝內翻畸形。而隨著脛骨下低密度區體積增大,脛骨平臺應力和位移也隨之增大。提示脛骨平臺下骨量減少的嚴重程度及范圍是預測膝內翻、力線內移的關鍵因素,對于臨床及早識別、及早干預具有重要意義。在治療上,目前公認的最佳矯正方式為力線經過“Fujisawa”點[39]。通過糾正力線,改變膝關節內、外側間室載荷的分布,從而減緩脛骨軟骨及軟骨下骨的骨重塑進程,延緩KOA的進展。同時,本研究也從生物力學角度驗證了團隊前期臨床觀察結果,表明脛骨平臺下低密度區需要引起足夠重視。
本研究存在一定局限性。首先,僅選取單例受試者構建單個模型,且脛骨平臺下低密度區的3個模型外形與松質骨邊緣不完全貼合,可能會對結果的準確性造成影響。其次,考慮到計算時間的影響,僅設定股骨軟骨與半月板、股骨軟骨與脛骨軟骨之間為無摩擦的有限滑移,而其他接觸關系皆為綁定,未考慮結構間的微動,也未能將膝關節周圍重要肌群及韌帶納入研究,可能會對結果造成影響。另外,本研究只進行靜力分析,未進行下肢動態的受力分析[40],動態分析相較于靜力分析能提供更全面的力學結果,對于理解膝關節受力狀態更具優勢。此外,對于骨質疏松與脛骨平臺下低密度區間的關系尚未見報道,對于理解KOA的發病及進展具有重要意義,有待今后繼續深入探討。
綜上述,本研究從生物力學角度闡釋了脛骨平臺下骨量減少可提示KOA膝內翻發生概率大大增加、力線內移趨勢明顯。因此,在臨床工作中要重視脛骨平臺下低密度區的改變,及早預防,避免膝內翻畸形發生及加重。
利益沖突 在課題研究和文章撰寫過程中不存在利益沖突;項目經費支持沒有影響文章觀點和對研究數據客觀結果的分析及其報道
倫理聲明 研究方案經廣州中醫藥大學第三附屬醫院倫理審查委員會批準(PJ-KY-20221227-018);研究對象知情同意
作者貢獻聲明 魏秋實:研究設計、經費支持;何敏聰、林天燁、何曉銘:研究設計、數據統計分析;詹芝瑋、陸舜、林錕、田佳慶、曾子俊、侯文淵、魏騰飛:負責應力計算,模型修改,數據獲取;韓龍飛:文稿撰寫