引用本文: 王希鵬, 劉江濤. 高分子聚乙烯假體在人工全髖關節置換術后遠期CT成像骨溶解分析. 中國修復重建外科雜志, 2024, 38(9): 1079-1085. doi: 10.7507/1002-1892.202403040 復制
版權信息: ?四川大學華西醫院華西期刊社《中國修復重建外科雜志》版權所有,未經授權不得轉載、改編
高分子聚乙烯假體磨損引起的骨溶解被認為是人工全髖關節置換術(total hip arthroplasty,THA)后發生假體無菌性松動和假體植入失敗的主要原因之一[1-4]。聚乙烯磨損碎片在關節間隙積聚,誘發巨噬細胞反應,加速假體附近骨吸收,最終導致假體松動[3,5-8]。既往文獻報道,高分子聚乙烯非骨水泥假體在THA術后15年隨訪期內的材料磨損率為10%~12%,骨溶解率為3%~6%,具有較好的耐磨性。但迄今為止,尚無研究對THA術后隨訪15年以上的高分子聚乙烯假體所致骨溶解情況進行評估。
既往對于骨溶解判斷多采用X線片測量確定[9-10];但X線片為二維圖像,具有一定局限性,且容易受病變位置影響,其檢測靈敏度只有41.5%[11]。研究發現,與X線片相比,橫斷面成像技術(包括CT和MRI)對骨溶解的檢測靈敏度更高[12-13]。Walde等[14-17]使用X線片、CT和MRI識別溶骨性病變,發現骨溶解表現在X線片上敏感性較差;而MRI因存在金屬偽影所致磁束硬化現象,所以對THA術后假體所致骨溶解的識別效果略差于CT。
隨著髖關節假體材料及結構不斷改進、外科技術不斷提高,THA手術成功率越來越高,患者對術后假體耐磨性要求亦越來越高。因此,本研究擬對使用第一代高分子聚乙烯假體行THA且術后隨訪15年以上患者,采用CT評估假體所致骨溶解情況,以期為臨床髖關節假體選擇提供依據。報告如下。
1 臨床資料
1.1 一般資料
患者納入標準:① 因髖關節疾病初次行THA治療;② 髖關節假體使用第一代高分子聚乙烯髖臼內襯(Zimmer公司,美國)聯合氧化鋯股骨頭(NGK Spark Plug公司,日本);③ 隨訪時間15年以上且臨床資料完整;④ 有完整CT三維多平面重建(three-dimensional multiplanar reconstruction,3D-MPR)影像學資料。排除既往行髖關節翻修手術者。
本研究患者資料均來源于日本金澤醫科大學附屬醫院,2000年6月—2004年4月,375例行THA治療患者中,共84例(105髖)符合選擇標準納入研究。本組男7例,女77例;年齡41~75歲,平均56.4歲。左髖52例,右髖53例。身體質量指數17.5~35.7 kg/m2,平均23.3 kg/m2。其中繼發性髖關節骨關節炎94髖、骨盆截骨術后4髖、原發性髖關節骨關節炎2髖、創傷性髖關節骨關節炎2髖、股骨頭壞死2髖、類風濕性關節炎1髖。Crowe分型:Ⅰ型79髖、Ⅱ型19髖、Ⅲ型6髖、Ⅳ型1髖。
1.2 手術方法
手術均由2名經驗豐富的關節外科醫生完成。患者于全身麻醉下取健側臥位,沿患側髖關節后外側作8~10 cm長切口,逐層切開皮膚及皮下組織筋膜。貼近股骨近端離斷包括梨狀肌等外旋肌群,向上經臀大肌肌纖維間隙,顯露髖關節囊;向上剝離至髖臼緣,向下剝離顯露股骨上段,切開并切除關節囊。給予髖關節后脫位,以外側平大轉子內側基底、內側平小轉子上方1 cm為截骨平面作股骨頸截骨,切除股骨頭,行髖關節周圍軟組織松解。做髖臼準備,真性髖臼為大量骨贅增生,用合適尺寸髖白銼將其銼至適中,髖臼邊緣滲血良好;安裝合適尺寸髖臼假體,并以2~4枚髖臼螺釘固定加固。股骨近端用矩形骨刀開口后,用髓腔銼擴至合適型號,予以復位。檢查髖關節被動活動良好且穩定后,大量生理鹽水沖洗,股骨近端安裝股骨柄假體,予以關節復位。再次檢查髖關節被動活動良好且穩定后,大量生理鹽水沖洗,止血,放置引流管。修復髖周肌肉,縫合各層。
根據患者股骨髓腔情況和解剖特征選擇髖關節假體,本組采用美國Zimmer公司的非骨水泥型Anatomic 75髖、VerSys-RM 4髖、VerSys-taper 11髖、骨水泥型CPT 15髖。髖臼內襯均采用高耐磨第一代高分子聚乙烯內襯。髖部采用平緣襯線82髖、抬高襯線10° 22髖、抬高襯線20° 1髖。所有患者均使用26 mm氧化鋯股骨頭。髖臼杯尺寸為46~54 mm,平均50 mm;內襯厚度為6.3 mm 3髖、7.3 mm 42髖、8.2 mm 60髖。
1.3 術后處理
術后24 h常規拔除引流管;使用外展枕使髖關節保持外展體位3周,防止早期髖關節脫位。術后在康復師指導下行常規康復訓練,以減小髖關節脫位風險,有利于患者肢體功能恢復。
1.4 骨溶解評價
1.4.1 X線片評價
術后當天、1年及末次隨訪時,攝患者仰臥位骨盆正位X線片,采用DeLee和Charnley分類[18-19]分析髖臼假體周圍輻射透光情況。根據X線片中骨皮質下散在的界限不清骨小梁吸收情況判斷骨溶解發生情況[20]。并于末次隨訪時測量以下影像學指標:① 垂直距離:骨盆下邊緣淚滴線與髖關節旋轉中心垂線相交處的距離,即髖關節中心高度;② 水平距離:髖關節旋轉中心至淚滴下緣淚滴間線與垂直線相交處的水平距離;③ 髖臼杯前傾角:通過髖臼杯開口的平面與淚滴間線之間的夾角。
1.4.2 CT評價
術后1年及末次隨訪時CT掃描評估髖關節冠狀面和矢狀面骨溶解情況。設置掃描切片厚度為1 mm,采用Synapse 3.1.1圖像分析軟件,3D-MPR視圖識別骨溶解區域。將骨溶解定義為骨內透明區域,無明顯骨小梁,且透明區域周圍有明顯皮質化[21-22];如果觀察到低密度區域,則進一步評估確定密度降低區域是否最初存在或隨著時間推移而進展。
由2名經驗豐富的關節外科醫生對CT及X線片影像資料進行盲評,1名放射科醫生根據Narkbunnam等[21]報道的評分系統對骨溶解進行評分。對比前后圖像以出現點對點異常來判斷是否發生了移位變形或磨損,如圖像中髖臼側變化記錄為磨損,而股骨柄側變化記錄為移位變形,這兩個影像學表現均可定義為發生骨溶解現象。
2 結果
術后發生下肢深靜脈血栓形成2例。患者均獲隨訪,隨訪時間15~18年,平均15.9年。術后發生髖關節脫位1髖,假體周圍骨折1髖;均未發生髖臼松動或內襯斷裂。除1例術后X線片檢查發現髖臼處有1條可透射線外,余83例X線片未顯示任何髖臼或股骨側可透射線;無1例患者行髖關節翻修術。末次隨訪時X線片檢查示,髖臼杯前傾角?10°~39°,平均22°;垂直距離3.5~47.1 mm,平均24.6 mm;水平距離22.6~48.1 mm,平均31.7 mm。末次隨訪時X線片和CT 3D-MPR圖像示患者均未出現髖臼或股骨骨溶解,根據Narkbunnam提出的骨溶解評分標準示任何區域均為0分。見圖1~3。
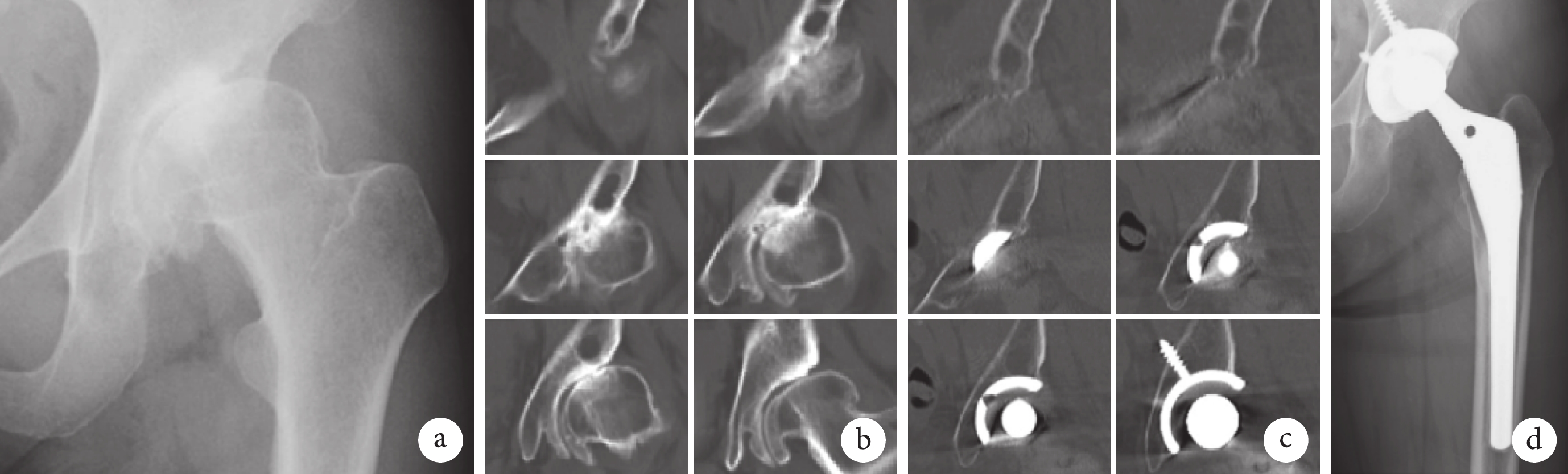 圖1
患者,女,47歲,左髖繼發性骨關節炎(Crowe Ⅱ型)
圖1
患者,女,47歲,左髖繼發性骨關節炎(Crowe Ⅱ型)
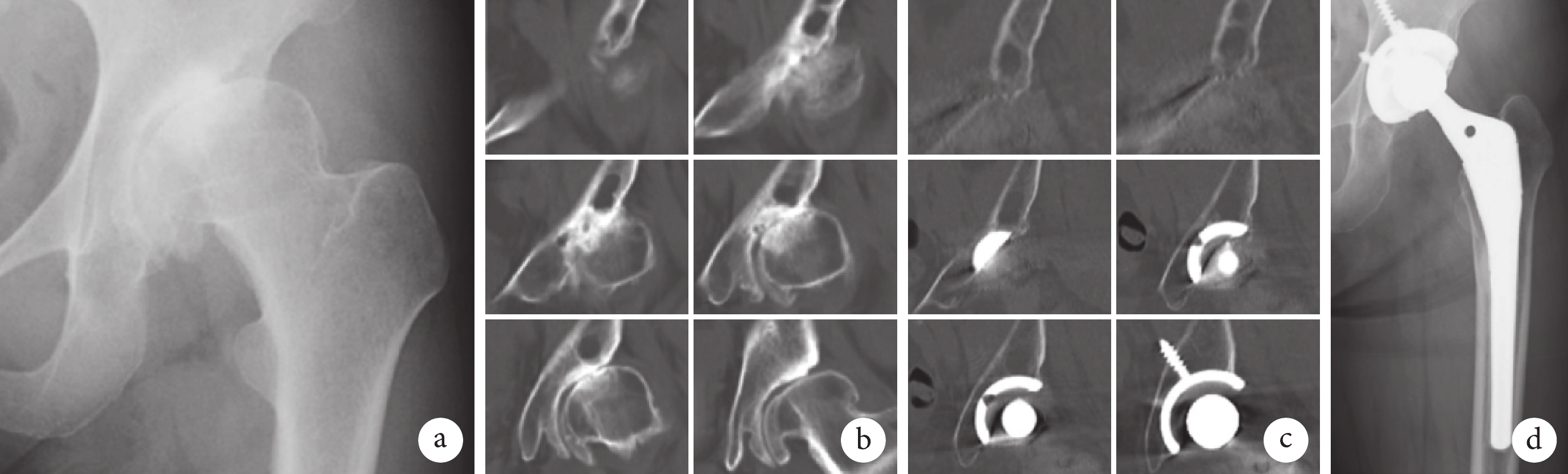
a. 術前骨盆正位X線片示髖臼圓頂無明顯骨囊腫;b. 術前CT 3D-MPR示髖臼中大型退行性骨囊腫;c. 術后15年CT 3D-MPR示未見骨溶解,退行性骨囊腫與術前相比無變化;d. 術后16年骨盆正位X線片示髖臼無明顯骨溶解
Figure1. A 47-year-old female patient with secondary osteoarthritis of the left hip (Crowe type Ⅱ)a. Preoperative pelvic anteroposterior X-ray film showed no obvious bone cyst in the dome of the acetabulum; b. Preoperative CT 3D-MPR showed a large degenerative bone cyst in the acetabulum; c. CT 3D-MPR at 15 years after operation showed no osteolysis, and there was no change in degenerative bone cyst compared with that before operation; d. Pelvic anteroposterior X-ray film at 16 years after operation showed no obvious osteolysis in the acetabulum
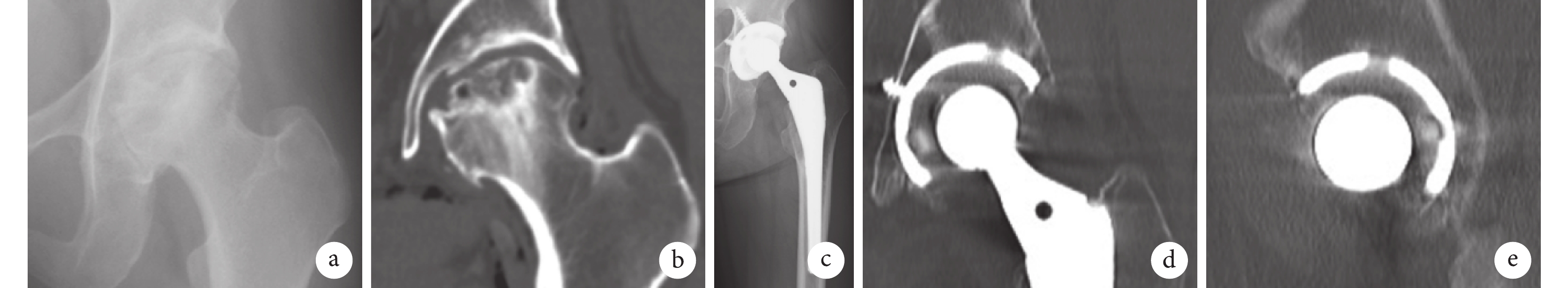 圖2
患者,女,48歲,左側股骨頭壞死(Crowe Ⅲ型)
圖2
患者,女,48歲,左側股骨頭壞死(Crowe Ⅲ型)
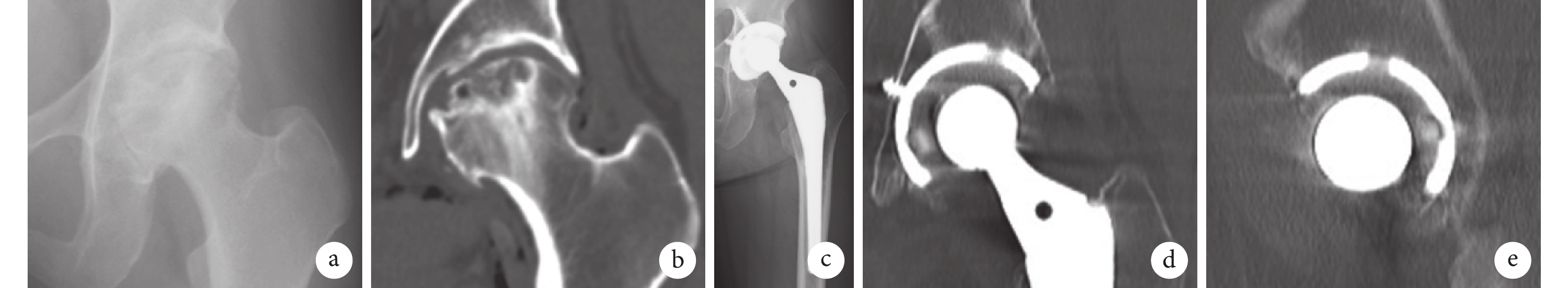
a. 術前正位X線片示髖臼無退行性骨囊腫;b. 術前CT冠狀位示髖臼內無骨囊腫;c. 術后16年X線片示髖臼和股骨側均未發生骨溶解;d、e. 術后16年CT冠狀位和矢狀位示髖臼或股骨近端無骨溶解
Figure2. A 48-year-old female patient with left osteonecrosis of the femoral head (Crowe type Ⅲ)a. Preoperative anteroposterior X-ray film showed no degenerative bone cyst in the acetabulum; b. Preoperative coronal CT showed no bone cyst in the acetabulum; c. X-ray film at 16 years after operation showed no osteolysis in the acetabulum and femur; d, e. Coronal and sagittal CT at 16 years after operation showed no osteolysis of the acetabulum or proximal femur
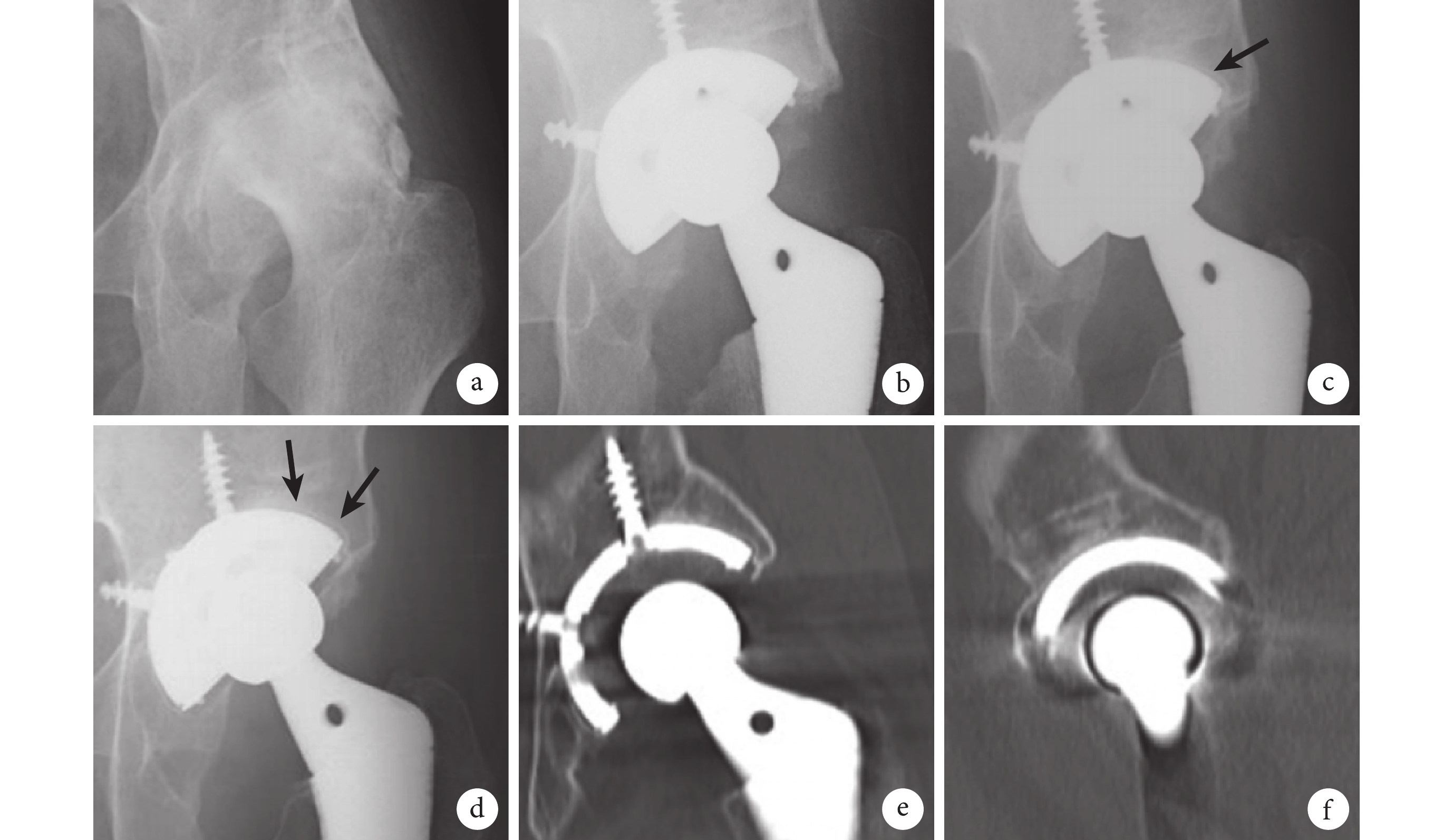 圖3
患者,女,55歲,左側終末期骨關節炎
圖3
患者,女,55歲,左側終末期骨關節炎
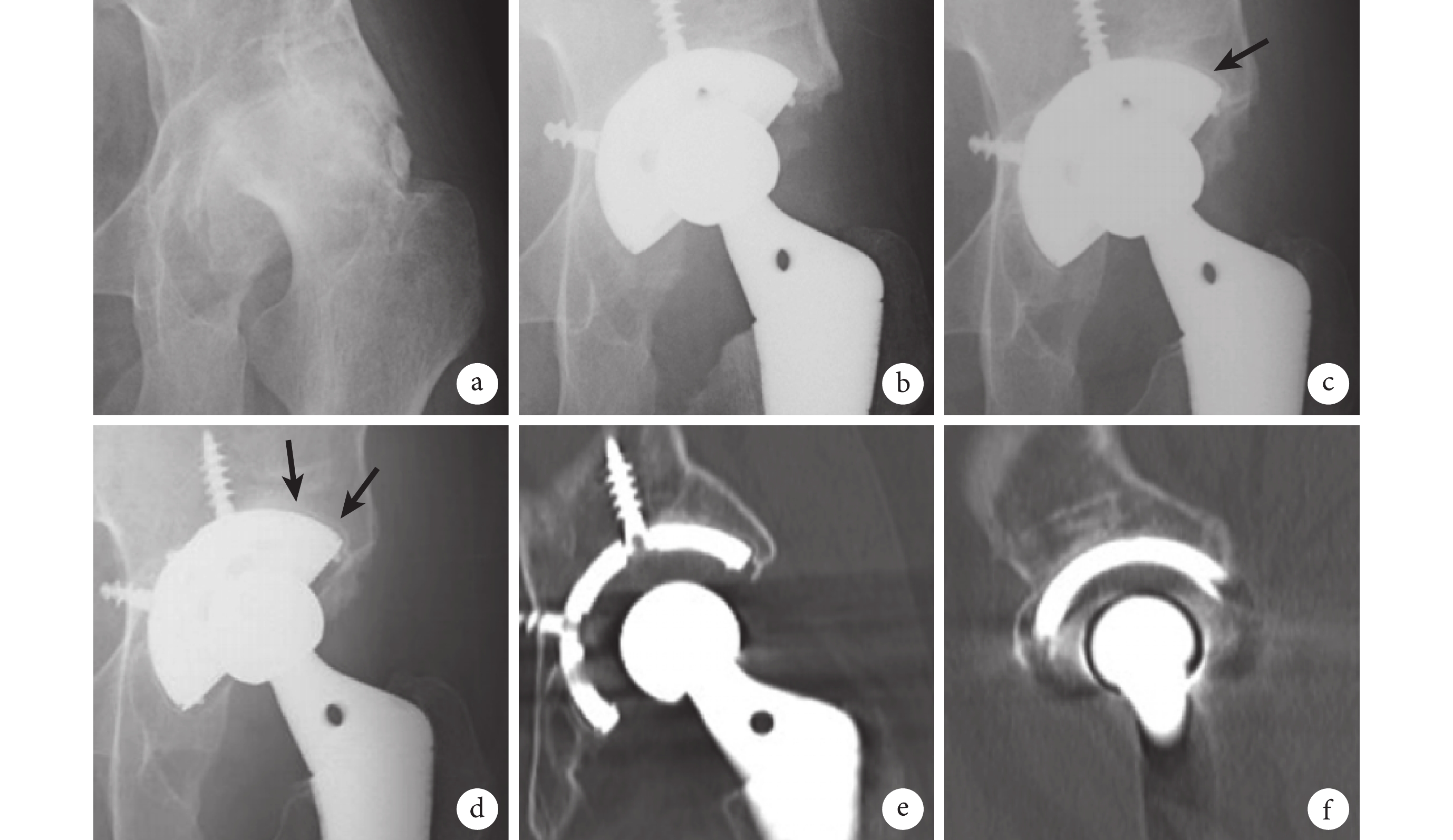
a. 術前X線片;b. 術后即刻X線片示髖臼杯周圍無可透射線;c. 術后6年X線片示Gruen 1 區可透射線(箭頭);d. 術后15年X線片可見1條略微延長的可透射線(箭頭);e、f. 術后15年CT冠狀位和矢狀位示髖臼與臼杯外側緣之間的骨整合
Figure3. A 55-year-old female patient with left end-stage osteoarthritisa. Preoperative X-ray film; b. Immediate postoperative X-ray film showed no radiolucency around the acetabular cup; c. X-ray film at 6 years after operation showed radiolucency in Gruen zone 1 (arrow); d. X-ray film at 15 years after operation showed a slightly extended radiolucency (arrow); e, f. CT coronal and sagittal images at 15 years after operation showed osseointegration between the acetabulum and the lateral edge of the acetabular cup
3 討論
術后假體松動和假體周圍骨溶解是THA術后翻修的最常見原因。骨溶解主要由于聚乙烯材料產生的磨損顆粒引起的炎癥反應,導致細胞受體介導反應,從而上調T-受體1、2和4[21,23-28]。超高分子聚乙烯材料的磨損顆粒大小通常為0.1~1.0 μm[29],在小鼠髖關節模型中,這種大小的顆粒具有更強生物活性,更有可能導致骨溶解。研究表明,高分子聚乙烯材料的磨損特性優于上一代超高分子聚乙烯材料[16,30-34]。但關于高分子聚乙烯材料與骨溶解的報道較少[35-37]。Broomfield等[38]通過CT分析發現1例使用高分子聚乙烯假體患者術后12年發生骨溶解;Tsukamoto等[39]通過分析THA術后發生骨溶解患者的臨床資料, 提出高分子聚乙烯材料可能在10~15年內發生過度磨損。而目前尚罕見高分子聚乙烯假體THA術后15年以上骨溶解發生情況的報道,因此本研究對此進行分析總結,以期為臨床實踐提供參考。
對于髖關節假體松動的研究,傳統方法是對比患者術后不同時間段X線片變化進行評估。但其存在一定局限性[40],術后早期X線片不容易發現髖關節假體周圍發生的局部松動,多需借助CT等影像學檢查進行判斷。CT能立體且清晰顯示骨骼正常解剖形態,突破了傳統平面成像技術的局限性,避免骨重疊對骨骼正常形態顯示的影響,能充分顯示骨折線的位置、類型、走向、形狀和骨折移位、脫位情況,對于判斷髖關節假體松動比X線片更加敏感、準確[20-24]。
目前,對于使用螺釘和螺釘孔是否會導致非骨水泥型THA髖臼骨溶解和植入物松動尚無定論。Taniguchi等[41]比較了THA術后7~10年使用螺釘和空置螺釘孔的效果,發現二者在穩定性、骨溶解或材料磨損率方面亦無顯著差異;有研究比較了使用實性髖臼杯和帶孔髖臼杯的術后遠期效果,結果顯示二者骨溶解發生率無明顯差異[42]。本研究結果也表明,使用帶多個螺釘孔的髖臼假體進行髖臼假體固定時,對高分子聚乙烯假體的THA結局無不良影響。
另一個需要考慮的問題是髖關節位置過高。既往使用傳統聚乙烯材料的高髖假體中心研究表明,聚乙烯磨損導致的無菌性松動率很高[43-44]。然而近年研究發現,髖關節中心高度與材料 磨損率無關[45]。雖然本研究中,患者平均髖關節中心高度(24.6 mm)比正常值高約10 mm,但術后15年以上隨訪顯示并未發生任何骨溶解情況,說明髖關節中心高度與骨溶解無直接關系。另外,有研究表明,使用氧化鋯股骨頭對高分子聚乙烯材料磨損率顯著低于使用傳統聚乙烯材料的磨損率[46-49]。本研究結果也驗證了上述觀點。
本研究發生髖關節脫位、假體周圍骨折各1髖。結合文獻分析THA術后發生髖關節脫位的因素主要有:① 與患者術后過早鍛煉有關, 術后6周內髖關節軟組織尚未完全愈合,過早進行不恰當運動可能會導致脫位。② 與患者生活習慣有關,若術后經常進行重體力勞動,可能導致假體下沉、股骨變短,從而易出現脫位癥狀;另外,如經常蹺二郎腿或內旋、外展髖關節,也可導致脫位。③ 假體不匹配,比如股骨頭過小,則容易從髖臼中脫出導致脫位。
綜上述,THA術中使用第一代高分子聚乙烯髖關節假體不會增加骨溶解風險,具有一定耐磨性。但本研究為單中心回顧性研究,缺乏對照組,并且因年限較長以及其他因素無法獲得部分患者術前CT 3D-MPR圖像,導致納入標本量有限,限制了研究結果的適用性,確切結論尚需進一步研究明確。
志謝 感謝博士在讀期間日本金澤醫科大學附屬醫院川原節夫教授對本文提供的數據支持
利益沖突 在課題研究和文章撰寫過程中不存在利益沖突;經費支持沒有影響文章觀點和對研究數據客觀結果的分析及其報道
倫理聲明 研究方案經日本金澤醫科大學附屬醫院臨床研究倫理委員會批準
作者貢獻聲明 王希鵬:論文撰寫,數據收集、整理和分析;劉江濤:審查、修改論文
高分子聚乙烯假體磨損引起的骨溶解被認為是人工全髖關節置換術(total hip arthroplasty,THA)后發生假體無菌性松動和假體植入失敗的主要原因之一[1-4]。聚乙烯磨損碎片在關節間隙積聚,誘發巨噬細胞反應,加速假體附近骨吸收,最終導致假體松動[3,5-8]。既往文獻報道,高分子聚乙烯非骨水泥假體在THA術后15年隨訪期內的材料磨損率為10%~12%,骨溶解率為3%~6%,具有較好的耐磨性。但迄今為止,尚無研究對THA術后隨訪15年以上的高分子聚乙烯假體所致骨溶解情況進行評估。
既往對于骨溶解判斷多采用X線片測量確定[9-10];但X線片為二維圖像,具有一定局限性,且容易受病變位置影響,其檢測靈敏度只有41.5%[11]。研究發現,與X線片相比,橫斷面成像技術(包括CT和MRI)對骨溶解的檢測靈敏度更高[12-13]。Walde等[14-17]使用X線片、CT和MRI識別溶骨性病變,發現骨溶解表現在X線片上敏感性較差;而MRI因存在金屬偽影所致磁束硬化現象,所以對THA術后假體所致骨溶解的識別效果略差于CT。
隨著髖關節假體材料及結構不斷改進、外科技術不斷提高,THA手術成功率越來越高,患者對術后假體耐磨性要求亦越來越高。因此,本研究擬對使用第一代高分子聚乙烯假體行THA且術后隨訪15年以上患者,采用CT評估假體所致骨溶解情況,以期為臨床髖關節假體選擇提供依據。報告如下。
1 臨床資料
1.1 一般資料
患者納入標準:① 因髖關節疾病初次行THA治療;② 髖關節假體使用第一代高分子聚乙烯髖臼內襯(Zimmer公司,美國)聯合氧化鋯股骨頭(NGK Spark Plug公司,日本);③ 隨訪時間15年以上且臨床資料完整;④ 有完整CT三維多平面重建(three-dimensional multiplanar reconstruction,3D-MPR)影像學資料。排除既往行髖關節翻修手術者。
本研究患者資料均來源于日本金澤醫科大學附屬醫院,2000年6月—2004年4月,375例行THA治療患者中,共84例(105髖)符合選擇標準納入研究。本組男7例,女77例;年齡41~75歲,平均56.4歲。左髖52例,右髖53例。身體質量指數17.5~35.7 kg/m2,平均23.3 kg/m2。其中繼發性髖關節骨關節炎94髖、骨盆截骨術后4髖、原發性髖關節骨關節炎2髖、創傷性髖關節骨關節炎2髖、股骨頭壞死2髖、類風濕性關節炎1髖。Crowe分型:Ⅰ型79髖、Ⅱ型19髖、Ⅲ型6髖、Ⅳ型1髖。
1.2 手術方法
手術均由2名經驗豐富的關節外科醫生完成。患者于全身麻醉下取健側臥位,沿患側髖關節后外側作8~10 cm長切口,逐層切開皮膚及皮下組織筋膜。貼近股骨近端離斷包括梨狀肌等外旋肌群,向上經臀大肌肌纖維間隙,顯露髖關節囊;向上剝離至髖臼緣,向下剝離顯露股骨上段,切開并切除關節囊。給予髖關節后脫位,以外側平大轉子內側基底、內側平小轉子上方1 cm為截骨平面作股骨頸截骨,切除股骨頭,行髖關節周圍軟組織松解。做髖臼準備,真性髖臼為大量骨贅增生,用合適尺寸髖白銼將其銼至適中,髖臼邊緣滲血良好;安裝合適尺寸髖臼假體,并以2~4枚髖臼螺釘固定加固。股骨近端用矩形骨刀開口后,用髓腔銼擴至合適型號,予以復位。檢查髖關節被動活動良好且穩定后,大量生理鹽水沖洗,股骨近端安裝股骨柄假體,予以關節復位。再次檢查髖關節被動活動良好且穩定后,大量生理鹽水沖洗,止血,放置引流管。修復髖周肌肉,縫合各層。
根據患者股骨髓腔情況和解剖特征選擇髖關節假體,本組采用美國Zimmer公司的非骨水泥型Anatomic 75髖、VerSys-RM 4髖、VerSys-taper 11髖、骨水泥型CPT 15髖。髖臼內襯均采用高耐磨第一代高分子聚乙烯內襯。髖部采用平緣襯線82髖、抬高襯線10° 22髖、抬高襯線20° 1髖。所有患者均使用26 mm氧化鋯股骨頭。髖臼杯尺寸為46~54 mm,平均50 mm;內襯厚度為6.3 mm 3髖、7.3 mm 42髖、8.2 mm 60髖。
1.3 術后處理
術后24 h常規拔除引流管;使用外展枕使髖關節保持外展體位3周,防止早期髖關節脫位。術后在康復師指導下行常規康復訓練,以減小髖關節脫位風險,有利于患者肢體功能恢復。
1.4 骨溶解評價
1.4.1 X線片評價
術后當天、1年及末次隨訪時,攝患者仰臥位骨盆正位X線片,采用DeLee和Charnley分類[18-19]分析髖臼假體周圍輻射透光情況。根據X線片中骨皮質下散在的界限不清骨小梁吸收情況判斷骨溶解發生情況[20]。并于末次隨訪時測量以下影像學指標:① 垂直距離:骨盆下邊緣淚滴線與髖關節旋轉中心垂線相交處的距離,即髖關節中心高度;② 水平距離:髖關節旋轉中心至淚滴下緣淚滴間線與垂直線相交處的水平距離;③ 髖臼杯前傾角:通過髖臼杯開口的平面與淚滴間線之間的夾角。
1.4.2 CT評價
術后1年及末次隨訪時CT掃描評估髖關節冠狀面和矢狀面骨溶解情況。設置掃描切片厚度為1 mm,采用Synapse 3.1.1圖像分析軟件,3D-MPR視圖識別骨溶解區域。將骨溶解定義為骨內透明區域,無明顯骨小梁,且透明區域周圍有明顯皮質化[21-22];如果觀察到低密度區域,則進一步評估確定密度降低區域是否最初存在或隨著時間推移而進展。
由2名經驗豐富的關節外科醫生對CT及X線片影像資料進行盲評,1名放射科醫生根據Narkbunnam等[21]報道的評分系統對骨溶解進行評分。對比前后圖像以出現點對點異常來判斷是否發生了移位變形或磨損,如圖像中髖臼側變化記錄為磨損,而股骨柄側變化記錄為移位變形,這兩個影像學表現均可定義為發生骨溶解現象。
2 結果
術后發生下肢深靜脈血栓形成2例。患者均獲隨訪,隨訪時間15~18年,平均15.9年。術后發生髖關節脫位1髖,假體周圍骨折1髖;均未發生髖臼松動或內襯斷裂。除1例術后X線片檢查發現髖臼處有1條可透射線外,余83例X線片未顯示任何髖臼或股骨側可透射線;無1例患者行髖關節翻修術。末次隨訪時X線片檢查示,髖臼杯前傾角?10°~39°,平均22°;垂直距離3.5~47.1 mm,平均24.6 mm;水平距離22.6~48.1 mm,平均31.7 mm。末次隨訪時X線片和CT 3D-MPR圖像示患者均未出現髖臼或股骨骨溶解,根據Narkbunnam提出的骨溶解評分標準示任何區域均為0分。見圖1~3。
 圖1
患者,女,47歲,左髖繼發性骨關節炎(Crowe Ⅱ型)
圖1
患者,女,47歲,左髖繼發性骨關節炎(Crowe Ⅱ型)
a. 術前骨盆正位X線片示髖臼圓頂無明顯骨囊腫;b. 術前CT 3D-MPR示髖臼中大型退行性骨囊腫;c. 術后15年CT 3D-MPR示未見骨溶解,退行性骨囊腫與術前相比無變化;d. 術后16年骨盆正位X線片示髖臼無明顯骨溶解
Figure1. A 47-year-old female patient with secondary osteoarthritis of the left hip (Crowe type Ⅱ)a. Preoperative pelvic anteroposterior X-ray film showed no obvious bone cyst in the dome of the acetabulum; b. Preoperative CT 3D-MPR showed a large degenerative bone cyst in the acetabulum; c. CT 3D-MPR at 15 years after operation showed no osteolysis, and there was no change in degenerative bone cyst compared with that before operation; d. Pelvic anteroposterior X-ray film at 16 years after operation showed no obvious osteolysis in the acetabulum
 圖2
患者,女,48歲,左側股骨頭壞死(Crowe Ⅲ型)
圖2
患者,女,48歲,左側股骨頭壞死(Crowe Ⅲ型)
a. 術前正位X線片示髖臼無退行性骨囊腫;b. 術前CT冠狀位示髖臼內無骨囊腫;c. 術后16年X線片示髖臼和股骨側均未發生骨溶解;d、e. 術后16年CT冠狀位和矢狀位示髖臼或股骨近端無骨溶解
Figure2. A 48-year-old female patient with left osteonecrosis of the femoral head (Crowe type Ⅲ)a. Preoperative anteroposterior X-ray film showed no degenerative bone cyst in the acetabulum; b. Preoperative coronal CT showed no bone cyst in the acetabulum; c. X-ray film at 16 years after operation showed no osteolysis in the acetabulum and femur; d, e. Coronal and sagittal CT at 16 years after operation showed no osteolysis of the acetabulum or proximal femur
 圖3
患者,女,55歲,左側終末期骨關節炎
圖3
患者,女,55歲,左側終末期骨關節炎
a. 術前X線片;b. 術后即刻X線片示髖臼杯周圍無可透射線;c. 術后6年X線片示Gruen 1 區可透射線(箭頭);d. 術后15年X線片可見1條略微延長的可透射線(箭頭);e、f. 術后15年CT冠狀位和矢狀位示髖臼與臼杯外側緣之間的骨整合
Figure3. A 55-year-old female patient with left end-stage osteoarthritisa. Preoperative X-ray film; b. Immediate postoperative X-ray film showed no radiolucency around the acetabular cup; c. X-ray film at 6 years after operation showed radiolucency in Gruen zone 1 (arrow); d. X-ray film at 15 years after operation showed a slightly extended radiolucency (arrow); e, f. CT coronal and sagittal images at 15 years after operation showed osseointegration between the acetabulum and the lateral edge of the acetabular cup
3 討論
術后假體松動和假體周圍骨溶解是THA術后翻修的最常見原因。骨溶解主要由于聚乙烯材料產生的磨損顆粒引起的炎癥反應,導致細胞受體介導反應,從而上調T-受體1、2和4[21,23-28]。超高分子聚乙烯材料的磨損顆粒大小通常為0.1~1.0 μm[29],在小鼠髖關節模型中,這種大小的顆粒具有更強生物活性,更有可能導致骨溶解。研究表明,高分子聚乙烯材料的磨損特性優于上一代超高分子聚乙烯材料[16,30-34]。但關于高分子聚乙烯材料與骨溶解的報道較少[35-37]。Broomfield等[38]通過CT分析發現1例使用高分子聚乙烯假體患者術后12年發生骨溶解;Tsukamoto等[39]通過分析THA術后發生骨溶解患者的臨床資料, 提出高分子聚乙烯材料可能在10~15年內發生過度磨損。而目前尚罕見高分子聚乙烯假體THA術后15年以上骨溶解發生情況的報道,因此本研究對此進行分析總結,以期為臨床實踐提供參考。
對于髖關節假體松動的研究,傳統方法是對比患者術后不同時間段X線片變化進行評估。但其存在一定局限性[40],術后早期X線片不容易發現髖關節假體周圍發生的局部松動,多需借助CT等影像學檢查進行判斷。CT能立體且清晰顯示骨骼正常解剖形態,突破了傳統平面成像技術的局限性,避免骨重疊對骨骼正常形態顯示的影響,能充分顯示骨折線的位置、類型、走向、形狀和骨折移位、脫位情況,對于判斷髖關節假體松動比X線片更加敏感、準確[20-24]。
目前,對于使用螺釘和螺釘孔是否會導致非骨水泥型THA髖臼骨溶解和植入物松動尚無定論。Taniguchi等[41]比較了THA術后7~10年使用螺釘和空置螺釘孔的效果,發現二者在穩定性、骨溶解或材料磨損率方面亦無顯著差異;有研究比較了使用實性髖臼杯和帶孔髖臼杯的術后遠期效果,結果顯示二者骨溶解發生率無明顯差異[42]。本研究結果也表明,使用帶多個螺釘孔的髖臼假體進行髖臼假體固定時,對高分子聚乙烯假體的THA結局無不良影響。
另一個需要考慮的問題是髖關節位置過高。既往使用傳統聚乙烯材料的高髖假體中心研究表明,聚乙烯磨損導致的無菌性松動率很高[43-44]。然而近年研究發現,髖關節中心高度與材料 磨損率無關[45]。雖然本研究中,患者平均髖關節中心高度(24.6 mm)比正常值高約10 mm,但術后15年以上隨訪顯示并未發生任何骨溶解情況,說明髖關節中心高度與骨溶解無直接關系。另外,有研究表明,使用氧化鋯股骨頭對高分子聚乙烯材料磨損率顯著低于使用傳統聚乙烯材料的磨損率[46-49]。本研究結果也驗證了上述觀點。
本研究發生髖關節脫位、假體周圍骨折各1髖。結合文獻分析THA術后發生髖關節脫位的因素主要有:① 與患者術后過早鍛煉有關, 術后6周內髖關節軟組織尚未完全愈合,過早進行不恰當運動可能會導致脫位。② 與患者生活習慣有關,若術后經常進行重體力勞動,可能導致假體下沉、股骨變短,從而易出現脫位癥狀;另外,如經常蹺二郎腿或內旋、外展髖關節,也可導致脫位。③ 假體不匹配,比如股骨頭過小,則容易從髖臼中脫出導致脫位。
綜上述,THA術中使用第一代高分子聚乙烯髖關節假體不會增加骨溶解風險,具有一定耐磨性。但本研究為單中心回顧性研究,缺乏對照組,并且因年限較長以及其他因素無法獲得部分患者術前CT 3D-MPR圖像,導致納入標本量有限,限制了研究結果的適用性,確切結論尚需進一步研究明確。
志謝 感謝博士在讀期間日本金澤醫科大學附屬醫院川原節夫教授對本文提供的數據支持
利益沖突 在課題研究和文章撰寫過程中不存在利益沖突;經費支持沒有影響文章觀點和對研究數據客觀結果的分析及其報道
倫理聲明 研究方案經日本金澤醫科大學附屬醫院臨床研究倫理委員會批準
作者貢獻聲明 王希鵬:論文撰寫,數據收集、整理和分析;劉江濤:審查、修改論文