引用本文: 史伯翀, 鄭皓予, 吳華健, 胡湘麟, 嚴望軍. 惡性周圍神經鞘瘤患者的臨床特征、治療方式和預后影響因素分析. 中國修復重建外科雜志, 2024, 38(10): 1193-1201. doi: 10.7507/1002-1892.202406040 復制
版權信息: ?四川大學華西醫院華西期刊社《中國修復重建外科雜志》版權所有,未經授權不得轉載、改編
惡性周圍神經鞘瘤(malignant peripheral nerve sheath tumor,MPNST)起源于間充質細胞,是一種具有侵襲性和轉移潛力的軟組織肉瘤,并且容易復發和產生耐藥性。它是一種罕見疾病,總人群患病率約為1/10萬,占所有軟組織肉瘤的2%~4%[1],其中23%~51%的MPNST是由Ⅰ型神經纖維瘤病(neurofibromatosis type 1,NF1)惡變而來。四肢和軀干是MPNST最常見發病部位,而頭頸部較少。根治性手術切除是目前主要治療方法,但可能因復雜的解剖結構而受限。目前尚無充分證據支持放療和化療能夠改善MPNST患者的預后。同時,有許多免疫和靶向療法的臨床研究正在展開,包括利用哺乳動物雷帕霉素靶蛋白(mTOR)抑制劑依維莫司聯合貝伐單抗治療NF1[2],通過絲裂原活化蛋白激酶激酶(mitogen-activated protein kinase kinase,MEK)抑制劑司美替尼聯合程序性死亡配體1(programmed death-ligand 1,PD-L1)單抗德瓦魯單抗治療包括MPNST在內的軟組織肉瘤[3],還有運用受體酪氨酸激酶(receptor tyrosine kinase,RTK)抑制劑安羅替尼聯合艾立布林和替雷利珠單抗治療復發難治性軟組織肉瘤[4]等,但是目前幾乎沒有令人滿意的結果。
既往研究報道腫瘤完全切除和較寬的陰性切緣可降低遠處復發風險[5]。而隨著外科技術的發展,除了一些腫瘤與重要血管、神經毗鄰難以達陰性切緣手術外,大部分手術可達到腫瘤完全切除的目的。因此我們對患者預后影響因素的認識仍不全面。本研究收集了復旦大學附屬腫瘤醫院治療的MPNST患者,根據相關因素進行1年無疾病生存期(disease-free survival,DFS)和3年總生存期(overall survival,OS)的生存分析,結合患者臨床資料,探索不同因素與患者預后的相關性,并使用多因素COX比例風險模型分析影響MPNST患者的獨立預后影響因素。報告如下。
1 資料與方法
1.1 研究對象
患者納入標準:① 排除手術禁忌證進行相應部位手術后,經病理學專家評估存在高度異型性腫瘤細胞、核分裂象增多以及S-100蛋白等相關標志物的陽性表達,再根據病例信息排除其他可疑診斷而確診為MPNST的患者;② 確診時間為2015年1月1日—2021年12月31日,以確保研究數據的時效性和一致性;③ 隨訪資料齊全。該期間復旦大學附屬腫瘤醫院共96例患者符合標準納入研究。
本組男46例,女50例;年齡15~87歲,平均48.2歲,其中<35歲29例、35~60歲34例、≥60歲33例。腫瘤部位:軀干50例,四肢39例,頭頸部7例。腫瘤大小:最大徑<5 cm 49例,≥5 cm 32例,缺失15例。腫瘤深度:深部(腫瘤位于肌肉、骨骼、肌間隙或腹腔、腹膜后)77例,表淺(腫瘤位于淺筋膜或更淺位置)19例。法國國家癌癥中心聯盟(FNCLCC)組織學分級[6]:G1 9例,G2 12例,G3 34例,缺失41例。37例為復發型MPNST,32例合并NF1,26例為Ⅳ期MPNST(即出現淋巴結轉移或遠處轉移)。25例接受術后輔助放療,45例接受圍術期化療,30例接受安羅替尼靶向治療,73例行R0切除(即術后病理顯示切除標本各切緣均為陰性,原病灶區無腫瘤殘留)。見圖1~4。
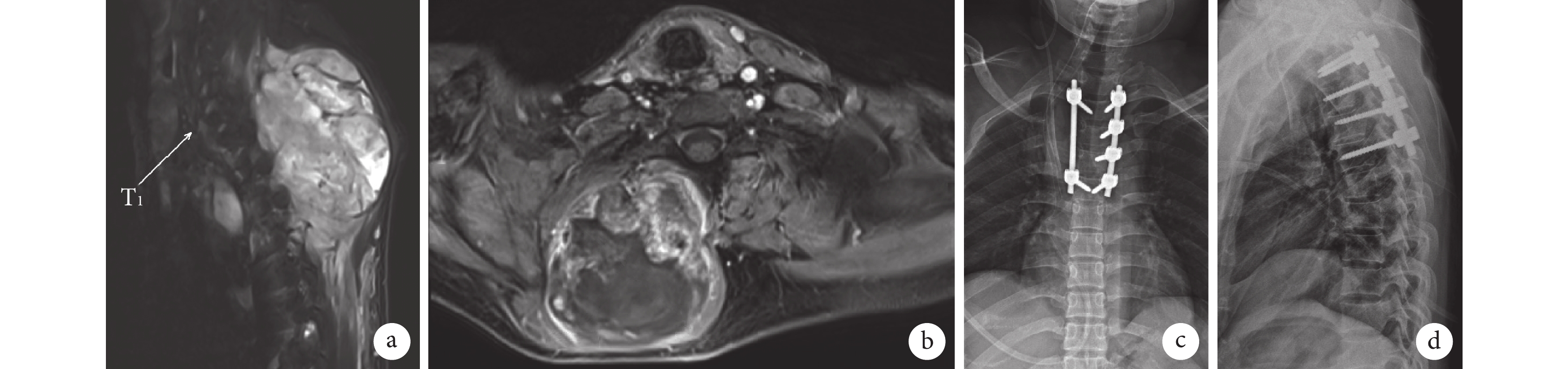 圖1
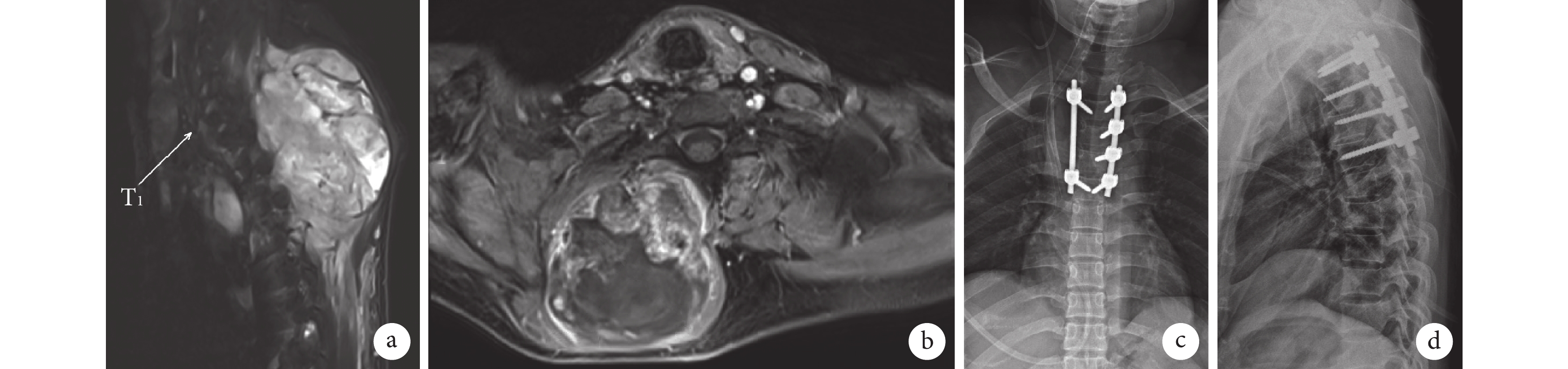
患者,男,25歲,胸椎(C7~T6)Ⅳ期MPNST,行胸椎腫瘤切除術+胸椎(植骨)融合術+鄰近皮瓣修復術
圖1
患者,男,25歲,胸椎(C7~T6)Ⅳ期MPNST,行胸椎腫瘤切除術+胸椎(植骨)融合術+鄰近皮瓣修復術
a、b. 術前MRI示瘤體位于右胸背部并壓迫胸椎,大小約100 mm×80 mm,伴發雙肺及縱膈淋巴結轉移;c、d. 術后4 d正側位X線片示T2~T5椎弓根螺釘內固定影
Figure1. A 25-year-old male patient with thoracic spine (C7-T6) stage Ⅳ MPNST, underwent thoracic spine tumor resection+thoracic spine (bone graft) fusion+adjacent flap repaira, b. Preoperative MRI showed that the tumor was located in the right thoracic back and compressed the thoracic spine, about 100 mm×80 mm in size, with bilateral lung and mediastinal lymph node metastasis; c, d. Anteroposterior and lateral X-ray films at 4 days after operation showed the image of pedicle screw fixation at T2-T5
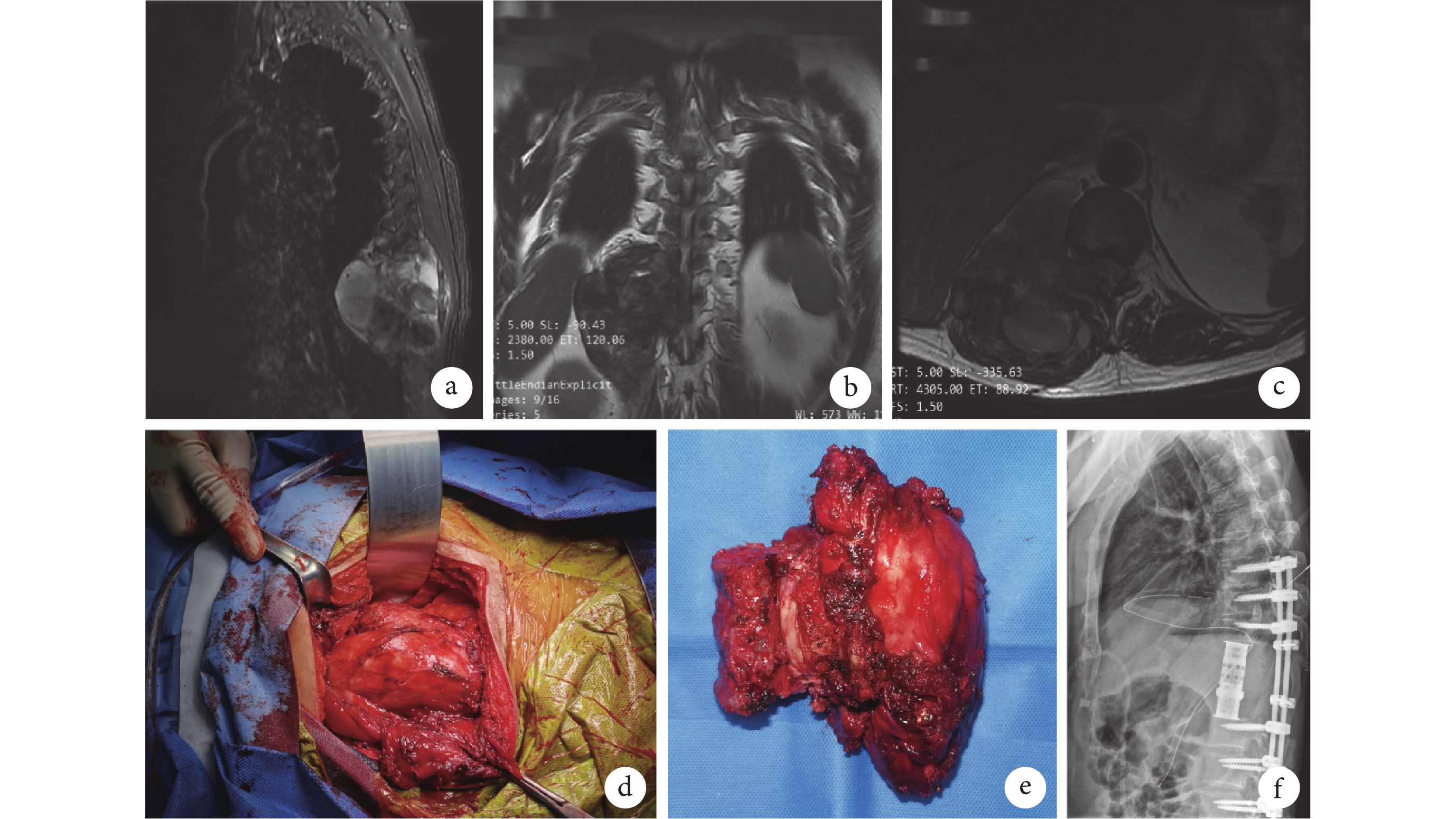 圖2
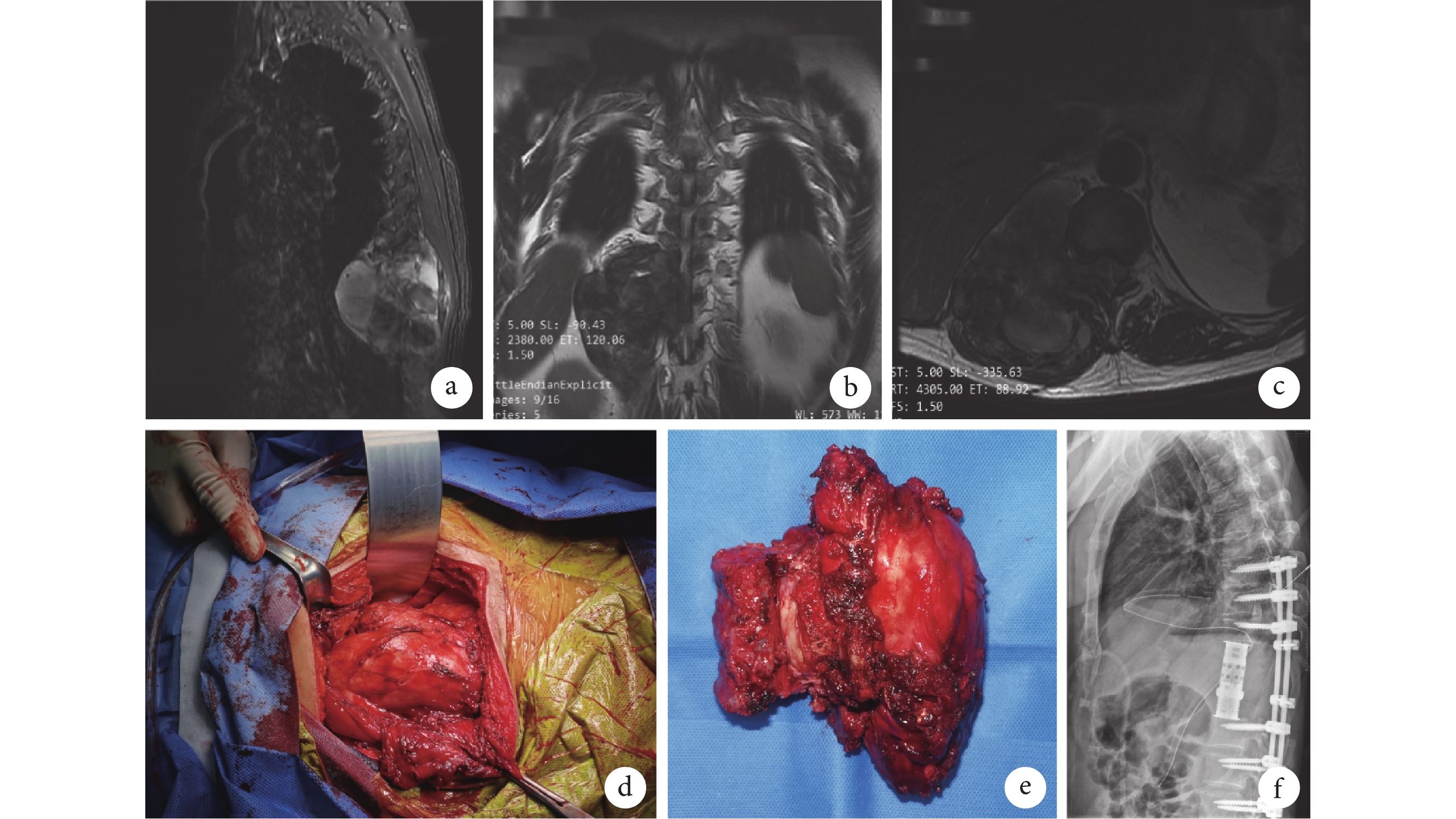
患者,男,51歲,胸腰段(T10~L1)復發型MPNST,行后路胸腰椎腫瘤切除術+胸腰椎融合內固定術
圖2
患者,男,51歲,胸腰段(T10~L1)復發型MPNST,行后路胸腰椎腫瘤切除術+胸腰椎融合內固定術
a~c. 術前MRI示胸腰椎旁軟組織腫塊,約99 mm×90 mm,T9、T10水平脊髓和神經根受壓;d、e. 術中T11病灶部位及切除的軟組織腫塊和T11、12椎體;f. 術后7 d X線片示T11、12人工椎體及T8~10、L1~3椎弓根螺釘影
Figure2. A 51-year-old male patient with thoracolumbar (T10-L1) recurrent MPNST, underwent posterior thoracolumbar tumor resection+thoracolumbar fusion and internal fixationa-c. Preoperative MRI showed a thoracolumbar paravertebral soft tissue mass, about 99 mm×90 mm, spinal cord and nerve root compression at T9 and T10 levels; d, e. The location of T11 lesion and the resected soft tissue mass and T11, 12 vertebral bodies during operation; f. X-ray film of T11, 12 artificial vertebral bodies and pedicle screw shadows of T8-10 and L1-3 vertebral bodies at 7 days after operation
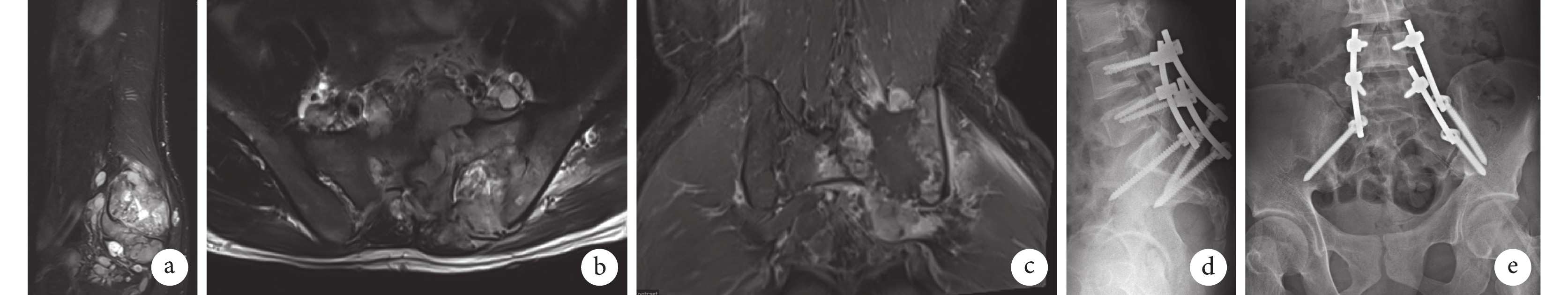 圖3
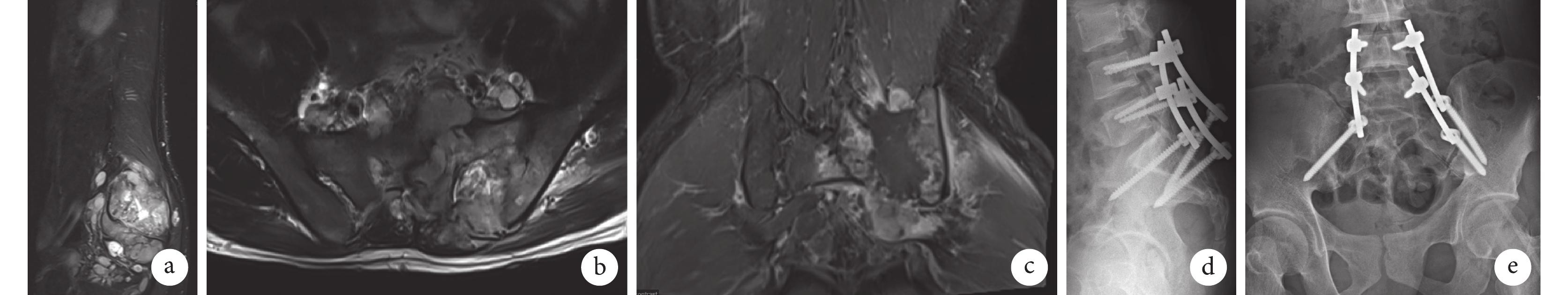
患者,男,26歲,L4~S4節段初發型MPNST,行后路骶骨腫瘤切除植骨融合內固定術
圖3
患者,男,26歲,L4~S4節段初發型MPNST,行后路骶骨腫瘤切除植骨融合內固定術
a~c. 術前MRI示左側骶髂關節骨質破壞伴軟組織腫塊形成,大小約86 mm×79 mm×95 mm,累及周圍組織、神經根及椎管;d、e. 術后1 d正側位X線片示骶骨腫瘤切除術后,L4、5至骶骨椎弓根螺釘內固定影
Figure3. A 26-year-old male patient with L4-S4 segment initial MPNST, underwent posterior sacral tumor resection, bone graft fusion, and internal fixationa-c. Preoperative MRI showed left sacroiliac joint bone destruction with soft tissue mass formation, about 86 mm×79 mm×95 mm in size, involving surrounding tissues, nerve roots, and spinal canal; d, e. Anteroposterior and lateral X-ray films at 1 day after operation showed the image of pedicle screws fixation from L4, 5 to sacrum after sacral tumor resection
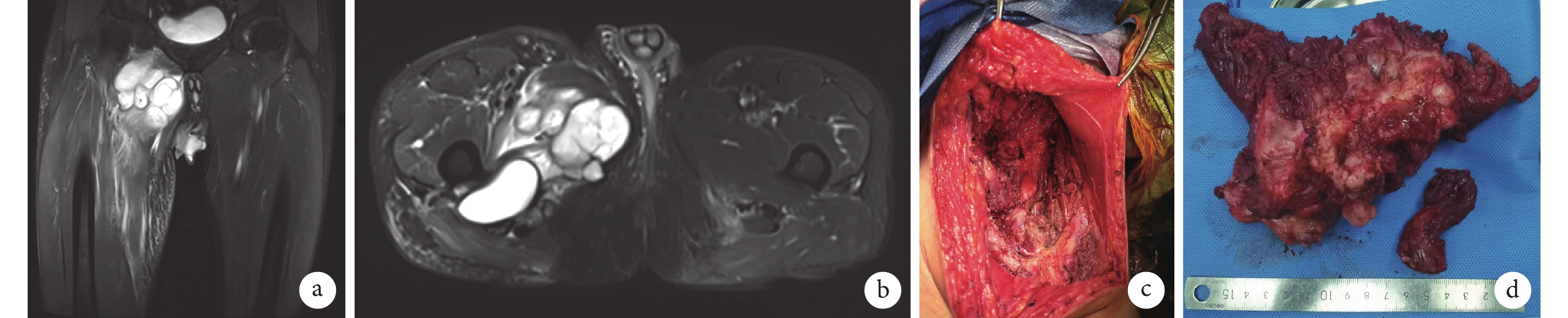 圖4
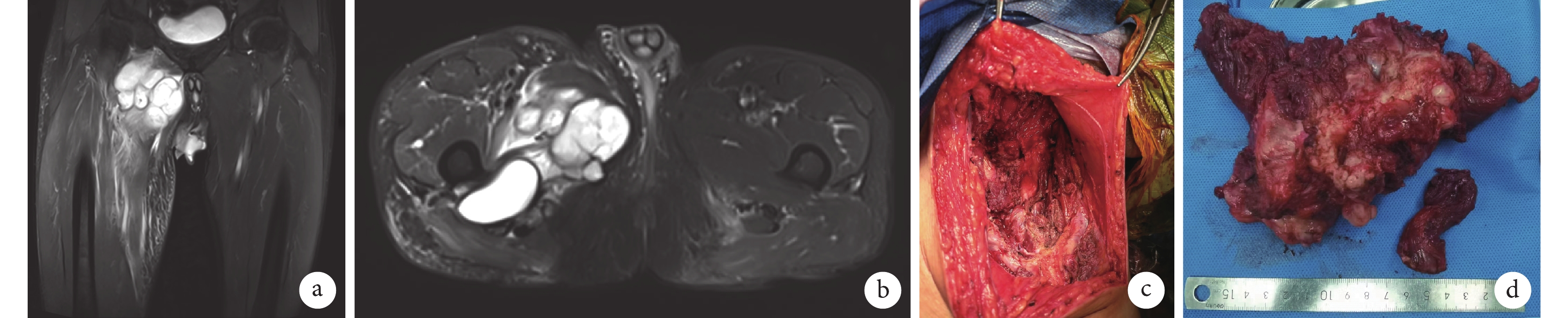
患者,男,66歲,右下肢復發型MPNST,行右大腿軟組織腫塊切除術+神經松解術+鄰近皮瓣修復術
圖4
患者,男,66歲,右下肢復發型MPNST,行右大腿軟組織腫塊切除術+神經松解術+鄰近皮瓣修復術
a、b. 術前MRI示右大腿內側不規則分葉狀軟組織腫塊;c、d. 術中右大腿病灶部位及切除的軟組織腫塊
Figure4. A 66-year-old male patient with recurrent MPNST of right lower limb, underwent resection of soft tissue mass of right thigh+neurolysis+adjacent flap repaira, b. Preoperative MRI showed irregular lobulated soft tissue mass of right medial thigh; c, d. The lesion site of right thigh and the resected soft tissue mass during operation
1.2 研究內容
① 按照是否合并NF1進行分組,比較兩組患者的基線特征。② 本研究1年DFS是以出現有臨床記錄的復發、疾病進展或死亡為結局事件,3年OS是以患者死亡為結局事件。使用Kaplan-Meier法分別繪制每個因素(年齡、性別、是否合并NF1、是否復發型MPNST、是否Ⅳ期MPNST、FNCLCC分級、是否R0切除、腫瘤部位、腫瘤大小、腫瘤深度、是否圍術期化療、是否術后輔助放療、是否安羅替尼靶向治療)下各分組人群的1年DFS和3年OS生存曲線,并用Log-Rank檢驗不同生存曲線間的差異是否有統計學意義。③ 使用多因素COX比例風險模型探索MPNST的獨立預后影響因素。
1.3 統計學方法
采用R 4.1.3統計軟件進行分析。分類資料以例數及率(%)表示,組間比較采用四格表卡方檢驗或列聯表卡方檢驗。生存分析組間比較采用Log-Rank檢驗,MPNST的獨立預后影響因素采用多因素COX比例風險模型分析。檢驗水準取雙側α=0.05。
2 結果
2.1 以合并NF1與否分組的MPNST患者基線資料比較
合并NF1組較未合并NF1組患者腫瘤更多位于表淺、FNCLCC分級較低者更多,差異有統計學意義(P<0.05);其他指標兩組間比較差異均無統計學意義(P<0.05)。見表1。
2.2 對MPNST預后產生影響的因素
2.2.1 1年DFS影響因素
Kaplan-Meier分析示,是否復發型MPNST、是否Ⅳ期MPNST、FNCLCC分級、是否R0切除、是否圍術期化療、是否安羅替尼靶向治療均為1年DFS影響因素(P<0.05)。其中FNCLCC分級G1級患者的1年DFS明顯高于G2、G3級者,非R0切除患者也呈現更高的1年DFS,而接受圍術期化療和安羅替尼靶向者的1年DFS則明顯低于未接受上述治療者,復發型MPNST和Ⅳ期MPNST者1年DFS也顯著低于未具備上述特征者,差異均有統計學意義(P<0.05)。此外,年齡、性別以及是否合并NF1、腫瘤部位、腫瘤大小、腫瘤深度、是否術后輔助放療等因素對1年DFS無顯著影響(P>0.05)。
2.2.2 3年OS影響因素
Kaplan-Meier分析示,是否Ⅳ期MPNST、FNCLCC分級以及是否圍術期化療是3年OS影響因素(P<0.05)。其中FNCLCC分級G1級患者3年OS明顯高于G2、G3級者(G3級最低),接受圍術期化療者3年OS低于未接受圍術期化療者,Ⅳ期MPNST者3年OS也顯著低于非Ⅳ期MPNST者,差異均有統計學意義(P<0.05)。而年齡、性別、是否合并NF1、是否復發型MPNST、是否R0切除、腫瘤部位、腫瘤大小、腫瘤深度、是否術后輔助放療、是否安羅替尼靶向治療等因素對3年OS無顯著影響(P>0.05)。
2.3 多因素COX比例風險模型分析MPNST的獨立預后影響因素
多因素COX比例風險模型分析示,對于1年DFS,復發型MPNST和高級別FNCLCC分級(G3)是獨立預后影響因素(P<0.05)。對于3年OS,Ⅳ期MPNST和腫瘤表淺患者預后較差(P<0.05);>60歲患者、接受術后輔助放療和安羅替尼靶向治療的患者預后較好(P<0.05)。這說明上述幾個因素在被單獨評估時可能存在總生存獲益。見表2、3。
3 討論
MPNST是一種較罕見的軟組織肉瘤,具有較高復發率和轉移率[7]。既往研究多聚焦于單一因素對MPNST的影響,本研究則納入了多種因素探索與MPNST患者預后的相關性。
本研究首先關注NF1與MPNST的緊密聯系。8%~13%的NF1患者可能繼發MPNST,諸多研究也提示了兩種疾病之間存在相關性[8-9]。既往的大樣本臨床研究表明,合并NF1的MPNST患者預后差于未合并NF1者[9-10];但我們的研究顯示,32例(33.3%)合并NF1的MPNST患者與64例(66.7%)未合并NF1的MPNST患者在1年DFS和3年OS上并未出現具有統計學意義的差異。
NF1是一種常染色體顯性遺傳病,由NF1基因種系雜合喪失功能致病性突變引起,其特征性臨床表現為多發性良性神經纖維瘤、Lisch結節和牛奶咖啡斑。叢狀神經纖維瘤是NF1的亞型,占比約50%,雖然腫瘤部位更表淺,FNCLCC分級也較低,但相較而言侵襲性更大,并導致受累區域外觀和功能受損[11]。這也解釋了我們的研究中合并NF1的MPNST患者出現如此基線特征的原因[12]。
值得注意的是,盡管多柔比星+異環磷酰胺(AI方案)廣泛應用于軟組織腫瘤的化療治療中[13],但很多研究表明,MPNST患者對化療的反應較差,尤其是NF1相關患者[14-15]。此外,雖然有研究表明放療對改善MPNST局部復發有效,但它對總體生存優勢的改善作用仍存在爭議[14,16-18]。本研究同樣驗證了這一點,患者接受化療被視為病情進展后的治療選擇,且并無明顯的生存獲益;盡管多因素COX比例風險模型分析顯示接受術后輔助放療為改善3年OS預后的獨立影響因素,但依舊缺乏足夠證據。
意外的是,有研究[19-20]在NF1相關MPNST小鼠模型中發現了一種癌癥干細胞,這反而使化療治療MPNST促進腫瘤再生。因此,目前主要的研究方向聚焦于靶向治療中。一些研究將BRAF/MEK抑制劑應用于NF1和NF1相關的MPNST并開展臨床研究,其中司美替尼已被美國食品藥品監督管理局(FDA)批準用于NF1的靶向治療[21]。還有細胞周期依賴性激酶4/6-MEK被抑制,使聯用的免疫藥物PD-L1增敏,增加細胞毒性,促進腫瘤殺傷[22]。此外,還有一些新的靶點抑制劑也帶來了更多治療MPNST尤其是NF1相關MPNST的可能[23-31]。
本研究收集接受靶向治療的患者所用藥物為安羅替尼,是一種多靶點小分子酪氨酸激酶抑制劑,其應用于軟組織腫瘤治療的臨床研究已取得積極成果[32-34]。事實上,證據等級較高的臨床研究對適用靶向治療的患者有較為嚴格的篩選,而本研究所納入患者無較多限制,因此盡管我們的生存分析顯示這部分患者無顯著生存獲益,但這可能是由于采取靶向治療的患者主要多處于無法接受手術的進展期所導致;而我們的多因素COX比例風險模型分析發現接受安羅替尼靶向治療可能是改善預后的獨立預測影響因素,這與既往臨床研究結論相一致。針對MPNST的靶向治療,可在日后開展更為完善的臨床研究深入討論。
眾多回顧性研究表明,手術切緣對患者局部復發及生存等有較大影響。Sobczuk等[35]的回顧性研究顯示,有微觀或宏觀殘留病灶的患者局部復發風險顯著增加。Zou等[36]和Okada等[37]的研究也表明,手術切緣陽性增加了局部腫瘤復發概率,并認為不充分的手術切緣是復發的危險因素。不僅如此,手術切緣狀態還與患者總生存率有關,盡管R1切除(肉眼下觀察腫瘤切除干凈,但在顯微鏡下發現腫瘤細胞殘留)可能并不影響生存預后[36],但充分切除可大幅降低死亡風險[38-39],而R2切除(在肉眼下觀察到腫瘤細胞殘留)被證明與更差的生存預后相關[40]。然而,對于有條件完成R0切除的患者,不同的特征性因素也影響預后獲益。本研究的生存分析顯示R0切除與患者的1年DFS相關,這印證了既往的研究結論。然而,多因素COX比例風險模型分析結果顯示接受R0切除并非改善預后的獨立影響因素,說明R0切除的選擇受到其他因素的限制。
本研究中的多因素COX比例風險模型分析還顯示,>60歲患者可能有3年OS的獲益,該結論與既往文獻結論有所不同。諸多文獻認為年齡較大的患者是預測較差OS的獨立預后因素[10,41],提示不同年齡結構患者的選擇可能存在偏倚,需要更大范圍和樣本量的研究進一步驗證。另外,本研究結果顯示FNCLCC分級是MPNST患者1年DFS的獨立預后因素。FNCLCC分級已廣泛應用于各種軟組織腫瘤的病理分級中[42-43],并與MPNST的預后密切相關[44]。鑒于FNCLCC清晰且較簡便的分級標準,我們認為FNCLCC可以更廣泛地用于包括MPNST在內的軟組織腫瘤中,便于類似臨床研究更廣泛、更深層次的開展。
但本研究存在諸多局限性。首先,為單中心回顧性研究,樣本量較少,存在選擇偏倚,使本研究部分結果與主流研究結論存在一定偏差;其次,部分數據存在缺失,主要是由于一些患者為轉診而來,病理會診相較本院手術后病理缺少腫瘤大小、分級等信息;第三,所有患者的靶向治療具體用藥時間未被統計,因此我們只能針對靶向治療與否而非更具體的靶向治療策略展開研究;最后,本研究僅為相關性研究而非機制研究,MPNST的致病機制仍需要基礎實驗進一步探討。
綜上述,NF1、FNCLCC分級、R0切除和輔助治療是MPNST患者重要的預后因素,后兩者的更廣泛應用可能會提供更優的DFS或OS。盡管合并NF1的MPNST腫瘤深度較表淺、分級較低,但眾多研究已表明其進展較快,侵襲性高,與復發型MPNST和轉移期MPNST相關性較高。對于MPNST,臨床治療中應優先考慮完全切除腫瘤,并結合輔助治療以改善患者預后,尤其是合并NF1的患者。
利益沖突 在課題研究和文章撰寫過程中不存在利益沖突
倫理聲明 研究方案經復旦大學附屬腫瘤醫院醫學倫理委員會批準(161267-18)
作者貢獻聲明 嚴望軍:研究設計和指導,審閱并修改論文;胡湘麟、鄭皓予:參與臨床信息收集,論文修改;吳華健:核對患者信息;嚴望軍、胡湘麟、吳華健:提供部分患者的影像學圖片;史伯翀:臨床信息收集、數據統計分析、論文撰寫
惡性周圍神經鞘瘤(malignant peripheral nerve sheath tumor,MPNST)起源于間充質細胞,是一種具有侵襲性和轉移潛力的軟組織肉瘤,并且容易復發和產生耐藥性。它是一種罕見疾病,總人群患病率約為1/10萬,占所有軟組織肉瘤的2%~4%[1],其中23%~51%的MPNST是由Ⅰ型神經纖維瘤病(neurofibromatosis type 1,NF1)惡變而來。四肢和軀干是MPNST最常見發病部位,而頭頸部較少。根治性手術切除是目前主要治療方法,但可能因復雜的解剖結構而受限。目前尚無充分證據支持放療和化療能夠改善MPNST患者的預后。同時,有許多免疫和靶向療法的臨床研究正在展開,包括利用哺乳動物雷帕霉素靶蛋白(mTOR)抑制劑依維莫司聯合貝伐單抗治療NF1[2],通過絲裂原活化蛋白激酶激酶(mitogen-activated protein kinase kinase,MEK)抑制劑司美替尼聯合程序性死亡配體1(programmed death-ligand 1,PD-L1)單抗德瓦魯單抗治療包括MPNST在內的軟組織肉瘤[3],還有運用受體酪氨酸激酶(receptor tyrosine kinase,RTK)抑制劑安羅替尼聯合艾立布林和替雷利珠單抗治療復發難治性軟組織肉瘤[4]等,但是目前幾乎沒有令人滿意的結果。
既往研究報道腫瘤完全切除和較寬的陰性切緣可降低遠處復發風險[5]。而隨著外科技術的發展,除了一些腫瘤與重要血管、神經毗鄰難以達陰性切緣手術外,大部分手術可達到腫瘤完全切除的目的。因此我們對患者預后影響因素的認識仍不全面。本研究收集了復旦大學附屬腫瘤醫院治療的MPNST患者,根據相關因素進行1年無疾病生存期(disease-free survival,DFS)和3年總生存期(overall survival,OS)的生存分析,結合患者臨床資料,探索不同因素與患者預后的相關性,并使用多因素COX比例風險模型分析影響MPNST患者的獨立預后影響因素。報告如下。
1 資料與方法
1.1 研究對象
患者納入標準:① 排除手術禁忌證進行相應部位手術后,經病理學專家評估存在高度異型性腫瘤細胞、核分裂象增多以及S-100蛋白等相關標志物的陽性表達,再根據病例信息排除其他可疑診斷而確診為MPNST的患者;② 確診時間為2015年1月1日—2021年12月31日,以確保研究數據的時效性和一致性;③ 隨訪資料齊全。該期間復旦大學附屬腫瘤醫院共96例患者符合標準納入研究。
本組男46例,女50例;年齡15~87歲,平均48.2歲,其中<35歲29例、35~60歲34例、≥60歲33例。腫瘤部位:軀干50例,四肢39例,頭頸部7例。腫瘤大小:最大徑<5 cm 49例,≥5 cm 32例,缺失15例。腫瘤深度:深部(腫瘤位于肌肉、骨骼、肌間隙或腹腔、腹膜后)77例,表淺(腫瘤位于淺筋膜或更淺位置)19例。法國國家癌癥中心聯盟(FNCLCC)組織學分級[6]:G1 9例,G2 12例,G3 34例,缺失41例。37例為復發型MPNST,32例合并NF1,26例為Ⅳ期MPNST(即出現淋巴結轉移或遠處轉移)。25例接受術后輔助放療,45例接受圍術期化療,30例接受安羅替尼靶向治療,73例行R0切除(即術后病理顯示切除標本各切緣均為陰性,原病灶區無腫瘤殘留)。見圖1~4。
 圖1
患者,男,25歲,胸椎(C7~T6)Ⅳ期MPNST,行胸椎腫瘤切除術+胸椎(植骨)融合術+鄰近皮瓣修復術
圖1
患者,男,25歲,胸椎(C7~T6)Ⅳ期MPNST,行胸椎腫瘤切除術+胸椎(植骨)融合術+鄰近皮瓣修復術
a、b. 術前MRI示瘤體位于右胸背部并壓迫胸椎,大小約100 mm×80 mm,伴發雙肺及縱膈淋巴結轉移;c、d. 術后4 d正側位X線片示T2~T5椎弓根螺釘內固定影
Figure1. A 25-year-old male patient with thoracic spine (C7-T6) stage Ⅳ MPNST, underwent thoracic spine tumor resection+thoracic spine (bone graft) fusion+adjacent flap repaira, b. Preoperative MRI showed that the tumor was located in the right thoracic back and compressed the thoracic spine, about 100 mm×80 mm in size, with bilateral lung and mediastinal lymph node metastasis; c, d. Anteroposterior and lateral X-ray films at 4 days after operation showed the image of pedicle screw fixation at T2-T5
 圖2
患者,男,51歲,胸腰段(T10~L1)復發型MPNST,行后路胸腰椎腫瘤切除術+胸腰椎融合內固定術
圖2
患者,男,51歲,胸腰段(T10~L1)復發型MPNST,行后路胸腰椎腫瘤切除術+胸腰椎融合內固定術
a~c. 術前MRI示胸腰椎旁軟組織腫塊,約99 mm×90 mm,T9、T10水平脊髓和神經根受壓;d、e. 術中T11病灶部位及切除的軟組織腫塊和T11、12椎體;f. 術后7 d X線片示T11、12人工椎體及T8~10、L1~3椎弓根螺釘影
Figure2. A 51-year-old male patient with thoracolumbar (T10-L1) recurrent MPNST, underwent posterior thoracolumbar tumor resection+thoracolumbar fusion and internal fixationa-c. Preoperative MRI showed a thoracolumbar paravertebral soft tissue mass, about 99 mm×90 mm, spinal cord and nerve root compression at T9 and T10 levels; d, e. The location of T11 lesion and the resected soft tissue mass and T11, 12 vertebral bodies during operation; f. X-ray film of T11, 12 artificial vertebral bodies and pedicle screw shadows of T8-10 and L1-3 vertebral bodies at 7 days after operation
 圖3
患者,男,26歲,L4~S4節段初發型MPNST,行后路骶骨腫瘤切除植骨融合內固定術
圖3
患者,男,26歲,L4~S4節段初發型MPNST,行后路骶骨腫瘤切除植骨融合內固定術
a~c. 術前MRI示左側骶髂關節骨質破壞伴軟組織腫塊形成,大小約86 mm×79 mm×95 mm,累及周圍組織、神經根及椎管;d、e. 術后1 d正側位X線片示骶骨腫瘤切除術后,L4、5至骶骨椎弓根螺釘內固定影
Figure3. A 26-year-old male patient with L4-S4 segment initial MPNST, underwent posterior sacral tumor resection, bone graft fusion, and internal fixationa-c. Preoperative MRI showed left sacroiliac joint bone destruction with soft tissue mass formation, about 86 mm×79 mm×95 mm in size, involving surrounding tissues, nerve roots, and spinal canal; d, e. Anteroposterior and lateral X-ray films at 1 day after operation showed the image of pedicle screws fixation from L4, 5 to sacrum after sacral tumor resection
 圖4
患者,男,66歲,右下肢復發型MPNST,行右大腿軟組織腫塊切除術+神經松解術+鄰近皮瓣修復術
圖4
患者,男,66歲,右下肢復發型MPNST,行右大腿軟組織腫塊切除術+神經松解術+鄰近皮瓣修復術
a、b. 術前MRI示右大腿內側不規則分葉狀軟組織腫塊;c、d. 術中右大腿病灶部位及切除的軟組織腫塊
Figure4. A 66-year-old male patient with recurrent MPNST of right lower limb, underwent resection of soft tissue mass of right thigh+neurolysis+adjacent flap repaira, b. Preoperative MRI showed irregular lobulated soft tissue mass of right medial thigh; c, d. The lesion site of right thigh and the resected soft tissue mass during operation
1.2 研究內容
① 按照是否合并NF1進行分組,比較兩組患者的基線特征。② 本研究1年DFS是以出現有臨床記錄的復發、疾病進展或死亡為結局事件,3年OS是以患者死亡為結局事件。使用Kaplan-Meier法分別繪制每個因素(年齡、性別、是否合并NF1、是否復發型MPNST、是否Ⅳ期MPNST、FNCLCC分級、是否R0切除、腫瘤部位、腫瘤大小、腫瘤深度、是否圍術期化療、是否術后輔助放療、是否安羅替尼靶向治療)下各分組人群的1年DFS和3年OS生存曲線,并用Log-Rank檢驗不同生存曲線間的差異是否有統計學意義。③ 使用多因素COX比例風險模型探索MPNST的獨立預后影響因素。
1.3 統計學方法
采用R 4.1.3統計軟件進行分析。分類資料以例數及率(%)表示,組間比較采用四格表卡方檢驗或列聯表卡方檢驗。生存分析組間比較采用Log-Rank檢驗,MPNST的獨立預后影響因素采用多因素COX比例風險模型分析。檢驗水準取雙側α=0.05。
2 結果
2.1 以合并NF1與否分組的MPNST患者基線資料比較
合并NF1組較未合并NF1組患者腫瘤更多位于表淺、FNCLCC分級較低者更多,差異有統計學意義(P<0.05);其他指標兩組間比較差異均無統計學意義(P<0.05)。見表1。
2.2 對MPNST預后產生影響的因素
2.2.1 1年DFS影響因素
Kaplan-Meier分析示,是否復發型MPNST、是否Ⅳ期MPNST、FNCLCC分級、是否R0切除、是否圍術期化療、是否安羅替尼靶向治療均為1年DFS影響因素(P<0.05)。其中FNCLCC分級G1級患者的1年DFS明顯高于G2、G3級者,非R0切除患者也呈現更高的1年DFS,而接受圍術期化療和安羅替尼靶向者的1年DFS則明顯低于未接受上述治療者,復發型MPNST和Ⅳ期MPNST者1年DFS也顯著低于未具備上述特征者,差異均有統計學意義(P<0.05)。此外,年齡、性別以及是否合并NF1、腫瘤部位、腫瘤大小、腫瘤深度、是否術后輔助放療等因素對1年DFS無顯著影響(P>0.05)。
2.2.2 3年OS影響因素
Kaplan-Meier分析示,是否Ⅳ期MPNST、FNCLCC分級以及是否圍術期化療是3年OS影響因素(P<0.05)。其中FNCLCC分級G1級患者3年OS明顯高于G2、G3級者(G3級最低),接受圍術期化療者3年OS低于未接受圍術期化療者,Ⅳ期MPNST者3年OS也顯著低于非Ⅳ期MPNST者,差異均有統計學意義(P<0.05)。而年齡、性別、是否合并NF1、是否復發型MPNST、是否R0切除、腫瘤部位、腫瘤大小、腫瘤深度、是否術后輔助放療、是否安羅替尼靶向治療等因素對3年OS無顯著影響(P>0.05)。
2.3 多因素COX比例風險模型分析MPNST的獨立預后影響因素
多因素COX比例風險模型分析示,對于1年DFS,復發型MPNST和高級別FNCLCC分級(G3)是獨立預后影響因素(P<0.05)。對于3年OS,Ⅳ期MPNST和腫瘤表淺患者預后較差(P<0.05);>60歲患者、接受術后輔助放療和安羅替尼靶向治療的患者預后較好(P<0.05)。這說明上述幾個因素在被單獨評估時可能存在總生存獲益。見表2、3。
3 討論
MPNST是一種較罕見的軟組織肉瘤,具有較高復發率和轉移率[7]。既往研究多聚焦于單一因素對MPNST的影響,本研究則納入了多種因素探索與MPNST患者預后的相關性。
本研究首先關注NF1與MPNST的緊密聯系。8%~13%的NF1患者可能繼發MPNST,諸多研究也提示了兩種疾病之間存在相關性[8-9]。既往的大樣本臨床研究表明,合并NF1的MPNST患者預后差于未合并NF1者[9-10];但我們的研究顯示,32例(33.3%)合并NF1的MPNST患者與64例(66.7%)未合并NF1的MPNST患者在1年DFS和3年OS上并未出現具有統計學意義的差異。
NF1是一種常染色體顯性遺傳病,由NF1基因種系雜合喪失功能致病性突變引起,其特征性臨床表現為多發性良性神經纖維瘤、Lisch結節和牛奶咖啡斑。叢狀神經纖維瘤是NF1的亞型,占比約50%,雖然腫瘤部位更表淺,FNCLCC分級也較低,但相較而言侵襲性更大,并導致受累區域外觀和功能受損[11]。這也解釋了我們的研究中合并NF1的MPNST患者出現如此基線特征的原因[12]。
值得注意的是,盡管多柔比星+異環磷酰胺(AI方案)廣泛應用于軟組織腫瘤的化療治療中[13],但很多研究表明,MPNST患者對化療的反應較差,尤其是NF1相關患者[14-15]。此外,雖然有研究表明放療對改善MPNST局部復發有效,但它對總體生存優勢的改善作用仍存在爭議[14,16-18]。本研究同樣驗證了這一點,患者接受化療被視為病情進展后的治療選擇,且并無明顯的生存獲益;盡管多因素COX比例風險模型分析顯示接受術后輔助放療為改善3年OS預后的獨立影響因素,但依舊缺乏足夠證據。
意外的是,有研究[19-20]在NF1相關MPNST小鼠模型中發現了一種癌癥干細胞,這反而使化療治療MPNST促進腫瘤再生。因此,目前主要的研究方向聚焦于靶向治療中。一些研究將BRAF/MEK抑制劑應用于NF1和NF1相關的MPNST并開展臨床研究,其中司美替尼已被美國食品藥品監督管理局(FDA)批準用于NF1的靶向治療[21]。還有細胞周期依賴性激酶4/6-MEK被抑制,使聯用的免疫藥物PD-L1增敏,增加細胞毒性,促進腫瘤殺傷[22]。此外,還有一些新的靶點抑制劑也帶來了更多治療MPNST尤其是NF1相關MPNST的可能[23-31]。
本研究收集接受靶向治療的患者所用藥物為安羅替尼,是一種多靶點小分子酪氨酸激酶抑制劑,其應用于軟組織腫瘤治療的臨床研究已取得積極成果[32-34]。事實上,證據等級較高的臨床研究對適用靶向治療的患者有較為嚴格的篩選,而本研究所納入患者無較多限制,因此盡管我們的生存分析顯示這部分患者無顯著生存獲益,但這可能是由于采取靶向治療的患者主要多處于無法接受手術的進展期所導致;而我們的多因素COX比例風險模型分析發現接受安羅替尼靶向治療可能是改善預后的獨立預測影響因素,這與既往臨床研究結論相一致。針對MPNST的靶向治療,可在日后開展更為完善的臨床研究深入討論。
眾多回顧性研究表明,手術切緣對患者局部復發及生存等有較大影響。Sobczuk等[35]的回顧性研究顯示,有微觀或宏觀殘留病灶的患者局部復發風險顯著增加。Zou等[36]和Okada等[37]的研究也表明,手術切緣陽性增加了局部腫瘤復發概率,并認為不充分的手術切緣是復發的危險因素。不僅如此,手術切緣狀態還與患者總生存率有關,盡管R1切除(肉眼下觀察腫瘤切除干凈,但在顯微鏡下發現腫瘤細胞殘留)可能并不影響生存預后[36],但充分切除可大幅降低死亡風險[38-39],而R2切除(在肉眼下觀察到腫瘤細胞殘留)被證明與更差的生存預后相關[40]。然而,對于有條件完成R0切除的患者,不同的特征性因素也影響預后獲益。本研究的生存分析顯示R0切除與患者的1年DFS相關,這印證了既往的研究結論。然而,多因素COX比例風險模型分析結果顯示接受R0切除并非改善預后的獨立影響因素,說明R0切除的選擇受到其他因素的限制。
本研究中的多因素COX比例風險模型分析還顯示,>60歲患者可能有3年OS的獲益,該結論與既往文獻結論有所不同。諸多文獻認為年齡較大的患者是預測較差OS的獨立預后因素[10,41],提示不同年齡結構患者的選擇可能存在偏倚,需要更大范圍和樣本量的研究進一步驗證。另外,本研究結果顯示FNCLCC分級是MPNST患者1年DFS的獨立預后因素。FNCLCC分級已廣泛應用于各種軟組織腫瘤的病理分級中[42-43],并與MPNST的預后密切相關[44]。鑒于FNCLCC清晰且較簡便的分級標準,我們認為FNCLCC可以更廣泛地用于包括MPNST在內的軟組織腫瘤中,便于類似臨床研究更廣泛、更深層次的開展。
但本研究存在諸多局限性。首先,為單中心回顧性研究,樣本量較少,存在選擇偏倚,使本研究部分結果與主流研究結論存在一定偏差;其次,部分數據存在缺失,主要是由于一些患者為轉診而來,病理會診相較本院手術后病理缺少腫瘤大小、分級等信息;第三,所有患者的靶向治療具體用藥時間未被統計,因此我們只能針對靶向治療與否而非更具體的靶向治療策略展開研究;最后,本研究僅為相關性研究而非機制研究,MPNST的致病機制仍需要基礎實驗進一步探討。
綜上述,NF1、FNCLCC分級、R0切除和輔助治療是MPNST患者重要的預后因素,后兩者的更廣泛應用可能會提供更優的DFS或OS。盡管合并NF1的MPNST腫瘤深度較表淺、分級較低,但眾多研究已表明其進展較快,侵襲性高,與復發型MPNST和轉移期MPNST相關性較高。對于MPNST,臨床治療中應優先考慮完全切除腫瘤,并結合輔助治療以改善患者預后,尤其是合并NF1的患者。
利益沖突 在課題研究和文章撰寫過程中不存在利益沖突
倫理聲明 研究方案經復旦大學附屬腫瘤醫院醫學倫理委員會批準(161267-18)
作者貢獻聲明 嚴望軍:研究設計和指導,審閱并修改論文;胡湘麟、鄭皓予:參與臨床信息收集,論文修改;吳華健:核對患者信息;嚴望軍、胡湘麟、吳華健:提供部分患者的影像學圖片;史伯翀:臨床信息收集、數據統計分析、論文撰寫