引用本文: 朱寶晨, 肖楊, 廖睿恒, 趙焓杏, 許學文, 張艷閣. Ⅰ型神經纖維瘤病相關巨大叢狀神經纖維瘤破裂出血急診處理及圍術期管理策略. 中國修復重建外科雜志, 2024, 38(10): 1180-1185. doi: 10.7507/1002-1892.202406074 復制
版權信息: ?四川大學華西醫院華西期刊社《中國修復重建外科雜志》版權所有,未經授權不得轉載、改編
叢狀神經纖維瘤(plexiform neurofibroma,PNF)是一種幾乎只出現在Ⅰ型神經纖維瘤病(neurofibromatosis type 1,NF1)的良性腫瘤,在NF1患者中發生率為27%~44%[1],其沿著全身各處神經叢生長,與周圍組織邊界不清,具有局部侵襲性。先天性PNF的瘤體隨年齡增加而逐漸增大,部分可發展成瘤體面積>100 cm2的巨大神經纖維瘤,導致患者功能障礙甚至毀容。此外,NF1患者PNF有8%~13%概率會惡變為惡性周圍神經鞘瘤[2]。因顯著的腫瘤血管形成和豐富的畸形血管,PNF的急性瘤體內出血更是NF1患者繼腫瘤惡變外較為常見的死因[3]。對于PNF的擇期手術治療策略,國內外學者提出了相關意見[4-6]。但部分PNF患者因為經濟或未接受過此疾病科普教育等原因,并未獲得合適的早期治療,最后以巨大PNF破裂出血急診入院。巨大PNF破裂出血較為兇險且復發概率高,目前國內外尚無較為系統的急診處理及圍術期管理策略。本文將復習相關文獻并結合我科處理巨大PNF破裂出血的臨床實踐,綜述急診超選擇動脈栓塞聯合手術切除治療巨大PNF破裂出血方法及療效,并討論圍術期管理策略,以期為臨床治療提供參考。
1 巨大PNF破裂出血的可能機制
巨大PNF破裂出血的機制可能有:① 神經纖維瘤組織侵入血管壁,導致自發性出血[7];② 創傷導致脆弱血管壁破裂[8];③ 瘤體內存在大量血管畸形,包括動脈瘤、動脈狹窄及動靜脈畸形等[3]。組織學研究表明,腫瘤內大量新生血管的血管壁僅由內皮和幾條結締組織纖維組成,沒有肌層,由于中膜變薄和彈性膜破裂,血管壁變得脆弱,因此在輕微創傷下就可能導致瘤內出血[9-11]。
2 巨大PNF破裂出血的診斷
巨大PNF瘤體內出血的臨床表現為:① 腫瘤體積快速變大,伴有壓迫癥狀。無論是自發性出血或是創傷后血腫形成,瘤體會在短時間出現明顯體積增大,往往伴有疼痛及神經壓迫表現。② 瘤體表面緊張或出現波動感,繼而破潰出血。病程較長的瘤體內出血由于對皮膚持續性壓迫,導致腫瘤中心區域皮膚出現壞死及破潰,進而可能持續性排出陳舊性血液。③ 血流動力學不穩定。巨大PNF破裂出血后由于瘤體內大量血液蓄積,患者轉診至醫院時多存在血流動力學不穩定,但較少出現短期內危及生命的情形,不過仍然有部分巨大瘤體患者出血后數小時即發展為低血容量休克甚至死亡[9,12]。當NF1患者發生不明原因休克時,往往需要考慮腫瘤內出血的可能。
除了以上初診時快速判斷的方法,巨大PNF破裂出血多依賴于影像學診斷。三維CT和MRI均能揭示腫瘤的內部特征及其對周圍組織的侵襲,活動性出血和血腫形成也可較為容易地通過影像學判斷[13]。瘤體在CT中邊界不清,形成的血腫在平掃CT中表現為高密度和等密度,對比增強CT圖像無增強表現。MRI T1加權像上,瘤體內血腫顯示出異質的中到高信號強度;在T2加權像上,瘤體內血腫則顯示出輕微的低到中等信號強度,圍繞血腫的區域有時還會出現一低信號環。有研究表明[14],MRI上的“流空征”可能是手術切除軀干巨大PNF時發生圍術期出血事件的唯一預測因素。而術前經導管血管栓塞術(transcatheter aortic embolization,TAE)可以降低有流空征的巨大PNF圍術期出血事件風險。但如高度懷疑巨大PNF破裂出血,CT血管造影(CT angiography,CTA)可能是早期判斷出血責任血管更好的選擇。
3 巨大PNF破裂出血的治療
巨大PNF破裂出血患者的一般情況較差,且手術出血量大,其臨床治療往往面臨許多挑戰。常見治療方法有單純清除血腫、TAE、減瘤或根治性切除手術。在20世紀中葉,因外科手術技術的限制,針對巨大PNF破裂出血多采取單純清除血腫同時結扎出血血管來控制活動性出血及腫瘤的占位效應。但由于病因未解除,這種方式復發出血概率較高,患者出院后多因輕微創傷或自發性出血而再次入院[9,15],甚至手術操作本身就可能引發更嚴重出血[16]。隨著血管介入技術的發展,術前TAE被用于控制巨大PNF手術中出血,超選擇動脈栓塞聯合外科序貫治療也成為巨大神經纖維瘤的重要治療策略[4]。許多入院時血流動力學不穩定的巨大PNF出血患者也受益于數字減影血管造影(digital subtraction angiography,DSA)聯合TAE的止血策略,極大地提高了此類患者的生存率[12]。如單獨應用TAE而不結合手術減瘤,栓塞血管可能再通或者建立側支循環,往往后期會再發出血[17]。考慮到以上情況,目前較為主流的手術治療策略多聯合術前病灶栓塞、術中清除血腫并完成減瘤或根治性切除的綜合方案。
3.1 巨大PNF破裂出血的急診處理
NF1患者因快速增大的PNF于急診就診時,應積極完成以下評估及處置:① 完善血常規、凝血常規、生化常規等血液學檢查及生命體征評估,判斷是否存在活動性出血及血流動力學不穩定的情況。如存在則積極啟動液體復蘇抗休克、輸血、應用止血藥物等治療措施,同時早期聯系血管外科評估DSA聯合TAE的急診止血策略。② 評估腫瘤是否有持續進展壓迫氣道或氣道內出血的風險,若有則應完成氣道保護[18]。③ 評估腫瘤表面是否發生破潰出血,對于破潰處應行加壓包扎,并積極抗感染治療,避免繼發傷口感染甚至敗血癥。④ 如出血部位不明確,可完善CTA檢查。⑤ 在患者生命體征較穩定情況下,給予對癥支持治療,積極完善MRI及相應術前準備,評估手術安全性及安排擇期手術。
3.2 TAE治療
對于血流動力學不穩定、診斷明確的巨大PNF破裂出血患者可首選TAE治療。我們主張在DSA引導下進行超選擇TAE,對瘤體滋養動脈進行栓塞以實現急診止血。但需注意的是,過度或者范圍過大的動脈栓塞止血可能會造成皮瓣壞死,導致血腫破潰,進而繼發感染或增加再次出血風險;并且皮瓣壞死后,瘤體切除后殘留的創面無法用瘤體皮反剔回植修復,需另取皮或轉移皮瓣修復創面,會進一步加重患者創傷。
3.3 手術治療
3.3.1 手術時機
聯合血管外科完成超選擇介入栓塞瘤體滋養動脈后,手術切除破裂出血瘤體的時機尚無統一意見。在臨床實踐中我們發現栓塞術后48 h,血腫周圍自然形成了水腫帶,此水腫帶界限清楚,瘤體內畸形血管顯露明確,沿著水腫帶切除有助于控制術中出血。部分文獻報道了栓塞后即刻或短期內進行手術的患者,可能因血管尚未完全血栓化,此時栓塞效果仍不確切[19]。急診行介入栓塞的主要目的是控制活動性出血,合適的觀察期可明確患者出血是否已得到有效控制。有文獻報道栓塞后患者短期再次出血,提示對栓塞術后患者仍需要繼續嚴密觀察[20]。同時,還需考慮到過長的觀察期會帶來一些潛在風險,一是栓塞后血管可能再通或建立側支循環,二是壞死組織的溶解吸收可能引發一系列并發癥。綜合以上因素,我們建議在栓塞術后至少48 h,但不超過1周的時間內進行瘤體血腫切除。這個時間窗口既可以確保栓塞效果穩定,又能避免因延遲手術帶來的并發癥。我們發現,遵循這一策略可以有效控制術中出血,顯著降低圍術期并發癥發生率,從而提高手術安全性和成功率。
3.3.2 術前準備
巨大PNF的特點是血供豐富、血管脆弱,加之患者常因自發性出血處于貧血狀態,使得術中大出血危及生命的風險顯著增高[21]。鑒于此,全面的術前準備至關重要。充足的血液儲備是手術成功的基礎,需積極備血并進行術前支持治療,包括補充血容量、維持白蛋白水平等。為應對可能的術中大出血,還應備妥凝血因子和人纖維蛋白原。考慮到手術復雜性,應組織多學科團隊共同評估患者手術風險并制定詳細方案,包括完善心肺功能、氣道評估以及圍術期麻醉相關風險評估,同時準備術后重癥監護病房,以確保全面的圍術期管理。這些綜合措施的實施將有效降低手術風險,提高手術成功率。
3.3.3 術中減少出血及監護策略
為了減少PNF術中出血,Lin等[22]提出了3個策略,即麻醉中控制性低血壓,提前對病灶周圍進行初步縫合,結扎血腫內有限數量的供血血管。但有部分學者[23-24]質疑結扎的有效性,指出其無法避免術中大量出血。
對于已經完成了術前瘤體供血動脈介入栓塞的患者,為了減少圍術期并發癥,我們對以上觀點進行了修訂和補充:① 無需術中控制性低血壓。部分術者建議在術中通過控制性低血壓結扎血管以減少出血[25],但對于大多數巨大PNF創面,往往需要植皮覆蓋,而術前栓塞過程已完成了充分止血,術中低血壓可能會導致術后反射性血壓升高,進而引起創面滲血,降低植皮成活率。并且維持正常的術中血壓也有助于保證心、腦、腎等器官充分灌注。② 備好自體血回輸。自體血可避免大量同種異體血輸入導致肺水腫、凝血障礙、發熱等并發癥。但如腫瘤存在破潰感染,則不推薦使用自體血回輸,有可能導致繼發全身感染。③ 手術采用血腫周圍水腫帶入路,沿水腫帶小心剝除瘤體,充分結扎血管,雙極電凝止血。④ 對于無法拉攏閉合的創面,可利用瘤體皮回植覆蓋。⑤ 術中密切監測患者液體出入量、凝血功能、水電解質及動脈血氣。
3.3.4 巨大PNF破裂出血術后管理
在巨大PNF切除術后應持續監測各項血液學指標及生命體征,對癥支持治療,并留意切口情況,定期換藥,根據情況調整抗生素。對于無法一期閉合的大面積創面,Cavallaro等[26]報道了1例巨大PNF患者在栓塞術后出現了廣泛瘤體壞死,隨后行部分瘤體切除術,由于創面過大無法直接縫合,術者采用封閉式負壓引流輔助治療,數月后最終成功完成了二期創面閉合。該病例報道為處理復雜的巨大PNF術后創面提供了新的思路。既往有多篇文獻也報道了在巨大PNF術后或潰瘍創面上使用封閉式負壓引流技術輔助治療,顯示在相對較低的負壓(9.975 kPa)下,治療具有一定安全性和有效性[27-31]。但考慮到巨大PNF有大量脆弱的血管以及極易出血的特性,術后使用負壓創面治療仍需非常謹慎,關于此技術應用于巨大PNF患者的風險與獲益,仍需進一步研究。
4 本中心3例巨大PNF破裂出血典型病例
本中心應用DSA+栓塞技術聯合手術,有效治療了3例巨大PNF破裂出血患者。
例1 患者,男,43歲。因“腰背部PNF突然增大伴疼痛”急診入院。查體:腰背部腫物大小為38 cm×30 cm×10 cm,伴有11 cm×8 cm×7 cm皮膚壞死。血常規檢查示血紅蛋白76 g/L;MRI檢查示病灶內有大小為21.7 cm×17.3 cm×7.1 cm的血腫。急診行DSA+TAE控制出血,DSA示腹主動脈分支和髂內動脈分支供血;予以輸血等對癥支持治療,積極術前準備,栓塞術后48 h在全身麻醉下切除腫瘤及血腫。術中出血約400 mL。術后病理檢查證實為PNF伴血腫形成。術后20 d出院,隨訪12個月未見復發[32]。
例2 患者,女,25歲。因“右大腿部PNF急劇增大伴疼痛”急診入院。查體:右大腿有一大小為26 cm×18 cm×8 cm的巨大腫物,腫物后側伴有15 cm×10 cm大小的潰瘍。血常規示血紅蛋白62 g/L;MRI T2加權像示軟組織腫塊位于右側腰骶區、臀部和大腿,腫塊內可見增粗、增多的血管;CTA示右大腿有大量血腫和活動出血,軟組織腫塊起源于右側腰骶區的皮下組織,腫塊中的血管增粗、迂曲,與股深動脈和股淺動脈的1個分支密切相關。急診行DSA+TAE控制出血,DSA示股深動脈的3條穿支動脈和股淺動脈的1個分支動脈供血;予以輸血等對癥支持治療,積極術前準備,于栓塞術后第3天在全身麻醉下切除腫瘤及血腫。見圖1。術后病理檢查證實為PNF伴血腫形成。術后15 d出院,12個月隨訪未見復發。
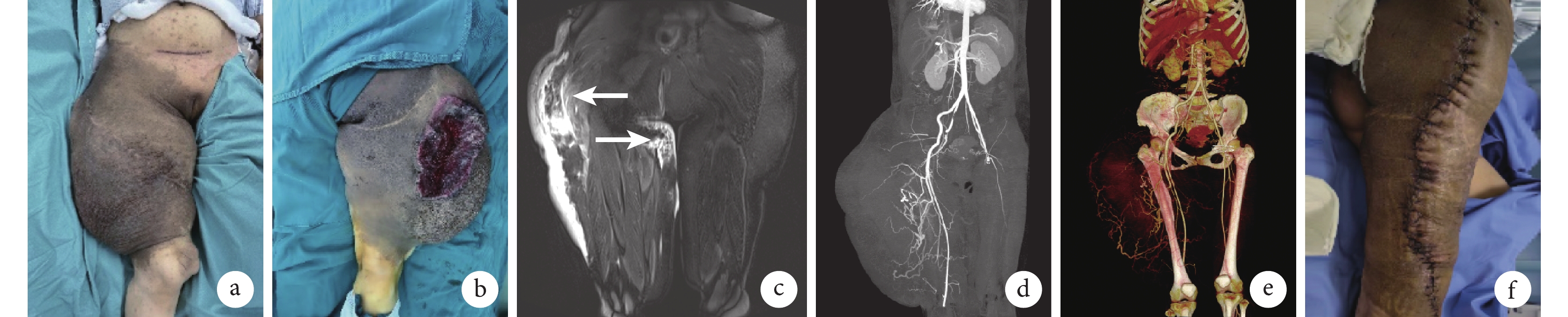 圖1
病例2
圖1
病例2
a. 術前右大腿外觀;b. 術前右大腿后側潰瘍;c. 術前MRI T2加權像(箭頭示腫塊內增粗、增多的血管);d、e. 術前CTA;f. 右大腿PNF血腫及部分瘤體切除術后即刻
Figure1. Case 2a. Preoperative appearance of the right thigh; b. Preoperative ulceration on the posterior aspect of the right thigh; c. Preoperative MRI T2-weighted image (arrow indicated thickened and increased vasculature within the tumor); d, e. Preoperative CTA; f. Immediate postoperative view following hematoma evacuation and partial tumor resection of the right thigh PNF
例3 患者,女,27歲。因“背部PNF急劇增大”急診入院。查體:右側背部腫物大小為55 cm×36 cm×14 cm,伴有表面15 cm×4 cm的皮膚壞死。血常規示血紅蛋白60 g/L;CTA示右側背部及胸腹壁軟組織明顯增厚,右側背部皮下見巨大混雜密度腫塊影,邊界不清,大小難以測量,內見片團狀高密度影,增強不均勻強化,可見胸外動脈走行。急診行DSA+TAE控制出血,DSA示右肩胛下動脈分支為瘤體供血。患者合并重度脊柱側彎,予以輸血等對癥支持治療,積極術前準備,經多學科會診后于栓塞術后第6天在全身麻醉下切除腫瘤,在切除瘤體內可見約44 cm×27 cm的血腫形成。術后16 d出院,10個月隨訪未見復發。見圖2。
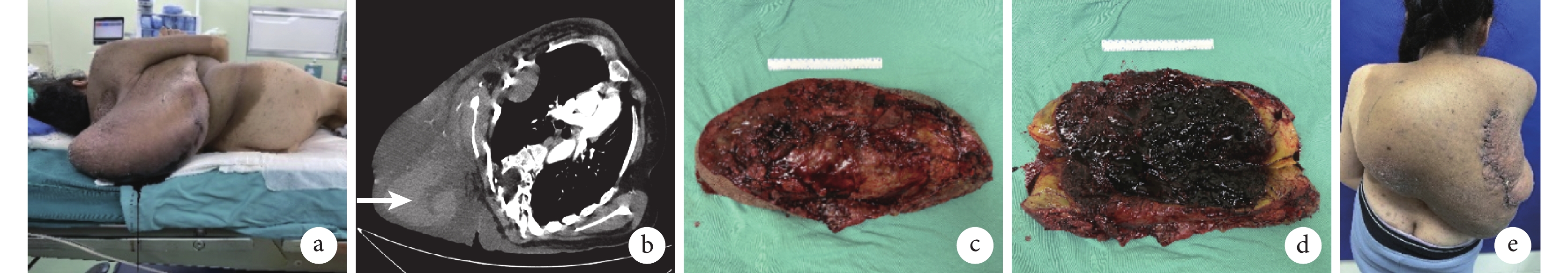 圖2
病例3
圖2
病例3
a. 術前背部外觀;b. 術前CT示腫塊內血腫形成(箭頭);c、d. 術中切除的病灶,可見瘤體內血腫形成(約44 cm×27 cm);e. 術后3周背部外觀
Figure2. Case 3a. Preoperative appearance of the back; b. Preoperative CT showed hematoma formation within the tumor (arrow); c, d. Intraoperative view of the excised lesion demonstrating hematoma formation within the tumor (44 cm×27 cm); e. Appearance of the back at 3 weeks after operation
5 總結及展望
本文通過回顧臨床文獻并結合我科在處理NF1相關巨大PNF破裂出血中的實踐經驗,提出了一系列急診處理方案及圍術期管理策略。巨大PNF急性出血較為兇險且處理棘手,患者危重風險高,需要影像學、血管介入、重癥監護等學科緊密協作,以達到精確診斷、及時治療,有效控制出血,減少術中與術后并發癥的目標。
目前,關于巨大PNF破裂出血的文獻多為個案報道,對于其急診處理及圍術期管理的文獻非常罕見,仍缺乏高質量臨床研究及更高級別循證醫學證據。可通過公眾科普教育和提高NF1患者對自身疾病的認識,促進患者獲得早期診斷、治療及醫生和患者共同進行疾病全生命周期管理,以提高患者生存質量并降低合并PNF的患者腫瘤急性破裂出血風險。未來研究需關注PNF手術治療后患者長期生存質量的評估及進一步優化治療方案。
利益沖突 在課題研究和文章撰寫過程中不存在利益沖突
作者貢獻聲明 朱寶晨:文獻檢索及文稿撰寫;肖楊、趙焓杏、廖睿恒:內容構思和設計、觀點形成、文章內容修改整理;許學文、張艷閣:指導論文寫作,審閱文章知識性內容
叢狀神經纖維瘤(plexiform neurofibroma,PNF)是一種幾乎只出現在Ⅰ型神經纖維瘤病(neurofibromatosis type 1,NF1)的良性腫瘤,在NF1患者中發生率為27%~44%[1],其沿著全身各處神經叢生長,與周圍組織邊界不清,具有局部侵襲性。先天性PNF的瘤體隨年齡增加而逐漸增大,部分可發展成瘤體面積>100 cm2的巨大神經纖維瘤,導致患者功能障礙甚至毀容。此外,NF1患者PNF有8%~13%概率會惡變為惡性周圍神經鞘瘤[2]。因顯著的腫瘤血管形成和豐富的畸形血管,PNF的急性瘤體內出血更是NF1患者繼腫瘤惡變外較為常見的死因[3]。對于PNF的擇期手術治療策略,國內外學者提出了相關意見[4-6]。但部分PNF患者因為經濟或未接受過此疾病科普教育等原因,并未獲得合適的早期治療,最后以巨大PNF破裂出血急診入院。巨大PNF破裂出血較為兇險且復發概率高,目前國內外尚無較為系統的急診處理及圍術期管理策略。本文將復習相關文獻并結合我科處理巨大PNF破裂出血的臨床實踐,綜述急診超選擇動脈栓塞聯合手術切除治療巨大PNF破裂出血方法及療效,并討論圍術期管理策略,以期為臨床治療提供參考。
1 巨大PNF破裂出血的可能機制
巨大PNF破裂出血的機制可能有:① 神經纖維瘤組織侵入血管壁,導致自發性出血[7];② 創傷導致脆弱血管壁破裂[8];③ 瘤體內存在大量血管畸形,包括動脈瘤、動脈狹窄及動靜脈畸形等[3]。組織學研究表明,腫瘤內大量新生血管的血管壁僅由內皮和幾條結締組織纖維組成,沒有肌層,由于中膜變薄和彈性膜破裂,血管壁變得脆弱,因此在輕微創傷下就可能導致瘤內出血[9-11]。
2 巨大PNF破裂出血的診斷
巨大PNF瘤體內出血的臨床表現為:① 腫瘤體積快速變大,伴有壓迫癥狀。無論是自發性出血或是創傷后血腫形成,瘤體會在短時間出現明顯體積增大,往往伴有疼痛及神經壓迫表現。② 瘤體表面緊張或出現波動感,繼而破潰出血。病程較長的瘤體內出血由于對皮膚持續性壓迫,導致腫瘤中心區域皮膚出現壞死及破潰,進而可能持續性排出陳舊性血液。③ 血流動力學不穩定。巨大PNF破裂出血后由于瘤體內大量血液蓄積,患者轉診至醫院時多存在血流動力學不穩定,但較少出現短期內危及生命的情形,不過仍然有部分巨大瘤體患者出血后數小時即發展為低血容量休克甚至死亡[9,12]。當NF1患者發生不明原因休克時,往往需要考慮腫瘤內出血的可能。
除了以上初診時快速判斷的方法,巨大PNF破裂出血多依賴于影像學診斷。三維CT和MRI均能揭示腫瘤的內部特征及其對周圍組織的侵襲,活動性出血和血腫形成也可較為容易地通過影像學判斷[13]。瘤體在CT中邊界不清,形成的血腫在平掃CT中表現為高密度和等密度,對比增強CT圖像無增強表現。MRI T1加權像上,瘤體內血腫顯示出異質的中到高信號強度;在T2加權像上,瘤體內血腫則顯示出輕微的低到中等信號強度,圍繞血腫的區域有時還會出現一低信號環。有研究表明[14],MRI上的“流空征”可能是手術切除軀干巨大PNF時發生圍術期出血事件的唯一預測因素。而術前經導管血管栓塞術(transcatheter aortic embolization,TAE)可以降低有流空征的巨大PNF圍術期出血事件風險。但如高度懷疑巨大PNF破裂出血,CT血管造影(CT angiography,CTA)可能是早期判斷出血責任血管更好的選擇。
3 巨大PNF破裂出血的治療
巨大PNF破裂出血患者的一般情況較差,且手術出血量大,其臨床治療往往面臨許多挑戰。常見治療方法有單純清除血腫、TAE、減瘤或根治性切除手術。在20世紀中葉,因外科手術技術的限制,針對巨大PNF破裂出血多采取單純清除血腫同時結扎出血血管來控制活動性出血及腫瘤的占位效應。但由于病因未解除,這種方式復發出血概率較高,患者出院后多因輕微創傷或自發性出血而再次入院[9,15],甚至手術操作本身就可能引發更嚴重出血[16]。隨著血管介入技術的發展,術前TAE被用于控制巨大PNF手術中出血,超選擇動脈栓塞聯合外科序貫治療也成為巨大神經纖維瘤的重要治療策略[4]。許多入院時血流動力學不穩定的巨大PNF出血患者也受益于數字減影血管造影(digital subtraction angiography,DSA)聯合TAE的止血策略,極大地提高了此類患者的生存率[12]。如單獨應用TAE而不結合手術減瘤,栓塞血管可能再通或者建立側支循環,往往后期會再發出血[17]。考慮到以上情況,目前較為主流的手術治療策略多聯合術前病灶栓塞、術中清除血腫并完成減瘤或根治性切除的綜合方案。
3.1 巨大PNF破裂出血的急診處理
NF1患者因快速增大的PNF于急診就診時,應積極完成以下評估及處置:① 完善血常規、凝血常規、生化常規等血液學檢查及生命體征評估,判斷是否存在活動性出血及血流動力學不穩定的情況。如存在則積極啟動液體復蘇抗休克、輸血、應用止血藥物等治療措施,同時早期聯系血管外科評估DSA聯合TAE的急診止血策略。② 評估腫瘤是否有持續進展壓迫氣道或氣道內出血的風險,若有則應完成氣道保護[18]。③ 評估腫瘤表面是否發生破潰出血,對于破潰處應行加壓包扎,并積極抗感染治療,避免繼發傷口感染甚至敗血癥。④ 如出血部位不明確,可完善CTA檢查。⑤ 在患者生命體征較穩定情況下,給予對癥支持治療,積極完善MRI及相應術前準備,評估手術安全性及安排擇期手術。
3.2 TAE治療
對于血流動力學不穩定、診斷明確的巨大PNF破裂出血患者可首選TAE治療。我們主張在DSA引導下進行超選擇TAE,對瘤體滋養動脈進行栓塞以實現急診止血。但需注意的是,過度或者范圍過大的動脈栓塞止血可能會造成皮瓣壞死,導致血腫破潰,進而繼發感染或增加再次出血風險;并且皮瓣壞死后,瘤體切除后殘留的創面無法用瘤體皮反剔回植修復,需另取皮或轉移皮瓣修復創面,會進一步加重患者創傷。
3.3 手術治療
3.3.1 手術時機
聯合血管外科完成超選擇介入栓塞瘤體滋養動脈后,手術切除破裂出血瘤體的時機尚無統一意見。在臨床實踐中我們發現栓塞術后48 h,血腫周圍自然形成了水腫帶,此水腫帶界限清楚,瘤體內畸形血管顯露明確,沿著水腫帶切除有助于控制術中出血。部分文獻報道了栓塞后即刻或短期內進行手術的患者,可能因血管尚未完全血栓化,此時栓塞效果仍不確切[19]。急診行介入栓塞的主要目的是控制活動性出血,合適的觀察期可明確患者出血是否已得到有效控制。有文獻報道栓塞后患者短期再次出血,提示對栓塞術后患者仍需要繼續嚴密觀察[20]。同時,還需考慮到過長的觀察期會帶來一些潛在風險,一是栓塞后血管可能再通或建立側支循環,二是壞死組織的溶解吸收可能引發一系列并發癥。綜合以上因素,我們建議在栓塞術后至少48 h,但不超過1周的時間內進行瘤體血腫切除。這個時間窗口既可以確保栓塞效果穩定,又能避免因延遲手術帶來的并發癥。我們發現,遵循這一策略可以有效控制術中出血,顯著降低圍術期并發癥發生率,從而提高手術安全性和成功率。
3.3.2 術前準備
巨大PNF的特點是血供豐富、血管脆弱,加之患者常因自發性出血處于貧血狀態,使得術中大出血危及生命的風險顯著增高[21]。鑒于此,全面的術前準備至關重要。充足的血液儲備是手術成功的基礎,需積極備血并進行術前支持治療,包括補充血容量、維持白蛋白水平等。為應對可能的術中大出血,還應備妥凝血因子和人纖維蛋白原。考慮到手術復雜性,應組織多學科團隊共同評估患者手術風險并制定詳細方案,包括完善心肺功能、氣道評估以及圍術期麻醉相關風險評估,同時準備術后重癥監護病房,以確保全面的圍術期管理。這些綜合措施的實施將有效降低手術風險,提高手術成功率。
3.3.3 術中減少出血及監護策略
為了減少PNF術中出血,Lin等[22]提出了3個策略,即麻醉中控制性低血壓,提前對病灶周圍進行初步縫合,結扎血腫內有限數量的供血血管。但有部分學者[23-24]質疑結扎的有效性,指出其無法避免術中大量出血。
對于已經完成了術前瘤體供血動脈介入栓塞的患者,為了減少圍術期并發癥,我們對以上觀點進行了修訂和補充:① 無需術中控制性低血壓。部分術者建議在術中通過控制性低血壓結扎血管以減少出血[25],但對于大多數巨大PNF創面,往往需要植皮覆蓋,而術前栓塞過程已完成了充分止血,術中低血壓可能會導致術后反射性血壓升高,進而引起創面滲血,降低植皮成活率。并且維持正常的術中血壓也有助于保證心、腦、腎等器官充分灌注。② 備好自體血回輸。自體血可避免大量同種異體血輸入導致肺水腫、凝血障礙、發熱等并發癥。但如腫瘤存在破潰感染,則不推薦使用自體血回輸,有可能導致繼發全身感染。③ 手術采用血腫周圍水腫帶入路,沿水腫帶小心剝除瘤體,充分結扎血管,雙極電凝止血。④ 對于無法拉攏閉合的創面,可利用瘤體皮回植覆蓋。⑤ 術中密切監測患者液體出入量、凝血功能、水電解質及動脈血氣。
3.3.4 巨大PNF破裂出血術后管理
在巨大PNF切除術后應持續監測各項血液學指標及生命體征,對癥支持治療,并留意切口情況,定期換藥,根據情況調整抗生素。對于無法一期閉合的大面積創面,Cavallaro等[26]報道了1例巨大PNF患者在栓塞術后出現了廣泛瘤體壞死,隨后行部分瘤體切除術,由于創面過大無法直接縫合,術者采用封閉式負壓引流輔助治療,數月后最終成功完成了二期創面閉合。該病例報道為處理復雜的巨大PNF術后創面提供了新的思路。既往有多篇文獻也報道了在巨大PNF術后或潰瘍創面上使用封閉式負壓引流技術輔助治療,顯示在相對較低的負壓(9.975 kPa)下,治療具有一定安全性和有效性[27-31]。但考慮到巨大PNF有大量脆弱的血管以及極易出血的特性,術后使用負壓創面治療仍需非常謹慎,關于此技術應用于巨大PNF患者的風險與獲益,仍需進一步研究。
4 本中心3例巨大PNF破裂出血典型病例
本中心應用DSA+栓塞技術聯合手術,有效治療了3例巨大PNF破裂出血患者。
例1 患者,男,43歲。因“腰背部PNF突然增大伴疼痛”急診入院。查體:腰背部腫物大小為38 cm×30 cm×10 cm,伴有11 cm×8 cm×7 cm皮膚壞死。血常規檢查示血紅蛋白76 g/L;MRI檢查示病灶內有大小為21.7 cm×17.3 cm×7.1 cm的血腫。急診行DSA+TAE控制出血,DSA示腹主動脈分支和髂內動脈分支供血;予以輸血等對癥支持治療,積極術前準備,栓塞術后48 h在全身麻醉下切除腫瘤及血腫。術中出血約400 mL。術后病理檢查證實為PNF伴血腫形成。術后20 d出院,隨訪12個月未見復發[32]。
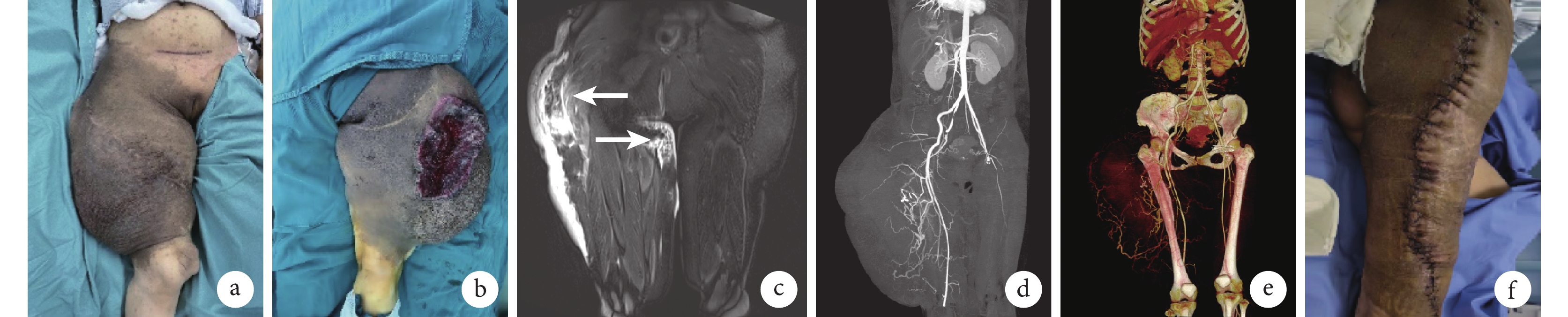
例2 患者,女,25歲。因“右大腿部PNF急劇增大伴疼痛”急診入院。查體:右大腿有一大小為26 cm×18 cm×8 cm的巨大腫物,腫物后側伴有15 cm×10 cm大小的潰瘍。血常規示血紅蛋白62 g/L;MRI T2加權像示軟組織腫塊位于右側腰骶區、臀部和大腿,腫塊內可見增粗、增多的血管;CTA示右大腿有大量血腫和活動出血,軟組織腫塊起源于右側腰骶區的皮下組織,腫塊中的血管增粗、迂曲,與股深動脈和股淺動脈的1個分支密切相關。急診行DSA+TAE控制出血,DSA示股深動脈的3條穿支動脈和股淺動脈的1個分支動脈供血;予以輸血等對癥支持治療,積極術前準備,于栓塞術后第3天在全身麻醉下切除腫瘤及血腫。見圖1。術后病理檢查證實為PNF伴血腫形成。術后15 d出院,12個月隨訪未見復發。
 圖1
病例2
圖1
病例2
a. 術前右大腿外觀;b. 術前右大腿后側潰瘍;c. 術前MRI T2加權像(箭頭示腫塊內增粗、增多的血管);d、e. 術前CTA;f. 右大腿PNF血腫及部分瘤體切除術后即刻
Figure1. Case 2a. Preoperative appearance of the right thigh; b. Preoperative ulceration on the posterior aspect of the right thigh; c. Preoperative MRI T2-weighted image (arrow indicated thickened and increased vasculature within the tumor); d, e. Preoperative CTA; f. Immediate postoperative view following hematoma evacuation and partial tumor resection of the right thigh PNF
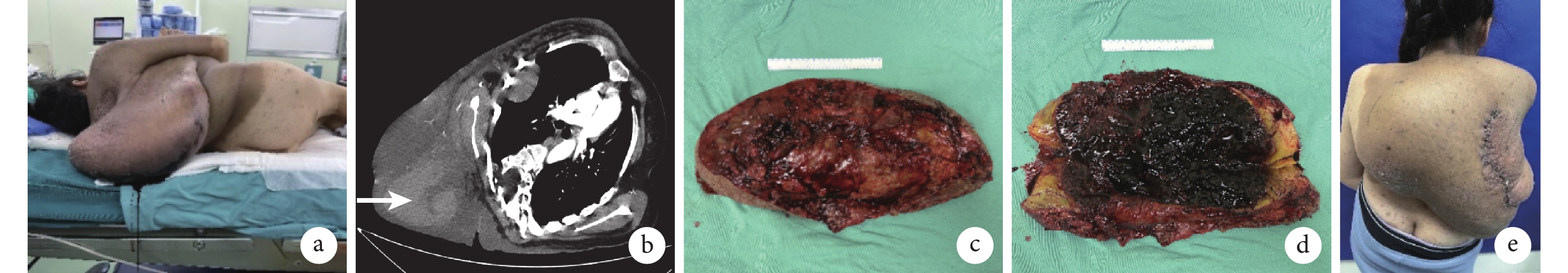
例3 患者,女,27歲。因“背部PNF急劇增大”急診入院。查體:右側背部腫物大小為55 cm×36 cm×14 cm,伴有表面15 cm×4 cm的皮膚壞死。血常規示血紅蛋白60 g/L;CTA示右側背部及胸腹壁軟組織明顯增厚,右側背部皮下見巨大混雜密度腫塊影,邊界不清,大小難以測量,內見片團狀高密度影,增強不均勻強化,可見胸外動脈走行。急診行DSA+TAE控制出血,DSA示右肩胛下動脈分支為瘤體供血。患者合并重度脊柱側彎,予以輸血等對癥支持治療,積極術前準備,經多學科會診后于栓塞術后第6天在全身麻醉下切除腫瘤,在切除瘤體內可見約44 cm×27 cm的血腫形成。術后16 d出院,10個月隨訪未見復發。見圖2。
 圖2
病例3
圖2
病例3
a. 術前背部外觀;b. 術前CT示腫塊內血腫形成(箭頭);c、d. 術中切除的病灶,可見瘤體內血腫形成(約44 cm×27 cm);e. 術后3周背部外觀
Figure2. Case 3a. Preoperative appearance of the back; b. Preoperative CT showed hematoma formation within the tumor (arrow); c, d. Intraoperative view of the excised lesion demonstrating hematoma formation within the tumor (44 cm×27 cm); e. Appearance of the back at 3 weeks after operation
5 總結及展望
本文通過回顧臨床文獻并結合我科在處理NF1相關巨大PNF破裂出血中的實踐經驗,提出了一系列急診處理方案及圍術期管理策略。巨大PNF急性出血較為兇險且處理棘手,患者危重風險高,需要影像學、血管介入、重癥監護等學科緊密協作,以達到精確診斷、及時治療,有效控制出血,減少術中與術后并發癥的目標。
目前,關于巨大PNF破裂出血的文獻多為個案報道,對于其急診處理及圍術期管理的文獻非常罕見,仍缺乏高質量臨床研究及更高級別循證醫學證據。可通過公眾科普教育和提高NF1患者對自身疾病的認識,促進患者獲得早期診斷、治療及醫生和患者共同進行疾病全生命周期管理,以提高患者生存質量并降低合并PNF的患者腫瘤急性破裂出血風險。未來研究需關注PNF手術治療后患者長期生存質量的評估及進一步優化治療方案。
利益沖突 在課題研究和文章撰寫過程中不存在利益沖突
作者貢獻聲明 朱寶晨:文獻檢索及文稿撰寫;肖楊、趙焓杏、廖睿恒:內容構思和設計、觀點形成、文章內容修改整理;許學文、張艷閣:指導論文寫作,審閱文章知識性內容