2023年9月于新加坡落下帷幕的世界肺癌大會公布了第九版胸腺腫瘤TNM分期。新版分期基于更龐大、全面的數據庫,對胸腺腫瘤的TNM分期進行了修改和驗證,目的是使第九版TNM分期在更具統計學力度的同時,也擁有更強的臨床可操作性。而第九版分期的推出,也必將會對胸腺腫瘤將來的臨床、科研工作帶來改變。
引用本文: 于豐浩, 谷志濤, 茅騰, 許寧, 章雪飛, 郝秀秀, 方文濤. UICC/IASLC/AJCC 胸腺腫瘤第九版 TNM 分期解讀:改變與傳承. 中國胸心血管外科臨床雜志, 2024, 31(2): 196-202. doi: 10.7507/1007-4848.202311063 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
惡性腫瘤的TNM分期基于原發灶(T)、淋巴結轉移(N)、遠處轉移(M)的解剖基礎對腫瘤進行分期劃分,是實體腫瘤應用最廣泛的分期方式,也是全球眾多醫務工作者的共同語言和腫瘤學臨床診療、研究的根基。在2023年9月召開的世界肺癌大會上,國際肺癌協會(International Association for the Study of Lung Cancer,IASLC) 分期委員會公布了最新的國際抗癌聯盟/美國癌癥聯合會(Union for International Cancer Control/American Joint Committee on Cancer,UICC/AJCC)TNM胸腺腫瘤分期,距第八版TNM分期的正式使用間隔將近7年。本文將集中對新版分期的數據依據以及新舊分期之間的變化和傳承進行說明,并就其對臨床工作的指導意義和對未來分期工作提供的經驗進行分析。
1 胸腺腫瘤分期背景
胸腺上皮腫瘤作為一種罕見、相對惰性的實體腫瘤,針對其開展的臨床研究一直面臨病例數少、終點事件數少、隨訪時間長等問題,因此既往的分期系統也存在構建數據量小、以經驗性為主的缺陷。從上個世紀60年代開始,曾先后出現過10多種胸腺腫瘤的分期系統,其中應用最廣泛的Masaoka-Koga分期也只是基于單中心不到100例患者的5年隨訪結果[1],雖然此分期在臨床上得到較好驗證,但由于其固有的缺陷,不能很好地反映臨床的具體情況和對不同患者進行精密區分。
鑒于胸腺腫瘤長期缺乏TNM分期這一問題,IASLC和國際胸腺腫瘤協會(International Thymic Malignancy Interest Group,ITMIG)兩大全球性組織,在UICC和AJCC的同意和支持下,于2010年成立了胸腺腫瘤分期和預后委員會 (Staging and Prognostic Factors Committee-Thymic Domain, SPFC-TD),擬利用全球多中心、多組織提供的數據,打造屬于胸腺腫瘤的TNM分期。第八版胸腺腫瘤TNM分期于2014年面世,該分期建立在來自全球105家中心、共8 145例患者的臨床、生存數據的基礎上,其中1 031例來自當時的中國胸腺腫瘤研究協作組(Chinese Alliance for Research in Thymomas,ChART)。第八版分期首次為胸腺瘤、胸腺癌、胸腺神經內分泌腫瘤建立了具有較強數據基礎、國際統一的共同語言[2]。
第八版分期的建立對于胸腺腫瘤具有劃時代的意義,很快得到全球醫學界的支持和使用,其較高的臨床可行性也快速得到了外部驗證[3]。但在廣泛的接受和支持中也存在質疑:第八版分期正式使用1年后,SPFC-TD針對分期的使用情況向全球217家中心發放調查問卷;調研結果顯示,雖然78%的中心支持TNM分期的使用,但是臨床醫生認為第八版分期中的部分分類缺乏依據、需要改進[4]。由于第八版分期使用的數據庫存在某些項目數據有限、早期晚期病例數據失衡等缺點,部分分類的劃分只能基于實用性、解剖位置、邏輯推理給出專家共識,而并非完全基于統計學的差異。這是第八版分期留下的最大遺憾,也自然成為第九版分期工作的一個重要出發點:以第八版分期作為修訂的參考,在新數據庫和既有證據的支持下,使第九版TNM分期更具有統計學力度,并兼顧臨床意義。因此,分期委員會在制定第九版分期時,提出遵守解剖學基礎、不使分期過度復雜化、在臨床和病理學上都能進行評估以及在所有國家都具備可行性幾項基本原則;并且提出在新分期的修訂過程中要前瞻性地挖掘未來分期驗證、修訂所需的數據[5]。
2 第九版分期的數據來源
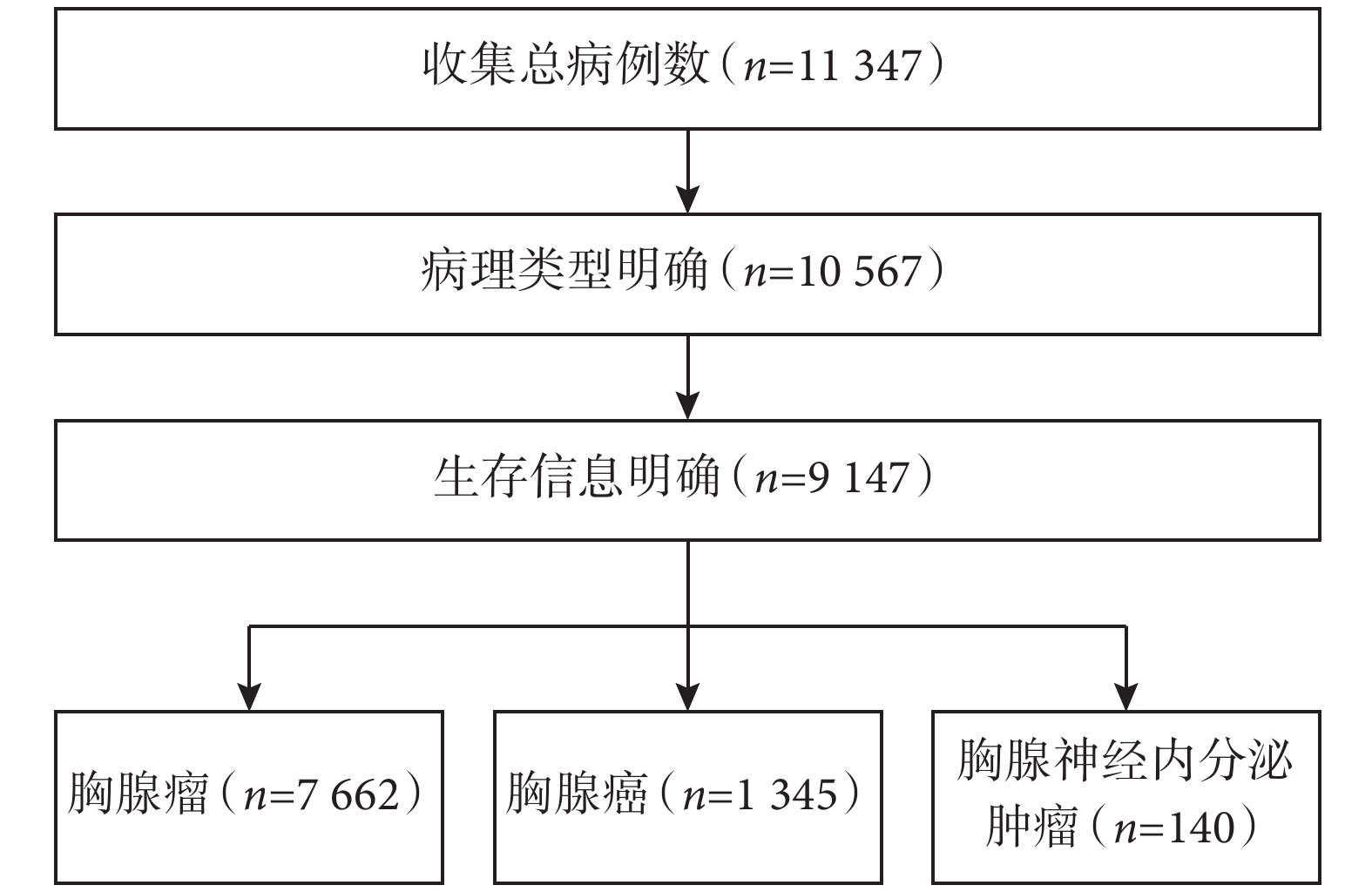
第九版分期的數據來自全球13家組織和機構,共收集了11 347例患者數據,時間跨度超過50年(1965—2021年),確保隨訪時間充足。在去除隨訪信息缺失和病理類型不明確的病例后,共有9 147例患者納入最終分析,相比于第八版分期的8 145例病例有進一步擴充。9 147例患者中胸腺瘤患者7 662例,占總體的83.8%(圖1)。數據的主要來源地為亞洲地區,其中中國抗癌協會縱隔腫瘤專業委員會的全國多中心回顧性和前瞻性數據庫分別提供了1 172例和343例患者[6]。相比于第八版,此次使用的數據庫不僅總數據量有所提升、病例時間跨度延長,而且淋巴結轉移和遠處轉移的晚期患者數量也有顯著增加,但仍存在以亞洲病例為主導(占62%)、以手術治療病例為主(占97%)的特征。
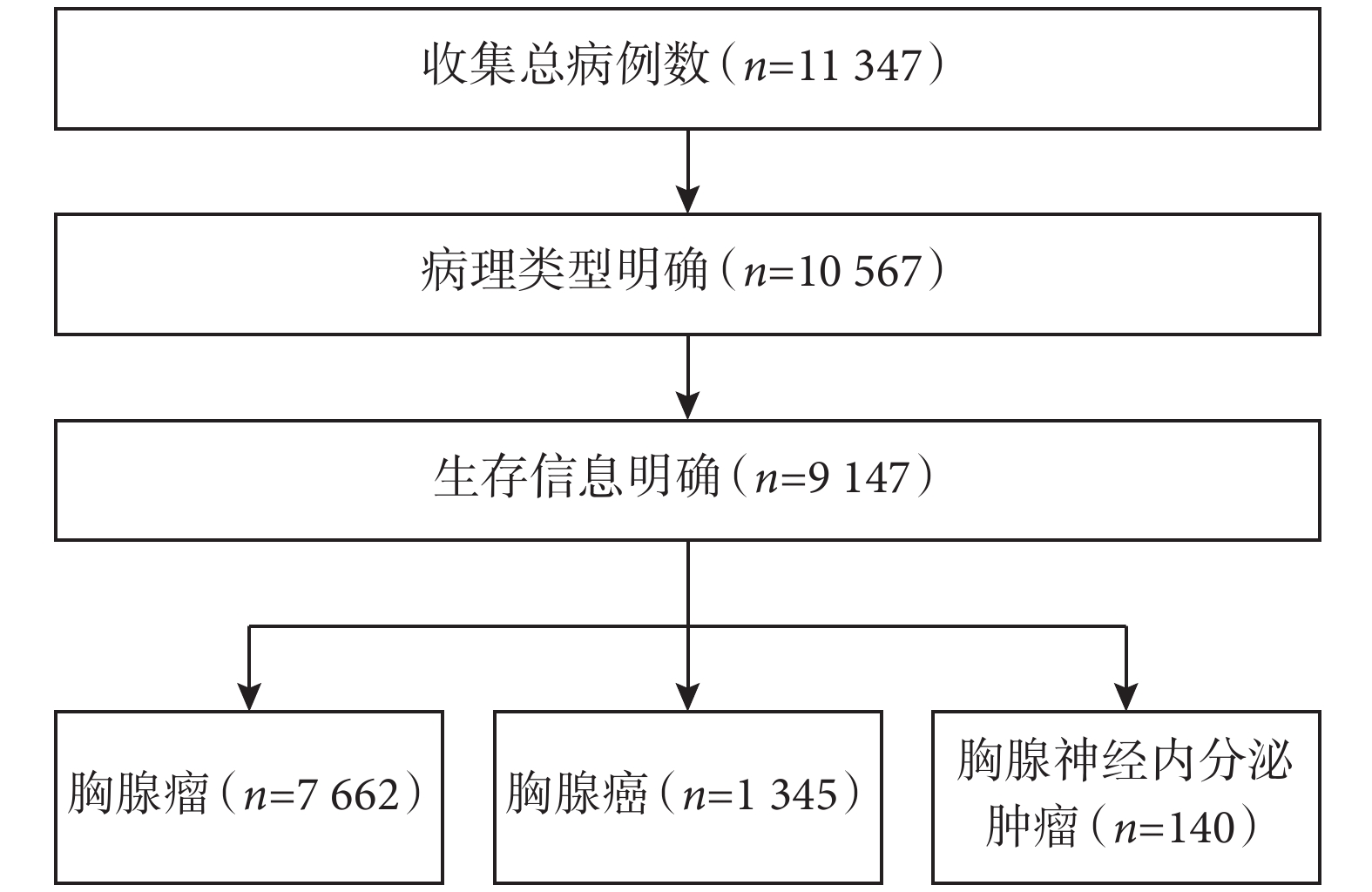 圖1
第九版UICC/IASLC/AJCC胸腺腫瘤TNM分期最終納入分析的患者例數
圖1
第九版UICC/IASLC/AJCC胸腺腫瘤TNM分期最終納入分析的患者例數
3 第九版分期的變與不變
如前所述,新分期并非單純追求改變,還需要對既往的分期進行驗證。一個良好的分期不僅要做到期別之間存在明顯區分有統計學差異、期別內部有較好的一致性,還要做到與前一版分期有較好的延續性,并且實現臨床價值和臨床可操作性間的均衡。同時,TNM分期需要維持其普適性原則,不僅應適用于不同國家、地區、醫院,而且也應適用于所有的病理類型。正如肺癌分期不會區分鱗癌與腺癌,胸腺腫瘤分期也不會區分瘤與癌,只要同一個分期在所有瘤種里達到相似的預后區分即可。
基于這些要求,第九版分期利用更為全面的臨床數據和復發、生存結果,對既往的TNM分期進行了重新劃分和組合,進一步貫徹不同期別間差異明顯、同一期別內部高度一致的原則;而對于既往更多是出于經驗進行的分類劃分則利用前所未有的大病例組數據給予驗證和肯定。同時,由于胸腺腫瘤相對比較惰性,早期胸腺腫瘤手術完整切除后有不易復發、復發時間較晚、復發后仍然可以獲得長期生存、死亡病例以非腫瘤相關原因為主的特點。例如 ChART 數據庫中手術完整切除的 Ⅰ ~ Ⅲ a 期 胸 腺 腫 瘤 患 者 , 1 0 年 總生 存 (overall survival,OS)高達 89.5%;基于這部分患者的復發信息建立的復發預測模型將T1期的所有胸腺瘤以及T2期、T3期的A、AB、B1型胸腺瘤劃分為轉移風險低危組,而T2期、T3期的B2、B3型胸腺瘤以及所有的胸腺癌和神經內分泌腫瘤劃分為轉移風險高危組,前者的復發率為2.7%,而后者則高達20.1%[7]。因此出于對胸腺腫瘤特殊生物學行為的考慮,對于早期胸腺腫瘤使用腫瘤無復發率(freedom from recurrence,FFR)作為劃分的終點,相比于生存更加能反映早期胸腺腫瘤臨床上的治療結果;而對于晚期胸腺腫瘤則參照其他惡性實體腫瘤使用OS作為劃分的終點。充足的數據和合理的劃分終點保證了新分期擁有堅實的統計學基礎。
3.1 以腫瘤大小決定T1a期和T1b期
第八版分期以是否侵犯縱隔胸膜把局限在前縱隔胸腺及其周圍脂肪的早期腫瘤劃分為T1a期和T1b期。而第九版分期則第一次將腫瘤大小納入T分期中,在T1分期中做出了以下更改:以5 cm為界限,局限在胸腺以及周圍脂肪的胸腺腫瘤,腫瘤直徑≤5 cm為T1a期,>5 cm為T1b期(表1)[5]。
將腫瘤大小納入分期是建立在新的數據庫中腫瘤大小的數據較第八版數據庫更加齊全的基礎上,通過在訓練數據集中選取可以區分預后的腫瘤大小臨界值,在驗證數據集中進行驗證。最終所選取、驗證的臨界值為4.5~9.0 cm,而所取5 cm是在借鑒既往研究[8]結果后的人為設定。對比>5 cm和≤5 cm的T1期腫瘤的OS和FFR可發現,在胸腺瘤中,前者OS和FFR都顯著低于后者(P均<0.05);而在胸腺癌中,前者和后者的OS和FFR有數值差別,但差異無統計學意義。由于T2期、T3期、T4期患者數量較少,無法在這些分期中進行驗證,同時考慮到腫瘤外侵程度對預后的影響遠大于腫瘤本身的大小,在第九版分期中腫瘤大小的區分僅用于T1期早期腫瘤中[9]。
胸膜侵犯雖然在新的數據庫中也有區分T1期腫瘤預后的作用,但在新分期中僅作為額外的病理學表述(additional histologic descriptor),而不作為T1a期和T1b期的區分標準。其中最主要的原因是分期委員會T分期小組認為胸膜侵犯無論是術前臨床影像還是術后病理評估均有一定難度,因此利用一個在臨床上難以判斷的因素作為標準可行性較差。但胸膜侵犯也不應因新分期的改變而被忽視,在癌癥報告國際合作組織(International Collaboration of Cancer Reporting,ICCR)最新提出的胸腺腫瘤手術切除標本的匯報標準中,腫瘤直接侵犯(包括胸膜侵犯)是匯報的10項“核心因素”之一[10]。這提醒臨床工作者,尤其是外科醫生和病理科醫生,在對標本處理和檢查上應有更好的溝通和交流,外科醫生應注重手術切除標本上縱隔胸膜的標注,以便病理科醫生在鏡下對腫瘤是否浸潤穿透胸膜彈力層進行判斷;同時,臨床醫生也應探索如何通過影像組學手段提高術前對胸膜侵犯判斷的準確性。
3.2 對T2期和T3期的修改
第八版中的T2期為心包侵犯,T3期為肺、膈神經、胸壁、頭臂靜脈、上腔靜脈以及心包外的肺動靜脈受侵。第九版分期則將肺與膈神經從T3期中移除,降至T2期(表1)[5]。
既往臨床實踐中,肺實質的局部侵犯以及膈神經的侵犯相比其他T3期結構的侵犯在臨床處理方面有較大不同,這一點在外科手術上體現得最為明顯:心包、局部肺、膈神經的侵犯更易完整切除,即使在微創手術下也有較大可行性;而靜脈系統和心包外肺血管的侵犯則可能會導致更多的非R0切除或開放手術。此前谷志濤等[11]針對這一點在進展期胸腺腫瘤微創對比開放的研究中,創新性地使用了切除指數(resection index,RI)對原T3期結構進行了較好的手術難度劃分,其RI所采用的計算方式與新分期T2期、T3期的重新劃分不謀而合。
既往Masaoka-Koga分期中局部進展期腫瘤均列入Ⅲ期,非常混雜;UICC/IASLC/ITMIG第八版分期利用T分期概念將常規手術無法切除的腫瘤劃分為T4期,首次將原發腫瘤按照手術切除可能性進行了區分[1];而第九版分期則進一步將肺與膈神經等易于手術完整切除的結構與胸壁、大血管等切除難度較高的結構進行了細分。通過利用新數據對原本T2期/T3期患者的預后進行分析發現,在胸腺瘤中,肺和膈神經的侵犯相比于其他T3期結構的侵犯,雖然OS差異無統計學意義,但有更好的FFR:在R0切除且N0M0期的前提下,前者的5年FFR為82%,后者為70%;在胸腺癌中,相比于其他T3N0M0期,侵犯肺/膈神經的T3N0M0期患者與僅侵犯心包的T2N0M0期在R0切除后有更加接近的FFR:侵犯心包、侵犯肺/膈神經和侵犯其他原T3期結構患者的5年FFR分別為50%、61%和41%[9]。T2期、T3期的修改無疑做到了不同分期間差異明顯、同一分期內部高度統一,但在細節方面仍存在著美中不足,比如局部肺實質侵犯和廣泛肺實質侵犯的區分,新T3期內部的繼續劃分,單側、雙側膈神經侵犯的區分,這些問題都因第九版數據庫中病例數據缺乏相應的細節項而無法做出更進一步的劃分。
膈神經和肺實質侵犯的分類下降,必將成為臨床治療改變的催化劑。首先在手術方面,此舉將進一步推動外科醫生對進展期胸腺腫瘤微創手術的探索和嘗試。在中國抗癌協會胸腺腫瘤診療指南中,UICCⅠ期胸腺腫瘤推薦微創手術,在微創技術較為成熟的大的臨床中心,對UICC Ⅱ~Ⅲa期(第八版)可嘗試進行微創胸腺手術[12]。此推薦來自于部分胸外科中心對于進展期胸腺腫瘤微創手術的成功嘗試,希望未來可以有多中心、隨機對照的研究結果支持微創手術在進展期胸腺腫瘤中的使用。其次,T2期、T3期的修改可能會推動胸腺腫瘤術后輔助治療的變化。對于局部進展期胸腺腫瘤完整切除后的輔助治療,各個指南、組織、中心都有不同的推薦, NCCN指南中,Masaoka-KogaⅢ期的胸腺瘤R0切除后建議術后放療[13];ITMIG的回顧性研究[14]結果則提示Masaoka-KogaⅡ~Ⅲ期 R0切除的胸腺瘤患者,術后放療組10年OS明顯高于未放療組(86% vs. 79%,P=0.002);而日本胸腺腫瘤研究協作組的研究[15]則發現術后輔助放療僅對Ⅲ期胸腺癌患者有益。中國抗癌協會胸腺腫瘤診療指南則推薦R0切除后,UICCⅠ期的胸腺瘤和Ⅱ~ⅢA期(第八版)的A、AB、B1型胸腺瘤,不進行術后輔助治療,UICC Ⅱ~ⅢA(第八版)的B2、B3型胸腺瘤,可考慮術后輔助放療或隨訪[12]。鑒于目前為止所有的回顧性研究都是基于以往的分期系統,希望新分期的推出有助于基于T分期的細分行進一步的研究,為未來胸腺腫瘤輔助治療策略提供高級別的新證據。
3.3 對N分期、M分期的繼承
第九版分期將繼續沿用第八版分期中關于淋巴結和遠處轉移的分期(表2)。鑒于第八版分期數據存在著晚期病例較少、分類依賴專家共識的問題,第九版分期在胸腺腫瘤淋巴結和遠處轉移所做的工作是利用總體病例數更龐大、陽性病例更豐富的新數據庫,對第八版分類進行驗證[16-17]。
由于第八版數據庫淋巴結轉移陽性的病例有限,將胸腺腫瘤淋巴結轉移分為位于前縱隔的N1期和居于縱隔深處和頸部的N2期并非完全出自統計分析,而是基于以下幾點:第一是解剖位置上遠近的猜測,N1期為前縱隔胸腺內的淋巴結,N2期為深縱隔和更遠的淋巴結;第二為手術摘除的困難程度不同,N1期淋巴結通過全胸腺切除可以一并去除,而N2期淋巴結的摘除則需要額外的操作;第三則為是否有足夠可用的數據將不同N分期的預后進行區分[18]。第九版數據庫中淋巴結信息的完整度明顯提高,病理學淋巴結信息存在的病例數占74.6%(6 820/9 147),但治療前臨床淋巴結信息存在的病例僅占25.3%(2 317/9 147),一定程度上反映了胸腺腫瘤基于影像對淋巴結轉移情況判斷的困難。病理學N1(pN1)期陽性患者有168例、病理學N2期(pN2)陽性患者123例,相比于第八版的75例pN1和68例pN2有大幅度增加。由于胸腺腫瘤淋巴結轉移并非常見事件,因此在新的數據庫中病理淋巴結陰性(pN0)和臨床淋巴結陰性(cN0)有較高的一致性,兩者的占比分別為89.0%和97.7%;而病理淋巴結陽性(pN+)和臨床淋巴結陽性(cN+)之間的一致性則較低,一定程度上由于臨床醫生對于胸腺腫瘤術前淋巴結狀態的忽視以及缺乏較好的手段判斷術前淋巴結狀態。第九版數據庫顯示淋巴結轉移率在不同病理類型中有明顯差異:在胸腺瘤中占1.5%,在胸腺癌中占17.6%,在胸腺神經內分泌腫瘤中占27.7%。此與既往來自ChART多中心回顧性數據庫得到的結果一致;而此前ChART前瞻性多中心觀察性研究結果也表明,術中主動清掃淋巴結的胸腺腫瘤病例淋巴結轉移比例較回顧性數據庫中報道的結果顯著增高,相比于胸腺瘤,胸腺癌和胸腺神經內分泌腫瘤更容易發生淋巴結轉移[19-20]。
利用新的數據庫對既往N分期進行驗證:在胸腺癌中,pN1病例的OS明顯低于pN0(P=0.017),pN2病例的OS也明顯低于pN1(P=0.006);在胸腺瘤中,pN1病例的OS明顯低于pN0(P<0.001),pN2和pN1的OS相近(P=0.85)。這些結果肯定了第八版分期N0、N1、N2的分類,為N分期維持不變提供了充足的證據。SPFC-TD N分期小組就此提醒臨床工作者今后應進一步重視胸腺腫瘤治療前淋巴結狀態評估、手術中加強對高級別和進展期腫瘤的淋巴結清掃、術后進行細致的病理評估,提高分期準確性,指導預后判斷和治療選擇,并為未來第十版分期的修訂提供更為詳實的數據基礎。
對于胸腺腫瘤的遠處轉移,第八版分期借鑒了既往Masaoka-Koga分期對于不同轉移方式機制的猜想以及臨床處理方式的不同,將胸膜、心包播散分類為M1a,肺實質、遠處器官轉移分類為M1b,但兩者在生存曲線上僅存在肉眼的區分[18]。在新的數據庫中,cM1a病例數為101例,cM1b病例數為29例;pM1a的病例數為326例,pM1b的病例數為155例。臨床上判斷有轉移的胸腺瘤和胸腺癌的病例僅有69.1%和51.0%接受了手術治療,再加上M0病例所占比例較高,導致cM和pM之間的一致性不高:胸腺瘤和胸腺癌中分別有76%和53%的cM1a最后診斷為pM1a,14%和33%的cM1b最后診斷為pM1b。
由于cM數據較少,新分期僅利用pM數據對既往M分期進行驗證。在胸腺瘤中, pM1a的OS 和FFR均顯著低于pM0[HR=3.23,95%CI (2.38,4.55),P<0.001;HR=14.30,95%CI(9.09,43.00),P<0.001];在胸腺癌中,pM1a的FFR顯著低于pM0[HR=2.63,95%CI(1.33,5.26),P=0.004],但OS差異無統計學意義。在胸腺瘤和胸腺癌中,并未找到pM1a和pM1b間顯著的OS或FFR差異。另外,分期委員會對同一分期內部不同描述進行了進一步分析,結果發現,對于pM1a期胸腺瘤患者,胸膜播散、心包播散或兼具兩者的OS無明顯差異;對于pM1b期胸腺瘤患者,肺轉移和胸外轉移的OS也無明顯差異;但對于pM1a期胸腺癌患者,胸膜播散的OS有優于心包播散和兼具兩者的趨勢。由于有細節分類的數據量過少以及將M1a和M1b繼續細分的證據尚不充足,第九版分期將維持第八版分期提出的M分期。但與此同時,分期委員會也基于臨床實踐對未來的M分期進行了猜測和暢想。在治療上,單一胸腔、遠處轉移患者,相比多發胸腔、遠處轉移患者,更容易通過局部治療獲得較好的治療效果,得到較好的預后;而一側胸腔多發轉移和雙側胸腔、遠處多發轉移在治療效果上也有不同。因此,分期委員會將在未來探討是否有將M分期劃分為單一的種植或轉移、同側多發轉移、雙側和遠處多發轉移的可能性。
4 總結和展望
總之,胸腺腫瘤的第九版分期基于全新的數據,對第八版分期進行了驗證傳承和修訂更新,將T1a和T1b期的區分從縱隔胸膜的侵犯更改為腫瘤大小,將肺侵犯、膈神經侵犯降至了T2期;而N、M分類保持不變,整體的TNM分期組合維持不變(表3)。其中的變是根據更大量、更全面的數據進行更有意義的區分,這種意義不僅僅是統計學層面,更體現在臨床應用上;而不變則是通過新的數據對既往經驗層面上的劃定進行統計學驗證,有力地說明了其合理性。這些改變也提醒臨床醫生在診斷和治療方面需要不斷進行相應的思考、改變和提高,比如如何提高臨床分期判斷的準確性,如何采取有效的手段發現隱匿的淋巴結和遠處轉移,從而為患者提供合適的治療模式;如何以分期的改變作為出發點,對局部進展期患者的手術治療、輔助治療甚至新輔助治療優化選擇。同時,新分期的提出也促使醫生用臨床一線發現的問題、得到的數據對分期進行進一步的驗證和改進。
雖然第九版分期在上一版的基礎上做到了改革和繼承齊頭并進,但此次收集的數據仍存在諸多問題:1/4的病例缺少病理學分期信息,3/4的病例缺少臨床分期信息;雖然晚期病例和前瞻性的病例數增加,但接受手術切除病例和來自回顧性數據庫的病例仍占絕大部分,導致數據庫中的病例仍以相對早期的病例為主,且在數據質量方面難以把控;一些細節變量的高頻率缺失以及部分分組數據豐度較低,比如胸腺癌和神經內分泌腫瘤病例較少,轉移病例缺少轉移數量、位置等細節。這些問題導致臨床醫生面臨的一些困擾沒有得到全部解答,比如肺侵犯范圍是否應在分期中進行細分,N2中的各站淋巴結是否有相同的預后價值,轉移的數量和位置是否應該加入分期中,胸腔內播散和其他遠處臟器轉移是否應該有所區分等,這些問題可能需要更龐大、更精細的數據進行回答。同時,第九版數據庫中的病例仍存在較大的地區性差異,并且非手術病例較少,無法更好地覆蓋晚期胸腺腫瘤的預后。要克服這些缺陷,不僅需要更加緊密的全球范圍內多組織、多中心的合作,而且對各個組織、中心提供的數據質量也提出了更高的要求。在ICCR最新提出的胸腺腫瘤手術切除標本的病理報告標準中,有10項“核心元素”和8項“非核心因素”,被認為與胸腺腫瘤的臨床管理、分期、預后息息相關[10],能否以此作為基石和啟發,為胸腺腫瘤分期數據錄入提供統一、詳細的模板,組建更高質量的數據庫,或將成為克服第九版分期缺陷的重要武器。
利益沖突:無。
作者貢獻:于豐浩負責內容構思和文章撰寫;谷志濤、茅騰、許寧、章雪飛、郝秀秀負責文章修改意見的提出;方文濤負責文章思路構架的提出以及提供文章修改意見。
惡性腫瘤的TNM分期基于原發灶(T)、淋巴結轉移(N)、遠處轉移(M)的解剖基礎對腫瘤進行分期劃分,是實體腫瘤應用最廣泛的分期方式,也是全球眾多醫務工作者的共同語言和腫瘤學臨床診療、研究的根基。在2023年9月召開的世界肺癌大會上,國際肺癌協會(International Association for the Study of Lung Cancer,IASLC) 分期委員會公布了最新的國際抗癌聯盟/美國癌癥聯合會(Union for International Cancer Control/American Joint Committee on Cancer,UICC/AJCC)TNM胸腺腫瘤分期,距第八版TNM分期的正式使用間隔將近7年。本文將集中對新版分期的數據依據以及新舊分期之間的變化和傳承進行說明,并就其對臨床工作的指導意義和對未來分期工作提供的經驗進行分析。
1 胸腺腫瘤分期背景
胸腺上皮腫瘤作為一種罕見、相對惰性的實體腫瘤,針對其開展的臨床研究一直面臨病例數少、終點事件數少、隨訪時間長等問題,因此既往的分期系統也存在構建數據量小、以經驗性為主的缺陷。從上個世紀60年代開始,曾先后出現過10多種胸腺腫瘤的分期系統,其中應用最廣泛的Masaoka-Koga分期也只是基于單中心不到100例患者的5年隨訪結果[1],雖然此分期在臨床上得到較好驗證,但由于其固有的缺陷,不能很好地反映臨床的具體情況和對不同患者進行精密區分。
鑒于胸腺腫瘤長期缺乏TNM分期這一問題,IASLC和國際胸腺腫瘤協會(International Thymic Malignancy Interest Group,ITMIG)兩大全球性組織,在UICC和AJCC的同意和支持下,于2010年成立了胸腺腫瘤分期和預后委員會 (Staging and Prognostic Factors Committee-Thymic Domain, SPFC-TD),擬利用全球多中心、多組織提供的數據,打造屬于胸腺腫瘤的TNM分期。第八版胸腺腫瘤TNM分期于2014年面世,該分期建立在來自全球105家中心、共8 145例患者的臨床、生存數據的基礎上,其中1 031例來自當時的中國胸腺腫瘤研究協作組(Chinese Alliance for Research in Thymomas,ChART)。第八版分期首次為胸腺瘤、胸腺癌、胸腺神經內分泌腫瘤建立了具有較強數據基礎、國際統一的共同語言[2]。
第八版分期的建立對于胸腺腫瘤具有劃時代的意義,很快得到全球醫學界的支持和使用,其較高的臨床可行性也快速得到了外部驗證[3]。但在廣泛的接受和支持中也存在質疑:第八版分期正式使用1年后,SPFC-TD針對分期的使用情況向全球217家中心發放調查問卷;調研結果顯示,雖然78%的中心支持TNM分期的使用,但是臨床醫生認為第八版分期中的部分分類缺乏依據、需要改進[4]。由于第八版分期使用的數據庫存在某些項目數據有限、早期晚期病例數據失衡等缺點,部分分類的劃分只能基于實用性、解剖位置、邏輯推理給出專家共識,而并非完全基于統計學的差異。這是第八版分期留下的最大遺憾,也自然成為第九版分期工作的一個重要出發點:以第八版分期作為修訂的參考,在新數據庫和既有證據的支持下,使第九版TNM分期更具有統計學力度,并兼顧臨床意義。因此,分期委員會在制定第九版分期時,提出遵守解剖學基礎、不使分期過度復雜化、在臨床和病理學上都能進行評估以及在所有國家都具備可行性幾項基本原則;并且提出在新分期的修訂過程中要前瞻性地挖掘未來分期驗證、修訂所需的數據[5]。
2 第九版分期的數據來源
第九版分期的數據來自全球13家組織和機構,共收集了11 347例患者數據,時間跨度超過50年(1965—2021年),確保隨訪時間充足。在去除隨訪信息缺失和病理類型不明確的病例后,共有9 147例患者納入最終分析,相比于第八版分期的8 145例病例有進一步擴充。9 147例患者中胸腺瘤患者7 662例,占總體的83.8%(圖1)。數據的主要來源地為亞洲地區,其中中國抗癌協會縱隔腫瘤專業委員會的全國多中心回顧性和前瞻性數據庫分別提供了1 172例和343例患者[6]。相比于第八版,此次使用的數據庫不僅總數據量有所提升、病例時間跨度延長,而且淋巴結轉移和遠處轉移的晚期患者數量也有顯著增加,但仍存在以亞洲病例為主導(占62%)、以手術治療病例為主(占97%)的特征。
 圖1
第九版UICC/IASLC/AJCC胸腺腫瘤TNM分期最終納入分析的患者例數
圖1
第九版UICC/IASLC/AJCC胸腺腫瘤TNM分期最終納入分析的患者例數
3 第九版分期的變與不變
如前所述,新分期并非單純追求改變,還需要對既往的分期進行驗證。一個良好的分期不僅要做到期別之間存在明顯區分有統計學差異、期別內部有較好的一致性,還要做到與前一版分期有較好的延續性,并且實現臨床價值和臨床可操作性間的均衡。同時,TNM分期需要維持其普適性原則,不僅應適用于不同國家、地區、醫院,而且也應適用于所有的病理類型。正如肺癌分期不會區分鱗癌與腺癌,胸腺腫瘤分期也不會區分瘤與癌,只要同一個分期在所有瘤種里達到相似的預后區分即可。
基于這些要求,第九版分期利用更為全面的臨床數據和復發、生存結果,對既往的TNM分期進行了重新劃分和組合,進一步貫徹不同期別間差異明顯、同一期別內部高度一致的原則;而對于既往更多是出于經驗進行的分類劃分則利用前所未有的大病例組數據給予驗證和肯定。同時,由于胸腺腫瘤相對比較惰性,早期胸腺腫瘤手術完整切除后有不易復發、復發時間較晚、復發后仍然可以獲得長期生存、死亡病例以非腫瘤相關原因為主的特點。例如 ChART 數據庫中手術完整切除的 Ⅰ ~ Ⅲ a 期 胸 腺 腫 瘤 患 者 , 1 0 年 總生 存 (overall survival,OS)高達 89.5%;基于這部分患者的復發信息建立的復發預測模型將T1期的所有胸腺瘤以及T2期、T3期的A、AB、B1型胸腺瘤劃分為轉移風險低危組,而T2期、T3期的B2、B3型胸腺瘤以及所有的胸腺癌和神經內分泌腫瘤劃分為轉移風險高危組,前者的復發率為2.7%,而后者則高達20.1%[7]。因此出于對胸腺腫瘤特殊生物學行為的考慮,對于早期胸腺腫瘤使用腫瘤無復發率(freedom from recurrence,FFR)作為劃分的終點,相比于生存更加能反映早期胸腺腫瘤臨床上的治療結果;而對于晚期胸腺腫瘤則參照其他惡性實體腫瘤使用OS作為劃分的終點。充足的數據和合理的劃分終點保證了新分期擁有堅實的統計學基礎。
3.1 以腫瘤大小決定T1a期和T1b期
第八版分期以是否侵犯縱隔胸膜把局限在前縱隔胸腺及其周圍脂肪的早期腫瘤劃分為T1a期和T1b期。而第九版分期則第一次將腫瘤大小納入T分期中,在T1分期中做出了以下更改:以5 cm為界限,局限在胸腺以及周圍脂肪的胸腺腫瘤,腫瘤直徑≤5 cm為T1a期,>5 cm為T1b期(表1)[5]。
將腫瘤大小納入分期是建立在新的數據庫中腫瘤大小的數據較第八版數據庫更加齊全的基礎上,通過在訓練數據集中選取可以區分預后的腫瘤大小臨界值,在驗證數據集中進行驗證。最終所選取、驗證的臨界值為4.5~9.0 cm,而所取5 cm是在借鑒既往研究[8]結果后的人為設定。對比>5 cm和≤5 cm的T1期腫瘤的OS和FFR可發現,在胸腺瘤中,前者OS和FFR都顯著低于后者(P均<0.05);而在胸腺癌中,前者和后者的OS和FFR有數值差別,但差異無統計學意義。由于T2期、T3期、T4期患者數量較少,無法在這些分期中進行驗證,同時考慮到腫瘤外侵程度對預后的影響遠大于腫瘤本身的大小,在第九版分期中腫瘤大小的區分僅用于T1期早期腫瘤中[9]。
胸膜侵犯雖然在新的數據庫中也有區分T1期腫瘤預后的作用,但在新分期中僅作為額外的病理學表述(additional histologic descriptor),而不作為T1a期和T1b期的區分標準。其中最主要的原因是分期委員會T分期小組認為胸膜侵犯無論是術前臨床影像還是術后病理評估均有一定難度,因此利用一個在臨床上難以判斷的因素作為標準可行性較差。但胸膜侵犯也不應因新分期的改變而被忽視,在癌癥報告國際合作組織(International Collaboration of Cancer Reporting,ICCR)最新提出的胸腺腫瘤手術切除標本的匯報標準中,腫瘤直接侵犯(包括胸膜侵犯)是匯報的10項“核心因素”之一[10]。這提醒臨床工作者,尤其是外科醫生和病理科醫生,在對標本處理和檢查上應有更好的溝通和交流,外科醫生應注重手術切除標本上縱隔胸膜的標注,以便病理科醫生在鏡下對腫瘤是否浸潤穿透胸膜彈力層進行判斷;同時,臨床醫生也應探索如何通過影像組學手段提高術前對胸膜侵犯判斷的準確性。
3.2 對T2期和T3期的修改
第八版中的T2期為心包侵犯,T3期為肺、膈神經、胸壁、頭臂靜脈、上腔靜脈以及心包外的肺動靜脈受侵。第九版分期則將肺與膈神經從T3期中移除,降至T2期(表1)[5]。
既往臨床實踐中,肺實質的局部侵犯以及膈神經的侵犯相比其他T3期結構的侵犯在臨床處理方面有較大不同,這一點在外科手術上體現得最為明顯:心包、局部肺、膈神經的侵犯更易完整切除,即使在微創手術下也有較大可行性;而靜脈系統和心包外肺血管的侵犯則可能會導致更多的非R0切除或開放手術。此前谷志濤等[11]針對這一點在進展期胸腺腫瘤微創對比開放的研究中,創新性地使用了切除指數(resection index,RI)對原T3期結構進行了較好的手術難度劃分,其RI所采用的計算方式與新分期T2期、T3期的重新劃分不謀而合。
既往Masaoka-Koga分期中局部進展期腫瘤均列入Ⅲ期,非常混雜;UICC/IASLC/ITMIG第八版分期利用T分期概念將常規手術無法切除的腫瘤劃分為T4期,首次將原發腫瘤按照手術切除可能性進行了區分[1];而第九版分期則進一步將肺與膈神經等易于手術完整切除的結構與胸壁、大血管等切除難度較高的結構進行了細分。通過利用新數據對原本T2期/T3期患者的預后進行分析發現,在胸腺瘤中,肺和膈神經的侵犯相比于其他T3期結構的侵犯,雖然OS差異無統計學意義,但有更好的FFR:在R0切除且N0M0期的前提下,前者的5年FFR為82%,后者為70%;在胸腺癌中,相比于其他T3N0M0期,侵犯肺/膈神經的T3N0M0期患者與僅侵犯心包的T2N0M0期在R0切除后有更加接近的FFR:侵犯心包、侵犯肺/膈神經和侵犯其他原T3期結構患者的5年FFR分別為50%、61%和41%[9]。T2期、T3期的修改無疑做到了不同分期間差異明顯、同一分期內部高度統一,但在細節方面仍存在著美中不足,比如局部肺實質侵犯和廣泛肺實質侵犯的區分,新T3期內部的繼續劃分,單側、雙側膈神經侵犯的區分,這些問題都因第九版數據庫中病例數據缺乏相應的細節項而無法做出更進一步的劃分。
膈神經和肺實質侵犯的分類下降,必將成為臨床治療改變的催化劑。首先在手術方面,此舉將進一步推動外科醫生對進展期胸腺腫瘤微創手術的探索和嘗試。在中國抗癌協會胸腺腫瘤診療指南中,UICCⅠ期胸腺腫瘤推薦微創手術,在微創技術較為成熟的大的臨床中心,對UICC Ⅱ~Ⅲa期(第八版)可嘗試進行微創胸腺手術[12]。此推薦來自于部分胸外科中心對于進展期胸腺腫瘤微創手術的成功嘗試,希望未來可以有多中心、隨機對照的研究結果支持微創手術在進展期胸腺腫瘤中的使用。其次,T2期、T3期的修改可能會推動胸腺腫瘤術后輔助治療的變化。對于局部進展期胸腺腫瘤完整切除后的輔助治療,各個指南、組織、中心都有不同的推薦, NCCN指南中,Masaoka-KogaⅢ期的胸腺瘤R0切除后建議術后放療[13];ITMIG的回顧性研究[14]結果則提示Masaoka-KogaⅡ~Ⅲ期 R0切除的胸腺瘤患者,術后放療組10年OS明顯高于未放療組(86% vs. 79%,P=0.002);而日本胸腺腫瘤研究協作組的研究[15]則發現術后輔助放療僅對Ⅲ期胸腺癌患者有益。中國抗癌協會胸腺腫瘤診療指南則推薦R0切除后,UICCⅠ期的胸腺瘤和Ⅱ~ⅢA期(第八版)的A、AB、B1型胸腺瘤,不進行術后輔助治療,UICC Ⅱ~ⅢA(第八版)的B2、B3型胸腺瘤,可考慮術后輔助放療或隨訪[12]。鑒于目前為止所有的回顧性研究都是基于以往的分期系統,希望新分期的推出有助于基于T分期的細分行進一步的研究,為未來胸腺腫瘤輔助治療策略提供高級別的新證據。
3.3 對N分期、M分期的繼承
第九版分期將繼續沿用第八版分期中關于淋巴結和遠處轉移的分期(表2)。鑒于第八版分期數據存在著晚期病例較少、分類依賴專家共識的問題,第九版分期在胸腺腫瘤淋巴結和遠處轉移所做的工作是利用總體病例數更龐大、陽性病例更豐富的新數據庫,對第八版分類進行驗證[16-17]。
由于第八版數據庫淋巴結轉移陽性的病例有限,將胸腺腫瘤淋巴結轉移分為位于前縱隔的N1期和居于縱隔深處和頸部的N2期并非完全出自統計分析,而是基于以下幾點:第一是解剖位置上遠近的猜測,N1期為前縱隔胸腺內的淋巴結,N2期為深縱隔和更遠的淋巴結;第二為手術摘除的困難程度不同,N1期淋巴結通過全胸腺切除可以一并去除,而N2期淋巴結的摘除則需要額外的操作;第三則為是否有足夠可用的數據將不同N分期的預后進行區分[18]。第九版數據庫中淋巴結信息的完整度明顯提高,病理學淋巴結信息存在的病例數占74.6%(6 820/9 147),但治療前臨床淋巴結信息存在的病例僅占25.3%(2 317/9 147),一定程度上反映了胸腺腫瘤基于影像對淋巴結轉移情況判斷的困難。病理學N1(pN1)期陽性患者有168例、病理學N2期(pN2)陽性患者123例,相比于第八版的75例pN1和68例pN2有大幅度增加。由于胸腺腫瘤淋巴結轉移并非常見事件,因此在新的數據庫中病理淋巴結陰性(pN0)和臨床淋巴結陰性(cN0)有較高的一致性,兩者的占比分別為89.0%和97.7%;而病理淋巴結陽性(pN+)和臨床淋巴結陽性(cN+)之間的一致性則較低,一定程度上由于臨床醫生對于胸腺腫瘤術前淋巴結狀態的忽視以及缺乏較好的手段判斷術前淋巴結狀態。第九版數據庫顯示淋巴結轉移率在不同病理類型中有明顯差異:在胸腺瘤中占1.5%,在胸腺癌中占17.6%,在胸腺神經內分泌腫瘤中占27.7%。此與既往來自ChART多中心回顧性數據庫得到的結果一致;而此前ChART前瞻性多中心觀察性研究結果也表明,術中主動清掃淋巴結的胸腺腫瘤病例淋巴結轉移比例較回顧性數據庫中報道的結果顯著增高,相比于胸腺瘤,胸腺癌和胸腺神經內分泌腫瘤更容易發生淋巴結轉移[19-20]。
利用新的數據庫對既往N分期進行驗證:在胸腺癌中,pN1病例的OS明顯低于pN0(P=0.017),pN2病例的OS也明顯低于pN1(P=0.006);在胸腺瘤中,pN1病例的OS明顯低于pN0(P<0.001),pN2和pN1的OS相近(P=0.85)。這些結果肯定了第八版分期N0、N1、N2的分類,為N分期維持不變提供了充足的證據。SPFC-TD N分期小組就此提醒臨床工作者今后應進一步重視胸腺腫瘤治療前淋巴結狀態評估、手術中加強對高級別和進展期腫瘤的淋巴結清掃、術后進行細致的病理評估,提高分期準確性,指導預后判斷和治療選擇,并為未來第十版分期的修訂提供更為詳實的數據基礎。
對于胸腺腫瘤的遠處轉移,第八版分期借鑒了既往Masaoka-Koga分期對于不同轉移方式機制的猜想以及臨床處理方式的不同,將胸膜、心包播散分類為M1a,肺實質、遠處器官轉移分類為M1b,但兩者在生存曲線上僅存在肉眼的區分[18]。在新的數據庫中,cM1a病例數為101例,cM1b病例數為29例;pM1a的病例數為326例,pM1b的病例數為155例。臨床上判斷有轉移的胸腺瘤和胸腺癌的病例僅有69.1%和51.0%接受了手術治療,再加上M0病例所占比例較高,導致cM和pM之間的一致性不高:胸腺瘤和胸腺癌中分別有76%和53%的cM1a最后診斷為pM1a,14%和33%的cM1b最后診斷為pM1b。
由于cM數據較少,新分期僅利用pM數據對既往M分期進行驗證。在胸腺瘤中, pM1a的OS 和FFR均顯著低于pM0[HR=3.23,95%CI (2.38,4.55),P<0.001;HR=14.30,95%CI(9.09,43.00),P<0.001];在胸腺癌中,pM1a的FFR顯著低于pM0[HR=2.63,95%CI(1.33,5.26),P=0.004],但OS差異無統計學意義。在胸腺瘤和胸腺癌中,并未找到pM1a和pM1b間顯著的OS或FFR差異。另外,分期委員會對同一分期內部不同描述進行了進一步分析,結果發現,對于pM1a期胸腺瘤患者,胸膜播散、心包播散或兼具兩者的OS無明顯差異;對于pM1b期胸腺瘤患者,肺轉移和胸外轉移的OS也無明顯差異;但對于pM1a期胸腺癌患者,胸膜播散的OS有優于心包播散和兼具兩者的趨勢。由于有細節分類的數據量過少以及將M1a和M1b繼續細分的證據尚不充足,第九版分期將維持第八版分期提出的M分期。但與此同時,分期委員會也基于臨床實踐對未來的M分期進行了猜測和暢想。在治療上,單一胸腔、遠處轉移患者,相比多發胸腔、遠處轉移患者,更容易通過局部治療獲得較好的治療效果,得到較好的預后;而一側胸腔多發轉移和雙側胸腔、遠處多發轉移在治療效果上也有不同。因此,分期委員會將在未來探討是否有將M分期劃分為單一的種植或轉移、同側多發轉移、雙側和遠處多發轉移的可能性。
4 總結和展望
總之,胸腺腫瘤的第九版分期基于全新的數據,對第八版分期進行了驗證傳承和修訂更新,將T1a和T1b期的區分從縱隔胸膜的侵犯更改為腫瘤大小,將肺侵犯、膈神經侵犯降至了T2期;而N、M分類保持不變,整體的TNM分期組合維持不變(表3)。其中的變是根據更大量、更全面的數據進行更有意義的區分,這種意義不僅僅是統計學層面,更體現在臨床應用上;而不變則是通過新的數據對既往經驗層面上的劃定進行統計學驗證,有力地說明了其合理性。這些改變也提醒臨床醫生在診斷和治療方面需要不斷進行相應的思考、改變和提高,比如如何提高臨床分期判斷的準確性,如何采取有效的手段發現隱匿的淋巴結和遠處轉移,從而為患者提供合適的治療模式;如何以分期的改變作為出發點,對局部進展期患者的手術治療、輔助治療甚至新輔助治療優化選擇。同時,新分期的提出也促使醫生用臨床一線發現的問題、得到的數據對分期進行進一步的驗證和改進。
雖然第九版分期在上一版的基礎上做到了改革和繼承齊頭并進,但此次收集的數據仍存在諸多問題:1/4的病例缺少病理學分期信息,3/4的病例缺少臨床分期信息;雖然晚期病例和前瞻性的病例數增加,但接受手術切除病例和來自回顧性數據庫的病例仍占絕大部分,導致數據庫中的病例仍以相對早期的病例為主,且在數據質量方面難以把控;一些細節變量的高頻率缺失以及部分分組數據豐度較低,比如胸腺癌和神經內分泌腫瘤病例較少,轉移病例缺少轉移數量、位置等細節。這些問題導致臨床醫生面臨的一些困擾沒有得到全部解答,比如肺侵犯范圍是否應在分期中進行細分,N2中的各站淋巴結是否有相同的預后價值,轉移的數量和位置是否應該加入分期中,胸腔內播散和其他遠處臟器轉移是否應該有所區分等,這些問題可能需要更龐大、更精細的數據進行回答。同時,第九版數據庫中的病例仍存在較大的地區性差異,并且非手術病例較少,無法更好地覆蓋晚期胸腺腫瘤的預后。要克服這些缺陷,不僅需要更加緊密的全球范圍內多組織、多中心的合作,而且對各個組織、中心提供的數據質量也提出了更高的要求。在ICCR最新提出的胸腺腫瘤手術切除標本的病理報告標準中,有10項“核心元素”和8項“非核心因素”,被認為與胸腺腫瘤的臨床管理、分期、預后息息相關[10],能否以此作為基石和啟發,為胸腺腫瘤分期數據錄入提供統一、詳細的模板,組建更高質量的數據庫,或將成為克服第九版分期缺陷的重要武器。
利益沖突:無。
作者貢獻:于豐浩負責內容構思和文章撰寫;谷志濤、茅騰、許寧、章雪飛、郝秀秀負責文章修改意見的提出;方文濤負責文章思路構架的提出以及提供文章修改意見。