引用本文: 張韶鵬, 趙豐, 白云鵬, 付博, 陳彤云, 李景輝, 陳慶良, 姜楠. 經導管瓣中瓣技術治療外科生物瓣衰敗的單中心回顧性研究. 中國胸心血管外科臨床雜志, 2024, 31(6): 842-847. doi: 10.7507/1007-4848.202312020 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
自上世紀60年代第一代外科生物瓣誕生以來,生物瓣膜已歷經多次技術更新和產品迭代,然而其耐久性問題始終未得到根本性解決[1-3]。隨著技術改進和患者對生活質量需求的不斷增長,瓣膜病指南[4]中生物瓣的植入年齡進一步減小,未來可能將有越來越多的患者面臨二次手術[5]。經導管瓣中瓣技術以其較小的創傷和極低的手術風險優勢,成為此類患者的首選。美國和歐洲兩大瓣膜指南[4, 6]均將其作為Ⅱa級推薦。
然而,由于人種和瓣膜使用情況等差異[2],西方經驗并不完全適用于我國國情。首先,國人小瓣環患者占比高,瓣中瓣術后殘余較高跨瓣壓差的問題尤為突出。其次,國內外外科瓣和介入瓣的使用情況及產品特點有較大差異[2],冠狀動脈(冠脈)風險、起搏器植入風險也不盡相同。本研究旨在通過總結本中心經驗,探討經導管瓣中瓣技術在我國主動脈瓣位外科瓣衰敗患者中應用的可行性。
1 資料與方法
1.1 臨床資料
連續納入2019年1月—2023年4月因主動脈瓣位外科生物瓣衰敗于天津大學胸科醫院(天津市胸科醫院)心外科行經導管瓣中瓣手術患者,收集患者基本信息和瓣膜應用情況,并進行持續隨訪。術后抗凝方案參照傳統外科手術管理。
納入標準:(1)符合生物瓣衰敗診斷標準[3, 7];(2)外科高危或患者拒絕外科開胸手術者;(3)不耐受體外循環者。排除標準:(1)急性感染性心內膜炎;(2)同期行其他開胸手術者(如冠脈旁路移植術);(3)外周血管入路存在禁忌等;(4)合并中度及以上瓣周漏者。
1.2 術前評估
所有患者術前均行經胸超聲心動圖、心電圖、冠脈及全主動脈增強CT檢查。查詢既往手術資料,明確前次外科手術所用瓣膜品牌及型號,CT測量外科瓣內徑。
1.3 手術方法
手術均在雜交手術室進行。患者仰臥位,靜脈吸入復合全身麻醉,均采取經股動脈入路。理想情況下,選擇擴大率為10%~20%的支架瓣膜(以真實內徑為準)。所有患者均未進行球囊預擴張,常規跨瓣,160~180 次/min快速起搏,根據外科瓣架顯影調整好植入深度后快速釋放。Mosaic瓣膜縫合緣在X線下不顯影,以無冠竇為最低點進行定位。植入深度為術中經食管超聲測量所得。
1.4 結局指標
主要結局指標包括:全因死亡、主動脈瓣峰值流速、平均跨瓣壓差。次要結局指標包括:冠脈阻塞、瓣周漏、循環崩潰、入路血管并發癥等。
1.5 統計學分析
統計分析采用SPSS 26.0軟件。符合正態分布的計量資料以均數±標準差(x±s)描述,不符合正態分布的計量資料以中位數(上下四分位數)[M(P25,P75)]描述,計數資料采用頻數(百分比)描述。術后及隨訪期間心臟彩色超聲相關指標采用單因素重復測量方差分析,不滿足球形假設的資料采用Greenhouse-Geisser檢驗。采用Pearson系數進行兩變量間相關性分析。雙側檢驗P≤0.05為差異有統計學意義。
1.6 倫理審查
本研究已經過天津市胸科醫院倫理委員會批準,審批號:2021YS-014-01。
2 結果
2.1 患者一般資料
共納入24例患者,其中男14例、女10例,平均年齡(68.17±7.72)歲,初次手術平均年齡(57.70±8.29)歲。中位EuroSCOREⅡ評分為5.12%(2.79%,7.02%)。既往高血壓病史者15例(62.5%),慢性阻塞性肺疾病4例(16.7%),紐約心臟協會心功能分級Ⅲ級及以上17例(70.8%),起搏器植入3例(12.5%),冠脈旁路移植術后3例(12.5%),主動脈手術史1例(4.2%)。術前中位腦鈉肽308.52(76.39,616.00)pg/mL。瓣膜衰敗原因以單純狹窄為主(62.5%),狹窄合并中度以上反流9例(37.5%);見表1。
兩次手術間隔時間(10.48±4.09)年,外科瓣植入時間最長為20年,所用瓣膜為23# HancockⅡ;最短時間為3年,因心內膜炎致瓣膜衰敗。外科瓣包括HancockⅡ(9例)、Mosaic(6例)、Epic(6例)、CE Standard(2例)、Magana Ease(1例)。CT測量瓣架平均內徑為(18.65±1.42)mm,其中真實內徑<19 mm者19例(79.2%)。左冠開口高度為(9.52±3.31)mm,最低為3.5 mm,右冠開口高度為(14.84±6.68)mm。左冠竇、右冠竇、無冠竇直徑分別為(33.31±7.48)mm、(32.09±7.66)mm、(33.12±8.19)mm;見表2。
2.2 手術結果
手術均順利完成;見圖1。無死亡、冠脈阻塞、循環崩潰、傳導阻滯等并發癥。1例患者發生股動脈撕裂,同期行股動脈切開修補。所有患者均采用國產自彭式支架瓣膜,包括Venus A/Plus 4例,VitaFlow 18例,Taurus 2例,平均植入深度為(7.33±3.62)mm。術后即刻峰值跨瓣流速為(2.44±0.55)m/s,平均跨瓣壓差為(13.18±6.24)mm Hg(1 mm Hg=0.133 kPa)。6例(25.0%)患者術后即刻流速≥3 m/s。
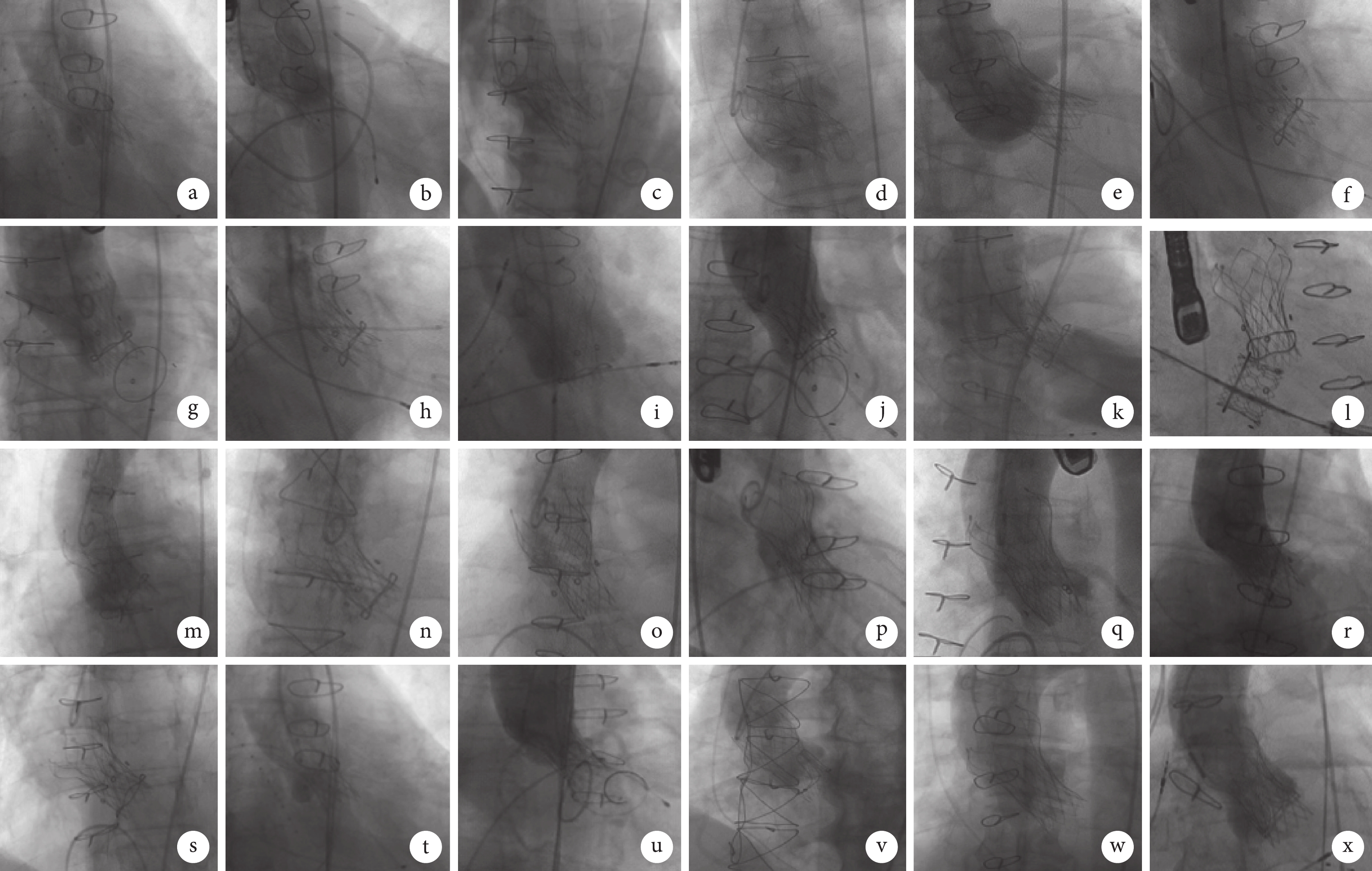 圖1
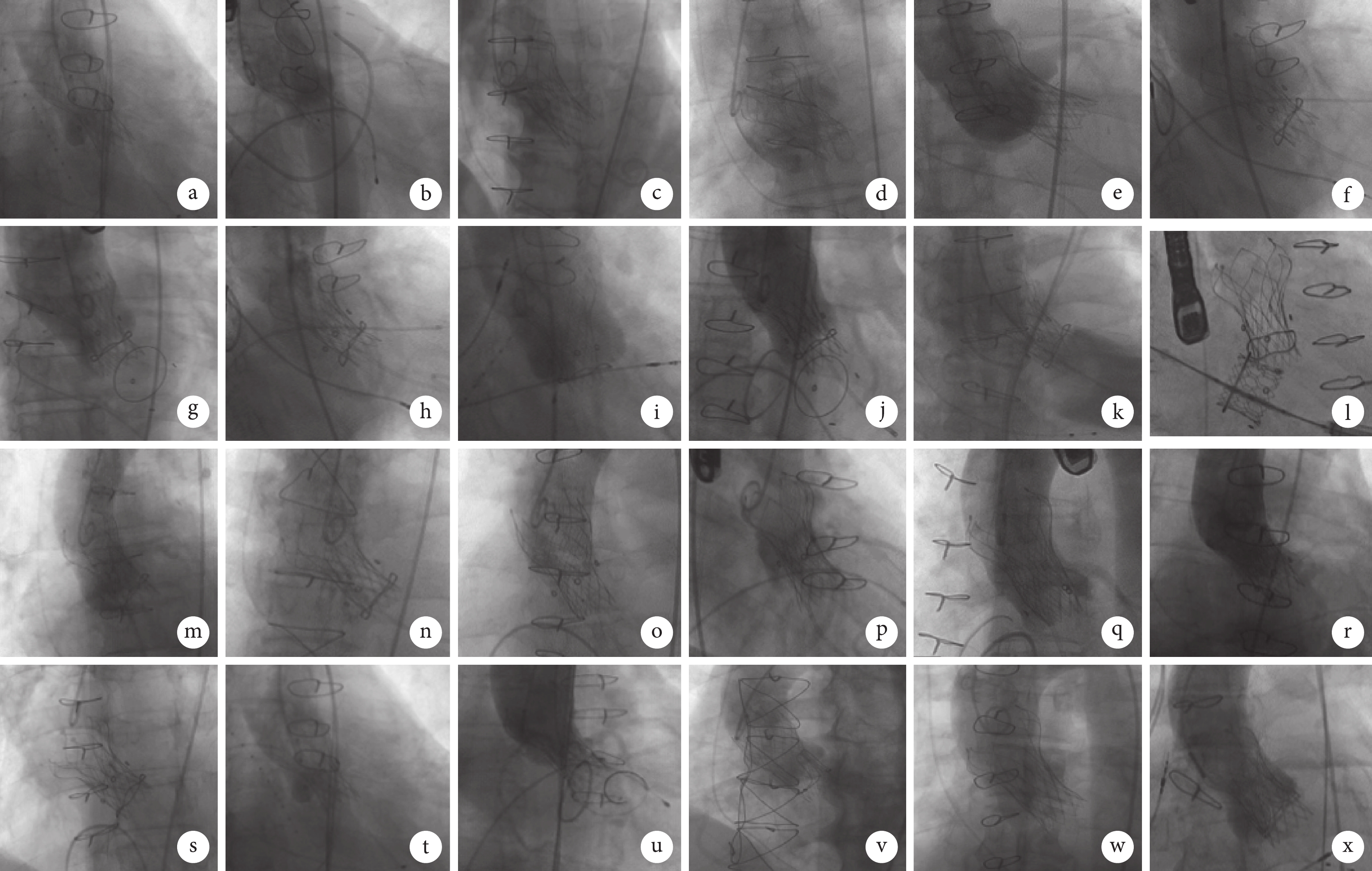
24例患者術中影像
圖1
24例患者術中影像
a~x代表每例患者;患者a、e、j、m、q、u術后即刻流速≥3 m/s;患者a、e、j瓣膜植入過深;患者m為Wheat術后,26 mm人工血管嚴重限制花冠部位展開,導致支架瓣膜流出口狹窄;患者q支架底端內凹導致流入口狹窄;患者u既往采用21# CE Standard外科瓣,測量支架內徑17 mm,真實內徑為14~15 mm,為瓣膜不匹配所致
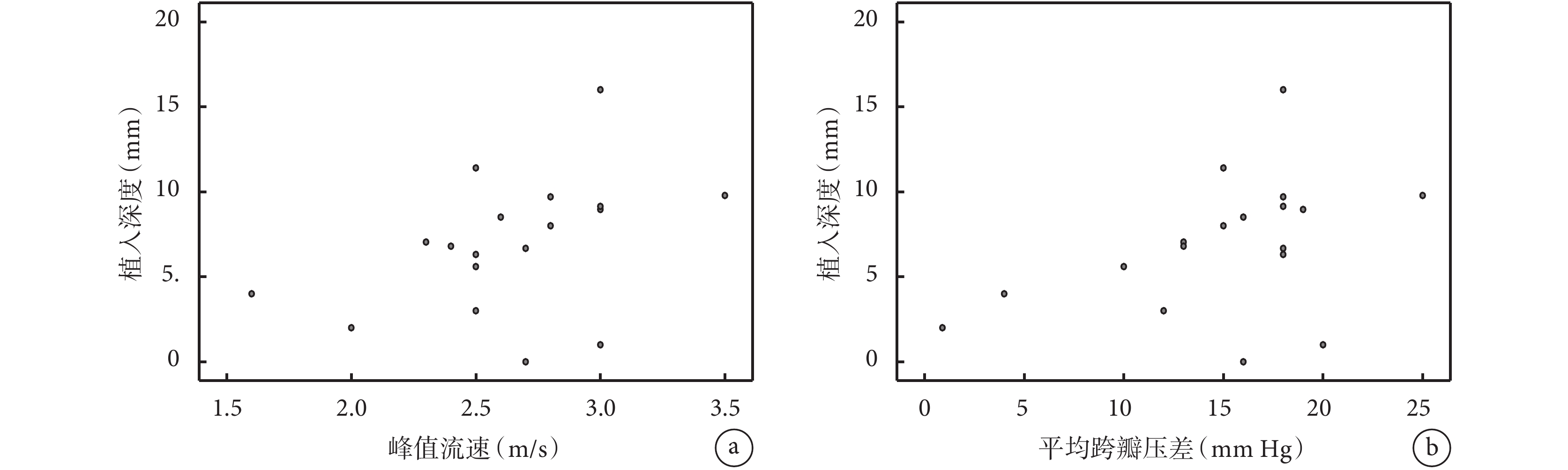
對真實內徑<19 mm的19例患者進行血流動力學參數與植入深度的相關性分析,結果顯示,植入深度與術后主動脈瓣峰值流速(Pearson系數為0.480,P=0.044)和平均跨瓣壓差(Pearson系數為0.451,P=0.011)呈正相關;見圖2。
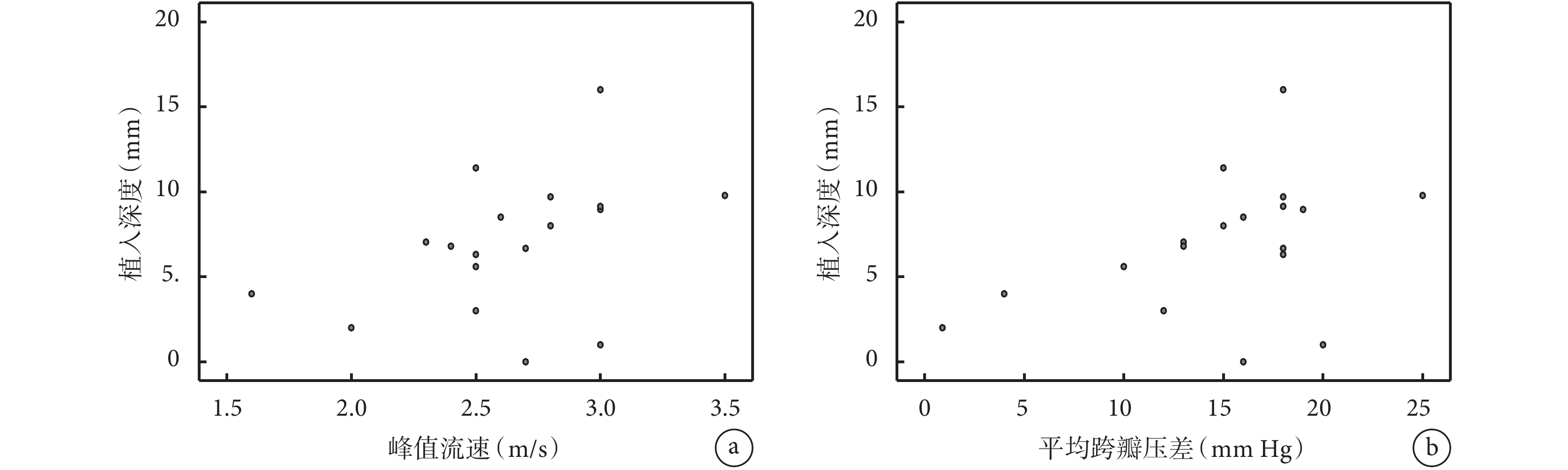 圖2
術后即刻峰值流速和平均跨瓣壓差與植入深度相關性的散點圖
圖2
術后即刻峰值流速和平均跨瓣壓差與植入深度相關性的散點圖
a:術后即刻峰值流速與植入深度的相關性(Pearson系數為0.480,
2.3 隨訪結果
所有患者均順利出院。中位隨訪時間16個月,最長隨訪期為63個月,最短為1個月。1例患者于術后第4年因感染新型冠狀病毒(新冠)去世,1例感染新冠后長期臥床,1例失訪。
出院前、術后3個月、術后6個月、術后1年、術后2年主動脈瓣峰值流速分別為(2.71±0.47)m/s、(2.90±0.62)m/s、(2.92±0.59)m/s、(2.97±0.71)m/s、(2.89±0.63)m/s。隨訪期內患者心功能得到持續改善,左心室舒張期末內徑在上述各隨訪節點分別為(57.13±8.94)mm、(54.95±8.08)mm、(53.13±3.98)mm、(53.40±3.95)mm、(50.20±2.78)mm(χ2=14.835,P<0.001);見表3~4。
3 討論
本研究發現:(1)本組病例小瓣環生物瓣占比較高(19/24);(2)介入支架瓣膜流入口或流出口展開受限,植入過深或支架瓣膜發生傾斜,均嚴重影響術后血流動力學表現;(3)國產自膨瓣植入支架內外科生物瓣,安全可行,且冠脈阻塞、永久起搏器植入等風險較小。
2007年德國Wenaweser等[8]完成全球第1例經皮主動脈瓣瓣中瓣手術,為外科生物瓣衰敗患者帶來福音。隨著PARTNER 2等瓣中瓣注冊研究[9-11]結果的公布,經導管瓣中瓣技術以其良好的血流動力學表現(5年隨訪平均跨瓣壓差16 mm Hg[9])、極低的手術風險(死亡率0.32%~0.52%[12-13]),替代再次開胸手術,成為此類患者的首選[4, 6]。
然而,國外研究結果并不完全適用于我國人群。首先,由于人種差異,國人體型較小,主動脈竇部結構普遍偏小。關于外科生物瓣的西方多中心研究[2, 14]結果顯示,23 mm以下瓣膜的使用率約為60%~70%。本組病例中小尺寸瓣膜的使用率為79.2%(19/24)。其次,相比國內市場,國外生物瓣品牌選擇豐富,其中支架外瓣膜(如Trifecta)占比達38%以上[12]。國內市面上以支架內瓣膜為主,在同一型號下,支架內瓣膜的內徑和有效開口面積有明顯劣勢[15]。因此,我國患者瓣中瓣術后殘余較高跨瓣壓差將顯得更為棘手。
本組病例出院前的平均跨瓣壓差為(16.39±6.52)mm Hg,與PARTNER 2研究結果相似,但隨訪期平均壓差上升至20 mm Hg,其中6例患者峰值流速持續在3 m/s以上,2例患者流速達4 m/s。過大的植入深度和支架瓣膜展開受限是殘余高跨瓣壓差的主要原因。
本研究結果顯示,植入深度與術后流速、跨瓣壓差呈明顯正相關關系。Sadat等[16]將23 mm Evolut PRO分別植入21 mm的Perimount Magna Ease、HancockⅡ和Trifecta中,通過體外人工心臟模擬和高速攝像機捕捉,結果提示4 mm的植入深度能夠獲得最大的有效瓣口面積和最低的跨瓣壓差。結合本組數據,筆者認為,在介入瓣膜擴大率<30%的情況下,3~5 mm的植入深度是比較合理的。
支架瓣膜展開形態直接影響術后血流動力學表現[17]。Fukui等[17]將支架瓣膜分為3部分:流入部分、功能部分和流出部分,任一部分展開不良均可能影響手術效果。圖1中患者m因前次植入的26 mm人工血管限制花冠部位展開,導致支架瓣膜流出口狹窄;患者q則因支架底端內凹導致流入口狹窄。生物瓣擴裂技術有利于支架瓣膜更好地展開,其有效性已得到證實[18]。然而,隨之增加的冠脈風險和遠期耐久性問題仍有待進一步研究。本組病例中未應用該技術。
國外研究[19]結果顯示,經導管瓣中瓣手術冠脈阻塞風險是原位主動脈瓣經導管主動脈瓣植入術的4倍,這一情況與本研究結果有較大差異。原因可能是:(1)國內外科瓣以支架內瓣膜為主,由于受外科瓣架限制,瓣葉或瓣腳難以阻擋冠脈開口;而國外人群支架外瓣膜或無支架瓣膜比例較高,瓣葉容易被推向冠脈開口[20](瓣葉切割技術的發明正是針對此類患者[21])。(2)國外球囊擴張式介入瓣膜占比超過50%,球囊擴張時可將較高的外科瓣瓣腳推向冠脈開口;而國內市場以3款國產的自膨式瓣膜為主,其徑向支撐力不足以改變外科瓣瓣腳形態。
綜上所述,國產自膨式介入瓣膜治療外科生物瓣衰敗安全可行,隨訪期間患者心臟結構和功能得到持續改善。支架瓣膜流入口、功能部分和花冠部分充分展開,良好的同軸性以及較小的植入深度是獲得術后良好血流動力學的關鍵。
但本研究為回顧性研究,樣本量較小,僅代表本中心經驗,且缺乏遠期隨訪結果。但本研究仍為國內目前納入病例數最多的一組報道,對其他中心有一定借鑒價值。
利益沖突:無。
作者貢獻:張韶鵬負責參與手術,研究設計,數據收集,病例隨訪,論文撰寫;趙豐負責手術,病例管理及隨訪;白云鵬負責試驗設計及數據分析;付博負責手術及隨訪;陳彤云負責統計分析,論文修改;李景輝負責隨訪及數據整理;陳慶良負責手術,論文修改;姜楠負責手術方案制定,質量管理,研究設計等。
自上世紀60年代第一代外科生物瓣誕生以來,生物瓣膜已歷經多次技術更新和產品迭代,然而其耐久性問題始終未得到根本性解決[1-3]。隨著技術改進和患者對生活質量需求的不斷增長,瓣膜病指南[4]中生物瓣的植入年齡進一步減小,未來可能將有越來越多的患者面臨二次手術[5]。經導管瓣中瓣技術以其較小的創傷和極低的手術風險優勢,成為此類患者的首選。美國和歐洲兩大瓣膜指南[4, 6]均將其作為Ⅱa級推薦。
然而,由于人種和瓣膜使用情況等差異[2],西方經驗并不完全適用于我國國情。首先,國人小瓣環患者占比高,瓣中瓣術后殘余較高跨瓣壓差的問題尤為突出。其次,國內外外科瓣和介入瓣的使用情況及產品特點有較大差異[2],冠狀動脈(冠脈)風險、起搏器植入風險也不盡相同。本研究旨在通過總結本中心經驗,探討經導管瓣中瓣技術在我國主動脈瓣位外科瓣衰敗患者中應用的可行性。
1 資料與方法
1.1 臨床資料
連續納入2019年1月—2023年4月因主動脈瓣位外科生物瓣衰敗于天津大學胸科醫院(天津市胸科醫院)心外科行經導管瓣中瓣手術患者,收集患者基本信息和瓣膜應用情況,并進行持續隨訪。術后抗凝方案參照傳統外科手術管理。
納入標準:(1)符合生物瓣衰敗診斷標準[3, 7];(2)外科高危或患者拒絕外科開胸手術者;(3)不耐受體外循環者。排除標準:(1)急性感染性心內膜炎;(2)同期行其他開胸手術者(如冠脈旁路移植術);(3)外周血管入路存在禁忌等;(4)合并中度及以上瓣周漏者。
1.2 術前評估
所有患者術前均行經胸超聲心動圖、心電圖、冠脈及全主動脈增強CT檢查。查詢既往手術資料,明確前次外科手術所用瓣膜品牌及型號,CT測量外科瓣內徑。
1.3 手術方法
手術均在雜交手術室進行。患者仰臥位,靜脈吸入復合全身麻醉,均采取經股動脈入路。理想情況下,選擇擴大率為10%~20%的支架瓣膜(以真實內徑為準)。所有患者均未進行球囊預擴張,常規跨瓣,160~180 次/min快速起搏,根據外科瓣架顯影調整好植入深度后快速釋放。Mosaic瓣膜縫合緣在X線下不顯影,以無冠竇為最低點進行定位。植入深度為術中經食管超聲測量所得。
1.4 結局指標
主要結局指標包括:全因死亡、主動脈瓣峰值流速、平均跨瓣壓差。次要結局指標包括:冠脈阻塞、瓣周漏、循環崩潰、入路血管并發癥等。
1.5 統計學分析
統計分析采用SPSS 26.0軟件。符合正態分布的計量資料以均數±標準差(x±s)描述,不符合正態分布的計量資料以中位數(上下四分位數)[M(P25,P75)]描述,計數資料采用頻數(百分比)描述。術后及隨訪期間心臟彩色超聲相關指標采用單因素重復測量方差分析,不滿足球形假設的資料采用Greenhouse-Geisser檢驗。采用Pearson系數進行兩變量間相關性分析。雙側檢驗P≤0.05為差異有統計學意義。
1.6 倫理審查
本研究已經過天津市胸科醫院倫理委員會批準,審批號:2021YS-014-01。
2 結果
2.1 患者一般資料
共納入24例患者,其中男14例、女10例,平均年齡(68.17±7.72)歲,初次手術平均年齡(57.70±8.29)歲。中位EuroSCOREⅡ評分為5.12%(2.79%,7.02%)。既往高血壓病史者15例(62.5%),慢性阻塞性肺疾病4例(16.7%),紐約心臟協會心功能分級Ⅲ級及以上17例(70.8%),起搏器植入3例(12.5%),冠脈旁路移植術后3例(12.5%),主動脈手術史1例(4.2%)。術前中位腦鈉肽308.52(76.39,616.00)pg/mL。瓣膜衰敗原因以單純狹窄為主(62.5%),狹窄合并中度以上反流9例(37.5%);見表1。
兩次手術間隔時間(10.48±4.09)年,外科瓣植入時間最長為20年,所用瓣膜為23# HancockⅡ;最短時間為3年,因心內膜炎致瓣膜衰敗。外科瓣包括HancockⅡ(9例)、Mosaic(6例)、Epic(6例)、CE Standard(2例)、Magana Ease(1例)。CT測量瓣架平均內徑為(18.65±1.42)mm,其中真實內徑<19 mm者19例(79.2%)。左冠開口高度為(9.52±3.31)mm,最低為3.5 mm,右冠開口高度為(14.84±6.68)mm。左冠竇、右冠竇、無冠竇直徑分別為(33.31±7.48)mm、(32.09±7.66)mm、(33.12±8.19)mm;見表2。
2.2 手術結果
手術均順利完成;見圖1。無死亡、冠脈阻塞、循環崩潰、傳導阻滯等并發癥。1例患者發生股動脈撕裂,同期行股動脈切開修補。所有患者均采用國產自彭式支架瓣膜,包括Venus A/Plus 4例,VitaFlow 18例,Taurus 2例,平均植入深度為(7.33±3.62)mm。術后即刻峰值跨瓣流速為(2.44±0.55)m/s,平均跨瓣壓差為(13.18±6.24)mm Hg(1 mm Hg=0.133 kPa)。6例(25.0%)患者術后即刻流速≥3 m/s。
 圖1
24例患者術中影像
圖1
24例患者術中影像
a~x代表每例患者;患者a、e、j、m、q、u術后即刻流速≥3 m/s;患者a、e、j瓣膜植入過深;患者m為Wheat術后,26 mm人工血管嚴重限制花冠部位展開,導致支架瓣膜流出口狹窄;患者q支架底端內凹導致流入口狹窄;患者u既往采用21# CE Standard外科瓣,測量支架內徑17 mm,真實內徑為14~15 mm,為瓣膜不匹配所致
對真實內徑<19 mm的19例患者進行血流動力學參數與植入深度的相關性分析,結果顯示,植入深度與術后主動脈瓣峰值流速(Pearson系數為0.480,P=0.044)和平均跨瓣壓差(Pearson系數為0.451,P=0.011)呈正相關;見圖2。
 圖2
術后即刻峰值流速和平均跨瓣壓差與植入深度相關性的散點圖
圖2
術后即刻峰值流速和平均跨瓣壓差與植入深度相關性的散點圖
a:術后即刻峰值流速與植入深度的相關性(Pearson系數為0.480,
2.3 隨訪結果
所有患者均順利出院。中位隨訪時間16個月,最長隨訪期為63個月,最短為1個月。1例患者于術后第4年因感染新型冠狀病毒(新冠)去世,1例感染新冠后長期臥床,1例失訪。
出院前、術后3個月、術后6個月、術后1年、術后2年主動脈瓣峰值流速分別為(2.71±0.47)m/s、(2.90±0.62)m/s、(2.92±0.59)m/s、(2.97±0.71)m/s、(2.89±0.63)m/s。隨訪期內患者心功能得到持續改善,左心室舒張期末內徑在上述各隨訪節點分別為(57.13±8.94)mm、(54.95±8.08)mm、(53.13±3.98)mm、(53.40±3.95)mm、(50.20±2.78)mm(χ2=14.835,P<0.001);見表3~4。
3 討論
本研究發現:(1)本組病例小瓣環生物瓣占比較高(19/24);(2)介入支架瓣膜流入口或流出口展開受限,植入過深或支架瓣膜發生傾斜,均嚴重影響術后血流動力學表現;(3)國產自膨瓣植入支架內外科生物瓣,安全可行,且冠脈阻塞、永久起搏器植入等風險較小。
2007年德國Wenaweser等[8]完成全球第1例經皮主動脈瓣瓣中瓣手術,為外科生物瓣衰敗患者帶來福音。隨著PARTNER 2等瓣中瓣注冊研究[9-11]結果的公布,經導管瓣中瓣技術以其良好的血流動力學表現(5年隨訪平均跨瓣壓差16 mm Hg[9])、極低的手術風險(死亡率0.32%~0.52%[12-13]),替代再次開胸手術,成為此類患者的首選[4, 6]。
然而,國外研究結果并不完全適用于我國人群。首先,由于人種差異,國人體型較小,主動脈竇部結構普遍偏小。關于外科生物瓣的西方多中心研究[2, 14]結果顯示,23 mm以下瓣膜的使用率約為60%~70%。本組病例中小尺寸瓣膜的使用率為79.2%(19/24)。其次,相比國內市場,國外生物瓣品牌選擇豐富,其中支架外瓣膜(如Trifecta)占比達38%以上[12]。國內市面上以支架內瓣膜為主,在同一型號下,支架內瓣膜的內徑和有效開口面積有明顯劣勢[15]。因此,我國患者瓣中瓣術后殘余較高跨瓣壓差將顯得更為棘手。
本組病例出院前的平均跨瓣壓差為(16.39±6.52)mm Hg,與PARTNER 2研究結果相似,但隨訪期平均壓差上升至20 mm Hg,其中6例患者峰值流速持續在3 m/s以上,2例患者流速達4 m/s。過大的植入深度和支架瓣膜展開受限是殘余高跨瓣壓差的主要原因。
本研究結果顯示,植入深度與術后流速、跨瓣壓差呈明顯正相關關系。Sadat等[16]將23 mm Evolut PRO分別植入21 mm的Perimount Magna Ease、HancockⅡ和Trifecta中,通過體外人工心臟模擬和高速攝像機捕捉,結果提示4 mm的植入深度能夠獲得最大的有效瓣口面積和最低的跨瓣壓差。結合本組數據,筆者認為,在介入瓣膜擴大率<30%的情況下,3~5 mm的植入深度是比較合理的。
支架瓣膜展開形態直接影響術后血流動力學表現[17]。Fukui等[17]將支架瓣膜分為3部分:流入部分、功能部分和流出部分,任一部分展開不良均可能影響手術效果。圖1中患者m因前次植入的26 mm人工血管限制花冠部位展開,導致支架瓣膜流出口狹窄;患者q則因支架底端內凹導致流入口狹窄。生物瓣擴裂技術有利于支架瓣膜更好地展開,其有效性已得到證實[18]。然而,隨之增加的冠脈風險和遠期耐久性問題仍有待進一步研究。本組病例中未應用該技術。
國外研究[19]結果顯示,經導管瓣中瓣手術冠脈阻塞風險是原位主動脈瓣經導管主動脈瓣植入術的4倍,這一情況與本研究結果有較大差異。原因可能是:(1)國內外科瓣以支架內瓣膜為主,由于受外科瓣架限制,瓣葉或瓣腳難以阻擋冠脈開口;而國外人群支架外瓣膜或無支架瓣膜比例較高,瓣葉容易被推向冠脈開口[20](瓣葉切割技術的發明正是針對此類患者[21])。(2)國外球囊擴張式介入瓣膜占比超過50%,球囊擴張時可將較高的外科瓣瓣腳推向冠脈開口;而國內市場以3款國產的自膨式瓣膜為主,其徑向支撐力不足以改變外科瓣瓣腳形態。
綜上所述,國產自膨式介入瓣膜治療外科生物瓣衰敗安全可行,隨訪期間患者心臟結構和功能得到持續改善。支架瓣膜流入口、功能部分和花冠部分充分展開,良好的同軸性以及較小的植入深度是獲得術后良好血流動力學的關鍵。
但本研究為回顧性研究,樣本量較小,僅代表本中心經驗,且缺乏遠期隨訪結果。但本研究仍為國內目前納入病例數最多的一組報道,對其他中心有一定借鑒價值。
利益沖突:無。
作者貢獻:張韶鵬負責參與手術,研究設計,數據收集,病例隨訪,論文撰寫;趙豐負責手術,病例管理及隨訪;白云鵬負責試驗設計及數據分析;付博負責手術及隨訪;陳彤云負責統計分析,論文修改;李景輝負責隨訪及數據整理;陳慶良負責手術,論文修改;姜楠負責手術方案制定,質量管理,研究設計等。