引用本文: 余愷濤, 賈杰, 殷保兵. 基于數字療法的肝癌術后康復案例報道. 中國普外基礎與臨床雜志, 2023, 30(11): 1294-1300. doi: 10.7507/1007-9424.202309052 復制
版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
全球癌癥統計(GLOBOCAN2020)項目發布的最新癌癥數據顯示,肝癌發病率位居全球第6位,死亡率位居第3位[1],其中我國肝癌所致的傷殘壽命年占全球肝癌負擔的一半[2]。手術是肝癌治療的首選,但部分患者在術后甚至出院后仍有較多的功能障礙,而運動康復作為肝癌康復的重要治療手段之一,術后早期活動可促進腸蠕動、促進胃腸道功能恢復,減少肺部并發癥和靜脈血栓形成,還能改善患者心肺功能、肢體活動能力、生活質量、緊張焦慮等生理狀態,增加術后歸屬感、被理解和支持感,故加強患者的運動康復管理至關重要,但患者大多缺乏專業的生物學和醫學知識,從而沒有足夠心理認同感;同時缺乏足夠的反饋、監督機制,進而難以長期堅持[3-9],且大多醫務人員對肝癌患者的康復認知尚不足,這就可能導致不良的預后。近年來我國醫療水平不斷提高,生物-心理-社會醫學模式不斷深入,以人為本的治療觀念已成為臨床實施的重點[10],基于數字療法(digital therapeutics)的康復理念也應運而生。數字療法是一種由軟件程序驅動,以循證醫學為基礎的干預方案,用以治療、管理或預防疾病。本研究報道了復旦大學附屬華山醫院的1例肝癌肝段切除術患者術后康復案例,分析其康復治療過程以及基于數字療法的綜合康復治療1個月后取得的臨床療效,以提高相關醫務人員對基于數字療法的肝癌康復的認知。本研究經患者本人簽署知情同意書,經復旦大學附屬華山醫院醫學倫理委員會審查批準(2021-794)。
1 臨床資料
1.1 病史簡介
患者,男,54歲,既往有乙型肝炎、肝硬化病史,余無特殊。2021年6月26日于外院查甲胎蛋白(alpha-fetoprotein,AFP)偏高(72.67 ng/mL),9 d后來復旦大學附屬華山醫院進一步檢查上腹部增強CT,發現肝內多發惡性腫瘤(malignant tumors,MT),肝部分梗死可能,肝門旁見多個腫大淋巴結。此外,異凝血酶原偏高(666.60 mAU/mL),初步診斷為肝癌伴肝內轉移。于7月14日行肝動脈化療栓塞術(transcatheter arterial chemoembolization,TACE)加侖伐替尼和信迪利單抗進行轉化治療;42 d后第2次行TACE,出院后予以侖伐替尼加信迪利單抗治療。第2次TACE后55 d查上腹部增強CT,見肝內彌漫大小不等的類圓形低密度影伴梗死,邊緣欠清,增強后呈環形強化,提示肝內多發MT伴部分梗死。遂收住入院準備手術。
1.2 入院后查體
體格檢查見神清,精神可,步入病房,言語清晰,對答切題,營養良好,全身皮膚黏膜未見黃染,淺表淋巴結未觸及,心肺未及異常。術前行體能檢查:6 min步行試驗,475 m;握力,27.0 kg;5次坐站試驗,10.04 s;多維度疲勞量表(Multidimensional Fatigue Inventory,MFI)評分為52分,自述疲乏無力;焦慮評分(Generalized Anxiety Disorder 7,GAD-7)為4分,抑郁評分(Patient Health Questionnaire,PHQ-9)為4分;視覺模擬評分(visual analogue scale,VAS)為4分,患者主訴肝區及其左側肩胛骨隱痛;匹茲堡睡眠指數評分(Pittsburgh Sleep Index Scale,PSQI)為12分,患者主訴有睡眠障礙。
2 診療經過
2.1 手術治療及結果
首次TACE后99 d行手術,術中見腫瘤位于肝中葉,累及Ⅳ、Ⅴ和Ⅶ段,巨塊型,大小為10 cm×7 cm×4 cm,腫塊質韌,有包膜。腫瘤周邊多枚子灶,局限集中在Ⅳ段和Ⅷ段,大小為0.3~1.5 cm。行肝中葉肝段切除術加肝門淋巴結清掃術、膽囊切除。手術時間約260 min,術中出血約600 mL,未輸血,術中肝門阻斷2次,術后無并發癥發生,未訴特殊不適。
術后病理診斷:肝腫瘤見大片壞死,未見腫瘤成分,切緣未見腫瘤累及,周圍肝組織示CH-G1S2-3;膽囊示慢性膽囊炎;肝門淋巴結5枚,均見腫瘤轉移(5/5);結合免疫組織化學結果,符合肝細胞癌(Ⅱ~Ⅲ級)轉移。
2.2 康復治療
術后完善常規檢查,排除康復禁忌,外科團隊和康復醫學小組(主管醫師、康復護士和物理治療師)討論患者情況,制定康復目標。短期目標為自主坐起、輔助下站立和功能性步行,在他人輔助下實現生活自理;長期目標為功能恢復至無瘤狀態。本例患者的康復干預方案見表1。
本例患者干預前后的生理指標變化見表2。經康復訓練后、術后第7天,患者可以自主站立和功能性步行,并在他人輔助下能大部分生活自理,生命體征穩定,傷口恢復良好,予以出院;但患者自述存在疼痛,并伴有活動無耐力、睡眠障礙等情況。
基于上述情況,康復醫學團隊制定基于移動APP的出院后訓練方案,具體內容包括:于出院前1 d,由康復治療師指導患者進行數字療法介導下的康復干預,首先采用術康APP軟件評估患者的疾病情況和采集基本信息,同時佩戴智能心率帶以實時監測患者運動時的心率、總運動時長和有效運動時長,以此來反映運動處方的完成情況和實施進度;在醫生的操作下智能推送可視化的運動處方,康復醫生采用遠程監督的方式督促患者進行每周3~5次、每次30~50 min的運動康復訓練,并每隔2天聯系患者反饋訓練情況,具體內容見表3,用戶端界面見圖1。
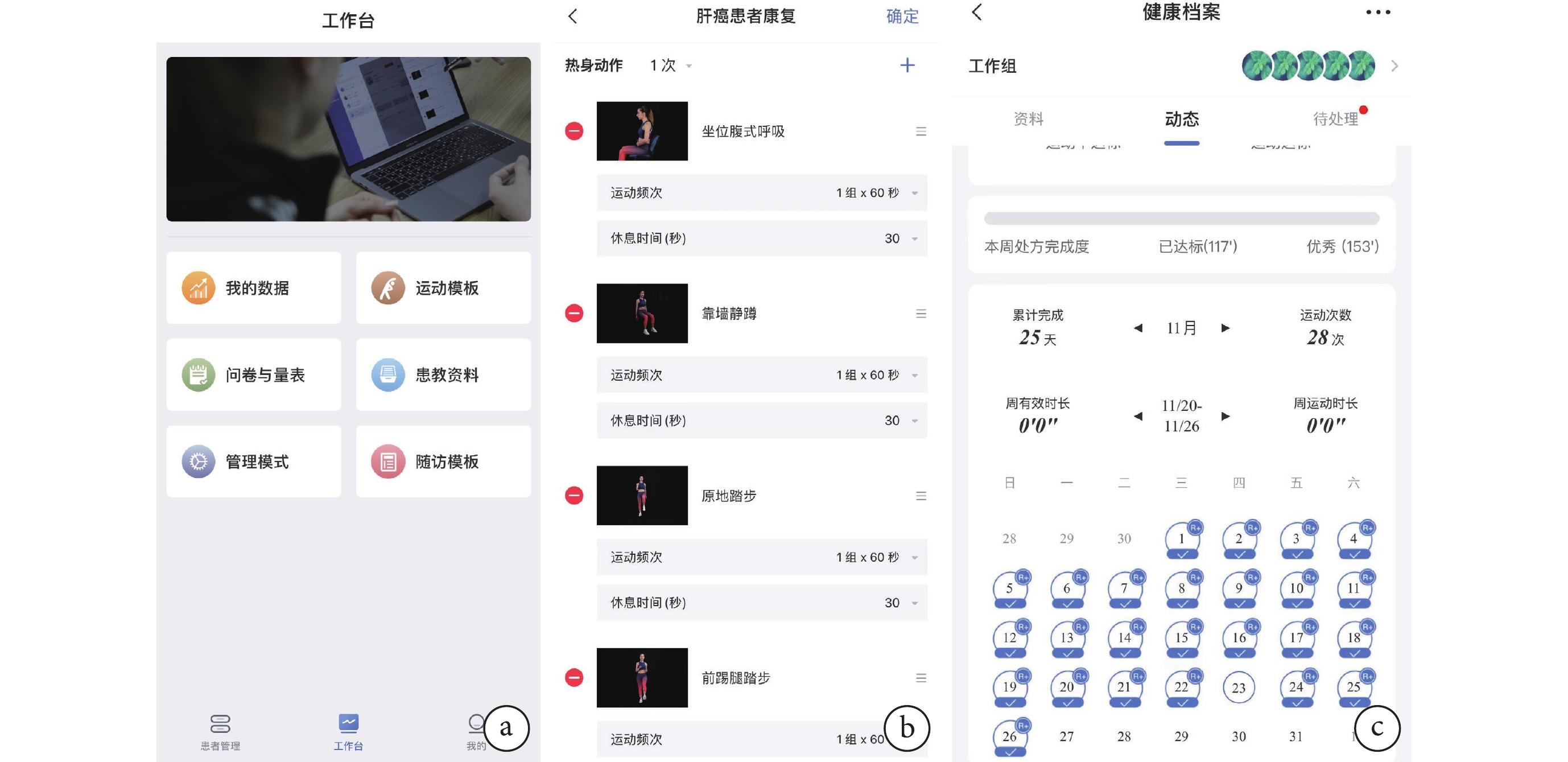 圖1
示基于數字療法的APP界面(a~c)
圖1
示基于數字療法的APP界面(a~c)
3 術后隨訪
術后1個月內,患者每周進行基于術康APP的運動康復鍛煉3~5次,每次運動時間在30~50 min之間,運動有效率為100%。傷口基本愈合無感染;術后1個月復查患者血常規、肝功能指標無異常,AFP偏高(8.59 ng/mL),但較之前下降。術后1個月的隨訪檢查結果見表2。術后1個月患者自述恢復情況顯著改善,傷口愈合良好,經康復評定后發現患者的體能、疼痛、疲勞狀況、緊張焦慮情緒和睡眠狀況均較前有所改善。
患者于術后1個月行第3次TACE治療,治療后1個月余于外院復查肝臟增強MRI檢查未見明顯活性灶;胰頭下方轉移淋巴結灶均較前范圍縮小,并行輸液港植入術,給予FOLFOX方案+吉西他濱化療2次;侖伐替尼加免疫治療維持。術后12個月接受增強MRI檢查發現肝臟多發強化結節,對肝臟轉移灶(肝右葉膈頂第二肝門附近0.8 cm病灶、右葉切緣附近0.8 cm病灶、門靜脈矢狀帶旁1.0 cm病灶、右后葉肝右靜脈后方0.8 cm病灶)行超聲引導下射頻消融。第1次射頻消融后7個月余接受增強MRI檢查發現肝臟多發強化結節,再次行超聲引導下射頻消融治療,并于第2次射頻消融后1個月余行第4次TACE治療,出院后一直繼續予以侖伐替尼加程序性死亡受體1治療,隨訪至目前(2023年10月)生存期約27個月(第1次TACE起算),恢復情況良好,目前已重返工作。
4 小結及討論
目前約64%的肝癌患者確診時已是中晚期階段,大多數已喪失根治性手術機會,中位生存期約為2年[11-12]。近年來,隨著免疫治療、靶向治療、介入治療等方式的出現,給中晚期不可切除肝癌的治療帶來轉機。目前已進入精準轉化醫學時代,既包括向外科可切除性的轉化,又涉及到向腫瘤學獲益的轉化[13]。肝癌轉化治療的短期目標是實現腫瘤根治性手術,最終目標是幫助患者實現高質量的長期生存,而晚期肝癌患者經轉化治療后生活質量下降,包括身體狀況、社會功能和精神心理狀況的下降[14],這就需要腫瘤康復的介入。當前的腫瘤治療模式受傳統科室劃分所限,各專業間較為獨立,患者較少獲得腫瘤康復的指導,未能將轉化治療后手術效果最大化。因此,開展肝癌術后多學科團隊的合作及對接較為重要[15]。數字療法是降低醫保費用并提供有效、便捷、遠程治療的解決方案,同時改善此類肝癌患者的預后 [16-20]。
本例患者接受肝癌晚期轉化治療后手術,術后運動功能障礙導致的疲乏無力,以及精神心理功能障礙引起的焦慮抑郁和睡眠障礙,經過院內康復和基于數字療法的院外康復,患者的心肺適能、睡眠狀況、疲乏和疼痛均恢復良好,目前患者生活完全自理,具有一定的臨床意義。
4.1 肝癌術后常見的功能障礙
4.1.1 運動功能障礙
運動功能障礙是指機體由于運動相關系統的結構或功能損害,導致運動功能部分和全部喪失。肝癌的運動功能障礙主要體現在軀干,軀干功能主要提供穩定性,為步行功能和上下肢的精細操作的實現提供支持。肝癌的運動功能障礙主要受到腫瘤疾病、手術治療、輔助治療、癌因性疲乏、精神心理功能障礙、營養狀況等影響。本例患者在術后主要表現為肌肉無力、肌肉萎縮、關節活動度受限、運動控制能力下降、虛弱和疲勞、活動減少、耐力下降等,在基于數字療法的康復后,患者恢復顯著好轉。此外,肝癌術后患者還存在肺功能障礙、疼痛和認知功能障礙,需要在早期關注患者的臨床癥狀,及時識別功能障礙,并進行有效康復訓練。
4.1.2 精神心理功能障礙
在肝癌的臨床診療過程中,患者會出現一系列復雜的心理問題[21]。患者在確診后,會產生抑郁、焦慮、憤怒、無助、絕望等多種不良情緒,以及自主神經癥狀和行為障礙[22]。在治療期間,手術及術后的一系列并發癥、放化療以及中晚期臨床癥狀均會給患者帶來生理-心理-社會功能的多重打擊,如疾病不確定感、焦慮、抑郁、癌癥復發恐懼等[23]。此外,照護者所承擔的經濟負擔、責任負擔和自我不良情緒抑制所激發的負性心理情緒,最終也會影響到患者的精神心理[24]。本例患者在術后主要表現為焦慮、抑郁并伴有睡眠障礙,在基于數字療法的康復后,患者焦慮抑郁情緒有所好轉,睡眠狀況也有顯著改善。
4.2 數字療法的優劣勢與難點
數字療法是一種由軟件程序驅動,以循證醫學為基礎的干預方案,用以治療、管理或預防疾病。其優勢在于:① 個性化治療。數字療法可以根據患者的個體需求提供個性化的治療方案。本案例中根據患者傷口、活動無耐力等情況為其制定保護傷口的運動方案,同時數字療法通過與虛擬現實技術相結合,與患者進行互動和心理疏導,減少肝癌術后患者的抑郁和痛苦情緒[25];并提供實時的支持技術激勵其健康習慣的養成,這與?sberg 等[26]通過研究表明數字化醫療可作為一種干預措施,使患者在術前減少乙醇消耗、改善飲食攝入、增加體力活動和戒煙作用一致,對于肝癌患者的圍手術期治療效果和預后具有一定的積極意義。② 便捷性。本案例中的患者在術后1個月均在家中接受治療并進行康復,在這期間減少醫院訪問次數的同時又通過軟件后臺增加了與醫生溝通的頻率。因此數字療法在一定程度上去除地理障礙,協助患者遠距離體驗到醫療資源,獲得更好的醫療服務。③ 實時監測。數字療法可以實時監測患者的狀況,以便及時干預,本案例中的患者實時佩戴心率帶(即可穿戴設備),并在每次運動完后完成評估量表。系統可以及時獲取患者的身體情況,并自行更改下一次運動強度。④ 成本效益。數字療法可以減少醫療成本,尤其是長期慢性疾病的治療費用。但同時,數字療法也存在一些隱患:① 隱私問題。數字療法可能涉及患者隱私,因此需要強化數據安全和隱私保護。② 技術障礙。患者在前期可能不熟悉或無法使用數字工具,這可能導致數字療法的不平等,因此需要醫務人員在出院前盡可能教會患者。③ 監管挑戰。數字療法需要合規性監管,以確保安全和有效性。
筆者認為目前數字療法的難點包括:① 技術發展。數字療法需要不斷的技術創新和發展,以滿足患者需求。如在運動處方方面,美國運動醫學會指南是目前大多數腫瘤康復所遵循的指導方針[27-30],但運動訓練的選擇沒有考慮患者的腫瘤學背景[31]。因此數字療法在康復處方制定過程中仍需要完善,包括患者的個性化評估,除考慮患者的心肺適能或肌肉耐力外,還需關注患者的年齡、生活方式、運動偏好、既往治療等。② 文化和社會接受。文化和社會背景的不同可能影響患者對數字療法的接受程度,因此在臨床診療過程中醫務人員應結合病情,將數字療法與原先的診療方案進行結合。隨著技術的不斷發展,數字療法有望在未來繼續發揮重要作用,提供更多創新的治療方法,并改善醫療體驗。然而,需要處理相關的隱私、安全、文化和監管挑戰,以實現數字療法的潛在潛力。
4.3 數字療法在肝膽腫瘤中應用的展望
隨著技術的不斷發展,數字療法需要進一步整合人工智能和大數據分析,提供更精準的運動建議和治療方案。在關注腫瘤普遍存在的體適能恢復(旨在提升患者骨骼肌含量和心肺適能)的同時,數字療法也應該關注肝膽腫瘤及其圍手術期的特性,如肝癌圍手術期出現疼痛、惡心、嘔吐、腹瀉、乏力、營養不良、經濟負擔、焦慮、抑郁等不良反應[32],以及術后發生率較高的并發癥如胸腔積液、腹水、墜積性肺炎等。TACE聯合靶向免疫治療對中晚期肝癌的轉化治療是近年來的熱點關注領域[33-34],但患者在治療階段伴有的睡眠障礙、全身疲乏、肌力下降、注意力不集中、焦慮抑郁等情況較少獲得關注。針對肝癌患者的失眠問題,數字療法在未來可以從腦電波切入,將醫學治療和音樂助眠相結合進行干預,根據算法和大數據智能識別特征腦電波形和節律,精準識別睡眠階段并開展音樂療法,加速患者入睡[35];譬如肝癌患者長期惡病質導致營養不良,機體免疫力低下,再加上術后長期臥床、痰液淤積,均會增加術后肺部感染的發生率,而數字療法通過具有循證依據的肺康復鍛煉能減少肺部感染的進展[36]。
在運動處方的設計中,最常被忽視或低估的是休息和恢復。目前技術層面上該模塊僅通過醫生和患者的主觀判斷進行設定。未來有望在循證依據的指導下針對患者的生理指標和主觀感受,對休息與恢復的方式和時長進行設定[37]。因此,肝癌患者的術后康復需要實時地評估疾病與功能障礙的進展與演變,個性化給予治療方案,來促進疾病的有效轉歸以及運動功能的提高。
綜上所述,本案例提供較為創新的臨床治療策略和康復路徑,有助于臨床醫生對肝癌患者實施全周期康復;并對此類疾病的運動康復的思路和具體方法提供新途徑。今后將進一步開展更廣泛的臨床干預研究,形成可推廣的臨床康復方案。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:余愷濤主要負責臨床資料收集和論文撰寫,賈杰和殷保兵主要負責設計文章思路。
倫理聲明:本研究已通過復旦大學附屬華山醫院倫理審查委員會的審核批準(批文編號:2021-794)。
全球癌癥統計(GLOBOCAN2020)項目發布的最新癌癥數據顯示,肝癌發病率位居全球第6位,死亡率位居第3位[1],其中我國肝癌所致的傷殘壽命年占全球肝癌負擔的一半[2]。手術是肝癌治療的首選,但部分患者在術后甚至出院后仍有較多的功能障礙,而運動康復作為肝癌康復的重要治療手段之一,術后早期活動可促進腸蠕動、促進胃腸道功能恢復,減少肺部并發癥和靜脈血栓形成,還能改善患者心肺功能、肢體活動能力、生活質量、緊張焦慮等生理狀態,增加術后歸屬感、被理解和支持感,故加強患者的運動康復管理至關重要,但患者大多缺乏專業的生物學和醫學知識,從而沒有足夠心理認同感;同時缺乏足夠的反饋、監督機制,進而難以長期堅持[3-9],且大多醫務人員對肝癌患者的康復認知尚不足,這就可能導致不良的預后。近年來我國醫療水平不斷提高,生物-心理-社會醫學模式不斷深入,以人為本的治療觀念已成為臨床實施的重點[10],基于數字療法(digital therapeutics)的康復理念也應運而生。數字療法是一種由軟件程序驅動,以循證醫學為基礎的干預方案,用以治療、管理或預防疾病。本研究報道了復旦大學附屬華山醫院的1例肝癌肝段切除術患者術后康復案例,分析其康復治療過程以及基于數字療法的綜合康復治療1個月后取得的臨床療效,以提高相關醫務人員對基于數字療法的肝癌康復的認知。本研究經患者本人簽署知情同意書,經復旦大學附屬華山醫院醫學倫理委員會審查批準(2021-794)。
1 臨床資料
1.1 病史簡介
患者,男,54歲,既往有乙型肝炎、肝硬化病史,余無特殊。2021年6月26日于外院查甲胎蛋白(alpha-fetoprotein,AFP)偏高(72.67 ng/mL),9 d后來復旦大學附屬華山醫院進一步檢查上腹部增強CT,發現肝內多發惡性腫瘤(malignant tumors,MT),肝部分梗死可能,肝門旁見多個腫大淋巴結。此外,異凝血酶原偏高(666.60 mAU/mL),初步診斷為肝癌伴肝內轉移。于7月14日行肝動脈化療栓塞術(transcatheter arterial chemoembolization,TACE)加侖伐替尼和信迪利單抗進行轉化治療;42 d后第2次行TACE,出院后予以侖伐替尼加信迪利單抗治療。第2次TACE后55 d查上腹部增強CT,見肝內彌漫大小不等的類圓形低密度影伴梗死,邊緣欠清,增強后呈環形強化,提示肝內多發MT伴部分梗死。遂收住入院準備手術。
1.2 入院后查體
體格檢查見神清,精神可,步入病房,言語清晰,對答切題,營養良好,全身皮膚黏膜未見黃染,淺表淋巴結未觸及,心肺未及異常。術前行體能檢查:6 min步行試驗,475 m;握力,27.0 kg;5次坐站試驗,10.04 s;多維度疲勞量表(Multidimensional Fatigue Inventory,MFI)評分為52分,自述疲乏無力;焦慮評分(Generalized Anxiety Disorder 7,GAD-7)為4分,抑郁評分(Patient Health Questionnaire,PHQ-9)為4分;視覺模擬評分(visual analogue scale,VAS)為4分,患者主訴肝區及其左側肩胛骨隱痛;匹茲堡睡眠指數評分(Pittsburgh Sleep Index Scale,PSQI)為12分,患者主訴有睡眠障礙。
2 診療經過
2.1 手術治療及結果
首次TACE后99 d行手術,術中見腫瘤位于肝中葉,累及Ⅳ、Ⅴ和Ⅶ段,巨塊型,大小為10 cm×7 cm×4 cm,腫塊質韌,有包膜。腫瘤周邊多枚子灶,局限集中在Ⅳ段和Ⅷ段,大小為0.3~1.5 cm。行肝中葉肝段切除術加肝門淋巴結清掃術、膽囊切除。手術時間約260 min,術中出血約600 mL,未輸血,術中肝門阻斷2次,術后無并發癥發生,未訴特殊不適。
術后病理診斷:肝腫瘤見大片壞死,未見腫瘤成分,切緣未見腫瘤累及,周圍肝組織示CH-G1S2-3;膽囊示慢性膽囊炎;肝門淋巴結5枚,均見腫瘤轉移(5/5);結合免疫組織化學結果,符合肝細胞癌(Ⅱ~Ⅲ級)轉移。
2.2 康復治療
術后完善常規檢查,排除康復禁忌,外科團隊和康復醫學小組(主管醫師、康復護士和物理治療師)討論患者情況,制定康復目標。短期目標為自主坐起、輔助下站立和功能性步行,在他人輔助下實現生活自理;長期目標為功能恢復至無瘤狀態。本例患者的康復干預方案見表1。
本例患者干預前后的生理指標變化見表2。經康復訓練后、術后第7天,患者可以自主站立和功能性步行,并在他人輔助下能大部分生活自理,生命體征穩定,傷口恢復良好,予以出院;但患者自述存在疼痛,并伴有活動無耐力、睡眠障礙等情況。
基于上述情況,康復醫學團隊制定基于移動APP的出院后訓練方案,具體內容包括:于出院前1 d,由康復治療師指導患者進行數字療法介導下的康復干預,首先采用術康APP軟件評估患者的疾病情況和采集基本信息,同時佩戴智能心率帶以實時監測患者運動時的心率、總運動時長和有效運動時長,以此來反映運動處方的完成情況和實施進度;在醫生的操作下智能推送可視化的運動處方,康復醫生采用遠程監督的方式督促患者進行每周3~5次、每次30~50 min的運動康復訓練,并每隔2天聯系患者反饋訓練情況,具體內容見表3,用戶端界面見圖1。
 圖1
示基于數字療法的APP界面(a~c)
圖1
示基于數字療法的APP界面(a~c)
3 術后隨訪
術后1個月內,患者每周進行基于術康APP的運動康復鍛煉3~5次,每次運動時間在30~50 min之間,運動有效率為100%。傷口基本愈合無感染;術后1個月復查患者血常規、肝功能指標無異常,AFP偏高(8.59 ng/mL),但較之前下降。術后1個月的隨訪檢查結果見表2。術后1個月患者自述恢復情況顯著改善,傷口愈合良好,經康復評定后發現患者的體能、疼痛、疲勞狀況、緊張焦慮情緒和睡眠狀況均較前有所改善。
患者于術后1個月行第3次TACE治療,治療后1個月余于外院復查肝臟增強MRI檢查未見明顯活性灶;胰頭下方轉移淋巴結灶均較前范圍縮小,并行輸液港植入術,給予FOLFOX方案+吉西他濱化療2次;侖伐替尼加免疫治療維持。術后12個月接受增強MRI檢查發現肝臟多發強化結節,對肝臟轉移灶(肝右葉膈頂第二肝門附近0.8 cm病灶、右葉切緣附近0.8 cm病灶、門靜脈矢狀帶旁1.0 cm病灶、右后葉肝右靜脈后方0.8 cm病灶)行超聲引導下射頻消融。第1次射頻消融后7個月余接受增強MRI檢查發現肝臟多發強化結節,再次行超聲引導下射頻消融治療,并于第2次射頻消融后1個月余行第4次TACE治療,出院后一直繼續予以侖伐替尼加程序性死亡受體1治療,隨訪至目前(2023年10月)生存期約27個月(第1次TACE起算),恢復情況良好,目前已重返工作。
4 小結及討論
目前約64%的肝癌患者確診時已是中晚期階段,大多數已喪失根治性手術機會,中位生存期約為2年[11-12]。近年來,隨著免疫治療、靶向治療、介入治療等方式的出現,給中晚期不可切除肝癌的治療帶來轉機。目前已進入精準轉化醫學時代,既包括向外科可切除性的轉化,又涉及到向腫瘤學獲益的轉化[13]。肝癌轉化治療的短期目標是實現腫瘤根治性手術,最終目標是幫助患者實現高質量的長期生存,而晚期肝癌患者經轉化治療后生活質量下降,包括身體狀況、社會功能和精神心理狀況的下降[14],這就需要腫瘤康復的介入。當前的腫瘤治療模式受傳統科室劃分所限,各專業間較為獨立,患者較少獲得腫瘤康復的指導,未能將轉化治療后手術效果最大化。因此,開展肝癌術后多學科團隊的合作及對接較為重要[15]。數字療法是降低醫保費用并提供有效、便捷、遠程治療的解決方案,同時改善此類肝癌患者的預后 [16-20]。
本例患者接受肝癌晚期轉化治療后手術,術后運動功能障礙導致的疲乏無力,以及精神心理功能障礙引起的焦慮抑郁和睡眠障礙,經過院內康復和基于數字療法的院外康復,患者的心肺適能、睡眠狀況、疲乏和疼痛均恢復良好,目前患者生活完全自理,具有一定的臨床意義。
4.1 肝癌術后常見的功能障礙
4.1.1 運動功能障礙
運動功能障礙是指機體由于運動相關系統的結構或功能損害,導致運動功能部分和全部喪失。肝癌的運動功能障礙主要體現在軀干,軀干功能主要提供穩定性,為步行功能和上下肢的精細操作的實現提供支持。肝癌的運動功能障礙主要受到腫瘤疾病、手術治療、輔助治療、癌因性疲乏、精神心理功能障礙、營養狀況等影響。本例患者在術后主要表現為肌肉無力、肌肉萎縮、關節活動度受限、運動控制能力下降、虛弱和疲勞、活動減少、耐力下降等,在基于數字療法的康復后,患者恢復顯著好轉。此外,肝癌術后患者還存在肺功能障礙、疼痛和認知功能障礙,需要在早期關注患者的臨床癥狀,及時識別功能障礙,并進行有效康復訓練。
4.1.2 精神心理功能障礙
在肝癌的臨床診療過程中,患者會出現一系列復雜的心理問題[21]。患者在確診后,會產生抑郁、焦慮、憤怒、無助、絕望等多種不良情緒,以及自主神經癥狀和行為障礙[22]。在治療期間,手術及術后的一系列并發癥、放化療以及中晚期臨床癥狀均會給患者帶來生理-心理-社會功能的多重打擊,如疾病不確定感、焦慮、抑郁、癌癥復發恐懼等[23]。此外,照護者所承擔的經濟負擔、責任負擔和自我不良情緒抑制所激發的負性心理情緒,最終也會影響到患者的精神心理[24]。本例患者在術后主要表現為焦慮、抑郁并伴有睡眠障礙,在基于數字療法的康復后,患者焦慮抑郁情緒有所好轉,睡眠狀況也有顯著改善。
4.2 數字療法的優劣勢與難點
數字療法是一種由軟件程序驅動,以循證醫學為基礎的干預方案,用以治療、管理或預防疾病。其優勢在于:① 個性化治療。數字療法可以根據患者的個體需求提供個性化的治療方案。本案例中根據患者傷口、活動無耐力等情況為其制定保護傷口的運動方案,同時數字療法通過與虛擬現實技術相結合,與患者進行互動和心理疏導,減少肝癌術后患者的抑郁和痛苦情緒[25];并提供實時的支持技術激勵其健康習慣的養成,這與?sberg 等[26]通過研究表明數字化醫療可作為一種干預措施,使患者在術前減少乙醇消耗、改善飲食攝入、增加體力活動和戒煙作用一致,對于肝癌患者的圍手術期治療效果和預后具有一定的積極意義。② 便捷性。本案例中的患者在術后1個月均在家中接受治療并進行康復,在這期間減少醫院訪問次數的同時又通過軟件后臺增加了與醫生溝通的頻率。因此數字療法在一定程度上去除地理障礙,協助患者遠距離體驗到醫療資源,獲得更好的醫療服務。③ 實時監測。數字療法可以實時監測患者的狀況,以便及時干預,本案例中的患者實時佩戴心率帶(即可穿戴設備),并在每次運動完后完成評估量表。系統可以及時獲取患者的身體情況,并自行更改下一次運動強度。④ 成本效益。數字療法可以減少醫療成本,尤其是長期慢性疾病的治療費用。但同時,數字療法也存在一些隱患:① 隱私問題。數字療法可能涉及患者隱私,因此需要強化數據安全和隱私保護。② 技術障礙。患者在前期可能不熟悉或無法使用數字工具,這可能導致數字療法的不平等,因此需要醫務人員在出院前盡可能教會患者。③ 監管挑戰。數字療法需要合規性監管,以確保安全和有效性。
筆者認為目前數字療法的難點包括:① 技術發展。數字療法需要不斷的技術創新和發展,以滿足患者需求。如在運動處方方面,美國運動醫學會指南是目前大多數腫瘤康復所遵循的指導方針[27-30],但運動訓練的選擇沒有考慮患者的腫瘤學背景[31]。因此數字療法在康復處方制定過程中仍需要完善,包括患者的個性化評估,除考慮患者的心肺適能或肌肉耐力外,還需關注患者的年齡、生活方式、運動偏好、既往治療等。② 文化和社會接受。文化和社會背景的不同可能影響患者對數字療法的接受程度,因此在臨床診療過程中醫務人員應結合病情,將數字療法與原先的診療方案進行結合。隨著技術的不斷發展,數字療法有望在未來繼續發揮重要作用,提供更多創新的治療方法,并改善醫療體驗。然而,需要處理相關的隱私、安全、文化和監管挑戰,以實現數字療法的潛在潛力。
4.3 數字療法在肝膽腫瘤中應用的展望
隨著技術的不斷發展,數字療法需要進一步整合人工智能和大數據分析,提供更精準的運動建議和治療方案。在關注腫瘤普遍存在的體適能恢復(旨在提升患者骨骼肌含量和心肺適能)的同時,數字療法也應該關注肝膽腫瘤及其圍手術期的特性,如肝癌圍手術期出現疼痛、惡心、嘔吐、腹瀉、乏力、營養不良、經濟負擔、焦慮、抑郁等不良反應[32],以及術后發生率較高的并發癥如胸腔積液、腹水、墜積性肺炎等。TACE聯合靶向免疫治療對中晚期肝癌的轉化治療是近年來的熱點關注領域[33-34],但患者在治療階段伴有的睡眠障礙、全身疲乏、肌力下降、注意力不集中、焦慮抑郁等情況較少獲得關注。針對肝癌患者的失眠問題,數字療法在未來可以從腦電波切入,將醫學治療和音樂助眠相結合進行干預,根據算法和大數據智能識別特征腦電波形和節律,精準識別睡眠階段并開展音樂療法,加速患者入睡[35];譬如肝癌患者長期惡病質導致營養不良,機體免疫力低下,再加上術后長期臥床、痰液淤積,均會增加術后肺部感染的發生率,而數字療法通過具有循證依據的肺康復鍛煉能減少肺部感染的進展[36]。
在運動處方的設計中,最常被忽視或低估的是休息和恢復。目前技術層面上該模塊僅通過醫生和患者的主觀判斷進行設定。未來有望在循證依據的指導下針對患者的生理指標和主觀感受,對休息與恢復的方式和時長進行設定[37]。因此,肝癌患者的術后康復需要實時地評估疾病與功能障礙的進展與演變,個性化給予治療方案,來促進疾病的有效轉歸以及運動功能的提高。
綜上所述,本案例提供較為創新的臨床治療策略和康復路徑,有助于臨床醫生對肝癌患者實施全周期康復;并對此類疾病的運動康復的思路和具體方法提供新途徑。今后將進一步開展更廣泛的臨床干預研究,形成可推廣的臨床康復方案。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:余愷濤主要負責臨床資料收集和論文撰寫,賈杰和殷保兵主要負責設計文章思路。
倫理聲明:本研究已通過復旦大學附屬華山醫院倫理審查委員會的審核批準(批文編號:2021-794)。