引用本文: 徐齡聰, 鄭燕, 龔天樂, 周永強, 閆潔熙, 丁方回, 李汛. 基于脂代謝標志物的肝細胞癌微血管浸潤術前預測模型的建立與驗證. 中國普外基礎與臨床雜志, 2024, 31(3): 320-329. doi: 10.7507/1007-9424.202310046 復制
版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
肝細胞肝癌(hepatocellular carcinoma,HCC)是原發性肝癌最主要的類型(占病例的75%~85%),是全球第6大常見癌癥疾病,是導致腫瘤相關死亡的第3大常見原因。據統計[1-3],2020年全球原發性肝癌新增病例90.6萬,死亡病例83萬,其相對5年生存率約為18%;其中,中國原發性肝癌新增病例41萬,死亡病例39.1萬。肝切除術是早期HCC患者的主要治療選擇,但術后高達80%的肝臟腫瘤復發率,嚴重影響了患者的預后[3]。多項研究[4-6]表明,微血管浸潤(microvascular invade,MVI)是HCC患者術后復發及不良預后的關鍵因素。術中通過寬手術切緣、解剖性切除等手術決策可以降低具有MVI HCC患者的復發率,有效延長患者的無病生存時間,擁有更好的長期預后[7-8]。然而,目前MVI結果只能通過手術切除標本的病理學檢查獲得,缺乏對手術的實際指導意義。準確而恰當的預測術前MVI,可以評估HCC患者MVI潛在的存在風險,將有助于外科醫師作出更佳的術前治療決策,改善HCC患者的手術結局。此外,HCC的MVI預測還對極早期肝癌的治療選擇和肝移植手術的器官分配優先級有幫助。根據歐洲肝臟研究協會(European Association for the Study of the Liver,EASL)肝癌臨床實踐指南[9]和Lee等[10]的研究,當我們為小肝癌患者選擇最佳治療方案時,MVI風險高的患者在初始治療分配時應該接受手術治療而不是射頻消融術。有研究[11-12]表明,MVI與肝移植術后的不良預后密切相關。如果有可靠的非侵入性MVI檢測方法可用,MVI的存在可能是肝移植的禁忌。
異常脂質代謝是HCC代謝重編程的重要特征,已被證實可通過調節炎癥反應和改變免疫微環境促進腫瘤的生長和侵襲[13-16]。然而,脂質代謝對MVI的確切影響尚不清楚。本研究在以往預測模型納入指標基礎上,新納入了脂質代謝(總膽固醇、甘油三酯、脂蛋白、載脂蛋白)、營養代謝 [體質量指數(body mass index,BMI)]、預后營養指數(prognostic nutritional index,PNI)和控制營養狀態(control nutritional status, CONUT)評分相關指標,探討上述指標在預測肝癌MVI發生風險方面的潛在價值,以確定是否應將這些因素納入到新模型中,改善對相關患者MVI風險的預測,完善預測模型的準確性,以增強其臨床效用,為制定臨床治療方案提供新的依據。
1 資料和方法
1.1 研究對象
回顧性納入蘭州大學第一醫院2017年1月至2023年3月期間行手術切除并經病理組織學檢查證實為HCC的572例患者的臨床病理資料。HCC的診斷遵循《原發性肝癌診療指南(2022 年版) 》 [17]。納入標準:① 年齡 ≥18歲且 ≤80歲;② 行肝切除術,術后病理學檢查證實為HCC患者;③ 無肝內主血管侵犯或遠處轉移。排除標準:① 合并其他腫瘤患者;② 術前行其他抗腫瘤相關治療患者;③ 多次行肝切除術患者;④ 臨床數據不完整或缺失的患者。
根據上述納入及排除標準,572例患者中最后有389例符合條件被納入本研究,并按手術時間以7∶3的比例分為2個獨立組: 2017年1月至2021年1月期間接受手術的272例患者被分配到訓練組建立預測模型,2021年2月至2023年4月期間接受手術的117例患者被分配到驗證組以驗證模型。本回顧性研究使用匿名數據,并獲得蘭州大學第一醫院倫理委員會的批準(批文編號:LDYYLL2023-290)。
1.2 術前評估及相關定義
1.2.1 常規評估指標
對所有患者在行肝切除術前2周內進行術前常規檢查評估,包括:患者基本資料、既往病史、腫瘤標志物、血常規、肝腎功、血脂、凝血功能及影像學檢查結果。經臨床評估后均行解剖性或非解剖性肝切除術,并由兩名病理科醫生對所有獲得的手術標本進行組織學評估,確定是否存在MVI。MVI的診斷遵循《原發性肝癌規范化病理診斷指南( 2015 年版) 》 [18]。
1.2.2 其他評估指標
所涉及的其他評估指標包括BMI、PNI、COUNT評分和白蛋白-膽紅素(albumin-bilirubin,ALBI)評分。各指標計算公式如下:BMI=體質量(kg)/[身高(cm)2];PNI=血清白蛋白水平(g/L)+5×外周血淋巴細胞計數(×109/L)。根據患者的血清白蛋白水平、外周血淋巴細胞計數和總膽固醇水平計算COUNT評分[19],并根據實驗室檢查結果為每個指標賦值。① 血清白蛋白水平: ≥35 g/L為 0分,30~34.9 g/L 為2分,25~29 g/L 為4分,<25 g/L 為6分。② 淋巴細胞計數 ≥1.600×109/L 為0分,(1.200~1.599)×109/L為1分,(0.800~1.199)×109/L 為2分,<0.800×109/L 為3分。③ 總膽固醇 ≥4.655 mmol/L為 0分,3.620~4.654 mmol/L為1分,2.586~3.619 mmol/L為2分,<2.585 mmol/L為3分。 ALBI評分的計算公式為:0.66 × log10(膽紅素μmol/L)?0.085 ×(白蛋白g/L),并根據計算結果將患者分為ALBI 1級(≤–2.60)、ALBI 2級(>–2.60~–1.39)和ALBI 3級(>–1.39)。所有納入指標的最佳截斷值均通過受試者工作特征(receiver operating characteristic curve,ROC)曲線和最大約登指數確定[20-21]。
1.3 統計學方法
分類變量以頻數和百分比表示,采用卡方檢驗進行比較。連續變量先進行Shapiro-Wilk正態性檢驗,符合正態分布者用均數±標準差( ±s)描述,組間比較采用t檢驗;偏態分布的定量數據用中位數(M)和上下四分位數(P25,P75)表示,并采用Wilcoxon秩和檢驗進行組間比較。采用單因素logistic回歸分析方法對訓練集中各變量的顯著性進行評估,以探討MVI的獨立危險因素,所有與MVI顯著相關的變量均作為向前逐步多因素分析的候選變量。根據多因素logistic回歸分析的結果,基于R中的“rms”軟件包(version 4.2.2)建立MVI的預測模型。用1 000個bootstrap重抽樣的方法來測量區分度(模型區分HCC患者有無MVI的能力),生成校準圖來測量校準度(MVI患者的預測概率與觀察頻率之間的一致性)。通過ROC曲線的最大約登指數(即敏感度+特異度–1)確定預測模型的最佳截斷值。通過敏感度、特異度、預測值和似然比評估最佳截止值的準確性。同時通過校準曲線、ROC曲線及決策曲線分析(decision curve analysis,DCA)來評估所構建模型的臨床應用價值和效能。所有統計分析使用IBM SPSS Statistics軟件(Version 25)和R(version 4.2.2)進行。檢驗水準α=0.05。
±s)描述,組間比較采用t檢驗;偏態分布的定量數據用中位數(M)和上下四分位數(P25,P75)表示,并采用Wilcoxon秩和檢驗進行組間比較。采用單因素logistic回歸分析方法對訓練集中各變量的顯著性進行評估,以探討MVI的獨立危險因素,所有與MVI顯著相關的變量均作為向前逐步多因素分析的候選變量。根據多因素logistic回歸分析的結果,基于R中的“rms”軟件包(version 4.2.2)建立MVI的預測模型。用1 000個bootstrap重抽樣的方法來測量區分度(模型區分HCC患者有無MVI的能力),生成校準圖來測量校準度(MVI患者的預測概率與觀察頻率之間的一致性)。通過ROC曲線的最大約登指數(即敏感度+特異度–1)確定預測模型的最佳截斷值。通過敏感度、特異度、預測值和似然比評估最佳截止值的準確性。同時通過校準曲線、ROC曲線及決策曲線分析(decision curve analysis,DCA)來評估所構建模型的臨床應用價值和效能。所有統計分析使用IBM SPSS Statistics軟件(Version 25)和R(version 4.2.2)進行。檢驗水準α=0.05。
2 結果
2.1 研究對象的基線資料
共389例符合納入及排除標準的HCC患者納入本研究。其中乙肝、丙肝、乙肝丙肝并存和無肝炎病毒感染患者的占比分別為77.9%(303/389)、4.1%(1/389)、1.8%(7/389)和16.2%(6/389)。訓練組272例,驗證組117例,2 組患者中分別有135例(49.6%)和61例(52.1%)經組織病理學檢查確定存在MVI。2組患者的基線臨床病理學特征相似,具體見表1。
2.2 MVI預測模型的建立和評估結果
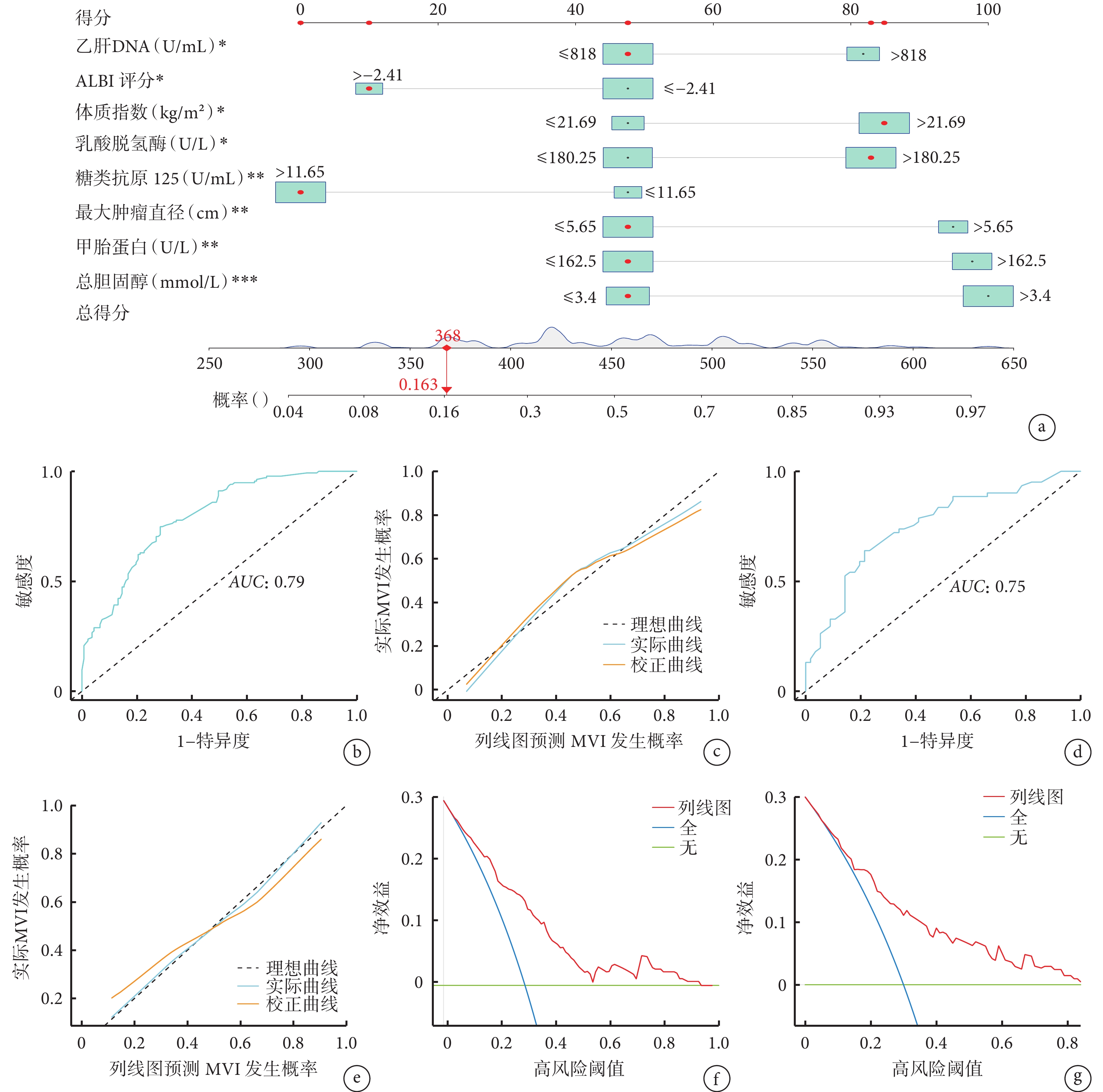
本研究納入分析的所有變量均基于術前獲得的數據。腫瘤直徑及數量均基于術前肝特異性核磁共振成像評估結果。在比較MVI陽性組和MVI陰性組之間的臨床病理學特征時,單因素logistic回歸分析結果顯示:年齡、總膽固醇、甘油三酯、高密度脂蛋白、低密度脂蛋白、載脂蛋白A1、載脂蛋白B、乳酸脫氫酶、谷草轉氨酶、白蛋白、總膽紅素、BMI、丙型肝炎、甲胎蛋白、糖類抗原125、乙肝DNA、C反應蛋白、血小板、淋巴細胞、單核細胞、凝血酶原時間、凝血酶原活動度、最大腫瘤直徑、ALBI評分、ALBI分級和PNI均與MVI有關(表2)。將所有與MVI相關的變量進一步行多因素logistic回歸分析,結果為:總膽固醇 >3.4 mmol/L、乳酸脫氫酶 >180.25 U/L、BMI >21.69 kg/m2、甲胎蛋白 >162.5 U/L、糖類抗原125 ≤11.65 U/mL、乙肝DNA >818 U/mL、最大腫瘤直徑 >5.65 cm和ALBI指數 ≤–2.41是MVI的獨立危險因素(表3)。根據上述獨立風險因素構建的MVI風險預測模型見圖1a,并使用bootstrap驗證方法對所建模型進行了內部驗證。 預測模型在估計MVI風險方面表現出良好的準確性,ROC曲線下面積為0.79,95%CI為(0.74,0.84),見圖1b。校準圖顯示了預測模型在對MVI的風險預測和手術標本的組織病理學驗證上存在良好的一致性(圖1c)。在驗證組中,顯示預測模型估計MVI風險的,ROC曲線下面積為0.75,95%CI為(0.66,0.84),見圖1d;驗證組對MVI的風險預測也有良好的校準曲線(圖1e)。DCA曲線顯示,預測模型在幾乎整個閾值概率范圍內具有高凈效益,表明預測模型具有較高的臨床應用獲益(圖1f和1g)。在最大約登指數下,預測模型ROC曲線的最佳截斷值被確定為0.48,根據該截斷值將HCC患者分為MVI存在的高風險組或低風險組,此時在訓練組中用于區分MVI存在與否的敏感度、特異度、陽性預測值和陰性預測值分別為74.8%、71.5%、72.1%和74.2%,在驗證組中分別為73.8%、64.3%、69.2%和69.2%(表4)。
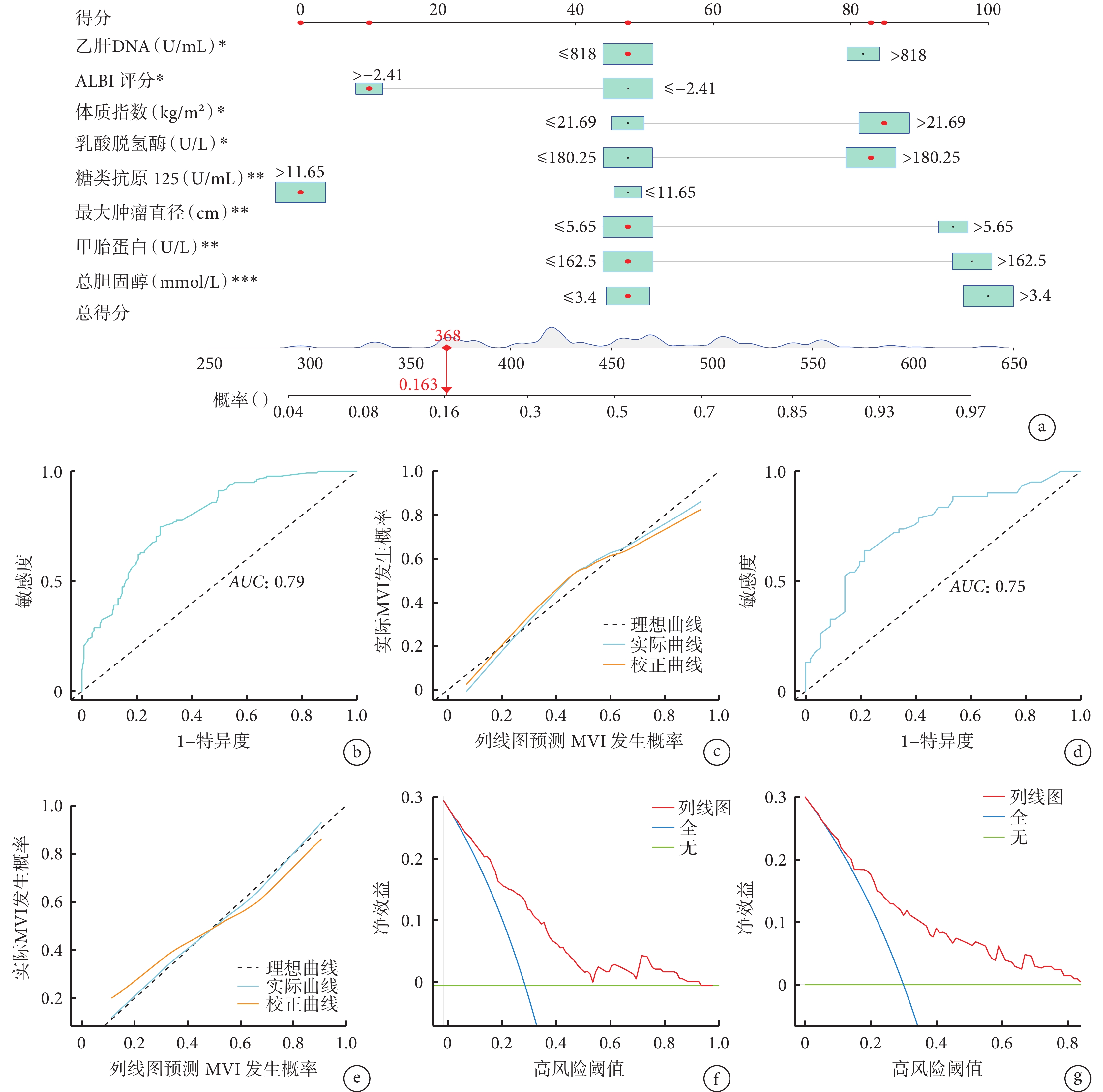 圖1
示術前預測MVI風險的預測模型及其預測效能驗證結果
圖1
示術前預測MVI風險的預測模型及其預測效能驗證結果
a:預測模型,*
3 討論
本研究基于脂質代謝相關指標構建并驗證了一種MVI存在風險的預測模型,風險指標包括總膽固醇、甲胎蛋白、腫瘤大小、糖類抗原125、乳酸脫氫酶、MBI、ALBI和乙肝病毒載量,用于術前預測HCC患者的MVI風險。本研究納入的389例HCC患者中有196例(50.4%)合并有MVI。
本研究主要選取血清學指標和簡單的影像學指標構建MVI預測模型。目前MVI預測模型中影像組學新報道較多,如Tian等[19]基于表觀彌散系數和肝膽期瘤周低信號2個指標建立了MVI預測模型,但該類模型的使用需要特定的計算機軟件;此外,影像學特征的識別易受放射科醫師的經驗和主觀診斷影響,限制了此類模型的臨床適用性,短時間內在臨床上難以得到較好的普及和應用。本研究建立的MVI預測模型,納入的8個術前變量較全面且易于獲得,在訓練組和驗證組中的ROC曲線下面積分別為0.79和0.77,校準曲線也顯示了預測與實際值之間的一致性。
在既往建立的MVI預測模型中,腫瘤體積大、高血清甲胎蛋白水平和高血清乙肝DNA載量已經被廣泛報道能增加HCC患者MVI的發生率[20-21]。本研究結果也顯示,上述這些因素的確與HCC的MVI顯著相關。此外本研究還發現,較高水平的總膽固醇(>3.4 mmol/L)、較高水平的BMI(>21.69 kg/m2)、較高水平的乳酸脫氫酶(>180.25 U/L)、較低水平的血清糖類抗原125(≤11.65 U/mL)與HCC患者MVI形成的可能性增加相關。
本研究結果顯示,較高水平的總膽固醇(>3.4 mmol/L)可促進HCC患者MVI的發生。盡管目前沒有關于總膽固醇水平和MVI之間存在關聯的報道,但在Kimura等[22]的研究結果提示,高脂肪、高蔗糖和高膽固醇飲食引起的總膽固醇等血脂升高會增加血管生成因子如血漿瘦素和單核細胞趨化蛋白-1 (monocyte chemotactic protein-1,MCP-1)的水平,降低抗血管生成因子脂聯素的水平,而且腫瘤中血管內皮生長因子(vascular endothelial growth factor,VEGF)、缺氧誘導因子-1α和MCP-1的表達水平均有所升高,這提示高脂血癥可能會影響血管生成因子與抗血管生成因子之間的表達水平,從而增強細胞侵襲和微血管形成。這些研究支持了本研究總膽固醇水平和MVI相關的這一臨床發現。在Yang等[23]的研究發現,他汀類藥物的使用顯著降低BCLC-0期或A期HCC患者復發的風險(HR=0.354,P<0.001)。這可能提示他汀類藥物通過降低總膽固醇以降低HCC細胞的侵襲性從而減少HCC的復發。若以上機制在后續研究中被證實,則可考慮將他汀類藥物作為HCC患者的輔助治療。
此外,本研究發現較高水平的BMI(>21.69 kg/m2)是HCC患者發生MVI的另一獨立危險因素。Mathur等[24]報道,超重(BMI ≥25 kg/m2)和肥胖(BMI ≥30 kg/m2)患者的肝移植后肝癌復發率是非肥胖患者(BMI <25 kg/m2)的2倍(P<0.05),復發時間也明顯縮短。這種效應可能是肥胖通過破壞脂聯素和瘦素水平之間的平衡,導致VEGF活性增加,從而刺激血管生成和腫瘤細胞增殖而增加MVI發生的風險。糖類抗原125作為一種腫瘤標志物在各種腫瘤中廣泛存在,在Huang等[25]的研究發現,糖類抗原125的敲低增強了HCC癌細胞的遷移和侵襲性,表明糖類抗原125在細胞介導的遷移和侵襲中具有抑制作用。Baert等[26]也報道了糖類抗原125與VEGF呈負相關關系(P=0.02)。這也與本研究結果一致,多因素logistic回歸分析表明,糖類抗原125 >11.65 U/mL的HCC患者發生MVI的風險較糖類抗原125較低的患者降低約61%。乳酸脫氫酶是一組代謝酶,主要催化丙酮酸至乳酸的可逆轉化,在癌癥代謝中起重要作用,通過增加糖酵解產物乳酸而酸化腫瘤微環境,促成反向pH梯度而增強腫瘤細胞的侵襲和轉移[27]。本研究還發現ALBI >-2.41是MVI的保護因素,顯著降低了MVI發生的風險。已有研究[28]表明,血清白蛋白可通過調節甲胎蛋白水平和激酶水平來調節腫瘤進展的動力學,低白蛋白水平與HCC高侵襲性和腫瘤復發密切相關。另一方面,血清膽紅素與炎性疾病和自身免疫性疾病的風險呈負相關,它通過減少氧化應激、減少炎性因子表達、抑制巨噬細胞和中性粒細胞計數發揮抗炎作用,從而抑制腫瘤細胞的增殖和侵襲[29-30]。
在本研究中,我們發現較高水平的總膽固醇(>3.4 mmol/L)、腫瘤體積大(>5.65 cm)、高血清甲胎蛋白水平(>162.5 U/L)、高血清乙肝DNA載量(>818 U/mL)、較高水平的BMI(>21.69 kg/m2)、較高水平的乳酸脫氫酶(>180.25 U/L)、較低水平的血清糖類抗原125(≤11.65 U/mL)和較低的ALBI(≤–2.41)8個因素與HCC患者MVI形成的可能性增加相關。并且總結了敏感度、特異度、陰性預測值和陽性預測值來輔助預測模型的臨床應用,根據模型的最佳截斷值可以將HCC患者分為MVI存在的高風險組或低風險組,幫助臨床醫生作出更佳的術前決策。同時,在HCC患者肝移植的適用性選擇和極早期肝癌患者的治療選擇時也可考慮使用本模型幫助決策,因為MVI的存在與否與以上患者的預后相關。此外,本研究所建模型中的指標簡單易得且不受醫生的主觀影響, 具有較為可靠穩定的預測效能,同時易于推廣應用。
本研究也存在一定的局限性:首先,該研究是基于單中心數據的回顧性研究,模型的可靠性還需要得到多中心、前瞻性、大樣本的驗證;其次,所納入分析的血清學指標的水平在一些情況下可能出現較大波動如感染、損傷或生命體征不穩定時,另外,臨床上這些血清學指標也會受到檢查時間、患者飲食、精神狀態等的影響。因此,如何避免或控制這些混雜因素來保持預測模型的準確性和穩定性仍需進一步研究。
4 結論
本研究將代謝相關的膽固醇參數、甲胎蛋白、腫瘤大小、糖類抗原125、乳酸脫氫酶、BMI、ALBI和乙肝病毒載量 8個影響MVI的危險因素相結合,構建了MVI的預測模型。該模型可為HCC患者MVI風險的術前評估提供評估標準,從而輔助醫生作出更合理的術前治療選擇。
重要聲明
利益沖突聲明: 本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:徐齡聰,研究構思與設計及撰寫文章;鄭燕、龔天樂和周永強,收集及整理數據;閆潔熙和丁方回,審閱及提出修改意見;李汛,指導研究。所有作者均審閱了此文稿并同意最終文稿。
倫理聲明:本研究通過了蘭州大學第一醫院醫學倫理委員會的審批,批文編號:LDYYLL2023-290。
肝細胞肝癌(hepatocellular carcinoma,HCC)是原發性肝癌最主要的類型(占病例的75%~85%),是全球第6大常見癌癥疾病,是導致腫瘤相關死亡的第3大常見原因。據統計[1-3],2020年全球原發性肝癌新增病例90.6萬,死亡病例83萬,其相對5年生存率約為18%;其中,中國原發性肝癌新增病例41萬,死亡病例39.1萬。肝切除術是早期HCC患者的主要治療選擇,但術后高達80%的肝臟腫瘤復發率,嚴重影響了患者的預后[3]。多項研究[4-6]表明,微血管浸潤(microvascular invade,MVI)是HCC患者術后復發及不良預后的關鍵因素。術中通過寬手術切緣、解剖性切除等手術決策可以降低具有MVI HCC患者的復發率,有效延長患者的無病生存時間,擁有更好的長期預后[7-8]。然而,目前MVI結果只能通過手術切除標本的病理學檢查獲得,缺乏對手術的實際指導意義。準確而恰當的預測術前MVI,可以評估HCC患者MVI潛在的存在風險,將有助于外科醫師作出更佳的術前治療決策,改善HCC患者的手術結局。此外,HCC的MVI預測還對極早期肝癌的治療選擇和肝移植手術的器官分配優先級有幫助。根據歐洲肝臟研究協會(European Association for the Study of the Liver,EASL)肝癌臨床實踐指南[9]和Lee等[10]的研究,當我們為小肝癌患者選擇最佳治療方案時,MVI風險高的患者在初始治療分配時應該接受手術治療而不是射頻消融術。有研究[11-12]表明,MVI與肝移植術后的不良預后密切相關。如果有可靠的非侵入性MVI檢測方法可用,MVI的存在可能是肝移植的禁忌。
異常脂質代謝是HCC代謝重編程的重要特征,已被證實可通過調節炎癥反應和改變免疫微環境促進腫瘤的生長和侵襲[13-16]。然而,脂質代謝對MVI的確切影響尚不清楚。本研究在以往預測模型納入指標基礎上,新納入了脂質代謝(總膽固醇、甘油三酯、脂蛋白、載脂蛋白)、營養代謝 [體質量指數(body mass index,BMI)]、預后營養指數(prognostic nutritional index,PNI)和控制營養狀態(control nutritional status, CONUT)評分相關指標,探討上述指標在預測肝癌MVI發生風險方面的潛在價值,以確定是否應將這些因素納入到新模型中,改善對相關患者MVI風險的預測,完善預測模型的準確性,以增強其臨床效用,為制定臨床治療方案提供新的依據。
1 資料和方法
1.1 研究對象
回顧性納入蘭州大學第一醫院2017年1月至2023年3月期間行手術切除并經病理組織學檢查證實為HCC的572例患者的臨床病理資料。HCC的診斷遵循《原發性肝癌診療指南(2022 年版) 》 [17]。納入標準:① 年齡 ≥18歲且 ≤80歲;② 行肝切除術,術后病理學檢查證實為HCC患者;③ 無肝內主血管侵犯或遠處轉移。排除標準:① 合并其他腫瘤患者;② 術前行其他抗腫瘤相關治療患者;③ 多次行肝切除術患者;④ 臨床數據不完整或缺失的患者。
根據上述納入及排除標準,572例患者中最后有389例符合條件被納入本研究,并按手術時間以7∶3的比例分為2個獨立組: 2017年1月至2021年1月期間接受手術的272例患者被分配到訓練組建立預測模型,2021年2月至2023年4月期間接受手術的117例患者被分配到驗證組以驗證模型。本回顧性研究使用匿名數據,并獲得蘭州大學第一醫院倫理委員會的批準(批文編號:LDYYLL2023-290)。
1.2 術前評估及相關定義
1.2.1 常規評估指標
對所有患者在行肝切除術前2周內進行術前常規檢查評估,包括:患者基本資料、既往病史、腫瘤標志物、血常規、肝腎功、血脂、凝血功能及影像學檢查結果。經臨床評估后均行解剖性或非解剖性肝切除術,并由兩名病理科醫生對所有獲得的手術標本進行組織學評估,確定是否存在MVI。MVI的診斷遵循《原發性肝癌規范化病理診斷指南( 2015 年版) 》 [18]。
1.2.2 其他評估指標
所涉及的其他評估指標包括BMI、PNI、COUNT評分和白蛋白-膽紅素(albumin-bilirubin,ALBI)評分。各指標計算公式如下:BMI=體質量(kg)/[身高(cm)2];PNI=血清白蛋白水平(g/L)+5×外周血淋巴細胞計數(×109/L)。根據患者的血清白蛋白水平、外周血淋巴細胞計數和總膽固醇水平計算COUNT評分[19],并根據實驗室檢查結果為每個指標賦值。① 血清白蛋白水平: ≥35 g/L為 0分,30~34.9 g/L 為2分,25~29 g/L 為4分,<25 g/L 為6分。② 淋巴細胞計數 ≥1.600×109/L 為0分,(1.200~1.599)×109/L為1分,(0.800~1.199)×109/L 為2分,<0.800×109/L 為3分。③ 總膽固醇 ≥4.655 mmol/L為 0分,3.620~4.654 mmol/L為1分,2.586~3.619 mmol/L為2分,<2.585 mmol/L為3分。 ALBI評分的計算公式為:0.66 × log10(膽紅素μmol/L)?0.085 ×(白蛋白g/L),并根據計算結果將患者分為ALBI 1級(≤–2.60)、ALBI 2級(>–2.60~–1.39)和ALBI 3級(>–1.39)。所有納入指標的最佳截斷值均通過受試者工作特征(receiver operating characteristic curve,ROC)曲線和最大約登指數確定[20-21]。
1.3 統計學方法
分類變量以頻數和百分比表示,采用卡方檢驗進行比較。連續變量先進行Shapiro-Wilk正態性檢驗,符合正態分布者用均數±標準差( ±s)描述,組間比較采用t檢驗;偏態分布的定量數據用中位數(M)和上下四分位數(P25,P75)表示,并采用Wilcoxon秩和檢驗進行組間比較。采用單因素logistic回歸分析方法對訓練集中各變量的顯著性進行評估,以探討MVI的獨立危險因素,所有與MVI顯著相關的變量均作為向前逐步多因素分析的候選變量。根據多因素logistic回歸分析的結果,基于R中的“rms”軟件包(version 4.2.2)建立MVI的預測模型。用1 000個bootstrap重抽樣的方法來測量區分度(模型區分HCC患者有無MVI的能力),生成校準圖來測量校準度(MVI患者的預測概率與觀察頻率之間的一致性)。通過ROC曲線的最大約登指數(即敏感度+特異度–1)確定預測模型的最佳截斷值。通過敏感度、特異度、預測值和似然比評估最佳截止值的準確性。同時通過校準曲線、ROC曲線及決策曲線分析(decision curve analysis,DCA)來評估所構建模型的臨床應用價值和效能。所有統計分析使用IBM SPSS Statistics軟件(Version 25)和R(version 4.2.2)進行。檢驗水準α=0.05。
±s)描述,組間比較采用t檢驗;偏態分布的定量數據用中位數(M)和上下四分位數(P25,P75)表示,并采用Wilcoxon秩和檢驗進行組間比較。采用單因素logistic回歸分析方法對訓練集中各變量的顯著性進行評估,以探討MVI的獨立危險因素,所有與MVI顯著相關的變量均作為向前逐步多因素分析的候選變量。根據多因素logistic回歸分析的結果,基于R中的“rms”軟件包(version 4.2.2)建立MVI的預測模型。用1 000個bootstrap重抽樣的方法來測量區分度(模型區分HCC患者有無MVI的能力),生成校準圖來測量校準度(MVI患者的預測概率與觀察頻率之間的一致性)。通過ROC曲線的最大約登指數(即敏感度+特異度–1)確定預測模型的最佳截斷值。通過敏感度、特異度、預測值和似然比評估最佳截止值的準確性。同時通過校準曲線、ROC曲線及決策曲線分析(decision curve analysis,DCA)來評估所構建模型的臨床應用價值和效能。所有統計分析使用IBM SPSS Statistics軟件(Version 25)和R(version 4.2.2)進行。檢驗水準α=0.05。
2 結果
2.1 研究對象的基線資料
共389例符合納入及排除標準的HCC患者納入本研究。其中乙肝、丙肝、乙肝丙肝并存和無肝炎病毒感染患者的占比分別為77.9%(303/389)、4.1%(1/389)、1.8%(7/389)和16.2%(6/389)。訓練組272例,驗證組117例,2 組患者中分別有135例(49.6%)和61例(52.1%)經組織病理學檢查確定存在MVI。2組患者的基線臨床病理學特征相似,具體見表1。
2.2 MVI預測模型的建立和評估結果
本研究納入分析的所有變量均基于術前獲得的數據。腫瘤直徑及數量均基于術前肝特異性核磁共振成像評估結果。在比較MVI陽性組和MVI陰性組之間的臨床病理學特征時,單因素logistic回歸分析結果顯示:年齡、總膽固醇、甘油三酯、高密度脂蛋白、低密度脂蛋白、載脂蛋白A1、載脂蛋白B、乳酸脫氫酶、谷草轉氨酶、白蛋白、總膽紅素、BMI、丙型肝炎、甲胎蛋白、糖類抗原125、乙肝DNA、C反應蛋白、血小板、淋巴細胞、單核細胞、凝血酶原時間、凝血酶原活動度、最大腫瘤直徑、ALBI評分、ALBI分級和PNI均與MVI有關(表2)。將所有與MVI相關的變量進一步行多因素logistic回歸分析,結果為:總膽固醇 >3.4 mmol/L、乳酸脫氫酶 >180.25 U/L、BMI >21.69 kg/m2、甲胎蛋白 >162.5 U/L、糖類抗原125 ≤11.65 U/mL、乙肝DNA >818 U/mL、最大腫瘤直徑 >5.65 cm和ALBI指數 ≤–2.41是MVI的獨立危險因素(表3)。根據上述獨立風險因素構建的MVI風險預測模型見圖1a,并使用bootstrap驗證方法對所建模型進行了內部驗證。 預測模型在估計MVI風險方面表現出良好的準確性,ROC曲線下面積為0.79,95%CI為(0.74,0.84),見圖1b。校準圖顯示了預測模型在對MVI的風險預測和手術標本的組織病理學驗證上存在良好的一致性(圖1c)。在驗證組中,顯示預測模型估計MVI風險的,ROC曲線下面積為0.75,95%CI為(0.66,0.84),見圖1d;驗證組對MVI的風險預測也有良好的校準曲線(圖1e)。DCA曲線顯示,預測模型在幾乎整個閾值概率范圍內具有高凈效益,表明預測模型具有較高的臨床應用獲益(圖1f和1g)。在最大約登指數下,預測模型ROC曲線的最佳截斷值被確定為0.48,根據該截斷值將HCC患者分為MVI存在的高風險組或低風險組,此時在訓練組中用于區分MVI存在與否的敏感度、特異度、陽性預測值和陰性預測值分別為74.8%、71.5%、72.1%和74.2%,在驗證組中分別為73.8%、64.3%、69.2%和69.2%(表4)。
 圖1
示術前預測MVI風險的預測模型及其預測效能驗證結果
圖1
示術前預測MVI風險的預測模型及其預測效能驗證結果
a:預測模型,*
3 討論
本研究基于脂質代謝相關指標構建并驗證了一種MVI存在風險的預測模型,風險指標包括總膽固醇、甲胎蛋白、腫瘤大小、糖類抗原125、乳酸脫氫酶、MBI、ALBI和乙肝病毒載量,用于術前預測HCC患者的MVI風險。本研究納入的389例HCC患者中有196例(50.4%)合并有MVI。
本研究主要選取血清學指標和簡單的影像學指標構建MVI預測模型。目前MVI預測模型中影像組學新報道較多,如Tian等[19]基于表觀彌散系數和肝膽期瘤周低信號2個指標建立了MVI預測模型,但該類模型的使用需要特定的計算機軟件;此外,影像學特征的識別易受放射科醫師的經驗和主觀診斷影響,限制了此類模型的臨床適用性,短時間內在臨床上難以得到較好的普及和應用。本研究建立的MVI預測模型,納入的8個術前變量較全面且易于獲得,在訓練組和驗證組中的ROC曲線下面積分別為0.79和0.77,校準曲線也顯示了預測與實際值之間的一致性。
在既往建立的MVI預測模型中,腫瘤體積大、高血清甲胎蛋白水平和高血清乙肝DNA載量已經被廣泛報道能增加HCC患者MVI的發生率[20-21]。本研究結果也顯示,上述這些因素的確與HCC的MVI顯著相關。此外本研究還發現,較高水平的總膽固醇(>3.4 mmol/L)、較高水平的BMI(>21.69 kg/m2)、較高水平的乳酸脫氫酶(>180.25 U/L)、較低水平的血清糖類抗原125(≤11.65 U/mL)與HCC患者MVI形成的可能性增加相關。
本研究結果顯示,較高水平的總膽固醇(>3.4 mmol/L)可促進HCC患者MVI的發生。盡管目前沒有關于總膽固醇水平和MVI之間存在關聯的報道,但在Kimura等[22]的研究結果提示,高脂肪、高蔗糖和高膽固醇飲食引起的總膽固醇等血脂升高會增加血管生成因子如血漿瘦素和單核細胞趨化蛋白-1 (monocyte chemotactic protein-1,MCP-1)的水平,降低抗血管生成因子脂聯素的水平,而且腫瘤中血管內皮生長因子(vascular endothelial growth factor,VEGF)、缺氧誘導因子-1α和MCP-1的表達水平均有所升高,這提示高脂血癥可能會影響血管生成因子與抗血管生成因子之間的表達水平,從而增強細胞侵襲和微血管形成。這些研究支持了本研究總膽固醇水平和MVI相關的這一臨床發現。在Yang等[23]的研究發現,他汀類藥物的使用顯著降低BCLC-0期或A期HCC患者復發的風險(HR=0.354,P<0.001)。這可能提示他汀類藥物通過降低總膽固醇以降低HCC細胞的侵襲性從而減少HCC的復發。若以上機制在后續研究中被證實,則可考慮將他汀類藥物作為HCC患者的輔助治療。
此外,本研究發現較高水平的BMI(>21.69 kg/m2)是HCC患者發生MVI的另一獨立危險因素。Mathur等[24]報道,超重(BMI ≥25 kg/m2)和肥胖(BMI ≥30 kg/m2)患者的肝移植后肝癌復發率是非肥胖患者(BMI <25 kg/m2)的2倍(P<0.05),復發時間也明顯縮短。這種效應可能是肥胖通過破壞脂聯素和瘦素水平之間的平衡,導致VEGF活性增加,從而刺激血管生成和腫瘤細胞增殖而增加MVI發生的風險。糖類抗原125作為一種腫瘤標志物在各種腫瘤中廣泛存在,在Huang等[25]的研究發現,糖類抗原125的敲低增強了HCC癌細胞的遷移和侵襲性,表明糖類抗原125在細胞介導的遷移和侵襲中具有抑制作用。Baert等[26]也報道了糖類抗原125與VEGF呈負相關關系(P=0.02)。這也與本研究結果一致,多因素logistic回歸分析表明,糖類抗原125 >11.65 U/mL的HCC患者發生MVI的風險較糖類抗原125較低的患者降低約61%。乳酸脫氫酶是一組代謝酶,主要催化丙酮酸至乳酸的可逆轉化,在癌癥代謝中起重要作用,通過增加糖酵解產物乳酸而酸化腫瘤微環境,促成反向pH梯度而增強腫瘤細胞的侵襲和轉移[27]。本研究還發現ALBI >-2.41是MVI的保護因素,顯著降低了MVI發生的風險。已有研究[28]表明,血清白蛋白可通過調節甲胎蛋白水平和激酶水平來調節腫瘤進展的動力學,低白蛋白水平與HCC高侵襲性和腫瘤復發密切相關。另一方面,血清膽紅素與炎性疾病和自身免疫性疾病的風險呈負相關,它通過減少氧化應激、減少炎性因子表達、抑制巨噬細胞和中性粒細胞計數發揮抗炎作用,從而抑制腫瘤細胞的增殖和侵襲[29-30]。
在本研究中,我們發現較高水平的總膽固醇(>3.4 mmol/L)、腫瘤體積大(>5.65 cm)、高血清甲胎蛋白水平(>162.5 U/L)、高血清乙肝DNA載量(>818 U/mL)、較高水平的BMI(>21.69 kg/m2)、較高水平的乳酸脫氫酶(>180.25 U/L)、較低水平的血清糖類抗原125(≤11.65 U/mL)和較低的ALBI(≤–2.41)8個因素與HCC患者MVI形成的可能性增加相關。并且總結了敏感度、特異度、陰性預測值和陽性預測值來輔助預測模型的臨床應用,根據模型的最佳截斷值可以將HCC患者分為MVI存在的高風險組或低風險組,幫助臨床醫生作出更佳的術前決策。同時,在HCC患者肝移植的適用性選擇和極早期肝癌患者的治療選擇時也可考慮使用本模型幫助決策,因為MVI的存在與否與以上患者的預后相關。此外,本研究所建模型中的指標簡單易得且不受醫生的主觀影響, 具有較為可靠穩定的預測效能,同時易于推廣應用。
本研究也存在一定的局限性:首先,該研究是基于單中心數據的回顧性研究,模型的可靠性還需要得到多中心、前瞻性、大樣本的驗證;其次,所納入分析的血清學指標的水平在一些情況下可能出現較大波動如感染、損傷或生命體征不穩定時,另外,臨床上這些血清學指標也會受到檢查時間、患者飲食、精神狀態等的影響。因此,如何避免或控制這些混雜因素來保持預測模型的準確性和穩定性仍需進一步研究。
4 結論
本研究將代謝相關的膽固醇參數、甲胎蛋白、腫瘤大小、糖類抗原125、乳酸脫氫酶、BMI、ALBI和乙肝病毒載量 8個影響MVI的危險因素相結合,構建了MVI的預測模型。該模型可為HCC患者MVI風險的術前評估提供評估標準,從而輔助醫生作出更合理的術前治療選擇。
重要聲明
利益沖突聲明: 本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:徐齡聰,研究構思與設計及撰寫文章;鄭燕、龔天樂和周永強,收集及整理數據;閆潔熙和丁方回,審閱及提出修改意見;李汛,指導研究。所有作者均審閱了此文稿并同意最終文稿。
倫理聲明:本研究通過了蘭州大學第一醫院醫學倫理委員會的審批,批文編號:LDYYLL2023-290。