引用本文: 劉肖鳳, 侯圣忠, 黃興, 田伯樂. 膽固醇代謝在胰腺導管腺癌發生發展及診療中的研究進展. 中國普外基礎與臨床雜志, 2024, 31(6): 754-760. doi: 10.7507/1007-9424.202312071 復制
版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
胰腺導管腺癌(pancreatic ductal adenocarcinoma,PDAC)因其高致死率,稱為“癌中之王” 。最新癌癥統計顯示,PDAC新發病例數位居前10,有逐年上升的趨勢,且PDAC死亡病例數居第3位;經過多年的努力,PDAC的5年生存率仍然處于最低水平,僅為13%[1]。在中國,PDAC新發病例數居第8位,死亡病例數居第6位[2]。PDAC的發病率以每年0.5%~10%的增長率將于2030年成為第二大癌癥相關死亡原因[3]。PDAC高死亡率的主要原因除了高度惡性的生物學行為外,還在于缺乏早期診斷手段,將近一半的病例在診斷時已處于晚期,失去了根治性手術這唯一可能治愈該疾病的機會,只有13%的病例能夠得到根治性手術治療[3-4]。目前用于幫助診斷PDAC的生物標志物主要是CA19-9,但是其敏感度及特異度均不高。盡管在過去的幾十年里出現了幾種治療方法,如化療、放射治療、免疫治療和靶向治療,但其效果仍然不理想,比如作為治療晚期PDAC的一線藥物吉西他濱已經在PDAC的治療中有20多年歷史,但并未顯著提升其生存率,耐藥是其主要原因[5]。因此,探索PDAC發生和發展的分子機制,發現新的靶點和開發有效的治療策略勢在必行。越來越多的研究表明,膽固醇代謝在腫瘤細胞的增殖、侵襲、遷移等惡性生物學行為中具有重要作用[6-7]。因此,筆者現就膽固醇代謝重塑在PDAC發生發展中的研究進展作一綜述,并總結膽固醇代謝重塑與PDAC早期診斷、靶向治療以及協同治療的相關研究,旨在為未來PDAC的研究與診療提供思路。
1 膽固醇代謝及重塑
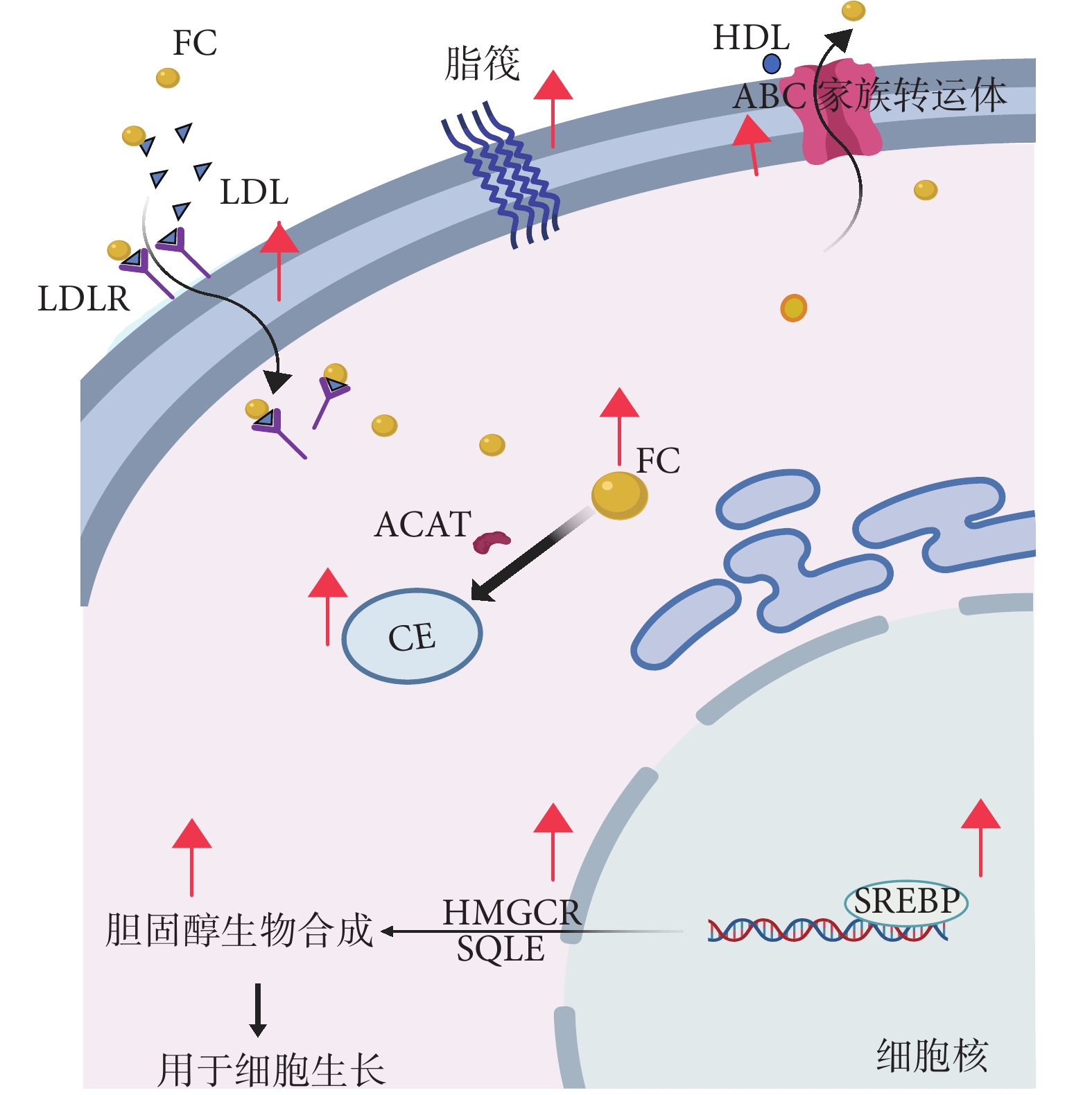
膽固醇是真核細胞生存必需物質之一,是組成細胞內膜性結構的重要成分。膽固醇相關代謝產物也是重要的信號傳遞分子。目前細胞獲取膽固醇主要通過兩條途徑,一是甲羥戊酸從頭合成途徑:2個乙酰輔酶A分子通過一系列縮合反應形成甲羥戊酸,這個過程中甲羥戊酸鹽還原酶(3-hydroxy-3-methylglutaryl-coenzyme A reductase,HMGCR)是主要限速酶;合成甲羥戊酸之后通過一系列的酶促反應形成焦磷酸法尼酯、角鯊烯等,最終形成膽固醇。另一途徑是細胞直接攝取,也是主要的途徑:食物中的膽固醇進入人體循環與低密度脂蛋白(low density lipoprotein,LDL)結合轉運,然后與細胞膜表面的低密度脂蛋白受體(low density lipoprotein receptor,LDLR)相結合,通過細胞內吞作用進入細胞。細胞內膽固醇水平是動態變化的。剩余的膽固醇酯化后儲存于脂筏中,或者是通過膽固醇外流轉運出細胞。在這個復雜的動態代謝過程中有多種酶或者受體直接介導。膽固醇外流過程主要借助于ATP結合盒(ATP-binding cassette,ABC)家族轉運體,如ABCA1、ABCG1、ABCG5以及ABCG8,還借助于細胞外高密度脂蛋白(high density lipoprotein,HDL)的輔助轉運[8]。此外,膽固醇通過酰基輔酶A:膽固醇酰基轉移酶(acyl-coenzyme A: cholesterol acyltransferases,ACATs)酯化為低毒性的膽固醇酯(cholesterol ester,CE)儲存于脂滴或脂筏中。細胞內膽固醇內源性合成、內吞、外流或者合成膽固醇酯均受到細胞內轉錄因子信號調控,主要包括固醇調節元件結合蛋白-2(steroid regulatory element-binding protein-2, SREBP-2)、肝X受體(lver X receptors,LXRs)、核因子紅系2相關因子1(nuclear factor-erythroid 2 related factor 1,NRF1)等。SREBP-2是特定調控膽固醇合成及轉運的轉錄因子,屬于SREBPs轉錄因子家族之一,該家族主要通過控制內源性膽固醇、脂肪酸、三酰甘油和磷脂合成所需的一系列酶的表達來調節脂質穩態。LXRs主要包括LXRα和LXRβ,可通過調控膽固醇外流相關基因(如ABCA1、ABCG1等)的表達介導細胞內膽固醇的動態平衡,此外還可通過靶向SRFBPs轉錄因子影響膽固醇的合成途徑等。細胞內膽固醇還通過NRF1解除對LXRs通路的抑制作用,促進膽固醇的動態外流。此外,還有其他轉錄因子或輔轉錄因子通過介導靶基因轉錄進而調控膽固醇平衡,如載脂蛋白A-1結合蛋白通過激活SREBP-2介導膽固醇外流[9]。肝臟中特異表達的亞洲糖蛋白受體1的缺失通過穩定LXRα,上調ABCA1和ABCG5/G8,分別促進膽固醇向HDL的轉運和向膽汁及糞便的排泄,從而降低血清和肝臟中的脂質水平[10]。核受體共抑制因子-維甲酸和甲狀腺激素受體沉默介質,一種輔抑制因子復合物通過結合轉錄因子調控靶基因的表達,如該復合物結合LXRs形成復合物介導ABCA1及SREBP-1基因表達調控膽固醇平衡,或其復合物亞體,G蛋白通路抑制因子2,通過結合LXRs形成轉錄調控復合物共同調控ABCG1介導膽固醇外流。磷脂酰肌醇3激酶/蛋白激酶B(phosphatidylinositol 3 kinase/protein kinase B, PI3K/PKB,PI3K/AKT)信號通路通過調控SREBP-1以及其靶向基因的表達調控脂質水平維持細胞的生長。因此,膽固醇代謝是一動態且復雜的調控通路,多條調控通路協同確保細胞生長所必需的營養物質及信號分子,而當細胞發生病理變化如癌變時,這一動態平衡將受到重塑以滿足癌變細胞的特殊需求,此即膽固醇代謝重塑(圖1)。
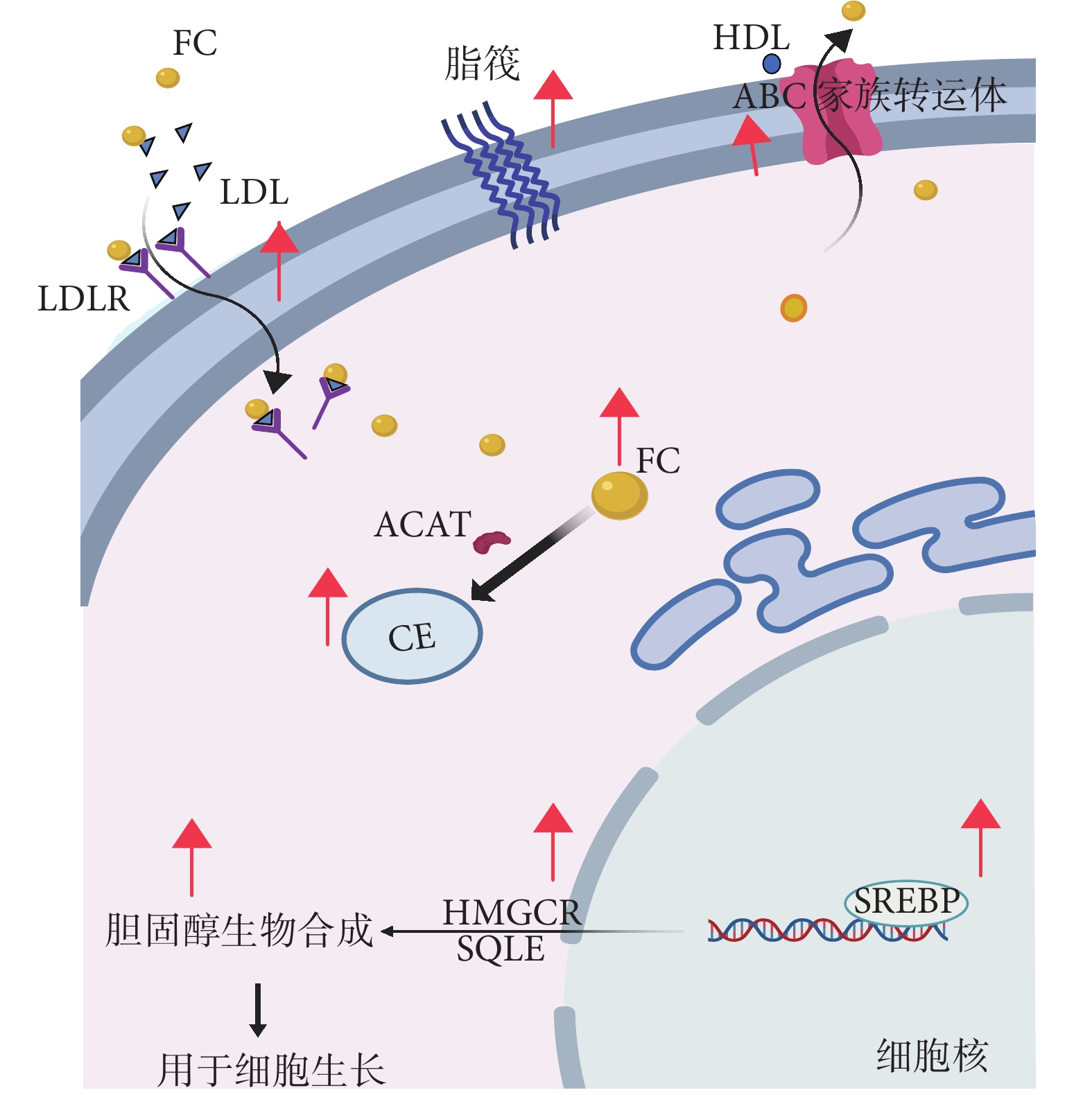 圖1
示膽固醇代謝重塑過程
圖1
示膽固醇代謝重塑過程
2 膽固醇代謝重塑與PDAC的發生發展
2.1 血清膽固醇
目前,有較多研究探討了血清膽固醇在預測PDAC發生風險、早期診斷及評估生存方面的應用。近年一項病例對照研究[11]發現,高總膽固醇可能表明胰腺癌的發病率較低,總膽固醇的下降可能表明胰腺癌的發病率較高,且低膽固醇合并糖尿病表明胰腺癌的發病率更高。這與PDAC患者診斷為糖尿病時多合并低總膽固醇相一致[12]。血清膽固醇也可用于預測空腹血糖受損患者的PDAC風險[13]。除此之外,較高的術前堿性磷酸酶/總膽固醇比率是根治性手術切除后PDAC患者較差生存的獨立預后因素[14]。 另有研究[15-16]卻發現,胰腺癌患者血清膽固醇及LDL水平較高,HDL水平較低,且與胰腺癌預后關系不大,LDLR高水平可能預示胰腺癌生存不良。
綜上,目前的臨床研究結果表明,血清膽固醇在PDAC的臨床應用價值是矛盾的,仍需要大量前瞻性臨床研究進一步深入挖掘血清膽固醇在PDAC風險評估、早期診斷及預后方面的應用價值。
2.2 膽固醇代謝重塑與PDAC
腫瘤組織以及腫瘤細胞內膽固醇代謝與人體血清膽固醇的差異表明膽固醇代謝的重要性。近年來,越來越多的研究探討膽固醇代謝包括膽固醇從頭合成、獲取、外流、酯化等過程的重塑在PDAC發生發展中的作用。
在膽固醇的合成途徑方面,膽固醇從頭合成基因及相關酶在PDAC中呈高表達,與癌旁的正常胰腺組織相比,胰腺腫瘤中的游離膽固醇含量顯著升高,且與PDAC患者的較差生存相關[16-19]。膽固醇合成代謝關鍵酶HMGCR在PDAC腫瘤細胞內呈高表達,抑制HMGCR增加了PDAC腫瘤細胞的死亡[20]。有研究發現,鋅指結構反義轉錄本1作為胰腺癌的癌基因,通過與胰腺癌中的輔助因子結合,穩定HMGCR的表達,是胰腺癌診斷和治療的候選靶點[21]。角鯊烯環氧酶(squalene epoxidase,SQLE)是膽固醇合成代謝中的第二限速酶,SQLE通過減輕內質網應激和激活脂筏調節的病毒癌基因/磷脂酰肌醇3激酶/蛋白激酶B(sarcoma/Phosphatidylinositol 3 kinase/protein kinase B,Src/PI3K/Akt)信號通路或激活哺乳動物雷帕霉素靶蛋白復合體1(mammalian target of rapamycin complex 1,mTORC1)和腫瘤壞死因子α/核因子-κB信號通路促進腫瘤生長。應用SQLE抑制劑如特比萘芬[22]或敲低SQLE[17]可以有效抑制胰腺癌細胞的增殖生長。SQLE抑制劑也能夠增強鉑類、吉西他濱和5-氟尿嘧啶對PDAC腫瘤細胞的敏感性[22]。人-微小核糖核酸-363-3p(human serum albumin-microRNA-363-3p, HSA-mir-363-3p)被認為是調節SQLE表達的關鍵microRNA,從而影響PDAC患者的預后[19]。2,3-氧化角鯊烯環化酶抑制劑8-8071在體內及體外降低p27、細胞周期蛋白 B1和細胞周期蛋白 E的表達及c-Jun氨基末端激酶(c-Jun N-terminal kinase,JNK)和細胞外調節蛋白激酶的磷酸化水平來抑制PANC-1細胞的活力,誘導細胞周期停滯在G1期[23]。在PDAC小鼠模型以及體外人PDAC細胞株中也表現腫瘤局部高膽固醇水平[16]。除此之外,還有研究[18]表明,遠離惡性細胞的區域就已經顯示出膽固醇代謝重塑,這些變化影響預后并可能成為藥物靶點。并且發現膽固醇合成途徑的基因,比如法尼基二磷酸法尼基轉移酶1基因的表達升高時,胰腺癌患者具有較差的生存[16-17]。
高膽固醇水平可促進PDAC的發生發展。例如,膽固醇與Wnt/β-連環蛋白信號通路卷曲蛋白5(Frizzled5,Fzd5)受體相結合激活β-連環蛋白分子及核內蓄積,進而通過結合轉錄因子促進下游靶基因的轉錄影響PDAC細胞的增殖,而25-羥基膽固醇能夠靶向抑制膽固醇與內質網表面Fzd5的結合抑制下一步信號通路激活[24]。并且膽固醇還促進PDAC腫瘤微環境的形成[25]。膽固醇25-羥基酶是一種能將膽固醇轉化為25-羥基膽固醇的酶,參與抑制膽固醇的生物合成和膽固醇的消耗。膽固醇25-羥基酶在胰腺癌細胞中表觀基因下調促進免疫逃避和腫瘤生長[26]。
一些廣泛使用的膽固醇靶向藥物,如治療血脂異常的他汀類藥物,可能會潛在地影響癌細胞中的膽固醇代謝[27-28]。辛伐他汀通過抑制HMGCR、聲波刺猬蛋白(sonic hedgehog, Shh)信號通路或通過激活JNK途徑降低Yes相關蛋白結合基序的表達抑制PDAC細胞存活、增殖、遷移和侵襲[20, 29-30]。辛伐他汀和吉西他濱聯合治療顯著減少了腫瘤內細胞程序性死亡-配體1(programmed cell death 1 ligand 1,PD-L1)的表達,顯著降低了總體腫瘤負擔和轉移發生率[31],且辛伐他汀與奧沙利鉑或抗程序性死亡受體1(Programmed cell death 1,PD-1)藥物聯合作用時表現出相加的抗生長作用[30]。也有研究表明,低劑量二甲雙胍和辛伐他汀聯合治療抑制PDAC的發展[32];匹伐他汀聯合二甲雙胍能激活單磷酸腺苷依賴的蛋白激酶,抑制PI3K/mTOR信號通路,展現出協同抗癌效果[33];洛伐他汀通過抑制質膜和線粒體中的膽固醇脂筏誘導人PDAC細胞凋亡[34]。上述研究表明,雖然同為他汀類藥物,均表現出其抑制PDAC腫瘤細胞的增殖,但其機制不盡相同[35]。除聯合應用并增敏化療藥物效果外,靶向膽固醇代謝也可促進放療敏感性。如唑來膦酸通過抑制膽固醇合成途徑的法尼基二磷酸合成酶提高PDAC化療敏感性。體內體外研究表明唑來膦酸通過影響Ras相關的C3肉毒素底物1和Ras相似物(Ras homologue,Rho)的戊烯化,從而調節DNA損傷和輻射反應信號,并改善系統免疫細胞促進放療敏感性[36]。
在膽固醇攝取途徑方面,LDLR參與膽固醇攝取,是調控膽固醇穩態重要的跨膜受體。LDLR在PDAC腫瘤細胞內呈高表達[20]。枯草桿菌前蛋白轉換酶9(proprotein convertase subtilisin/kexin type 9,PCSK9)可通過結合LDLR,促進LDLR的降解。具有抗LDL聚集特性的多肽可能具有抗PDAC作用[37]。PCSK9與FOLFIRINOX聯合治療轉移性胰腺癌處于臨床前研究階段[38]。LDL協同膽固醇轉運,其高表達促進癌細胞的增殖、侵襲及轉移,機制上,LDL的高表達激活大量的信號傳導和轉錄激活子3(sgnal transduction and transcription activator 3,STAT3)、Janus激酶1/Janus激酶2(Janus kinase 1/Janus kinase 2,JAK1/JAK2)及酪氨酸蛋白激酶,對于STAT3缺失的PDAC腫瘤細胞有降低LDL的作用[39]。
ABCG2、ABCB1、ABCC1-4等ABC轉運蛋白被認為與多藥耐藥有關[40-41]。HSA-miR-3178通過RhoB/PI3K/Akt信號通路上調ABC轉運蛋白表達,促進吉西他濱耐藥。這些發現提示HSA-miR-3178可能成為克服胰腺癌吉西他濱耐藥的新的治療靶點[42]。胞漿ABCC8蛋白表達對PDAC有預后價值[43]。此外,通過包裝HDL,介導細胞內膽固醇外流,降低細胞內總膽固醇水平,亦能抑制PDAC腫瘤細胞的增殖活性[44]。
與其他腫瘤一致,膽固醇酯化可導致PDAC發展及轉移。一項研究卻表明,相較正常胰腺導管上皮細胞,PDAC細胞膽固醇酯含量較低,負責膽固醇酯合成的甾醇O-酰基轉移酶(sterol O-acyltransferase 1,SOAT1)含量也較低[20]。SOAT1的膽固醇酯化作用阻止了膽固醇在PDAC細胞中對膽固醇合成的負反饋,從而促進了甲氧戊酸途徑[45]。這可能解釋了為什么SOAT1基因敲除或SOAT1抑制劑avasimibe抑制膽固醇酯化會抑制PDAC的生長和轉移[46]。
SREBP在膽固醇代謝中起著關鍵作用,許多在PDAC腫瘤中高表達的分子都與之有密切的關系,比如細胞維甲酸結合蛋白Ⅱ(cellular retinoic acid binding protein Ⅱ,CRABP-Ⅱ) [47]、驅動蛋白樣蛋白1抗體(kinesin like protein 1,KIF11) [48]、轉錄因子CP2(transcription factor,TFCP2) [49]。CRABP-Ⅱ能調控SREBP-1活性使HMGCR和LDLR過度表達促進細胞內膽固醇合成及攝取,同時降低ABCA1蛋白表達抑制細胞內膽固醇外排,導致腫瘤細胞內脂筏內膽固醇的蓄積,通過P13K/AKT信號通路介導腫瘤化療耐藥性,而通過SNIPER-11靶向抑制CRABP-Ⅱ能提升吉西他濱敏感性,協同提升抗腫瘤活性[47]。KIF11是雙極紡錘體關鍵成分,該分子通過減少SREBP-2的降解導致細胞內SREBP-2蛋白水平升高,從而調節膽固醇從頭合成升高細胞內游離膽固醇水平[48]。TFCP2通過與SREBP-2協同激活膽固醇合成限速酶HMGCR的表達從而抑制PDAC腫瘤細胞的衰老[49]。他汀藥物均能逆轉KIF11及TFCP2對腫瘤細胞的惡性生物學行為的影響[48-49]。硫代皂苷A3是一種有效的抗癌化合物,其通過抑制SREBP-1控制PDAC細胞的生長[50]。有研究[51]表明,苦瓜素也對PDAC具有一定的抗癌作用,具體機制不明。
因此,無論是直接靶向膽固醇代謝途徑相關基因及分子,或是調控膽固醇代謝的驅動基因,均為治療PDAC提供了可能。
2.3 膽固醇代謝重塑與PDAC腫瘤微環境
除包含腫瘤細胞外,PDAC腫瘤組織內含有大量的纖維性成分,內有大量的免疫細胞、成纖維細胞(cancer associated fibroblasts,CAFs)、腫瘤相關巨噬細胞(tumor-associated macrophages,TAMs)等,而PDAC腫瘤組織內免疫抑制使得患者一直未取得較好的免疫治療效果。有研究[18]表明,腫瘤細胞間質與正常組織間質相比很明顯的區別是其內含有大量的載脂蛋白。載脂蛋白E(apolipoprotein E,ApoE)是由肝臟細胞及巨噬細胞分泌,能夠調控膽固醇等脂質代謝。研究[52]發現: ApoE在小鼠和人的PDAC腫瘤組織內主要由TAMs和CAFs表達,ApoE敲除小鼠的腫瘤具有較低的腫瘤負擔、較少的纖維化、較低的先天免疫反應和增加的適應性免疫細胞浸潤;進一步分析發現,ApoE敲除小鼠腫瘤具有較少的未成熟骨髓細胞和調節性T細胞,與腫瘤浸潤CD8+ T細胞增加一致,這提示了腫瘤組織內免疫抑制降低;過表達ApoE的PDAC細胞的轉錄組測序及功能富集分析核因子-κB上調并介導趨化因子Cxcl1和Cxcl5合成分泌增加,這兩種趨化因子可進一步損害PDAC腫瘤組織內的T細胞浸潤,從而導致腫瘤組織免疫抑制。Shh通過介導間質重塑在形成PDAC腫瘤微環境中發揮重要作用,PDAC腫瘤細胞的高膽固醇狀態促進Shh的釋放和腫瘤微環境的形成,癌基因下調的細胞黏附相關分子可抑制膽固醇介導的Shh釋放[25]。同時,IL-1軸在宿主對PDAC的免疫應答中起著復雜而關鍵的作用[53]。在腫瘤微環境中,氧化甾醇可介導LXR和SREBP-2通路的相互改變,導致T細胞膽固醇缺乏,隨后導致T細胞耗竭或功能障礙[54]。并且,SQLE與腫瘤免疫細胞浸潤、免疫檢查點(包括PD-1和細胞毒性T淋巴細胞相關蛋白和腫瘤免疫微環境的生物學標志物顯著相關[19]。膽固醇可能會減少CD8+ T淋巴細胞在胰腺癌組織中的浸潤,影響抗腫瘤免疫功能和免疫治療效果[55]。
3 總結及未來研究方向
大量的基礎研究及臨床研究均表明,不論是腫瘤內還是腫瘤微環境內均發生膽固醇代謝重塑,且這種重塑與PDAC的發生發展、侵襲轉移及治療效果密切相關。盡管基礎研究表明靶向膽固醇代謝或聯合應用化療藥物能夠起到抗癌效果,但是目前仍有很多問題需要進一步解決以促進實現PDAC治療的臨床轉化。首先,需要進一步解決膽固醇代謝重編最核心的調控因素。如上所述,細胞內膽固醇水平是動態平衡的,其合成、攝取、酯化存儲及外排保證了膽固醇水平即滿足腫瘤細胞所需又能避免細胞毒性,因此確定其動態平衡的核心調控是關鍵問題,如CRABP-Ⅱ的分子調控[47]。其次,循環膽固醇水平并不能反應腫瘤組織內膽固醇水平,需要進一步闡明細胞內膽固醇及循環膽固醇水平的具體關系,以評判其在發生風險、后期治療效果及復發風險的可實用性生物標志物的應用。再者,需要闡明膽固醇代謝在腫瘤微環境的具體作用以及其協同增強免疫治療的效果;需要解決膽固醇代謝及其各類代謝物在腫瘤細胞與免疫細胞之間的作用及調控關系,是否介導免疫耐受。最后,需要更多的研究來支持實現膽固醇代謝調控在臨床治療的轉化應用,猶如目前PDAC化療方案的組合,尋找靶向膽固醇代謝與各類化療藥物、放療或免疫治療聯合應用的最佳策略。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:劉肖鳳和侯圣忠收集文獻資料并撰寫文章;黃興設計選題并參與查閱文獻;田伯樂審閱并修改文章。
胰腺導管腺癌(pancreatic ductal adenocarcinoma,PDAC)因其高致死率,稱為“癌中之王” 。最新癌癥統計顯示,PDAC新發病例數位居前10,有逐年上升的趨勢,且PDAC死亡病例數居第3位;經過多年的努力,PDAC的5年生存率仍然處于最低水平,僅為13%[1]。在中國,PDAC新發病例數居第8位,死亡病例數居第6位[2]。PDAC的發病率以每年0.5%~10%的增長率將于2030年成為第二大癌癥相關死亡原因[3]。PDAC高死亡率的主要原因除了高度惡性的生物學行為外,還在于缺乏早期診斷手段,將近一半的病例在診斷時已處于晚期,失去了根治性手術這唯一可能治愈該疾病的機會,只有13%的病例能夠得到根治性手術治療[3-4]。目前用于幫助診斷PDAC的生物標志物主要是CA19-9,但是其敏感度及特異度均不高。盡管在過去的幾十年里出現了幾種治療方法,如化療、放射治療、免疫治療和靶向治療,但其效果仍然不理想,比如作為治療晚期PDAC的一線藥物吉西他濱已經在PDAC的治療中有20多年歷史,但并未顯著提升其生存率,耐藥是其主要原因[5]。因此,探索PDAC發生和發展的分子機制,發現新的靶點和開發有效的治療策略勢在必行。越來越多的研究表明,膽固醇代謝在腫瘤細胞的增殖、侵襲、遷移等惡性生物學行為中具有重要作用[6-7]。因此,筆者現就膽固醇代謝重塑在PDAC發生發展中的研究進展作一綜述,并總結膽固醇代謝重塑與PDAC早期診斷、靶向治療以及協同治療的相關研究,旨在為未來PDAC的研究與診療提供思路。
1 膽固醇代謝及重塑
膽固醇是真核細胞生存必需物質之一,是組成細胞內膜性結構的重要成分。膽固醇相關代謝產物也是重要的信號傳遞分子。目前細胞獲取膽固醇主要通過兩條途徑,一是甲羥戊酸從頭合成途徑:2個乙酰輔酶A分子通過一系列縮合反應形成甲羥戊酸,這個過程中甲羥戊酸鹽還原酶(3-hydroxy-3-methylglutaryl-coenzyme A reductase,HMGCR)是主要限速酶;合成甲羥戊酸之后通過一系列的酶促反應形成焦磷酸法尼酯、角鯊烯等,最終形成膽固醇。另一途徑是細胞直接攝取,也是主要的途徑:食物中的膽固醇進入人體循環與低密度脂蛋白(low density lipoprotein,LDL)結合轉運,然后與細胞膜表面的低密度脂蛋白受體(low density lipoprotein receptor,LDLR)相結合,通過細胞內吞作用進入細胞。細胞內膽固醇水平是動態變化的。剩余的膽固醇酯化后儲存于脂筏中,或者是通過膽固醇外流轉運出細胞。在這個復雜的動態代謝過程中有多種酶或者受體直接介導。膽固醇外流過程主要借助于ATP結合盒(ATP-binding cassette,ABC)家族轉運體,如ABCA1、ABCG1、ABCG5以及ABCG8,還借助于細胞外高密度脂蛋白(high density lipoprotein,HDL)的輔助轉運[8]。此外,膽固醇通過酰基輔酶A:膽固醇酰基轉移酶(acyl-coenzyme A: cholesterol acyltransferases,ACATs)酯化為低毒性的膽固醇酯(cholesterol ester,CE)儲存于脂滴或脂筏中。細胞內膽固醇內源性合成、內吞、外流或者合成膽固醇酯均受到細胞內轉錄因子信號調控,主要包括固醇調節元件結合蛋白-2(steroid regulatory element-binding protein-2, SREBP-2)、肝X受體(lver X receptors,LXRs)、核因子紅系2相關因子1(nuclear factor-erythroid 2 related factor 1,NRF1)等。SREBP-2是特定調控膽固醇合成及轉運的轉錄因子,屬于SREBPs轉錄因子家族之一,該家族主要通過控制內源性膽固醇、脂肪酸、三酰甘油和磷脂合成所需的一系列酶的表達來調節脂質穩態。LXRs主要包括LXRα和LXRβ,可通過調控膽固醇外流相關基因(如ABCA1、ABCG1等)的表達介導細胞內膽固醇的動態平衡,此外還可通過靶向SRFBPs轉錄因子影響膽固醇的合成途徑等。細胞內膽固醇還通過NRF1解除對LXRs通路的抑制作用,促進膽固醇的動態外流。此外,還有其他轉錄因子或輔轉錄因子通過介導靶基因轉錄進而調控膽固醇平衡,如載脂蛋白A-1結合蛋白通過激活SREBP-2介導膽固醇外流[9]。肝臟中特異表達的亞洲糖蛋白受體1的缺失通過穩定LXRα,上調ABCA1和ABCG5/G8,分別促進膽固醇向HDL的轉運和向膽汁及糞便的排泄,從而降低血清和肝臟中的脂質水平[10]。核受體共抑制因子-維甲酸和甲狀腺激素受體沉默介質,一種輔抑制因子復合物通過結合轉錄因子調控靶基因的表達,如該復合物結合LXRs形成復合物介導ABCA1及SREBP-1基因表達調控膽固醇平衡,或其復合物亞體,G蛋白通路抑制因子2,通過結合LXRs形成轉錄調控復合物共同調控ABCG1介導膽固醇外流。磷脂酰肌醇3激酶/蛋白激酶B(phosphatidylinositol 3 kinase/protein kinase B, PI3K/PKB,PI3K/AKT)信號通路通過調控SREBP-1以及其靶向基因的表達調控脂質水平維持細胞的生長。因此,膽固醇代謝是一動態且復雜的調控通路,多條調控通路協同確保細胞生長所必需的營養物質及信號分子,而當細胞發生病理變化如癌變時,這一動態平衡將受到重塑以滿足癌變細胞的特殊需求,此即膽固醇代謝重塑(圖1)。
 圖1
示膽固醇代謝重塑過程
圖1
示膽固醇代謝重塑過程
2 膽固醇代謝重塑與PDAC的發生發展
2.1 血清膽固醇
目前,有較多研究探討了血清膽固醇在預測PDAC發生風險、早期診斷及評估生存方面的應用。近年一項病例對照研究[11]發現,高總膽固醇可能表明胰腺癌的發病率較低,總膽固醇的下降可能表明胰腺癌的發病率較高,且低膽固醇合并糖尿病表明胰腺癌的發病率更高。這與PDAC患者診斷為糖尿病時多合并低總膽固醇相一致[12]。血清膽固醇也可用于預測空腹血糖受損患者的PDAC風險[13]。除此之外,較高的術前堿性磷酸酶/總膽固醇比率是根治性手術切除后PDAC患者較差生存的獨立預后因素[14]。 另有研究[15-16]卻發現,胰腺癌患者血清膽固醇及LDL水平較高,HDL水平較低,且與胰腺癌預后關系不大,LDLR高水平可能預示胰腺癌生存不良。
綜上,目前的臨床研究結果表明,血清膽固醇在PDAC的臨床應用價值是矛盾的,仍需要大量前瞻性臨床研究進一步深入挖掘血清膽固醇在PDAC風險評估、早期診斷及預后方面的應用價值。
2.2 膽固醇代謝重塑與PDAC
腫瘤組織以及腫瘤細胞內膽固醇代謝與人體血清膽固醇的差異表明膽固醇代謝的重要性。近年來,越來越多的研究探討膽固醇代謝包括膽固醇從頭合成、獲取、外流、酯化等過程的重塑在PDAC發生發展中的作用。
在膽固醇的合成途徑方面,膽固醇從頭合成基因及相關酶在PDAC中呈高表達,與癌旁的正常胰腺組織相比,胰腺腫瘤中的游離膽固醇含量顯著升高,且與PDAC患者的較差生存相關[16-19]。膽固醇合成代謝關鍵酶HMGCR在PDAC腫瘤細胞內呈高表達,抑制HMGCR增加了PDAC腫瘤細胞的死亡[20]。有研究發現,鋅指結構反義轉錄本1作為胰腺癌的癌基因,通過與胰腺癌中的輔助因子結合,穩定HMGCR的表達,是胰腺癌診斷和治療的候選靶點[21]。角鯊烯環氧酶(squalene epoxidase,SQLE)是膽固醇合成代謝中的第二限速酶,SQLE通過減輕內質網應激和激活脂筏調節的病毒癌基因/磷脂酰肌醇3激酶/蛋白激酶B(sarcoma/Phosphatidylinositol 3 kinase/protein kinase B,Src/PI3K/Akt)信號通路或激活哺乳動物雷帕霉素靶蛋白復合體1(mammalian target of rapamycin complex 1,mTORC1)和腫瘤壞死因子α/核因子-κB信號通路促進腫瘤生長。應用SQLE抑制劑如特比萘芬[22]或敲低SQLE[17]可以有效抑制胰腺癌細胞的增殖生長。SQLE抑制劑也能夠增強鉑類、吉西他濱和5-氟尿嘧啶對PDAC腫瘤細胞的敏感性[22]。人-微小核糖核酸-363-3p(human serum albumin-microRNA-363-3p, HSA-mir-363-3p)被認為是調節SQLE表達的關鍵microRNA,從而影響PDAC患者的預后[19]。2,3-氧化角鯊烯環化酶抑制劑8-8071在體內及體外降低p27、細胞周期蛋白 B1和細胞周期蛋白 E的表達及c-Jun氨基末端激酶(c-Jun N-terminal kinase,JNK)和細胞外調節蛋白激酶的磷酸化水平來抑制PANC-1細胞的活力,誘導細胞周期停滯在G1期[23]。在PDAC小鼠模型以及體外人PDAC細胞株中也表現腫瘤局部高膽固醇水平[16]。除此之外,還有研究[18]表明,遠離惡性細胞的區域就已經顯示出膽固醇代謝重塑,這些變化影響預后并可能成為藥物靶點。并且發現膽固醇合成途徑的基因,比如法尼基二磷酸法尼基轉移酶1基因的表達升高時,胰腺癌患者具有較差的生存[16-17]。
高膽固醇水平可促進PDAC的發生發展。例如,膽固醇與Wnt/β-連環蛋白信號通路卷曲蛋白5(Frizzled5,Fzd5)受體相結合激活β-連環蛋白分子及核內蓄積,進而通過結合轉錄因子促進下游靶基因的轉錄影響PDAC細胞的增殖,而25-羥基膽固醇能夠靶向抑制膽固醇與內質網表面Fzd5的結合抑制下一步信號通路激活[24]。并且膽固醇還促進PDAC腫瘤微環境的形成[25]。膽固醇25-羥基酶是一種能將膽固醇轉化為25-羥基膽固醇的酶,參與抑制膽固醇的生物合成和膽固醇的消耗。膽固醇25-羥基酶在胰腺癌細胞中表觀基因下調促進免疫逃避和腫瘤生長[26]。
一些廣泛使用的膽固醇靶向藥物,如治療血脂異常的他汀類藥物,可能會潛在地影響癌細胞中的膽固醇代謝[27-28]。辛伐他汀通過抑制HMGCR、聲波刺猬蛋白(sonic hedgehog, Shh)信號通路或通過激活JNK途徑降低Yes相關蛋白結合基序的表達抑制PDAC細胞存活、增殖、遷移和侵襲[20, 29-30]。辛伐他汀和吉西他濱聯合治療顯著減少了腫瘤內細胞程序性死亡-配體1(programmed cell death 1 ligand 1,PD-L1)的表達,顯著降低了總體腫瘤負擔和轉移發生率[31],且辛伐他汀與奧沙利鉑或抗程序性死亡受體1(Programmed cell death 1,PD-1)藥物聯合作用時表現出相加的抗生長作用[30]。也有研究表明,低劑量二甲雙胍和辛伐他汀聯合治療抑制PDAC的發展[32];匹伐他汀聯合二甲雙胍能激活單磷酸腺苷依賴的蛋白激酶,抑制PI3K/mTOR信號通路,展現出協同抗癌效果[33];洛伐他汀通過抑制質膜和線粒體中的膽固醇脂筏誘導人PDAC細胞凋亡[34]。上述研究表明,雖然同為他汀類藥物,均表現出其抑制PDAC腫瘤細胞的增殖,但其機制不盡相同[35]。除聯合應用并增敏化療藥物效果外,靶向膽固醇代謝也可促進放療敏感性。如唑來膦酸通過抑制膽固醇合成途徑的法尼基二磷酸合成酶提高PDAC化療敏感性。體內體外研究表明唑來膦酸通過影響Ras相關的C3肉毒素底物1和Ras相似物(Ras homologue,Rho)的戊烯化,從而調節DNA損傷和輻射反應信號,并改善系統免疫細胞促進放療敏感性[36]。
在膽固醇攝取途徑方面,LDLR參與膽固醇攝取,是調控膽固醇穩態重要的跨膜受體。LDLR在PDAC腫瘤細胞內呈高表達[20]。枯草桿菌前蛋白轉換酶9(proprotein convertase subtilisin/kexin type 9,PCSK9)可通過結合LDLR,促進LDLR的降解。具有抗LDL聚集特性的多肽可能具有抗PDAC作用[37]。PCSK9與FOLFIRINOX聯合治療轉移性胰腺癌處于臨床前研究階段[38]。LDL協同膽固醇轉運,其高表達促進癌細胞的增殖、侵襲及轉移,機制上,LDL的高表達激活大量的信號傳導和轉錄激活子3(sgnal transduction and transcription activator 3,STAT3)、Janus激酶1/Janus激酶2(Janus kinase 1/Janus kinase 2,JAK1/JAK2)及酪氨酸蛋白激酶,對于STAT3缺失的PDAC腫瘤細胞有降低LDL的作用[39]。
ABCG2、ABCB1、ABCC1-4等ABC轉運蛋白被認為與多藥耐藥有關[40-41]。HSA-miR-3178通過RhoB/PI3K/Akt信號通路上調ABC轉運蛋白表達,促進吉西他濱耐藥。這些發現提示HSA-miR-3178可能成為克服胰腺癌吉西他濱耐藥的新的治療靶點[42]。胞漿ABCC8蛋白表達對PDAC有預后價值[43]。此外,通過包裝HDL,介導細胞內膽固醇外流,降低細胞內總膽固醇水平,亦能抑制PDAC腫瘤細胞的增殖活性[44]。
與其他腫瘤一致,膽固醇酯化可導致PDAC發展及轉移。一項研究卻表明,相較正常胰腺導管上皮細胞,PDAC細胞膽固醇酯含量較低,負責膽固醇酯合成的甾醇O-酰基轉移酶(sterol O-acyltransferase 1,SOAT1)含量也較低[20]。SOAT1的膽固醇酯化作用阻止了膽固醇在PDAC細胞中對膽固醇合成的負反饋,從而促進了甲氧戊酸途徑[45]。這可能解釋了為什么SOAT1基因敲除或SOAT1抑制劑avasimibe抑制膽固醇酯化會抑制PDAC的生長和轉移[46]。
SREBP在膽固醇代謝中起著關鍵作用,許多在PDAC腫瘤中高表達的分子都與之有密切的關系,比如細胞維甲酸結合蛋白Ⅱ(cellular retinoic acid binding protein Ⅱ,CRABP-Ⅱ) [47]、驅動蛋白樣蛋白1抗體(kinesin like protein 1,KIF11) [48]、轉錄因子CP2(transcription factor,TFCP2) [49]。CRABP-Ⅱ能調控SREBP-1活性使HMGCR和LDLR過度表達促進細胞內膽固醇合成及攝取,同時降低ABCA1蛋白表達抑制細胞內膽固醇外排,導致腫瘤細胞內脂筏內膽固醇的蓄積,通過P13K/AKT信號通路介導腫瘤化療耐藥性,而通過SNIPER-11靶向抑制CRABP-Ⅱ能提升吉西他濱敏感性,協同提升抗腫瘤活性[47]。KIF11是雙極紡錘體關鍵成分,該分子通過減少SREBP-2的降解導致細胞內SREBP-2蛋白水平升高,從而調節膽固醇從頭合成升高細胞內游離膽固醇水平[48]。TFCP2通過與SREBP-2協同激活膽固醇合成限速酶HMGCR的表達從而抑制PDAC腫瘤細胞的衰老[49]。他汀藥物均能逆轉KIF11及TFCP2對腫瘤細胞的惡性生物學行為的影響[48-49]。硫代皂苷A3是一種有效的抗癌化合物,其通過抑制SREBP-1控制PDAC細胞的生長[50]。有研究[51]表明,苦瓜素也對PDAC具有一定的抗癌作用,具體機制不明。
因此,無論是直接靶向膽固醇代謝途徑相關基因及分子,或是調控膽固醇代謝的驅動基因,均為治療PDAC提供了可能。
2.3 膽固醇代謝重塑與PDAC腫瘤微環境
除包含腫瘤細胞外,PDAC腫瘤組織內含有大量的纖維性成分,內有大量的免疫細胞、成纖維細胞(cancer associated fibroblasts,CAFs)、腫瘤相關巨噬細胞(tumor-associated macrophages,TAMs)等,而PDAC腫瘤組織內免疫抑制使得患者一直未取得較好的免疫治療效果。有研究[18]表明,腫瘤細胞間質與正常組織間質相比很明顯的區別是其內含有大量的載脂蛋白。載脂蛋白E(apolipoprotein E,ApoE)是由肝臟細胞及巨噬細胞分泌,能夠調控膽固醇等脂質代謝。研究[52]發現: ApoE在小鼠和人的PDAC腫瘤組織內主要由TAMs和CAFs表達,ApoE敲除小鼠的腫瘤具有較低的腫瘤負擔、較少的纖維化、較低的先天免疫反應和增加的適應性免疫細胞浸潤;進一步分析發現,ApoE敲除小鼠腫瘤具有較少的未成熟骨髓細胞和調節性T細胞,與腫瘤浸潤CD8+ T細胞增加一致,這提示了腫瘤組織內免疫抑制降低;過表達ApoE的PDAC細胞的轉錄組測序及功能富集分析核因子-κB上調并介導趨化因子Cxcl1和Cxcl5合成分泌增加,這兩種趨化因子可進一步損害PDAC腫瘤組織內的T細胞浸潤,從而導致腫瘤組織免疫抑制。Shh通過介導間質重塑在形成PDAC腫瘤微環境中發揮重要作用,PDAC腫瘤細胞的高膽固醇狀態促進Shh的釋放和腫瘤微環境的形成,癌基因下調的細胞黏附相關分子可抑制膽固醇介導的Shh釋放[25]。同時,IL-1軸在宿主對PDAC的免疫應答中起著復雜而關鍵的作用[53]。在腫瘤微環境中,氧化甾醇可介導LXR和SREBP-2通路的相互改變,導致T細胞膽固醇缺乏,隨后導致T細胞耗竭或功能障礙[54]。并且,SQLE與腫瘤免疫細胞浸潤、免疫檢查點(包括PD-1和細胞毒性T淋巴細胞相關蛋白和腫瘤免疫微環境的生物學標志物顯著相關[19]。膽固醇可能會減少CD8+ T淋巴細胞在胰腺癌組織中的浸潤,影響抗腫瘤免疫功能和免疫治療效果[55]。
3 總結及未來研究方向
大量的基礎研究及臨床研究均表明,不論是腫瘤內還是腫瘤微環境內均發生膽固醇代謝重塑,且這種重塑與PDAC的發生發展、侵襲轉移及治療效果密切相關。盡管基礎研究表明靶向膽固醇代謝或聯合應用化療藥物能夠起到抗癌效果,但是目前仍有很多問題需要進一步解決以促進實現PDAC治療的臨床轉化。首先,需要進一步解決膽固醇代謝重編最核心的調控因素。如上所述,細胞內膽固醇水平是動態平衡的,其合成、攝取、酯化存儲及外排保證了膽固醇水平即滿足腫瘤細胞所需又能避免細胞毒性,因此確定其動態平衡的核心調控是關鍵問題,如CRABP-Ⅱ的分子調控[47]。其次,循環膽固醇水平并不能反應腫瘤組織內膽固醇水平,需要進一步闡明細胞內膽固醇及循環膽固醇水平的具體關系,以評判其在發生風險、后期治療效果及復發風險的可實用性生物標志物的應用。再者,需要闡明膽固醇代謝在腫瘤微環境的具體作用以及其協同增強免疫治療的效果;需要解決膽固醇代謝及其各類代謝物在腫瘤細胞與免疫細胞之間的作用及調控關系,是否介導免疫耐受。最后,需要更多的研究來支持實現膽固醇代謝調控在臨床治療的轉化應用,猶如目前PDAC化療方案的組合,尋找靶向膽固醇代謝與各類化療藥物、放療或免疫治療聯合應用的最佳策略。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:劉肖鳳和侯圣忠收集文獻資料并撰寫文章;黃興設計選題并參與查閱文獻;田伯樂審閱并修改文章。