引用本文: 羅洋, 彭赟, 吳耀星, 謝小龍, 王琦, 呂勇, 李可為, 向波. 經腸系膜上靜脈入路的胰后隧道建立在兒童門靜脈海綿樣變肝門解剖中的作用. 中國普外基礎與臨床雜志, 2024, 31(8): 897-902. doi: 10.7507/1007-9424.202401105 復制
版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
兒童門靜脈海綿樣變(cavernous transformation of the portal vein,CTPV)最早于1869年由Balfour提出[1],常見于肝外門靜脈梗阻(extrahepatic portal vein obstruction,EHPVO)患兒,主要表現為門靜脈周圍大量側支循環形成、脾大、脾功能亢進,以及反復發作的致命性食管胃底靜脈曲張破裂出血。CTPV可于EHPVO后6~10 d(平均5周左右)出現[2]。在EHPVO進展期,部分患兒還可出現難治性膽管病變、反復發作的胰腺炎和胰腺假性囊腫形成[3]。CTPV的發病率低,約占兒童門靜脈高壓癥的40%左右[4]。兒童和成人CTPV的病因包括肝硬化、腹腔感染、腫瘤、外傷、上腹部手術史或者有創操作史(如臍靜脈穿刺)、凝血功能異常及先天性門靜脈系統發育異常[5]。兒童多為先天性和腹腔感染所致。
兒童CTPV可供選擇的治療方式有內科保守治療、內鏡下預防治療或止血、介入下門靜脈成形、經頸靜脈肝內門腔靜脈分流術(transjugular intrahepatic portosystemic shunt,TIPS)、外科斷流手術、以Rex和脾腎分流為代表的分流手術,以及疾病終末期的肝移植或者多器官聯合移植[6-9]。其中,符合生理的門靜脈重建方案有:Rex分流、器官移植和介入下門靜脈成形術[10-11]。目前Rex分流術被公認為兒童CTPV的首選手術方案,在成人患者中也有少量成功的病例報道[12]。Rex分流是一種技術要求較高的手術,經典的手術方式為取自體頸內靜脈搭橋,將腸系膜上靜脈血流分流到門靜脈左支遠端,即Rex隱窩(Rex recessus)。在此基礎上,各個中心根據患者的具體情況對原手術方案進行了一系列個體化的改良。筆者所在團隊也對符合相應解剖基礎的患兒,進行了手術方式的創新,即通過建立經腸系膜上靜脈入路的胰后隧道,簡化肝門解剖,迅速尋找門靜脈梗阻近端或腸系膜上靜脈-脾靜脈匯合部,并以門靜脈梗阻近端或匯合部為血管吻合部位,從而達到減少手術出血和降低分流血管并發癥風險的目的,現將該新技術報道如下。
1 臨床資料
1.1 病史簡介
患兒,男,4歲,2023年9月因“體檢發現貧血1+ 年,血小板減少6個月”來院就診。病史中未曾出現皮膚顏色發黃、四肢腫脹、吞咽困難、嘔血、腹脹、腹痛、黑便等情況。嬰兒期曾有腹腔感染病史,具體診治經過不詳。余無其他特殊病史、手術史及家族史。自患病以來,于外院反復復查血紅蛋白水平和血小板計數均降低。外院腹部超聲檢查提示:肝外門靜脈管徑約7 mm,血流單向向肝,流速約21.7 cm/s;腸系膜上靜脈管徑約5 mm,脾靜脈管徑約4.8 mm;門靜脈右支海綿樣變。胃十二指腸鋇劑造影提示:食管壁光滑、柔軟,黏膜連續、清晰,下段呈鳥嘴征,上段食管擴張;賁門形態、開放正常,胃內未見異常,幽門和十二指腸未見異常;考慮賁門失遲緩癥。患兒體質量16 kg,身高106 cm,生長發育無滯后。
1.2 術前實驗室檢查結果
患兒術前常規實驗室檢查結果見表1。術前肝功能正常,三系降低(白細胞計數3.36×109/L,紅細胞計數3.75×109/L,血紅蛋白100 g/L,血小板計數143×109/L),凝血功能輕度異常。術前特殊檢查:蛋白C活性、蛋白S活性和抗凝血酶Ⅲ均正常。Child-Turcotte-Pugh(CTP)評分為5分。肝炎標志物、腫瘤標志物(甲胎蛋白和糖類抗原199)均陰性。
1.3 術前影像學評估和特殊檢查
術前全腹增強CT和血管三維成像提示:門靜脈主干迂曲,門靜脈主干最寬處管徑約0.9 cm,門靜脈左右支部分顯示不清,肝門廣泛CTPV(圖1a);測量門靜脈矢狀部管徑約5 mm(圖1b);脾臟明顯增大,門靜脈高壓側支循環開放;胃、十二指腸及鄰近空腸腸壁節段性稍厚、強化明顯;膽囊未見。磁共振胰膽管造影(magnetic resonance cholangiopancreatography,MRCP)提示:肝門部病灶部分包繞鄰近肝內膽管,肝內膽管走行迂曲并略增寬,膽總管未見增寬。胃鏡結果提示:中-重度食管胃底靜脈曲張(gastroesophageal varices 1,GOV1),門靜脈高壓性胃病(圖1c和1d)。肝臟超聲提示:肝外門靜脈約6 mm,流速約32.2 cm/s,門靜脈右支海綿樣變,肝臟硬度測量(sound touch elastography,STE)值為7.27 kPa(正常參考值:<6.5 kPa),膽囊未見,脾臟肋間厚度為4.7 cm。
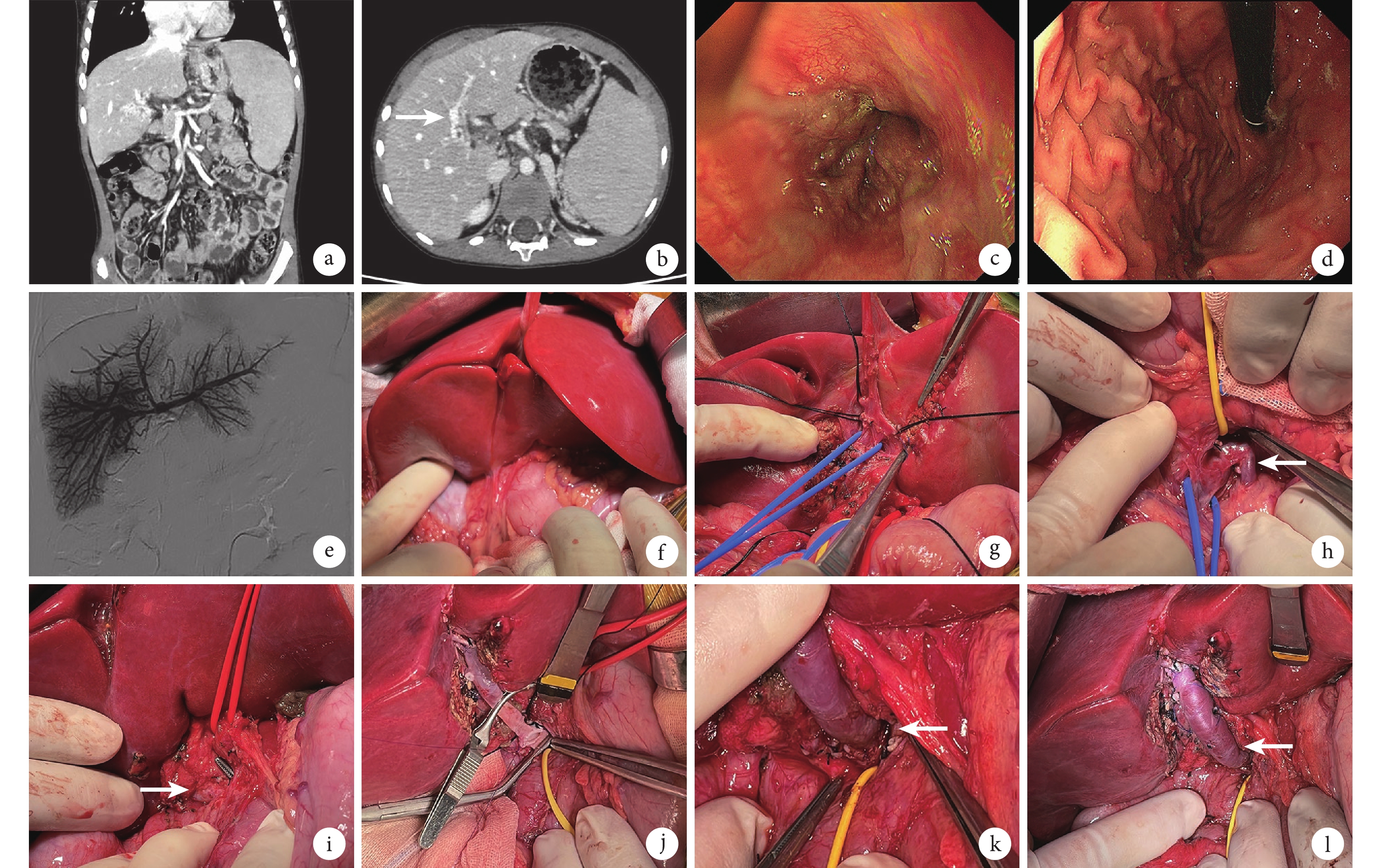 圖1
術前CT及內鏡檢查、肝內門靜脈直接造影及Rex分流手術過程
圖1
術前CT及內鏡檢查、肝內門靜脈直接造影及Rex分流手術過程
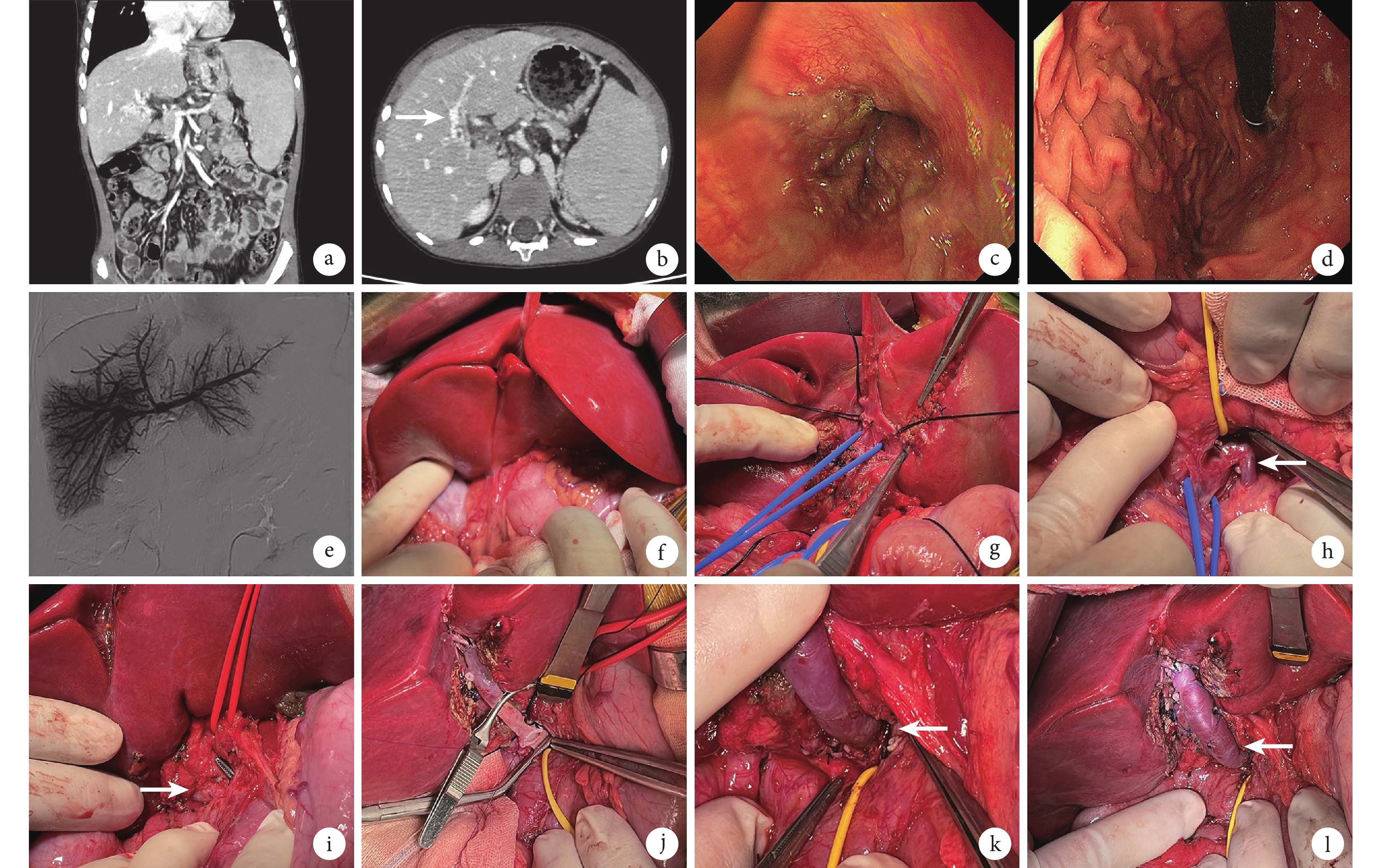
a:術前CT冠狀位圖像提示CTPV,門靜脈主干梗阻,梗阻上游門靜脈起始段、腸系膜上-脾靜脈匯合處通暢;b:CT圖像水平位示門靜脈矢狀部及曲張血管情況,白箭示門靜脈左支矢狀部及周圍曲張血管情況;c和d:內鏡顯示食管下段(c)和胃底(d)門靜脈高壓表現;e:超聲引導下經皮經肝穿刺肝內門靜脈系統直接造影結果提示門靜脈左右分支及遠端分支顯影良好;f:術中肝門處可見大量曲張血管;g:門靜脈矢狀部顯露;h:經腸系膜上靜脈(藍色牽引帶標記)途徑建立胰后隧道,白箭指示腸系膜下靜脈,黃色牽引帶標記胰腺;i:肝十二指腸韌帶下段解剖層面及與胰后隧道會師,紅色牽引帶標記左肝動脈,白箭指示膽管表面巨大曲張血管;j:門靜脈矢狀部端側吻合后,胰腺后方行門靜脈-搭橋血管吻合,黃色牽引帶標記十二指腸和胰腺,紅色牽引帶標記左肝動脈;k:門靜脈-搭橋血管端側吻合口(白箭),黃色牽引帶標記十二指腸和胰腺;i:搭橋血管吻合結束后外觀(白箭),無成角和扭曲
1.4 術前治療方案評估
經術前評估和多學科討論后認為,目前筆者所在醫院在超聲引導下經皮經肝肝內門靜脈穿刺、介入下肝內門靜脈系統造影以及門靜脈主干再通和成形領域累積了大量經驗,已經常規開展這些技術。本例患兒經術前評估門靜脈矢狀部深陷于肝臟實質組織內,被覆肥厚的肝橋,且有大量曲張血管包繞(圖1b)。因此為了在術前準確評估門靜脈矢狀部的解剖,并同期試行門靜脈主干開通,筆者所在團隊擬先行經皮經肝肝內門靜脈系統直接造影并同時嘗試門靜脈主干成形。若介入成形失敗,而造影結果顯示符合Rex分流的條件,再二期行Rex分流。此外,術前的CT血管三維成像提示梗阻上游的門靜脈起始部有約8 mm長、管徑9 mm的殘留門靜脈主干(圖1a),可滿足Rex分流的近端血管吻合條件。MRCP所提示的肝內膽管病變,考慮為CTPV膽管病變,目前僅有形態學上的細微改變,尚未造成有臨床意義的影響,Rex分流后,隨著門靜脈高壓的緩解,一般病程不再進展,暫可不予特別干預。
2 手術步驟
2.1 經皮經肝穿刺門靜脈系統造影結果
全身麻醉后,經術中超聲引導下經皮經肝穿刺門靜脈右前支,行門靜脈直接造影見肝內各門靜脈分支顯影清楚,門靜脈左右支近肝門處稍變細,門靜脈主干未顯影(圖1e),反復誘導導絲未能穿過閉塞段門靜脈,未能行門靜脈成形。
2.2 Rex分流手術主要步驟
靜脈復合麻醉,氣管插管,常規消毒鋪巾后,取右上腹肋緣下約3 cm切口。進腹后見少量清亮腹水,肝臟外觀和質地未見異常,未探及膽囊床和膽囊,肝門粘連,肝門呈典型的CTPV外觀,食管胃底靜脈明顯曲張(圖1f)。切除門靜脈左支外肝橋送病理學檢查,充分暴露門靜脈左支及其主要分支,探查門靜脈矢狀部后確定可供吻合使用(圖1g)。打開胃結腸韌帶,經腸系膜上靜脈入路,建立胰后隧道,探查腸系膜上靜脈和脾靜脈匯合后可見門靜脈近端長約8 mm殘留血管明顯充盈,管徑約9 mm,未探及血管內血栓形成。以血管牽引帶分別牽引胰腺下緣腸系膜上靜脈、脾靜脈備用(圖1h)。解剖肝十二指腸韌帶下段,以及幽門、十二指腸及胰腺上緣,解剖平面位于膽總管左側、正常門靜脈走行區域前方,仔細解剖,避開左右肝動脈,解剖平面的曲張血管予結扎離斷。沿肝固有動脈下緣、十二指腸、胰腺上緣向左側解剖肝十二指腸韌帶,直到顯露胃十二指腸動脈(gastroduodenal arteria,GDA),以血管牽引帶將動脈向左牽開后,沿腸系膜上靜脈/門靜脈走行方向,與肝十二指腸韌帶下段解剖部位會師后,在胰后隧道處尋找近端殘留門靜脈主干,備阻斷和吻合用(圖1i)。注意此處位置較深,應隨時確定解剖層面和方向,防止迷路。經門靜脈起始部位向右繼續解剖,繞行膽管下段和曲張血管背側,將膽管和曲張血管整體牽向右側,以獲得更好的術野暴露。取自體頸內靜脈搭橋,于胰腺后方行門靜脈近端與門靜脈矢狀部搭橋(圖1j),血管吻合線采用6-0 PDS。近端吻合口約8 mm(端側),見圖1k;遠端吻合口約7 mm(端側),見圖1l。Rex分流手術方案示意圖見圖2。該例患者手術總時間約8 h,術中出血約60 mL(包括血管吻合時放血);門靜脈矢狀部阻斷時間約50 min,門靜脈主干阻斷時間約30 min,肝動脈未阻斷。術后恢復順利,術后住院時間為12 d。
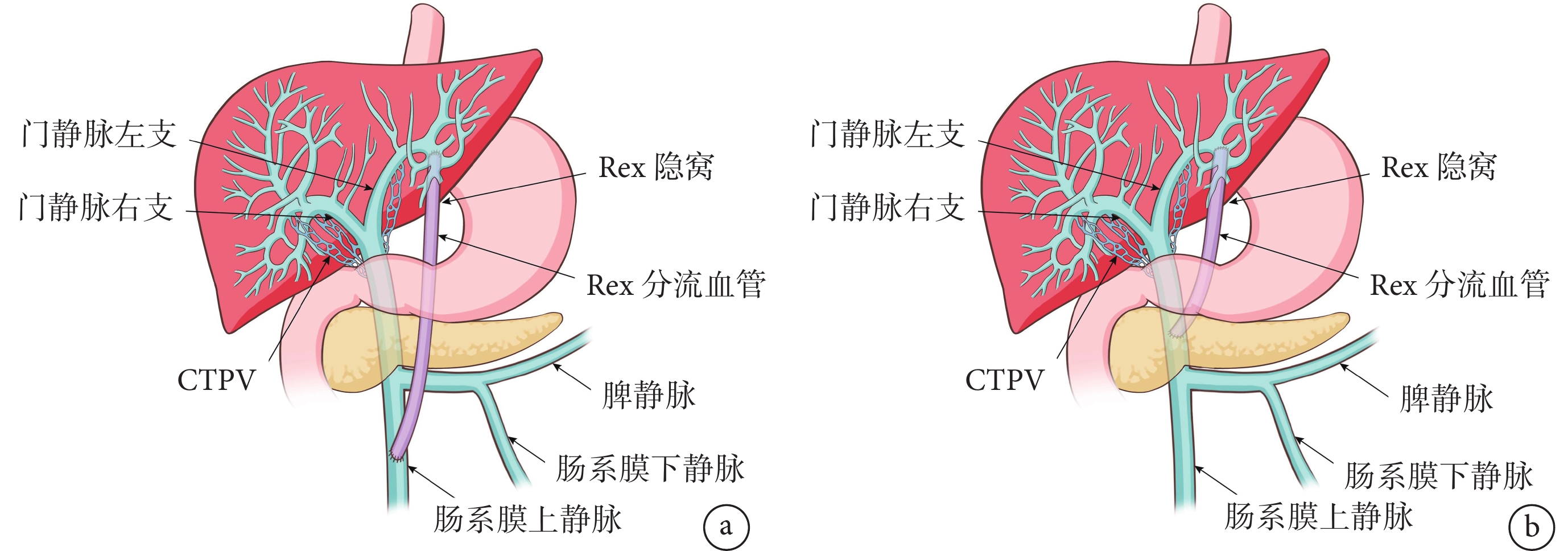 圖2
Rex分流手術方案示意圖
圖2
Rex分流手術方案示意圖
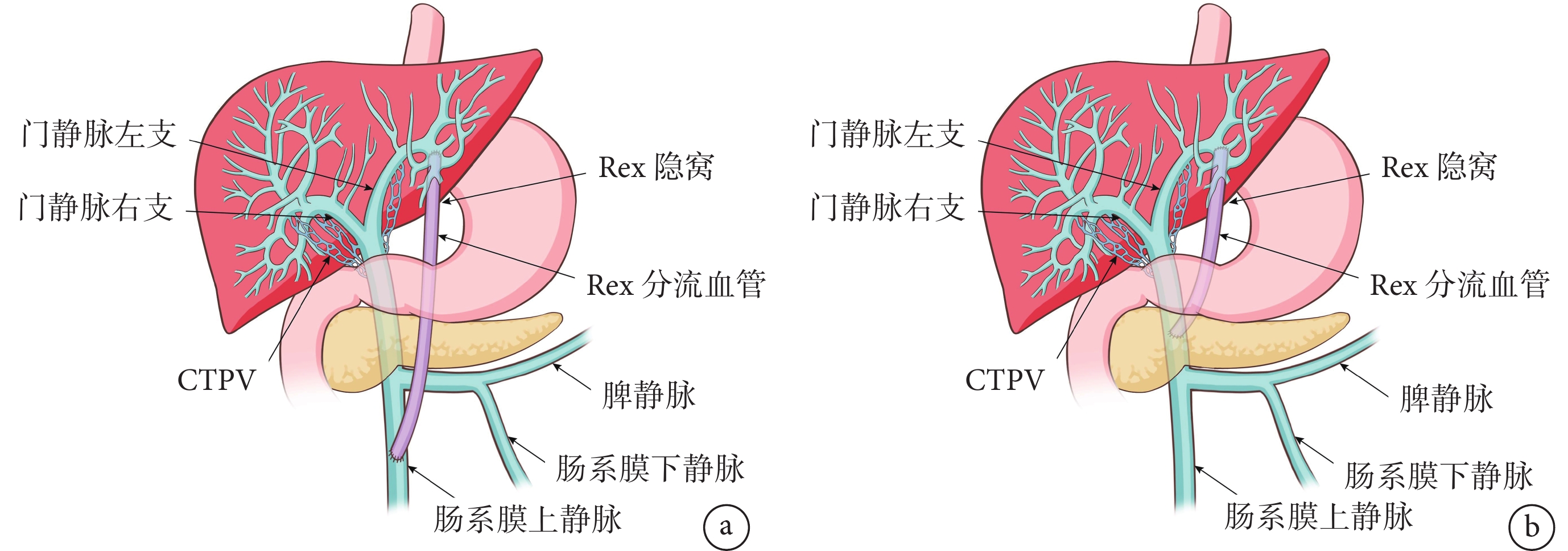
a:傳統Rex分流手術方式;b:筆者團隊所改良的Rex分流手術方式
3 抗凝方案及隨訪情況
術中準備阻斷門靜脈左支前立即給予全身肝素化。術后給予肝素抗凝,維持活化部分凝血活酶時間在60~80 s,口服華法林重疊3 d后于術后第7天改為華法林單藥抗凝至術后 6 個月,維持國際標準化比值在1.5~2.5。術后第 1、3、7 天時監測肝功能指標提示:丙氨酸氨基轉移酶和天門冬氨酸氨基轉移酶輕度升高(表1)。術后病理結果提示:肝細胞水樣變性,未見脂肪變性,界板尚完整,門管區少量淋巴細胞、單核細胞及個別漿細胞、中性粒細胞浸潤;部分門靜脈分支擴張伴周圍炎細胞浸潤,可見疝入周圍肝組織內現象;小葉間膽管未見減少,周邊細膽管未見增生,無纖維組織增生及門管區擴大;特殊染色均未見異常。考慮為:肝臟輕度慢性炎(G1S1),CTPV。目前該患兒術后已隨訪3個月,術后脾功能亢進得到糾正。術后3個月增強CT和血管成像提示:搭橋血管通暢,食管胃底及胃網膜靜脈曲張程度與術前對比明顯減輕。術后3個月超聲結果提示:搭橋血管通暢,脾臟肋間厚度約3.8 cm。
4 討論
Rex分流由de Ville de Goyet 等于1992年首次報道,即腸系膜上靜脈-門靜脈左支分流治療肝移植術后發生的CTPV[13]。經典的手術方式為自體頸內靜脈移植搭橋[14]。目前該手術方式主要應用于兒童無肝硬化背景的CTPV。由于該手術本質上為門靜脈系統到門靜脈系統的分流,曾一度被認為是唯一符合生理的手術方式和唯一的治愈性手術方式。除了可以有效降低門靜脈壓力,緩解門靜脈高壓導致的各種并發癥(包括致命性上消化道出血、脾大、脾功能亢進、CTPV膽管病變、頑固性腹水等)外,還可以減輕肝臟由于血流灌注不足導致的器官萎縮,改善生長發育滯后和兒童認知能力[15-16]。
文獻報道的Rex分流方式主要為經胃后隧道、胰腺前方的搭橋方式,分流血管(一般取自體血管)遠端與門靜脈矢狀部吻合,近端與胰腺下緣的腸系膜上靜脈或經結腸系膜下方解剖腸系膜上靜脈后行端側吻合[17],見圖2a。但該方式需要更長的搭橋血管,以及更遠的血管走行路徑規劃。因此,從理論上考慮,這種傳統的Rex分流手術方式對搭橋血管的長度、血管質地均有較高要求,且隨著兒童體型長大,有出現血管扭曲成角等風險。最新的文獻報道[18]顯示,兒童中廣泛累及門靜脈主干、脾靜脈和腸系膜上靜脈的CTPV(Ⅴ型)僅占9%,累及門靜脈主干和腸系膜上靜脈者(Ⅳ型)占8.4%,累及門靜脈主干和脾靜脈者(Ⅲ型)占5.2%,這與筆者所在團隊的數據基本一致。理想的Rex分流應當將腸系膜上靜脈和脾靜脈的血流均較好地引流到肝內。雖然Ⅲ型和Ⅳ型也能提供門靜脈系統的血流,但Ⅲ型可能無法有效解決脾胃區的門靜脈高壓問題,而Ⅳ型由于患兒疾病發展階段不同,可能存在部分患兒分流后門靜脈血流量不足的問題,從而最終影響Rex分流后的效果。綜上,為了實現更加符合生理的手術規劃、提供充足的入肝血流量、縮短分流血管路徑(減少分流血管并發癥發生可能),以及為后期可能手術失敗后需要進一步選擇肝移植方案盡可能預留理想的門靜脈吻合口,筆者所在團隊對存在腸系膜上靜脈-脾靜脈匯合部位,以及門靜脈主干起始段的患兒(該類型為最常見類型),Rex分流采用肝門和胰腺后方解剖的方式尋找分流部位,即將匯合部位或者門靜脈主干起始段作為分流吻合部位,同時將搭橋血管經胰腺后方直接搭橋到門靜脈矢狀部,縮短搭橋血管走行路徑(圖2b)。
由于CTPV患者的曲張血管密集分布、成瘤樣擴張且血管內壓力極高,直接解剖肝門尋找門靜脈起始段甚至脾靜脈-腸系膜上靜脈匯合部位比較危險,甚至可能出現難以控制的出血。而且隨著病情進展,部分曲張血管逐漸變成厚壁結構,擠壓正常肝門管道,使得正常肝十二指腸韌帶內管道結構位置異常,時常難以辨認,直接解剖也可能存在迷路和損傷正常管道的風險。Moon DB及其同事[19]在既往的文獻中描述過肝移植過程中CTPV肝門解剖的困難程度,甚至直接解剖已無可能。為了重建該例合并CTPV的肝移植患者的門靜脈系統血流,他們將左肝動脈牽開保護后,將剩余肝門結構一起鉗夾離斷,此時才能分辨管道結構進行后續重建。筆者所在醫院王文濤教授團隊[20]也曾報道過肝包蟲病合并CTPV,以及在自體肝移植手術中對這種困難肝門解剖的處理經驗。有學者[21]在對CTPV的解剖研究中發現,曲張血管主要是因門靜脈梗阻后,門靜脈系統的血流通過擴張的膽管旁靜脈叢(Petren靜脈叢)和膽管表面靜脈叢(Saint靜脈叢)繞行。這個曲張血管系統向下可與胰十二指腸后上靜脈、胃結腸干、胃右靜脈、腸系膜上靜脈交通,向上可與肝內門靜脈系統交通,可通過這種交通緩解部分梗阻上游門靜脈系統的壓力。這也與筆者所在團隊前期的手術發現結果一致,肝十二指腸韌帶內的曲張血管大多數集中在膽道周圍。
在這些前期研究的基礎上,筆者進一步探索發現,經過簡單解剖左肝動脈與膽道之間的相對少曲張血管分布區域,將動脈牽開后,可以通過經腸系膜上靜脈入路的胰后隧道的建立,避開曲張靜脈的主要分布區域(即環繞膽道分布),快速定位門靜脈。這種解剖途徑不但可以直接、安全地尋找到門靜脈起始段和腸系膜上靜脈-脾靜脈匯合部位,縮短肝門解剖時間并降低出血風險,而且通過在胰腺上緣/后方阻斷和吻合,可以縮短搭橋血管長度,理論上可以降低血管并發癥發生概率。當然,我們也期待后續能通過對更多病例的經驗累積以獲得更有力的證據支持。尋找到門靜脈后,還可以進一步向右解剖,繞過膽道后方,將膽道及其周圍曲張血管叢牽向右側,從而更好地暴露出吻合空間。另外,在部分腹腔較深的患者中,筆者團隊發現也可以通過解剖Kocker切口(該區域較少曲張血管分布),更好地墊高胰頭和門靜脈后方以方便血管吻合時的暴露。當然,我們不能忽視極少數CTPV的患兒既往曾發生胰腺炎,這類患兒胰后隧道的建立會有一定解剖上的難度。筆者的體會是,提前解剖好Kocker切口,必要時可前后雙合診控制胰腺后方的門靜脈系統洶涌的出血。
總之,隨著對CTPV解剖特點的進一步認識,以及外科技術的不斷創新和優化,筆者所在團隊提出的Rex分流術中經腸系膜上靜脈入路的胰后隧道建立方案可以簡化大部分兒童CTPV的肝門解剖,從而更迅速、安全地尋找到血管吻合部位。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:李可為規劃手術方案,完成手術和論文總體指導;羅洋負責臨床資料收集和論文初步撰寫;彭赟、吳耀星、謝小龍、王琦、呂勇以助手身份共同完成手術,并參與臨床資料收集、論文初步修改;向波負責論文指導。
倫理聲明:本研究已通過四川大學華西醫院生物醫學倫理審查委員會的審核批準 [批文編號:2021年審(638)號]。
兒童門靜脈海綿樣變(cavernous transformation of the portal vein,CTPV)最早于1869年由Balfour提出[1],常見于肝外門靜脈梗阻(extrahepatic portal vein obstruction,EHPVO)患兒,主要表現為門靜脈周圍大量側支循環形成、脾大、脾功能亢進,以及反復發作的致命性食管胃底靜脈曲張破裂出血。CTPV可于EHPVO后6~10 d(平均5周左右)出現[2]。在EHPVO進展期,部分患兒還可出現難治性膽管病變、反復發作的胰腺炎和胰腺假性囊腫形成[3]。CTPV的發病率低,約占兒童門靜脈高壓癥的40%左右[4]。兒童和成人CTPV的病因包括肝硬化、腹腔感染、腫瘤、外傷、上腹部手術史或者有創操作史(如臍靜脈穿刺)、凝血功能異常及先天性門靜脈系統發育異常[5]。兒童多為先天性和腹腔感染所致。
兒童CTPV可供選擇的治療方式有內科保守治療、內鏡下預防治療或止血、介入下門靜脈成形、經頸靜脈肝內門腔靜脈分流術(transjugular intrahepatic portosystemic shunt,TIPS)、外科斷流手術、以Rex和脾腎分流為代表的分流手術,以及疾病終末期的肝移植或者多器官聯合移植[6-9]。其中,符合生理的門靜脈重建方案有:Rex分流、器官移植和介入下門靜脈成形術[10-11]。目前Rex分流術被公認為兒童CTPV的首選手術方案,在成人患者中也有少量成功的病例報道[12]。Rex分流是一種技術要求較高的手術,經典的手術方式為取自體頸內靜脈搭橋,將腸系膜上靜脈血流分流到門靜脈左支遠端,即Rex隱窩(Rex recessus)。在此基礎上,各個中心根據患者的具體情況對原手術方案進行了一系列個體化的改良。筆者所在團隊也對符合相應解剖基礎的患兒,進行了手術方式的創新,即通過建立經腸系膜上靜脈入路的胰后隧道,簡化肝門解剖,迅速尋找門靜脈梗阻近端或腸系膜上靜脈-脾靜脈匯合部,并以門靜脈梗阻近端或匯合部為血管吻合部位,從而達到減少手術出血和降低分流血管并發癥風險的目的,現將該新技術報道如下。
1 臨床資料
1.1 病史簡介
患兒,男,4歲,2023年9月因“體檢發現貧血1+ 年,血小板減少6個月”來院就診。病史中未曾出現皮膚顏色發黃、四肢腫脹、吞咽困難、嘔血、腹脹、腹痛、黑便等情況。嬰兒期曾有腹腔感染病史,具體診治經過不詳。余無其他特殊病史、手術史及家族史。自患病以來,于外院反復復查血紅蛋白水平和血小板計數均降低。外院腹部超聲檢查提示:肝外門靜脈管徑約7 mm,血流單向向肝,流速約21.7 cm/s;腸系膜上靜脈管徑約5 mm,脾靜脈管徑約4.8 mm;門靜脈右支海綿樣變。胃十二指腸鋇劑造影提示:食管壁光滑、柔軟,黏膜連續、清晰,下段呈鳥嘴征,上段食管擴張;賁門形態、開放正常,胃內未見異常,幽門和十二指腸未見異常;考慮賁門失遲緩癥。患兒體質量16 kg,身高106 cm,生長發育無滯后。
1.2 術前實驗室檢查結果
患兒術前常規實驗室檢查結果見表1。術前肝功能正常,三系降低(白細胞計數3.36×109/L,紅細胞計數3.75×109/L,血紅蛋白100 g/L,血小板計數143×109/L),凝血功能輕度異常。術前特殊檢查:蛋白C活性、蛋白S活性和抗凝血酶Ⅲ均正常。Child-Turcotte-Pugh(CTP)評分為5分。肝炎標志物、腫瘤標志物(甲胎蛋白和糖類抗原199)均陰性。
1.3 術前影像學評估和特殊檢查
術前全腹增強CT和血管三維成像提示:門靜脈主干迂曲,門靜脈主干最寬處管徑約0.9 cm,門靜脈左右支部分顯示不清,肝門廣泛CTPV(圖1a);測量門靜脈矢狀部管徑約5 mm(圖1b);脾臟明顯增大,門靜脈高壓側支循環開放;胃、十二指腸及鄰近空腸腸壁節段性稍厚、強化明顯;膽囊未見。磁共振胰膽管造影(magnetic resonance cholangiopancreatography,MRCP)提示:肝門部病灶部分包繞鄰近肝內膽管,肝內膽管走行迂曲并略增寬,膽總管未見增寬。胃鏡結果提示:中-重度食管胃底靜脈曲張(gastroesophageal varices 1,GOV1),門靜脈高壓性胃病(圖1c和1d)。肝臟超聲提示:肝外門靜脈約6 mm,流速約32.2 cm/s,門靜脈右支海綿樣變,肝臟硬度測量(sound touch elastography,STE)值為7.27 kPa(正常參考值:<6.5 kPa),膽囊未見,脾臟肋間厚度為4.7 cm。
 圖1
術前CT及內鏡檢查、肝內門靜脈直接造影及Rex分流手術過程
圖1
術前CT及內鏡檢查、肝內門靜脈直接造影及Rex分流手術過程
a:術前CT冠狀位圖像提示CTPV,門靜脈主干梗阻,梗阻上游門靜脈起始段、腸系膜上-脾靜脈匯合處通暢;b:CT圖像水平位示門靜脈矢狀部及曲張血管情況,白箭示門靜脈左支矢狀部及周圍曲張血管情況;c和d:內鏡顯示食管下段(c)和胃底(d)門靜脈高壓表現;e:超聲引導下經皮經肝穿刺肝內門靜脈系統直接造影結果提示門靜脈左右分支及遠端分支顯影良好;f:術中肝門處可見大量曲張血管;g:門靜脈矢狀部顯露;h:經腸系膜上靜脈(藍色牽引帶標記)途徑建立胰后隧道,白箭指示腸系膜下靜脈,黃色牽引帶標記胰腺;i:肝十二指腸韌帶下段解剖層面及與胰后隧道會師,紅色牽引帶標記左肝動脈,白箭指示膽管表面巨大曲張血管;j:門靜脈矢狀部端側吻合后,胰腺后方行門靜脈-搭橋血管吻合,黃色牽引帶標記十二指腸和胰腺,紅色牽引帶標記左肝動脈;k:門靜脈-搭橋血管端側吻合口(白箭),黃色牽引帶標記十二指腸和胰腺;i:搭橋血管吻合結束后外觀(白箭),無成角和扭曲
1.4 術前治療方案評估
經術前評估和多學科討論后認為,目前筆者所在醫院在超聲引導下經皮經肝肝內門靜脈穿刺、介入下肝內門靜脈系統造影以及門靜脈主干再通和成形領域累積了大量經驗,已經常規開展這些技術。本例患兒經術前評估門靜脈矢狀部深陷于肝臟實質組織內,被覆肥厚的肝橋,且有大量曲張血管包繞(圖1b)。因此為了在術前準確評估門靜脈矢狀部的解剖,并同期試行門靜脈主干開通,筆者所在團隊擬先行經皮經肝肝內門靜脈系統直接造影并同時嘗試門靜脈主干成形。若介入成形失敗,而造影結果顯示符合Rex分流的條件,再二期行Rex分流。此外,術前的CT血管三維成像提示梗阻上游的門靜脈起始部有約8 mm長、管徑9 mm的殘留門靜脈主干(圖1a),可滿足Rex分流的近端血管吻合條件。MRCP所提示的肝內膽管病變,考慮為CTPV膽管病變,目前僅有形態學上的細微改變,尚未造成有臨床意義的影響,Rex分流后,隨著門靜脈高壓的緩解,一般病程不再進展,暫可不予特別干預。
2 手術步驟
2.1 經皮經肝穿刺門靜脈系統造影結果
全身麻醉后,經術中超聲引導下經皮經肝穿刺門靜脈右前支,行門靜脈直接造影見肝內各門靜脈分支顯影清楚,門靜脈左右支近肝門處稍變細,門靜脈主干未顯影(圖1e),反復誘導導絲未能穿過閉塞段門靜脈,未能行門靜脈成形。
2.2 Rex分流手術主要步驟
靜脈復合麻醉,氣管插管,常規消毒鋪巾后,取右上腹肋緣下約3 cm切口。進腹后見少量清亮腹水,肝臟外觀和質地未見異常,未探及膽囊床和膽囊,肝門粘連,肝門呈典型的CTPV外觀,食管胃底靜脈明顯曲張(圖1f)。切除門靜脈左支外肝橋送病理學檢查,充分暴露門靜脈左支及其主要分支,探查門靜脈矢狀部后確定可供吻合使用(圖1g)。打開胃結腸韌帶,經腸系膜上靜脈入路,建立胰后隧道,探查腸系膜上靜脈和脾靜脈匯合后可見門靜脈近端長約8 mm殘留血管明顯充盈,管徑約9 mm,未探及血管內血栓形成。以血管牽引帶分別牽引胰腺下緣腸系膜上靜脈、脾靜脈備用(圖1h)。解剖肝十二指腸韌帶下段,以及幽門、十二指腸及胰腺上緣,解剖平面位于膽總管左側、正常門靜脈走行區域前方,仔細解剖,避開左右肝動脈,解剖平面的曲張血管予結扎離斷。沿肝固有動脈下緣、十二指腸、胰腺上緣向左側解剖肝十二指腸韌帶,直到顯露胃十二指腸動脈(gastroduodenal arteria,GDA),以血管牽引帶將動脈向左牽開后,沿腸系膜上靜脈/門靜脈走行方向,與肝十二指腸韌帶下段解剖部位會師后,在胰后隧道處尋找近端殘留門靜脈主干,備阻斷和吻合用(圖1i)。注意此處位置較深,應隨時確定解剖層面和方向,防止迷路。經門靜脈起始部位向右繼續解剖,繞行膽管下段和曲張血管背側,將膽管和曲張血管整體牽向右側,以獲得更好的術野暴露。取自體頸內靜脈搭橋,于胰腺后方行門靜脈近端與門靜脈矢狀部搭橋(圖1j),血管吻合線采用6-0 PDS。近端吻合口約8 mm(端側),見圖1k;遠端吻合口約7 mm(端側),見圖1l。Rex分流手術方案示意圖見圖2。該例患者手術總時間約8 h,術中出血約60 mL(包括血管吻合時放血);門靜脈矢狀部阻斷時間約50 min,門靜脈主干阻斷時間約30 min,肝動脈未阻斷。術后恢復順利,術后住院時間為12 d。
 圖2
Rex分流手術方案示意圖
圖2
Rex分流手術方案示意圖
a:傳統Rex分流手術方式;b:筆者團隊所改良的Rex分流手術方式
3 抗凝方案及隨訪情況
術中準備阻斷門靜脈左支前立即給予全身肝素化。術后給予肝素抗凝,維持活化部分凝血活酶時間在60~80 s,口服華法林重疊3 d后于術后第7天改為華法林單藥抗凝至術后 6 個月,維持國際標準化比值在1.5~2.5。術后第 1、3、7 天時監測肝功能指標提示:丙氨酸氨基轉移酶和天門冬氨酸氨基轉移酶輕度升高(表1)。術后病理結果提示:肝細胞水樣變性,未見脂肪變性,界板尚完整,門管區少量淋巴細胞、單核細胞及個別漿細胞、中性粒細胞浸潤;部分門靜脈分支擴張伴周圍炎細胞浸潤,可見疝入周圍肝組織內現象;小葉間膽管未見減少,周邊細膽管未見增生,無纖維組織增生及門管區擴大;特殊染色均未見異常。考慮為:肝臟輕度慢性炎(G1S1),CTPV。目前該患兒術后已隨訪3個月,術后脾功能亢進得到糾正。術后3個月增強CT和血管成像提示:搭橋血管通暢,食管胃底及胃網膜靜脈曲張程度與術前對比明顯減輕。術后3個月超聲結果提示:搭橋血管通暢,脾臟肋間厚度約3.8 cm。
4 討論
Rex分流由de Ville de Goyet 等于1992年首次報道,即腸系膜上靜脈-門靜脈左支分流治療肝移植術后發生的CTPV[13]。經典的手術方式為自體頸內靜脈移植搭橋[14]。目前該手術方式主要應用于兒童無肝硬化背景的CTPV。由于該手術本質上為門靜脈系統到門靜脈系統的分流,曾一度被認為是唯一符合生理的手術方式和唯一的治愈性手術方式。除了可以有效降低門靜脈壓力,緩解門靜脈高壓導致的各種并發癥(包括致命性上消化道出血、脾大、脾功能亢進、CTPV膽管病變、頑固性腹水等)外,還可以減輕肝臟由于血流灌注不足導致的器官萎縮,改善生長發育滯后和兒童認知能力[15-16]。
文獻報道的Rex分流方式主要為經胃后隧道、胰腺前方的搭橋方式,分流血管(一般取自體血管)遠端與門靜脈矢狀部吻合,近端與胰腺下緣的腸系膜上靜脈或經結腸系膜下方解剖腸系膜上靜脈后行端側吻合[17],見圖2a。但該方式需要更長的搭橋血管,以及更遠的血管走行路徑規劃。因此,從理論上考慮,這種傳統的Rex分流手術方式對搭橋血管的長度、血管質地均有較高要求,且隨著兒童體型長大,有出現血管扭曲成角等風險。最新的文獻報道[18]顯示,兒童中廣泛累及門靜脈主干、脾靜脈和腸系膜上靜脈的CTPV(Ⅴ型)僅占9%,累及門靜脈主干和腸系膜上靜脈者(Ⅳ型)占8.4%,累及門靜脈主干和脾靜脈者(Ⅲ型)占5.2%,這與筆者所在團隊的數據基本一致。理想的Rex分流應當將腸系膜上靜脈和脾靜脈的血流均較好地引流到肝內。雖然Ⅲ型和Ⅳ型也能提供門靜脈系統的血流,但Ⅲ型可能無法有效解決脾胃區的門靜脈高壓問題,而Ⅳ型由于患兒疾病發展階段不同,可能存在部分患兒分流后門靜脈血流量不足的問題,從而最終影響Rex分流后的效果。綜上,為了實現更加符合生理的手術規劃、提供充足的入肝血流量、縮短分流血管路徑(減少分流血管并發癥發生可能),以及為后期可能手術失敗后需要進一步選擇肝移植方案盡可能預留理想的門靜脈吻合口,筆者所在團隊對存在腸系膜上靜脈-脾靜脈匯合部位,以及門靜脈主干起始段的患兒(該類型為最常見類型),Rex分流采用肝門和胰腺后方解剖的方式尋找分流部位,即將匯合部位或者門靜脈主干起始段作為分流吻合部位,同時將搭橋血管經胰腺后方直接搭橋到門靜脈矢狀部,縮短搭橋血管走行路徑(圖2b)。
由于CTPV患者的曲張血管密集分布、成瘤樣擴張且血管內壓力極高,直接解剖肝門尋找門靜脈起始段甚至脾靜脈-腸系膜上靜脈匯合部位比較危險,甚至可能出現難以控制的出血。而且隨著病情進展,部分曲張血管逐漸變成厚壁結構,擠壓正常肝門管道,使得正常肝十二指腸韌帶內管道結構位置異常,時常難以辨認,直接解剖也可能存在迷路和損傷正常管道的風險。Moon DB及其同事[19]在既往的文獻中描述過肝移植過程中CTPV肝門解剖的困難程度,甚至直接解剖已無可能。為了重建該例合并CTPV的肝移植患者的門靜脈系統血流,他們將左肝動脈牽開保護后,將剩余肝門結構一起鉗夾離斷,此時才能分辨管道結構進行后續重建。筆者所在醫院王文濤教授團隊[20]也曾報道過肝包蟲病合并CTPV,以及在自體肝移植手術中對這種困難肝門解剖的處理經驗。有學者[21]在對CTPV的解剖研究中發現,曲張血管主要是因門靜脈梗阻后,門靜脈系統的血流通過擴張的膽管旁靜脈叢(Petren靜脈叢)和膽管表面靜脈叢(Saint靜脈叢)繞行。這個曲張血管系統向下可與胰十二指腸后上靜脈、胃結腸干、胃右靜脈、腸系膜上靜脈交通,向上可與肝內門靜脈系統交通,可通過這種交通緩解部分梗阻上游門靜脈系統的壓力。這也與筆者所在團隊前期的手術發現結果一致,肝十二指腸韌帶內的曲張血管大多數集中在膽道周圍。
在這些前期研究的基礎上,筆者進一步探索發現,經過簡單解剖左肝動脈與膽道之間的相對少曲張血管分布區域,將動脈牽開后,可以通過經腸系膜上靜脈入路的胰后隧道的建立,避開曲張靜脈的主要分布區域(即環繞膽道分布),快速定位門靜脈。這種解剖途徑不但可以直接、安全地尋找到門靜脈起始段和腸系膜上靜脈-脾靜脈匯合部位,縮短肝門解剖時間并降低出血風險,而且通過在胰腺上緣/后方阻斷和吻合,可以縮短搭橋血管長度,理論上可以降低血管并發癥發生概率。當然,我們也期待后續能通過對更多病例的經驗累積以獲得更有力的證據支持。尋找到門靜脈后,還可以進一步向右解剖,繞過膽道后方,將膽道及其周圍曲張血管叢牽向右側,從而更好地暴露出吻合空間。另外,在部分腹腔較深的患者中,筆者團隊發現也可以通過解剖Kocker切口(該區域較少曲張血管分布),更好地墊高胰頭和門靜脈后方以方便血管吻合時的暴露。當然,我們不能忽視極少數CTPV的患兒既往曾發生胰腺炎,這類患兒胰后隧道的建立會有一定解剖上的難度。筆者的體會是,提前解剖好Kocker切口,必要時可前后雙合診控制胰腺后方的門靜脈系統洶涌的出血。
總之,隨著對CTPV解剖特點的進一步認識,以及外科技術的不斷創新和優化,筆者所在團隊提出的Rex分流術中經腸系膜上靜脈入路的胰后隧道建立方案可以簡化大部分兒童CTPV的肝門解剖,從而更迅速、安全地尋找到血管吻合部位。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:李可為規劃手術方案,完成手術和論文總體指導;羅洋負責臨床資料收集和論文初步撰寫;彭赟、吳耀星、謝小龍、王琦、呂勇以助手身份共同完成手術,并參與臨床資料收集、論文初步修改;向波負責論文指導。
倫理聲明:本研究已通過四川大學華西醫院生物醫學倫理審查委員會的審核批準 [批文編號:2021年審(638)號]。