引用本文: 毛益虎, 黃理賓, 楊烈. 基于SEER數據庫的Ⅳ期結直腸癌早期死亡危險因素分析和預測模型構建及驗證. 中國普外基礎與臨床雜志, 2024, 31(5): 555-564. doi: 10.7507/1007-9424.202402001 復制
版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
結直腸癌(colorectal cancer,CRC)是全球常見的惡性腫瘤之一,發病率在全球范圍都有上升趨勢,2020年中國CRC發病率及死亡率已分別躍居第2位和第5位[1]。最新一項研究[2]結果顯示,我國CRC患者的總體5年生存率為62%,其中Ⅰ期為85%,而Ⅳ期僅為30%。約20%的CRC患者在初診時就已經發生遠處轉移[3]。據統計,中國是目前全球每年CRC新發病例和死亡病例最多的國家,為國家和人民帶來了沉重的疾病負擔,因此,在CRC的治療方面我國現階段仍面臨巨大挑戰。近年來,隨著對CRC手術及藥物綜合治療的深入研究,Ⅳ期CRC的臨床治療取得較大進展[4],以靶向藥物、免疫治療等新型治療方法為代表的綜合治療方案為Ⅳ期CRC的治療提供了新的手段,但Ⅳ期CRC的綜合治療效果仍有待提升。在臨床中觀察到有部分患者在確診Ⅳ期CRC后短時間內出現疾病進展或器官功能衰竭,導致死亡,這種事件被定義為早期死亡,即首次確診后3個月內各種原因引起的死亡[5],而目前少有針對Ⅳ期CRC早期死亡的研究報道,也缺乏對Ⅳ期CRC發生早期死亡相關風險因素的研究,因此有必要開發一種可以精準預測Ⅳ期CRC患者早期死亡的工具,精確識別可能導致患者早期死亡的風險因素并加以干預,提升Ⅳ期CRC患者的綜合治療效果。
美國監測、流行病學和結果(the Surveillance, Epidemiology, and End Results,SEER)數據庫是美國最大的公共癌癥數據庫之一,其樣本量巨大、隨訪信息齊全,包含大量癌癥病例的診療數據和生存隨訪數據,已被廣泛用于多種腫瘤的臨床研究[6]。本研究從SEER數據庫中收集了Ⅳ期CRC患者的人口信息數據、臨床病理學數據、隨訪數據,對數據進行分析以探索Ⅳ期CRC患者發生早期死亡的危險因素,并基于篩選出來的危險因素建立Ⅳ期CRC患者全因早期死亡和癌癥特異性早期死亡的預測模型,繪制Nomogram圖并進行驗證,以幫助臨床醫師早期識別高危患者,幫助制定個體化治療方案。
1 資料與方法
1.1 病例資料來源
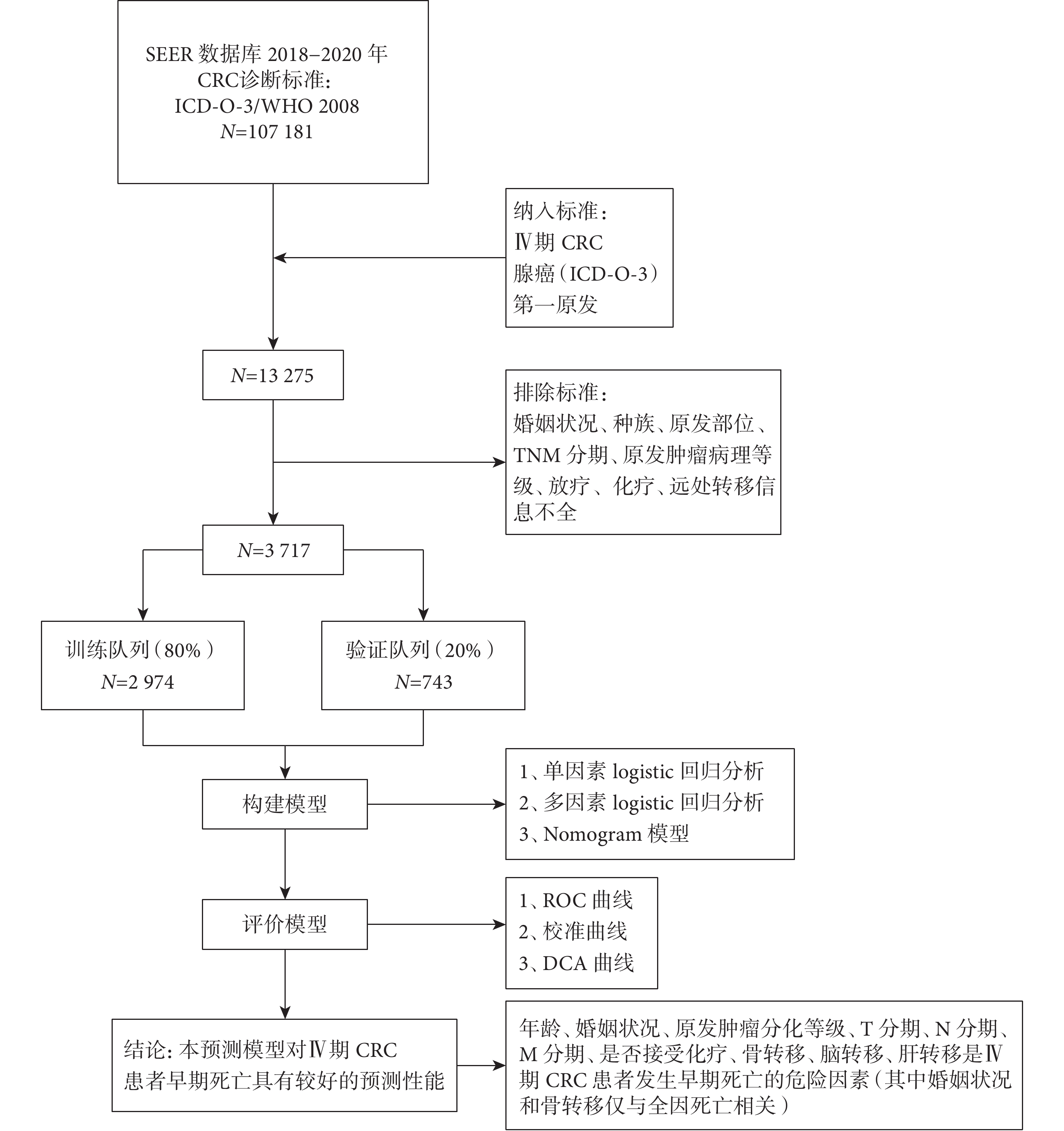
從美國SEER數據庫(版本:SEER*Stat8.4.2)中下載獲取2018–2020年期間診斷為Ⅳ期CRC的患者數據(SEER數據庫中AJCC分期在2018年前后版本有所不同,為了減少不同分期版本導致的偏倚,本研究選擇2018–2020年數據作為研究對象),病例篩選及研究流程見圖1。
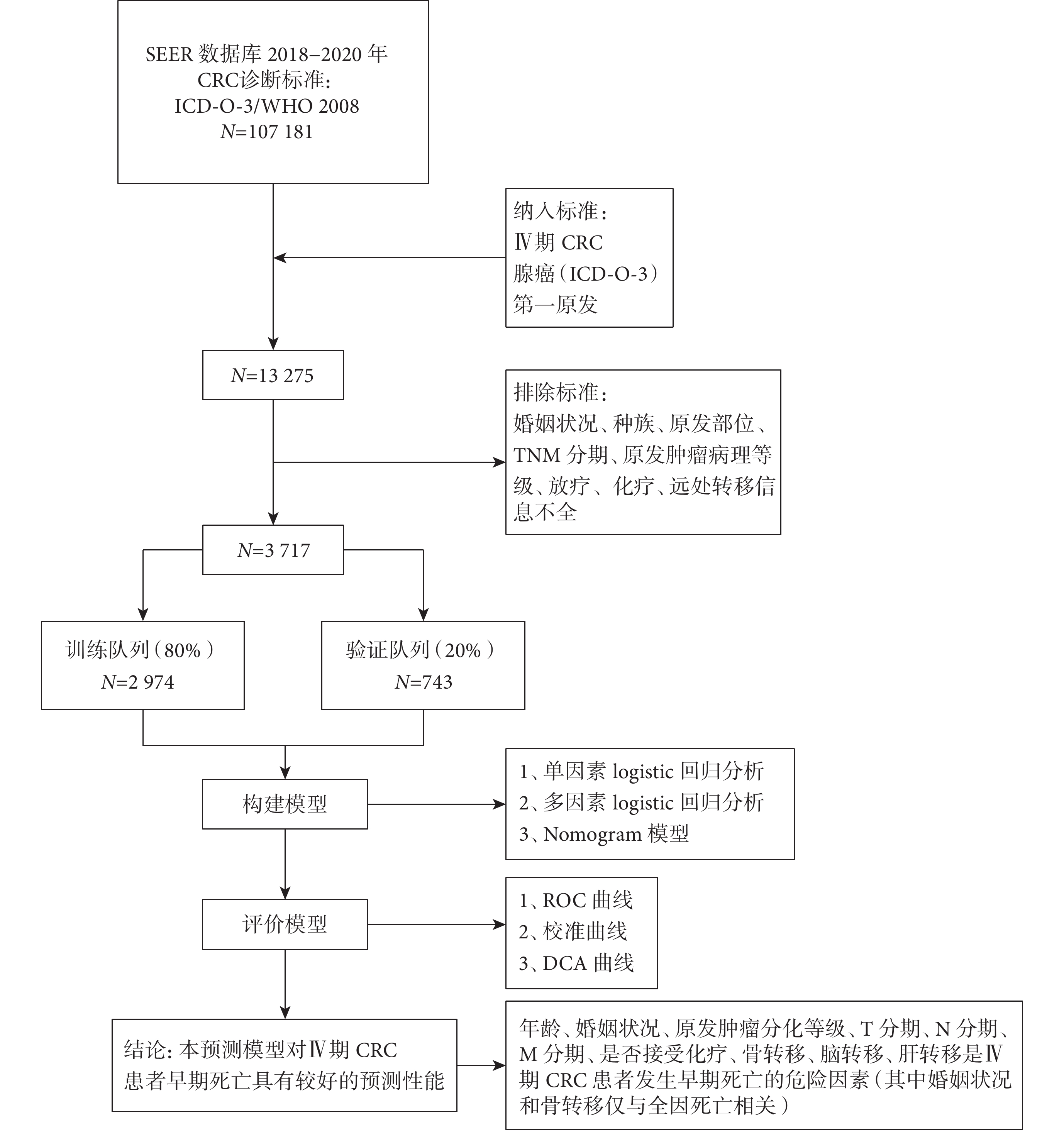 圖1
示本研究技術路線圖
圖1
示本研究技術路線圖
1.2 納入標準和排除標準
納入標準:腫瘤原發部位為結腸和直腸;病理確診為腺癌;TNM分期為Ⅳ期,分期標準依據AJCC第8版CRC分期;腫瘤為單發病灶。
排除標準:尸檢來源;婚姻、種族信息未知;原發腫瘤分化等級及T、N、M分期不詳;遠處轉移部位不詳。
1.3 數據收集
基本數據:包括年齡(參考既往文獻[7]分為<50歲組、50~70歲組和>70歲組)、性別、婚姻狀況、種族;臨床及病理學數據:包括病灶位置、腫瘤直徑(參考既往文獻[7]分為≤5.6 cm組、>5.6組和未知組)、原發腫瘤分化等級、T分期、N分期、M分期、原發部位手術方式、腫瘤轉移情況(腦轉移、肝轉移、肺轉移、骨轉移)、是否接受放療、是否接受化療。生存數據:包括生存時間、生存狀態、死亡原因。本研究的結局事件為全因早期死亡及癌癥特異性早期死亡,全因早期死亡定義為首次診斷后3個月內所有原因引起的死亡;癌癥特異性早期死亡定義為首次診斷后3個月內由癌癥引起的死亡。
1.4 統計學方法
采用SPSS 25.0和R 4.3.0軟件進行統計分析。按照8∶2將研究數據隨機分為訓練隊列和驗證隊列,訓練隊列和驗證隊列各因素間比較采用四格表或R×C列聯表χ2檢驗;訓練隊列用于分析Ⅳ期CRC患者早期死亡的影響因素并建立Nomogram模型,驗證隊列用于驗證Nomogram模型。首先在訓練隊列中進行單因素logistic回歸分析,再連同臨床認為對預后有影響的因素,納入多因素logistic回歸模型,篩選出Ⅳ期CRC早期死亡的危險因素,用于構建Nomogram預測模型。logistic回歸模型的擬合優度檢驗采用霍斯默-萊梅肖檢驗(Hosmer-Lemeshow goodness-of-fit test)。采用受試者工作特征曲線(receiver operating characteristic curve,ROC)評估模型的區分度,校準曲線用于評估模型的校準度,臨床決策曲線分析(decision curve analysis,DCA)用于評估模型的臨床實用性。檢驗水準α=0.05。
2 結果
2.1 研究對象的一般情況
根據納入和排除標準,本次共納入3 717例Ⅳ期CRC患者用于早期死亡研究。按照8∶2將研究數據隨機分為訓練隊列和驗證隊列,其中訓練隊列2 974例患者,用于分析Ⅳ期CRC患者早期死亡的影響因素并建立Nomogram模型;驗證隊列743例患者,用于驗證Nomogram模型。所有患者發生全因早期死亡494例,早期死亡率為13.3%;其中癌癥特異性相關早期死亡439例,癌癥特異性相關早期死亡率為11.8%,占全因早期死亡的88.9%。四格表或R×C列聯表χ2檢驗結果顯示:訓練隊列和驗證隊列之間的臨床病理特征比較差異均無統計學意義(P>0.05),見表1。
2.2 早期死亡的危險因素
訓練隊列的單因素logistic回歸分析結果顯示,年齡、婚姻狀況、腫瘤部位、原發腫瘤分化等級、T分期、N分期、M分期、原發部位手術方式、放療、化療、骨轉移、腦轉移、肺轉移、腫瘤直徑(僅與全因早期死亡相關)與Ⅳ期CRC患者的早期死亡相關(P<0.05)。既往研究認為肝轉移是CRC預后的風險因素,故將肝轉移變量連同單因素分析有統計學意義的因素一同進行多因素logistic回歸分析,結果表明:年齡、婚姻狀況、原發腫瘤分化等級、T分期、N分期、M分期、化療、骨轉移、腦轉移、肝轉移是Ⅳ期CRC患者發生全因早期死亡的影響因素(P<0.05),年齡≥50歲、未婚、原發腫瘤分化等級G3+G4、T4期、N2期、M1c期、未接受化療、伴骨轉移、伴腦轉移、伴肝轉移的Ⅳ期CRC患者更容易發生早期死亡,見表2。年齡、原發腫瘤分化等級、T分期、N分期、M分期、化療、腦轉移、肝轉移是Ⅳ期CRC患者發生癌癥特異性早期死亡的影響因素(P<0.05),年齡≥50歲、原發腫瘤分化等級G3+G4、T4期、N2期、M1c期、未接受化療、伴腦轉移、伴肝轉移的Ⅳ期CRC患者更容易發生癌癥特異性早期死亡,見表3。多因素模型共線性診斷結果顯示各變量的方差膨脹因子值均小于10,表明模型自變量間不存在多重共線性,說明結果穩定可靠,見補充材料1。全因早期死亡模型的擬合優度檢驗結果顯示:χ2=3.424,P=0.905;癌癥特異性早期死亡模型的擬合優度檢驗結果顯示:χ2=3.246,P=0.918,表明建立的2個模型均具有較高的擬合優度。
2.3 Nomogram預測模型的建立
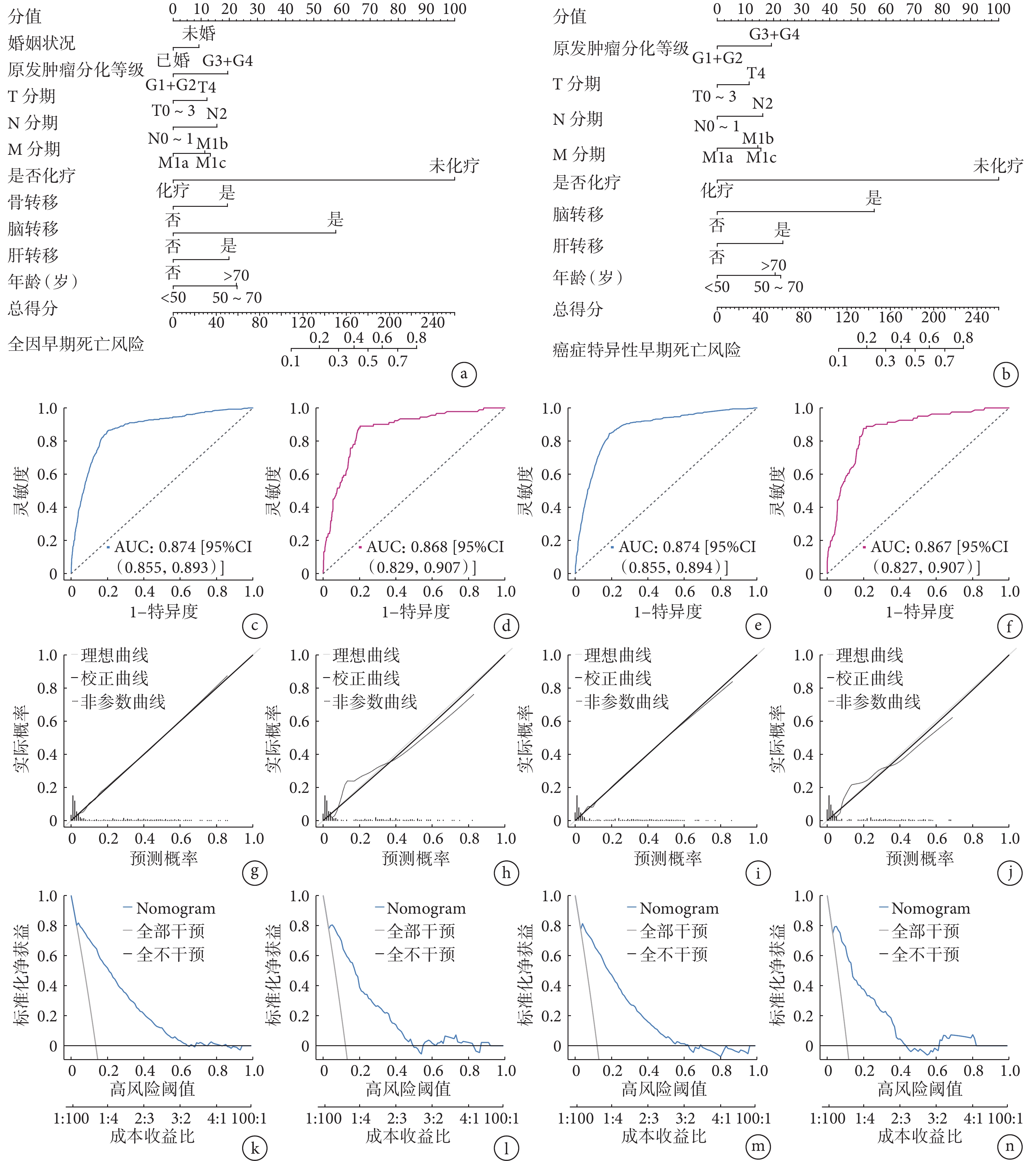
根據多因素logistic分析結果,將P<0.05的因素用于構建Nomogram模型以預測Ⅳ期CRC患者的早期死亡,Nomogram圖將患者的各個預測變量分值相加計算總分,對應下方數值即可得到患者早期死亡的概率,見圖2a和2b。
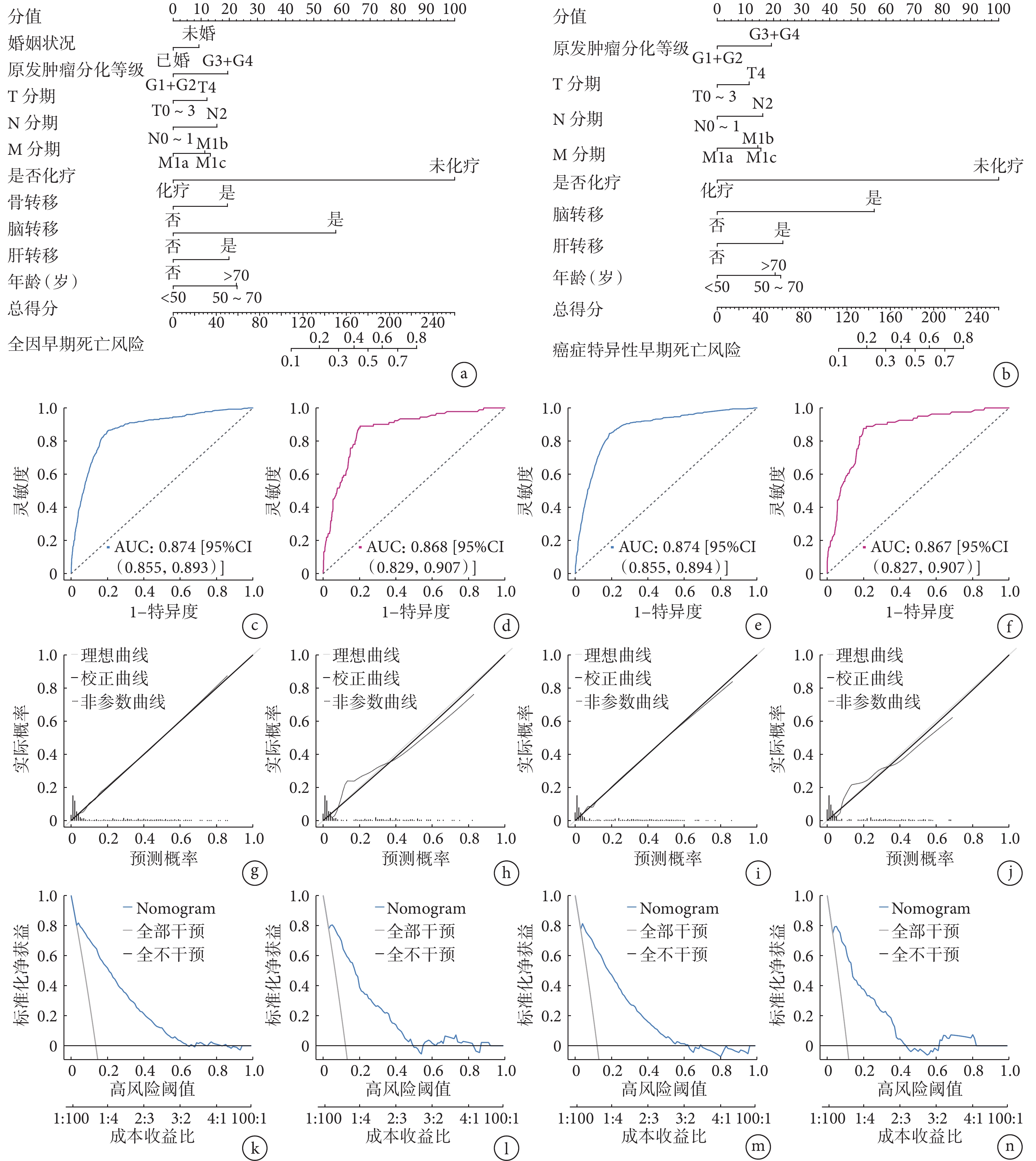 圖2
示預測Ⅳ期CRC全因早期死亡和癌癥特異性早期死亡的Nomogram圖及其驗證結果
圖2
示預測Ⅳ期CRC全因早期死亡和癌癥特異性早期死亡的Nomogram圖及其驗證結果
a:訓練隊列預測Ⅳ期CRC全因早期死亡的Nomogram圖;b:訓練隊列預測Ⅳ期CRC癌癥特異性早期死亡的Nomogram圖;c、d:訓練隊列(c)和驗證隊列(d)患者全因早期死亡的ROC曲線;e、f:訓練隊列(e)和驗證隊列(f)患者癌癥特異性早期死亡的ROC曲線;g、h:訓練隊列(g)和驗證隊列(h)患者全因早期死亡的校準曲線;i、j:訓練隊列(i)和驗證隊列(j)患者癌癥特異性早期死亡的校準曲線;k、l:訓練隊列(k)和驗證隊列(l)患者全因早期死亡的DCA曲線;m、n:訓練隊列(m)和驗證隊列(n)患者癌癥特異性早期死亡的DCA曲線
2.4 Nomogram預測模型的驗證
采用ROC曲線及其曲線下面積(area under curve,AUC)評價模型的區分度,訓練隊列中全因早期死亡預測模型的AUC值為0.874 [95%CI(0.855,0.893)],癌癥特異性早期死亡預測模型的AUC值為0.874 [95%CI(0.855,0.894)];驗證隊列中全因早期死亡預測模型的AUC值為0.868 [95%CI(0.829,0.907)],癌癥特異性早期死亡預測模型的AUC值為0.867 [95%CI(0.827,0.907)],說明該模型具備較好的預測能力,見圖2c~2f;校準曲線顯示該模型的預測結果和實際結果一致性良好,見圖2g~2j;用DCA曲線評價該模型的臨床實用性,顯示該模型在預測Ⅳ期CRC患者的早期死亡方面有非常高的凈獲益,提示該模型具有良好的臨床實用性,見圖2k~2n。
3 討論
隨著人們生活飲食習慣的改變,CRC的發病率有升高趨勢,同時發病趨于年輕化,Ⅳ期CRC的治療仍然是個難題,其治療手段主要包括手術、放療、化療、靶向治療、免疫治療等[8]。隨著對CRC治療的深入研究,Ⅳ期CRC在手術和全身藥物治療方面取得較大進展[9],但是目前研究大多針對Ⅳ期CRC的臨床治療而開展,少有研究關注Ⅳ期CRC的早期死亡,臨床中仍觀察到部分患者在確診Ⅳ期CRC后3個月內發生死亡。截至目前,少有針對Ⅳ期CRC早期死亡的研究報道,因此有必要開發一種可以精準預測Ⅳ期CRC患者早期死亡的工具。
3.1 Ⅳ期CRC患者早期死亡的危險因素
本研究根據納入和排除標準,從SEER數據庫提取3 717例Ⅳ期CRC患者的資料進行研究,分析了發生全因早期死亡及癌癥特異性早期死亡的危險因素,構建、驗證并評價了Nomogram預測模型。本研究結果顯示婚姻狀況是Ⅳ期CRC患者發生早期死亡的影響因素,非婚狀態患者比已婚患者有更高的早期死亡風險,提示婚姻及家庭照顧對CRC患者的生存起重要作用。陳樹斌[10]對28 243例轉移性食管癌患者的研究分析發現,婚姻狀況是食管癌發生早期死亡的危險因素。俞洋麗等[11]對3 946例老年上皮性卵巢癌患者的研究發現,已婚是早期死亡的保護因素,可降低早期死亡的風險,分析其原因可能是相對已婚患者而言,非婚狀態患者具有更差的治療依從性,而婚姻為患者提供了社會和經濟支持。原發腫瘤分化等級、T分期、N分期、M分期是Ⅳ期CRC患者早期死亡的影響因素,較高的分期提示預后越差,這與傳統TNM分期對預后的預測作用相似[12],腫瘤分化程度越低、T分期越高、N分期越高、M分期越高的患者預后越差。本研究結果還顯示接受化療是Ⅳ期CRC發生早期死亡的保護性因素,這與Cheong等[13]的研究一致,該研究納入803例Ⅳ期CRC患者,研究結果顯示接受化療的Ⅳ期CRC患者的預后要優于未接受化療的患者,進一步證實了化療是晚期CRC的重要治療措施。此外本研究還發現骨轉移及腦轉移患者更容易發生早期死亡,和王磊等[7]的研究結果相符,表明轉移性CRC出現骨轉移和腦轉移有更高的早期死亡風險。肝臟是CRC常見的轉移部位,本研究顯示肝轉移是發生早期死亡的危險因素,劉代江等[14]的研究顯示CRC伴肝轉移患者的中位生存時間約8個月,肝臟轉移灶的數目是影響CRC肝轉移患者生存的危險因素。既往研究[15]證實年齡和腫瘤患者的生存時間相關,本研究也支持這一觀點,相對年輕患者,老年患者合并心、腦、肺等合并癥的概率更大,同時放化療的副作用可能對老年患者的影響更加明顯[16]。
本研究結果顯示原發腫瘤部位不是早期死亡的危險因素,與先前研究結果有所差異。徐洪麗等[17]對1 088例結腸癌患者的研究顯示Ⅳ期結腸癌患者腫瘤病灶位于乙狀結腸者的預后最優;Diez-Alonso等[18]的研究顯示CRC原發腫瘤部位和預后相關,右半結腸癌較左半結腸癌和直腸癌的生存率更低。考慮其原因可能是本研究關注的是早期死亡,而徐洪麗等[17]及Diez-Alonso等[18]研究關注的是總生存率。本研究顯示未接受放療不是Ⅳ期CRC患者發生早期死亡的危險因素,分析其原因是相對于其他惡性腫瘤而言,CRC對放療的敏感性更低[19]。本研究顯示肺轉移對Ⅳ期CRC患者早期死亡的影響無統計學意義,這與王磊等[7]對SEER數據庫的6 669例轉移性CRC早期死亡的研究結果相似,但與楊奕[6]對SEER數據庫2 174例Ⅳ期胃癌患者的研究不符。可能表明不同原發部位癌癥的肺轉移對早期死亡的影響程度有所差異。
3.2 Ⅳ期CRC的治療
積極的綜合治療是降低Ⅳ期CRC患者早期死亡的有效措施,Ⅳ期CRC的治療方案尚無統一標準,包括化療、放化、靶向治療、免疫治療、手術治療等措施。化療是Ⅳ期CRC治療的主要手段[20],中國結直腸癌診療規范(2023版)推薦以氟尿嘧啶為基礎的多藥聯合輔助化療方案[1],如FOLFOX、CAPEOX、FOLFIRI、CAPIRI等方案。靶向治療主要包括針對血管內皮生長因子以及表皮生長因子受體的靶向藥。隨著新的靶向藥物的研發以及免疫治療逐步走向成熟,化療聯合靶向治療或化療聯合免疫治療已被證明可以有效改善Ⅳ期CRC的生存時間[21],化療聯合靶向治療是目前治療轉移性CRC的標準模式[22]。免疫治療和基因治療是目前研究治療CRC的熱點方向[23],FDA已經批準Pembrolizumab和Nivolumab兩種程序性死亡受體1或程序性死亡配體1抑制劑用于治療Ⅳ期CRC[24]。對于Ⅳ期無出血、無梗阻、無穿孔的CRC患者是否行原發部位手術治療,目前尚存爭議[9],既往指南及學者均不推薦Ⅳ期CRC患者行原發腫瘤病灶手術治療。但隨著外科手術的發展,越來越多的學者認為Ⅳ期CRC患手術切除原發腫瘤病灶能讓患者獲得更長的總生存時間,董德嘉等[25]對13 077例Ⅳ期CRC患者的臨床數據分析結果表明,接受手術治療的Ⅳ期CRC患者比未接受手術治療的患者有更好的生存獲益,同時建議未接受化療的患者避免單一原發病灶切除,接受化療的患者實施轉移病灶切除可以有更好的獲益。Ho等[26]對162例Ⅳ期CRC患者預后數據的研究分析顯示,Ⅳ期無癥狀的CRC患者行原發腫瘤病灶切除是預后良好的獨立因素。但是轉移灶的切除時機仍具有一定爭議[27]。
本研究存在如下缺陷:SEER數據庫中未記載患者的一般情況,如BMI、腫瘤家族史,以及基礎疾病,如糖尿病、高血壓、心臟疾病等,無法納入分析;無放療和化療具體方案及治療時間;無靶向治療或免疫治療的詳細方案記錄,這些指標都可能會影響研究結果。下一階段可設計多中心前瞻性臨床隊列研究,增加上述指標的收集,提高數據完整性,以提高模型的穩定性。
綜上所述,本研究從SEER數據庫中收集到Ⅳ期CRC患者的人口信息數據、臨床病理學數據、隨訪數據,探索了Ⅳ期CRC發生早期死亡的危險因素,建立了Ⅳ期CRC患者全因早期死亡和癌癥特異性早期死亡的Nomogram預測模型,有助于臨床醫師早期識別高危患者,幫助臨床制定個體化治療方案。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:毛益虎負責查閱文獻并撰寫文稿;楊烈負責研究方案設計、審閱,黃理賓負責指導論文撰寫及控制文章質量。
倫理聲明:由于SEER數據庫是公開匿名的,因此本研究無需獲得倫理委員會批準。
結直腸癌(colorectal cancer,CRC)是全球常見的惡性腫瘤之一,發病率在全球范圍都有上升趨勢,2020年中國CRC發病率及死亡率已分別躍居第2位和第5位[1]。最新一項研究[2]結果顯示,我國CRC患者的總體5年生存率為62%,其中Ⅰ期為85%,而Ⅳ期僅為30%。約20%的CRC患者在初診時就已經發生遠處轉移[3]。據統計,中國是目前全球每年CRC新發病例和死亡病例最多的國家,為國家和人民帶來了沉重的疾病負擔,因此,在CRC的治療方面我國現階段仍面臨巨大挑戰。近年來,隨著對CRC手術及藥物綜合治療的深入研究,Ⅳ期CRC的臨床治療取得較大進展[4],以靶向藥物、免疫治療等新型治療方法為代表的綜合治療方案為Ⅳ期CRC的治療提供了新的手段,但Ⅳ期CRC的綜合治療效果仍有待提升。在臨床中觀察到有部分患者在確診Ⅳ期CRC后短時間內出現疾病進展或器官功能衰竭,導致死亡,這種事件被定義為早期死亡,即首次確診后3個月內各種原因引起的死亡[5],而目前少有針對Ⅳ期CRC早期死亡的研究報道,也缺乏對Ⅳ期CRC發生早期死亡相關風險因素的研究,因此有必要開發一種可以精準預測Ⅳ期CRC患者早期死亡的工具,精確識別可能導致患者早期死亡的風險因素并加以干預,提升Ⅳ期CRC患者的綜合治療效果。
美國監測、流行病學和結果(the Surveillance, Epidemiology, and End Results,SEER)數據庫是美國最大的公共癌癥數據庫之一,其樣本量巨大、隨訪信息齊全,包含大量癌癥病例的診療數據和生存隨訪數據,已被廣泛用于多種腫瘤的臨床研究[6]。本研究從SEER數據庫中收集了Ⅳ期CRC患者的人口信息數據、臨床病理學數據、隨訪數據,對數據進行分析以探索Ⅳ期CRC患者發生早期死亡的危險因素,并基于篩選出來的危險因素建立Ⅳ期CRC患者全因早期死亡和癌癥特異性早期死亡的預測模型,繪制Nomogram圖并進行驗證,以幫助臨床醫師早期識別高危患者,幫助制定個體化治療方案。
1 資料與方法
1.1 病例資料來源
從美國SEER數據庫(版本:SEER*Stat8.4.2)中下載獲取2018–2020年期間診斷為Ⅳ期CRC的患者數據(SEER數據庫中AJCC分期在2018年前后版本有所不同,為了減少不同分期版本導致的偏倚,本研究選擇2018–2020年數據作為研究對象),病例篩選及研究流程見圖1。
 圖1
示本研究技術路線圖
圖1
示本研究技術路線圖
1.2 納入標準和排除標準
納入標準:腫瘤原發部位為結腸和直腸;病理確診為腺癌;TNM分期為Ⅳ期,分期標準依據AJCC第8版CRC分期;腫瘤為單發病灶。
排除標準:尸檢來源;婚姻、種族信息未知;原發腫瘤分化等級及T、N、M分期不詳;遠處轉移部位不詳。
1.3 數據收集
基本數據:包括年齡(參考既往文獻[7]分為<50歲組、50~70歲組和>70歲組)、性別、婚姻狀況、種族;臨床及病理學數據:包括病灶位置、腫瘤直徑(參考既往文獻[7]分為≤5.6 cm組、>5.6組和未知組)、原發腫瘤分化等級、T分期、N分期、M分期、原發部位手術方式、腫瘤轉移情況(腦轉移、肝轉移、肺轉移、骨轉移)、是否接受放療、是否接受化療。生存數據:包括生存時間、生存狀態、死亡原因。本研究的結局事件為全因早期死亡及癌癥特異性早期死亡,全因早期死亡定義為首次診斷后3個月內所有原因引起的死亡;癌癥特異性早期死亡定義為首次診斷后3個月內由癌癥引起的死亡。
1.4 統計學方法
采用SPSS 25.0和R 4.3.0軟件進行統計分析。按照8∶2將研究數據隨機分為訓練隊列和驗證隊列,訓練隊列和驗證隊列各因素間比較采用四格表或R×C列聯表χ2檢驗;訓練隊列用于分析Ⅳ期CRC患者早期死亡的影響因素并建立Nomogram模型,驗證隊列用于驗證Nomogram模型。首先在訓練隊列中進行單因素logistic回歸分析,再連同臨床認為對預后有影響的因素,納入多因素logistic回歸模型,篩選出Ⅳ期CRC早期死亡的危險因素,用于構建Nomogram預測模型。logistic回歸模型的擬合優度檢驗采用霍斯默-萊梅肖檢驗(Hosmer-Lemeshow goodness-of-fit test)。采用受試者工作特征曲線(receiver operating characteristic curve,ROC)評估模型的區分度,校準曲線用于評估模型的校準度,臨床決策曲線分析(decision curve analysis,DCA)用于評估模型的臨床實用性。檢驗水準α=0.05。
2 結果
2.1 研究對象的一般情況
根據納入和排除標準,本次共納入3 717例Ⅳ期CRC患者用于早期死亡研究。按照8∶2將研究數據隨機分為訓練隊列和驗證隊列,其中訓練隊列2 974例患者,用于分析Ⅳ期CRC患者早期死亡的影響因素并建立Nomogram模型;驗證隊列743例患者,用于驗證Nomogram模型。所有患者發生全因早期死亡494例,早期死亡率為13.3%;其中癌癥特異性相關早期死亡439例,癌癥特異性相關早期死亡率為11.8%,占全因早期死亡的88.9%。四格表或R×C列聯表χ2檢驗結果顯示:訓練隊列和驗證隊列之間的臨床病理特征比較差異均無統計學意義(P>0.05),見表1。
2.2 早期死亡的危險因素
訓練隊列的單因素logistic回歸分析結果顯示,年齡、婚姻狀況、腫瘤部位、原發腫瘤分化等級、T分期、N分期、M分期、原發部位手術方式、放療、化療、骨轉移、腦轉移、肺轉移、腫瘤直徑(僅與全因早期死亡相關)與Ⅳ期CRC患者的早期死亡相關(P<0.05)。既往研究認為肝轉移是CRC預后的風險因素,故將肝轉移變量連同單因素分析有統計學意義的因素一同進行多因素logistic回歸分析,結果表明:年齡、婚姻狀況、原發腫瘤分化等級、T分期、N分期、M分期、化療、骨轉移、腦轉移、肝轉移是Ⅳ期CRC患者發生全因早期死亡的影響因素(P<0.05),年齡≥50歲、未婚、原發腫瘤分化等級G3+G4、T4期、N2期、M1c期、未接受化療、伴骨轉移、伴腦轉移、伴肝轉移的Ⅳ期CRC患者更容易發生早期死亡,見表2。年齡、原發腫瘤分化等級、T分期、N分期、M分期、化療、腦轉移、肝轉移是Ⅳ期CRC患者發生癌癥特異性早期死亡的影響因素(P<0.05),年齡≥50歲、原發腫瘤分化等級G3+G4、T4期、N2期、M1c期、未接受化療、伴腦轉移、伴肝轉移的Ⅳ期CRC患者更容易發生癌癥特異性早期死亡,見表3。多因素模型共線性診斷結果顯示各變量的方差膨脹因子值均小于10,表明模型自變量間不存在多重共線性,說明結果穩定可靠,見補充材料1。全因早期死亡模型的擬合優度檢驗結果顯示:χ2=3.424,P=0.905;癌癥特異性早期死亡模型的擬合優度檢驗結果顯示:χ2=3.246,P=0.918,表明建立的2個模型均具有較高的擬合優度。
2.3 Nomogram預測模型的建立
根據多因素logistic分析結果,將P<0.05的因素用于構建Nomogram模型以預測Ⅳ期CRC患者的早期死亡,Nomogram圖將患者的各個預測變量分值相加計算總分,對應下方數值即可得到患者早期死亡的概率,見圖2a和2b。
 圖2
示預測Ⅳ期CRC全因早期死亡和癌癥特異性早期死亡的Nomogram圖及其驗證結果
圖2
示預測Ⅳ期CRC全因早期死亡和癌癥特異性早期死亡的Nomogram圖及其驗證結果
a:訓練隊列預測Ⅳ期CRC全因早期死亡的Nomogram圖;b:訓練隊列預測Ⅳ期CRC癌癥特異性早期死亡的Nomogram圖;c、d:訓練隊列(c)和驗證隊列(d)患者全因早期死亡的ROC曲線;e、f:訓練隊列(e)和驗證隊列(f)患者癌癥特異性早期死亡的ROC曲線;g、h:訓練隊列(g)和驗證隊列(h)患者全因早期死亡的校準曲線;i、j:訓練隊列(i)和驗證隊列(j)患者癌癥特異性早期死亡的校準曲線;k、l:訓練隊列(k)和驗證隊列(l)患者全因早期死亡的DCA曲線;m、n:訓練隊列(m)和驗證隊列(n)患者癌癥特異性早期死亡的DCA曲線
2.4 Nomogram預測模型的驗證
采用ROC曲線及其曲線下面積(area under curve,AUC)評價模型的區分度,訓練隊列中全因早期死亡預測模型的AUC值為0.874 [95%CI(0.855,0.893)],癌癥特異性早期死亡預測模型的AUC值為0.874 [95%CI(0.855,0.894)];驗證隊列中全因早期死亡預測模型的AUC值為0.868 [95%CI(0.829,0.907)],癌癥特異性早期死亡預測模型的AUC值為0.867 [95%CI(0.827,0.907)],說明該模型具備較好的預測能力,見圖2c~2f;校準曲線顯示該模型的預測結果和實際結果一致性良好,見圖2g~2j;用DCA曲線評價該模型的臨床實用性,顯示該模型在預測Ⅳ期CRC患者的早期死亡方面有非常高的凈獲益,提示該模型具有良好的臨床實用性,見圖2k~2n。
3 討論
隨著人們生活飲食習慣的改變,CRC的發病率有升高趨勢,同時發病趨于年輕化,Ⅳ期CRC的治療仍然是個難題,其治療手段主要包括手術、放療、化療、靶向治療、免疫治療等[8]。隨著對CRC治療的深入研究,Ⅳ期CRC在手術和全身藥物治療方面取得較大進展[9],但是目前研究大多針對Ⅳ期CRC的臨床治療而開展,少有研究關注Ⅳ期CRC的早期死亡,臨床中仍觀察到部分患者在確診Ⅳ期CRC后3個月內發生死亡。截至目前,少有針對Ⅳ期CRC早期死亡的研究報道,因此有必要開發一種可以精準預測Ⅳ期CRC患者早期死亡的工具。
3.1 Ⅳ期CRC患者早期死亡的危險因素
本研究根據納入和排除標準,從SEER數據庫提取3 717例Ⅳ期CRC患者的資料進行研究,分析了發生全因早期死亡及癌癥特異性早期死亡的危險因素,構建、驗證并評價了Nomogram預測模型。本研究結果顯示婚姻狀況是Ⅳ期CRC患者發生早期死亡的影響因素,非婚狀態患者比已婚患者有更高的早期死亡風險,提示婚姻及家庭照顧對CRC患者的生存起重要作用。陳樹斌[10]對28 243例轉移性食管癌患者的研究分析發現,婚姻狀況是食管癌發生早期死亡的危險因素。俞洋麗等[11]對3 946例老年上皮性卵巢癌患者的研究發現,已婚是早期死亡的保護因素,可降低早期死亡的風險,分析其原因可能是相對已婚患者而言,非婚狀態患者具有更差的治療依從性,而婚姻為患者提供了社會和經濟支持。原發腫瘤分化等級、T分期、N分期、M分期是Ⅳ期CRC患者早期死亡的影響因素,較高的分期提示預后越差,這與傳統TNM分期對預后的預測作用相似[12],腫瘤分化程度越低、T分期越高、N分期越高、M分期越高的患者預后越差。本研究結果還顯示接受化療是Ⅳ期CRC發生早期死亡的保護性因素,這與Cheong等[13]的研究一致,該研究納入803例Ⅳ期CRC患者,研究結果顯示接受化療的Ⅳ期CRC患者的預后要優于未接受化療的患者,進一步證實了化療是晚期CRC的重要治療措施。此外本研究還發現骨轉移及腦轉移患者更容易發生早期死亡,和王磊等[7]的研究結果相符,表明轉移性CRC出現骨轉移和腦轉移有更高的早期死亡風險。肝臟是CRC常見的轉移部位,本研究顯示肝轉移是發生早期死亡的危險因素,劉代江等[14]的研究顯示CRC伴肝轉移患者的中位生存時間約8個月,肝臟轉移灶的數目是影響CRC肝轉移患者生存的危險因素。既往研究[15]證實年齡和腫瘤患者的生存時間相關,本研究也支持這一觀點,相對年輕患者,老年患者合并心、腦、肺等合并癥的概率更大,同時放化療的副作用可能對老年患者的影響更加明顯[16]。
本研究結果顯示原發腫瘤部位不是早期死亡的危險因素,與先前研究結果有所差異。徐洪麗等[17]對1 088例結腸癌患者的研究顯示Ⅳ期結腸癌患者腫瘤病灶位于乙狀結腸者的預后最優;Diez-Alonso等[18]的研究顯示CRC原發腫瘤部位和預后相關,右半結腸癌較左半結腸癌和直腸癌的生存率更低。考慮其原因可能是本研究關注的是早期死亡,而徐洪麗等[17]及Diez-Alonso等[18]研究關注的是總生存率。本研究顯示未接受放療不是Ⅳ期CRC患者發生早期死亡的危險因素,分析其原因是相對于其他惡性腫瘤而言,CRC對放療的敏感性更低[19]。本研究顯示肺轉移對Ⅳ期CRC患者早期死亡的影響無統計學意義,這與王磊等[7]對SEER數據庫的6 669例轉移性CRC早期死亡的研究結果相似,但與楊奕[6]對SEER數據庫2 174例Ⅳ期胃癌患者的研究不符。可能表明不同原發部位癌癥的肺轉移對早期死亡的影響程度有所差異。
3.2 Ⅳ期CRC的治療
積極的綜合治療是降低Ⅳ期CRC患者早期死亡的有效措施,Ⅳ期CRC的治療方案尚無統一標準,包括化療、放化、靶向治療、免疫治療、手術治療等措施。化療是Ⅳ期CRC治療的主要手段[20],中國結直腸癌診療規范(2023版)推薦以氟尿嘧啶為基礎的多藥聯合輔助化療方案[1],如FOLFOX、CAPEOX、FOLFIRI、CAPIRI等方案。靶向治療主要包括針對血管內皮生長因子以及表皮生長因子受體的靶向藥。隨著新的靶向藥物的研發以及免疫治療逐步走向成熟,化療聯合靶向治療或化療聯合免疫治療已被證明可以有效改善Ⅳ期CRC的生存時間[21],化療聯合靶向治療是目前治療轉移性CRC的標準模式[22]。免疫治療和基因治療是目前研究治療CRC的熱點方向[23],FDA已經批準Pembrolizumab和Nivolumab兩種程序性死亡受體1或程序性死亡配體1抑制劑用于治療Ⅳ期CRC[24]。對于Ⅳ期無出血、無梗阻、無穿孔的CRC患者是否行原發部位手術治療,目前尚存爭議[9],既往指南及學者均不推薦Ⅳ期CRC患者行原發腫瘤病灶手術治療。但隨著外科手術的發展,越來越多的學者認為Ⅳ期CRC患手術切除原發腫瘤病灶能讓患者獲得更長的總生存時間,董德嘉等[25]對13 077例Ⅳ期CRC患者的臨床數據分析結果表明,接受手術治療的Ⅳ期CRC患者比未接受手術治療的患者有更好的生存獲益,同時建議未接受化療的患者避免單一原發病灶切除,接受化療的患者實施轉移病灶切除可以有更好的獲益。Ho等[26]對162例Ⅳ期CRC患者預后數據的研究分析顯示,Ⅳ期無癥狀的CRC患者行原發腫瘤病灶切除是預后良好的獨立因素。但是轉移灶的切除時機仍具有一定爭議[27]。
本研究存在如下缺陷:SEER數據庫中未記載患者的一般情況,如BMI、腫瘤家族史,以及基礎疾病,如糖尿病、高血壓、心臟疾病等,無法納入分析;無放療和化療具體方案及治療時間;無靶向治療或免疫治療的詳細方案記錄,這些指標都可能會影響研究結果。下一階段可設計多中心前瞻性臨床隊列研究,增加上述指標的收集,提高數據完整性,以提高模型的穩定性。
綜上所述,本研究從SEER數據庫中收集到Ⅳ期CRC患者的人口信息數據、臨床病理學數據、隨訪數據,探索了Ⅳ期CRC發生早期死亡的危險因素,建立了Ⅳ期CRC患者全因早期死亡和癌癥特異性早期死亡的Nomogram預測模型,有助于臨床醫師早期識別高危患者,幫助臨床制定個體化治療方案。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:毛益虎負責查閱文獻并撰寫文稿;楊烈負責研究方案設計、審閱,黃理賓負責指導論文撰寫及控制文章質量。
倫理聲明:由于SEER數據庫是公開匿名的,因此本研究無需獲得倫理委員會批準。